Амины — органические соединения, продукты замещения атомов водорода в аммиаке NH3 различными углеводородными радикалами. Функциональная
группой аминов является аминогруппа — NH2.

Классификация аминов
По числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные.

Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций.
Таким образом,
у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены).

Номенклатура и изомерия аминов
Названия аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин,
пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке.
Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации.

Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы.

Получение
- Нагревание галогеналканов с аммиаком
- Восстановление нитросоединений
- Восстановление амидов
- Восстановление нитрилов
- Реакция аммиака со спиртами
- Реакция галогеналканов с аминами
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония.

При такой реакции нитрогруппа превращается в аминогруппу, образуется вода.

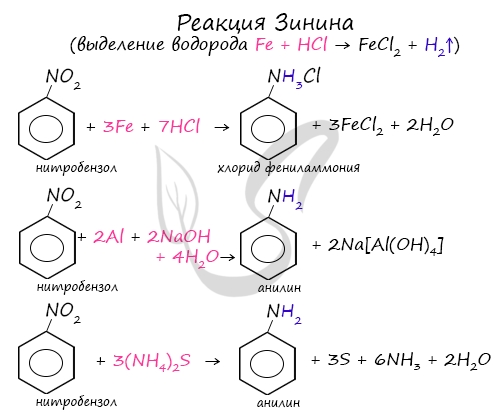
Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина
и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород.
Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды.

Этим способом в промышленности получают гексаметилендиамин, используемый в изготовлении волокна — нейлон.

В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу.

В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов.


Химические свойства аминов
- Основные свойства
- Реакция с азотистой кислотой
- Конденсация аминов с альдегидами и кетонами
- Разложение солей аминов
- Горение аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет.
В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием.

Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония.

Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют.

При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C».

Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода.

При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая
температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ.
4C2H5NH2 + 15O2 → 8CO2 + 14H2O + 2N2
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы –NH2.
Природные аминокислоты можно разделить на следующие основные группы:
| 1) Алифатические предельные аминокислоты (глицин, аланин) | NH2-CH2-COOH глицин
NH2-CH(CH3)-COOH аланин |
| 2) Серосодержащие аминокислоты (цистеин) | 
цистеин |
| 3) Аминокислоты с алифатической гидроксильной группой (серин) | NH2-CH(CH2OH)-COOH серин |
| 4) Ароматические аминокислоты (фенилаланин, тирозин) | NH2-CH(CH2C6H5)-COOH
фенилаланин _________________________________ тирозин |
| 5) Аминокислоты с двумя карбоксильными группами (глутаминовая кислота) | HOOC-CH(NH2)-CH2-CH2-COOH
глутаминовая кислота |
| 6) Аминокислоты с двумя аминогруппами (лизин) | CH2(NH2)-CH2-CH2-CH2-CH(NH2)-COOH
лизин |
Номенклатура аминокислот
- Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
- По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
- Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Физические свойства аминокислот
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, водные растворы хорошо проводят электрический ток.
Получение аминокислот
- Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:
- Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):
Химические свойства аминокислот
При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион:
1. Кислотно-основные свойства аминокислот
Аминокислоты — это амфотерные соединения.
Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами.
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп.
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин — щелочной (одна группа -СООН, две -NH2).
1.1. Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:
1.2. Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с кислотами:
2. Взаимодействие с азотистой кислотой
Аминокислоты способны реагировать с азотистой кислотой.
Например, глицин взаимодействует с азотистой кислотой:
3. Взаимодействие с аминами
Аминокислоты способны реагировать с аминами, образуя соли или амиды.
4. Этерификация
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир:
Например, глицин взаимодействует с этиловым спиртом:
5. Декарбоксилирование
Протекает при нагревании аминокислот с щелочами или при нагревании.
Например, глицин взаимодействует с гидроксидом бария при нагревании:
Например, глицин разлагается при нагревании:
6. Межмолекулярное взаимодействие аминокислот
При взаимодействии аминокислот образуются пептиды. При взаимодействии двух α-аминокислот образуется дипептид.
Например, глицин реагирует с аланином с образованием дипептида (глицилаланин):
Фрагменты молекул аминокислот, образующие пептидную цепь, называются аминокислотными остатками, а связь CO–NH — пептидной связью.
Аланин – одна из 20 основных аминокислот, соединенных в определенной последовательности пептидными связями в полипептидные цепи (белки). Относится к числу заменимых аминокислот, т.к. легко синтезируется в организме животных и человека из безазотистых предшественников и усвояемого азота.
Аланин входит в состав многих белков (в фиброине шелка до 40%), содержится в свободном состоянии в плазме крови.
Аланин — 2-аминопропановая или α-аминопропионовая кислота — с неполярным (гидрофобным) боковым алифатическим радикалом.
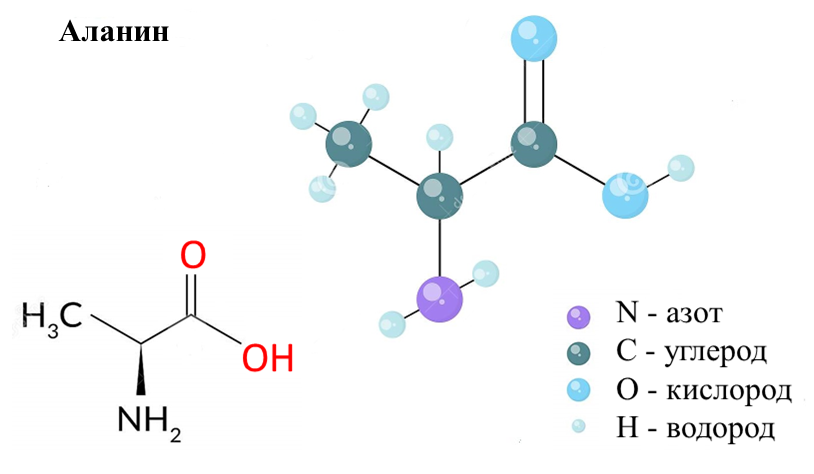
Аланин – это органическое соединение в продуктах разложения белковых веществ, иначе называемое амидопропионовая кислота:
Аланин (Ала, Аlа, А) – ациклическая аминокислота СН3СН(NH2)СООН.
Аланин в живых организмах находится как в свободном состоянии, так и входит в состав белков, а также других биологически активных веществ, например, пантеоновой кислоты (витамин В3).
Аланин впервые выделен из фиброина шелка в 1888 г. Т. Вейлем, синтезирован А. Штреккером в 1850 г.
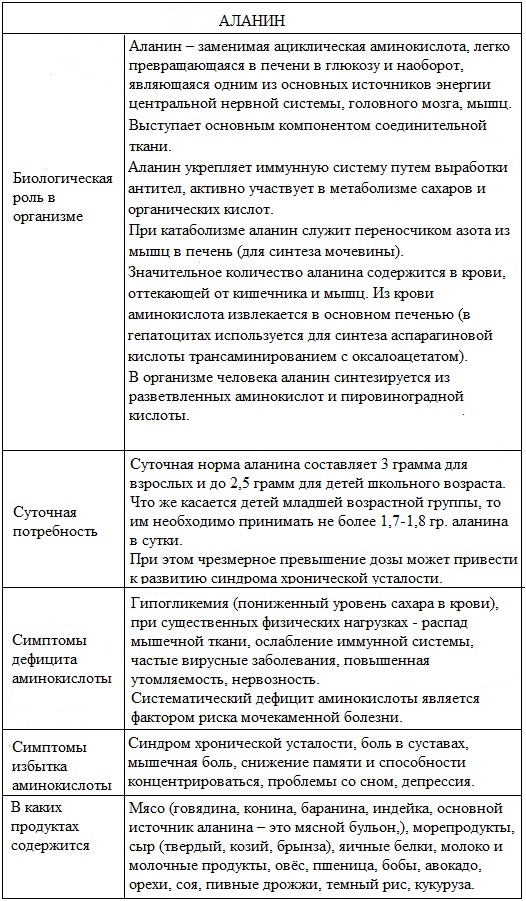
Суточная потребность организма для взрослого человека в аланине составляет 3 грамма.
Физические свойства
Аланин – представляет собой бесцветные ромбические кристаллы, температура плавления 315-316 0С. Хорошо растворим в воде, плохо – в этаноле, не растворим в ацетоне, диэтиловом эфире.
Аланин – один из источников глюкозы в организме. Синтезируется из разветвленных аминокислот (лейцин, изолейцин, валин).
Химические свойства
Аланин – типичная алифатическая α-аминокислота. Аланину свойственны все химические реакции, характерные для альфа-амино- и альфа-карбоксильных групп аминокислот (ацилирование, алкилирование, нитрование, этереификации и др.). Важнейшее свойства аминокислот – взаимодействие их между собой с образованием пептидов.
Биологическая роль
Главные биологические функции аланина – это поддержание азотистого баланса и постоянного уровня глюкозы в крови.
Аланин принимает участие в детоксикации аммиака при больших физических нагрузках.
Аланин вовлекается в углеводный обмен при снижении поступления глюкозы в организм. Аланин также переносит азот из периферийных тканей в печень для его выведения из организма. Принимает участие в детоксикации аммиака при больших физических нагрузках.
Аланин снижает риск развития камней в почках; является основой нормального обмена веществ в организме; способствует борьбе с гипокликемией и накоплению гликогена печенью и мышцами; содействует смягчению колебаний уровня глюкозы в крови между приемами пищи; предшествует образованию оксида азота, который расслабляет гладкие мышцы, в том числе коронарных сосудов, улучшает память, сперматогенез и др. функции.
Повышает уровень энергетического обмена, стимулирует иммунитет, регулирует уровень сахара в крови. Необходим для поддержания тонуса мышц и адекватной половой функции.
Значительная часть азота аминокислот переносится в печень из других органов в составе аланина. Многие органы выделяют в кровь аланин.
Аланин является важным источником энергии для мышечных тканей, головного мозга и центральной нервной системы, укрепляет иммунную систему путем выработки антител. Активно участвует в метаболизме сахаров и органических кислот. Аланин нормализует метаболизм углеводов.
Аланин является составной частью пантотеновой кислоты и коэнзима А. В составе фермента аланинаминотрансфераза в печени и других тканях.
Аланин – аминокислота, входящая в состав белков мышечной и нервной ткани. В свободном состоянии находится в тканях мозга. Особенно много аланина содержится в крови, оттекающей от мышц и от кишечника. Из крови аланин извлекается в основном печенью и используется для синтеза аспарагиновой кислоты.
Аланин может быть сырьем для синтеза глюкозы в организме. Это делает его важным источником энергии и регулятором уровня сахара в крови. Падение уровня сахара и недостаток углеводов в пище приводит к тому, что мышечный протеин разрушается, и печень превращает полученный аланин в глюкозу, чтобы выровнять уровень глюкозы в крови.
При интенсивной работе в течение более одного часа потребность в аланине возрастает, поскольку истощение запасов гликогена в организме приводит к расходу этой аминокислоты для их пополнения.
При катаболизме аланин служит переносчиком азота из мышц в печень (для синтеза мочевины).
Аланин способствует формированию сильной и здоровой мускулатуры.
Основной пищевой источник аланина- мясной бульон, белки животного и растительного происхождения.
Природные источники аланина
Желатин, кукуруза, говядина, яйца, свинина, рис, молочные продукты, бобы, сыр, орехи, соя, пивные дрожжи, овес, рыба, птица.
С избыточным уровнем аланина и пониженным уровнем тирозина и фенилаланина развивается синдром хронической усталости.
Недостаток его приводит к повышению потребности в разветвленных аминокислотах.
Области применения аланина
Доброкачественная гиперплазия предстательной железы, поддержание концентрации сахара в крови, источник энергии, гипертоническая болезнь.
В медицине аланин используется как аминокислота для парентерального питания.
В мужском организме аланин содержится в железистой ткани и в секрете предстательной железы. По этой причине распространена точка зрения, что ежедневный прием аланина в виде пищевой добавки помогает предотвратить развитие доброкачественной гиперплазии предстательной железы, или аденомы простаты.
БАДы
Простакс
Натуральный комплекс растительного происхождения, компоненты которого благотворно влияют на состояние предстательной железы и мужскую репродуктивную систему в целом, подобраны с учетом биологической совместимости и физиологических процессов мужского организма, служат для профилактики развития аденомы простаты, способствуют нормализации работы мочевыделительной системы.
Простакс поддерживает полноценную репродуктивную функцию мужчин, в том числе сперматогенез, а также нормальную работу мочевыделительной системы. Способствует восстановлению клеточных структур железистой ткани, поддерживает баланс мужских половых гормонов. Повышает защитные силы организма, иммунитет, работоспособность.
При гипертонии аланин в сочетании с глицином и аргинином позволяет уменьшить атеросклеротические изменения в сосудах.
В бодибилдинге принято принимать аланин в дозировке 250-500 миллиграмм непосредственно перед тренировкой. Прием аланина в виде раствора позволяет организму усваивать его практически мгновенно, что дает дополнительные преимущества во время тренировок и при наборе мышечной массы.
Аминокислоты
Классификация аминокислот






