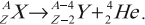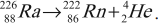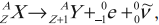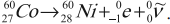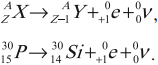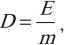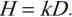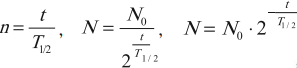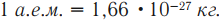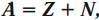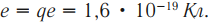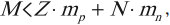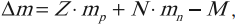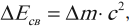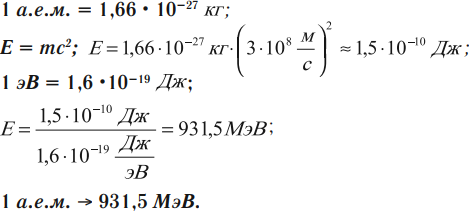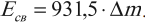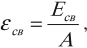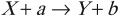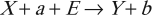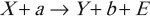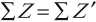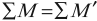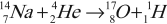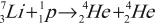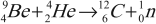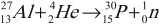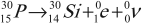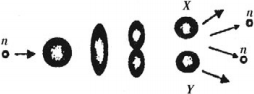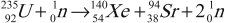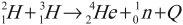Всего: 32 1–20 | 21–32
Добавить в вариант
Установите соответствие между описанием ядерной реакции и видом радиоактивного распада, происходящего в ходе этой реакции. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ОПИСАНИЕ ЯДЕРНОЙ РЕАКЦИИ
А) Ядро урана превращается в ядро тория
с вылетом одной массивной заряженной частицы
Б) Ядро углерода превращается в ядро бора
с вылетом одной массивной заряженной частицы и нейтрино
ВИД РАДИОАКТИВНОГО РАСПАДА
1) Альфа-распад
2) Электронный бета-распад
3) Позитронный бета-распад
4) Гамма-распад
Что представляют собой следующие виды излучения?
ПРОЦЕСС
А) Альфа-излучение
Б) Бета-излучение
В) Гамма-излучение
ФИЗИЧЕСКОЕ ЯВЛЕНИЕ
1) Поток электронов
2) Электромагнитные волны
3) Ядра атома гелия
К каждой позиции первого столбца подберите соответствующую позицию второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
Установите соответствие между видами радиоактивного распада и уравнениями, описывающими этот процесс. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ВИДЫ РАСПАДА
А) электронный бета-распад
Б) альфа-распад
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по физике 2020. Досрочная волна. Вариант 2
В результате серии радиоактивных распадов ядро урана превращается в ядро свинца
Какое количество α— и β-распадов оно испытывает при этом?
| Количество α-распадов | Количество β-распадов |
|---|---|
Установите соответствие между видами радиоактивного распада и уравнениями, описывающими этот процесс. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ВИДЫ РАСПАДА
А) альфа-распад
Б) бета-распад
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по физике 2020. Досрочная волна. Вариант 1
Установите соответствие между видами радиоактивного распада и уравнениями, описывающими этот процесс.
В каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ВИДЫ РАСПАДА
А) альфа-распад
Б) Бета-распад
Ядро атома радия претерпевает бета-распад. Какими станут массовое и зарядовое число образовавшегося ядра? Ответ запишите в виде двух чисел без пробела и запятой.
Источник: ЕГЭ по физике 11.06.2021. Основная волна. Москва
Источник: Демонстрационная версия ЕГЭ—2023 по физике
Период полураспада некоторого радиоактивного изотопа йода составляет 8 суток. За какое время изначально большое число ядер этого изотопа уменьшится в 16 раз? (Ответ дать в сутках.)
Ядро элемента претерпевает гамма-распад. Как изменятся следующие физические величины: зарядовое число; массовое число у образовавшегося (дочернего) ядра по отношению к исходному?
Для каждой величины определите соответствующий характер изменения:
1) увеличится
2) уменьшится
3) не изменится
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Зарядовое число | Массовое число |
Источник: ЕГЭ по физике 11.06.2021. Основная волна. Москва
Ядро элемента претерпевает альфа-распад. Как изменятся следующие физические величины: зарядовое число; массовое число у образовавшегося (дочернего) ядра по отношению к исходному?
Для каждой величины определите соответствующий характер изменения:
1) увеличится
2) уменьшится
3) не изменится
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Зарядовое число | Массовое число |
Радиоактивное ядро испытало -распад. Как изменились в результате этого число нуклонов в ядре и заряд ядра?
Для каждой величины определите соответствующий характер изменения:
1) увеличилась;
2) уменьшилась;
3) не изменилась.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Число нуклонов в ядре | Заряд ядра |
Как изменяется заряд и массовое число радиоактивного ядра в результате его -распада?
Для каждой величины определите соответствующий характер изменения:
1) увеличилась;
2) уменьшилась;
3) не изменилась.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Радиоактивное ядро испытало -распад. Как изменились в результате этого заряд ядра и число протонов в ядре?
Для каждой величины определите соответствующий характер изменения:
1) увеличилась;
2) уменьшилась;
3) не изменилась.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Заряд ядра | Число протонов в ядре |
В результате нескольких α— и β-распадов ядро урана U превращается в ядро свинца
Pb. Определите количество α-распадов и количество β-распадов в этой реакции.
| Количество α-распадов | Количество β-распадов |
Изотоп превратился в изотоп
При этом произошло X
-распадов и Y
-распадов.
Чему равны X и Y?
| X | Y |
|---|---|
При радиоактивном распаде ядра вылетает α-частица с энергией 4800 кэВ. Известно, что в образце радия, массой 1 мкг, каждую секунду распадаются 3,7·104 ядер. Какую суммарную энергию имеют α-частицы, образующиеся в этом образце за 1 час? Ответ приведите в миллиджоулях, округлите до одного знака после запятой.
В результате некоторого числа α-распадов и некоторого числа электронных β-распадов из ядра получается ядро
Чему равно число β-распадов в этой ядерной реакции?
Всего: 32 1–20 | 21–32
Физика атомного ядра
Содержание
- Радиоактивность. Альфа-распад. Бета-распад. Гамма-излучение
- Закон радиоактивного распада
- Нуклонная модель ядра. Заряд ядра. Массовое число ядра
- Энергия связи нуклонов в ядре. Ядерные силы
- Ядерные реакции. Деление и синтез ядер
- Основные формулы по теме «Физика атомного ядра»
Радиоактивность. Альфа-распад. Бета-распад. Гамма-излучение
Радиоактивность – способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений.
Виды радиоактивности:
- естественная радиоактивность – это радиоактивность, которая наблюдается у неустойчивых изотопов, существующих в природе и имеющих в таблице Менделеева порядковый номер больше 83;
- искусственная радиоактивность – это радиоактивность, которая наблюдается у изотопов, полученных посредством ядерных реакций в лабораторных условиях.
Явление естественной радиоактивности открыл в 1896 году французский физик А. Беккерель. Проводя опыты с солями урана, он заметил, что они самопроизвольно испускают лучи неизвестной природы, которые проходят через бумагу, дерево, металлические пластины и делают воздух проводником электричества.
Радиоактивность данного химического элемента не зависит от того, является ли химический элемент чистым или входит в состав какоголибо химического соединения. Радиоактивность не зависит от внешних условий: температуры, освещения, давления. Это означает, что радиоактивность представляет собой внутреннее свойство атомов радиоактивного элемента.
Виды радиоактивных излучений
Излучение радиоактивных веществ имеет сложный характер и состоит из трех видов излучений. Если радиоактивное излучение пропустить через электрическое и магнитное поля, то оно распадается на три части, две из них отклоняются в противоположные стороны, а третий не отклоняется.
- ( alpha )-излучение представляет собой ядра атомов гелия ( {}^4_2He ), движущиеся со скоростью 107 м/с, несет положительный заряд;
- ( beta )-излучение представляет собой поток быстрых электронов, движущихся со скоростями, близкими к скорости света, несет отрицательный заряд;
- ( gamma )-излучение представляет собой электромагнитное излучение с длиной волны 10-12 м, заряда не имеет.
При одинаковой энергии частиц разные виды излучений неодинаково взаимодействуют с веществом.
Вследствие сильного ионизирующего действия глубина проникновения ( alpha )-частиц в твердых телах обычно очень мала. ( beta )-частицы менее эффективно взаимодействуют с атомами вещества, поэтому их проникающая способность больше, чем у ( alpha )-частиц. ( gamma )-кванты взаимодействуют с электронными оболочками атомов и имеют самую большую проникающую способность. Для защиты от ( gamma )-излучения необходимы защитные стены или оболочки толщиной несколько десятков сантиметров или даже метров.
Радиоактивный распад – самопроизвольный распад атомов радиоактивного вещества, в результате которого ядра одних химических элементов превращаются в ядра других химических элементов.
Превращения атомных ядер, которые сопровождаются испусканием ( alpha )- и ( beta )-частиц, называются соответственно ( alpha )— и ( beta )-распадом. Термина «( gamma )-распад» не существует, так как ( alpha )— и ( beta )-распад сопровождаются γ-излучением.
Распадающееся ядро Х называется материнским ядром, ядро продукта распада Y – дочерним ядром.
Правила радиоактивного смещения
Это правила, позволяющие установить, какое ядро возникает в результате распада данного материнского ядра.
- ( alpha )-распад:
Если при радиоактивном превращении испускаются ( alpha )-частицы, то в результате такого превращения образуется ядро элемента, находящегося в таблице Менделеева на две клетки раньше исходного ядра плюс ядро атома гелия ( {}^4_2He ) (или ( alpha )-частица):
- ( beta )-распад.
Если при радиоактивном превращении испускаются ( beta )-частицы, то в результате такого превращения образуется ядро элемента, находящегося в таблице Менделеева:
– при ( beta^- )-распаде в следующей после исходного ядра клетке плюс электрон и антинейтрино (частица, не имеющая заряда и масса покоя которой равна нулю):
– при ( beta^+ )-распаде в предшествующей исходному ядру клетке плюс позитрон и нейтрино (частица, не имеющая заряда и масса покоя которой равна нулю):
( gamma )-излучение сопровождает ( alpha )- и ( beta )-распады, а также возникает при ядерных реакциях, торможении частиц, их распаде и т. д.
( gamma )-излучение испускается дочерним ядром, которое в момент своего образования оказывается в возбужденном состоянии, а затем переходит в невозбужденное состояние.
Спектр ( gamma )-излучения является линейчатым.
Биологическое действие радиоактивных излучений
При облучении вещества ( alpha )-, ( beta )-, ( gamma )-частицами происходит возбуждение или ионизация атомов вещества. При этом сами частицы могут тормозиться, что сопровождается рентгеновским излучением. Кроме того, частицы могут упруго или неупруго соударяться с атомами вещества. Все это может привести к изменению свойств облучаемого вещества и к отрицательному воздействию на живые организмы. Вредное действие излучений на организм связано с образованием свободных химических радикалов и с мутацией в клетках, которые могут оказывать влияние на потомство, приводить к лучевой болезни и образованию злокачественных опухолей.
Методы защиты от внешнего радиоактивного облучения:
- удаление от источника излучения на большое расстояние;
- ограничение времени пребывания на загрязненной местности или вблизи радиоактивных источников;
- ограждение радиоактивных источников экранами из материалов, эффективно поглощающих радиоактивные излучения (графит, свинец, кадмий, бор).
Методы защиты от внутреннего радиоактивного облучения:
- дозиметрический контроль воздуха, осадков в близлежащей местности;
- дозиметрический контроль продуктов питания;
- применение веществ, ослабляющих воздействие радиоактивных излучений на организм.
В дозиметрии различают поглощенную и эквивалентную дозы.
Поглощенная доза равна энергии радиоактивного излучения, поглощенного единицей массы вещества.
Обозначение – ( D ), единица измерения в СИ – грей (Гр).
где ( E ) – энергия излучения; ( m ) – масса вещества.
Для характеристики биологического воздействия на организм используется коэффициент качества излучения ( (k) ), или коэффициент относительной биологической активности.
( k ) = 1 для ( gamma )-квантов, ( k ) = 3 для тепловых нейтронов, ( k ) = 10 для нейтронов с энергией порядка 0,5 МэВ.
Эквивалентная доза равна произведению коэффициента качества излучения и поглощенной дозы.
Обозначение – ( H ), единица измерения в СИ – зиверт (Зв).
1 зиверт – это эквивалентная доза, при которой поглощенная доза равна 1 Гр при коэффициенте качества, равном 1.
Естественный фон составляет 2 мЗв за год.
Предельно допустимая доза – 5 мЗв за год.
При дозе 0,5 Зв наступает острое лучевое поражение организма.
При дозе 3–5 Зв – смертельный исход.
Допустимая доза облучения за среднее время жизни человека (70 лет) составляет 0,35 Зв.
Закон радиоактивного распада
Если имеется большое количество одинаковых радиоактивных ядер, то вероятность распада каждого из них в любой момент времени одинакова. Радиоактивный распад любого ядра является случайным процессом, поэтому момент его распада предсказать невозможно.
Однако для большого числа частиц, находящихся в образце вещества, выполняется статистический закон радиоактивного распада.
Закон радиоактивного распада:
число нераспавшихся атомных ядер при естественном радиоактивном распаде экспоненциально уменьшается с течением времени.
Период полураспада – это время, в течение которого распадается половина способных к распаду ядер.
В начальный момент времени ( t ) = 0, число атомных ядер ( N_0 ).
Через промежуток времени, равный периоду полураспада ( t=T_{1/2} ), число атомных ядер ( N=frac{N_0}{2} ).
Через промежуток времени, равный двум периодам полураспада ( t=2T_{1/2} ), число атомных ядер ( N=frac{N_0}{4}=frac{N_0}{2^2} ).
Через промежуток времени, равный ( n ) периодам полураспада ( t=nT_{1/2} ), число атомных ядер ( N=frac{N_0}{2^n} ).
где ( N ) – число нераспавшихся атомных ядер к моменту времени ( t ); ( N_0 ) – начальное число атомных ядер; ( T_{1/2} ) – период полураспада.
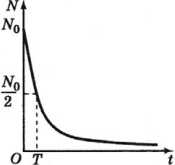
На рисунке период полураспада соответствует времени, в течение которого число радиоактивных ядер (активность) уменьшается вдвое.
Нуклонная модель ядра. Заряд ядра. Массовое число ядра
Элементарные частицы:
- протон
Обозначение – ( p ), заряд ( q_p ) = 1,6·10-19 Кл, масса ( m_p ) = 1,67·10-27 кг. - нейтрон
Обозначение – ( n ), заряд отсутствует, масса ( m_n ) = 1,66·10-27 кг. - электрон
Обозначение – ( e ), заряд ( q_e ) = –1,6·10-19 Кл, масса ( m_e ) = 9,1·10-31 кг.
Нуклон – это частица, входящая в состав атомного ядра.
Атомное ядро любого химического элемента состоит из протонов и нейтронов.
Массовое число – это число, которое определяет количество протонов и нейтронов в ядре и равно округленному до целого значению массы атомного ядра в а.е.м.
Обозначение – ( A ), единица измерения – 1 атомная единица массы (а.е.м.).
Массовое число равно сумме количества протонов и нейтронов в ядре:
где ( A ) – массовое число; ( Z ) – количество протонов в ядре; ( N ) – количество нейтронов в ядре.
Зарядовое число – это число, которое показывает количество протонов в ядре.
Зарядовое число равно сумме зарядов протонов, входящих в состав ядра, выраженной в элементарных электрических зарядах.
Элементарный электрический заряд равен заряду электрона:
( Z ) – порядковый номер химического элемента в периодической таблице Менделеева.
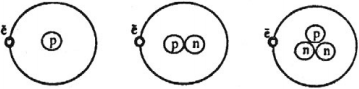
Если некоторый химический элемент обозначить ( {}^A_ZX ), это означает, что в его ядре ( Z ) – протонов и ( N=A-Z ) – нейтронов.
Измерения массы атомов показали, что практически все химические элементы имеют изотопы.
Изотопы – это атомы одного и того же химического элемента, имеющие одинаковое количество протонов, но отличающиеся количеством нейтронов в ядре.
Изотопы имеют:
- одинаковый атомный номер ( Z ) (одинаковое число протонов);
- различные массовые числа ( A ) (различное число нуклонов);
- одинаковое строение электронных оболочек;
- близкие химические свойства.
Изотопы бывают:
- стабильные – это изотопы, которые сохраняются сколь угодно долго;
- радиоактивные – это изотопы, которые превращаются в ядра других элементов с течением времени.
Изотопы водорода: водород имеет два стабильных изотопа – водород ( {}^1_1H ), дейтерий ( {}^2_1H ) и один радиоактивный изотоп тритий ( {}^3_1H ).
Энергия связи нуклонов в ядре. Ядерные силы
Между нуклонами ядра действуют самые мощные силы природы – ядерные силы.
Ядерные силы – это силы притяжения, связывающие протоны и нейтроны в атомном ядре и обеспечивающие существование устойчивых ядер.
Свойства ядерных сил:
- являются силами притяжения;
- являются короткодействующими силами (действуют на малых расстояниях, не превышающих 2·10-15 м; на таком расстоянии ядерные силы больше кулоновских приблизительно в 100 раз);
- обладают свойством зарядовой независимости (ядерные силы, действующие между двумя протонами, двумя нейтронами и между протоном и нейтроном, одинаковы);
- имеют свойство насыщения (каждый нуклон взаимодействует только с ограниченным числом ближайших к нему нуклонов, а не со всеми нуклонами ядра);
- не являются центральными (не действуют по линии, соединяющей центры взаимодействующих нуклонов).
Массу ядра можно точно определить с помощью масс-спектрографов, которые разделяют заряженные частицы с разными удельными зарядами с помощью электрических и магнитных полей.
Опытным путем было установлено, что благодаря действию сил притяжения масса ядра всегда меньше суммы масс протонов и масс нейтронов, входящих в состав этого ядра:
где ( M ) – масса ядра.
Дефект масс – это величина, равная разности суммы масс входящих в ядро нуклонов и массы ядра:
где ( Delta m ) – дефект масс.
Благодаря ядерным силам ядра атомов обладают огромной энергией связи.
Энергия связи – это энергия, которую необходимо затратить, чтобы разделить ядро на составляющие его нуклоны, или энергия, которая выделяется при образовании ядра из отдельных нуклонов:
где ( Delta E_{св} ) – энергия связи, ( c ) – скорость света.
Если в формуле энергии связи массы протона и нейтрона выражены в килограммах, а скорость света – в метрах в секунду, то энергия связи будет измерена в джоулях. Однако в физике атома и атомного ядра энергию ядер и элементарных частиц чаще выражают в мегаэлектронвольтах (МэВ).
Энергетический эквивалент 1 а.е.м.
Поэтому энергию связи можно рассчитать следующим образом:
В этом случае энергия связи измеряется в мегаэлектронвольтах (МэВ).
Для характеристики прочности ядра используется величина, которая называется удельной энергией связи.
Удельная энергия связи – это энергия связи ядра, приходящаяся на один нуклон ядра:
где ( A ) – массовое число.
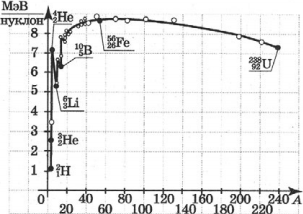
Удельная энергия связи неодинакова для разных химических элементов и даже для изотопов одного и того же химического элемента. Удельная энергия связи нуклона в ядре меняется в среднем в пределах от 1 МэВ у легких ядер до 8,6 МэВ у ядер средней массы (с массовым числом ( A ) ≈ 100). У тяжелых ядер (( A ) ≈ 200) удельная энергия связи нуклона меньше, чем у ядер средней массы, приблизительно на 1 МэВ, так что их превращение в ядра среднего веса (деление на 2 части) сопровождается выделением энергии в количестве около 1 МэВ на нуклон, или около 200 МэВ на ядро. Превращение легких ядер в более тяжелые ядра дает еще больший энергетический выигрыш в расчете на нуклон.
Зависимость удельной энергии связи от массового числа установили экспериментально. Из рисунка хорошо видно, что, не считая самых легких ядер, удельная энергия связи примерно постоянна и равна 8 МэВ/нуклон. Отметим, что энергия связи электрона и ядра в атоме водорода, равная энергии ионизации, почти в миллион раз меньше этого значения. Кривая на рисунке имеет слабо выраженный максимум. Максимальную удельную энергию связи (8,6 МэВ/нуклон) имеют элементы с массовыми числами от 50 до 60, т. е. железо и близкие к нему по порядковому номеру элементы. Ядра этих элементов наиболее устойчивы.
У тяжелых ядер удельная энергия связи уменьшается за счет возрастающей с увеличением ( Z ) кулоновской энергии отталкивания протонов. Кулоновские силы стремятся разорвать ядро.
Ядерные реакции. Деление и синтез ядер
Атомные ядра при взаимодействиях испытывают превращения. Эти превращения сопровождаются увеличением или уменьшением кинетической энергии участвующих в них частиц.
Ядерные реакции – это изменения атомных ядер при взаимодействии их с элементарными частицами или друг с другом.
Ядерные реакции происходят, когда частицы вплотную приближаются к ядру и попадают в сферу действия ядерных сил. Одноименно заряженные частицы отталкиваются друг от друга, поэтому сближение положительно заряженных частиц с ядрами (или ядер друг с другом) возможно, если этим частицам (или ядрам) сообщена достаточно большая кинетическая энергия. Эта энергия сообщается протонам, ядрам дейтерия, α-частицам и другим более тяжелым ядрам с помощью ускорителей.
Для осуществления ядерных реакций такой метод гораздо эффективнее, чем использование ядер гелия, испускаемых радиоактивными элементами. Во-первых, с помощью ускорителей частицам может быть сообщена энергия порядка 105 МэВ, т. е. гораздо большая той, которую имеют ( alpha )-частицы (максимально 9 МэВ). Во-вторых, можно использовать протоны, которые в процессе радиоактивного распада не появляются (это целесообразно потому, что заряд протонов вдвое меньше заряда α-частиц, и поэтому действующая на них сила отталкивания со стороны ядер тоже в 2 раза меньше). В-третьих, можно ускорить ядра более тяжелые, чем ядра гелия.
Наиболее распространенный вид ядерной реакции:
где ( X ) и ( Y ) – исходное и конечное ядра; ( a ) и ( b ) – бомбардирующая и испускающая частицы.
Эндотермическая реакция – это реакция с поглощением энергии:
Экзотермическая реакция – это реакция с выделением энергии:
При ядерных реакциях выполняются следующие законы.
- Закон сохранения электрического заряда:
сумма электрических зарядов атомных ядер и частиц до реакции равна сумме электрических зарядов атомных ядер и частиц после реакции:
- Закон сохранения массового числа:
сумма нуклонов атомных ядер и частиц до реакции равна сумме нуклонов атомных ядер и частиц после реакции:
- Закон сохранения энергии.
Примеры ядерных реакций
- Первое наблюдавшееся превращение ядра (Ю. Резерфорд, 1919):
- Первая ядерная реакция на быстрых протонах (1932):
- Открытие нейтрона (Дж. Чедвик, 1932):
- Первое искусственное получение радиоактивного распада и открытие позитрона. Радиоактивный распад под действием ( alpha )-частиц наблюдал Ф. Жолио-Кюри:
Изотоп фосфора оказался радиоактивным: его ядро распадается с испусканием позитрона и нейтрино:
Классификация ядерных реакций
Ядерные реакции классифицируются:
- по роду участвующих в них частиц – реакции под действием нейтронов, заряженных частиц, ( gamma )-квантов;
- по энергии вызывающих их частиц – реакции при малых, средних, высоких энергиях;
- по роду участвующих в них ядер – реакции на легких ядрах (А < 50), средних ядрах (50 < А < 100) и тяжелых ядрах (А > 100);
- по характеру происходящих ядерных превращений – реакции с испусканием нейтронов, заряженных частиц, реакции захвата.
Деление ядер – это деление атомного ядра урана на несколько более легких ядер (осколков), чаще всего на два ядра, близких по массе.
- Делиться могут только ядра некоторых тяжелых элементов.
- При делении ядер испускаются нейтроны и ( gamma )-лучи.
- При делении ядер выделяется большая энергия.
Механизм деления ядер (капельная модель)
В тяжелых ядрах действуют значительные ядерные силы, которые удерживают ядро от распада. Под влиянием поглощенного нейтрона ядро возбуждается и начинает деформироваться, приобретая вытянутую форму. Оно растягивается до тех пор, пока силы отталкивания половинок ядра не начинают преобладать над силами притяжения, действующими в перешейке. В результате ядро разрывается на два осколка X и Y.
Под действием сил кулоновского отталкивания осколки разлетаются со скоростью, равной приблизительно 1/30 скорости света. Одновременно испускается излучение высокой частоты.
Цепная ядерная реакция – ядерная реакция деления тяжелых ядер нейтронами, в результате которой число нейтронов возрастает и поэтому может возникнуть самоподдерживающийся процесс деления.
В 1939 году было обнаружено, что при попадании нейтрона в ядро изотопа урана-235 происходит деление ядра на два или три осколка с испусканием 2–3 нейтронов:
Эти нейтроны способны вызвать деление 2–3 новых ядер урана с испусканием 4–9 новых нейтронов и т. д., процесс может продолжаться самостоятельно, вовлекая все большее число новых ядер.
Условия протекания цепной ядерной реакции:
- должны отсутствовать примеси, поглощающие нейтроны;
- количество вещества, способного делиться, должно быть достаточным для того, чтобы образующиеся нейтроны могли соударяться с другими ядрами, не покидая объем, не испытывая взаимодействия;
- скорость нейтронов должна быть достаточной, чтобы вызвать деление ядер.
Минимальное количество вещества, необходимое для осуществления цепной ядерной реакции, называется критической массой.
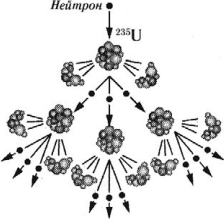
Устройства, в которых осуществляются управляемые цепные ядерные реакции, называются ядерными реакторами.
Основные элементы ядерного реактора:
- Ядерное горючее (сырьевые и делящиеся вещества в реакторах – изотопы урана, плутоний, торий).
- Замедлитель и отражатель нейтронов, которые способствуют увеличению числа медленных нейтронов, наиболее эффективных для развития цепной реакции деления (графит, тяжелая или обычная вода).
- Регулирующие стержни, которые вводят в активную зону реактора для поддержания стационарного режима реактора, так как быстрое развитие реакции сопровождается выделением большого количества тепла и перегревом реактора; стержни выполнены из материалов, сильно поглощающих тепловые нейтроны (из бора, кадмия).
- Теплоноситель, который необходим для отвода тепла, образующегося в реакторе (вода, жидкий натрий и др.).
- Защитные устройства, которые применяют для защиты персонала, обслуживающего реактор, от действия на организм нейтронных потоков и ( gamma )-лучей.
Термоядерный синтез
График зависимости удельной энергии связи нуклонов в ядре от массового числа показывает, что кроме реакции деления тяжелых ядер с выделением энергии идут реакции синтеза легких ядер.
Синтез ядер – это слияние ядер в одно ядро, сопровождающееся выделением энергии.
Для осуществления реакции синтеза легких ядер требуются высокие энергии сливающихся частиц, так как необходимо преодолеть кулоновское отталкивание. Этого можно достичь за счет высокой температуры вещества.
Термоядерная реакция – это реакция синтеза легких атомных ядер в более тяжелые, происходящая при сверхвысоких температурах (порядка 107 К и выше).
В природе термоядерные реакции происходят в недрах звезд.
При термоядерном синтезе энергетический выход на единицу массы топлива оказывается выше, чем при реакции деления тяжелых ядер урана.
Пример реакции синтеза:
Синтез гелия из тяжелых изотопов водорода – дейтерия и трития – происходит при температуре около 5·107 К.
При синтезе 1 г гелия из дейтерия и трития выделяется 4,2·1011 Дж – такая же энергия выделяется при сгорании 10 т дизельного топлива.
Термоядерный синтез может стать одним из возможных альтернативных источников энергии. Поиск таких источников энергии важен, так как запасы нефти и газа на Земле ограничены.
В настоящее время ведется испытание установок для осуществления управляемых термоядерных реакций синтеза гелия из водорода. Запасы водорода на Земле практически неисчерпаемы. Количество дейтерия в океанической воде составляет примерно 4·1011 т, чему соответствует энергетический запас 1017 МВт·год. Наиболее заманчивой является возможность извлечения энергии дейтерия, содержащегося в обычной воде.
Основные формулы по теме «Физика атомного ядра»
Физика атомного ядра
3.1 (61.41%) 128 votes
Радиоактивность.
Автор — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев.
Темы кодификатора ЕГЭ : радиоактивность, альфа-распад, бета-распад, гамма-излучение, закон радиоактивного распада.
Явление радиоактивности обнаружил французский физик Анри Антуан Беккерель, и произошло это совершенно случайно.
В начале 1896 года всё научное сообщество было охвачено интересом к недавно открытым всепроникающим рентгеновским лучам. Беккерель решил выяснить, не появляются ли рентгеновские лучи при освещении солнечным светом некоторых минералов, и выбрал для своих экспериментов весьма редкую соль урана.
Опыт Беккереля был чрезвычайно прост. Кристаллы соли выставлялись на солнце и лежали при этом на фотопластинке. Разумеется, фотопластинка заворачивалась в чёрную бумагу, чтобы её не засветил солнечный свет. Но чёрная бумага — не помеха рентгеновским лучам, и если они действительно возникают, то засветят фотопластинку.
Итак, Беккерель положил завёрнутую фотопластинку с насыпанной поверх урановой солью на солнечный свет, подержал несколько часов и затем проявил фотопластинку. Ожидания подтвердились! После проявления на фотопластинке проступили очертания кристаллов соли урана.
Полагая, что и впрямь обнаружись рентгеновские лучи, испускаемые урановой солью под действием солнечного света, Беккерель доложил об этом на заседании Французской академии. Доклад вызвал большой интерес, и было решено, что на следующем заседании, то есть через неделю, Беккерель расскажет о результатах новых опытов.
А погода тем временем испортилась, и солнце на всю неделю скрылось за облаками. Медный крест, покрытый урановой солью и приготовленный для опытов, в ожидании солнца несколько дней пролежал в ящике письменного стола — поверх фотопластинки, завёрнутой в чёрную бумагу.
Накануне нового доклада облачность так и не рассеялась, и докладывать Беккерелю было нечего. Однако отчаяние и удачу порой разделяет лишь один шаг. Неизвестно почему, но Беккерель решил проявить фотопластинку, лежавшую в столе. Каково же было его удивление, когда он увидел проступившие на ней почернения в виде отчётливой тени креста!
Таким образом, солнце оказалось совершенно ни при чём. Было обнаружено новое явление природы: урановая соль без каких-либо внешних факторов, сама по себе испускает некоторое излучение, пронизывающее чёрную бумагу.
На следующий день Беккерель доложил об этом на заседании Французской академии и затем приступил к интенсивным исследованиям. В ходе своих экспериментов он обнаружил мследующие черты нового явления.
-Новые лучи могут проникать сквозь предметы и ионизировать воздух.
-Засвечивают фотопластинку только те вещества, которые содержат уран.
-Интенсивность излучения зависит только от количества урана в веществе. Само химическое соединение при этом роли не играет. Максимально интенсивным является излучение чистого урана.
Новое явление было впоследствии названо радиоактивностью. Из опытов Беккереля следовало, что радиоактивность есть свойство химического элемента урана самого по себе — то есть свойство, которым обладают атомы урана.
Уран оказался не единственным радиоактивным элементом. Мария Склодовская-Кюри спустя два года после открытия Беккереля обнаружила аналогичное излучение тория. Вместе с мужем, Пьером Кюри, они открыли новый радиоактивный химический элемент — полоний. Наконец, вручную переработав 11 тонн руды, Мария Склодовская-Кюри получила маленькую капельку чистого радия, который излучал в три миллиона раз интенсивнее урана.
Виды радиоактивных излучений.
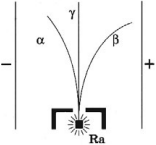
Каков состав радиоактивного излучения? Оказалось, что радиоактивные вещества испускают три типа лучей, различающихся по своим физическим свойствам. Эти три компоненты обнаруживаются в результате пропускания радиоактивного излучения солей урана через сильное магнитное поле (рис. 1).
 |
| Рис. 1. Виды радиоактивных излучений |
А именно, излучение радиоактивного препарата, находящегося внутри свинцового контейнера с узким каналом, направляется на фотопластинку. В отсутствии магнитного поля на фотопластинке наблюдается одно тёмное пятно. Но если пропустить излучение сквозь область магнитного поля, то пятен становится три — одно на прежнем месте и два по бокам от него на разных расстояниях. Это означает, что радиоактивное излучение в магнитном поле распалось на три существенно различные части.
То, что две компоненты отклонились в разные стороны, означает, что они являются соответственно потоками положительных и отрицательных зарядов. Третья компонента, не отклоняющаяся магнитным полем, электрического заряда не несёт.
Положительно заряженной компоненте была присвоена буква ; её называли
-излучением,
-лучами или потоком
-частиц. Альфа-лучи достаточно слабо отклонялись магнитным полем. Тщательные исследования Резерфорда показали, что
-частицы — это полностью ионизованные атомы гелия, то есть ядра гелия.
Отрицательно заряженная компонента была названа -излучением (или
-лучами
). Они отклонялись магнитным полем значительно сильнее, чем -частицы. Бета-лучи оказались потоком электронов, мчащихся со скоростями, близкими к скорости света.
Нейтральная компонента получила название -излучения (или
-лучей). (Электромагнитная природа гамма-излучения была установлена экспериментально: обнаружилась дифракция гамма-лучей на кристаллических решётках. Эти же опыты позволили измерить и длину волны гамма-излучения. Гамма-лучи оказались электромагнитными волнами чрезвычайно высокой частоты — выше, чем у рентгеновского излучения.) Соответственно, проникающая способность гамма-лучей также больше, чем у рентгеновских лучей.
Среди трёх компонент радиоактивного излучения наибольшей проникающей способностью также обладают гамма-лучи — они могут пробиться сквозь слой свинца толщиной в несколько сантиметров. Сильнее поглощаются веществом бета-лучи: тут хватит нескольких миллиметров свинца, чтобы поглотить их полностью. Слабее всего проникают сквозь вещество -частицы: они не могут, например, пройти через лист бумаги
Радиоактивные превращения.
Многочисленные эксперименты с радиоактивными веществами показали, что радиоактивность сопровождается изменениями атомов, и в результате этих изменений одни химические элементы превращаются в другие.
Положение химического элемента в таблице Менделеева определяется числом электронов в нейтральном атоме, или, что то же самое — зарядом ядра атома. Поэтому превращения химических элементов означают, что в результате радиоактивных процессов изменения претерпевают атомные ядра.
Ядра атомов радиоактивных элементов являются нестабильными. Каждое такое ядро в некоторый момент распадается, поэтому явление радиоактивности называют ещё радиоактивным распадом.
В процессе радиоактивного распада исходное вещество постепенно исчезает. Новые вещества, являющиеся продуктами распада, также могут быть нестабильными и распадаться дальше. Наблюдаются целые цепочки радиоактивных распадов — вплоть до образования стабильных элементов.
Самой известной такой цепочкой является радиоактивное семейство урана. Начинается эта цепочка с альфа-распада ядра , в результате которого образуется ядро тория
и вылетает
-частица:
. (1)
Затем родившееся ядро тория испытывает бета-распад, испуская электрон и превращаясь в ядро протактиния :
. (2)
Обратите внимание, что электрону приписывается зарядовое число -1 (так как заряд электрона равен -e) и массовое число 0 (так как электрон не содержит нуклонов).
В обеих формулах (1) и (2) мы наблюдаем два важных момента.
-Сумма массовых чисел продуктов распада равна массовому числу исходного ядра. Этот баланс массовых чисел отражает неизменность общего числа нуклонов до и после распада.
-Сумма зарядовых чисел продуктов распада равна зарядовому числу исходного ядра. Этот факт служит одним из многочисленных экспериментальных подтверждений закона сохранения заряда.
Поскольку -частица уносит заряд +2e, а электрон уносит заряд -e , то возникает следующая закономерность превращения химических элементов при
— и
-распадах.
Правило смещения. После -распада элемент смещается на две клетки назад, то есть к началу периодической системы. После
-распада элемент смещается на одну клетку вперёд, то есть к концу периодической системы.
Общие формулы, выражающие правило смещения при альфа- и бета-распадах, выглядят так:
,
.
Формулы (1) и (2) — это самое начало радиоактивного семейства урана. Всего в этой цепочке происходит восемь -распадов и шесть
-распадов (причём при каждом
-распаде вдобавок излучается
-квант), пока в самом конце цепочки не образуется стабильное ядро свинца
.
Излучение всех элементов радиоактивного семейства урана как раз и засветило фотопластинку Беккереля, и именно эта смесь излучений была впервые разложена на компоненты в магнитном поле (рис. 1).
Закон радиоактивного распада.
Нестабильное ядро распадается самопроизвольно (или, как ещё говорят, спонтанно). Происходит это в случайный момент времени, так что невозможно предсказать, когда именно распадётся каждое конкретное ядро.Тем не менее, ядра каждого элемента обладают определённым средним временем жизни, характерным для данного элемента.
А именно, опыт показывает, что распад радиоактивного элемента происходит со строго определённой, присущей именно этому элементу скоростью. Скорость распада у разных элементов различна; она является такой же неотъемлемой характеристикой радиоактивного элемента, как зарядовое или массовое число. Вне зависимости от условий опыта можно точно сказать, спустя какой промежуток времени интенсивность излучения данного элемента уменьшится, например, в два раза.
Период полураспада — это время, в течение которого распадается половина имеющихся радиоактивных атомов. Период полураспада как раз и является количественной характеристикой скорости радиоактивного распада.
Величина периода полураспада может быть очень разной. Например, период полураспада урана равен 4,5 млрд. лет, радия
— 1600 лет, полония
-138 дней, а у инертного газа радона
— он составляет всего 3,8 суток.
Выведем теперь закон радиоактивного распада, а именно — найдём, как зависит от времени количество атомов, не претерпевших пока радиоактивный распад. Начальное число радиоактивных атомов равно
, период полураспада равен
.
Имеем следующую простую цепочку рассуждений.
Спустя время количество оставшихся атомов будет равно
.
Спустя время атомов останется
.
Спустя время атомов останется
.
Становится ясно, что спустя время атомов останется
.
Поставляя сюда , получим:
.
Отбрасывая индекс k, находим число оставшихся атомов в зависимости от времени:
. (3).
Мы получили закон радиоактивного распада. Количество нераспавшихся атомов оказывается показательной функцией, убывающей с течением времени.
Непосредственной характеристикой скорости распада радиоактивного элемента является активность — число радиоактивных распадов, происходящих в единицу времени. Активность есть производная по времени от числа
распавшихся атомов:
.
Обозначая множитель перед показательной функцией через (это будет активность в начальный момент времени), получим:
.
Мы видим, что зависимость активности от времени имеет точно такой же вид, как и закон радиоактивного распада (3). График зависимости активности от времени приведён на рис. 2.
 |
| Рис. 2. Зависимость активности от времени |
Ясно, что активность убывает тем быстрее, чем меньше период полураспада. И наоборот, при большом периоде полураспада активность меняется медленно. Например, активность радона (T= 3,8 суток) уменьшается буквально на глазах, а активность солей урана (T= 4,5 млрд.лет) остаётся практически неизменной на протяжении человеческой жизни.
Благодарим за то, что пользуйтесь нашими материалами.
Информация на странице «Радиоактивность.» подготовлена нашими авторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать нужные и поступить в высшее учебное заведение или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
08.03.2023
Атомная физика на ОГЭ. Вся теория и разбор заданий от преподавателя MAXIMUM
06.02.2021
17404
Атомная физика — один из труднейших разделов экзамена, а задания по этой теме кочуют из варианта в вариант каждый год. Не пугаемся! Для решения заданий ОГЭ на радиоактивность, распады и ядерные реакции нужно знать лишь самые базовые понятия. Из этой статьи вы узнаете все необходимое — атомная физика на ОГЭ обязательно вам покорится!
Чтобы перейти к практике и научиться решать хитрые задания, сначала нужно вспомнить теорию, связанную с ними.
Вспомним, что химические элементы обозначаются в виде , где
- X – название химического элемента
- А – массовое число, равное сумме протонов и нейтронов
- Z – зарядовое число, равное числу протонов в ядре
Давайте раз и навсегда узнаем, что скрывается за числами рядом с названием каждого элемента. Рассмотрим пример углерода:
- 6 — это порядковый номер и зарядовое число Z. Таким образом, в ядре атома углерода 6 протонов. Z=6.
- 12,011 — это атомная масса. Мы будем его округлять до 12 и называть массовым числом A, то есть суммой протонов и нейтронов. A=12.
- Получается, в ядре атома углерода 6 протонов и 6 нейтронов.
Какие ядерные распады нужно знать?
На ОГЭ часто встречаются три типа распадов: альфа, бета и гамма.
Альфа-распад
α-распад — испускание ядром альфа-частицы. Что это такое? Все просто — так называют ядро атома гелия, то есть частицу из двух протонов и двух нейтронов.
- У нас был элемент X с массовым числом A и с зарядовым числом Z
- Атом испускает альфа-частицу с массовым числом=4 и зарядовым числом=2
- Мы получаем новый элемент с массовым числом=A-4 и зарядовым числом=Z-2
В α-распаде заряд уменьшается на 2, а масса уменьшается на 4.
Самостоятельно подготовиться к ОГЭ непросто. На то, чтобы разобраться со всеми темами, понадобится много времени. Но и это не решит проблему! Например, если вы запомнили какое-то решение из интернета, а оно оказалось неправильным, можно на пустом месте потерять баллы. Если хотите научиться решать все задания ОГЭ по физике, обратите внимание на онлайн-курсы MAXIMUM! Наши специалисты уже проанализировали сотни вариантов ОГЭ и подготовили для вас вас максимально полезные занятия.
Приходите к нам на пробный урок! Вы узнаете всю структуру ОГЭ-2021, разберете сложные задания из первой части, получите полезные рекомендации и узнаете, как устроена подготовка к экзаменам в MAXIMUM. Все это абсолютно бесплатно!
Задача №1
Используя фрагмент Периодической системы элементов Д.И. Менделеева, представленный на рисунке, определите, какое ядро образуется в результате α-распада ядра нептуния-237.
Разбор
- Как мы говорили чуть выше, порядковый номер элемента — это, по совместительству, зарядовое число. То есть, количество протонов. Получается, в Нептунии 93 протона.
- У α-частицы количество протонов = 2.
- Посчитаем, чему равно зарядовое число нашего нового элемента: зарядовое число = 93-2 = 91. Взглянув на табличку, находим элемент под номером 91 — Протактиний.
Ответ: 1) Ядро протактиния
Изотопы
Теперь давай обратим внимание на массовые числа нептуния и протактиния. Отличаются ли они на массовое число альфа-частицы — на 4?
237-231=6
Время бить тревогу! Неужели мы что-то напутали и решили задачу неверно? Но нет, оказывается, мы все сделали правильно — ведь у протактиния более 15 изотопов.
Изотопы — это разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковое зарядовое число, но разные массовые числа.
Например, изотопы азота:
и
Задача №2
Ядро тория превратилось в ядро радия
. Какую частицу испустило при этом ядро тория?
- нейтрон
- протон
- альфа-частицу
- бета-частицу
Разбор
- Сверху находится массовое число — масса частицы. Вычтем из массы Тория массу Радия: 230-226=4. Получили массу неизвестной частицы.
- Снизу находится зарядовое число — это заряд неизвестной частицы. Вычтем из заряда Тория заряд Радия: 90-88=2. Получили заряд неизвестной частицы.
- Итого: массовое число = 4. Зарядовое число = 2
- Взглянем на табличку самых распространенных частиц.
Вуаля! Наша незнакомка — это альфа-частица — частица с двумя протонами и двумя нейтронами.
Ответ: 3) альфа-частица
Бета-распад
β-распад — испускание ядром бета-частицы. Бета-частицей называют электрон. Посмотрим в списке основных частиц наверху, чему равны массовое и зарядовое число бета-частицы (электрона).
- У нас был элемент X с массовым числом A и с зарядовым числом Z
- Атом испускает бета-частицу с массовым числом=0 и зарядовым числом=-1
- Мы получаем новый элемент с прежним массовым числом=A и зарядовым числом=Z+1
В β-распаде заряд увеличивается на 1, а масса не меняется.
Задача №3
Изотоп криптона в результате серии распадов превратился изотоп молибдена . Сколько β-частиц было испущено в этой серии распадов?
Разбор
- Обозначим количество испущенных β-частиц за N
- Зарядовое число криптона до серии β-распадов равнялось 36
- Зарядовое число молибдена после серии β-распадов 42
- Тогда 42-36=6 β распадов
Ответ: было испущено 6 β распадов
Задача №4
Радиоактивный атом превратился в атом
в результате цепочки альфа- и бета-распадов. Чему было равно число альфа- и бета-распадов?
Разбор
Эта задача требует максимальной концентрации — многие школьники ее решают неверно. Давайте разберем правильный подход к этой задаче.
- Для начала рассмотрим альфа-распады
- Добьемся, чтобы массовое число изменилось с 232 до 208. Для этого производим альфа-распады, вычитая 4 из массового числа и 2 из зарядового числа.
- Получили элемент с массовым числом=208 и зарядовым числом=78. Для этого мы произвели 6 альфа распадов.
- Теперь перейдем к бета-распадам. Бета-распады влияют только на зарядовое число.
- Добьемся того, чтобы зарядовое число изменилось с 78 до 82.
- Получили элемент с массовым числом = 208 и зарядовым числом = 82. Для этого мы произвели 4 бета распада.
Ответ: 6 альфа распадов и 4 бета распада.
Гамма-распад
?-частицы — это излучение, а ?-распад — испускание ядром гамма-излучения. Пожалуй, это самый простой распад, потому что он ничего не меняет.
Элемент X до распада и элемент Y после распада — это одно и то же.
Внимание! На ОГЭ ученики часто попадают в ловушки экзамена, считая, что ? излучение меняет элемент. Но это совсем не так! Какой элемент был до гамма-распада, такой и останется.
При ?-распаде заряд и масса не меняются.
Ядерные реакции
Атомная физика на ОГЭ включает в себя не только распады, но и ядерные реакции. Ядерные реакции происходят при столкновении ядер или элементарных частиц с другими ядрами. В результате изменяется массовое и зарядовое число элементов, появляются новые частицы.
Во всех ядерных реакциях работает очень простой лайфхак: при протекании ядерной реакции сохраняется суммарное массовое число и суммарный заряд.
Сумма масс слева равна сумме масс справа: A1+A2=A3+A4.
Сумма зарядов слева равна сумме зарядов справа: Z1+Z2=Z3+Z4.
Сразу же закрепим эти правила на практике.
Задача 5
В результате столкновения ядра урана с частицей X произошло деление урана, описываемое реакцией:
Определите зарядовое и массовое числа частицы X, с которой столкнулось ядро урана.
Разбор
- Сначала разберемся с массовым числом. Используем лайфхак: то, что слева, равно тому, что справа.
- Также заметим, что у нас 3 нейтрона. Получается, нам нужно умножить массовое число нейтрона на 3.
- С гамма-частицей разобраться легко — как мы показали ранее, она ни на что не влияет.
A+235 = 133+139+3*1
Отсюда A=133+139+3-235=40
- Теперь настал черед зарядового числа.
Z+92 = 36+56+3*0
Отсюда Z=36+56+0-92=0
Ответ: получили элемент X c массовым числом 40 и зарядовым числом 0.
Атомная физика на ОГЭ: что нужно запомнить?
- В α-распаде заряд уменьшается на 2, а масса уменьшается на 4.
- α-частица — это ядро атома гелия. α-частица состоит из двух протонов и двух нейтронов.
- В β-распаде заряд увеличивается на 1, а масса не меняется.
- β-частица — это электрон.
- В ?-распаде заряд и масса не меняются.
- ?-частица — это порция электромагнитного излучения.
- Изотопы — это разновидности атомов (и ядер) какого либо химического элемента, которые имеют одинаковое зарядовое число, но разные массовые числа.
- В ядерных реакциях сохраняется суммарное массовое число и суммарный заряд.
Теперь вы знаете, как решать задания на ядерные распады и реакции! Надеюсь, атомная физика на ОГЭ стала для вас намного понятнее. Если хотите разобраться в остальных темах по физике и не только, обратите внимание на наши онлайн-курсы. Уже более 150 тысяч выпускников подготовились с нами к ОГЭ и ЕГЭ. Кстати, у меня на курсах MAXIMUM тоже можно поучиться! Приходите на бесплатный пробный урок, чтобы познакомиться с нашей образовательной системой и узнать массу полезного про ОГЭ.
Лайфхаки экзамена
К рубрике
Радиоактивность. Излучения. Распад
Раздел ОГЭ по физике: 4.1. Радиоактивность. Альфа-, бета-, гамма-излучения. Реакции альфа- и бета-распада.
Радиоактивностью называют явление самопроизвольного излучения некоторых химических элементов, а вид этого излучения называют радиоактивным излучением. Первым радиоактивное излучение обнаружил Анри Беккерель, который, проводя эксперименты с солями урана, по почернению фотопластинки установил, что они самопроизвольно испускают невидимое излучение сильной проникающей способности. В дальнейшем было обнаружено, что не только уран, но и такие элементы, как радий и полоний, тоже испускают невидимое излучение.
Радиоактивность, которой обладают вещества, существующие в природе, называют естественной радиоактивностью. Она проявляется у всех элементов таблицы Д.И. Менделеева, порядковый номер которых больше 83. В дальнейшем было установлено, что и некоторые искусственно полученные вещества радиоактивны.
Резерфорд, изучая радиоактивное излучение, обнаружил его сложный состав. Он поместил радиоактивный препарат в свинцовый сосуд с отверстием. Над сосудом расположил фотопластинку, на которую падало радиоактивное излучение, выходившее через отверстие и прошедшее через магнитное поле.
Когда фотопластинку проявили, то на ней обнаружили три тёмных пятна. Одно пятно располагалось точно напротив отверстия. Это значит, что магнитное поле на него не действовало и заряженных частиц в этом излучении нет. Его назвали гамма-излучением (γ-излучение). Гамма-излучение представляет собой электромагнитное излучение или поток фотонов.
Наличие двух боковых пятен по разную сторону от центрального означает, что существуют два излучения, состоящие из частиц, имеющих заряды противоположных знаков. Эксперимент показывает, что одно из них представляет собой поток положительно заряженных частиц. Их назвали α-частицами. Другое излучение состоит из отрицательно заряженных частиц. Их назвали β-частицами.
Изучение этих излучений позволило сделать вывод, что α-частицы — это ядра атома гелия. Их массовое число — 4, а зарядовое число (электрический заряд) +2, т.е.
β-частицы представляют собой электроны. Их массовое число равно 0, а зарядовое число равно –1, т.е.
Радиоактивный распад
Радиоактивные элементы, испуская излучение, превращаются в другие элементы. При этом, поскольку излучение приводит к появлению нового химического элемента, можно сделать вывод, что изменения происходят именно с ядром атома. Радиоактивное превращение ядер одних элементов в ядра других элементов называют радиоактивным распадом. Существует три вида радиоактивного распада: альфа–, бета– и гамма–излучения.
Альфа–распад. Превращение атомных ядер, сопровождаемое испусканием альфа–частиц (ядер гелия ).
Если – материнское ядро, то превращение этого ядра при альфа–распаде происходит по следующей схеме (правило смещения):
, где
– символ дочернего ядра;
– ядро атома гелия.
При альфа–распаде происходит смещение химического элемента на две клетки влево в таблице Менделеева.
Бета–распад. Радиоактивные ядра могут выбрасывать поток электронов, которые рождаются, согласно гипотезе Ферми, в результате превращения нейтронов в протоны. В соответствии с правилом смещения массовое число ядра не изменяется: .
При бета–распаде химический элемент перемещается на одну клетку вправо в периодической системе Менделеева и, кроме электронов, испускается антинейтрино.
Гамма–излучение. Возникает при ядерных превращениях и представляет собой электромагнитное излучение. Имеет высокую энергию.
Э. Резерфорд установил, что воздух сильнее всего ионизуют альфа–лучи, в меньшей степени – бета–лучи и совсем плохо – гамма–лучи. Поэтому проникающая способность оказалась самая малая у альфа–лучей (лист бумаги, несколько сантиметров слоя воздуха), а бета–лучи проходят сквозь алюминиевую пластину толщиной в несколько миллиметров. Очень велика проникающая способность у гамма–лучей (например, для алюминия – пластины толщиной в десятки сантиметров).
Период полураспада
В процессе радиоактивного распада число радиоактивных атомов уменьшается. Распад разных радиоактивных веществ происходит с разной интенсивностью. Например, радиоактивные изотопы йода распадаются значительно быстрее, чем изотопы стронция. Характеристикой интенсивности радиоактивного распада является величина, называемая периодом полураспада.
Периодом полураспада Т называют промежуток времени, в течение которого распадается половина первоначального числа атомов радиоактивного вещества. Чем меньше период полураспада, тем быстрее распадутся все радиоактивные атомы.
Например, имеется 4 • 108 атомов радиоактивного изотопа йода, период полураспада которого 25 минут. Это означает, что в течение 25 минут распадается половина ядер изотопа иода, т.е. 2 • 108 ядер, а 2 • 108 ядер останется нераспавшимися. Еще через 25 минут нераспавшимися останется 108 ядер йода, еще через 25 минут — 0,5 • 108 ядер и так далее.
Особенностью закона радиоактивного распада является то, что невозможно предсказать, когда произойдет распад каждого конкретного атома. Оно может произойти во время одного периода полураспада, или двух, или трех. Период полураспада относится не к конкретному атому, а к совокупности атомов радиоактивного вещества.
Конспект урока «Радиоактивность. Излучения».
Следующая тема: «Опыты Резерфорда. Планетарная модель атома».
Альфа-
бета- и гамма- распады (подготовка к ОГЭ по физике, теория, 9 кл.)
Однако ядра атомов радиоактивных
веществ в процессе радиоактивного распада самопроизвольно превращаются в ядра
атомов других веществ. Так в 1903 году Резерфорд обнаружил, что помещенный в
сосуд радий через некоторое время превратился в радон. А в сосуде дополнительно
появился гелий:
(88^226)Ra→(86^222)Rn+(2^4)He.
Удалось установить, что
основные виды радиоактивного распада: альфа и бета-распад происходят согласно
следующему правилу смещения:
Альфа-распад
При
альфа-распаде излучается α-частица (ядро атома гелия). Из вещества с
количеством протонов Z и нейтронов N в атомном ядре оно превращается в вещество
с количеством протонов Z-2 и количеством нейтронов N-2 и, соответственно,
атомной массой А-4:
(Z^A)X→(Z-2^(A-4))Y
+(2^4)He.
То
есть происходит смещение образовавшегося элемента на две клетки назад в
периодической системе.
Пример
α-распада: (92^238)U→(90^234)Th+(2^4)He.
Альфа-распад
– это внутриядерный процесс. В составе тяжелого ядра за счет
сложной картины сочетания ядерных и электростатических сил образуется
самостоятельная α-частица, которая выталкивается кулоновскими силами гораздо
активнее остальных нуклонов. При определенных условиях она может преодолеть
силы ядерного взаимодействия и вылететь из ядра.
Бета-распад
При
бета-распаде излучается электрон (β-частица). В результате распада одного
нейтрона на протон, электрон и антинейтрино, состав ядра увеличивается на один
протон, а электрон и антинейтрино излучаются вовне:
(Z^A)X→(Z+1^A)Y+(-1^0)e+(0^0)v.
Соответственно, образовавшийся элемент смещается в периодической системе на
одну клетку вперед.
Пример
β-распада: (19^40)K→(20^40)Ca+(-1^0)e+(0^0)v.
Бета-распад
– это внутринуклонный процесс. Превращение претерпевает нейтрон.
Существует также бета-плюс-распад или позитронный бета-распад.
При позитронном распаде ядро испускает позитрон и нейтрино, а элемент смещается
при этом на одну клетку назад по периодической таблице. Позитронный бета-распад
обычно сопровождается электронным захватом.
Гамма-распад
Кроме альфа и бета-распада
существует также гамма-распад. Гамма-распад – это излучение гамма-квантов
ядрами в возбужденном состоянии, при котором они обладают большой по сравнению
с невозбужденным состоянием энергией. В возбужденное состояние ядра могут
приходить при ядерных реакциях либо при радиоактивных распадах других ядер.
Большинство возбужденных состояний ядер имеют очень непродолжительное время
жизни – менее наносекунды.
The process of spontaneous disintegration of some unstable atomic nuclei is known as radioactivity. In other words, the phenomenon of spontaneous emission of radiations by heavy elements is called radioactivity. The elements which show this phenomenon is called radioactive elements. Radioactivity is a continuous and irreversible nuclear phenomenon.
- Radioactivity was discovered by Henry Becquerel in uranium salt in the year 1896.
- After the discovery of radioactivity in Uranium, Pierre Curie and Madame Curie discovered a new radioactive element called radium.
- Some examples of radioactive substances are Uranium, Radium, Thorium, Neptunium, etc.
- The radioactivity of a sample cannot be controlled by any physical ( pressure, temperature, electric or magnetic field) or chemical changes.
- All the elements with atomic number (Z) > 82 and naturally radioactive.
- The conversion of lighter elements into radioactive elements by the bombardment of fast-moving particles is called artificial or induced radioactivity.
- Radioactivity is a nuclear event and not an atomic one. Hence the electronic configuration of the atom doesn’t have any relation with radioactivity.
When the radiation enters into an external electric field, it splits into three parts: alpha rays, beta rays, and gamma rays.
Alpha (α) Decay
The spontaneous emission of an alpha particle from a radioactive nucleus is called Alpha decay. α decay occurs when the nucleus emits α particles.
This process involves the spontaneous emission of nucleons since α particles (2He4) contain two protons and two neutrons therefore the emission of α particles causes the nucleus to get transmuted into a daughter nucleus having atomic number (Z) two less and atomic mass (A) four less.
Let us consider some examples of α decay:
- 88Ra226 ⇢ 86Rn222 + 2He4
- 92U238 ⇢ 90Th234 + 2He4
- 94Pu242 ⇢ 92U238 + 2He4
Properties of alpha decay:
- Alpha particles have charge +2e and mass 4u.
- Alpha particles have a kinetic energy of 5MeV.
- Nearly 90% of the 2500 known nuclides are radioactive. They are not stable but decay into other nuclides.
- When unstable nuclides decay into different nuclides, they usually emit alpha or beta particles.
- Alpha emission occurs principally with nuclei that are too large to be stable.
- Alpha decay is mainly governed by strong nuclear force and electromagnetic force.
Beta (β) Decay
The spontaneous process of emission of beta particles from a radioactive nucleus is called Beta-decay.
The nucleus achieves greater stability in beta decay. In beta decay, either a neutron is converted into a proton or a proton is converted into a neutron.
The general reaction for beta decay is given as:
ZXA ⇢ Z+1YA+ -1e0
Beta-decay is mainly of three types: Beta-minus (β–), Beta-plus (β+), and electron capture.
Beta-minus (β–)
In beta-minus, the neutron inside the nucleus is converted into a proton and an electron like a particle.
Those nuclei having more neutrons (N) than protons (Z) become unstable and tend to be beta-minus decay (β–). A β– particle is like an electron. The emission of β– involves the transformation of a neutron into a proton, an electron, and a third particle called Antineutrino.
β– decay usually occurs with nuclides for which the neutron-to-proton ratio (N/Z ratio) is too large for stability. In β– decay, N decreases by 1, Z increases by 1 and A remains the same. β– decay can occur whenever the neutral atomic mass of the original atom is larger than that of the final atom.
For Example:
15P32 ⇢ 16S32+ -1e0
Beta-plus (β+)
In a β+ decay, a proton is converted into a neutron and a positron (-1e0 ) is emitted if a nucleus has more protons than neutrons.
Nuclides for which N/Z is too small for stability can emit a positron, the electron’s antiparticle, which is identical to the electron but with a positive charge. The basic process is called beta-plus (β+) decay.
p ⇢ n + β+ + v (v=neutrino)
β+ decay can occur whenever the neutral atomic mass of the original atom is at least two electron masses larger than that of the final atom. There are a few nuclides for which β+ emission is not energetically possible but in which an orbital electron can combine with a proton in the nucleus to form a neutron and a neutrino. The neutron remains in the nucleus and the neutrino is emitted.
For Example:
11Ne22 ⇢ 10Ne22 + -1e0
Electron Capture
Electron capture, nucleus absorbs one of the inner electrons revolving around it and hence a nuclear proton becomes a neutron and a neutrino (v) is emitted.
The process is represented as:
1H1 + -1e0 ⇢ 0n1 + v (v=neutrino)
Electron capture is compatible with a positron emission as both processes lead to the same nuclear transformation. However, electron capture occurs more frequently than positron emission in heavy elements. This is because the orbits of electrons in heavy elements have small radii and hence orbital electrons are very close to the nucleus.
For Example:
54Xe120 + -1e0 ⇢ 53I120 + v
Properties β Decay:
- In a β decay, the neutron inside the nucleus changes into protons, as a result, the charge number remains the same, and the atomic number increases by one.
- In emission of β particle is accompanied by a companion particle having variable energy.
- The companion particle is massless and chargeless and is called Antineutrino.
- The emission of Antineutrino along with β particle conserves the angular momentum during β decay.
- The mass of neutrino and antineutrino is zero. The spin of both is 1/2 in units of h/2π. The charge on both is zero.
- The spin of neutrino is antiparallel to its momentum while that of antineutrino is parallel to its momentum.
Gamma (γ) Decay
It is the spontaneous process of emission of high energy photons from a radioactive nucleus. The emission of alpha and beta particles leave the daughter nucleus in the excited state which in turn emits one or more Gamma-ray photons in single or successive transitions.
Since the gamma rays are emitted by the daughter nucleus emission of gamma rays for the emission of alpha and beta particles. The energy of gamma-ray is equal to the difference between the energy of the excited state or higher energy state and the ground state of the nucleons.
For Example:
- 82Pb210 ⇢ 83Bi210* + -1e0 + Antineutrino
- 83Bi210* ⇢ 83Bi210 + γ-ray
Properties Gamma (γ) Decay:
- When the nucleus is placed in an excited state, either by bombardment with high energy particles or by a radioactive transformation, it can decay to the ground state by emission of one or more photons called gamma rays.
- The order of energy of Gamma Photon is 100 KeV.
- The rest mass of the Gamma Photon is zero.
Terminologies used:
- Antineutrino – It is a very little particle having almost no mass. It is emitted with beta-minus (β–) particles during radioactive decay.
- Positron – It is the antiparticle of an electron. the properties of a positron are the same as that of an electron except a positron carries a positive charge while an electron carries a negative charge.
- Neutrino – It is a very little neutral particle having almost no mass. It is emitted with β+ particles during radioactive decay. It interacts very weakly with materials and hence is not detected easily.
Comparison between Properties of Alpha(α), Beta(β) Particles and Gamma(γ) Rays
|
Property |
Alpha(α) particles |
Beta(β) particles |
Gamma(γ) rays |
|---|---|---|---|
| Charge | Positively Charged particles | Negatively charged particles | Electromagnetic rays. So no charge |
| Speed | 1/100th of the speed of light | 1/10th of the speed of light | Equal to the speed of light |
| Ionization power | Maximum | Less than α particles | Very low less than β particles |
| Penetrating Power | Minimum | More than α particles | Maximum |
| Effect of electric field and magnetic field | Being charged particle, it is deflected by both fields. | Being charged particle, it is deflected by both fields. | Being an Electromagnetic wave, not deflected by both fields. |
| Change in mass number and atomic number | When an alpha particle is emitted by a nucleus its atomic number decreases by 2 and the mass number decreases by 4. | When a beta particle is emitted by the nucleus its atomic number increases by 1 and mass number is unchanged. | Mass number and atomic number are not affected by the emission of gamma rays |
| Nature | Alpha particle is a helium nucleus. | A beta particle is an electron. | It is a wave. |
Sample Questions
Question 1: Write the symbolic expression for β– the decay process of 15P32.
Answer:
The symbolic expression for β– decay process of 15P32 is,
15P32 ⇢ 16X32 + -1e0 + ̅ν
Question 2: Give an example to show that most of the decay energy appears as kinetic energy of α particle.
Answer:
The mass number of alpha emitters is 210, and in the decay of polonium 84Po210, the alpha particle emitted is found to have energy 5.3 MeV.
Therefore from equation, we have
Q = (K.E) α × A/A – 4
= 5.3 × 210 / 210 -4
= 5.4 MeV
This example clearly illustrates that the most of the disintegration energy appears as the kinetic energy of alpha particle.
Question 3: Calculate the disintegration energy 92U232 (mass = 232.037146 u) decays to 90Th228 (mass = 228.028731 u) with the emission of an α particle.
Answer:
Use conservation of energy 92U232 is the parent, 90Th228 is the daughter.
Since the mass of the helium is 4.002603u, the total mass in the final state is 228.028731 u + 4.002603 u = 232.031334 u
The mass last when the 92U232 decays is 232.037146 u – 232.031334 u = 0.005812 u
Since, 1 u = 931.5MeV,the energy Q released is,
Q = (0.005812 u) × (931.5 MeV/u)
~5.4 MeV
And this energy appears as kinetic energy of the α particle and the daughter nucleus.
Question 4: Find the maximum energy that a β particle can have in the following decay:
8O19 ⇢ 9F19 + –1e0 + ̅ν
(Given: m(8O19) = 19.003576 a.m.u, m(9F19) = 18.998403 a.m.u and m(-1e0) = 0.000549 a.m.u.)
Answer:
The Rest mass of ̅ν = 0
Q- value of β decay = m(O) – {m(F) + m(e)}
= 19.003576 – (18.998403 + 0.000549)
= 19.003576 – 18.998952
= 0.004624 a.m.u
Since 1 a.m.u = 931 MeV
= 0.004624 × 931 MeV
= 4.3049 MeV
The energy is shared by β– particle and antineutrino ( ̅ν ). If ̅ν does not get any share then the maximum K.E of β– particle is 4.3049 MeV.
Question 5: Given the following atomic masses: 92U238 = 238.05079u, 90Th234 = 234.04363u, 91Pa237 = 237.05121u; 1H1 = 1.00783, 2He4 = 4.00260u. Show that 92U238 cannot spontaneously emit a proton.
Answer:
92U238 —> 91Pa237 + 1H1
Mass Defect,
Δm = ( 238.05079 – 237.05121 – 1.00783) u
=> Energy released Q = -0.00825u
= -0.00825 × 931.5 = -7.68 MeV
Since, Q value is negative, so proton cannot be emitted spontaneously.