Ниже приведен подробный разбор демоверсии ЕГЭ-2023 по химии, проектная версия. Задания разобраны от 1 до 34 подряд, приведена логика рассуждения по каждому из них. Если есть желание разобраться более детально, то переходите по ссылкам в тексте или записывайтесь к нам на курс.
Для выполнения первого задания всегда рекомендую расписать электронно-графические формулы элементов (с ячейками). В большинстве случаев достаточно изобразить внешний и предвнешний уровень. Напомню также, что для элементов дальше IV периода не нужно изображать формулу целиком, а можно воспользоваться аналогией строения валентных подуровней с соседом из подгруппы. По приведенным элементам:
- Цезий находится в первой группе, главной подгруппе, аналог натрия по строению внешнего уровня. Имеет 1 электрон на 6s-подуровне, он же является неспаренным.
- Углерод находится в четвертой группе, главной подгруппе. На внешнем уровне имеет 4 электрона, из них неспаренных два, которые находятся на 2р-подуровне.
- Кислород находится в шестой группе, главной подгруппе. На внешнем уровне имеет 6 электронов, из них неспаренных два, которые находятся на 2р-подуровне.
- Хром находится в шестой группе, побочной подгруппе. Необходимо вспомнить о проскоке электрона, за счет которого на внешнем уровне, 4s-подуровне, имеет 1 электрон, а не предвнешнем, 3d-подуровне, – пять. Итого 6 неспаренных.
- Азот находится в пятой группе, главной подгруппе. На внешнем уровне имеет 5 электронов, из них неспаренных три, которые находятся на 2р-подуровне.
Выбираем углерод и кислород, у обоих по два неспаренных электрона.
Ответ: 23
Необходимо вспомнить, что к р-элементам можно отнести элементы главных подгрупп шести последних групп в периоде. Представители первых двух относятся к s-элементам, а элементы побочных подгрупп относим к d-элементам. Исходя из приведенных соображений, выбираем пункты 2), 3), 5).
Атомный радиус уменьшается направо по периоду, поэтому располагаем выбранные ранее элементы в порядке 2), 5), 3).
Ответ: 253
Для выполнения такого рода заданий рекомендую выписать на лист бумаги высшую и низшую степени окисления для каждого из элементов.
- Цезий имеет высшую степень окисления +1, низшую – 0. Разность 1.
- Углерод имеет высшую степень окисления +4, низшую – -4. Разность 8.
- Кислород имеет высшую степень окисления +2, низшую – -2. Разность 4.
- Хром имеет высшую степень окисления +6, низшую – 0. Разность 6.
- Азот имеет высшую степень окисления +5, низшую – -3. Разность 8.
Таким образом, выбираем углерод и азот.
Ответ: 25
В задании, по сути, есть два фильтра: по типу строения и по характеру связи. Начнем с типа строения. Поскольку необходимо выбрать вещества молекулярного строения, то сразу можно исключить соли и иные соединения, имеющие ионные связи. Убираем из рассмотрения пункты 1) и 4). Среди оставшихся нужно найти вещества с ковалентной полярной связью. Вспомним, что такая связь может возникать между атомами разных неметаллов (или сильно различающихся фрагментов в органических молекулах). По такому принципу можно исключить пункт 5). Остаются вещества 2) и 3).
Ответ: 23
К двухосновным кислотам относятся те из них, которые содержат в молекуле 2 атома водорода, способных замещаться на катионы металлов. Подобным требованиям отвечает сернистая кислота, пункт 4).
К средним можно отнести соли, не содержащие способных к замещению атомов водорода, фрагментов ОН, комплексных ионов и подобного. Из приведенного списка можно взять аммиачную селитру, тривиальное название нитрата аммония.
К амфотерным гидроксидам можно отнести гидроксиды металлов в степенях окисления +3 и +4, также гидроксиды бериллия, цинка, свинца, олова. Подойдет пункт 2).
Ответ: 482
Попробуем найти в приведенном списке сильные кислоты. Пункт 1) подходит, поскольку в пункте 3) находится слабая кислота. Таким образом X уже установлен.
Среди оставшихся пунктов нужно найти вещество, которое при добавлении вызовет растворение гидроксида алюминия. Поскольку гидроксид является амфотерным, то сможет прореагировать с кислотой, кроме наиболее слабых, или щелочью. Среди приведенных соединений можно взять 4), поскольку гидроксид калия является щелочью.
Ответ: 14
Для выполнения подобных заданий советую следующий порядок действий:
- Берем вещество из левого столбика
- Классифицируем его, вспоминаем характерные типы реакций для такого класса соединений
- Оцениваем его с точки зрения кислотно-основных и окислительно-восстановительных свойств
- Подбираем вещества и правого столбика, противоположные по свойствам и способные реагировать с веществом из правого столбика
Пункт А):
Сера относится к простым веществам-неметаллам, средняя по активности. Способна вступать в реакцию со щелочами, сильными окислителями и активными восстановителями. С водой и кислотами, кроме кислот-окислителей, реакции нет.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 3) водород выступит против серы в качестве восстановителя, хлор и кислород – окислители. Подходит.
В пункте 4) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 5) нет реакции уже с первым веществом, дальше не продолжаем.
Пункт Б):
Оксид серы (VI) относится к кислотным оксидам, реагирует с водой, большинством веществ основной и амфотерной природы. Восстановительных свойств не проявляет, может быть окислителем.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) оксид бария – основный, КОН – щелочь, с водой реакция тоже есть. Подходит.
В пункте 3) хлор и кислород – окислители, не подходит.
В пункте 4) нет реакции с уксусной кислотой, не подходит.
В пункте 5) нет реакции уже со вторым веществом, дальше не продолжаем.
Пункт В):
Гидроксид цинка относится к амфотерным гидроксидам, может реагировать со щелочами, кислотами. Выраженных окислительных или восстановительных свойств не проявляет. В воде нерастворим, с солями не обменивается.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) нет реакции с водой, не подходит.
В пункте 3) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 4) реагирует с кислотами и щелочью. Подходит.
В пункте 5) нет реакции с хлоридом бария, не подходит.
Пункт Г):
Бромид цинка относится к солям, может вступать в реакции обмена со щелочами и солями. Может проявлять восстановительные свойства за счет бромид-иона.
В пункте 1) обмен имеет смысл с первым и вторым веществам, с третьим будет ОВР. Подходит.
В пункте 2) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 3) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 4) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 5) нет реакции уже с первым веществом, дальше не продолжаем.
Ответ: 3241
Для ответа на вопрос имеет смысл оценить свойства веществ в каждой паре, а при необходимости записать уравнение реакции между ними. Сделаем и то, и другое.
В пункте А) магний является сильным восстановителем, а концентрированная серная кислота – окислителем. Магний способен восстановить серу до низшей степени окисления:
4Mg + 5H2SO4 = 4MgSO4 + H2S + 4H2O
В пункте Б) встречаются основный оксид и кислота, произойдет обмен:
MgO + H2SO4 = MgSO4 + H2O
В пункте В) сера выступает в качестве восстановителя, а концентрированная серная кислота – окислитель. Произойдет ОВР:
S + 2H2SO4 = 3SO2 + 2H2O
В пункте Г) сероводород выступает в качестве восстановителя, а кислород – окислитель. Произойдет ОВР:
2H2S + 3O2 = 2SO2 + 2H2O
Ответ: 5144
Обратим внимание, что железо в одну стадию переходит в степень окисления +3. Для этого нам нужен сильный окислитель- хлор.
2Fe + 3Cl2 = 2FeCl3
Во второй реакции железо понижает степень окисления до +2, поэтому необходимо найти восстановитель. Им тут может быть только йодид калия.
2FeCl3 + 2KI = 2FeCl2 + I2 + 2KCl
Ответ: 43
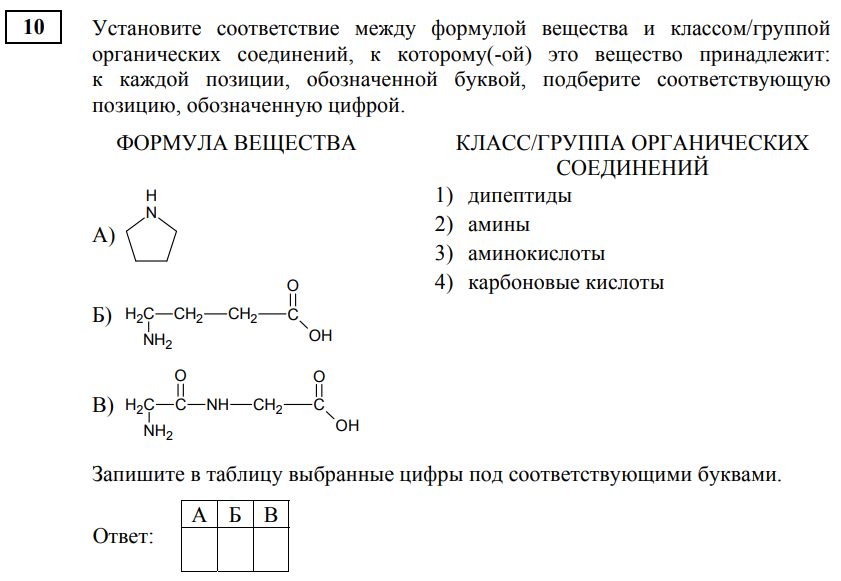
Для установления соответствия имеет смысл найти в структурах из левого столбика характерные функциональные группы и фрагменты.
В структуре А) видим фрагмент -NH-, который можно отнести ко вторичному амину. Циклическая структура молекулы в данном случае ничего не значит.
В структуре Б) есть аминогруппа и карбоксильная группа. Соответственно, вещество можно отнести к аминокислотам.
В структуре В) есть структурный фрагмент -С(О)NH- и просматриваются два остатка от аминокислот, что указывает на дипептид.
Ответ: 231
К решению подобных заданий может быть несколько подходов. Можно для начала определить молекулярную формулу бутена-1, а затем сравнить ее с молекулярными формулами предложенных вариантов. Изомеры по определению должны иметь одинаковые молекулярные формулы.
Бутен-1 – С4Н8
- С4Н10
- С4Н8
- С4Н6
- С4Н6
- С4Н8
Ответ: 25
Поскольку подкисленный раствор перманганата проявляет сильные окислительные свойства, следует поискать вещества, которые могут окисляться с образованием карбоновой кислоты. Прокомментируем все предложенные пункты:
- Окисляется с разрывом кратной связи, кислота будет
- Не окисляется
- Окисляется по боковой цепи, кислота будет
- Не окисляется
- Окисляется до кислоты
Ответ: 135
Метиламин относится к первичным алифатическим аминам, проявляет выраженные основные свойства, вступает в реакции алкилирования, реагирует с азотистой кислотой. Прокомментируем все предложенные пункты:
- Алкан, низкая активность, реакции нет
- Хлоралкан, реакция алкилирования, реагирует
- Водород, гидрировать нечего, не реагирует
- Основание, не реагирует
- Кислота, образование соли, реагирует
Ответ: 25
Для решения имеет смысл записать классы соединений из левого столбика, далее оценить происходящие изменения:
А) 1,2-дигалогеналкан – алкен
Б) моногалогеналкан – алкен
В) моногалогеналкан – алкан
Г) 1,2-дигалогеналкан – алкин
По изменениям назвать тип происходящей реакции и подобрать к ней подходящий реагент:
А) дегалогенирование, магний
Б) дегидрогалогенирование, спиртовой раствор щелочи
В) реакция Вюрца, натрий
Г) дегидрогалогенирование, спиртовой раствор щелочи
Ответ: 1252
Для надежности перед выбором ответа имеет смысл преобразовать названия веществ в формулы и прописать предложенные реакции. Попробуем это сделать:
А) 2CH3COOH + Na2S = 2CH3COONa + H2S
Б) HCOOH + NaOH = HCOONa + H2O
В) HCOH + 4Cu(OH)2 = 2Cu2O + CO2 + 5H2O
Г) 2CH3CH2OH + 2Na = 2CH3CH2ONa + H2
Ответ: 5462
При рассмотрении цепочек превращений бывает полезно посмотреть через одну стадию и оценить, как можно осуществить такое превращение. Также очень полезно сравнить число атомов углерода в исходной молекуле и продукте, может навести на мысль.
В первых двух реакциях цепочки число атомов углерода удваивается, что наводит на мысль о реакции Вюрца. Если рассуждение верное, то веществом Х должен быть галогеналкан. Действительно, его можно получить в одну стадию из спирта, а затем превратить в алкан.
Следующее превращение можно понять, если посмотреть на условия реакции. Нагревание линейного алкана в присутствии хлорида алюминия приводит к его изомеризации в разветвленный алкан.
Ответ: 54
Для решения можно переписать вещества в парах в виде формул, оценить их окислительно-восстановительные свойства и возможность реакции между ними:
- K2S – восстановитель, KMnO4 – окислитель, имеет смысл
- H2SO4 – окислитель, NaCl – очень слабый восстановитель, не ОВР
- NH4Cl – очень слабый восстановитель, NaNO2 – окислитель, специфический случай обмена, сопровождаемого ОВР
- SiO2 – выраженных окислительно-восстановительных свойств не проявляет, Na2CO3 — выраженных окислительно-восстановительных свойств не проявляет, не ОВР
- HI – восстановитель, Na2Cr2O7 – сильный окислитель, имеет смысл
Для надежности можно записать уравнения реакций между ними:
- 2KMnO4 + 3K2S + 4H2O = 2MnO2 + 3S + 8KOH
- NaCl + H2SO4 = NaHSO4 + HCl
- NaNO2 + NH4Cl = NaCl + N2 + 2H2O
- Na2CO3 + SiO2 = Na2SiO3 + CO2
- Na2Cr2O7 + 14HI = 2NaI + 2CrI3 + 3I2 + 7H2O
Ответ: 135
Изменение давления не будет влиять на скорость реакций, в которых нет газообразных реагентов. Среди приведенных пунктов это будут 2), 3), 5).
Ответ: 235
Для решения подобных заданий нужно расставить степени окисления на атомах азота до и после реакции.
Если степень не меняется, то азот не проявляет окислительно-восстановительных свойств. Так будет в пункте А) (переход -3 в -3).
Если степень увеличится, то азот проявляет восстановительные свойства. Так будет в пунктах Б) (переход -3 в 0) и В) (переход -3 в +2).
Ответ: 422
В первом случае для решения необходимо вспомнить зависимость продуктов электролиза от состава соли:
А) соль образована катионом активного металла и кислородсодержащим анионом, на электродах выделятся водород и кислород.
Б) соль образована катионом активного металла и галогенид-ионом, на электродах выделятся водород и галоген.
В) соль образована катионом малоактивного металла и галогенид-ионом, на электродах выделятся металл и галоген.
Ответ: 342
Во втором случае нужно помнить, что алюминий получают при электролизе раствора оксида в расплаве криолита. Калий и подобные наиболее активные металлы только из расплавов галогенидов. Кислород в данном случае можно получить при электролизе водного раствора фторида калия.
Ответ: 124
Для начала имеет смысл определить класс каждого из соединений:
- Средняя соль
- Средняя соль
- Средняя соль
- Сильная кислота
Исходя из этого уже можно сказать, что наиболее низкое значение рН (самая кислая среда) будет в пункте 4).
Как разобраться с солями? Нужно оценить их способность к гидролизу и потенциальное влияние на среду раствора:
- Соль сильной кислоты и сильного основания, не гидролизуется, среда нейтральная
- Соль слабого основания и сильной кислоты, гидролиз по катиону, среда кислая
- Соль сильного основания и слабой кислоты, гидролиз по аниону, среда щелочная
Ответ: 4213
В задании на равновесие следует учитывать разные факторы. Пройдем по каждому из пунктов:
А) кислота при диссоциации может дать дополнительное количество ионов Н+, которые участвуют в равновесии. При увеличении их концентрации равновесие сместится в сторону обратной реакции.
Б) давление в данном случае не окажет влияния, поскольку нет участников-газов
В) повышение температуры сместит равновесие в сторону эндотермической реакции. В данном случае – прямой.
Г) твердая щелочь может раствориться и прореагировать с Н+, уменьшая концентрацию таких ионов в системе. Равновесие сместится в сторону прямой реакции.
Ответ: 2311
Задания подобного типа удобнее всего решать с помощью таблицы. Данный подход к решению задания ЕГЭ-2023 на равновесие в реакторе можно посмотреть по ссылке ниже:
Способ, на мой взгляд, наиболее оптимальный и доступный каждому.
Ответ: 25
В первом случае нужно подобрать такое вещество из правого столбика, которое реагирует с одним или двумя веществами из пары в левом столбике. При этом очень важно, чтобы реакция сопровождалась видимыми признаками:
Пара А):
- Есть реакция с азотной кислотой, сопровождается выделением газа и растворением твердого вещества. Нитрат натрия не реагирует. Подходит.
- Есть реакция с азотной кислотой, но внешних признаков нет. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
Пара Б):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с гидроксидом калия, но внешних признаков нет. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с гидроксидом натрия, сопровождается образованием осадка. Хлорид калия не реагирует. Подходит.
Пара В):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с хлоридом бария, сопровождается образованием осадка. Хлорид натрия не реагирует. Подходит.
Пара Г):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Специфический случай, поскольку один из изначально образовавшихся нерастворимых гидроксидов (Al(OH)3) может раствориться снова при избытке щелочи. Подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
В заданиях второго типа имеет смысл записать происходящие реакции и попытаться себе их представить. Как может выглядеть и что увидим:
- 2CH3CH2COOH + 2Li = 2CH3CH2COOLi + H2
- 2CH3CH(OH)CH3 + 2K = 2CH3CH(OK)CH3 + H2
- Zn(OH)2 + 2CH3COOH = Zn(CH3COO)2 + 2H2O
- C2H2 + 2Br2 = CHBr2-CHBr2
В первом и втором случаях наблюдаем выделение газообразного водорода. В третьем наблюдаем растворение осадка гидроксида цинка. В четвертом исчезнет окраска брома, наблюдается обесцвечивание.
Ответ: 4415
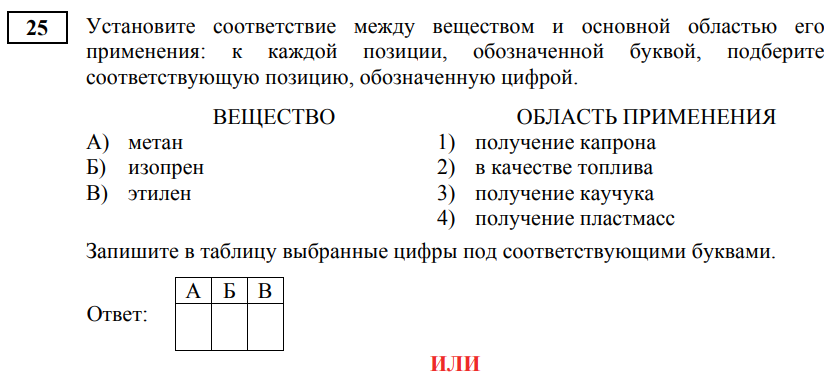
Задание 25 охватывает несколько совершенно разнородных тем, каждая из которых требует отдельного блока знаний. Приведу здесь ссылки на полезные материалы по заданию, поскольку многое здесь нужно просто выучить.
По первому блоку следует знать, что сопряженные алкадиены используются для производства каучуков, а алкены – пластмасс. Метан в составе природного газа используют в качестве топлива.
По второму блоку можно относительно легко соотнести мономер и полимер, если представить себе структуру молекулы мономера. В молекуле этена всего два атома углерода, поэтому элементарное звено формулы полимера тоже содержит два атома углерода. По той же логике здесь можно действовать и для пропена с дивинилом.
Третий блок нужно просто выучить. По переработке углеводородов можно заглянуть сюда. Хорошее описание технологических процессов можно посмотреть здесь.
Ответ: 234; 214; 312
Для решения подобных заданий на растворы рекомендую использовать метод таблиц, подробно описанный здесь.
В итоге решение задачи сводится к уравнению вида
(15+х)/(150+х) = 0,12
15+х = 18+0,12х
0,88х = 3
х = 3,4
Ответ: 3,4 г
Задания такого типа сводятся к решению пропорции. Для начала переведем известный объем аммиака в количество:
n(NH3) = V(NH3)/Vm = 0,56/22,4 = 0,025 (моль)
2 моль – 92 кДж
0,025 моль – х кДж
х = 1,15 кДж
Ответ: 1,15 кДж
Для решения первой задачи запишем уравнение протекающей реакции:
CaCO3 + 2HNO3 = Ca(NO3)2 + CO2 + H2O
Далее вычислим количество нитрата кальция:
n(Ca(NO3)2) = m(Ca(NO3)2)/M(Ca(NO3)2) = 196800/164 = 1200 (моль)
Вычислим массу чистого карбоната кальция, который содержался в известняке:
m(CaCO3) = n(Ca(NO3)2)·M(Ca(NO3)2) = 1200·100 = 120000 (г) = 120 (кг)
Вычислим массу примесей в известняке:
m(примеси) = m(известняка) – m(CaCO3) = 150 — 120 = 30 (кг)
Определим массовую долю примеси в известняке:
ω(примеси) = m(примеси)/m(известняка)·100% = 30/150·100% = 20%
Ответ: 20%
Для решения второй задачи запишем уравнение протекающей реакции:
3С2Н2 = С6Н6
Вычислим количества ацетилена и практически полученного бензола:
n(С2Н2) = V(С2Н2)/Vm = 26,88/22,4 = 1,2 (моль)
n(С6Н6 практ.) = m(С6Н6)/M(С6Н6) = 23,4/78 = 0,3 (моль)
Вычислим теоретически возможное количество бензола и сравним его с практическим:
n(С6Н6 теор.) = n(С2Н2)/3 = 1,2/3 = 0,4 (моль)
η(С6Н6) = n(С6Н6 практ.)/n(С6Н6 теор.)·100% = 0,3/0,4·100% = 75%
Ответ: 75%
При выполнении заданий 29 и 30 имеет смысл записать все представленные вещества в виде молекулярных формул:
KMnO4, NaHCO3, Na2SO3, BaSO4, KOH, H2O2
Далее следует внимательно прочитать описание реакции. Поскольку должно происходить изменение цвета раствора, нужно найти окрашенный реагент. Из предложенных это может быть только KMnO4. Это вещество проявляет сильные окислительные свойства, поэтому нужно подобрать восстановитель. Осадка в ходе реакции образоваться не должно, поэтому брать нейтральную среду нельзя. В противном случае выпадет осадок MnO2. Среда может быть кислой или щелочной. Кислоты в предложенном наборе нет, поэтому выберем гидроксид калия для создания среды. Восстановителей в предложенном наборе два: сульфит натрия и пероксид водорода. Пероксид брать нельзя, поскольку по описанию реакции газа образоваться не должно. Таким образом приходим к выводу, что нужно взять сульфит, перманганат и щелочь. Приведем соответствующую реакцию и электронный баланс:
2KMnO4 + Na2SO3 + 2KOH = 2K2MnO4 + Na2SO4 + H2O
2∙ | Mn+7 + 1ē → Mn+6
1∙ | S+4 – 2ē → S+6
марганец в степени окисления +7 (или перманганат калия) является окислителем.
сера в степени окисления +4 (или сульфит натрия) – восстановителем.
Есть хороший инструмент для отработки данного задания, рекомендую.
При выполнении заданий 29 и 30 имеет смысл записать все представленные вещества в виде молекулярных формул:
KMnO4, NaHCO3, Na2SO3, BaSO4, KOH, H2O2
Далее следует внимательно прочитать описание реакции. К кислым солям здесь относится только NaHCO3. В обмен с ней вступит только гидроксид калия, поскольку кислое и щелочь точно смогут прореагировать. Приведем молекулярное, полное и сокращенное ионные уравнения:
2NaHCO3 + 2KOH = Na2CO3 + K2CO3 + 2H2O
2Na+ + 2HCO3− + 2K+ + 2OH− = 2Na+ + CO32− + 2K+ + CO32− + 2H2O
HCO3− + OH− = CO32− + H2O
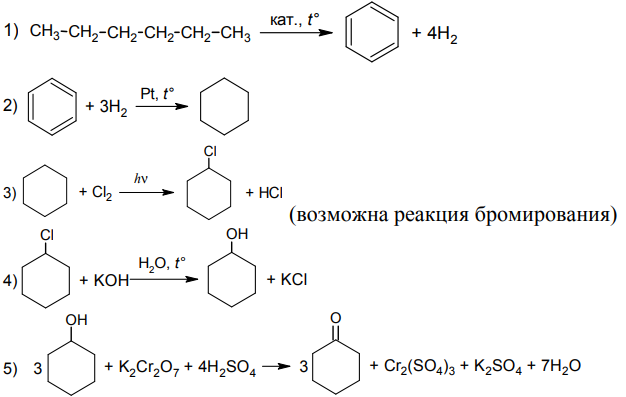
Решение 31 номера сводится к знанию неорганической химии, свойств и реакций отдельных веществ. Приведем уравнения протекающих процессов:
2Cu(NO3)2 + 2H2O = 2Cu + O2 + 4HNO3
Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O
SO2 + 2H2S = 3S + 2H2O
3S + 6KOH = K2SO3 + 2K2S + 3H2O
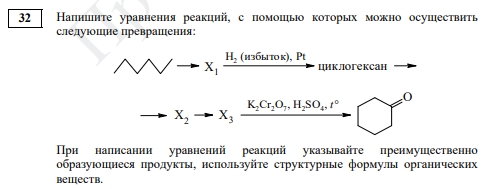
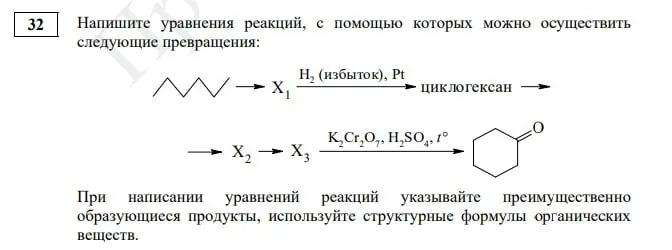
При рассмотрении цепочек превращений бывает полезно посмотреть через одну стадию и оценить, как можно осуществить такое превращение. Также очень полезно сравнить число атомов углерода в исходной молекуле и продукте, может навести на мысль.
Начнем с циклогексана. Получить его путем гидрирования можно, например, из бензола. Его, в свою очередь, можно получить из гексана по реакции дегидроциклизации. Х1 – бензол. Далее в цепочке много неизвестных веществ, заглянем в самый конец. Циклогексанон относится к кетонам, получить его можно из вторичного спирта. Условия последней реакции на это указывают, поскольку там дан сильный окислитель в кислой среде. Тогда Х3 – циклогексанол. Получить такой спирт в две стадии нужно из циклоалкана. Тогда можно предположить последовательно галогенирование и замещение полученного галогенпроизводного под действием водного раствора щелочи. Тогда Х2 – хлорциклогексан, можно бромциклогексан. Последовательность реакций получается следующей:
Решение задачи начинается с анализа и расчета молекулярной формулы. Поскольку продуктами сгорания являются только углекислый газ и вода, можно приписать веществу формулу CxHyOz. Вычислим количества углекислого газа и воды:
n(H2O) = m(H2O)/M(H2O) = 1,8/18 = 0,1 (моль)
n(СО2) = V(CO2)/Vm = 4,48/22,4 = 0,2 (моль)
Тогда можно определить количества и массы элементов, входивших в состав исходного вещества:
n(С) = n(СО2) = 0,2 моль
m(С) = n(С)·M(С) = 0,2·12 = 2,4 г
n(H) = 2n(H2O) = 0,2 моль
m(H) = n(H)·M(H) = 0,2·1 = 0,2 г
m(О) = m(CxHyOz) − m(С) − m(H) = 3,4 − 2,4 − 0,2 = 0,8 (г)
n(O) = m(O)/M(O) = 0,8/16 = 0,05 (моль)
Вычислим молекулярную формулу неизвестного вещества:
x : y : z = n(С) : n(H) : n(O) = 0,2 : 0,2 : 0,05 = 4 : 4 : 1
Поскольку по условию один из фрагментов молекулы должен содержать 7 атомов углерода, разумным будет удвоить простейшее соотношение и получить формулу C8H8O2.
С8Н8О2 – молекулярная формула
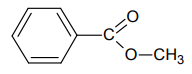
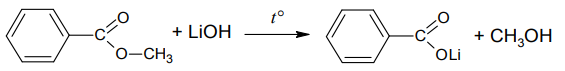
Вещество по условию реагирует со щелочью, процесс гидролиза с образованием соли и спирта. В остатке кислоты 7 атомов углерода и малое количество атомов водорода, что вполне соответствует бензоату. Тогда на спирт приходится всего один атом углерода, что соответствует метанолу. Тогда можно предложить структуру метилбензоата:
Запишем уравнение его реакции с гидроксидом лития:
К заданию 34 следует приступать только после ПОЛНОГО выполнения и проверки всех остальных заданий КИМа. Убедитесь также, что все прочие задания перенесены в бланк ответов, а не остались на черновике. Времени на это задание нужно больше всего, поэтому велик риск потерять остальное и не успеть что-то перенести в бланк.
Для решения следует внимательно прочитать условие и написать реакции, которые сразу же очевидны, без дополнительных расчетов. Здесь их можно записать две:
Ca + 2HCl = CaCl2 + H2
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
Поскольку напрямую ничего не известно про массу и количество кальция и карбоната кальция, можно сказать, что кальция было х моль, а его карбоната у моль. Тогда в ходе реакций выделилось х моль водорода и у моль углекислого газа. Выразим массы указанных веществ:
m(Ca) = n·M = 40х г
m(CaCO3) = n·M = 100у г
m(Н2) = n·M = 2х г
m(CO2) = n·M = 44у г
Выразим массу раствора после добавления исходной твердой смеси к соляной кислоте:
m(р-ра) = m(Ca) + m(CaCO3) + m(р-ра HCl) − m(Н2) − m(CO2)
m(р-ра) = 40х + 100у + 300 − 2х − 44у = 330 (г)
38х + 56у = 30
Первое уравнение системы готово. Второе составим по массовой доле кальция в исходной смеси:
m(смеси) = m(Ca) + m(CaCO3) = 40х + 100у (г)
m(Ca) = 40х + 40у (г)
ω(Са) = m(Ca)/m(смеси)·100% = (40х+40у)/(40х+100у)·100% = 50%
(40х+40у)/(40х+100у) = 0,5
Составим и решим систему уравнений:
38х + 56у = 30
(40х + 40у)/(40х + 100у) = 0,5
38х + 56у = 30
(2х + 2у)/(2х + 5у) = 0,5
38х + 56у = 30
2х + 2у = х + 2,5у
38х + 56у = 30
х = 0,5у
75у = 30
у = 0,4
х = 0,2
n(Ca) = 0,2 моль
n(CaСО3) = 0,4 моль
Далее вычислим количество и массу углекислого газа:
n(СО2) = n(CaСО3) = 0,4 моль
m(СО2) = n(СО2)·M(СО2) = 0,4·44 = 17,6 г
Вычислим массу и количество гидроксида натрия:
m(NaOH) = m(р-ра NaOH)·ω(NaOH)/100% = 400·4%/100% = 16 (г)
n(NaOH) = m(NaOH)/M(NaOH) = 16/40 = 0,4 (моль)
Далее нужно сравнить количества щелочи и углекислого газа, чтобы понять, какая будет реакция между ними:
n(СО2)/n(NaOH) = 0,4/0,4 = 1:1
Соотношение 1:1, поэтому образуется кислая соль:
NaOH + CO2 = NaHCO3
Вычислим массу образовавшейся соли и массу раствора:
n(NaHCO3) = n(СО2) = 0,4 моль
m(NaHCO3) = n·M = 0,4·84 = 33,6 г
m(р-ра конечн.) = m(р-ра NaOH) + m(CO2) = 400 + 17,6 = 417,6 (г)
Вычислим массовую долю гидрокарбоната натрия в полученном растворе:
ω(NaHCO3) = m(NaHCO3)/m(р-ра конечн.)·100% = 33,6/417,6·100% = 8,05%
Ответ: 8,05%
В этой статье вместе с преподавательницей Вебиума Таисией Фламель разбираем демоверсию ЕГЭ 2023 по химии. Расскажем об:
- Изменениях в КИМе — новых формулировках заданий и способах их решения;
- Уровне сложности — стал ли ЕГЭ по химии 2023 года сложнее;
- Как решать изменившиеся задания.
В конце статьи — видео с подробным разбором демоверсии ЕГЭ 2023 по химии.
Как пользоваться сайтом ФИПИ и где смотреть демоверсии, спецификации и кодификаторы рассказали в этой статье.
Изменения в ЕГЭ 2023 по химии
Серьёзных изменений в ЕГЭ по химии в 2023 году нет, но есть нюансы, на которые стоит обратить внимание:
33 и 34 задания
Изменён порядок этих заданий, их поменяли местами. Теперь 33 задание — это задача по органике, а 34 задача — по неорганике. На сложность задания это не повлияло, но будьте внимательны при выполнении этих номеров и заполнении бланков! Многие допускают досадные ошибки, путая номера заданий, и теряют драгоценные баллы.
9 задание
Повышен уровень сложности. Но пока, как именно это будет сделано, составители ЕГЭ не уточнили. Формулировка задания такая же, как в ЕГЭ 2022 года. Возможно будут: более сложные, специфические и менее распространённые реакции или будет больше пропусков в цепочке превращений (больше X и Y). Чтобы быть в курсе изменений, подписывайтесь на наш телеграм-канал.
12 задание
Это задание было усложнено ещё в 2022 году. В нём присутствуют и углеводороды, и кислородсодержащие соединения, а также незафиксированное количество ответов. В 2023 году оно тоже входит в ряд заданий повышенной сложности. Что ещё в нём можно усложнить, только предполагаем 🤷♀️
💡 При выполнении задания обращайте внимание на формулировку!
Забирай бесплатный чек-лист по всем темам ЕГЭ по химии, чтобы не упустить ничего важного во время подготовки и быть готовым на все 💯
16 задание
Теперь задание относится к повышенному уровню сложности. Формулировка задания прежняя: необходимо определить, какие из указанных веществ являются веществами X и Y в схеме превращений. Как задание усложнится, можно только гадать, но скорее всего будут более сложные реакции.
💡 При выборе ответов обратите внимание на то, что одни и те же цифры не могут повторяться в ответе! X и Y — разные вещества. Это указано в формулировке задания.
23 задание
Задание проверяет умение проводить расчёты концентраций веществ в равновесной системе. В демо ЕГЭ 2023 по химии оно представлено в виде текста, а не таблицы.
Смотрите видео, где мы решаем все виды 23 задания ЕГЭ по химии. Эти задания дают 2 первичных балла, а решаются всего за минуту.
Подведём итог разбора демоверсии ЕГЭ 2023 по химии: значительных изменений в нет, задания практически такие же как в ЕГЭ 2022 года. Но есть задания, которые будут усложнены. Скорее всего, в них будут присутствовать более сложные, специфичные реакции и свойства веществ. На это стоит обратить внимание.
Материалы, которые помогут во время подготовки к ЕГЭ по химии:
📚 18 ресурсов и пособий для подготовки к ЕГЭ по химии
❗️10 типичных ошибок на ЕГЭ по химии
🧪Куда поступать с химией: 5 перспективных вариантов
👍Шпаргалки полезные материалы по химии
👩🏼🔬Специальности в химии: какую профессию выбрать
🧑🏼🔬«Поступить на химфак сложнее, чем его окончить»: история Таси Фламель
На нашем курсе «Основа» за 9 месяцев подготовки мы разбираем и отрабатываем на практике всю теорию, необходимую для получения заветной сотки по химии. На курсе тебя ждут:
- от 12 занятий в месяц, а также индивидуальный план подготовки;
- личный наставник, который объяснит непонятное, проверит домашку и мотивирует тебя на всём пути подготовки;
- ламповая атмосфера и удобный формат занятий.
⚡️ Видео с полным разбором демоверсии ЕГЭ по химии 2023 года:
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter. Мы обязательно поправим!
Химия — один из самых сложных предметов для сдачи ЕГЭ. Задания меняются каждый год: то, что раньше казалось трудным, нынешние выпускники должны успевать за пару минут. Несмотря на это экзамен необходим будущим врачам, фармацевтам и, конечно же, химикам. Давайте обсудим, как устроен ЕГЭ по химии 2023 и что нужно выучить для успешной сдачи!
Структура ЕГЭ по химии 2023
ЕГЭ по химии состоит из двух частей. В первой выпускникам предлагают решить 28 заданий — нужен краткий ответ в виде одного числа или последовательности чисел. Во второй части — 6 заданий с развернутым ответом. В них нужно записывать уравнения химических реакций и решать сложные математические задачи. Если выполнить работу без ошибок, можно набрать 56 первичных баллов.
Нововведение ЕГЭ по химии 2023 — сокращение количества заданий и появление новых прототипов.
Изменения в ЕГЭ по химии 2023
Задание № 23. В прошлом году ребята впервые решали задание на расчет равновесных и исходных концентраций. Оно представляло собой уравнение химической реакции, а также таблицу с концентрациями каждого участника. В этом году таблицы не будет, вместо нее предлагается найти исходные данные в тексте. Советуем вам не отходить от уже отработанного алгоритма и самостоятельно составлять таблицы. Немного практики и навык владения калькулятором помогут получить за этот номер максимальные баллы даже с новым условием.
Задания № 9, 12 и 16. Эти задания не изменились на вид. В №9 и 16 предстоит разобраться с небольшими цепочками превращений – неорганической и органической соответственно. А в задании 12 выпускников вновь ожидают химические свойства органических веществ и неизвестное количество правильных ответов. Но в этом году задания станут сложнее, их переносят в разряд заданий повышенного уровня сложности. К сожалению, при неизменном 1 балле за каждый из номеров.
Задания № 33 и 34. Каждый выпускник накануне ЕГЭ по химии очень хочет знать, чему будут посвящены задачи 33 и 34. Конечно же, тайну нам не открыли, но зато эти задания поменяли местами. Теперь №33 – это задача на установление органической формулы, а №34 – сложная расчетная задача, основанная на неорганических превращениях.
Задание № 32. Эта органическая цепочка существенно не изменилась, ребятам предстоит записать пять уравнений химических реакций. Но стоит обратить пристальное внимание на изображение гексана, с такими формулами мы в ЕГЭ еще не сталкивались, но есть вероятность, что видеть их мы теперь будем чаще.
Это главные изменения ЕГЭ по химии 2023. Но для того, чтобы получить высокий балл, просто знать о них недостаточно. Когда ФИПИ обновляет формулировки заданий, может измениться и способ их решения и критерии оценивания. Если не учитывать это во время подготовки к ЕГЭ, то можно потерять немало баллов. Обидно!
Это — лишь малая часть ловушек экзамена, которые составители расставляют выпускникам. На своих занятиях по подготовке ЕГЭ по химии я показываю ученикам их все. Мы учимся обходить каждую из них и делать такие решения заданий, к которым никто не придерется. А еще я всегда делюсь лайфхаками быстрого и правильного решения типичных задач — так можно сэкономить много времени на более сложные вещи.
Всему этому я могу научить и вас! Приходите ко мне на уроки, и я подготовлю вас к ЕГЭ по химии на 80+ 💪🤓
Какие темы есть в ЕГЭ по химии?
Чтобы успешно сдать ЕГЭ по химии 2023, нужно освоить пять разделов этой науки.
Теоретические основы химии
Этот блок включает в себя информацию о строении атомов, об их существовании в молекулах вещества. Выпускникам нужно продемонстрировать навыки работы с таблицей химических элементов Д.И. Менделеева. Этот раздел поможет решить задания 1-4, 18-20, 23 в первой части, а также задание 29 во второй части.
Неорганическая химия
Этой теме посвящены задания 5-9, 17, 21 (первая часть), 30, 31 (вторая часть). Вас ждут любые свойства неорганических соединений: от простых веществ-металлов и неметаллов до комплексных солей и кристаллогидратов. Чтобы получить высокие баллы, необходимо также знать правила номенклатуры, способы получения и основы процессов гидролиза и электролиза.
Органическая химия
В заданиях 10-16 и 32 вы столкнетесь с органической химией. Ученики, которые готовятся самостоятельно, часто стараются выучить все классы веществ по стандартному плану: название класса, номенклатура, физические и химические свойства, способы получения и применение. На самом деле можно значительно облегчить себе жизнь и начать со строения органических молекул. Как только вы поймете, что кратные связи можно разорвать одним набором реактивов, в группе –ОН замещают атом водорода, а –NH2 группа реагирует с кислотами, классы органических веществ и их реакции покажутся однотипными.
Химия и жизнь
Название этого раздела кажется простым и понятным. К сожалению, именно здесь ученики чаще всего теряют баллы. В задании 24 необходимо мысленно представить эксперимент и написать, что произойдет при смешивании заданных веществ. Например, может выпасть осадок, выделиться газ, а может вообще ничего не произойти. В задании 25 нужно определить, где используют то или иное химическое соединение. Ответом может быть химическая промышленность, медицина, сельское хозяйство и, конечно, повседневная жизнь человека.
Решение расчетных задач
Очень важная часть экзамена по химии. В заданиях 26, 27 и 28 в первой части нужно дать ответ в виде числа, не записывая решение. Обычно эти задачи решаются в одно действие — они проверяют не знания химических процессов, а навыки работы с калькулятором.
Задание 34, по мнению многих учеников — самое сложное во всем экзамене. Чтобы его решить, нужно знать химические свойства веществ, уметь составлять причинно-следственные связи в химических системах, понимать, какие вещества реагируют без остатка и почему. Кроме того, в последние годы все чаще встречаются задачи, которые необходимо решать с помощью линейных уравнений или их систем.
В задаче 32 нужно выполнить расчеты, которые позволят установить молекулярную формулу некоторого органического вещества. Далее, используя описание, необходимо представить эту формулу в структурном виде, показывая связи между атомами. Обязательно запишите в ответе уравнение реакции, о которой идет речь в условии!
Как подготовиться к ЕГЭ по химии 2023?
По структуре экзамена видно, что вам придется повторить или освоить заново весь курс химии за год. С какой темы начать? За что взяться в первую очередь?
Скачайте кодификатор по химии 2023 года. Обычно он находится вместе в демоверсией. В этом документе перечислены все темы, которые необходимо хорошо подготовить. Этот перечень охватывает все задания ЕГЭ, в нем нет ничего лишнего.
Подружитесь с таблицами. Периодическая система химических элементов Д. И. Менделеева, таблица растворимости кислот, солей и оснований, ряд активности металлов – это отличные шпаргалки, которые раздают вместе с вариантами на ЕГЭ. Если правильно ими воспользоваться, можно не только понять, протекает ли реакция между веществами, но даже установить среду раствора, силу кислоты и цвет осадка. И это еще не все!
Грамотно распределите время. Учите теорию, но и не забывайте практиковаться. Если вы не нарешаете тренировочных вариантов, время может сыграть злую шутку на реальном экзамене. 210 минут не хватает на размышления, решения, красивую запись и перепроверку. Необходимо работать в хорошем темпе!
Не оставляйте подготовку на конец года. Несмотря на распределение заданий по разделам химии, старайтесь решать их с самого начала подготовки, постепенно усложняя условия. И помните, что задачи второй части ЕГЭ оцениваются по критериям. Даже если вы не знаете, как решить задание полностью, вы всегда можете заработать 1-2 первичных балла, записав без ошибок уравнения химических реакций и проведя простейшие расчеты.
Прорешивайте как можно больше заданий. Это, пожалуй, самый главный совет. Чем больше вы будете тренироваться и решать типовые задачи, тем выше шансы получить на экзамене высокий балл. Все потому, что вы поймете алгоритм решения и сможете находить правильный ответ намного быстрее, чем другие выпускники.
Когда я готовлю к ЕГЭ по химии в MAXIMUM Education, мы посвящаем немало времени решению всех заданий экзамена. Мы разбираем все части экзамена и учимся правильно оформлять ответы, чтобы не потерять ни одного балла. Чтобы проверить, все ли понятно ученикам, я провожу срезы знаний и даже пробный экзамен. После него я разбираю ошибки с каждым учеником отдельно, и дополнительно объясняю сложные темы.
После такой подготовки мои выпускники пишут настоящий экзамен уверенно и получают высокие баллы. Точно выше среднего балла по стране 🙃 Хотите так же? Приходите на мои занятия, и я научу вас всему, что знаю!
- ЕГЭ по химии
Видео разбор демоверсии ЕГЭ по химии 2023 года от Елены Тарасовой.
Изменения в КИМ ЕГЭ 2023 года в сравнении с КИМ 2022 года
В экзаменационной работе 2023 г. по сравнению с работой 2022 г. приняты следующие изменения.
1. Изменён формат предъявления условия задания 23, ориентированного на проверку умения проводить расчёты концентраций веществ в равновесной системе: вместо табличной формы предъявления количественных данных все элементы будут представлены в форме текста.
2. Изменён порядок следования заданий 33 и 34.
3. Изменён уровень сложности заданий 9, 12 и 16: в 2023 г. указанные задания будут представлены на повышенном уровне сложности.
В целом принятые изменения в экзаменационной работе 2023 г. ориентированы на повышение объективности проверки сформированности ряда важных метапредметных умений, в первую очередь таких, как анализ текста условия задания, представленного в различной форме (таблица, схема, график), комбинирование аналитической и расчётной деятельности, анализ состава веществ и прогноз возможности протекания реакций между ними, моделирование процессов и описание признаков их протекания и др.
Смотрите также:
Фотографии: АГН «Москва» / Pixabay. Иллюстрация: Юлия Замжицкая
О нововведениях и нюансах подготовки рассказывает руководитель комиссии по разработке контрольно-измерительных материалов ЕГЭ по химии, кандидат педагогических наук Дмитрий Добротин.
Основные изменения
В этом году изменения минимальные. В целом структура работы осталась практически без корректировок.
Изменилось условие задания 23
Скриншот задания 23 из демоверсии ЕГЭ-2023 по химии
Из условия убрали таблицу, в которые были представлены концентрации, характерные для веществ, находящихся в данном состоянии равновесия.
Эксперты предполагают, что такую таблицу экзаменуемый может составить сам. Для этого не требуется каких-то специальных навыков: это классическая таблица, где заложены и концентрации исходных вещественных продуктов реакции, и, соответственно, их значения.
Изменения в задании 32 на «цепочки превращений»
Скриншот задания 32 из демоверсии ЕГЭ-2023 по химии
Если традиционная цепочка предполагает, что превращения идут слева направо, то в этом году появилось новшество, которое предполагает, что стрелочки к веществу или обозначению, который заменяет вещество (имеется в виду x1, x2 и т. д.) могут стоять как в направлении к веществу, так и от вещества.
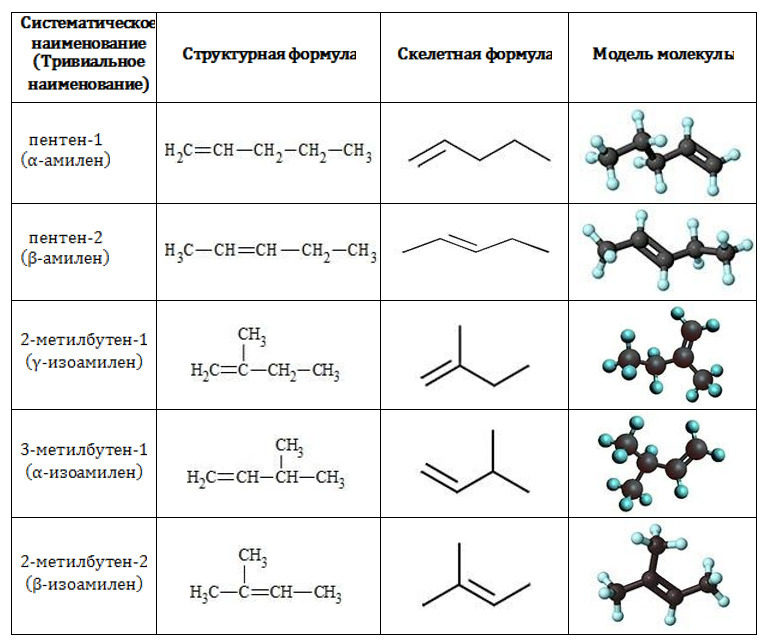
Появились «скелетные формулы»
«Скелетная формула» — это когда отдельные атомы обозначаются только в виде ломанной линии.
Примеры «скелетных формул»
К такой форме записи органических веществ многие уже привыкли, но для некоторых это может стать неожиданностью. Но такие формулы записи молекул могут быть. На это обращает внимание и примечание, которое идет после критериев оценивания.
Кому-то такая форма записи органических веществ будет удобна, и это можно использовать и в рамках записи своих уравнений, реакций. Но и в целом можно переводить и в привычный формат так называемых свернутых формул — в этом тоже нет никаких нарушений.
Задания 33 и 34 поменяли местами
Это сделали, чтобы после того, как учащиеся выполнят цепочку превращений с использованием знания в органических веществах, им будет удобнее сразу перейти именно к расчетной задаче, в которой нужно вывести молекулярную формулу органического вещества.
Завершающая задача 34 действительно самая сложная. На последнем месте ее разместили затем, чтобы экзаменуемый мог спокойно сосредоточиться на ней и уделить ей столько времени, сколько потребуется.
На что обратить внимание и как готовиться
-
Внимательно читать задание и инструкции
Например, в расчетных задачах 27 и 28 в качестве относительной атомной массы хлора используют значение 35,5. Это принципиальный момент, потому что в этих задачах нужно записать ответ с конкретной точностью, тоже указанной в условии задания.
Совет от эксперта:
«Машина не распознает никакое другое значение, кроме того, которое было заложено. Поэтому в данном случае очень важно следовать инструкциям и округлять с той заданной точностью, которая указана в условии задания».
Бывают случаи, когда экзаменуемый прорешал много вариантов и у него сложился стереотип, что значения PH, как правило, выстраиваются в порядке возрастания. Однако встречаются и задания, в которых их надо выстроить в порядке убывания.
-
Выделить достаточно времени на проверку работы
За 20 минут до окончания экзамена стоит начать проверку: все ли решено, все ли инструкции учтены. В тех заданиях, где это играет принципиальную роль, стоит быть максимально внимательным к деталям, которые могут привести к серьезной потере баллов.
-
При подготовке обратить особое внимание на самые сложные задания
Как показывает практика, это задания 33, 34, а также 24 и 25, которое связано с промышленным производством, способами получения веществ и их применением.
Совет от эксперта:
«Для того, чтобы лучше справиться с заданиями 24 и 25, ведите таблицы, которые помогают фиксировать внешние наблюдения за химическим экспериментом. Стоит вести их в течение всего периода обучения химии, а уж когда выпускник определился с выбором предметов, это точно пригодится».
Отдельное внимание стоит обратить на задание 25, которое предполагает проверку знаний и умения определять, какой аппарат требуется для получения того или иного вещества, в какой области его применяют. Нередко в школе педагоги отдают этот вопрос на самостоятельное изучение. Поэтому полезно до экзамена собрать и систематизировать эту информацию, как по органической химии, так и по неорганической.
-
Не ограничиваться подготовкой только по моделям ЕГЭ
Практика показывает, что если старшеклассник идет по пути подготовки к конкретным моделям экзамена, то как только встречаются нюансы в условии, отличные от того, к чему он готовился, он испытывает стресс. А если экзаменуемый в целом владеет необходимым теоретическим материалом, то не будет принципиальным, как его о нем спрашивают.
Самый оптимальный вариант — интенсифицировать процесс подготовки с опорой на классические учебники, либо пособия для подготовки абитуриентов, либо школьные учебники углубленного уровня, либо на материалы, которые размещены на сайте ФИПИ. В навигаторе ФИПИ приведены задания, которые соответствуют тем позициям, которые встречаются в экзаменационном варианте. Кроме того, там есть ссылки учебники, которые могут выступать в качестве помощников при подготовке.
Посмотреть полную версию консультации Дмитрия Добротина в эфире Рособрнадзора можно здесь.
Материалы по теме:
- Что изменится в ЕГЭ по русскому языку в 2023 году
- Что изменится в ЕГЭ по английскому языку в 2023 году
- Что изменится в ЕГЭ по истории в 2023 году
Если вам нравятся материалы на Педсовете, подпишитесь на наш канал в Телеграме, чтобы быть в курсе событий раньше всех.
Подписаться
Содержание
- 1 Общая информация
- 2 Изменения 2023 года
- 3 Даты проведения
- 4 Структура КИМов
- 5 Оценивание
- 6 Подготовка
Если вы планируете связать свою жизнь с медициной, биохимией, фармацевтической отраслью, а также различного рода лабораторными исследованиями, то в 2023 году на ЕГЭ среди предметов по выбору стоит сдавать экзамен по химии. В данном материале мы детально разберем, какие изменения будут внесены ФИПИ в материалы 2023 года, какой будет структура КИМов, когда станет известна дата испытаний и какой должна быть самостоятельная подготовка 11-классника для достижения наилучшего результата.
Общая информация
В 2023 году ЕГЭ по химии предположительно будут сдавать около 15% выпускников. В прошлом сезоне из 701 000 участников ГИА предмет выбрали 95 000 человек. Стоит заметить, что, несмотря на небольшой процент участников, количество ребят, которые справились с поставленной задачей на высокий балл, значительно выше, чем в дисциплинах ТОП-3 (обществознание, биология, информатика). Это говорит о том, что ЕГЭ по химии выбирают осознанно, а значит и подготовка к экзамену осуществляется более качественно (и 2023 год не станет исключением).
Неизменными для предмета «химия» в 2023 году останутся такие основные факты:
- время на выполнение работы – 210 мин (3,5 часа);
- КИМ состоит из 2-х частей;
- общее количество вопросов – 34 шт.;
- максимальный балл – 56 ПБ;
- разрешенные материалы: таблица Менделеева, таблица растворимости солей, электрохимический ряд напряжений металлов.
- на экзамене разрешено использовать непрограммируемый калькулятор.
Важно! В отличие от ОГЭ по химии, Единый Государственный Экзамен не включает в себя проведение реального химического эксперимента. Организаторы ограничиваются проверкой умения выпускника планировать проведение эксперимента.
Изменения 2023 года
В 2023 году многие КИМы ЕГЭ будут модернизированы, затронут изменения и экзаменационные материалы по химии. Новый вариант будет отличаться от билетов 2022 года такими позициями:
| Задание | Изменение |
| № 9, 12, 16 | уровень сложности изменен на «повышенный» |
| № 23 | вместо табличного формата представления данных в задаче на расчет концентрации веществ будет использован классический текстовый |
| № 33 и 34 | просто поменяли местами |
В спецификациях указано, что каждый вариант КИМа будет включать в себя задачи с условиями, представленными в виде текста, таблицы, графика и схемы.
Даты проведения
Рособрнадзор планирует в полном объеме провести все три сессии ЕГЭ, а для допуска к основным испытаниям 11-классникам традиционно необходимо будет получить зачет по декабрьскому сочинению.
Календарь ГИА-2023 определяет для сдачи ЕГЭ по химии такие даты:
| Сессия | Основной день | Резерв |
| Досрочная | 10 апреля | 12 апреля |
| Основная | 26 мая | 28 июня, 1 июля |
| Дополнительная | — | — |
Важно! Пересдать химию, как и любой другой необязательный предмет, в сентябре, уже нельзя.
Структура КИМов
В экзаменационной работе выпускникам будет предложено 34 вопроса, среди которых встретятся задания различного уровня сложности:
| Уровень сложности | Кол-во | Вопросы |
| базовый | 17 шт. | № 1–5, 10, 11, 13, 17–21, 25–28 |
| повышенный | 11 шт. | № 6–9, 12, 14–16, 22–24 |
| высокий | 6 шт. | № 29–34 |
КИМ будет разделен на I и II часть:
| Часть | Ответ | Кол-во вопросов |
| I ч. | краткий | 28 шт. |
| II ч. | развернутый | 6 шт. |
Экзаменационная работа будет проверять знания и умения выпускника по всем темам школьного курса:
- теоретическая основа химии;
- химические реакции;
- органические и неорганические вещества;
- методы познания;
- уравнения реакций (расчеты по формулам).
Полный список требований можно найти в кодификаторе на сайте ФИПИ.
Оценивание
За идеальное решение всех 34 заданий КИМа эксперты могут выставить экзаменуемому максимально 56 ПБ.
Каждое задание 1 части и каждая задача 2 части имеют свой максимальный ПБ:
| Макс. ПБ | Задания |
| 1 ПБ | № 1 – 5, 9 – 13, 16 – 21, 25 – 28 |
| 2 ПБ | № 6 – 8, 14 – 15, 22 – 24, 29 – 30 |
| 3 ПБ | № 33 |
| 4 ПБ | № 31, 34 |
| 5 ПБ | № 32 |
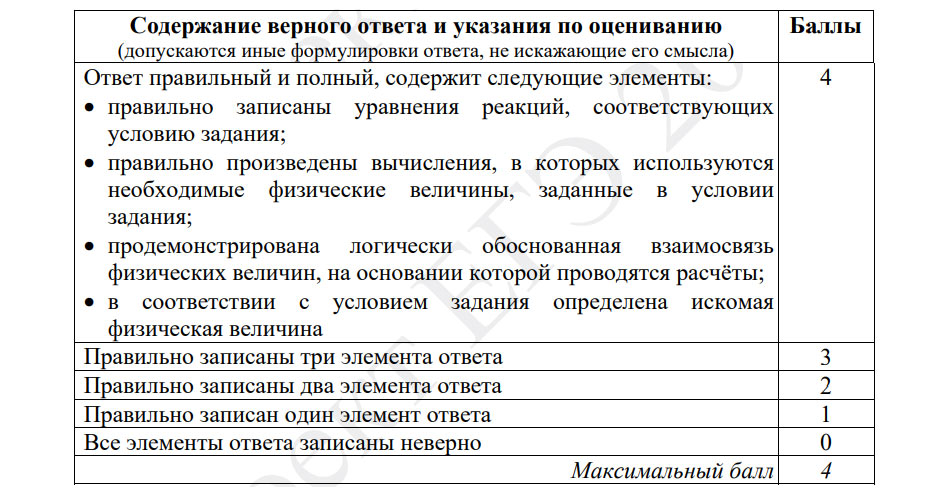
При этом для каждой из задач, оцениваемых по 3-5 баллов, разработаны свои критерии оценивания, которые детально описаны в демоверсии КИМа 2023 года, представленной на сайте fipi.ru.
Задача № 31
Задача № 32
Задача № 33
Задача № 34
Важно! Если выпускник допустил ошибку в вычислениях, которая в итоге привела к неправильному ответу, но при этом все остальные критерии выполнены, оценка за решение задачи снижается только на 1 ПБ.
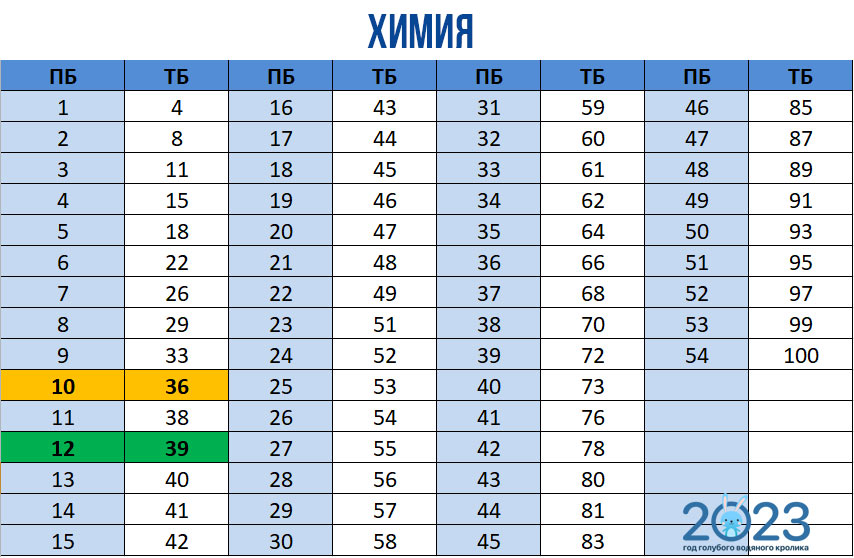
После завершения проверки баллы за первую и вторую часть суммируют, а далее переводят результат в тестовые баллы по такой таблице соответствия:
Обратите внимание, что необходимый минимум 2023 года по химии – всего 10 ПБ (36 ТБ), а рекомендованный минимум для ВУЗов Минобрнуаки – 12 ПБ (39 ТБ). В реальности выпускникам стоит брать ориентир на более высокий результат – 85+ ТБ.
Подготовка
Реально ли сдать ЕГЭ по химии в 2023 году на 100 баллов, и какой должна быть подготовка для достижения такого результата?
Педагоги едины во мнении, что начинать готовиться к выпускному экзамену по химии лучше всего еще в 9 классе, выбрав для сдачи ОГЭ по химии. Таким образом, выпускник может заложить хорошую основу для дальнейшей подготовки к ЕГЭ.
Но даже если вы решили сдавать предмет, перейдя в 11 класс, есть все шансы добиться успеха, если:
- вы настойчивы и готовы серьезно потрудиться;
- ваш уровень владения предметом – твердая «четверка» и выше;
- вам готов помогать школьный учитель или хороший репетитор.
Традиционно подготовка начинается с разбора особенностей КИМов, и в этом мы вам немного помогли. Следующий шаг – составление индивидуального плана занятий, с учетом тем, которые вы помните хорошо и разделов, знания по которым необходимо освежить или сформировать «с нуля».
Прорабатывайте материал блоками, закрепляя теоретический материал решением типовых экзаменационных заданий. Найти материал для тренировки можно либо в печатных сборниках, либо в режиме онлайн – в открытой базе ФИПИ.
Если с какой-то темой возникают затруднения, не ищите готовых решений экзаменационных вопросов – ищите хороший разбор самой темы от опытного педагога.
Также учителя советуют:
- научиться использовать таблицы – это ваши официальные «подсказки» на ЕГЭ;
- следить за временем в ходе тренировки, ведь на экзамене не будет лишних минут на размышления;
- помнить о правильности оформления ответов (особенно развернутых к задачам 2-й части).
Поднять подробнее, на что обратить особе внимание, выполняя каждое из предложенных заданий ЕГЭ 2023 года по химии, поможет разбор демонстрационного варианта:
Читайте также:
- ЕГЭ по физике в 2023 году
- Орфоэпический минимум ЕГЭ в 2023 году
- ЕГЭ по информатике в 2023 году











































.jpg)
.jpg)