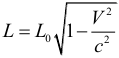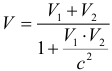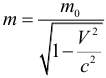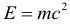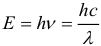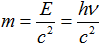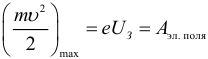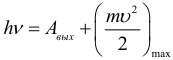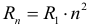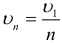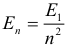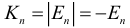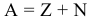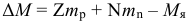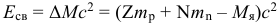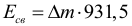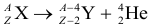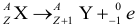Атомная физика на ОГЭ. Вся теория и разбор заданий от преподавателя MAXIMUM
06.02.2021
17404
Атомная физика — один из труднейших разделов экзамена, а задания по этой теме кочуют из варианта в вариант каждый год. Не пугаемся! Для решения заданий ОГЭ на радиоактивность, распады и ядерные реакции нужно знать лишь самые базовые понятия. Из этой статьи вы узнаете все необходимое — атомная физика на ОГЭ обязательно вам покорится!
Чтобы перейти к практике и научиться решать хитрые задания, сначала нужно вспомнить теорию, связанную с ними.
Вспомним, что химические элементы обозначаются в виде , где
- X – название химического элемента
- А – массовое число, равное сумме протонов и нейтронов
- Z – зарядовое число, равное числу протонов в ядре
Давайте раз и навсегда узнаем, что скрывается за числами рядом с названием каждого элемента. Рассмотрим пример углерода:
- 6 — это порядковый номер и зарядовое число Z. Таким образом, в ядре атома углерода 6 протонов. Z=6.
- 12,011 — это атомная масса. Мы будем его округлять до 12 и называть массовым числом A, то есть суммой протонов и нейтронов. A=12.
- Получается, в ядре атома углерода 6 протонов и 6 нейтронов.
Какие ядерные распады нужно знать?
На ОГЭ часто встречаются три типа распадов: альфа, бета и гамма.
Альфа-распад
α-распад — испускание ядром альфа-частицы. Что это такое? Все просто — так называют ядро атома гелия, то есть частицу из двух протонов и двух нейтронов.
- У нас был элемент X с массовым числом A и с зарядовым числом Z
- Атом испускает альфа-частицу с массовым числом=4 и зарядовым числом=2
- Мы получаем новый элемент с массовым числом=A-4 и зарядовым числом=Z-2
В α-распаде заряд уменьшается на 2, а масса уменьшается на 4.
Самостоятельно подготовиться к ОГЭ непросто. На то, чтобы разобраться со всеми темами, понадобится много времени. Но и это не решит проблему! Например, если вы запомнили какое-то решение из интернета, а оно оказалось неправильным, можно на пустом месте потерять баллы. Если хотите научиться решать все задания ОГЭ по физике, обратите внимание на онлайн-курсы MAXIMUM! Наши специалисты уже проанализировали сотни вариантов ОГЭ и подготовили для вас вас максимально полезные занятия.
Приходите к нам на пробный урок! Вы узнаете всю структуру ОГЭ-2021, разберете сложные задания из первой части, получите полезные рекомендации и узнаете, как устроена подготовка к экзаменам в MAXIMUM. Все это абсолютно бесплатно!
Задача №1
Используя фрагмент Периодической системы элементов Д.И. Менделеева, представленный на рисунке, определите, какое ядро образуется в результате α-распада ядра нептуния-237.
Разбор
- Как мы говорили чуть выше, порядковый номер элемента — это, по совместительству, зарядовое число. То есть, количество протонов. Получается, в Нептунии 93 протона.
- У α-частицы количество протонов = 2.
- Посчитаем, чему равно зарядовое число нашего нового элемента: зарядовое число = 93-2 = 91. Взглянув на табличку, находим элемент под номером 91 — Протактиний.
Ответ: 1) Ядро протактиния
Изотопы
Теперь давай обратим внимание на массовые числа нептуния и протактиния. Отличаются ли они на массовое число альфа-частицы — на 4?
237-231=6
Время бить тревогу! Неужели мы что-то напутали и решили задачу неверно? Но нет, оказывается, мы все сделали правильно — ведь у протактиния более 15 изотопов.
Изотопы — это разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковое зарядовое число, но разные массовые числа.
Например, изотопы азота:
и
Задача №2
Ядро тория превратилось в ядро радия
. Какую частицу испустило при этом ядро тория?
- нейтрон
- протон
- альфа-частицу
- бета-частицу
Разбор
- Сверху находится массовое число — масса частицы. Вычтем из массы Тория массу Радия: 230-226=4. Получили массу неизвестной частицы.
- Снизу находится зарядовое число — это заряд неизвестной частицы. Вычтем из заряда Тория заряд Радия: 90-88=2. Получили заряд неизвестной частицы.
- Итого: массовое число = 4. Зарядовое число = 2
- Взглянем на табличку самых распространенных частиц.
Вуаля! Наша незнакомка — это альфа-частица — частица с двумя протонами и двумя нейтронами.
Ответ: 3) альфа-частица
Бета-распад
β-распад — испускание ядром бета-частицы. Бета-частицей называют электрон. Посмотрим в списке основных частиц наверху, чему равны массовое и зарядовое число бета-частицы (электрона).
- У нас был элемент X с массовым числом A и с зарядовым числом Z
- Атом испускает бета-частицу с массовым числом=0 и зарядовым числом=-1
- Мы получаем новый элемент с прежним массовым числом=A и зарядовым числом=Z+1
В β-распаде заряд увеличивается на 1, а масса не меняется.
Задача №3
Изотоп криптона в результате серии распадов превратился изотоп молибдена . Сколько β-частиц было испущено в этой серии распадов?
Разбор
- Обозначим количество испущенных β-частиц за N
- Зарядовое число криптона до серии β-распадов равнялось 36
- Зарядовое число молибдена после серии β-распадов 42
- Тогда 42-36=6 β распадов
Ответ: было испущено 6 β распадов
Задача №4
Радиоактивный атом превратился в атом
в результате цепочки альфа- и бета-распадов. Чему было равно число альфа- и бета-распадов?
Разбор
Эта задача требует максимальной концентрации — многие школьники ее решают неверно. Давайте разберем правильный подход к этой задаче.
- Для начала рассмотрим альфа-распады
- Добьемся, чтобы массовое число изменилось с 232 до 208. Для этого производим альфа-распады, вычитая 4 из массового числа и 2 из зарядового числа.
- Получили элемент с массовым числом=208 и зарядовым числом=78. Для этого мы произвели 6 альфа распадов.
- Теперь перейдем к бета-распадам. Бета-распады влияют только на зарядовое число.
- Добьемся того, чтобы зарядовое число изменилось с 78 до 82.
- Получили элемент с массовым числом = 208 и зарядовым числом = 82. Для этого мы произвели 4 бета распада.
Ответ: 6 альфа распадов и 4 бета распада.
Гамма-распад
?-частицы — это излучение, а ?-распад — испускание ядром гамма-излучения. Пожалуй, это самый простой распад, потому что он ничего не меняет.
Элемент X до распада и элемент Y после распада — это одно и то же.
Внимание! На ОГЭ ученики часто попадают в ловушки экзамена, считая, что ? излучение меняет элемент. Но это совсем не так! Какой элемент был до гамма-распада, такой и останется.
При ?-распаде заряд и масса не меняются.
Ядерные реакции
Атомная физика на ОГЭ включает в себя не только распады, но и ядерные реакции. Ядерные реакции происходят при столкновении ядер или элементарных частиц с другими ядрами. В результате изменяется массовое и зарядовое число элементов, появляются новые частицы.
Во всех ядерных реакциях работает очень простой лайфхак: при протекании ядерной реакции сохраняется суммарное массовое число и суммарный заряд.
Сумма масс слева равна сумме масс справа: A1+A2=A3+A4.
Сумма зарядов слева равна сумме зарядов справа: Z1+Z2=Z3+Z4.
Сразу же закрепим эти правила на практике.
Задача 5
В результате столкновения ядра урана с частицей X произошло деление урана, описываемое реакцией:
Определите зарядовое и массовое числа частицы X, с которой столкнулось ядро урана.
Разбор
- Сначала разберемся с массовым числом. Используем лайфхак: то, что слева, равно тому, что справа.
- Также заметим, что у нас 3 нейтрона. Получается, нам нужно умножить массовое число нейтрона на 3.
- С гамма-частицей разобраться легко — как мы показали ранее, она ни на что не влияет.
A+235 = 133+139+3*1
Отсюда A=133+139+3-235=40
- Теперь настал черед зарядового числа.
Z+92 = 36+56+3*0
Отсюда Z=36+56+0-92=0
Ответ: получили элемент X c массовым числом 40 и зарядовым числом 0.
Атомная физика на ОГЭ: что нужно запомнить?
- В α-распаде заряд уменьшается на 2, а масса уменьшается на 4.
- α-частица — это ядро атома гелия. α-частица состоит из двух протонов и двух нейтронов.
- В β-распаде заряд увеличивается на 1, а масса не меняется.
- β-частица — это электрон.
- В ?-распаде заряд и масса не меняются.
- ?-частица — это порция электромагнитного излучения.
- Изотопы — это разновидности атомов (и ядер) какого либо химического элемента, которые имеют одинаковое зарядовое число, но разные массовые числа.
- В ядерных реакциях сохраняется суммарное массовое число и суммарный заряд.
Теперь вы знаете, как решать задания на ядерные распады и реакции! Надеюсь, атомная физика на ОГЭ стала для вас намного понятнее. Если хотите разобраться в остальных темах по физике и не только, обратите внимание на наши онлайн-курсы. Уже более 150 тысяч выпускников подготовились с нами к ОГЭ и ЕГЭ. Кстати, у меня на курсах MAXIMUM тоже можно поучиться! Приходите на бесплатный пробный урок, чтобы познакомиться с нашей образовательной системой и узнать массу полезного про ОГЭ.
Лайфхаки экзамена
К рубрике
Оглавление:
- Основные теоретические сведения
- Основы специальной теории относительности
- Фотон и его свойства
- Внешний фотоэффект
- Постулаты Бора
- Атомное ядро
- Радиоактивность. Закон радиоактивного распада
- Ядерные реакции
Основные теоретические сведения
Основы специальной теории относительности
К оглавлению…
Специальная теория относительности (СТО) базируется на двух постулатах:
- Принцип относительности: в любых инерциальных системах отсчета все физические явления при одних и тех же исходных условиях протекают одинаково, т.е. никакими опытами, проведенными в замкнутой системе тел, нельзя обнаружить покоится ли тело или движется равномерно и прямолинейно.
- Принцип постоянства скорости света: во всех инерциальных системах отсчета скорость света в вакууме одинакова и не зависит от скорости движущегося источника света.
Равное с постулатами СТО имеет значение положение СТО о предельном характере скорости света в вакууме: скорость любого сигнала в природе не может превосходить скорость света в вакууме: c = 3∙108 м/с. При движении объектов со скоростью сопоставимой со скоростью света, наблюдаются различные эффекты, описанные далее.
1. Релятивистское сокращение длины.
Длина тела в системе отсчета, где оно покоится, называется собственной длиной L0. Тогда длина тела движущегося со скоростью V в инерциальной системе отсчета уменьшается в направлении движения до длины:
где: c – скорость света в вакууме, L0 – длина тела в неподвижной системе отсчета (длина покоящегося тела), L – длина тела в системе отсчета, движущейся со скоростью V (длина тела, движущегося со скоростью V). Таким образом, длина тела является относительной. Сокращение тел заметно, только при скоростях, сопоставимых со скоростью света.
2. Релятивистское удлинение времени события.
Длительность явления, происходящего в некоторой точке пространства, будет наименьшей в той инерциальной системе отсчета, относительно которой эта точка неподвижна. Это означает, что часы, движущиеся относительно инерциальной системы отсчета, идут медленнее неподвижных часов и показывают больший промежуток времени между событиями. Релятивистское замедление времени становится заметным лишь при скоростях сопоставимых со скоростью света, и выражается формулой:
Время τ0, замеренное по часам, покоящимся относительно тела, называется собственным временем события.
3. Релятивистский закон сложения скоростей.
Закон сложения скоростей в механике Ньютона противоречит постулатам СТО и заменяется новым релятивистским законом сложения скоростей. Если два тела движутся навстречу друг другу, то их скорость сближения выражается формулой:
где: V1 и V2 – скорости движения тел относительно неподвижной системы отсчета. Если же тела движутся в одном направлении, то их относительная скорость:
4. Релятивистское увеличение массы.
Масса движущегося тела m больше, чем масса покоя тела m0:
5. Связь энергии и массы тела.
С точки зрения теории относительности масса тела и энергия тела – это практически одно и то же. Таким образом, только факт существования тела означает, что у тела есть энергия. Наименьшей энергией Е0 тело обладает в инерциальной системе отсчета относительно которой оно покоится и называется собственной энергией тела (энергия покоя тела):
Любое изменение энергии тела означает изменение массы тела и наоборот:
где: ∆E – изменение энергии тела, ∆m – соответствующее изменение массы. Полная энергия тела:
где: m – масса тела. Полная энергия тела Е пропорциональна релятивистской массе и зависит от скорости движущегося тела, в этом смысле важны следующие соотношения:
Кстати кинетическую энергию тела, движущегося с релятивистской скоростью, можно считать только по формуле:
С точки зрения теории относительности закон сохранения масс покоя несправедлив. Например, масса покоя атомного ядра меньше суммы масс покоя частиц, входящих в ядро. Однако, масса покоя частицы способной к самопроизвольному распаду больше суммы собственных масс составляющих ее.
Это не означает нарушения закона сохранения массы. В теории относительности справедлив закон сохранения релятивистской массы, так как в изолированной системе тел сохраняется полная энергия, а значит и релятивистская масса, что следует из формулы Эйнштейна, таким образом можно говорить о едином законе сохранения массы и энергии. Это не означает возможность перехода массы в энергию и наоборот.
Между полной энергией тела, энергией покоя и импульсом существует зависимость:
Фотон и его свойства
К оглавлению…
Свет – это поток квантов электромагнитного излучения, называемых фотонами. Фотон – это частица, переносящая энергию света. Он не может находиться в покое, а всегда движется со скоростью, равной скорости света. Фотон обладает следующими характеристиками:
1. Энергия фотонов равна:
где: h = 6,63∙10–34 Дж∙с = 4,14∙10–15 эВ∙с – постоянная Планка, ν – частота света, λ – длина волны света, c – скорость света в вакууме. Энергия фотона в Джоулях очень мала, поэтому для математического удобства ее часто измеряют во внесистемной единице – электрон-вольтах:
1 эВ = 1,6∙10–19 Дж.
2. Фотон движется в вакууме со скоростью света c.
3. Фотон обладает импульсом:
4. Фотон не обладает массой в привычном для нас смысле (той массой, которую можно измерить на весах, рассчитать по второму закону Ньютона и так далее), но в соответствии с теорией относительности Эйнштейна, обладает массой как мерой энергии (E = mc2). Действительно, любое тело, имеющее некоторую энергию, имеет и массу. Если учесть, что фотон обладает энергией, то он обладает и массой, которую можно найти как:
5. Фотон не обладает электрическим зарядом.
Свет обладает двойственной природой. При распространении света проявляются его волновые свойства (интерференция, дифракция, поляризация), а при взаимодействии с веществом – корпускулярные (фотоэффект). Эта двойственная природа света получила название корпускулярно-волнового дуализма.
Внешний фотоэффект
К оглавлению…
Фотоэлектрический эффект – явление, заключающееся в появлении фототока в вакуумном баллоне при освещении катода монохроматическим светом некоторой длины волны λ.
Когда напряжение на аноде отрицательно, электрическое поле между катодом и анодом тормозит электроны. Измеряя данное задерживающее напряжение при котором исчезает фототок, можно определить максимальную кинетическую энергию фотоэлектронов вырываемых из катода:
Многочисленными экспериментаторами были установлены следующие основные закономерности фотоэффекта:
- Фотоэффект безынерционен. Это значит, что электроны начинают вылетать из металла сразу же после начала облучения светом.
- Максимальная кинетическая энергия фотоэлектронов линейно возрастает с увеличением частоты света ν и не зависит от его интенсивности.
- Для каждого вещества существует так называемая красная граница фотоэффекта, то есть наименьшая частота νmin (или наибольшая длина волны λmax) при которой еще возможен внешний фотоэффект.
- Число фотоэлектронов, вырываемых светом из катода за 1 с, прямо пропорционально интенсивности света.
При взаимодействии с веществом фотон целиком передает всю свою энергию E = hν одному электрону. Часть этой энергии электрон может рассеять при столкновениях с атомами вещества. Кроме того, часть энергии электрона затрачивается на преодоление потенциального барьера на границе металл–вакуум. Для этого электрон должен совершить работу выхода Aвых, зависящую от свойств материала катода. Наибольшая кинетическая энергия, которую может иметь вылетевший из катода фотоэлектрон, в таком случае, определяется законом сохранения энергии:
Эту формулу принято называть уравнением Эйнштейна для внешнего фотоэффекта. С помощью уравнения Эйнштейна можно объяснить все закономерности внешнего фотоэффекта. Для красной границы фотоэффекта, согласно формуле Эйнштейна, можно получить выражение:
Постулаты Бора
К оглавлению…
Первый постулат Бора (постулат стационарных состояний): атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная номер n и энергия En. В стационарных состояниях атом не излучает и не поглощает энергию.
Состоянию с наименьшей энергией присваивается номер «1». Оно называется основным. Всем остальным состояниям присваиваются последовательные номера «2», «3» и так далее. Они называются возбужденными. В основном состоянии атом может находиться бесконечно долго. В возбужденном состоянии атом живет некоторое время (порядка 10 нс) и переходит в основное состояние.
Согласно первому постулату Бора, атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию. Механическая энергия электрона, движущегося по замкнутой траектории вокруг положительно заряженного ядра, отрицательна. Поэтому всем стационарным состояниям соответствуют значения энергии En < 0. При En ≥ 0 электрон удаляется от ядра (происходит ионизация). Величина |E1| называется энергией ионизации. Состояние с энергией E1 называется основным состоянием атома.
Второй постулат Бора (правило частот): при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний:
Атом водорода
Простейший из атомов – атом водорода. Он содержит единственный электрон. Ядром атома является протон – положительно заряженная частица, заряд которой равен по модулю заряду электрона. Обычно электрон находится на первом (основном, невозбужденном) энергетическом уровне (электрон, как и любая другая система, стремится к состоянию с минимумом энергии). В этом состоянии его энергия равна E1 = –13,6 эВ. В атоме водорода выполняются следующие соотношения, связывающие радиус траектории вращающегося вокруг ядра электрона, его скорость и энергию на первой орбите с аналогичными характеристиками на остальных орбитах:
На любой орбите в атоме водорода кинетическая (К) и потенциальная (П) энергии электрона связаны с полной энергией (Е) следующими формулами:
Атомное ядро
К оглавлению…
В настоящее время твердо установлено, что атомные ядра различных элементов состоят из двух частиц – протонов и нейтронов, которые принято называть нуклонами. Для характеристики атомных ядер вводится ряд обозначений. Число протонов, входящих в состав атомного ядра, обозначают символом Z и называют зарядовым числом или атомным номером (это порядковый номер в периодической таблице Менделеева). Число нейтронов обозначают символом N. Общее число нуклонов (то есть протонов и нейтронов) называют массовым числом A, для которого можно записать следующую формулу:
Энергия связи. Дефект массы
Важнейшую роль в ядерной физике играет понятие энергии связи ядра. Энергия связи ядра равна минимальной энергии, которую необходимо затратить для полного расщепления ядра на отдельные частицы. Из закона сохранения энергии следует, что энергия связи равна той энергии, которая выделяется при образовании ядра из отдельных частиц.
Энергию связи любого ядра можно определить с помощью точного измерения его массы. Такие измерения показывают, что масса любого ядра Mя всегда меньше суммы масс входящих в его состав протонов и нейтронов: Mя < Zmp + Nmn. При этом разность этих масс называется дефектом масс, и вычисляется по формуле:
По дефекту массы можно определить с помощью формулы Эйнштейна E = mc2 энергию, выделившуюся при образовании данного ядра, то есть энергию связи ядра Eсв:
Но удобнее рассчитывать энергию связи по другой формуле (здесь массы берутся в атомных единицах, а энергия связи получается в МэВ):
Радиоактивность. Закон радиоактивного распада
К оглавлению…
Почти 90% из известных атомных ядер нестабильны. Нестабильное ядро самопроизвольно превращается в другие ядра с испусканием частиц. Это свойство ядер называется радиоактивностью.
Альфа-распад. Альфа-распадом называется самопроизвольное превращение атомного ядра с числом протонов Z и нейтронов N в другое (дочернее) ядро, содержащее число протонов Z – 2 и нейтронов N – 2. При этом испускается α-частица – ядро атома гелия 42He. Общая схема альфа-распада:
Бета-распад. При бета-распаде из ядра вылетает электрон (0–1e). Схема бета-распада:
Гамма-распад. В отличие от α— и β-радиоактивности γ-радиоактивность ядер не связана с изменением внутренней структуры ядра и не сопровождается изменением зарядового или массового чисел. Как при α-, так и при β-распаде дочернее ядро может оказаться в некотором возбужденном состоянии и иметь избыток энергии. Переход ядра из возбужденного состояния в основное сопровождается испусканием одного или нескольких γ-квантов, энергия которых может достигать нескольких МэВ.
Закон радиоактивного распада. В любом образце радиоактивного вещества содержится огромное число радиоактивных атомов. Так как радиоактивный распад имеет случайный характер и не зависит от внешних условий, то закон убывания количества N(t) нераспавшихся к данному моменту времени t ядер может служить важной статистической характеристикой процесса радиоактивного распада. Закон радиоактивного распада имеет вид:
Величина T называется периодом полураспада, N0 – начальное число радиоактивных ядер при t = 0. Период полураспада – основная величина, характеризующая скорость радиоактивного распада. Чем меньше период полураспада, тем интенсивнее протекает распад.
При α— и β-радиоактивном распаде дочернее ядро также может оказаться нестабильным. Поэтому возможны серии последовательных радиоактивных распадов, которые заканчиваются образованием стабильных ядер.
Ядерные реакции
К оглавлению…
Ядерная реакция – это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, сопровождающийся изменением состава и структуры ядра и выделением вторичных частиц или γ-квантов. В результате ядерных реакций могут образовываться новые радиоактивные изотопы, которых нет на Земле в естественных условиях.
При ядерных реакциях выполняется несколько законов сохранения: импульса, энергии, момента импульса, заряда. В дополнение к этим классическим законам сохранения при ядерных реакциях выполняется закон сохранения так называемого барионного заряда (то есть числа нуклонов – протонов и нейтронов). Например, в реакции общего вида:
Выполняются следующие условия (общее число нуклонов до и после реакции остается неизменным):
Энергетический выход ядерной реакции
Ядерные реакции сопровождаются энергетическими превращениями. Энергетическим выходом ядерной реакции называется величина:
где: MA и MB – массы исходных продуктов, MC и MD – массы конечных продуктов реакции. Величина ΔM называется дефектом масс. Ядерные реакции могут протекать с выделением (Q > 0) или с поглощением энергии (Q < 0). Во втором случае первоначальная кинетическая энергия исходных продуктов должна превышать величину |Q|, которая называется порогом реакции.
Для того чтобы ядерная реакция имела положительный энергетический выход, удельная энергия связи нуклонов в ядрах исходных продуктов должна быть меньше удельной энергии связи нуклонов в ядрах конечных продуктов. Это означает, что величина ΔM должна быть положительной.
ВОПРОСЫ
К ЭКЗАМЕНУ ПО АТОМНОЙ И ЯДЕРНОЙ ФИЗИКЕ.
(в
скобках указан уровень вопроса: 0 ‑
обязательный минимум;
1
‑ на оценку «хорошо»; 2 ‑ на
оценку «отлично»)
1.(0).
Опыты Резерфорда. Планетарная модель
атома.
2.(0).
Квантовые постулаты Бора. Опыты Франка
и Герца.
3.(0).
Модель водородоподобного атома по
теории Бора.
4.(0).
Волновые свойства микрочастиц. Волны
де‑Бройля.
5.(1).
Экспериментальные доказательства
волновых свойств микрочастиц.
6.(1).
Волновая функция, ее физический смысл.
7.(2).
Соотношения неопределенности.
8.(2).
Уравнение Шредингера.
9.(2).
Простейшие задачи квантовой механики.
Частица в «потенциальной яме»
(«ящике»).
10.(2).
Простейшие задачи квантовой механики.
Прохождение частицы через потенциальный
барьер. Туннельный эффект.
11.(2).
Простейшие задачи квантовой механики.
Линейный гармонический осциллятор.
12.(0).
Водородоподобный атом. Орбитальный и
собственный моменты импульса электрона
и описание различных состояний
электрона в атоме.
13.(1).
Спин и магнитный момент электрона.
14.(1).
Экспериментальные доказательства
существования спина и магнитного
момента электрона.
15.(0).
Ферми‑ и Бозе‑частицы. Принцип
Паули.
16.(0).
Строение электронных оболочек. Объяснение
периодической системы Д.И.Менделеева.
17.(1).
Полный момент импульса электрона в
атоме. Символические обозначения
термов. Правила отбора для оптических
переходов.
18.(2).
Векторная модель многоэлектронного
атома.
19.(2).
Квантовые состояния многоэлектронных
атомов. Правило Хунда.
20.(2).
Магнитный момент атома.
21.(2).
Эффект Зеемана.
22.(1).
Рентгеновские спектры. Закон Мозли.
23.(0).
Физика молекулы. Ковалентная и ионная
связь.
24.(0).
Состав атомного ядра. Изотопы и изобары.
Энергия связи атомного ядра.
25.(1).
Радиус, спин и магнитный момент ядра.
Статистика и четность ядер.
26.(2).
Методы измерения спина и магнитного
момента ядра. Ядерный магнитный
резонанс (ЯМР).
27.(1).
Капельная модель ядра. Формула Вейцзеккера
для энергии связи ядра.
28.(2).
Оболочечная модель ядра. Спин‑орбитальное
взаимодействие нуклонов в ядре.
29.(2).
Гиромагнитное отношение нуклона в
оболочечной модели ядра.
30.(0).
Радиоактивный распад ядер. Основной
закон радиоактивного распада.
31.(0).
Альфа‑распад ядер.
32.(2).
Теория альфа‑распада.
33.(0).
Бета‑распад ядер.
34.(0).
Гамма‑излучение ядер.
35.(2).
Эффект Мессбауэра.
36.(1).
Спонтанное деление ядер. Трансурановые
элементы.
37.(1).
Прохождение заряженных частиц и
гамма-квантов через вещество.
38.(0).
Дозиметрические единицы и защита от
радиоактивных излучений.
39.(0).
Детекторы частиц (счетчики и трековые
регистраторы).
40.(0).
Ядерные реакции; их классификация,
способы записи и общие закономерности.
41.(1).
Энергия и порог ядерной реакции. Законы
сохранения энергии, импульса, момента
импульса и четности в ядерных
реакциях.
42.(2).
Теория ядерных реакций.
43.(2).
Ядерные реакции под действием нейтронов.
Формулы Брейта‑Вигнера.
44.(0).
Цепная реакция деления тяжелых ядер
под действием нейтронов.
45.(0).
Ядерные реакторы на медленных и на
быстрых нейтронах.
46.(0).
Реакции термоядерного синтеза. Ядерные
реакции в звездах. Нуклеосинтез во
Вселенной.
47.(0).
Проблема управляемого термоядерного
синтеза (УТС). Магнитное удержание
плазмы. Установки типа ТОКАМАК.
48.(1).
Инерционное удержание плазмы. Лазерный
термоядерный синтез. Пузырьковый
термоядерный синтез. Мюонный катализ.
49.(0).
Элементарные частицы и их свойства.
Законы сохранения в физике элементарных
частиц.
50.(0).
Типы взаимодействий и классификация
элементарных частиц. Античастицы.
Виртуальные частицы.
51.(2).
Электромагнитные взаимодействия.
Диаграммы Фейнмана.
52.(1).
Сильные взаимодействия. Кварковая
структура мезонов и барионов.
Экспериментальные подтверждения
кварковой теории.
53.(2).Слабые
взаимодействия. Основные свойства
лептонов. Несохранение четности
в слабых взаимодействиях. Опыт
Ву.
54.(1).
Свойства нейтрино.
55.(1).
Космические лучи.
56.(2).
Стандартная
модель фундаментальных взаимодействий
в физике элементарных частиц.
Бозон Хиггса.
57.(2).
Недостатки Стандартной модели. Теория
струн.
ВОПРОСЫ ОБЯЗАТЕЛЬНОГО
МИНИМУМА
К ЭКЗАМЕНУ ПО
АТОМНОЙ И ЯДЕРНОЙ ФИЗИКЕ.
1.Опыты Резерфорда.
Планетарная модель атома.
2.Квантовые постулаты
Бора. Опыты Франка и Герца.
3.Модель атома
водорода по Бору.
4.Волновые свойства
микрочастиц. Волны де‑Бройля.
5.Орбитальный момент
импульса электрона и описание различных
состояний электрона в атоме.
6. Ферми‑ и
Бозе‑частицы. Принцип Паули.
7. Строение электронных
оболочек. Объяснение периодической
системы Д.И.Менделеева.
8. Физика молекулы.
Ковалентная и ионная связь.
9. Состав атомного
ядра. Изотопы и изобары. Энергия связи
атомного ядра.
10. Радиоактивный
распад ядер. Основной закон радиоактивного
распада.
11. Альфа‑распад
ядер.
12. Бета‑распад
ядер.
13. Гамма‑излучение
ядер.
14. Дозиметрические
единицы и защита от радиоактивных
излучений.
15. Ядерные реакции;
их классификация, способы записи и общие
закономерности.
16. Цепная реакция
деления тяжелых ядер под действием
нейтронов.
17. Ядерные реакторы
на медленных и на быстрых нейтронах.
18. Реакции термоядерного
синтеза. Проблема управляемого
термоядерного синтеза (УТС).
19. Элементарные
частицы и их свойства. Законы сохранения
в физике элементарных частиц.
20. Типы взаимодействий
и классификация элементарных частиц.
Античастицы. Виртуальные частицы.
МЕТОДИКА ПРОВЕДЕНИЯ
ЭКЗАМЕНА
ПО АТОМНОЙ И ЯДЕРНОЙ
ФИЗИКЕ.
Перечисленные выше
48 вопросов, выносимых на экзамен, разбиты
на 3 уровня: 0, 1 и 2. Вопросы нулевого
уровня (их 20) составляют обязательный
минимум, который должен знать каждый
студент; эти вопросы включены в основные
экзаменационные билеты. Вопросы уровней
1 и 2 (их по 14) не входят в обязательный
минимум и различаются тем, что
вопросы 2-го уровня либо являются более
сложными, либо не рассматриваются
подробно на лекциях, а предлагаются для
самостоятельного изучения. Для
получения на экзамене оценки
«удовлетворительно»
студент должен подготовить вопросы
уровня 0, для оценки «хорошо» — уровня
0 и 1, для оценки «отлично» — все
предлагаемые вопросы.
Весь курс делится
на две части: первая часть — атомная
физика, вторая часть — ядерная физика,
включающая несколько вопросов
из физики элементарных частиц.
Первая часть содержит 20 вопросов
(из них 8 уровня 0 и по 6 вопросов уровня
1 и 2), вторая — 28 вопросов (12 уровня 0 и по
8 вопросов уровня 1 и 2).
На экзамене студентам
предлагаются два пакета билетов: основные
и дополнительные. В каждый основной
билет входит два вопроса нулевого уровня
(один по атомной и один по ядерной
физике). В каждый дополнительный билет
входит один вопрос уровня 1 и один вопрос
уровня 2 (также из разных частей курса).
Все вопросы в билетах сформулированы
точно так же, как в приведенном
выше списке; других вопросов (кроме
списка) в билетах нет.
Если студент
претендует на хорошую или отличную
оценку, он тянет один основной и один
дополнительный билет. Для получения
отличной оценки он должен дать
правильные ответы на все вопросы в обоих
билетах, а для получения оценки
«хорошо» — на оба вопроса основного
билета и на один (любой) вопрос
дополнительного билета. Если студент
правильно ответил на оба вопроса
основного билета, но не смог дать
правильных ответов ни на один вопрос
дополнительного билета, он, по
своему желанию, либо соглашается с
оценкой «удовлетворительно»,
либо тянет еще один дополнительный
билет, и, если сумеет правильно
ответить на оба вопроса этого билета,
то получает оценку «хорошо»,
а в противном случае — оценку
«удовлетворительно».
Если студент во
время экзамена не может дать правильный
ответ хотя бы на один из вопросов нулевого
уровня, он получает неудовлетворительную
оценку независимо от ответов на
другие вопросы (поэтому начинать ответ
надо с вопросов основного билета, а
замена основного билета не разрешается).
С другой стороны, студент может
подготовить к экзамену только вопросы
нулевого уровня. В этом случае
он тянет только один основной билет и,
правильно ответив на оба вопроса
этого билета, получает оценку
«удовлетворительно».
В сомнительных
случаях (например, при пересдаче экзамена,
или если у студента было много
пропусков занятий) экзаменатор по своему
усмотрению может задать студенту
дополнительно (кроме билета) несколько
вопросов нулевого уровня (в той
формулировке, в какой они даны в списке),
чтобы убедиться в знании студентом
обязательного минимума.
Слайд 1
Подготовка к ГИА по физике Тема: Атомная физика Ефимова Г.И. МБОУ СОШ №8 г.Приморск
Слайд 2
2 1. Строение атома
Слайд 3
Строение атома. Опыт Резерфорда Из опытов Резерфорда непосредственно вытекает планетарная модель атома. В центре расположено положительно заряженное атомное ядро, в котором сосредоточена почти вся масса атома. В целом атом нейтрален. Поэтому число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической системе. Ядро обозначается тем же символом, что и нейтральный атом: A Z Х, где X — символ химического элемента, Z — атомный номер (число протонов в ядре), А — массовое число ( число нуклонов в ядре). Уравнение Иваненко — Гейзенберга А = Z + N А – массовое число Z – порядковый номер элемента N – число нейтронов в ядре
Слайд 4
2. Правила смещения При альфа — распаде ядро теряет положительный заряд 2 e и масса его убывает приблизительно на четыре атомных единицы массы. В результате элемент смещается на две клетки к началу периодической системы. X A Z = Y A-4 Z-2 + He 4 2 При бета — распаде из ядра вылетает электрон. В результате заряд ядра увеличивается на единицу, а масса остаётся почти неизменной. После бета-распада элемент смещается на одну клетку ближе к концу периодической системы. X A Z = Y A Z+1 + e 0 -1 ( Модель α — и β -распада. Воспроизводится по щелчку) Гамма-излучение происходит из-за перехода ядра в состояние с более низкой энергией с испусканием электромагнитного излучения. Гамма-излучение может происходить вслед за испусканием альфа- или бета-частицы после радиоактивного распада.
Слайд 5
3. Закон радиоактивного распада Период полураспада ( Т )- это то время, в течение которого распадается половина начального числа радиоактивных атомов. N=No · 2 -t/T N – число не распавшихся радиоактивных ядер No – число радиоактивных ядер в начальный момент времени t – время распада Т – период полураспада
Слайд 6
Энергетическим выходом ядерной реакции называется разность энергий покоя ядер и частиц до и после реакции. ΔE = Δm · с 2 Δm = ( m 1 + m 2 ) – ( m 3 + m 4 ) Данная энергия выражается в Джоулях, но в атомной физике ее принято выражать в МэВ. Для этого наша формула будет выглядеть следующим образом: ΔE = Δm · 9 31,5 МэВ / а . е . м . 4. Энергетический выход ядерной реакции
Слайд 7
1 . (Постулат стационарных состояний): Атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия E n . В стационарных состояниях атом не излучает. 2. (Правило частот): При переходе атома из одного стационарного состояния с энергией E n в другое стационарное состояние с энергией E m излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний: h ν nm = E n – E m 5 . Постулаты Бора
Слайд 8
Постулаты Бора объясняют закономерности в спектре атома водорода, происхождение характеристических спектров рентгеновских лучей и т. д. На рисунке показана часть энергетической диаграммы стационарных состояний атома водорода. Стрелками показаны переходы атома, приводящие к излучению энергии. 5 . Постулаты Бора
Слайд 9
Задание Какие утверждения соответствуют планетарной модели атома? 1) ядро — в центре атома, заряд ядра положителен, электроны на орбитах вокруг ядра 2) ядро — в центре атома, заряд отрицателен, электроны на орбитах вокруг ядра 3) электроны — в центре атома, ядро обращается вокруг электронов, заряд ядра положителен 4) электроны — в центре атома, ядро обращается вокруг электронов, заряд ядра отрицателен Тренировочные задания Решение. Согласно планетарной модели атома, в центре атома расположено положительно заряженное ядро, в котором сосредоточена почти вся масса атома, а электроны обращаются по орбитам вокруг ядра, подобно тому, как планеты обращаются вокруг Солнца. Верное утверждение 1. Правильный ответ: 1 .
Слайд 10
2. Задание На рисунке представлена диаграмма энергетических уровней атома. Какой из отмеченных стрелками переходов между энергетическими уровнями сопровождается поглощением кванта минимальной частоты? Тренировочные задания Решение. Квант энергии поглощается при переходе на более высокий уровень. При этом расстояние между уровнями пропорционально частоте ΔΕ= h ν . Из диаграммы видно, что среди предложенных вариантов ответа минимальному расстоянию между уровнями, а значит, и минимальной частоте поглощенного кванта соответствует переход с уровня 1 на уровень 2. Правильный ответ: 2 . 1) с уровня 1 на уровень 5 2) с уровня 1 на уровень 2 3) с уровня 5 на уровень 1 4) с уровня 2 на уровень 1
Слайд 11
3. Задание На рисунке изображены схемы четырех атомов. Электроны обозначены черными точками. Атому 4 7 Ве соответствует схема Тренировочные задания Решение. Число электронов в нейтральном атоме совпадает с числом протонов, которое записывается внизу перед наименованием элемента. В атоме четыре электрона, следовательно, этому элементу соответствует схема 3. Правильный ответ: 3. 1) 1 2) 2 3) 3 4) 4
Слайд 12
4. Задание На рисунке показаны энергетические уровни атома водорода. Переходу, показанному на рисунке стрелкой, соответствует Тренировочные задания Решение. Согласно постулатам Бора, при переходе атома в состояние с меньшей энергией происходит излучение фотона (кванта энергии). При этом энергия, уносимая фотоном, равна разности энергий начального и конечного уровней. Таким образом, переходу, показанному на рисунке, соответствует излучение атомом энергии – 1,5эВ – (– 13,6эВ) = 12,1эВ Правильный ответ: 4. 1) поглощение атомом энергии 1,5 эВ 2) излучение атомом энергии 13,6 эВ 3) поглощение атомом энергии 12,1 эВ 4) излучение атомом энергии 12,1 эВ
Слайд 13
5. Задание Опыты Резерфорда по рассеянию α-частиц показали, что А. масса атома близка к массе всех электронов. Б. размеры атома близки к размерам атомного ядра. Какое(- ие ) из утверждений правильно(- ы )? 1) только А 2) только Б 3) и А, и Б 4) ни А, ни Б Тренировочные задания Решение. Опыты Резерфорда по рассеянию α-частиц показали, что практически вся масса атома сосредоточена в его ядре, при этом размеры ядер во много раз меньше размеров атома (по сути, атом состоит из пустоты). Поэтому оба утверждения не верны. Правильный ответ: 4.
Слайд 14
Задание Согласно одному из квантовых постулатов Н. Бора 1) излучение или поглощение энергии атомом происходит непрерывно 2) атом излучает или поглощает энергию только тогда, когда электроны находятся в стационарных состояниях 3) при переходе электрона с орбиты на орбиту излучается или поглощается квант энергии, равный энергии электрона в данном стационарном состоянии 4) при переходе электрона с орбиты на орбиту излучается или поглощается квант энергии, равный разности энергий электрона в стационарных состояниях Тренировочные задания Решение. Согласно постулатам Бора атом может находиться только в определённых квантовых состояниях, называемых стационарными, в которых он не излучает. Излучение или поглощение в виде кванта энергии происходит только при переходе атома из одного состояния в другое состояние, т. е. при переходе электрона с орбиты на орбиту, причём квант энергии равен разности энергий электрона в стационарных состояниях. Правильный ответ: 4.
Слайд 15
7. Задание На рисунке изображена диаграмма энергетических уровней атома. Какой цифрой обозначен переход, который соответствует излучению фотона с наименьшей длиной волны? Тренировочные задания Решение. Квант энергии излучается при переходе с высокого на более низкий уровень. При этом расстояние между уровнями пропорционально частоте: ΔΕ= h ν= h с/ λ . Из диаграммы видно, что среди предложенных вариантов ответа максимальному расстоянию между уровнями, а значит, и минимальной длине волны излученного кванта соответствует переход с уровня 4 на уровень 1. Правильный ответ: 3. 1) 1 2) 2 3) 3 4) 4
Слайд 16
8. Задание Связанная система элементарных частиц содержит 9 электронов, 13 нейтронов и 8 протонов. Эта система может являться 1) нейтральным атомом хлора 2) ионом кислорода 3) ионом фтора 4) нейтральным атомом кислорода Тренировочные задания Решение. Ядро данной системы будет обладать массовым числом 21 и зарядовым числом 8. Электронов больше чем протонов, а значит заряд системы не нейтрален. Таким образом искомый элемент — ион кислорода Правильный ответ: 2.
Слайд 17
9. Задание В ядре 8 17 О содержится 1) 17 протонов и 8 нейтронов 2) 8 протонов и 17 нейтронов 3) 8 протонов и 9 нейтронов 4) 9 протонов и 8 нейтронов Тренировочные задания Решение. Зарядовое число, то есть число протонов в ядре, записывается внизу перед наименованием элемента. Число вверху обозначает массовое число, то есть суммарное число протонов и нейтронов. Таким образом, атом кислорода содержит 8 протонов и 9 нейтронов. Правильный ответ: 3.
Слайд 18
10. Задание На рисунке схематически изображены спектральные линии 1, 2, 3 и 4 атома водорода, принадлежащие видимой области спектра. В верхней части рисунка приведены деления шкалы длин волн, проградуированной в нанометрах. Укажите номер спектральной линии, которой соответствует частота света, лежащая в диапазоне от 4·10 14 Гц до 5·10 14 Гц. Тренировочные задания Решение. Частота и длина волны связаны соотношением ν= c/ λ : Следовательно, частоте 4·10 14 Гц соответствует длина волны А частоте 5·10 14 Гц соответствует длина волны Из рисунка видно, что спектральная линия 4 лежит в требуемом диапазоне длин волн. Правильный ответ: 4.
Слайд 19
11. Задание Ядра A , B , C и D отличаются массовыми и зарядовыми числами так, как показано ниже: Изотопами являются ядра А и В А и С С и D С и В Тренировочные задания Решение. Изотопы — это ядра с одинаковым зарядовым числом и различной массой, следовательно, изотопами являются ядра A и С . Правильный ответ: 2 .
Слайд 20
1 2 . Задание На рисунке представлен фрагмент Периодической системы элементов Д.И. Менделеева. Под названием элемента приведены массовые числа его основных стабильных изотопов, нижний индекс около массового числа указывает (в процентах) распространённость изотопа в природе. Тренировочные задания Решение. Самый распространенный изотоп меди — это медь с массовым числом 63, который распространен в природе на 69%. Порядковый номер меди — 29, это значит, что в ядре у нее 29 протонов. Массовое число есть сумма нейтронов и протонов. Таким образом, число нейтронов равно 63-29=34. Правильный ответ: 2 . Число протонов и число нейтронов в ядре самого распространённого изотопа меди равно 1) 36 протонов, 29 нейтронов 2) 29 протонов, 34 нейтрона 3) 31 протон, 33 нейтрона 4) 29 протонов, 63 нейтрона
Слайд 21
Тренировочные задания 13. Задание Ядро изотопа тория претерпевает α -распад, затем два электронных β -распада и еще один α -распад. После этих превращений получится ядро 1) франция 2) радона 3) полония 4) радия Решение. Ядро изотопа тория имеет 90 протонов. При α -распаде оно испускает α -частицу (ядро атома гелия), имеющую заряд +2(в единицах заряда протона). Согласно закону сохранения электрического заряда, получившееся ядро имеет на два протона меньше, чем исходный торий. Далее, при β -распаде один из нейтронов в ядре превращается в протон, испуская электрон. Поскольку ядро испытало 2 β -распада, образовавшееся ядро имеет опять столько же протонов, как и исходный торий. Наконец, после еще одного α -распада число протонов вновь уменьшается на два. Таким образом, получившееся ядро имеет 88 протонов, а значит, это радий Данный ответ можно также проверить проследив за изменением массового числа: после α -распада232→228 после двух β -распадов →228 после α -распада→224 . Правильный ответ: 4.
Слайд 22
Тренировочные задания 14. Задание Сколько процентов ядер некоторого радиоактивного элемента останется через время, равное трем периодам полураспада этого элемента? 1) 12,5% 2) 0,125% 3) 33,3% 4) 80% Решение. Согласно закону радиоактивного распада, от первоначального количества радиоактивных ядер к моменту времени t должно остаться примерно , где T — период полураспада. Следовательно, к моменту времени, равному трем периодам полураспада, ядер останется приблизительно Правильный ответ: 1.
Слайд 23
Тренировочные задания 15. Задание На рисунке схематически изображён трек частицы в камере Вильсона, помещённой во внешнее магнитное поле В. Данный трек может принадлежать 1) электрону 2) ά -частице 3) нейтрону 4) Позитрону Решение. На заряженные частицы в камере Вильсона действует сила Лоренца, сообщающая им центростремительное ускорение. Направление силы Лоренца определяется правилом левой руки: «Если левую руку расположить так, чтобы линии индукции магнитного поля входили в ладонь перпендикулярно ей, а четыре пальца были направлены по току (по движению положительно заряженной частицы или против движения отрицательно заряженной), то отставленный большой палец покажет направление действующей силы Лоренца». Мысленно проделав указанные действия, получаем, что трек соответствует отрицательно заряженной частице. Таким образом, трек может принадлежать электрону. Правильный ответ: 1.
Слайд 24
Тренировочные задания 16. Задание На основании приведённой ниже таблицы можно сделать вывод, что при протекании ядерной реакции + → + 1) выделяется энергия, равная ≈ 1,63 МэВ 2) выделяется энергия, равная ≈ 15,8 МэВ 3) поглощается энергия, равная ≈ 1,63 МэВ 4) поглощается энергия, равная ≈ 15,8 МДж Решение. В результате этой реакции возникает дефект масс, равный 7,01601 + 1,00783 − 7,01693 — 1,00866 = −0,00175 а.е.м . Согласно уравнению Эйнштейна этому дефекту масс соответствует энергия примерно равная 1,63 МэВ. Знак «−» означает, что произошло увеличение массы вещества, то есть масса вещества до реакции меньше массы вещества после реакции. Для образования дополнительной массы энергия должна поглощаться. Следовательно, в этой реакции поглощается энергия равная 1,63 МэВ. Правильный ответ указан под номером: 3.
Слайд 25
Спасибо за внимание! удачи на ЕГЭ!!!
Слайд 26
https://oge.sdamgia.ru/test?theme=61 Источники: