Чтобы поделиться, нажимайте
Получение карбоновых кислот
I. В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов:
2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O
метан муравьиная кислота
2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O
н-бутан уксусная кислота
3. Окисление алкенов:
CH2=CH2 + O2 t,kat → CH3COOH
этилен
СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота)
4. Окисление гомологов бензола (получение бензойной кислоты):
C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O
5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O
толуол бензойная кислота
5. Получение муравьиной кислоты:
1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль)
2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4
6. Получение уксусной кислоты:
CH3OH + CO t,p → CH3COOH
Метанол
II. В лаборатории
1. Гидролиз сложных эфиров:
2. Из солей карбоновых кислот:
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде:
(R-CO)2O + H2O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:
III. Общие способы получения карбоновых кислот
1. Окисление альдегидов:
R-COH + [O] → R-COOH
Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II) – качественные реакции альдегидов
2. Окисление спиртов:
R-CH2-OH + 2[O] t,kat → R-COOH + H2O
3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода.
4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь:
СH3-Br + Na-C≡N → CH3-CN + NaBr
CH3—CN — метилцианид ( нитрил уксусной кислоты)
СH3-CN + 2H2O t → CH3COONH4
ацетат аммония
CH3COONH4 + HCl → CH3COOH + NH4Cl
5. Использование реактива Гриньяра
R-MgBr + CO2 → R-COO-MgBr H2O → R-COOH + Mg(OH)Br
ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ
Муравьиная кислота – в медицине — муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество.
Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов.
Щавелевая кислота – в металлургической промышленности (удаление окалины).
Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.
Олеиновая кислота C17H33COOH – флотореагент и собиратель при обогащении руд цветных металлов.
Бензойная кислота относится к органическим кислотам. Впервые была 
Бензойная кислота C6H5COOH в нормальных условиях представляет собой бесцветные игольчатые кристаллы, очень тонкие, блестящие. Вещество отличается характерным запахом, хорошей растворимостью в жирах, этиловом спирте, эфире, крайне низкой растворимостью в воде. При нагревании порошок бензойной кислоты возгоняется.
Химические свойства соответствуют свойствам слабой органической кислоты.
Бензойная кислота — эффективное противогрибковое средство, убивает плесень, дрожжи, активна против многих видов бактерий и паразитов. Для человека не токсична, хотя при попадании в дыхательные пути в аэрозольной форме может вызвать сильный кашель и даже рвоту. Вызывает раздражение при попадании на кожу.
Бензойная кислота токсична для семейства кошачьих даже в малых дозах.
Получение
Бензойная кислота и ее эфиры входят в состав природных веществ (эфирные масла гвоздики, туберозы, иланг-иланга; бензойная смола; ягоды брусники, клюквы; образуется в простокваше и йогурте), продуктов жизнедеятельности некоторых травоядных животных. Для нужд промышленности ее получают искусственным путем — синтезируют из других химических реактивов.
Применение бензойной кислоты
— В пищевой и косметической индустрии в качестве консерванта. Бензойная кислота и ее соли, бензоаты натрия, калия и кальция — это пищевые добавки Е210-Е213, обладающие выраженной противогрибковой активностью и антибактериальными свойствами. Используются при консервировании мясных, рыбных, фруктовых и ягодных продуктов, газированных, алкогольных и безалкогольных напитков, мармелада, майонеза, кетчупа, маргарина, мороженого, жевательной резинки. При производстве бальзамов, кремов, шампуней, губной помады.
— В фармакологии добавляется в средства против кашля, в дерматологические кожные мази против чесотки и грибковых заболеваний.
— В химической промышленности реактив используется как сырье для производства большого класса соединений — производных бензойной кислоты: эфиров, фенола, капролактама (сырья для искусственных тканей класса нейлона), пластификаторов, бензоилхлорида.
— Улучшает блеск алкидных лаков, их сцепление с поверхностью, прочность покрытия.
— Для калибровки калориметров.
Широко применяются также производные бензойной кислоты:
— Бензоат натрия хорошо растворяется в воде, поэтому он чаще всего используется в качестве пищевых добавок. Также это средство против коррозии; отхаркивающее средство; стабилизатор в процессах полимеризации.
— Бензоаты натрия, калия и кальция — пищевые добавки, консерванты, антисептики.
— Аммониевую соль добавляют как консервант в пищевые продукты; в средства против коррозии; как стабилизатор в клеи и латексы.
— Метиловый, этиловый, изоамиловый, бензиловый эфиры применяются при изготовлении парфюмерных композиций.
— Изоамиловый эфир входит в состав фруктовых эссенций.
— Метиловый эфир используется как растворитель эфиров целлюлозы.
— Бензиловый эфир применяется в бытовой химии в средствах от моли; в противовоспалительных препаратах; для фиксации запахов в парфюмерных отдушках; для растворения ароматических веществ.
— Хлорбензойная и нитробензойная кислоты используются в производстве красителей.
Среди химических реактивов, купить которые можно в Москве и области с доставкой из магазина «ПраймКемикалсГрупп» есть как бензойная кислота, так и натрий бензойнокислый, а также широкий спектр других хим. реактивов и веществ, лабораторной техники и посуды. Ассортимент и цены, как правило, радуют покупателей.
Получение и применение карбоновых кислот. Краткие сведения о непредельных карбоновых кислотах
I. Получение карбоновых кислот
1. В промышленности
- Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
- Окисление алканов
2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O
метан муравьиная кислота
2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O
н-бутан уксусная кислота
- Окисление алкенов
CH2=CH2 + O2 t,kat → CH3COOH
этилен
СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота)
5СHR=CHR + 8KMnO4 + 12H2SO4 → 10RCOOH + 8MnSO4 + 4K2SO4 + 12H2O
Слева – раствор перманганата калия, справа – результат его взаимодействия с алкеном.
Рис. 1. Окисление непредельных углеводородов
- Окисление гомологов бензола (получение бензойной кислоты)
C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O
5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O
толуол бензойная кислота
5С6Н5-СН2-СН3 + 8KMnO4 + 12H2SO4 → 5С6Н5COOH + 5СО2 + 8MnSO4 + 4K2SO4 + 22H2O
- Получение муравьиной кислоты
1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль)
2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4
- Получение уксусной кислоты
- CH3OH + CO t,p → CH3COOH
Метанол
- Ферментативное окисление водных растворов этилового спирта:
CH3CH2OH + O2
- Каталитическое окисление бутана кислородом воздуха (в промышленности) (Рис. 2):
Рис. 2. Центральный пульт управления цеха уксусной кислоты (Источник)
2CH3–CH2–CH2–CH3 + 5O2
2. В лаборатории
- Гидролиз сложных эфиров
- Из солей карбоновых кислот
R-COONa + HCl → R-COOH + NaCl
- Растворением ангидридов карбоновых кислот в воде
(R-CO)2O + H2O → 2 R-COOH
- Щелочной гидролиз галоген производных карбоновых кислот
3. Общие способы получения карбоновых кислот
- Окисление альдегидов
R-COH + [O] → R-COOH
Например, реакция «серебряного зеркала» или окисление гидроксидом меди (II) – качественные реакции альдегидов.
R-CHO + Ag2O → R-COOH + 2Ag¯
R-CHO + 2Cu(OH)2→ R-COOH + Cu2O¯ + 2H2O
Рис. 3. Окисление альдегидов
- Окисление спиртов
R-CH2-OH + 2[O] t,kat → R-COOH + H2O
3С2Н5ОН + 2K2Cr2O7 + 8H2SO4 → 3СН3СООН + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
Слева – раствор дихромата калия, справа – результат его взаимодействия с этиловым спиртом.
Рис. 4. Окисление спиртов
- Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода
- Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь
СH3-Br + Na-C≡N → CH3-CN + NaBr
CH3-CN — метилцианид ( нитрил уксусной кислоты)
СH3-CN + 2H2O t → CH3COONH4
ацетат аммония
CH3COONH4 + HCl → CH3COOH + NH4Cl
- Использование реактива Гриньяра
R-MgBr + CO2 → R-COO-MgBr H2O → R-COOH + Mg(OH)Br
II. Применение карбоновых кислот
- Муравьиная кислота – в медицине — муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество.
- Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов.
- Щавелевая кислота – в металлургической промышленности (удаление окалины).
- Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке.
- Олеиновая кислота C17H33COOH – флотореагент и собиратель при обогащении руд цветных металлов.
III. Отдельные представители одноосновных предельных карбоновых кислот
- Муравьиная кислота впервые была выделена в XVII веке из красных лесных муравьев. Содержится также в соке жгучей крапивы. Безводная муравьиная кислота – бесцветная жидкость с острым запахом и жгучим вкусом, вызывающая ожоги на коже. Применяется в текстильной промышленности в качестве протравы при крашении тканей, для дубления кож, а также для различных синтезов.
- Уксусная кислота широко распространена в природе – содержится в выделениях животных (моче, желчи, испражнениях), в растениях (в зеленых листьях). Образуется при брожении, гниении, скисании вина, пива, содержится в кислом молоке и сыре. Температура плавления безводной уксусной кислоты + 16,5°C, кристаллы ее прозрачны как лед, поэтому ее называют ледяной уксусной кислотой. Впервые получена в конце XVIII века русским ученым Т. Е. Ловицем. Натуральный уксус содержит около 5% уксусной кислоты. Из него приготовляют уксусную эссенцию, используемую в пищевой промышленности для консервирования овощей, грибов, рыбы. Уксусная кислота широко используется в химической промышленности для различных синтезов.
IV. Представители ароматических и непредельных карбоновых кислот
- Бензойная кислота C6H5COOH — наиболее важный представитель ароматических кислот. Распространена в природе в растительном мире: в бальзамах, ладане, эфирных маслах. В животных организмах она содержится в продуктах распада белковых веществ. Это кристаллическое вещество, температура плавления 122°C, легко возгоняется. В холодной воде растворяется плохо. Хорошо растворяется в спирте и эфире.
- Ненасыщенные непредельные кислоты с одной двойной связью в молекуле имеют общую формулу CnH2n-1COOH.
- Высокомолекулярные непредельные кислоты часто упоминаются диетологами (они называют их ненасыщенными). Самая распространенная из них – олеиновая СН3–(СН2)7–СН=СН–(СН2)7–СООН или C17H33COOH. Она представляет собой бесцветную жидкость, затвердевающую на холоде.
- Особенно важны полиненасыщенные кислоты с несколькими двойными связями: линолевая СН3–(СН2)4–(СН=СН–СН2)2–(СН2)6–СООН или C17H31COOH с двумя двойными связями, линоленовая СН3–СН2–(СН=СН–СН2)3–(СН2)6–СООН илиC17H29COOH с тремя двойными связями и арахидоновая СН3–(СН2)4–(СН=СН–СН2)4–(СН2)2–СООН с четырьмя двойными связями; их часто называют незаменимыми жирными кислотами. Именно эти кислоты обладают наибольшей биологической активностью: они участвуют в переносе и обмене холестерина, синтезе простагландинов и других жизненно важных веществ, поддерживают структуру клеточных мембран, необходимы для работы зрительного аппарата и нервной системы, влияют на иммунитет. Отсутствие в пище этих кислот тормозит рост животных, угнетает их репродуктивную функцию, вызывает различные заболевания. Линолевую и линоленовую кислоты организм человека сам синтезировать не может и должен получать их готовыми с пищей (как витамины). Для синтеза же арахидоновой кислоты в организме необходима линолевая кислота. Полиненасыщенные жирные кислоты с 18 атомами углерода в виде эфиров глицерина находятся в так называемых высыхающих маслах – льняном, конопляном, маковом и др.Линолевая кислота C17H31COOH и линоленовая кислота C17H29COOH входят в состав растительных масел. Например, льняное масло содержит около 25% линолевой кислоты и до 58% линоленовой.
- Сорбиновая (2,4-гексадиеновая) кислота СН3–СН=СН–СН=СНСООН была получена из ягод рябины (на латыни – sorbus). Эта кислота – прекрасный консервант, поэтому ягоды рябины не плесневеют.
- Простейшая непредельная кислота, акриловая СН2=СНСООН, имеет острый запах (на латыни acris – острый, едкий). Акрилаты (эфиры акриловой кислоты) используются для получения органического стекла, а ее нитрил (акрилонитрил) – для изготовления синтетических волокон.
- Называя вновь выделенные кислоты, химики, нередко, дают волю фантазии. Так, название ближайшего гомолога акриловой кислоты, кротоновой СН3–СН=СН–СООН, происходит вовсе не от крота, а от растения Croton tiglium, из масла которого она была выделена. Очень важен синтетический изомер кротоновой кислоты –метакриловая кислота СН2=С(СН3)–СООН, из эфира которой (метилметакрилата), как и из метилакрилата, делают прозрачную пластмассу – оргстекло.
- Непредельные карбоновые кислоты способны к реакциям присоединения:
СН2=СН-СООН + Н2 → СН3-СН2-СООН
СН2=СН-СООН + Сl2 → СН2Сl-СНСl-СООН
Видео-опыт:“Взаимодействие бромной воды с олеиновой кислотой”
СН2=СН-СООН + HCl → СН2Сl-СН2-СООН
СН2=СН-СООН + Н2O → НО-СН2-СН2-СООН
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации.
V. Тренажеры
Тренажер №1: “Получение карбоновых кислот”
Тренажер №2:“Химические свойства предельных одноосновных карбоновых кислот”
Тестовые задания по теме «Карбоновые кислоты»
ЦОРы
Видео-опыт: “Взаимодействие бромной воды с олеиновой кислотой”
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Насыщенные кислоты
Предельные одноосновные
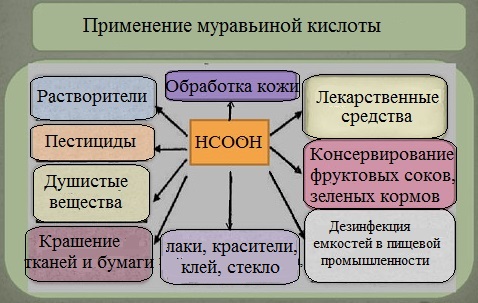
Благодаря своему уникальному молекулярному составу муравьиная кислота обладает антибактериальными свойствами, поэтому основная сфера ее применения – это пищевая промышленность (пищевая добавка E 236). В пищевой промышленности она используется в качестве дезинфицирующего и консервирующего средства при производстве кондитерских изделий, консервированных и молочных продуктов, безалкогольных напитков. Помимо этого, муравьиная кислота применяется для дезинфекции пивных и винных бочек.
Она применяется в химической промышленности в качестве восстановителя при синтезе органических веществ, при получении щавелевой кислоты. А также, при изготовлении стекла, промышленного клея, промышленных лаков и химических красителей.
Сложные эфиры муравьиной кислоты используют в качестве растворителей и душистых веществ.
В текстильной промышленности ее используют в качестве протравы при крашении тканей, в кожевенном производстве – для отмывания извести, используемой при обработке шкур.
Муравьиная кислота обладает болеутоляющим, бактерицидным, противовоспалительным, согревающим действием и благодаря этим свойствам находит широкое применение в медицине. Ее используют в медицине в качестве наружного обезболивающего средства. Смесь кислоты с водой, так называемый муравьиный спирт, используется как раздражающее кожу, рефлекторно действующее средство при ревматических и неврологических болях.
Муравьиная кислота входит в состав не только лечебных, но и косметических препаратов.
Кроме того ее применяют в сельском хозяйстве при заготовке различных кормов. Муравьиной кислотой обрабатывают сено, силос, что помогает замедлить процессы гниение и распада, благодаря чему корма способны храниться намного дольше.
Муравьиная кислота также используется для борьбы с паразитами в пчеловодстве.
Из всех карбоновых кислот уксусная кислота находит наиболее широкое применение. Она необходима для синтеза красителей для тканей, лекарственных веществ, сложных эфиров, растворителей лаков. Большое ее количество расходуются для производства искусственного волокна (ацетатного шелка), пластических масс, невоспламеняющейся кинопленки, органического стекла, ядохимикатов, стимуляторов роста растений.
В пищевой промышленности (пищевая добавка Е 260) уксусную кислоту применяют для консервирования овощей, грибов, рыбы и в качестве приправы к пище. Консервирующее действие кислоты связано с подавлением развития гнилостных бактерий и плесневых грибков.
Солями уксусной кислоты (Al, Fe, Cr) протравливают ткани при крашении, они способствуют закреплению красителей на волокне.
Ацетат свинца применяется для изготовления свинцовых белил и свинцовой примочки в медицине.
Соли уксусной кислоты используются также в сельском хозяйстве. В результате применения 2,4-дихлорфеноксиуксусной кислоты и ее солей на полях с зерновыми погибают только широколиственные сорняки, что используется при выращивании зерновых культур.
Уксусный ангидрид применяется в производстве пластических масс, искусственного шелка, ацетанилида.
Из монохлоруксусной кислоты получают негорючую кинопленку, органическое стекло, пропускающее ультрафиолетовые лучи.
Применение уксусной кислоты

Масляная кислота применяется для лечения некоторых заболеваний желудочно-кишечного тракта. В процессе ферментативных реакций кислота и ее соли создают в кишечнике кислую среду, благоприятную для развития полезных бактерий и подавляющую развитие патогенных, таких как возбудитель сальмонеллы и кишечная палочка. Кроме этого, масляная кислота способствует регуляции водно-электролитного баланса в кишечнике, регулирует его моторику.
Соли масляной кислоты используются в животноводстве, птицеводстве и рыбоводстве как кормовые добавки. Эти добавки усиливают иммунитет, способствуют лучшей усвояемости пищи, подавляют деятельность многих вредных кишечных бактерий, уменьшают необходимость применения антибиотиков.
Также она используется для изготовления лакокрасочных материалов, пластификаторов для лаков, эмульгаторов.
Применяется в парфюмерной и кондитерской промышленностях в виде сложных эфиров, являющихся ценными ароматическими веществами.
Стеариновая и пальмитиновая кислота входят в состав животных жиров и растительных масел. Натриевые и калиевые соли этих кислот входят в состав мыла.
Стеариновая кислота часто используется при изготовлении косметических средств, в качестве стабилизатора смеси и эмульгатора. Она делает состав непрозрачным и густым. Косметические средства, содержащие активные вещества стеарина быстро впитываются в сухую кожу и оказывают на нее благотворное влияние.
При производстве мыла часто используется соль стеариновой кислоты, поскольку она обладает хорошим моющим свойством и применяется в роли загустителя. Стеариновая кислота в мыле постепенно затвердевает.
Другое применение активных веществ стеарина – это возможность создания на их основе пластичных масок и наполнителей резиновых смесей. Эти компоненты помогают сделать резину более пластичной и однородной.
Пальмитиновая кислота используется в качестве одного из основных компонентов для приготовления напалма, различных моющих и косметических средств, а также при производстве стеарина (смесь со стеариновой кислотой).
Пальмитиновая кислота используется в производстве технических масел для смазки, для изготовления пластификаторов и свечей.
Пальмитат натрия находит свое применение в производстве хозяйственного и туалетного мыла, где он выполняет роль загустителя.
Соли пальмитиновой кислоты нашли применение в производстве косметических препаратов в качестве эмульгатора.
Метилпальминат (метиловый эфир пальмитиновой кислоты) используется для ароматизации некоторых пищевых продуктов.
Предельные двухосновные
Щавелевая кислота благодаря своим уникальным свойствам применяется во многих отраслях промышленности.
В химической промышленности щавелевая кислота используется при синтезе красителей, при производстве чернил, пластмасс, пиротехники.
Также она используется как дезинфицирующее и отбеливающее средство в составе синтетических моющих средств. В бытовой химии ее применяют в качестве одного из основных компонентов чистящих и моющих средств для раковин, унитазов.
В металлургической промышленности щавелевая кислота используется в виде специального состава при очистке металлов, котлов от коррозии, накипи, ржавчины, оксидов.
В кожевенной и текстильной промышленности она находит применение в качестве потравы при окраске шелка и шерсти, для дубления кожи. Это обработка поверхности необходима для того, чтобы краситель лег на материю равномерно.
Широко применяется щавелевая кислота для уменьшения жесткости воды и очистка ее от примесей.
В косметологии она применяется как отбеливающий компонент в кремах от пигментных пятен, веснушек.
В сельском хозяйстве ее используют как инсектицид, особенно она востребована у пчеловодов для обработки пчел.
В настоящее время щавелевая кислота широко применяется в пищевой промышленности для производства пищевых добавок.
Малоновая (пропандиовая, метандикарбоновая кислота) кислота используется при производстве непредельных кислот, флавонов, аминокислот, витаминов В1 и В6.
Янтарная кислота нашла свое применение в медицинской промышленности для производства лекарственных препаратов, в косметологии, аналитической химии и химической промышленности — в производстве пластмасс и смол, в птицеводстве и животноводстве — как средство, снижающее заболеваемость, в сельском хозяйстве = как средство, повышающее урожайность растений и их устойчивость к неблагоприятным внешним факторам.
Она способна стимулировать адаптационные и защитные функции организма, повышать диастолическое артериальное давление и секреторную функцию желез желудка, улучшать аппетит, повышать физическую работоспособность, нейтрализует образующиеся свободные радикалы.
Янтарная кислота участвует в обменных процессах, протекающих в организме. Она необходима для обеспечения клеточного дыхания, синтеза белков, выработки внутриклеточной энергии. Кроме того янтарная кислота способствует выведению из организма отравляющих веществ и уменьшает токсическое действие алкоголя.
В аналитической химии с помощью щавелевой кислоты осаждают редкоземельные металлы.
Ненасыщенные кислоты
Акриловая кислота и её производные используются при производстве акриловых эмульсий для лакокрасочных материалов, пропитки тканей и кожи, в качестве сырья для полиакрилонитрильных волокон и акриловых каучуков, строительных смесей и клеев.
В производстве полимеров широко применяют сложные эфиры акриловой и метакриловой кислот. Например, полиакрилонитрил – основа волокна нитрон, используемого для производства лечебного белья.
Жирные ненасыщенные кислоты
Олеиновая кислота применяется как флотореагент и собиратель при обогащении руд цветных металлов.
Олеиновая кислота и ее эфиры применяют как пластификаторы для изготовления лакокрасочных материалов.
В пищевой промышленности она применяется при производстве ароматизаторов.
Также олеиновая кислота широко применяется в качестве смазывающе-охлаждающих жидкостей при сверлении и обработке труднообрабатываемых нержавеющих сталей и сплавов. Выступает эмульгатором в резинотехнической промышленности.
Олеиновая кислота применяется при изготовлении хозяйственного мыла, моющих средств.
Небольшие количества олеиновой кислоты используют в качестве наполнителя в фармацевтических препаратов.
Особенно нужно подчеркнуть роль линолевой и линоленовой кислот как соединений, незаменимых для человека (в организме они не могут быть синтезированы и должны поступать с пищей около 5 гр в день). По этой причине эти кислоты относят к так называемым незаменимым жирным кислотам. Линолевая и линоленовая кислоты содержатся в основном в растительных маслах.
Линолевая кислота регулирует жировой и белковый обмен, предотвращает накопление холестерина в сосудах, препятствует возникновению тромбов, защищает клетки от преждевременного старения, улучшает функции нервной системы, повышает усвояемость жирорастворимых витаминов и витаминов группы В. Она нормализует, а также ускоряет обменные процессы в организме, повышает иммунитет.
Линоленовая кислота регулирует артериальное давление, предупреждает инфаркт миокарда. Снижает уровень холестерина в крови, предотвращая развитие атеросклероза. Обладает противовоспалительными свойствами и применяется для лечения кожных заболеваний.
Линоленовая кислота улучшает усвоение жирорастворимых витаминов (D, А, Е, К). Витамин Е является важным элементом в питании беременной женщины, так как он снижает вероятность отслойки плаценты.
Она способствует сохранению влаги в коже и волосах, поэтому ее применяют для ухода за сухой кожей.
Ароматические кислоты
Бензойная кислота
Эфиры бензойной кислоты, обладающие сильным запахом, применяют в парфюмерной промышленности. Различные производные бензойной кислоты (нитро- и хлорбензойная кислота) широко применяют для синтеза красителей (например, анилинового синего).
Также ее используют в качестве консерванта для пищевых продуктов. Она проявляет антимикробное и антигрибковое действие, оказывает угнетающее воздействие на плесень, дрожжи и некоторые виды бактерий.
Бензойную кислоту применяют в медицине при кожных заболеваниях как наружное антисептическое (противомикробное) и фунгицидное (противогрибковое) средства, натриевую соль бензойной кислоты добавляют в сиропы от кашля, поскольку она обладает отхаркивающим свойством и разжижает мокроту. Оно прекрасно борется с потливостью ног.
Карбоновые кислоты
КАРБОНОВЫЕ КИСЛОТЫ.
Карбоновыми кислотами называются производные углеводородов, в молекуле которых содержится одна или несколько карбоксильных групп
Общая формула предельных одноосновных карбоновых кислот: СnH2nO2
КЛАССИФИКАЦИЯ КАРБОНОВЫХ КИСЛОТ.
1. По числу карбоксильных групп:
— одноосновные (монокарбоновые)
— многоосновные (дикарбоновые, трикарбоновые и т.д.).
- По характеру углеводородного радикала:
— предельные CH3-CH2-CH2-COOH; бутановая кислота.
— непредельные CH2=CH-CH2-COOH; бутен-3-овая кислота.
— ароматические
пара-метилбензойная кислота
НАЗВАНИЯ КАРБОНОВЫХ КИСЛОТ.
|
Название |
Формула кислоты |
||
|
кислоты |
её соли и (эфиры) |
||
|
муравьиная |
метановая |
формиат |
HCOOH |
|
уксусная |
этановая |
ацетат |
CH3COOH |
|
пропионовая |
пропановая |
пропионат |
CH3CH2COOH |
|
масляная |
бутановая |
бутират |
CH3(CH2)2COOH |
|
валериановая |
пентановая |
валерат |
CH3(CH2)3COOH |
|
капроновая |
гексановая |
гексанат |
CH3(CH2)4COOH |
|
пальмитиновая |
гексадекановая |
пальмитат |
С15Н31СООН |
|
стеариновая |
октадекановая |
стеарат |
С17Н35СООН |
|
акриловая |
пропеновая |
акрилат |
CH2=CH–COOH |
|
олеиновая |
цис-9-октадеценовая |
олеат |
СН3(СН2)7СН=СН(СН2)7СООН |
|
бензойная |
бензойная |
бензоат |
C6H5 -COOH |
|
щавелевая |
этандиовая |
оксалат |
НООС — COOH |
ИЗОМЕРИЯ КАРБОНОВЫХ КИСЛОТ.
1. Изомерия углеродной цепи. Начинается с бутановой кислоты (С3Н7СООН), которая существует в виде двух изомеров: масляной (бутановой) и изомасляной (2-метилпропановой) кислот.
2. Изомерия положения кратной связи в непредельных кислотах, например:
СН2=СН—СН2—СООН СН3—СН=СН—СООН
Бутен-3-овая кислота Бутен-2-овая кислота
(винилуксусная кислота) (кротоновая кислота)
3. Цис-, транс-изомерия в непредельных кислотах, например:
4. Межклассовая изомерия: Карбоновые кислоты изомерны сложным эфирам:
Уксусная кислота СН3-СООН и метилформиат Н-СООСН3
5. Изомерия положения функциональных групп у гетерофункционалъных кислот.
Например, существуют три изомера хлормасляной кислоты: 2-хлорбутановая, 3-хлорбутановая и 4-хлорбутановая.
СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ.
Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризацией связи О–Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей. С увеличением молекулярной массы растворимость кислот в воде уменьшается.
ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ – в них гидроксогруппа замещена на некоторые другие группы. Все они при гидролизе образуют карбоновые кислоты.
|
Соли |
Сложные эфиры |
Галогенангидриды |
Ангидриды |
Амиды. |
|
|
|
|
|
|
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ.
|
1. Окисление спиртов в жестких условиях – раствором перманганата или дихромата калия в кислой среде при нагревании. |
|
|
2.Окисление альдегидов: раствором перманганата или дихромата калия в кислой среде при нагревании, реакцией серебряного зеркала, гидроксидом меди при нагревании. |
|
|
3. Щелочной гидролиз трихлоридов: |
R-CCl3 + 3NaOH 🡪 [R-C(OH)3] + 3NaCl неустойчивое вещество [R-C(OH)3] 🡪 RCOOH + H2O |
|
4. Гидролиз сложных эфиров. |
R-COOR1 + KOH 🡪 RCOOK + R1OH RCOOK + HCl 🡪 R-COOH + KCl |
|
5. Гидролиз нитрилов, ангидридов, солей. |
1)нитрил: R-CN + 2H2O –(H+)🡪 RCOOH 2)ангидрид: (R-COO)2O + H2O 🡪 2RCOOH 3)натриевая соль: R-COONa+HCl🡪R-COOH + NaCl |
|
6. Взаимодействие реактива Гриньяра с СО2: |
R-MgBr + CO2 🡪 R-COO-MgBr R-COO-MgBr -(+H2O)🡪 R-COOH +Mg(OH)Br |
|
7. Муравьиную кислоту получают нагреванием оксида углерода (II) с гидроксидом натрия под давлением: |
NaOH + CO –(200oC,p)🡪 HCOONa 2HCOONa+ H2SO4🡪2HCOOH + Na2SO4 |
|
8. Уксусную кислоту получают каталитическим окислением бутана: |
2C4H10 + 5O2 🡪 4CH3-COOH + 2H2O |
|
9. Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия: |
5C6H5–CH3+6KMnO4+9H2SO4🡪5C6H5-COOH+3K2SO4 + MnSO4 + 14H2O |
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ.
1. Кислотные свойства – замещение атома Н в карбоксильной группе на металл или ион аммония.
|
1.Взаимодействие с металлами |
2CH3COOH+Ca 🡪(CH3COO)2Ca+H2 ацетат кальция |
|
2.Взаимодействие с оксидами металлов |
2CH3COOH+BaO 🡪(CH3COO)2Ba+H2O |
|
3.Реакция нейтрализации с гидроксидами металлов |
2CH3COOH+Cu(OH)2 🡪 (CH3COO)2Cu + 2H2O |
|
4.Взаимодействие с солями более слабых и летучих (или нерастворимых) кислот |
2CH3COOH+CaCO3 🡪 (CH3COO)2Ca + H2O + CO2 |
|
4*. Качественная реакция на карбоновые кислоты: взаимодействие с содой (гидрокарбонатом натрия) или другими карбонатами и гидрокарбонатами. В результате наблюдается выделение углекислого газа. 2CH3COOH+Na2CO3 🡪 2CH3COONa+H2O+CO2↑ |
|
|
2. Замещение гидроксильной группы: |
|
|
5.Реакция этерификации |
|
|
6.Образование галоген-ангидридов – с помощью хлоридов фосфора (III) и (V). |
|
|
7. Образование амидов: |
|
|
8. Получение ангидридов. |
С помощью Р2О5 можно дегидратировать карбоновую кислоту – в результате получается ангидрид. 2СН3 – СООН + Р2О5 🡪 (СН3СО)2О + НРО3 |
|
3. Замещение атома водорода при атоме углерода, ближайшем к карбоксильной группе ( α-углеродный атом) |
|
|
9.Галогенирование кислот – реакция идёт в присутствии красного фосфора или на свету. |
CH3-COOH+Br2 –(Ркр)🡪 CH2-COOH + НВr ⎮ Br |
|
Особенности муравьиной кислоты. |
|
|
1. Разложение при нагревании. |
Н-СООН –(H2SO4конц,t)🡪 CO + H2O |
|
2. Реакция серебряного зеркала и с гидроксидом меди (II) – муравьиная кислота проявляет свойства альдегидов. |
Н-COOH+2[Ag(NH3)2]OH🡪(NH4)2СО3+2Ag+2NH3+H2O H-COOH + Cu(OH)2 –t🡪 CO2 + Cu2O + H2O |
|
3. Окисление хлором и бромом, а также азотной кислотой. |
H-COOH + Cl2 🡪 CO2 + 2HCl |
|
Особенности бензойной кислоты. |
|
|
1. Разложение при нагревании – декарбоксилирование. |
При нагревании бензойной кислоты она разлагается на бензол и углекислый газ: -(t)🡪 + CO2 |
|
2. Реакции замещения в ароматическом кольце. |
Карбоксильная группа является электроноакцепторной, она уменьшает электронную плотность бензольного кольца и является мета-ориентантом. + HNO3 –(H2SO4)🡪 +H2O |
|
Особенности щавелевой кислоты. |
|
|
1. Разложение при нагревании |
|
|
2. Окисление перманганатом калия. |
|
|
Особенности непредельных кислот (акриловой и олеиновой). |
|
|
1. Реакции присоединения. |
Присоединение воды и бромоводорода к акриловой кислоте происходит против правила Марковникова, т.к. карбоксильная группа является электроноакцепторной: СН2=СН-СООН + НBr 🡪 Br-CH2-CH2-COOH Также к непредельным кислотам можно присоединять галогены и водород: С17Н33-СООН+H2🡪 C17H35-COOH(стеариновая) |
|
2. Реакции окисления |
При мягком окислении акриловой кислоты образуется 2 гидроксогруппы: 3СН2=СН-СООН+2KMnO4+2H2O 🡪2CH2(OH)-CH(OH)-COOК + CH2(OH)-CH(OH)-COOH +2MnO2 |
Свойства солей карбоновых кислот.
|
1. Обменные реакции с более сильными кислотами и со щелочами. |
CH3-COONa + HCl 🡪 CH3-COOH + NaCl (CH3-COO)2Cu + KOH 🡪 Cu(OH)2 ↓+ CH3COOK |
|
2. Термическое разложение солей двухвалентных металлов (кальция, магния, бария)- образуются кетоны. |
(CH3-COO)2Ca -(t)🡪 CaCO3 + CH3-C-CH3 ǁ O |
|
3. Сплавление солей щелочных металлов со щелочью (реакция Дюма)- получаются алканы. |
CH3-COONa + NaOH -(t)🡪 CH4 + Na2CO3 |
|
4. Электролиз водных растворов солей карбоновых кислот (реакция Кольбе). |
2CH3-COONa +2Н2О -(эл.ток)🡪 🡪 C2H6 +2CO2 + H2+2NaOH анод катод |
Свойства галогенангидридов
|
1. Гидролиз – получается кислота. |
CH3-COCl + H2O 🡪 CH3-COOH + HCl |
|
2. Реакции ацилирования бензола, аминов, солей фенола. |
CH3-COCl+ -(AlCl3)🡪HCl+ |
|
3. Получение амидов и сложных эфиров |
CH3-COCl + NH3 🡪 CH3-CONH2 + NH4Cl С6Н5-ОNa+ C2H5-C=O -(t)🡪 NaCl + C6H5-O-C=O
Cl C2H5 |














 Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество.
Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество.