1 августа 2021
В закладки
Обсудить
Жалоба
Демоверсия 2023
Официальная демоверсия ЕГЭ 2022 от ФИПИ по химии.
В демонстрационном варианте представлено по несколько примеров заданий на некоторые позиции экзаменационной работы. В реальных вариантах экзаменационной работы на каждую позицию будет предложено только одно задание.
Экзаменационная работа состоит из двух частей, включающих в себя 34 задания. Часть 1 содержит 28 заданий с кратким ответом, часть 2 содержит 6 заданий с развёрнутым ответом.
На выполнение экзаменационной работы по химии отводится 3,5 часа.
Обновлено 10 ноября. Демоверсия утверждена.
→ Демоверсия: him-demo2022-v2.pdf
→ Кодификатор: him-k2022-v2.pdf
→ Спецификация: him-s2022-v2.pdf
→ Скачать одним архивом: him-demo2022-v2.zip
Изменения в КИМ 2022 года в сравнении с КИМ 2021 года
В экзаменационной работе 2022 г. по сравнению с работой 2021 г. приняты следующие изменения.
1. В экзаменационном варианте уменьшено с 35 до 34 общее количество заданий. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
− Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
− Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8.
2. Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
3. Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
4. Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
5. Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).
В целом принятые изменения в экзаменационной работе 2022 г. ориентированы на повышение объективности проверки сформированности ряда важных общеучебных умений, в первую очередь таких, как анализ текста условия задания, представленного в различной форме (таблица, схема, график), комбинирование аналитической и расчётной деятельности, анализ состава веществ и прогноз возможности протекания реакций между ними, моделирование химических процессов и описание признаков их протекания и др.
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности
Курсы ЕГЭ Lancman School подготовили для вас подробную информацию о заданиях ЕГЭ по химии 2022 года.
Изменения в КИМах ЕГЭ по химии 2022 года (справка ФИПИ):
«1) В экзаменационном варианте уменьшено с 35 до 34 общее количество заданий. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
— Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
— Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8.
2) Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
3) Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
4) Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
5) Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).».
Хочешь БЕСПЛАТНО разобрать с опытным преподавателем все детали новых усложнённых вариантов ЕГЭ по химии 2022 года — приходи на пробное занятие в Lancman School. Мы 13 лет готовим к ЕГЭ на высокие баллы и знаем об экзаменах и поступлении в хорошие вузы буквально всё. Решишь продолжить готовиться к ЕГЭ вместе с нами весь год — дадим скидку после бесплатного пробного занятия. Любой вопрос смело пиши сюда.
Если ты живешь не в Москве, но хочешь заниматься с лучшими столичными репетиторами и сдать ЕГЭ на 80+ баллов, то регистрируйся на наши онлайн-курсы. В этом году мы включили в договор пункт, гарантирующий поступление на бюджет в любой вуз страны. Если ученик будет соблюдать все обговоренные условия, он обязательно поступит. В противном случае мы вернём деньги. Первое пробное занятие БЕСПЛАТНО.
Разбор демоверсии ЕГЭ по химии 2022 года с сайта ФИПИ
Источник: fipi.ru
Если материал показался интересным – ставь лайк, делись с друзьями в соцсетях и подписывайся на обновления нашего блога. Кнопку подписки ты найдёшь сразу под постом. Мы пишем о ЕГЭ много (а главное, интересно).
Редактор колонки — ЕГЭ-блогер Мария Кучерова (mel.fm, newtonew.com).

В демонстрационном варианте представлено по несколько примеров заданий на некоторые позиции экзаменационной работы. В реальных вариантах экзаменационной работы на каждую позицию будет предложено только одно задание.
Экзаменационная работа состоит из двух частей, включающих в себя 34 задания. Часть 1 содержит 28 заданий с кратким ответом, часть 2 содержит 6 заданий с развёрнутым ответом. На выполнение экзаменационной работы по химии отводится 3,5 часа.
— Демоверсия: Скачать
— Спецификация: Скачать
— Кодификатор: Скачать
Смотреть демо вариант онлайн:
Интересные задания
1. Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют одинаковое число неспаренных электронов. Запишите номера выбранных элементов.
2. Из указанных в ряду химических элементов выберите три p-элемента. Расположите выбранные элементы в порядке уменьшения их атомного радиуса. Запишите номера выбранных элементов в нужной последовательности.
3.
Из числа указанных в ряду элементов выберите два элемента, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления. Запишите номера выбранных элементов.
6. В одну из пробирок с осадком гидроксида алюминия добавили сильную кислоту X, а в другую – раствор вещества Y. В результате в каждой из пробирок наблюдали растворение осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
1) бромоводородная кислота
2) гидросульфид натрия
3) сероводородная кислота
4) гидроксид калия
5) гидрат аммиака
11. Из предложенного перечня выберите два вещества, которые являются структурными изомерами бутена-1.
1) бутан
2) циклобутан
3) бутин-2
4) бутадиен-1,3
5) метилпропен
12. Из предложенного перечня выберите все вещества, при взаимодействии которых с раствором перманганата калия в кислой среде образуется карбоновая кислота.
1) гексен-1
2) бензол
3) метилбензол
4) этилацетат
5) уксусный альдегид
13. Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
1) пропан
2) хлорметан
3) водород
4) гидроксид натрия
5) соляная кислота
17. Из предложенного перечня выберите все реакции, которые являются окислительно-восстановительными.
1) взаимодействие сульфида калия с перманганатом калия
2) взаимодействие концентрированной серной кислоты с хлоридом натрия
3) взаимодействие при нагревании хлорида аммония и нитрита натрия
4) взаимодействие при нагревании оксида кремния с карбонатом натрия
5) взаимодействие иодоводородной кислоты с дихроматом натрия
Изменения в КИМ 2022 года в сравнении с КИМ 2021 года
В экзаменационной работе 2022 г. по сравнению с работой 2021 г. приняты следующие изменения.
1. В экзаменационном варианте уменьшено с 35 до 34 общее количество заданий. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
− Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
− Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8.
2. Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
3. Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
4. Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
5. Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).
В целом принятые изменения в экзаменационной работе 2022 г. ориентированы на повышение объективности проверки сформированности ряда важных общеучебных умений, в первую очередь таких, как анализ текста условия задания, представленного в различной форме (таблица, схема, график), комбинирование аналитической и расчётной деятельности, анализ состава веществ и прогноз возможности протекания реакций между ними, моделирование химических процессов и описание признаков их протекания и др.
Обобщённый план варианта КИМ ЕГЭ 2022 года по химии
| Номер | Проверяемые элементы содержания | Уровень сложности задания | Макс. балл за выпол нение задания | Примерное время выполнения задания (мин.) |
| Часть 1 | ||||
| 1 | Строение электронных оболочек атомов элементов первых четырёх периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояния атомов |
Б | 1 | 2–3 |
| 2 | Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов. Общая характеристика неметаллов IVА– VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | Б | 1 | 2–3 |
| 3 | Электроотрицательность. Степень окисления и валентность химических элементов | Б | 1 | 2–3 |
| 4 | Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения |
Б | 1 | 2–3 |
| 5 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная) | Б | 1 | 2–3 |
| 6 | Характерные химические свойства простых веществ – металлов: щелочных, щёлочноземельных, магния, алюминия; переходных металлов: меди, цинка, хрома, железа. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния. Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот. Характерные химические свойства солей: средних, кислых, оснóвных; комплексных (на примере гидроксосоединений алюминия и цинка). Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена | П | 2 | 5–7 |
| 7 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная). Характерные химические свойства неорганических веществ:
комплексных (на примере гидроксосоединений алюминия и цинка) |
П | 2 | 5–7 |
| 8 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная); Характерные химические свойства неорганических веществ:
|
П | 2 | 5–7 |
| 9 | Взаимосвязь неорганических веществ | Б | 1 | 2–3 |
| 10 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) |
Б | 1 | 2–3 |
| 11 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа |
Б | 1 | 2–3 |
| 12 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Основные способы получения углеводородов (в лаборатории). Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Основные способы получения кислородсодержащих органических соединений (в лаборатории) |
Б | 1 | 2–3 |
| 13 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки |
Б | 1 | 2–3 |
| 14 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Важнейшие способы получения углеводородов. Ионный (правило В.В. Марковникова) и радикальные механизмы реакций в органической химии | П | 2 | 5–7 |
| 15 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, карбоновых кислот, сложных эфиров. Важнейшие способы получения кислородсодержащих органических соединений | П | 2 | 5–7 |
| 16 | Взаимосвязь углеводородов, кислородсодержащих и азотсодержащих органических соединений | Б | 1 | 2–3 |
| 17 | Классификация химических реакций в неорганической и органической химии |
Б | 1 | 2–3 |
| 18 | Скорость реакции, её зависимость от различных факторов |
Б | 1 | 2–3 |
| 19 | Реакции окислительно-восстановительные | Б | 1 | 2–3 |
| 20 | Электролиз расплавов и растворов (солей, щелочей, кислот) |
Б | 1 | 2–3 |
| 21 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная | Б | 1 | 2–3 |
| 22 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов |
П | 2 | 5–7 |
| 23 | Обратимые и необратимые химические реакции. Химическое равновесие. Расчёты количества вещества, массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ | П | 2 | 5–7 |
| 24 | Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений | П | 2 | 5–7 |
| 25 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ. Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки |
Б | 1 | 2–3 |
| 26 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе» |
Б | 1 | 3–4 |
| 27 | Расчёты теплового эффекта (по термохимическим уравнениям) | Б | 1 | 3–4 |
| 28 | Расчёты массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ. Расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного. Расчёты массовой доли (массы) химического соединения в смеси |
Б | 1 | 3–4 |
| Часть 2 | ||||
| 29 | Окислитель и восстановитель. Реакции окислительно-восстановительные | В | 2 | 10–15 |
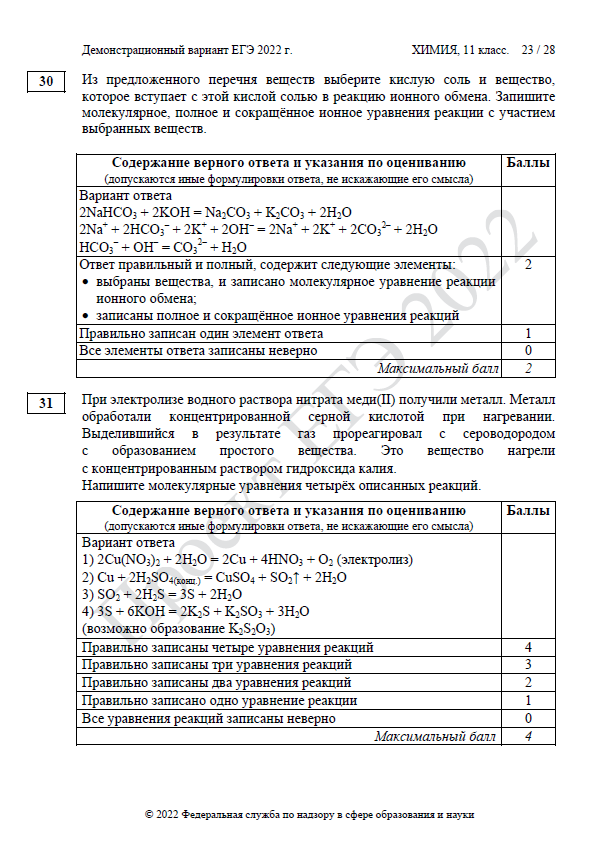
| 30 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена |
В | 2 | 10–15 |
| 31 | Реакции, подтверждающие взаимосвязь различных классов неорганических веществ | В | 4 | 10-15 |
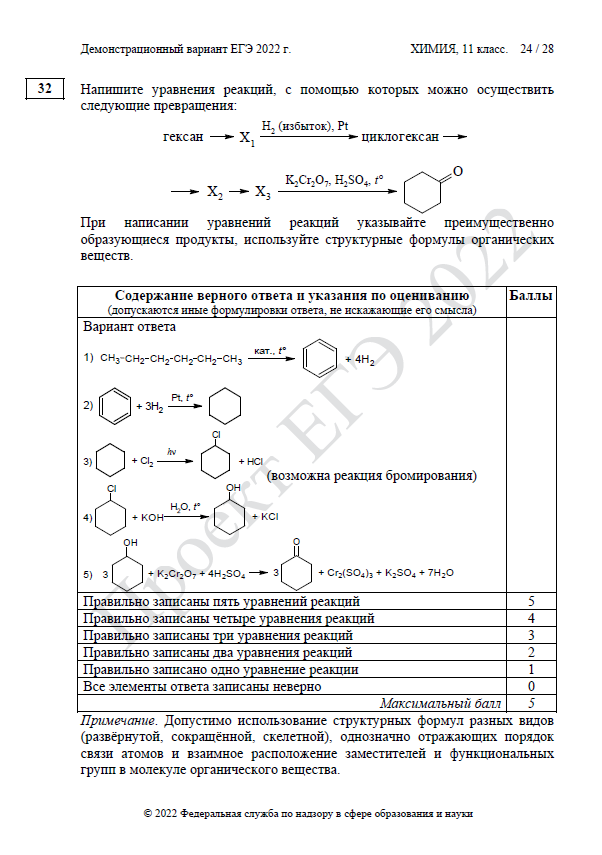
| 32 | Реакции, подтверждающие взаимосвязь органических соединений | В | 5 | 10–15 |
| 33 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе». Расчёты массы (объёма, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси). Расчёты массы (объёма, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определённой массовой долей растворённого вещества. Расчёты массовой доли (массы) химического соединения в смеси |
В | 4 | 20–25 |
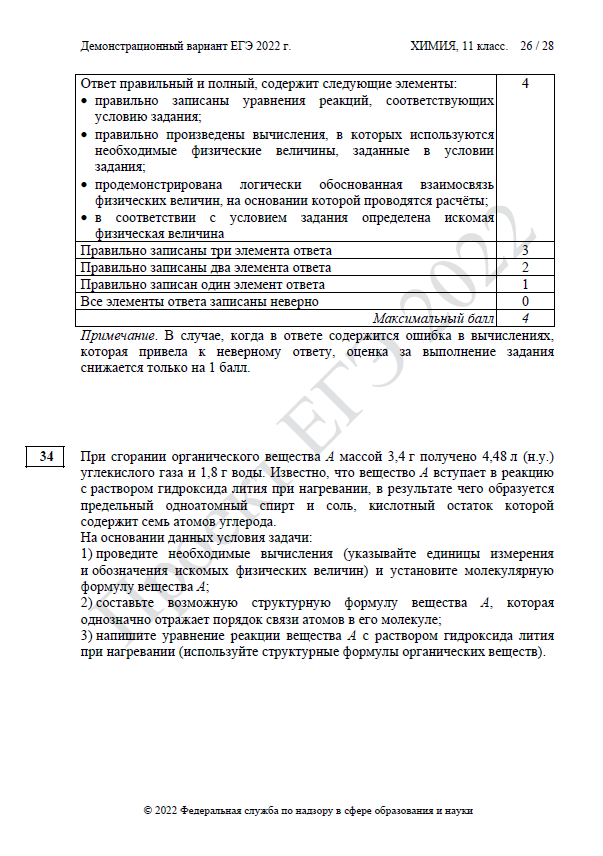
| 34 | Установление молекулярной и структурной формул вещества | В | 3 | 10–15 |
| Всего заданий – 34; из них по уровню сложности: Б – 20; П – 8; В – 6. Максимальный первичный балл за работу – 56. Общее время выполнения работы – 210 мин. |
Вам будет интересно:
Официальная демоверсия и изменения ЕГЭ 2022 по информатике от ФИПИ (задания и ответы)
* Олимпиады и конкурсы
* Готовые контрольные работы
* Работы СтатГрад
* Официальные ВПР
Поделиться:
Главная ЕГЭ 2022
Добавлено: 5-11-2021, 20:09
По демоверсиям можно понять какие задания будут на настоящем экзамене. По подобным вариантам можно определить не только количество заданий, их содержание , но и уровень сложности. Регулярное решение демовариантов помогут выявить «слабые» места, пробелы в изучении школьной программы того или иного предмета, а также велика вероятность того, что на настоящем экзамене встретится знакомое или похожее задание.
Скачать файл: hi-11-ege-2022-demo.pdf [954,01 Kb] (cкачиваний: 63)
Посмотреть онлайн файл: hi-11-ege-2022-demo.pdf
Официальная демоверсия от ФИПИ на 2022 год — ХИМИЯ
- Демоверсия: ЕГЭ по химии 2022
- Кодификатор: ЕГЭ по химии 2022
- Спецификация: ЕГЭ по химии 2022
Официальная демоверсия от ФИПИ на 2022 год — МАТЕМАТИКА
| профиль | база |
|
|
Официальная демоверсия от ФИПИ на 2022 год — БИОЛОГИЯ
- Демоверсия: ЕГЭ биология 2022
- Кодификатор: ЕГЭ биология 2022
- Спецификация: ЕГЭ биология 2022
Официальная демоверсия от ФИПИ на 2022 год -ФИЗИКА
- Демоверсия: ЕГЭ физика 2022
- Кодификатор: ЕГЭ физика 2022
- Спецификация: ЕГЭ физика 2022
Информация об изменениях в КИМ ЕГЭ 2022 г. в сравнении с КИМ ЕГЭ 2021 г.
| Учебный предмет | Изменения в КИМ ЕГЭ |
| Химия |
|
| Математика | Профильный уровень
Базовый уровень
|
| Физика |
|
| Биология |
|
| Русский язык |
|