Досрочный вариант ЕГЭ по химии-2022. Скачать разбор досрочного варианта ЕГЭ по химии-2022 от 23 марта 2022 с ответами и решениями
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) Na 2) S 3) Al 4) O 5) Cr
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1. Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число s-электронов. Запишите в поле ответа номера выбранных элементов.
2. Из указанных в ряду химических элементов выберите три элемента-металла. Расположите выбранные элементы в порядке возрастания восстановительных свойств образуемых ими простых веществ. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3. Из указанных в ряду элементов выберите два элемента, у которых в образуемых ими ионах ЭОх2- совпадает степень окисления. Запишите в поле ответа номера выбранных элементов.
4. Из предложенного перечня выберите два вещества, которые имеют ионную и ковалентную неполярную связь.
1) фосфат натрия
2) метилацетат
3) бензоат аммония
4) диэтиловый эфир
5) пероксид натрия
Запишите номера выбранных веществ.
5. Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) кислоты; Б) средней соли; В) кислотного оксида.
Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
6. В одну из пробирок с порошком оксида цинка добавили слабый электролит X, а в другую – раствор вещества Y. В результате в первой пробирке наблюдали растворение твердого вещества. В пробирке с раствором вещества Y произошла реакция, которую описывает сокращенное ионное уравнение:
ZnO + 2H+ = Zn2+ + H2O
выберите вещества X и Y, которые могут вступать в описанные реакции.
1) йодоводород
2) хлорид аммония
3) гидрокарбонат натрия
4) гидроксид натрия
5) фтороводород
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
7. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) CuBr2
Б) Cu В) CO2 Г) HCl(р-р) |
1) Cl2, KOH, KI
2) Mg, CaO, C 3) S, Cl2, HNO3 4) Mg, MgO, Al2O3 5) NaCl, H2SO4, O2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
8. Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ |
| А) Fe2O3 и HI
Б) KI и H2SO4(конц.) В) NaCl(тв.) и H2SO4(конц.) Г) Fe3O4 и HI |
1) FeI2, I2 и H2O
2) FeI2 и H2O 3) K2SO4, I2, H2S и H2O 4) K2SO4, I2, SO3 и H2O 5) Cl2, Na2SO4и H2O 6) HCl и NaНSO4 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
9. Задана следующая схема превращений веществ:
Fe X
FeS
Определите, какие из указанных веществ являются веществами X и Y.
1) S
2) CuS
3) FeCl3
4) K2S
5) FeCl2
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
10. Установите соответствие между формулой вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| КЛАСС/ГРУППА | НАЗВАНИЕ ВЕЩЕСТВА |
| А) нитросоединение
Б) сложный эфир В) спирт |
1) тринитроглицерин
2) диизопропиловый эфир 3) глицерин 4) нитротолуол |
Запишите в таблицу выбранные цифры под соответствующими буквами.
11. Из предложенного перечня выберите два вещества, которые являются межклассовыми изомерами.
1) пропаналь
2) пропановая кислота
3) уксусная кислота
4) нитроэтан
5) глицин
Запишите в поле ответа номера выбранных веществ.
12. Из предложенного перечня выберите все вещества, которые реагируют с водородом.
1) олеиновая кислота
2) стеариновая кислота
3) ацетон
4) изопрен
5) изопропиловый спирт
Запишите в поле ответа номера выбранных веществ.
13. Из предложенного перечня выберите два вещества, которые реагируют и с глюкозой, и с фруктозой.
1) гидроксид меди (II)
2) сульфат калия
3) водород
4) медь
5) метан
Запишите в поле ответа номера выбранных веществ.
14. Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | ВЕЩЕСТВО Х |
| А) Х + Н2О ⟶ (кат.) изопропиловый спирт
Б) Х + KMnO4 + Н2О ⟶ пропандиол-1,2 В) Х + KMnO4 + H+ ⟶ пропионовая кислота Г) Х + Н2О ⟶ (кат.) ацетон |
1) бутен-1
2) этен 3) бутен-2 4) пропин 5) пропен 6) бутин-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
15. Установите соответствие между веществом и его способом получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную
цифрой.
| ВЕЩЕСТВО | СПОСОБ ПОЛУЧЕНИЯ |
| А) этанол
Б) уксусная кислота В) этиленгликоль Г) этаналь |
1) окисление этена перманганатом калия в нейтральной среде
2) щелочной гидролиз метилацетата 3) щелочной гидролиз 1,1-дихлорэтана 4) окисление бутена-2 перманганатом калия в кислой среде 5) термолиз ацетата кальция 6) восстановление ацетальдегида |
Запишите в таблицу выбранные цифры под соответствующими буквами.
16. Задана следующая схема превращений веществ:
метан ⟶ Х ⟶ бензол ⟶ Y ⟶ толуол
Определите, какие из указанных веществ являются веществами X и Y.
1) бромметан
2) этен
3) нитробензол
4) ацетилен
5) бромбензол
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
17. Из предложенного перечня выберите все типы реакций, к которым можно отнести взаимодействие водорода с хлором.
1) гомогенная
2) замещения
3) экзотермическая
4) нейтрализации
5) окислительно-восстановительная
Запишите номера выбранных ответов.
18. Из предложенного перечня выберите все реакции, для которых будет увеличиваться скорость реакции при добавлении кислорода.
1) O2 ⟶ O3
2) N2 + O2 ⟶ NO
3) C + O2 ⟶ CO2
4) CuO ⟶ Cu2O + O2
5) S + O2 = SO2
Запишите номера выбранных ответов.
19. Установите соответствие между схемой реакции и свойством элемента фосфора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВА ФОСФОРА |
| А) Mg + H3PO4 → Mg(H2PO4) 2 + H2
Б) P + HNO3 → H3PO4 + NO2 + H2O В) PH3 + O2 → H3PO4 |
1) является окислителем
2) является восстановителем 3) является и окислителем, и восстановителем 4) не проявляет окислительно-восстановительных свойств |
Запишите в таблицу выбранные цифры под соответствующими буквами.
20. Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
| А) бромид лития
Б) сульфат натрия В) хлорид алюминия |
1) водород, галоген
2) металл, галоген 3) водород, кислород 4) металл, кислород |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
21. Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) Na2SO4
2) Fe(NO3)2
3) K2SO3
4) НClO3
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
22. Установите соответствие между способом воздействия на равновесную систему
S2− (р-р) + H2O(ж.) ⇆ HS− (р-р) + OH− (р-р) — Q
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | СМЕЩЕНИЕ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) нагревание
Б) разбавление водой В) добавление твердой щелочи Г) понижение давления |
1) в сторону прямой реакции
2) в сторону обратной реакции 3) практически не смещается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
23. В реактор постоянного объёма поместили некоторое количество серного ангидрида. В результате протекания обратимой реакции
2SO3(г) ⇄ 2SO2(г) + O2(г)
в реакционной системе установилось химическое равновесие.
Используя данные, приведённые в таблице, определите равновесную концентрацию сернистого газа (X) и равновесную концентрацию кислорода (Y).
Выберите из списка номера правильных ответов.
1) 0,02 моль/л
2) 0,04 моль/л
3) 0,08 моль/л
4) 0,3 моль/л
5) 0,15 моль/л
6) 0,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
24. Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить водные растворы этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛЫ ВЕЩЕСТВ | РЕАГЕНТ |
| А) HNO3 и Na2SO4
Б) K2CO3 и NaОН В) NaCl и Na3PO4 Г) Mgl2 и Sr(NO3) |
1) LiCl
2) NaBr 3) Cu 4) H2SO4 (р-р) 5) NaNO3 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
25. Установите соответствие между названием вещества и основной областью применения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ОБЛАСТЬ ПРИМЕНЕНИЯ | НАЗВАНИЕ ВЕЩЕСТВА |
| А) пищевая промышленность
Б) получение взрывчатых веществ В) водоочиститель |
1) азотная кислота
2) хлор 3) уксусная кислота 4) хлорбензол |
Запишите в таблицу выбранные цифры под соответствующими буквами.
26. Вычислите массу (в г) воды, которую нужно добавить в 600 г 10%-ного раствор сульфата аммония для получения 3%-ного раствора. (Запишите число с точностью до целых.)
27. Синтез углекислого газа протекает в соответствии с термохимическим уравнением реакции
С(тв.) + О2(г) = СО2(г) + 393,3 кДж
Определите объем (в л) кислорода, который образуется в результате выделения 944 кДж тепла. (Запишите число точностью до целых.)
28. 175 г технического карбоната магния, содержащего 4% некарбонатной примеси, нагрели. Найдите объем (в л) выделившегося газа (н.у.) (Запишите число с точностью до десятых.)
Для записи ответов на задания 29–34 используйте чистый лист бумаги. Запишите сначала номер задания (29, 30 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 29 и 30 используйте следующий перечень веществ: хлор, хромат калия, нитрит калия, сернистый газ, ацетат серебра, нитрат алюминия. Допустимо использование водных растворов этих веществ.
29. Из предложенного перечня веществ выберите вещества, между которыми может протекать окислительно-восстановительная реакция, в которой в растворе образуется только кислоты. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций. Составьте электронный баланс, укажите окислитель и восстановитель в этой реакции.
Cl2; K2CrO4; KNO2; SO2; CH3COOAg; Al(NO3)3
Cl20 + SO2 + 2H2O → 2HCl + H2SO4
2Cl0 2Cl− Cl20 – окислитель
S+4 S+6 SO2+4 – восстановитель
30. Из предложенного перечня веществ выберите вещества, между которыми может протекать реакция ионного обмена, в результате которой из окрашенного раствора выпадает осадок. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций.
2CH3COOAg + K2CrO4 → 2CH3COOK + Ag2CrO4
2CH3COO− + 2Ag+ + 2H+ + CrO42− → 2CH3COO− + 2H+ + Ag2CrO4
2Ag+ + CrO42− → Ag2CrO4
31. Бромоводородной кислотой нейтрализовали карбонат калия. Через полученный раствор пропустили электрический ток. Образовавшийся на катоде газ пропустили над нагретым оксидом меди (II). Полученное простое вещество растворили в концентрированном растворе азотной кислоты. Напишите уравнения четырёх описанных реакций
2HBr + K2CO3 → H2O + CO2 + 2KBr
2KBr + 2H2O H2 + 2KOH + Br2
CuO + H2 → Cu + H2O
Cu0 + 4HN+5O3 (конц) → Cu2+(NO3)2 + 2H2O + 2N+4O2
32. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
бутен-1 ⟶ Х1 ⟶ бутин-1 ⟶ Х2 ⟶ гексин-3 Х3
При написании уравнений реакций используйте структурные формулы органических веществ.
CH3CH2CH=CH2 + Cl2 →

CH3-CH2-C≡CH + [Ag(NH3)2]OH → CH3-CH2-C≡CAg + 2NH3 + H2O
CH3-CH2-C≡CAgg + CH3-CH2-Cl → CH3-CH2-C≡C-CH2-CH3 + AgCl
5CH3-CH2-C≡C-CH2-CH3 + 6KMnO4 + 9H2SO4 10CH3CH2COOH + 3K2SO4 + 6MnSO4 + 4H2O
33. К раствору сульфата железа (III) массой 632 г, содержащего в общей сложности 1,806∙1025 атомов кислорода, добавили 79 г сульфита калия. После окончания реакции к образовавшемуся раствору прилили 552 г 10%-ного раствора карбоната калия. Вычислите массовую долю сульфата калия в образовавшемся растворе. (Образованием кислых солей пренебречь.) В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Fe2(SO4)3 + K2SO3 + H2O → 2FeSO4↓ + K2SO4 + H2SO4
nO = 1,306·1025/6,02·1023 = 30 моль
n(Fe2(SO4)3) = х моль, n(Н2O) = у моль,
m(Fe2(SO4)3) = 400х г, m(Н2O) = 18у г,
тогда nFe = 2x моль, nS = 3x моль, n1(O) = 12x моль
n2(O) = y моль
Получаем систему:
у + 12х = 30
400х + 18y = 632
Получаем:
х = 0,5 моль
у = 24 моль
nFe2(SO4)3 = 0,5 моль
nK2SO3 = 39/158 = 0,5 моль
nFeSO4 = 1 моль
nH2SO4 = nK2SO3 = 0,5 моль
H2SO4 + K2CO3 → H2O + CO2 + K2SO4
nK2CO3 = 552·0,1/(39·2+12+16·3) = 0,4 моль
nCO2 = nK2CO3 = 0,4 моль
nK2CO3 = nK2SO4 = 0,4 моль
ω(K2SO4) = (0,4+0,5)·174/(632+79+552 — 0,4·44) = 0,1257 или 12,57%
34. При взаимодействии соли первичного амина с нитратом серебра образуется органическое вещество А и бромид серебра. Вещество А содержит 25,93% азота, 7,41% водорода и 44,44% кислорода по массе. Напишите уравнение реакции получения вещества А из соли первичного амина и нитрата серебра. На основании данных условия задания:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества А и запишите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из соли первичного амина и нитрата серебра
n(С):n(H):n(N):n(O) = 1:4:1:1,5|2 = 2:8:2:3
m(N) = 25,93г n(N) = 25,93/14 = 1,852143 моль
m(H) = 7,41г n(H) = 7,41 моль
m(O) = 44,44г n(O) = 2,7775 моль
m(C) = 22,22г n(C) = 1,3516667 моль
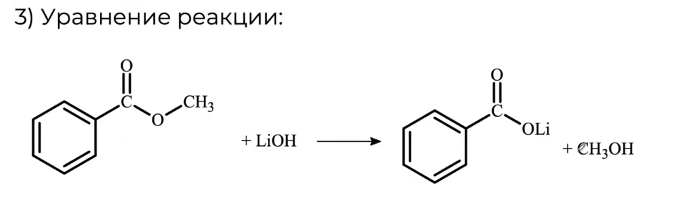
[CH3-CH2-NH3]Br + AgNO3 → [CH3-CH2-NH3]NO3 + AgBr
Skip to content
Чтобы поделиться, нажимайте
Представляем вашему вниманию вариант 2 из досрочного ЕГЭ по химии 2020, который должен был состояться в марте 2020, но был отменён из-за короновируса.
После каждого задания представлены видео-объяснения, а в конце страницы — текстовые ответы.
Скачать Досрочный ЕГЭ по химии 2020. Вариант 2 (с ответами) в формате pdf
Ответы:
| № задания | Ответ | Ссылка на видео-объяснение |
| 1 | 13 | https://youtu.be/r8GtRWFu2zU |
| 2 | 154 | https://youtu.be/DhSc8MAV0HI |
| 3 | 25 | https://youtu.be/gnw8YUSofSM |
| 4 | 25 | https://youtu.be/MbB4gphL3so |
| 5 | 214 | https://youtu.be/4ax9FiQb8S8 |
| 6 | 15 | https://youtu.be/GmzgahOfefg |
| 7 | 15 | https://youtu.be/b1r9sbmZ-PM |
| 8 | 3422 | https://youtu.be/tNSwMk4mioU |
| 9 | 4155 | https://youtu.be/IJHV7hqvaTQ |
| 10 | 51 | https://youtu.be/vtp17r5SFo4 |
| 11 | 214 | https://youtu.be/T5BzUX2e48s |
| 12 | 35 | https://youtu.be/Hgss136Df_Y |
| 13 | 25 | https://youtu.be/c9fXRhGMGcM |
| 14 | 23 | https://youtu.be/J6AGeUmg1hg |
| 15 | 14 | https://youtu.be/0AKwwWb6UuM |
| 16 | 6164 | https://youtu.be/BjvPVowZ-5E |
| 17 | 3614 | https://youtu.be/lo6xCAtUOzw |
| 18 | 45 | https://youtu.be/kx-3EgX5cuM |
| 19 | 45 | https://youtu.be/jPT9cs0OBH4 |
| 20 | 14 | https://youtu.be/FZgFwMa254k |
| 21 | 122 | https://youtu.be/cUt-16o0mT8 |
| 22 | 3135 | https://youtu.be/wbdgd7W2Tw0 |
| 23 | 3312 | https://youtu.be/pgV22LCynhU |
| 24 | 1123 | https://youtu.be/dAu_3jrBdqw |
| 25 | 2543 | https://youtu.be/W5Xd9XRt5bA |
| 26 | 214 | https://youtu.be/TP-ojG22zo0 |
| 27 | 7 | https://youtu.be/8CbPV_1EOmA |
| 28 | 1188 | https://youtu.be/iKsuy5bD6vY |
| 29 | 10,8 | https://youtu.be/BLqFrpjjrqQ |
30. Видео-объяснение https://youtu.be/DJnNkK8DHzA
2Cr(OH)3 + 3H2O2 + 4KOH = 2K2CrO4 + 8H2O
2 Cr+3 – 3ē → Cr+6
3 2O-1 + 2ē → 2O-2
Гидроксид хрома (III) или хром в степени окисления +3 является восстановителем.
Пероксид водорода или кислород в степени окисления –1 –окислителем
31. Видео-объяснение https://youtu.be/Et0i9RYw28k
(NH4)2SO4 + 2KOH = 2NH3∙H2O + K2SO4
2NH4+ + SO42- + 2K+ + 2OH— = 2NH3∙H2O + 2K+ + SO42-
NH4+ + OH— = NH3∙H2O
32. Видео-объяснение https://youtu.be/kqi0NE6WY0E
- 2Na + 2H2O = 2NaOH + H2
- 4H2 + Fe3O4 3Fe + 4H2O
- 2Fe + 6H2SO4 (конц.) Fe2(SO4)3 + 3SO2 + 6H2O
- Fe2(SO4)3 + 3K2CO3 + 3H2O = 3K2SO4 + 2Fe(OH)3 + 3CO2
33. Видео-объяснение https://youtu.be/sE1BAHSTKNA
34. 20,8%, видео-объяснение https://youtu.be/JCqhgd3ZNZ4
35. Видео-объяснение https://youtu.be/zOeAPLUUdxY
Скачать Досрочный ЕГЭ по химии 2020. Вариант 2 (с ответами) в формате pdf
Также:
- Посмотреть реальные, досрочные и пробные варианты ЕГЭ всех лет вы можете здесь, нажав на эту строку
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки для подготовки к ЕГЭ вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ вы можете здесь, нажав на эту строку
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами.
Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
- 1. B
- 2. Sn
- 3. Cr
- 4. N
- 5. C
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Задание №1
Определите элементы, атомы которых в основном состоянии на внешнем энергетическом уровне содержат один неспаренный электрон.
Запишите номера выбранных элементов.
Ответ:
Задание №2
Из указанных в ряду химических элементов выберите три элемента-неметалла.
Расположите выбранные элементы в порядке уменьшения восстановительных свойств соответствующих им простых веществ.
Запишите номера выбранных элементов в нужной последовательности.
Ответ:
Задание №3
Из указанных в ряду элементов выберите два элемента, степень окисления которых в высших оксидах равна +4.
Запишите номера выбранных элементов.
Ответ:
Задание №4
Из предложенного перечня выберите два вещества, в которых присутствует ковалентная полярная связь.
- 1. SrO
- 2. PBr3
- 3. CsCl
- 4. P4
- 5. NH4NO3
Запишите номера выбранных ответов.
Задание №5
Установите соответствие между формулой оксида и группой, к которой этот оксид принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ОКСИДА | ГРУППА ОКСИДОВ |
|
А) CrO3 Б) NO В) MnO2 |
1) несолеобразующие 2) кислотные 3) оснóвные 4) амфотерные |
Запишите в таблицу выбранные цифры под соответствующими буквами.
[adsp-pro-3]
Задание №6
Из предложенного перечня выберите два оксида, которые реагируют с водой.
- 1. оксид бария
- 2. оксид азота(II)
- 3. оксид меди(II)
- 4. оксид железа(II)
- 5. оксид хрома(VI)
Запишите номера выбранных ответов.
Задание №7
Даны две пробирки с раствором гидросульфита натрия. В одну из них добавили раствор вещества X, а в другую – раствор вещества Y. В результате в пробирке с веществом Х выделился газ, а в пробирке с веществом Y выпал осадок. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1. иодоводород
- 2. сульфат бария
- 3. гидроксид натрия
- 4. фосфат калия
- 5. гидроксид кальция
Запишите номера выбранных веществ под соответствующими буквами.
Задание №8
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
|
А) H2 Б) Si В) O2 Г) Cl2 |
1) H2S, NaOH, K2SO4 2) C2H6, H2S, Fe 3) N2, CO, CuO 4) Cl2, KOH, Ca 5) CO2, HF, CH4 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №9
Установите соответствие между исходным(и) веществом(-ами), вступающим(и) в реакцию, и продуктами этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИСХОДНОЕ(-ЫЕ) ВЕЩЕСТВО(-А) | ПРОДУКТЫ РЕАКЦИИ |
|
А) AgNO3 Б) Ag и HNO3 (разб.) В) CaO и HNO3 (разб.) Г) Ca(OH)2 и HNO3 (разб.) |
1) AgNO3, NO и H2O 2) Ca(NO3)2, NH4NO3 и H2O 3) Ag2O, NO2 и O2 4) Ag, NO2 и O2 5) Ca(NO3)2 и H2O 6) AgNO3 и H2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №10
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
- 1. Mg
- 2. Fe
- 3. SO2
- 4. H2O
- 5. HNO3
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
[adsp-pro-3]
Задание №11
Установите соответствие между названием вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА |
КЛАСС/ГРУППА ОРГАНИЧЕСКИХ |
|
А) бензилацетат Б) диэтиловый эфир В) бутаналь |
1) простые эфиры 2) сложные эфиры 3) фенолы 4) альдегиды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №12
Из предложенного перечня выберите два вещества, для которых нехарактерна изомерия углеродного скелета.
1) 2-метилбутен-2
2) бутандиол-1,2
3) пропаналь
4) изобутан
5) бутин-1
Запишите номера выбранных ответов.
Задание №13
Из предложенного перечня выберите две реакции, в ходе которых может образоваться бензол.
1) дегидрирование циклопентана
2) дегидрирование циклогексана
3) гидрирование фенола
4) дегидрирование гептана
5) дегидрирование гексана
Запишите номера выбранных ответов.
Задание 14
Из предложенного перечня выберите два вещества, с которыми взаимодействуют и метанол, и этиленгликоль.
1) бромная вода
2) хлороводород
3) натрий
4) гидроксид меди(II)
5) толуол
Запишите номера выбранных ответов.
Задание №15
Из предложенного перечня выберите два вещества, которые подвергаются гидролизу.
1) сахароза
2) 2-аминопропановая кислота
3) глюкоза
4) триолеат глицерина
5) фруктоза
Запишите номера выбранных ответов.
[adsp-pro-3]
Задание №16
Установите соответствие между химической реакцией и органическим веществом, преимущественно образующимся в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАКЦИЯ | ПРОДУКТ РЕАКЦИИ |
|
А) тримеризация ацетилена Б) гидрирование бутадиена-1,3 В) дегидрирование циклогексана Г) гидратация бутена-1 |
|
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №17
Установите соответствие между схемой реакции и органическим веществом – продуктом реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | ВЕЩЕСТВО Х |
|
|
1) HBr 2) CuBr2 3) Br2 (водн.) 4) NaOH 5) NaHCO3 6) CuO |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №18
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) 1,1-дибромпропан
2) пропилен
3) пропанол-1
4) 1,3-дибромпропан
5) циклопропан
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Задание №19
Из предложенного перечня выберите две реакции, которые являются реакциями присоединения.
1) хлорирование метана
2) гидролиз этилата натрия
3) окисление метанола оксидом меди(II)
4) гидрирование ацетальдегида
5) гидратация пропина
Запишите номера выбранных ответов.
Задание №20
Из предложенного перечня выберите два фактора, которые приводят к увеличению скорости химической реакции между оксидом меди(II) и соляной кислотой.
1) измельчение оксида меди(II)
2) понижение температуры
3) добавление воды
4) увеличение концентрации HCl
5) повышение давления в системе
Запишите номера выбранных ответов.
[adsp-pro-3]
Задание №21
Установите соответствие между схемой реакции и свойством атома серы в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВО АТОМА СЕРЫ |
|
А) S + KOH → K2SO3 + K2S + H2O Б) H2SO4 + Mg → MgSO4 + H2 В) CuCl2 + H2S → CuS + HCl |
1) и окислитель, и восстановитель 2) не проявляет окислительно-восстановительных свойств 3) только окислитель 4) только восстановитель |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №22
Установите соответствие между веществом и возможным электролитическим способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ |
|
А) фтор Б) кислород В) натрий Г) этан |
1) водного раствора фторида натрия 2) водного раствора сульфида натрия 3) расплава фторида натрия 4) водного раствора бромида натрия 5) водного раствора ацетата натрия |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №23
Установите соответствие между названием соли и средой её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ СОЛИ | СРЕДА РАСТВОРА |
|
А) пальмитат калия Б) карбонат натрия В) сульфат алюминия Г) нитрат рубидия |
1) кислая 2) нейтральная 3) щелочная |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №24
Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при повышении давления: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) C2H2(г) + 2H2(г) ⇄ C2H6(г) Б) 2NO(г) + Cl2(г) ⇄ 2NOCl(г) В) C2H5OH(г) ⇄ C2H4(г) + H2O(г) Г) ZnCl2(p-p) + H2O(ж) ⇄ Zn(OH)Cl(p-p) + HCl(p-p) |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №25
Установите соответствие между реагирующими веществами и признаком(-ами) протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВА | ПРИЗНАК(И) РЕАКЦИИ |
|
А) уксусная кислота и Zn Б) хлорид метиламмония и AgNO3 (р-р) В) пропановая кислота (р-р) и KОН (р-р) Г) бутандиол-1,2 и Cu(OH)2 |
1) растворение жёлтого осадка 2) выделение бесцветного газа 3) растворение осадка и появление синей окраски раствора 4) видимые признаки реакции отсутствуют 5) образование белого осадка |
Запишите в таблицу выбранные цифры под соответствующими буквами.
[adsp-pro-3]
Задание №26
Установите соответствие между названием мономера и формулой соответствующего ему полимера: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ МОНОМЕРА | ПОЛИМЕР |
|
А) стирол Б) этен В) изопрен |
1) (–CH2–CH2–)n 2) (–СН2–СН(С6Н5)–)n 3) (–СН2–СН=CH–CH2–)n 4) (–СН2–С(CН3)=CH–CH2–)n |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
Задание №27
Какую массу 17%-ного раствора хлорида аммония надо взять, чтобы при добавлении 10 г воды получить раствор с массовой долей соли 7%? (Запишите число с точностью до целых.)
Ответ:___________________ г.
Задание №28
Окисление диоксида серы протекает в соответствии с термохимическим уравнением
2SO2(г) + O2(г) = 2SO3(г) + 198 кДж.
Вычислите количество теплоты, которое выделится при окислении 268,8 л (н.у.) диоксида серы. (Запишите число с точностью до целых.)
Ответ:___________________ кДж.
Задание №29
Какая масса алюминия потребуется для восстановления 0,2 моль оксида железа(III)? (Запишите число с точностью до десятых.)
Ответ:___________________ г.
Не забудьте перенести все ответы в бланк ответов № 1 в соответствии с инструкцией по выполнению работы. Проверьте, чтобы каждый ответ был записан в строке с номером соответствующего задания.
Для выполнения заданий 30, 31 используйте следующий перечень веществ:
пероксид водорода, сульфид цинка, гидроксид калия, гидроксид хрома(III), сульфат аммония, хлорид бария. Допустимо использование водных растворов веществ.
Задание №30
Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием раствора жёлтого цвета. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
[adsp-pro-3]
Задание №31
Из предложенного перечня выберите два вещества, реакция ионного обмена между которыми приводит к образованию слабого основания. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Задание №32
Натрий растворили в воде. Образовавшееся газообразное вещество при нагревании пропустили через железную окалину. Получившееся простое вещество при нагревании растворили в необходимом количестве концентрированной серной кислоты, при этом образовался бесцветный газа с резким запахом. К полученному раствору добавили раствор карбоната калия. Напишите уравнения четырёх описанных реакций.
Задание №33
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций используйте структурные формулы органических веществ.
Задание №34
Через 640 г 20%-ного раствора сульфата меди(II) пропускали электрический ток до тех пор, пока на аноде не выделилось 13,44 л (н.у.) газа. К образовавшемуся раствору добавили 65 г цинка. Определите массовую долю сульфата цинка в полученном растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Задание №35
При сгорании органического вещества А массой 3,4 г получено 4,48 л (н.у.) углекислого газа и 1,8 г воды. Известно, что вещество А вступает в реакцию с раствором гидроксида лития при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит семь атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте возможную структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с раствором гидроксида лития при нагревании (используйте структурные формулы органических веществ).
Ответы к первой части пробного варианта №2
| № задания, ответ | № задания, ответ |
|
1) 13 |
16) 6164 |
[adsp-pro-3]
Ответы ко второй части пробного варианта №2
Задание 30
3H2O2 + 2Cr(OH)3 + 4KOH = 2K2CrO4 + 8H2O
2∙ | Cr+3 − 3ē → Cr+6
3∙ | 2O-1 + 2ē → 2O-2
Кислород в степени окисления –1 (или пероксид водорода) является окислителем;
хром в степени окисления +3 (или гидроксид хрома(III)) является восстановителем.
Задание 31
2KOH + (NH4)2SO4 = K2SO4 + 2NH3 · H2O
2K+ + 2OH– + 2NH4+ + SO42– = 2K+ + SO42– + 2NH3 · H2O
NH4+ + OH– = NH3 · H2O
Задание 32
1) 2Na + 2H2O = 2NaOH + H2↑
2) Fe3O4 + 4H2 = 3Fe + 4H2O (нагрев)
3) 2Fe + 6H2SO4(конц.) = Fe2(SO4)3 + 3SO2 + 6H2O (нагрев)
4) Fe2(SO4)3 + 3K2CO3 + 3H2O = 2Fe(OH)3 + 3CO2 + 3K2SO4
Задание 33
Задание 34
Через 640 г 20%-ного раствора сульфата меди(II) пропускали электрический ток до тех пор, пока на аноде не выделилось 13,44 л (н.у.) газа. К образовавшемуся раствору добавили 65 г цинка. Определите массовую долю сульфата цинка в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение:
Запишем уравнения протекающих реакций:
2CuSO4 + 2H2O = 2Cu↓ + 2H2SO4 + O2↑ (электролиз) (I)
2H2O = 2H2↑ + O2↑ (электролиз) (II)
Zn + H2SO4 = ZnSO4↓ + H2 (III)
Вычислим массу и количество вешества сульфата меди (II) в исходном растворе:
m(CuSO4) = 640 · 0,2 = 128 г;
n(CuSO4) = 128/160 = 0,8 моль.
Вычислим общее количество выделившегося кислорода:
n(O2) = 13,44/22,4 = 0,6 моль.
При пропускании электрического тока через водный раствор сульфата меди (II) выделяется кислород, причем электролизу могут подвергаться и раствор сульфата меди (II) (реакция I) и вода (реакция II). Вычислим количество вещества кислорода, выделившегося по реакциям (I) и (II):
nI(O2) = 0,5 · nI(CuSO4) = 0,4 моль;
nII(O2) = 0,6 – 0,4 = 0,2 моль.
Вычислим количество вещества и массу прореагировавшей по реакции (II) воды:
nII(H2O) = 2nII(O2) = 0,4 моль;
mII(H2O) = 0,4 · 18 = 7,2 г.
Тогда масса выделившегося по реакции (I) кислорода равна:
mI(O2) = 32 · 0,4 = 12,8 г.
Вычислим количество вещества цинка, добавленного в раствор:
n(Zn) = 65/65 = 1 моль.
Тогда количества веществ и массы, образовавшихся по реакции I:
nI(H2SO4) = n(CuSO4) = 0,8 моль;
n(Cu) = n(CuSO4) = 0,8 моль;
m(Cu) = 0,8 · 64 = 51,2 г.
Количество вещества и масса водорода, выделившегося по реакции (III):
nIII(H2) = n(H2SO4) = 0,8 моль;
mIII(H2) = 0,8 · 2 = 1,6 г.
Количество образовавшейся по реакции (I) серной кислоты и прореагировавшего сульфата меди (II) равны, и, следовательно, количество вещества и масса прореагировавшего цинка составляют:
n(Zn) = n(CuSO4) = 0,8 моль;
m(Zn) = 0,8 · 65 = 52 г.
По уравнению реакции (III):
n(ZnSO4) = n(Zn) = 0,8 моль;
m(ZnSO4) = 0,8 · 161 = 128,8 г.
Вычислим массу образовавшегося раствора и сульфата цинка:
m(р-ра) = m(р-ра CuSO4) + m(Zn) – mI(O2) – mIII(H2) – mII(H2O) = 640 + 52 – 12,8 – 51,2 – 1,6 – 7,2 = 619,2 г;
тогда массовая доля сульфата цинка составит:
ω(ZnSO4) = m(ZnSO4)/ m(р-ра) = 128,8/619,2 = 0,208, или 20,8%.
Задание 35
При сгорании органического вещества А массой 3,4 г получено 4,48 л (н.у.) углекислого газа и 1,8 г воды. Известно, что вещество А вступает в реакцию с раствором гидроксида лития при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит семь атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте возможную структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с раствором гидроксида лития при нагревании (используйте структурные формулы органических веществ).
Решение:
1) Вычислим количества вещества углекислого газа и воды, образующихся при сгорании вещества А и перейдем к количествам составляющих их элементов:
n(CO2) = V(CO2)/Vm = 4,48 л/22,4 = 0,2 моль;
следовательно, n(С) = n(CO2) = 0,2 моль,
m(C) = M(C) · n(С) = 12 г/моль · 0,2 моль = 2,4 г;
n(H2O) = m(H2O)/M(H2O) = 1,8 г/18 г/моль = 0,1 моль,
следовательно, n(H) = 2n(H2O) = 2 · 0,1 моль = 0,2 моль,
m(H) = M(H) · n(H) = 1 г/моль · 0,2 моль = 0,2 г.
Проверим, есть ли в соединении кислород:
m(O) = m(орг. в-ва) − m(C) − m(H) = 3,4 г – 2,4 г − 0,2 г = 0,8 г, следовательно,
n(O) = m(O)/M(O) = 0,8 г/16 г/моль = 0,05 моль.
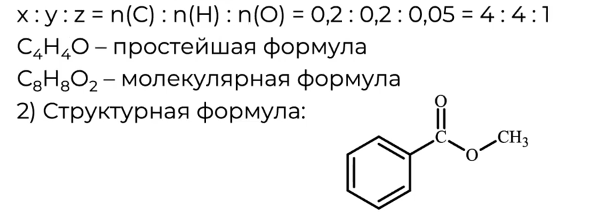
Найдем простейшую формулу данного соединения. Представим ее как CxHyOz:
x : y : z = 0,2 : 0,2 : 0,05 = 4 : 4 : 1.
Т.е. простейшая формула искомого соединения C4H4O.
Поскольку вещество А вступает в реакцию с раствором гидроксида лития при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит семь атомов углерода, т.е. ароматический фрагмент, следовательно, для нахождения истинной формулы индексы в простейшей формуле следует удвоить: C8H8O2.
2) Поскольку в кислотном остатке вещества А содержится 7 атомов углерода (остаток бензойной кислоты), следовательно, в спиртовом остатке содержится только 1 атом углерода (остаток метилового спирта). Структурная формула вещества А:
3) Запишем реакцию вещества А с раствором гидроксида лития при нагревании:
[adsp-pro-10]
Вариант с досрочного периода ЕГЭ 2022 по химии 11 класс с ответами и видео решением заданий, который был 21 марта 2022 года.
Скачать вариант №1 досрочного ЕГЭ 2022
Скачать вариант №2 досрочного ЕГЭ 2022
Другие тренировочные варианты ЕГЭ 2022 по химии
Вариант №1 с досрочного ЕГЭ 2022 по химии 11 класс:
Вариант №2 с досрочного ЕГЭ 2022 по химии 11 класс:
Разбор досрочного варианта ЕГЭ 2022 по химии:
Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) Al; 2) C; 3) P; 4) Na; 5) Se. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1)Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число s-электронов. Запишите в поле ответа номера выбранных элементов.
2)Из указанных в ряду химических элементов выберите три элемента, которые находятся в одном периоде. Расположите выбранные элементы в порядке возрастания их электроотрицательности. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3)Из числа указанных в ряду элементов выберите два элемента, которые могут проявлять степень окисления +3 в гидроксидах. Запишите в поле ответа номера выбранных элементов.
4)Из числа указанных в ряду элементов выберите два вещества ионного строения, которые содержат ковалентную неполярную связь.
- 1) пероксид натрия
- 2) фосфат калия
- 3) метилацетат
- 4) ацетиленид кальция
- 5) диэтиловый эфир
6)В одну из пробирок с порошком оксида цинка добавили слабый электролит X, а в другую – раствор вещества Y. В результате в первой пробирке наблюдали растворение твердого вещества. В пробирке с раствором вещества Y произошла реакция, которую описывает сокращенное ионное уравнение: ZnO + 2H+ = Zn2+ + H2O Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1) фтороводород
- 2) хлорид аммония
- 3) гидрокарбонат натрия
- 4) гидроксид натрия
- 5) иодоводород
11)Из предложенного перечня выберите два вещества, которые являются межклассовыми изомерами.
- 1) глицин
- 2) пропановая кислота
- 3) уксусная кислота
- 4) пропаналь
- 5) нитроэтан
12)Из предложенного перечня выберите все вещества, которые реагируют с водородом. 1) изопрен 2) стеариновая кислота 3) ацетон 4) изопропиловый спирт 5) олеиновая кислота Запишите в поле ответа номера выбранных веществ.
13)Из предложенного перечня выберите два вещества, которые реагируют с глюкозой. 1) гидроксид меди(II) 2) сульфат калия 3) метан 4) медь 5) аммиачный раствор оксида серебра(I) Запишите в поле ответа номера выбранных веществ.
17)Из предложенного перечня выберите все типы реакций, к которым можно отнести взаимодействие ацетальдегида и гидроксида меди (II). 1) гетерогенная 2) замещения 3) необратимая 4) окислительно-восстановительная 5) нейтрализация
18)Из предложенного перечня выберите все внешние воздействия, которые приводят к увеличению скорости реакции цинка с раствором гидроксида натрия. 1) увеличение концентрации гидроксида натрия 2) повышение давления 3) добавление воды 4) увеличение температуры 5) добавление индикатора.
26)Вычислите массу 7%-ого раствора соли, из которого нужно выпарить 13 г воды, для получения 18%-ного раствора. (Запишите число с точностью до целых.)
27)Горение угля протекает в соответствии с термохимическим уравнением реакции С(тв.) + О2(г) = СО2(г) + 393,3 кДж Определите объем кислорода, который израсходовался на сгорание угля, если выделилось 944 кДж тепла. (Запишите число точностью до целых.)
28)40 г оксида меди (II) растворили в избытке соляной кислоты. Рассчитайте массу образовавшейся соли, если практический выход реакции составляет 80% от теоретически возможного.
29)Из предложенного перечня веществ выберите вещества, между которыми может
протекать окислительно-восстановительная реакция, в которой в растворе образуется бурый
газ и окрашенный раствор. В ответе запишите уравнение только одной из возможных
окислительно-восстановительных реакций. Составьте электронный баланс, укажите
окислитель и восстановитель в этой реакции.
30)Из предложенного перечня веществ выберите кислую соль и вещество, между которыми может протекать реакция ионного обмена. Осадок в ходе реакции не образуется. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций.
31)Бромоводородную кислоту нейтрализовали карбонатом натрия. Полученный раствор подвергли электролизу. Газ, выделившийся на катоде, пропустили над нагретым оксидом меди(II). Получившееся твердое вещество растворили в концентрированной азотной кислоте.
33)К раствору сульфата железа (III) массой 632 г, содержащего в общей сложности 1,806∙1025 атомов кислорода, добавили 79 г сульфита калия. После окончания реакции к образовавшемуся раствору прилили 552 г 10%-ного раствора карбоната калия. Вычислите массовую долю сульфата калия в образовавшемся растворе. (Образованием кислых солей пренебречь.) В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)При взаимодействии соли первичного амина с нитратом серебра образуется органическое вещество А и бромид серебра. Вещество А содержит 25,93% азота, 7,41% водорода и 44,44% кислорода по массе. Напишите уравнение реакции получения вещества А из соли первичного амина и нитрата серебра. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества А и запишите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение реакции получения вещества А из соли первичного амина и нитрата серебра.
Задания с варианта №1
Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) S 2) Na 3) Al 4) O 5) Cr Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1)Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число s-электронов. Запишите номера выбранных элементов.
2)Из указанных в ряду химических элементов выберите три элемента-металла. Расположите выбранные элементы в порядке возрастания восстановительных свойств соответствующих им простых веществ. Запишите номера выбранных элементов в нужной последовательности.
3)Из числа указанных в ряду элементов выберите два элемента, которые в образованных ими анионах с общей формулой ЭOx 2− могут иметь одинаковую степень окисления. Запишите номера выбранных элементов.
4)Из предложенного перечня выберите два вещества, в каждом из которых присутствует как ионная, так и ковалентная неполярная химическая связь. 1) фосфат натрия 2) метилацетат 3) бензоат аммония 4) диэтиловый эфир 5) пероксид натрия
6)Даны две пробирки с порошком оксида цинка. В одну из них добавили раствор слабого электролита X, а в другую – раствор вещества Y. В результате в пробирке с веществом Х наблюдали растворение оксида цинка. В пробирке с веществом Y произошла реакция, которую описывает сокращённое ионное уравнение 2H+ + ZnO = Zn2+ + H2O Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) иодоводород 2) хлорид аммония 3) гидрокарбонат калия 4) гидроксид калия 5) фтороводород
11)Из предложенного перечня выберите два вещества, которые являются межклассовыми изомерами. 1) пропаналь 2) пропановая кислота 3) уксусная кислота 4) нитроэтан 5) глицин
12)Из предложенного перечня выберите все вещества, которые вступают в реакцию с водородом. 1) олеиновая кислота 2) стеариновая кислота 3) ацетон 4) изопрен 5) изопропиловый спирт
13)Из предложенного перечня выберите два вещества, с которыми взаимодействуют и глюкоза, и фруктоза. 1) гидроксид меди(II) 2) карбонат натрия 3) водород 4) медь 5) метан
17)Из предложенного перечня выберите все типы реакций, к которым можно отнести взаимодействие водорода с хлором. 1) гомогенная реакция 2) реакция замещения 3) экзотермическая реакция 4) реакция нейтрализации 5) окислительно-восстановительная реакция
18)Из предложенного перечня выберите схемы всех реакций, скорость которых увеличится при повышении концентрации кислорода. 1) O2(г) → O3(г) 2) O2(г) + N2(г) → NO(г) 3) CO(г) + O2(г) → CO2(г) 4) CuO(тв.) → Cu2O(тв.) + O2(г) 5) О2(г) + S(тв.) = SO2(г)
26)Сколько граммов воды следует добавить к 600 г 10%-ного раствора нитрата аммония, чтобы массовая доля соли стала равной 3%? (Запишите число с точностью до целых.)
27)Горение угля протекает в соответствии с термохимическим уравнением реакции C O CO 393,3 (тв.) 2(г) 2(г) += + кДж. Вычислите объём кислорода (н.у.), который необходим для получения 944 кДж теплоты. (Запишите число с точностью до целых.)
28)Вычислите объём газа (н.у.), полученного при прокаливании 175 г технического карбоната магния, в котором массовая доля некарбонатных примесей составляет 4% . (Запишите число с точностью до десятых.)
29)Из предложенного перечня выберите вещества, окислительновосстановительная реакция между которыми приводит к образованию бесцветного раствора, содержащего только кислоты. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите два вещества, реакция ионного обмена между которыми сопровождается выпадением осадка из окрашенного раствора. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
31)Бромоводородную кислоту нейтрализовали карбонатом натрия. Полученный раствор подвергли электролизу. Газ, выделившийся на катоде, пропустили при нагревании над оксидом меди(II). Образовавшееся твёрдое вещество поместили в концентрированный раствор азотной кислоты. Напишите уравнения четырёх описанных реакций.
33)К 632 г раствора сульфата железа(III), в котором в общей сложности содержится 1,806 · 1025 атомов кислорода, добавили 79 г сульфита калия. К образовавшемуся раствору прибавили 552 г 10%-ного раствора карбоната калия. Вычислите массовую долю сульфата калия в конечном растворе. (Возможностью образования кислых солей пренебречь.) В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
34)При взаимодействии соли первичного амина с нитратом серебра образуется органическое вещество А и бромид серебра. Вещество А содержит 25,93% азота, 7,41% водорода и 44,44% кислорода по массе. На основании данных условия задания: 1) проведите необходимые вычисления и установите молекулярную формулу органического вещества А; 2) составьте возможную структурную формулу вещества А, которая однозначно отражает порядок связи атомов; 3) напишите уравнение реакции получения вещества А взаимодействием соли первичного амина и нитрата серебра (используйте структурную формулу органического вещества).
ПОДЕЛИТЬСЯ МАТЕРИАЛОМ
ЕГЭ по химии 2020. Досрочная волна. Вариант 2
При выполнении заданий с кратким ответом впишите в поле для ответа цифру, которая соответствует номеру правильного ответа, или число, слово, последовательность букв (слов) или цифр. Ответ следует записывать без пробелов и каких-либо дополнительных символов. Дробную часть отделяйте от целой десятичной запятой. Единицы измерений писать не нужно.
Если вариант задан учителем, вы можете вписать или загрузить в систему ответы к заданиям с развернутым ответом. Учитель увидит результаты выполнения заданий с кратким ответом и сможет оценить загруженные ответы к заданиям с развернутым ответом. Выставленные учителем баллы отобразятся в вашей статистике.
Версия для печати и копирования в MS Word
1
Определите элементы, атомы которых в основном состоянии на внешнем энергетическом уровне содержат один неспаренный электрон. Запишите номера выбранных элементов.
Показать
Ответ:
2
Из указанных в ряду химических элементов выберите три элемента-неметалла. Расположите выбранные элементы в порядке уменьшения восстановительных свойств соответствующих им простых веществ. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Показать
Ответ:
3
Из указанных в ряду элементов выберите два элемента, степень окисления которых в высших оксидах равна +4. Запишите номера выбранных элементов.
Показать
Ответ:
4
Из предложенного перечня выберите два вещества, в которых присутствует ковалентная полярная связь.
1)
2)
3)
4)
5)
Запишите номера выбранных ответов.
Ответ:
5
Установите соответствие между формулой оксида и группой, к которой этот оксид принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ГРУППА ОКСИДОВ
1) несолеобразующие
2) кислотные
3) оснóвные
4) амфотерные
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
6
Из предложенного перечня выберите два оксида, которые реагируют с водой.
1) оксид бария
2) оксид азота(II)
3) оксид меди(II)
4) оксид железа(II)
5) оксид хрома(VI)
Запишите номера выбранных ответов.
Ответ:
7
Даны две пробирки с раствором гидросульфита натрия. В одну из них добавили раствор вещества X, а в другую — раствор вещества Y. В результате в пробирке с веществом Х выделился газ, а в пробирке с веществом Y выпал осадок. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
1) иодоводород
2) сульфат бария
3) гидроксид натрия
4) фосфат калия
5) гидроксид кальция
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Ответ:
8
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
9
Установите соответствие между исходным(и) веществом(-ами), вступающим(и) в реакцию, и продуктами этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ИСХОДНОЕ(-ЫЕ) ВЕЩЕСТВО(-А)
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
10
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
11
Установите соответствие между названием вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА
А) бензилацетат
Б) диэтиловый эфир
В) бутаналь
КЛАСС/ГРУППА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1) простые эфиры
2) сложные эфиры
3) фенолы
4) альдегиды
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
12
Из предложенного перечня выберите два вещества, для которых не характерна изомерия углеродного скелета.
1) 2-метилбутен-2
2) бутандиол-1,2
3) пропаналь
4) изобутан
5) бутин-1
Запишите номера выбранных ответов.
Ответ:
13
Из предложенного перечня выберите две реакции, в ходе которых может образоваться бензол.
1) дегидрирование циклопентана
2) дегидрирование циклогексана
3) гидрирование фенола
4) дегидрирование гептана
5) дегидрирование гексана
Запишите номера выбранных ответов.
Ответ:
14
Из предложенного перечня выберите все вещества, с которыми взаимодействуют и метанол, и этиленгликоль.
1) бромная вода
2) хлороводород
3) натрий
4) гидроксид меди(II)
5) толуол
Запишите номера выбранных ответов.
Ответ:
15
Из предложенного перечня выберите два вещества, которые подвергаются гидролизу.
1) сахароза
2) 2-аминопропановая кислота
3) глюкоза
4) триолеат глицерина
5) фруктоза
Запишите номера выбранных ответов.
Ответ:
16
Установите соответствие между химической реакцией и органическим веществом, преимущественно образующимся в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАКЦИЯ
А) тримеризация ацетилена
Б) гидрирование бутадиена-1,3
В) дегидрирование циклогексана
Г) гидратация бутена-1
ПРОДУКТ РЕАКЦИИ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Ответ:
17
Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
18
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами Х и Y.
1) 1,1-дибромпропан
2) пропилен
3) пропанол-1
4) 1,3-дибромпропан
5) циклопропан
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Ответ:
19
Из предложенного перечня выберите все реакции, которые являются реакциями присоединения.
1) хлорирование метана
2) гидролиз этилата натрия
3) окисление метанола оксидом меди(II)
4) гидрирование ацетальдегида
5) гидратация пропина
Запишите номера выбранных ответов.
Ответ:
20
Из предложенного перечня выберите все факторы, которые приводят к увеличению скорости химической реакции между оксидом меди(II) и соляной кислотой.
1) измельчение оксида меди(II)
2) понижение температуры
3) добавление воды
4) увеличение концентрации HCl
5) повышение давления в системе
Запишите номера выбранных ответов.
Ответ:
21
Установите соответствие между схемой реакции и свойством атома серы в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СВОЙСТВО АТОМА СЕРЫ
1) и окислитель, и восстановитель
2) не проявляет окислительно-восстановительных свойств
3) только окислитель
4) только восстановитель
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
22
Установите соответствие между веществом и возможным электролитическим способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) фтор
Б) кислород
В) натрий
Г) этан
ПОЛУЧЕНИЕМ ЭЛЕКТРОЛИЗОМ
1) водного раствора фторида натрия
2) водного раствора сульфида натрия
3) расплава фторида натрия
4) водного раствора бромида натрия
5) водного раствора ацетата натрия
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
23
Установите соответствие между названием соли и средой её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЛИ
А) пальмитат калия
Б) карбонат натрия
В) сульфат алюминия
Г) нитрат рубидия
СРЕДА РАСТВОРА
1) кислая
2) нейтральная
3) щелочная
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
24
Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при повышении давления: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
1) смещается в направлении прямой реакции
2) смещается в направлении обратной реакции
3) практически не смещается
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
25
Установите соответствие между реагирующими веществами и признаком(-ами) протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) уксусная кислота и
Б) хлорид метиламмония и
В) пропановая кислота (р-р) и
Г) бутандиол-1,2 и
ПРИЗНАК(И) РЕАКЦИИ
1) растворение жёлтого осадка
2) выделение бесцветного газа
3) растворение осадка и появление синей окраски раствора
4) видимые признаки реакции отсутствуют
5) образование белого осадка
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
26
Установите соответствие между названием мономера и формулой соответствующего ему полимера: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ МОНОМЕРА
А) стирол
Б) этен
В) изопрен
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Ответ:
27
Какую массу 17%-го раствора хлорида аммония надо взять, чтобы при добавлении 10 г воды получить раствор с массовой долей соли 7%? Запишите число с точностью до целых.
Ответ:
28
Окисление диоксида серы протекает в соответствии с термохимическим уравнением
Вычислите количество теплоты, которое выделится при окислении 268,8 л (н. у.) диоксида серы. Ответ дайте в кДж с точностью до целых.
Ответ:
29
Какая масса алюминия потребуется для восстановления 0,2 моль оксида железа(III)? Ответ дайте в граммах с точностью до десятых.
Ответ:
30
Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием раствора жёлтого цвета. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Показать
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
31
Из предложенного перечня выберите два вещества, реакция ионного обмена между которыми приводит к образованию слабого основания. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Показать
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
32
Натрий растворили в воде. Образовавшееся газообразное вещество при нагревании пропустили через железную окалину. Получившееся простое вещество при нагревании растворили в необходимом количестве концентрированной серной кислоты, при этом образовался бесцветный газа с резким запахом. К полученному раствору добавили раствор карбоната калия. Напишите уравнения четырёх описанных реакций.
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
33
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций используйте структурные формулы органических веществ.
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
34
Через 640 г 20%-ного раствора сульфата меди(II) пропускали электрический ток до тех пор, пока на аноде не выделилось 13,44 л (н. у.) газа. К образовавшемуся раствору добавили 65 г цинка. Определите массовую долю сульфата цинка в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
35
При сгорании органического вещества А массой 3,4 г получено 4,48 л (н. у.) углекислого газа и 1,8 г воды. Известно, что вещество А вступает в реакцию с раствором гидроксида лития при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит семь атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте возможную структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с раствором гидроксида лития при нагревании (используйте структурные формулы органических веществ).
Решения заданий с развернутым ответом не проверяются автоматически.
На следующей странице вам будет предложено проверить их самостоятельно.
Завершить тестирование, свериться с ответами, увидеть решения.
Официальный сайт ФИПИ опубликовал 2 варианта КИМ досрочного периода EГЭ-2020 по химии с ответами и критерии оценивания заданий с развёрнутым ответом.
Это дает дополнительную возможность участникам ознакомиться со структурой КИМ и уровнем сложности реальных заданий, оценить время выполнения каждого из заданий.
Досрочные варианты EГЭ 2020 по химии с ответами
→ вариант 1 | ответы | критерии
→ вариант 2 | ответы | критерии
Методические рекомендации ФИПИ обучающимся 11 классов по организации индивидуальной подготовки к ЕГЭ 2020 года по химии.
→ скачать
Каждый вариант экзаменационной работы ЕГЭ по химии построен по единому плану: работа состоит из двух частей, включающих в себя 35 заданий.
Часть 1 содержит 29 заданий с кратким ответом.
Из них 21 задание относится к базовому уровню сложности: 1–7, 10–15, 18–21, 26–29, и 8 заданий – к повышенному уровню сложности (их порядковые номера в варианте: 8, 9, 16, 17, 22–25).
Часть 2 содержит шесть заданий – с 30 по 35 – с развёрнутым ответом высокого уровня сложности.
Отнесение заданий к тому или иному уровню сложности определяется, прежде всего, отличиями в их направленности, количестве проверяемых элементов содержания и форме предъявления ответа.
Так, задания базового уровня сложности проверяют усвоение содержания всех разделов школьного курса химии:
— Теоретические основы химии (Строение вещества. Химическая реакция);
— Неорганические вещества;
— Органические вещества;
— Методы познания в химии;
— Химия и жизнь;
— Расчёты по химическим формулам и уравнениям реакций.
При этом каждое из заданий экзаменационного варианта ориентировано на проверку усвоения одного-двух элементов содержания, или группы близких по химической сути, но относящихся к одной теме элементов. Выполнение любого из них предполагает обязательный и тщательный анализ условия и применение знаний в системе.
Задания повышенного уровня сложности предусматривают выполнение большего числа мыслительных операций, действий по применению знаний в изменённой, нестандартной ситуации (например, для анализа сущности изученных типов реакций), а также сформированность умений систематизировать и обобщать полученные знания из тем, относящихся к одному содержательному блоку, например, «Неорганическая химия» или «Органическая химия».
Связанные страницы:
- 29.03.2022
Собираем варианты реального досрочного ЕГЭ 2022 по химии. ЕГЭ проходил 21 марта 2022 года.
- Все реальные варианты ЕГЭ 2022 по химии
На сегодня 01.05.2022 уже есть несколько вариантов с досрочного. С разборами, решениями и ответами. Сопровождаем варианты видеоразборами. Плюс открытый вариант от ФИПИ (в конце).
- Реальные варианты ЕГЭ 2022 по всем предметам
Досрочный вариант №1 от Тарасовой
Смотреть в PDF:
Или прямо сейчас: cкачать в pdf файле.
Досрочный вариант №2
Досрочный вариант №3
Досрочный вариант №4
Досрочный вариант №5
Досрочный ЕГЭ 2022 по химии вариант №6
Отдельно задания второй части досрочного
Смотреть в PDF:
Или прямо сейчас: cкачать в pdf файле.
Видеоразбор второй части досрочного реального ЕГЭ 2022 по химии
Смотреть в PDF:
Или прямо сейчас: cкачать в pdf файле.










































 3422
3422