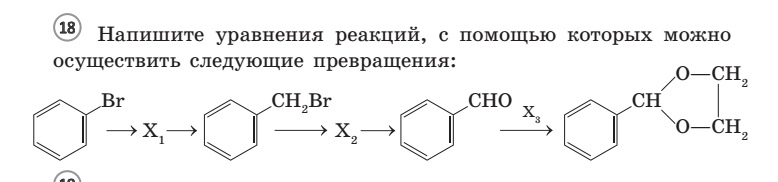
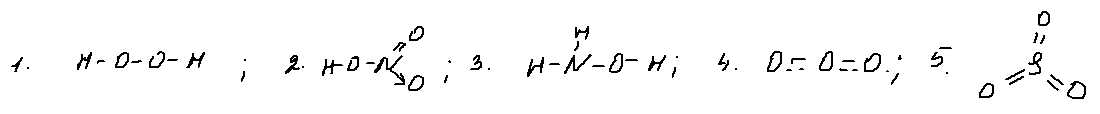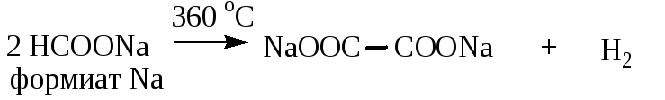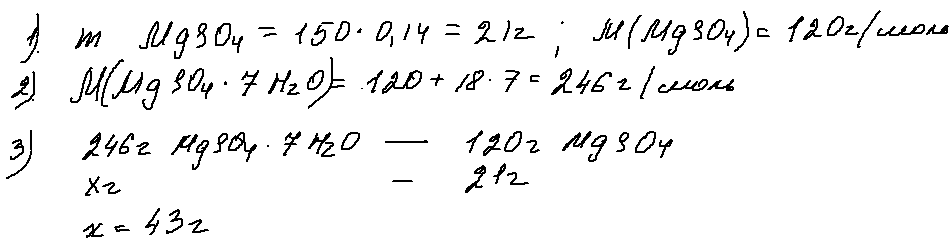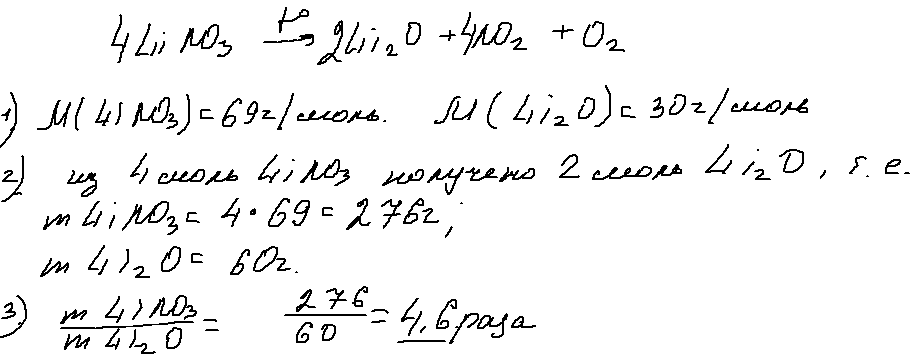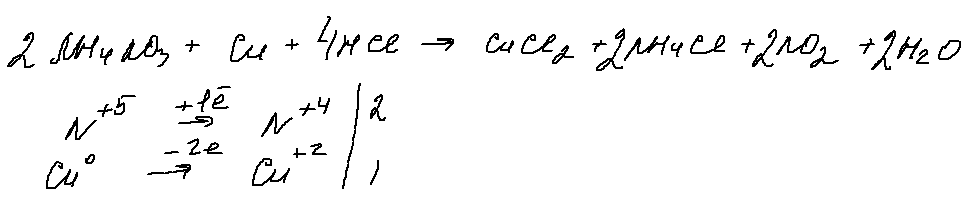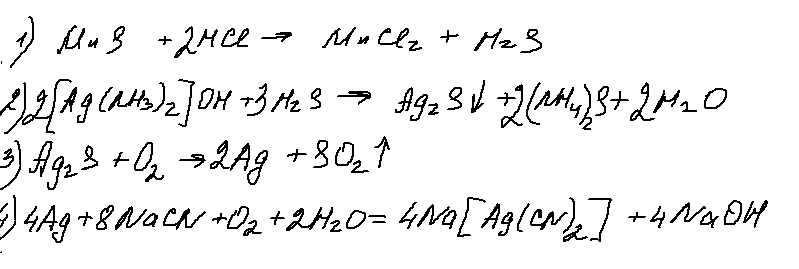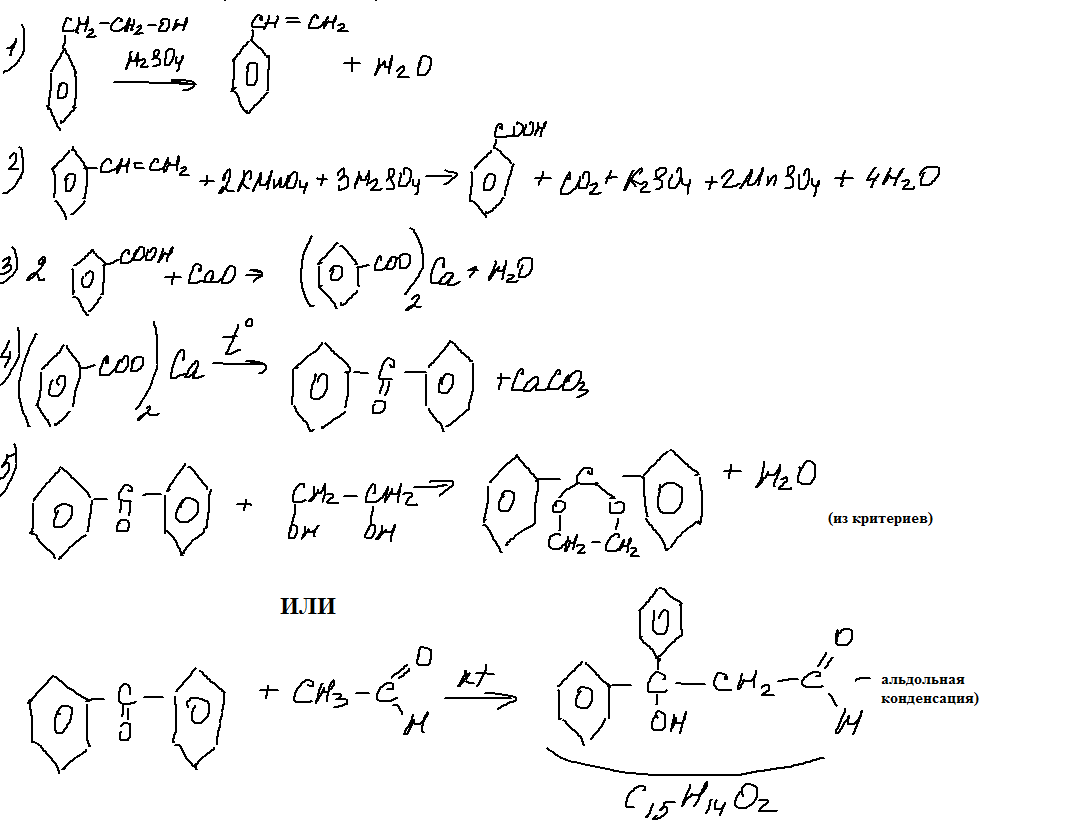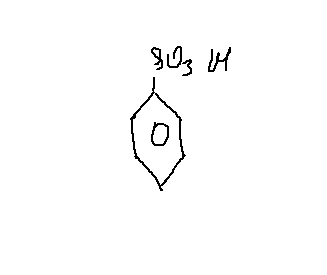Задания
Версия для печати и копирования в MS Word
Из предложенного перечня выберите два соединения, в которых между молекулами образуется водородная связь.
1) водорода
2) метанола
3) толуола
4) метаналя
5) метановой кислоты
Запишите в поле ответа номера выбранных соединений.
Спрятать решение
Решение.
Водородная связь образуется между молекулами веществ, в которых атом водорода связан с атомом с высокой электроотрицательностью (фтором, кислородом, азотом). Поэтому верный ответ — метанол и метановая (муравьиная) кислота.
Ответ: 25.
Источник: РЕШУ ЕГЭ
Подборка тренировочных вариантов ЕГЭ 2022 по химии с ответами.
Тренировочные варианты ЕГЭ 2022 по химии
| vk.com/repetitor_po_himii_i_biologii | |
| Вариант 1 | Ответы |
| vk.com/chem4you | |
| скачать вариант 1 | ответы |
| скачать вариант 2 | ответы |
| скачать вариант 3 | ответы |
| скачать вариант 4 | ответы |
| скачать вариант 5 | ответы |
| скачать вариант 6 | ответы |
| скачать вариант 7 | ответы |
| скачать вариант 8 | ответы |
| скачать вариант 9 | ответы |
| скачать вариант 10 | ответы |
| скачать вариант 11 | ответы |
| скачать вариант 12 | ответы |
| скачать вариант 13 | ответы |
| скачать вариант 14 | ответы |
| ЕГЭ 100 баллов (с решениями) | |
| Вариант 1 | скачать |
| Вариант 2 | скачать |
| Вариант 3 | скачать |
| Вариант 4 | скачать |
| Вариант 5 | скачать |
| Вариант 6 | скачать |
| Вариант 7 | скачать |
| Вариант 8 | скачать |
| Вариант 9 | скачать |
| Вариант 10 | скачать |
| Вариант 12 | скачать |
| Вариант 13 | скачать |
| Вариант 14 | скачать |
| Широкопояс (Источник: vk.com/naukadljatebja) | |
| Variant 1 | скачать |
| Variant 2 | скачать |
| Variant 3 | скачать |
| Variant 4 | скачать |
| Variant 5 | скачать |
| Variant 6 | скачать |
| Variant 7 | скачать |
| Variant 8 | скачать |
| Variant 9 | скачать |
| Variant 10 | скачать |
| Variant 11 | скачать |
| Variant 12 | скачать |
| Variant 13 | скачать |
| Variant 14 | скачать |
| Variant 15 | скачать |
| Variant 16 | скачать |
| Variant 17 | скачать |
| Variant 18 | скачать |
| Variant 19 | скачать |
| Variant 20 | скачать |
| Variant 21 | скачать |
| Variant 22 | скачать |
| Variant 23 | скачать |
| Variant 24 | скачать |
| Variant 25 | скачать |
| Variant 26 | скачать |
| Variant 27 | скачать |
| Variant 28 | скачать |
| Variant 29 | скачать |
| Variant 30 | скачать |
| vk.com/shkolkovo_him | |
| вариант 1 | разбор |
| вариант 2 | разбор |
| вариант 3 | ответы |
| вариант 4 | ответы |
| вариант 5 | ответы |
| vk.com/repetitor_korsakova | |
| variant 1 | otvet |
| variant 2 | otvet |
| variant 3 | otvet |
| СтатГрад | |
| Вариант 1-2 | критерии оценивания |
| Вариант 3-4 | критерии оценивания |
| vk.com/schoolzhukova | скачать вариант
ответы |
| → купить сборники типовых вариантов ЕГЭ по химии |
Варианты в соответствии с новой демоверсией ЕГЭ 2022 по химии.
→ Тренировочные варианты ЕГЭ 2021 по химии
Подходы к отбору содержания, разработке структуры КИМ ЕГЭ
Отбор содержания заданий КИМ для проведения ЕГЭ по химии в 2022 г. в целом осуществляют с сохранением установок, на основе которых формировались экзаменационные модели предыдущих лет. В числе этих установок наиболее важными с методической точки зрения являются следующие.
КИМ ориентированы на проверку усвоения системы знаний и умений, формирование которых предусмотрено действующими программами по химии для общеобразовательных организаций. Во ФГОС эта система знаний и умений представлена в виде требований к предметным результатам освоения учебного предмета. С данными требованиями соотносится уровень предъявления в КИМ проверяемых элементов содержания.
Экзаменационные варианты по химии содержат задания, различные по форме предъявления условия и виду требуемого ответа, по уровню сложности, а также по способам оценки их выполнения. Как и в предыдущие годы, задания КИМ ЕГЭ 2022 г. построены на материале основных разделов школьного курса химии: общей, неорганической и органической, изучение которых обеспечивает овладение учащимися системой химических знаний.
К числу главных составляющих этой системы относятся: ведущие понятия о химическом элементе, веществе и химической реакции; основные законы и теоретические положения химии; знания о системности и причинности
химических явлений, генезисе веществ, способах познания веществ.
В стандарте эта система знаний представлена в виде требований к уровню подготовке выпускников. В целях обеспечения возможности дифференцированной оценки учебных достижений выпускников КИМ ЕГЭ осуществляют проверку освоения основных образовательных программ по химии на трёх уровнях сложности: базовом, повышенном и высоком.
При разработке КИМ особое внимание было уделено реализации требований к конструированию заданий различного типа. Каждое задание строилось таким образом, чтобы его содержание соответствовало требованиям к уровню усвоения учебного материала и формируемым видам учебной деятельности.
Учебный материал, на основе которого строились задания, отбирался по признаку его значимости для общеобразовательной подготовки выпускников средней школы. Большое внимание при конструировании заданий было уделено усилению деятельностной и практико-ориентированной составляющей их содержания. Данный подход позволяет усилить дифференцирующую способность экзаменационной модели, так как требует от обучающихся последовательного выполнения нескольких мыслительных операций с опорой на понимание причинно- следственных связей, умений обобщать знания, применять ключевые понятия и др.
Смотрите также:
В результате выполнения задания 4 ЕГЭ по химии проверяются следующие требования/умения:
Коды проверяемых требований к уровню подготовки (по кодификатору):
Читать подробнее…
Коды проверяемых элементов содержания (по кодификатору):
Уровень сложности задания:
Максимальный балл за выполнение задания:
Примерное время выполнения задания выпускником, изучавшим предмет:
Межмолекулярные водородные связи в жидком состоянии характерны для:
1. водорода
2. воды
3. аммиака
4. ацетальдегида
5. изобутана
И ионные, и ковалентные химические связи имеются в веществе:
1. НСl
2. H2SO4
3. NaOH
4. NH4Br
5. С2Н5ОН
Ионные связи реализуются в каждом из двух веществ:
1. Аl2O3 и FeCl3
2. K2S и NaNO3
3. KNO2 и NO2
4. HF и НСl
5. NaBr и NH4F
Из предложенного перечня выберите два соединения, в которых присутствует ковалентная неполярная химическая связь.
1) N2
2) НСlO
3) NH4Br
4) НСl
5) Р4
Ковалентные неполярные химические связи имеются в веществах:
1. белый фосфор
2. ортофосфорная кислота
3. аммиак
4. этиловый спирт
5. сера ромбическая
Немолекулярное строение имеют:
1. гидроксид калия
2. аммиак
3. уксусная кислота
4. азотная кислота
5. графит
Из предложенного перечня выберите два соединения, в которых присутствует и ионная, и ковалентная химическая связь.
1. Ca(NO3)2
2. НСlO
3. NH4Br
4. НВг
5. H2SO4
Из предложенного перечня выберите два соединения, в которых присутствует ковалентная химическая связь.
1. H2
2. NH3
3. CaO
4. BaF2
5. NaBr
Из предложенного перечня выберите два соединения, между молекулами которых образуется водородная химическая связь.
1. H2
2. C2H5OH
3. C2H6
4. CH2=CH2
5. H2O
В сульфате калия присутствуют химические связи:
1. ионные
2. ковалентные неполярные
3. ковалентные полярные
4. водородные
5. металлические
5 новых пробных тренировочных вариантов по химии 11 класс в формате заданий решу ЕГЭ 2022 с ответами и решением по новой демоверсии из открытого банка ФИПИ со всем изменениями 2022 года, каждый вариант содержит 34 задания от 6 марта 2022 года.
Тренировочный вариант №26: задания, ответы
Тренировочный вариант №27: задания, ответы
Тренировочный вариант №28: задания, ответы
Тренировочный вариант №29: задания, ответы
Тренировочный вариант №30: задания, ответы
Решать тренировочный вариант №26 решу ЕГЭ 2022 по химии 11 класс:
1)Из указанных в ряду химических элементов выберите два элемента, атомы которых в основном состоянии содержат одинаковое число полностью заполненных подуровней. 1) Mg 2) Fe 3) N 4) Ar 5) Ca
Ответ: 25
2)Из указанных в ряду химических элементов выберите три элемента, электроотрицательность у которых выше, чем у марганца. Расположите выбранные элементы в порядке возрастания их высшей степени окисления. 1) Se 2) Ca 3) Br 4) K 5) As
Ответ: 513
3)Из предложенного перечня химических элементов выберите два элемента, которые могут иметь одинаковую степень окисления в образованных ими анионах с общей формулой ЭОх — . 1) C 2) N 3) I 4) Ti 5) K
Ответ: 23
4)Из предложенного перечня выберите два соединения, между структурными единицами которых имеют место водородные связи. 1) C2H6 2) CH3NH3Br 3) (CH3 )3N 4) (CH3 )2NH 5) CH3NH2
Ответ: 45
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) железной окалины; Б) несолеобразующего оксида; В) кислотного оксида.
Ответ: 927
6)К раствору сульфата меди(II) добавили раствор вещества Х, что привело к образованию раствора, практически не содержащего сильных электролитов. К раствору сульфата алюминия добавили избыток раствора вещества Y, что сопровождалось образованием осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) сероводород 2) фтороводород 3) гидроксид калия 4) гидроксид бария 5) гидрат аммиака
Ответ: 45
11)Из предложенного перечня соединений выберите два таких, любые изомеры которых не могут содержать π-связи. 1) 1,2,4-трихлорпентан 2) циклогексанол 3) бутилацетат 4) бутанол-2 5) 2-нитропропан
Ответ: 14
12)Из предложенного перечня выберите все типы реакций, характерных как для метилциклопропана, так и для 1,3-диметилциклогексана. 1) гидрирование 2) галогенирование 3) гидрогалогенирование 4) ароматизация 5) горение
Ответ: 25
13)Из предложенного перечня выберите два реагента, с которыми не взаимодействует водный раствор метиламина. 1) сульфид свинца 2) уксусная кислота 3) сульфат хрома(III) 4) гидроксид кальция 5) нитрат железа(III)
Ответ: 14
17)Из предложенного перечня выберите все реакции, которые при наличии или отсутствии катализатора протекают с образованием разных продуктов. 1) разложение карбоната магния 2) взаимодействие уксусной кислоты и метанола 3) взаимодействие аммиака и кислорода 4) горение фосфина 5) разложение хлората натрия
Ответ: 35
18)Из предложенного перечня внешних воздействий выберите все воздействия, которые приводят к увеличению скорости реакции CuSO4 ∙ 5H2O(тв.) → CuSO4(тв.) + 5H2O. 1) добавление кварцевого песка 2) охлаждение системы 3) повышение температуры 4) измельчение исходного вещества 5) добавление воды.
Ответ: 34
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л). 1) хлоруксусная кислота 2) перхлорат калия 3) хлорная кислота 4) метиламин
Ответ: 3124
23)В замкнутый реактор поместили смесь хлора, оксида азота(II) и нитрозилхлорида (NOCl), затем нагрели. В результате протекания обратимой реакции 2NO(г) + Cl2(г) ⇆ 2NOCl(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите исходную концентрацию нитрозилхлорида (X) и равновесную концентрацию оксида азота (II) (Y).
Ответ: 56
26)Какую массу 50%-ого раствора азотной кислоты (в граммах) нужно добавить к 200 г ее 5%-ного раствора, чтобы получить раствор с массовой долей азотной кислоты, равной 25%? (Запишите число с точностью до целых.)
Ответ: 160
27)Взаимодействие железа и серы описывается следующим термохимическим уравнением: Fe(тв.) + S(ромб.) = FeS(тв.) + Q. При образовании 8,8 г сульфида железа выделилось 10,01 кДж энергии. Вычислите количество энергии (в кДж), выделяющееся при расходовании 16,8 г железного порошка. (Запишите число с точностью до целых.)
Ответ: 30
28)Вычислите объем (в литрах) кислорода (н.у.), необходимый для полного обжига 8 г сульфида меди(I) при выходе реакции в 90%. (Запишите число с точностью до десятых.)
Ответ: 2,5
29)Из предложенного перечня выберите вещества, в результате окислительновосстановительной реакции, в которой атом-восстановитель меняет степень окисления с низшей на высшую. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите два вещества, при протекании ионного обмена между которыми образуется белый осадок, а в конечном растворе обнаруживаются гидроксид-ионы. Запишите молекулярное, полное и сокращенное ионные уравнения реакции с участием выбранных веществ.
31)К раствору сульфата хрома(III) добавили раствор сульфита цезия и наблюдали образование осадка и выделение бесцветного газа. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой, а осадок обработали раствором, содержащим пероксид водорода и гидроксид натрия, и нагрели. В полученный при этом желтый раствор добавили раствор серной кислоты. Напишите уравнения четырех описанных реакций.
33)Смесь алюминия и сульфида алюминия, в которой соотношение числа атомов алюминия к числу атомов серы равно 5:3, растворили в 500 г разбавленного раствора соляной кислоты. При этом все исходные вещества прореагировали полностью, и выделилось 1,11 г смеси газов. К этому раствору добавили 20%- ный раствор гидроксида натрия в минимальном количестве, необходимом для получения однородного раствора без осадка. Вычислите массовую долю хлорида натрия в конечном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин). В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)Неизвестное органическое соединение содержит 29,51% углерода, 8,20% водорода, 39,34% кислорода и азот. Определите молекулярную формулу данного соединения и установите его строение, если известно, что оно получается в одну стадию из неорганического соединения и вещества, молекулы которого не образуют водородные связи. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение взаимодействия этого вещества с избытком раствора гидроксида стронция (используйте структурные формулы органических веществ).
Решать тренировочный вариант №27 решу ЕГЭ 2022 по химии 11 класс:
1)Из указанных в ряду химических элементов выберите два элемента, атомы которых в основном состоянии содержат одинаковое число спаренных s-электронов и спаренных p-электронов: 1) O 2) F 3) Li 4) N 5) Mg
Ответ: 25
2)Из указанных в ряду химических элементов выберите три элемента, являющихся металлами. Расположите выбранные элементы в порядке усиления восстановительных свойств соответствующих им простых веществ. 1) I 2) Sn 3) Mg 4) Xe 5) Rb
Ответ: 235
3)Из предложенного перечня химических элементов выберите два элемента, находящихся в одном периоде Периодической системы Д.И. Менделеева, которые образуют водородные соединения, структурная единица которых содержит два атома водорода. 1) Ga 2) Se 3) Ca 4) Be 5) S
Ответ: 23
4)Из предложенного перечня выберите два соединения, все ковалентные связи в которых образованы только по обменному механизму. 1) метан 2) хлор 3) гексагидроксохромат(III) натрия 4) бромид аммония 5) азотная кислота
Ответ: 12
6)В пробирку с бесцветным раствором вещества Х добавили раствор ацетата свинца, наблюдая при этом образование желтого осадка. Во вторую пробирку с окрашенным раствором вещества Y добавили раствор ацетата бария, что также сопровождалось образованием желтого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) сероводород 2) хлорид аммония 3) хромат натрия 4) йодид калия 5) перманганат натрия
Ответ: 43
11)Из предложенного перечня соединений выберите два таких, изомеры которых могут содержать атомы углерода в sp2 -гибридизации. 1) диизопропиловый эфир 2) 1,3-диаминопропан 3) 1,2-диметилциклопропан 4) нитроэтан 5) метилпропиловый эфир
Ответ: 34
12)Из предложенного перечня выберите все углеводороды, из которых при окислении перманганатом калия в кислой среде можно получить соединение с двумя функциональными группами. 1) изопропилбензол 2) 1,2-диметилциклогексен-1 3) 1-метилциклогексен 4) 3,4-диметилгексен-3 5) 1,3-диметилбензол
Ответ: 235
13)Из предложенного перечня выберите два утверждения, справедливых и для анилина, и для глюкозы. 1) содержат атомы углерода в sp3 -гибридизации 2) являются твердыми веществами при обычных условиях 3) вступают в каталитическое гидрирование 4) содержат π-связи между атомами углерода 5) реагируют с бромом
Ответ: 35
17)Из предложенного перечня выберите все соединения, взаимодействие которых с концентрированным раствором азотной кислоты не относится к окислительно-восстановительным реакциям. 1) оксид серы(IV) 2) гидроксид меди(II) 3) фосфид алюминия 4) карбонат железа(II) 5) хромат калия
Ответ: 25
18)Из приведенного перечня выберите все реакции, скорость протекания которых при обычных условиях выше, чем скорость взаимодействия гранул цинка с 10%-ным водным раствором соляной кислоты. 1) взаимодействие таких же гранул цинка с 2%-ным водным раствором уксусной кислоты 2) взаимодействие раствора нитрата бария с раствором серной кислоты 3) взаимодействие цинковой пыли с 10%-ным водным раствором соляной кислоты 4) взаимодействие натрия с серой 5) взаимодействие железа с концентрированной серной кислотой
Ответ: 23
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов. 1) нитрат фениламмония (0,01 моль/л) 2) азотная кислота (0,02 моль/л) 3) гидроксид цезия (0,1 моль/л) 4) фенолят натрия (0,01 моль/л)
Ответ: 3412
23)В замкнутый реактор поместили смесь оксидов азота(II) и (IV) с кислородом, затем нагрели. В результате протекания обратимой реакции 2NO(г) + O2(г) ⇆ 2NO2(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите исходную концентрацию оксида азота(II) (X) и равновесную концентрацию оксида азота(IV) (Y).
Ответ: 15
26)В первой колбе, содержащей 100 мл воды, растворили 2,24 л хлороводорода, а во второй колбе, содержащей 200 г воды, растворили 672 мл хлороводорода. Рассчитайте массовую хлороводорода (в %) в растворе, полученном при смешении содержимого этих двух колб. (Запишите ответ с точностью до десятых.)
Ответ: 1,6
27)Обжиг сульфида свинца происходит согласно термохимическому уравнению: 2PbS(тв.) + 3O2 (г.) = 2PbO(тв.) + 2SO2 (г.) + Q При образовании 4,46 г оксида свинца(II) выделилось 8,32 кДж энергии. Рассчитайте объем израсходованного кислорода (л, н.у.), если при этом выделилось 374,4 кДж энергии. (Запишите число с точностью до десятых.)
Ответ: 30,2
28)Вычислите массу (в граммах) оксида азота(IV), который выделится при полном окислении 5,88 г сульфида хрома(III), содержащего 15% кварца, под действием концентрированной азотной кислоты. (Запишите число с точностью до десятых.)
Ответ: 27,6
29)Из предложенного перечня выберите вещества, в результате окислительновосстановительной реакции между которыми выделяется газ тяжелее кислорода и образуется окрашенный раствор. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите два вещества, при протекании реакции ионного обмена между которыми образуются сильный и слабый электролиты. Запишите молекулярное, полное и сокращенное ионные уравнения реакции с участием выбранных веществ.
31)Навеску манганата бария обработали большим избытком концентрированной соляной кислоты. К образовавшемуся раствору добавили сульфат аммония. Выпавший осадок отфильтровали, высушили и прокалили при высокой температуре с избытком кокса. Получившуюся соль внесли в избыток концентрированной азотной кислоты и нагревали до окончания реакции. Напишите уравнения четырех описанных реакций.
33)Смесь оксида железа(II) и оксида железа(III) массой 8,28 г растворили в 100 г концентрированной азотной кислоты, взятой в избытке. Полученный раствор упаривали до тех пор, пока твердый остаток не стал представлять собой одно единственное вещество. Данное вещество растворили в воде, а к образовавшемуся раствору добавили избыток раствора сульфида калия. При этом наблюдали образование осадка без выделения газа. Полученный в результате этого осадок отфильтровали и взвесили. Его масса оказалась равна 10,92 г. Определите массовую долю соли в растворе после растворения смеси оксидов. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)При сжигании 2,28 г неизвестного органического вещества А в качестве единственных продуктов сгорания были получены 1,8 г воды и 2,688 л углекислого газа (н.у.). Известно, что вещество А может быть синтезировано в одну стадию из углеводорода Б, который может реагировать с гидроксидом диамминсеребра в мольном соотношении 1:2 соответственно. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А; 2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение реакции получения вещества А из вещества Б. (используйте структурные формулы органических веществ).
Решать тренировочный вариант №28 решу ЕГЭ 2022 по химии 11 класс:
1)Из указанных в ряду химических элементов выберите два элемента, атомы которых в основном состоянии имеют одинаковую конфигурацию третьего энергетического уровня: 1) Ti 2) Mn 3) Zn 4) Cr 5) Sc
Ответ: 24
2)Из указанных в ряду химических элементов выберите три элемента, электроотрицательность которых больше, чем у брома, и расположите их в порядке убывания атомного радиуса. 1) As 2) N 3) Cl 4) Be 5) F
Ответ: 325
3)Из предложенного перечня химических элементов выберите два элемента, находящихся в одном периоде Периодической системы, которые могут иметь одинаковую степень окисления в образованных ими анионах с общей формулой ЭО2 — . 1) Se 2) Br 3) S 4) Al 5) Cl
Ответ: 45
4)Из предложенного перечня выберите два соединения, в частицах которых присутствуют все типы химической связи, что и в молекуле этандиовой кислоты. 1) трибромметан 2) пероксид водорода 3) пероксид бария 4) серная кислота 5) бутин-2
Ответ: 25
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) средней соли; Б) основного гидроксида; В) кислотного гидроксида.
Ответ: 579
6)В две пробирки поместили одинаковые медные пластинки. В первую пробирку добавили раствор вещества Х и наблюдали уменьшение массы пластинки после окончания реакции. Во вторую пробирку добавили раствор вещества Y и наблюдали увеличение массы пластинки после окончания процесса. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) соляная кислота 2) уксусная кислота 3) ацетат серебра 4) ацетат свинца 5) азотная кислота
Ответ: 53
11)Из предложенного перечня формул выберите две таких, которые не могут соответствовать веществам с двумя функциональными группами. 1) C3H7O2N 2) C2H2O2 3) C3H9N 4) C4H4O4 5) C6NH7
Ответ: 35
12)Из предложенного перечня выберите все соединения, которые могут вступить в реакцию замещения под действием металлического натрия и не являются газами. 1) метанол 2) пентен-1 3) гексин-1 4) пропин 5) гексадиин-1,3
Ответ: 135
13)Из предложенного списка соединений выберите те, при гидролизе которых можно получить трисахариды. 1) крахмал 2) нейлон 3) сахароза 4) рибоза 5) целлюлоза
Ответ: 15
17)Из предложенного перечня процессов выберите все такие, которые сопровождаются выделением газа. 1) взаимодействие ацетата железа(II) и азотной кислоты 2) сплавление карбоната калия и оксида цинка 3) нагревание раствора нитрата калия 4) взаимодействие раствора сульфата железа(III) и сернистого газа 5) взаимодействие горячих растворов нитрата аммония и нитрита бария
Ответ: 125
18)Из предложенного перечня реакций выберите все такие, скорость протекания которых можно ускорить как нагреванием, так и повышением давления в системе. 1) разложение карбоната магния 2) окисление алюминия хлором 3) обжиг пирита 4) взаимодействие натрия с водой 5) окисление сульфита натрия в растворе кислородом воздуха
Ответ: 235
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов. 1) хлорид калия (0,1 моль/л) 2) триметиламин (0,2 моль/л) 3) бромид метиламмония (0,01 моль/л) 4) этандиовая кислота (0,03 моль/л)
Ответ: 4312
23)В замкнутый реактор, содержащий катализатор, поместили пары метанола, смесь угарного газа и водорода, затем нагрели. В результате протекания обратимой реакции CO(г) + 2H2(г) ⇆ CH3OH(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите исходные концентрации водорода (X) и метанола (Y).
Ответ: 64
26)К раствору соляной кислоты с массовой долей воды 63,5% добавили 200 мл воды и получили раствор с массовой долей хлороводорода 18,25%. Вычислите массу исходного раствора. (Запишите ответ с точностью до целых.)
Ответ: 200
27)Взаимодействие лития с водой происходит согласно термохимическому уравнению: 2Li(тв) + 2H2O(ж) = 2LiOH(p-p) + Н2(г) + Q При образовании 12 г гидроксида лития выделилось 102 кДж энергии. Рассчитайте объем израсходованной воды в мл, если при этом выделилось 51 кДж энергии. (Запишите ответ с точностью до десятых.)
Ответ: 4,5
28)Рассчитайте массовую долю неона в смеси с углекислым газом общей массой 2400 мг, которая может прореагировать минимум с 61 г 5%-ного раствора силиката натрия. (Запишите ответ с точностью до десятых.)
Ответ: 8,3
29)Из предложенного перечня веществ выберите два таких, окислительновосстановительная реакция между которыми протекает с образованием белого осадка бинарного соединения. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня веществ выберите два таких, реакция ионного обмена между которыми протекает без видимых признаков. Запишите молекулярное, полное и сокращенное ионное уравнения данной реакции с участием выбранных веществ.
31)Навеску оксида фосфора(III) добавили к раствору, содержащему перекись водорода и гидроксид бария. Полученный раствор выпарили досуха, остаток прокалили с песком и углем. Выделившийся газ пропустили над оксидом железа(III), а образовавшийся при этом твердый остаток, представляющий собой одно вещество, растворили в разбавленной бромоводородной кислоте. При этом наблюдали образование желто-коричневого раствора. Напишите уравнения четырех описанных реакций.
33)Навеску смеси октагидрата гидроксида бария (Ba(OH)2 ·8H2O) и бромида цезия растворили в воде. В полученный раствор с массовой долей соли 5% пропустили углекислый газ до прекращения поглощения. Образовавшийся раствор разделили на две колбы. Первую колбу нагревали до окончания реакции. Во вторую колбу добавили 200 г 2%-ного раствора сульфата железа(III), причем реагенты прореагировали полностью. Вычислите массовую долю щелочи в исходном растворе, если известно, что отношение объемов газов, выделившихся из первой и второй колб, равно 7:6, а отношение масс бромида цезия во второй колбе и добавленного сульфата железа(III) равно 891:500. Растворимостью газов в воде пренебречь. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)При полном сгорании в кислороде неизвестного органического соединения массой 6,95 г в качестве единственных продуктов сгорания образовалось 7,84 л углекислого газа, 700 мг азота и 4,05 г воды. Определите молекулярную формулу данного соединения и установите его строение, если известно, что оно может быть получено в одну стадию из вещества с молекулярной формулой С7Н6О. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение взаимодействия этого вещества с нитрующей смесью.
Решать тренировочный вариант №29 решу ЕГЭ 2022 по химии 11 класс:
1)Из указанных в ряду химических элементов выберите два элемента, атомы которых в возбужденном состоянии не содержат валентных электронов на трех подуровнях: 1) I 2) Ge 3) S 4) Tl 5) Sb
Ответ: 24
2)Из указанных в ряду химических элементов выберите три элемента, находящихся в одном периоде Периодической системы, и расположите выбранные элементы в порядке увеличения числа валентных электронов на внешнем энергетическом уровне. 1) As 2) P 3) Mo 4) Cr 5) Ga
Ответ: 451
3)Из предложенного перечня химических элементов выберите два, у каждого из которых сумма степеней окисления в высшем оксиде и водородном соединении равна шести. 1) S 2) Ti 3) Cl 4) Te 5) Al
Ответ: 35
4)Из предложенного перечня суждений о строении и химических связях выберите два таких, которые справедливы и для тетрагидроксоалюмината натрия, и для хлорида аммония. 1) содержат неполярную ковалентную связь 2) имеют немолекулярное строение 3) образуют водородные связи 4) содержат ковалентную связь, образованную по донорно-акцепторному механизму 5) имеют атомную кристаллическую решетку
Ответ: 24
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) двухосновной кислоты; Б) сильной кислоты; В) амфотерного гидроксида.
Ответ: 352
6)Навески порошков Х и Y внесли в пробирки с избытком концентрированной серной кислотой. В случае вещества Х масса конечного раствора равна массе исходного. В случае вещества Y масса конечного раствора больше массы исходного. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) аморфный углерод 2) сера 3) фосфор 4) хлорид калия 5) медь
Ответ: 54
11)Из предложенного перечня формул выберите две таких, которые могут соответствовать веществам как с циклическим, так и с разветвленным строением. 1) C4H4 2) C3H6 3) C3H8 4) C5H8 5) C4H8
Ответ: 45
12)Из предложенного перечня веществ выберите все углеводороды, которые вступают в реакцию гидратации с образованием продуктов, способных вступать в реакцию гидрирования. 1) 1,2-дифенилэтен 2) стирол 3) толуол 4) бутин-1 5) циклогексен
Ответ: 124
13)Из предложенного перечня выберите два утверждения, справедливых для любого дисахарида, но несправедливых для любого дипептида. 1) относятся к слабым электролитам 2) реагируют с горячим раствором серной кислоты 3) при полном сгорании в кислороде образуют только два продукта 4) содержат σ-связи углерод-кислород 5) в продуктах их кислотного гидролиза нет органических солей
Ответ: 35
17)Из предложенного перечня процессов выберите все, протекание которых сопровождается выделением тепла. 1) разложение карбоната бария 2) взаимодействие растворов серной кислоты и гидроксида кальция 3) образование оксида азота(II) из простых веществ 4) образование йодоводорода из простых веществ 5) восстановление железа из железной окалины под действием алюминия
Ответ: 25
18)Из предложенного перечня реакций выберите все, которые при одинаковых условиях протекают быстрее взаимодействия гранулы цинка и 5%-ного раствора соляной кислоты. 1) магний + вода 2) медь + 10%-ный р-р HCl 3) магний(порошок) + 5%-ный р-р HCl 4) гидроксид натрия(р-р) + 5%-ный р-р СН3СООН 5) аммиак (р-р) + 1%-ный р-р H2SO4
Ответ: 345
21)Для смесей, приведённых в перечне, определите характер среды их водных растворов. 1) аммиак (0,09 моль/л) + метиламин (0,01 моль/л) 2) уксусная кислота (1%) + ацетон (1%) 3) гидроксид натрия (0,1 моль/л) + перхлорат калия (1 г/л) 4) нитрат калия (0,2 моль/л) + сахароза (1%)
Ответ: 2413
26)Газообразный аммиак объемом 4,48 л (н.у.) растворили в 166,6 мл воды, затем добавили его 10%-ный раствор, что привело к образованию раствора с массовой долей растворенного вещества 5%. Вычислите массу (в граммах) добавленного 10%-ного раствора аммиака. (Запишите ответ с точностью до целых.)
Ответ: 102
27)При расходовании 8 г кислорода на окисление оксида серы(IV) выделилось 71 кДж энергии. Вычислите количество энергии, выделяющееся при образовании 24 г оксида серы(VI). (Запишите ответ с точностью до десятых)
Ответ: 42,6
28)Рассчитайте выход кислорода, если при прокаливании навески перманганата натрия массой 7,1 г было получено 6,5 г твердого остатка. (Запишите ответ с точностью до целых)
Ответ: 75
29)Из предложенного перечня веществ выберите два таких, окислительновосстановительная реакция между которыми протекает с образованием четырех продуктов. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня веществ выберите два таких, в реакции ионного обмена между которыми образуется нерастворимый гидроксид. Запишите молекулярное, полное и сокращенное ионное уравнения данной реакции с участием выбранных веществ.
31)Навеску брома добавили в раствор, полученный при пропускании газа, выделившегося при взаимодействии серы и концентрированной серной кислоты, в недостаток гидроксида бария. При этом наблюдали обесцвечивание смеси и выпадение осадка. Полученный осадок отделили, высушили и прокалили при очень высокой температуре в потоке водорода. Напишите уравнения четырех описанных реакций.
33)Навеску нитрата меди(II) и нитрата серебра массой 31,55 г растворили в 400 мл воды и подвергли полученный раствор электролизу с инертными электродами. Процесс остановили, когда в растворе не осталось катионов металла. В ходе электролиза через цепь прошло 0,275 моль электронов. Вычислите массовую долю азотной кислоты в образовавшемся растворе, если известно, что в ходе процесса на катоде не выделялся газ. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)Неизвестное органическое соединение состоит из трех элементов и содержит 60% углерода по массе. При этом массовая доля кислорода в 4 раза больше, чем водорода. Известно, что данное соединение при гидролизе дает единственный продукт, обладающий линейным строением. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение взаимодействия этого вещества с гидроксидом калия.
Решать тренировочный вариант №30 решу ЕГЭ 2022 по химии 11 класс:
1)Из указанных в ряду химических элементов выберите два элемента, число валентных электронов у которых совпадает с числом полностью заполненных подуровней: 1) S 2) Al 3) Br 4) Fe 5) Si
Ответ: 35
2)Из предложенного перечня выберите три элемента, неспособных образовывать оксиды. Расположите выбранные элементы в порядке уменьшения атомного радиуса. 1) He 2) F 3) N 4) B 5) Kr
Ответ: 521
3)Из предложенного перечня химических элементов выберите два таких, которые могут иметь одинаковые степени окисления в образованных ими анионах с общей формулой ЭОх — . 1) Se 2) Fe 3) Cs 4) Cr 5) Sr
Ответ: 24
4)Из предложенного перечня выберите два соединения, имеющих немолекулярное строение, ковалентные связи в которых образованы только по обменному механизму. 1) нитрат диметиламмония 2) пероксид стронция 3) фторид аммония 4) силан 5) оксид кремния(IV)
Ответ: 25
6)При пропускании сероводорода через пробирку с раствором вещества Х наблюдали образование осадка, растворимого в горячем растворе щелочи. При пропускании сероводорода в пробирку с раствором вещества Y наблюдали образование осадка, нерастворимого в щелочах и концентрированной соляной кислоте. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) нитрат алюминия 2) хлорид цинка 3) ацетат серебра 4) сульфат марганца 5) бромид железа(III)
Ответ: 53
11)Из предложенного перечня формул выберите две таких, которые не могут соответствовать веществам с двумя π-связями в молекуле. 1) C6H11N 2) C5H12O 3) C5H8 4) C3H6O3 5) C3H4O4
Ответ: 24
12)Из предложенного перечня выберите все углеводороды, из которых можно в одну стадию получить дикарбоновую кислоту или ее соль. 1) циклопентен 2) 1,4-диметилбензол 3) бутен-2 4) бензол 5) ацетилен
Ответ: 125
13)Из предложенного перечня выберите два реагента, с которыми реагирует триолеин, но не реагирует сахароза. 1) серная кислота (1%-ный р-р) 2) гидроксид меди(II) 3) бромная вода 4) водород 5) анилин
Ответ: 34
17)Из предложенного перечня реакции выберите все, относящиеся к окислительно-восстановительным и в результате протекания которых образуется простое вещество. 1) взаимодействие хлорида железа(III) и сульфида натрия 2) разложение дихромата аммония при сильном нагревании 3) взаимодействие твердого хлорида аммония и концентрированной серной кислоты 4) взаимодействие горячих растворов сульфата аммония и нитрита калия 5) взаимодействие растворов сульфата меди(II) и йодида калия.
Ответ: 1245
18)Из предложенного перечня реакций выберите все, которые можно замедлить как охлаждением, так и увеличением объема реакционного сосуда. 1) окисление меди азотной кислотой 2) взаимодействие сероводорода и сернистого газа 3) нитрование бензола 4) электролиз раствора хлорида калия 5) нитрование этана.
Ответ: 25
21)Для смесей, приведённых в перечне, определите характер среды их водных растворов. 1) фенол (0,1%) + изопропанол (0,2%) 2) муравьиная кислота (10 г/л) + хлороводород (1%) 3) фосфат натрия (0,01 моль/л) + карбонат калия (1 г/л) 4) гидроксид бария (0,1 моль/л) + сахароза (10 г/л)
Ответ: 1232
23)В замкнутый реактор, содержащий катализатор, поместили смесь паров метанола, водорода и угарного газа, затем нагрели. В результате протекания обратимой реакции СO(г) + 2Н2(г) ⇆ СН3ОН(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите равновесные концентрации водорода (X) и метанола (Y).
Ответ: 54
26)В результате упаривания 200 г 10%-ного раствора нитрата калия масса раствора уменьшилась на 15%. Какую массу 25%-ного раствора нитрата калия (в граммах) необходимо добавить к полученному в результате упаривания раствору для получения раствора с массовой долей соли равной 20%? (Запишите число с точностью до целых).
Ответ: 280
27)При нейтрализации 49 г неизвестной кислоты раствором щелочи при определенных условиях выделяется 48 кДж теплоты. Вычислите количество теплоты, выделяющееся при нейтрализации 9,8 г данной кислоты в тех же условиях. (Запишите ответ с точностью до десятых).
Ответ: 9,6
28)Вычислите минимальную массу (в граммах) порошка технического алюминия (массовая доля примеси 3%), необходимую для полного восстановления в щелочном растворе 1,515 г нитрата калия. Считать, что реакция протекает с выходом 85%. (Запишите число с точностью до сотых.)
Ответ: 1,31
29)Из предложенного перечня веществ выберите такие, окислительновосстановительная реакция между которыми протекает с образованием нерастворимого в воде соединения желтого цвета. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня веществ выберите два таких, реакция ионного обмена между которыми может сопровождаться образованием раствора, практически не содержащего сильных электролитов. Запишите молекулярное, полное и сокращенное ионное уравнения данной реакции с участием выбранных веществ.
31)Сернистый газ пропустили через трубку с пероксидом натрия. Содержимое трубки растворили в воде с образованием нейтрального раствора, который подвергли электролизу. Образовавшийся раствор нагрели до кипения и внесли последовательно навеску питьевой соды, затем сульфат алюминия. Напишите уравнения четырех описанных реакций.
33)В стакан с 26%-ным раствором хлорида железа(III) внесли навеску железной стружки и нагревали некоторое время. В момент, когда количество ионов Fe2+ стало равно 0,24 моль, остаток стружки отделили от раствора магнитной сепарацией. В образовавшийся раствор пропустили газообразный хлор до момента, когда отношение количеств ионов Fe2+ и Fe3+ стало равно 1:4. Отделенную ранее железную стружку смешали с дополнительным количеством железа и внесли в полученный раствор. После образования однородного раствора без осадка добавили 260 г раствора сульфида калия. Образовавшийся при этом осадок представлял собой единственное соединение, а раствор над осадком имел нейтральную среду. Вычислите массовую долю воды в конечном растворе, если известно, что всего в ходе эксперимента использовали 13,44 г железной стружки. Испарением воды в ходе всех процессов пренебречь. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
34)При полном сгорании неизвестного органического соединения А массой 1,98 г образовалось 2,016 л углекислого газа (н.у.) и 1,62 г воды. Известно, что в молекуле данного соединения все атомы углерода находятся в состоянии sp3 -гибридизации, а также то, что молекула вещества А содержит в своем составе в два раз больше атомов углерода, чем молекула вещества Б — продукта окисления некоторого алкена раствором перманганата калия. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение получения А из вещества Б.
Другие тренировочные варианты ЕГЭ 2022 по химии 11 класс
ПОДЕЛИТЬСЯ МАТЕРИАЛОМ
Елена Шаврак. ЕГЭ по химии: новые упражнения и цепочки превращений. вопрос — хим. связь.. вопрос.
Елена Шаврак
ЕГЭ по химии: новые упражнения и цепочки превращений
Здравствуйте, уважаемые читатели!
Сегодня я хочу рассмотреть некоторые задания из нового СтатГрадовского пробника от 3 марта 2021 года. Причина — подобные упражнения ранее мне не встречались ни в одном из пробников и пособий за последние 8 лет. Про себя я данный факт обозначила как : «СтатГрад расширяет границы», причем это расширение носит как экстенсивный, так и интенсивный характер.
Итак, по порядку. Начинаю с заданий 1 варианта.
1. 4 вопрос — хим. связь.
Для выполнения этого задания запишем структурные формулы всех веществ (не учитываю валентные углы):
Только одинарные ковалентные связи есть в молекуле пероксида водорода (1) и гидроксиламина (3).
Новизна этого задания, скорее, экстенсивного характера. Т.е., несмотря на то, что ранее подобная формулировка 4 задания не встречалась в пробниках (мое субъективное мнение), для его выполнения вполне достаточно школьной базы.
2. 7 вопрос.
Для выполнения этого задания необходимо знать, что соединения меди могут выпадать в осадок при добавлении растворов трех реагентов из предложенного списка, а именно: аммиака, сероводорода и карбоната калия. Но в избытке аммиака осадок растворится вследствие образования аммиакатного комплекса меди. Одновременное образование осадка и газа — это маркерный признак совместного (или смешанного) гидролиза, протекающего при смешении растворов соли меди и карбоната. Т.о., ответы — Х- H2S, Y- K2CO3.
Новизна этого задания также условная. Аммиакатные комплексы меди (и цинка) в 7 задании встречались и ранее, но ОЧЕНЬ редко.
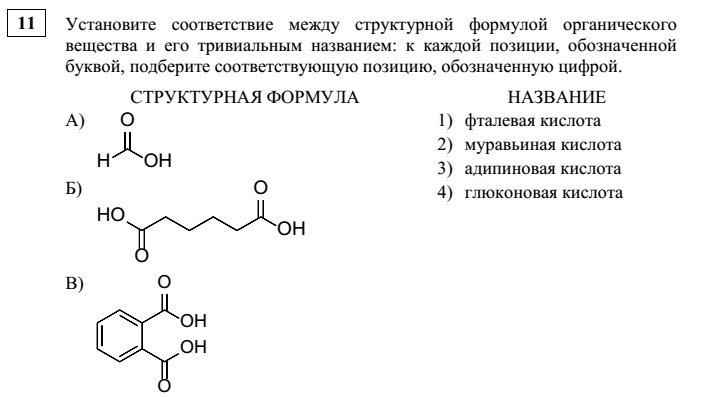
3. 11 вопрос
Практически во всех последних СтатГрадовских пробниках в 11 задании используются «скелетные» формулы органических веществ. Выскажу свою точку зрения: это хорошо, поскольку, опять же, — расширяет границы восприятия материала. Надеюсь, что, со временем, в формулировках будут использоваться классические скелетные формулы, в которых клинообразными линиями обозначаются связи, направленные вверх относительно плоскости, т.е. к наблюдателю, пунктирными линиями обозначаются связи, направленные вниз относительно плоскости, т.е. от наблюдателя.
Ответы — 231
Новизна этого задания невелика. Пожалуй, при подготовке стоит обратить внимание на отработку тривиальных названий органических соединений.
4. 17 вопрос
В 17 задании, посвященном кислородсодержащей органике, приведена практически не упоминавшаяся в пробниках и сборниках тестов реакция термического превращения формиата натрия до оксалата натрия:
Мой личный вывод: спасибо СтатГраду за актуализацию ранее невостребованной информации, относящейся, в принципе, к школьной программе (способы получения дикарбоновых кислот).
5. 27 задача.
Задача 27, в который уже раз в этом году, обращает внимание к кристаллогидратам. Решать ее можно разными способами — через моли, через пропорцию, правилом креста …
Ниже я привела один из вариантов решения., суть которого заключается в нахождении массы всей растворенной соли и последующем «заключении» ее в кристаллогидрат:
Ответ — 43 г.
6. 29 задача.
Задача 29 обращает на себя внимание формулировкой (полное отсутствие числовых данных) и «незамыленной» химией — разложением нитрата активного металла. Опять же и эту задачу можно решать несколькими способами. Ниже привожу один из них:
7. 30 задание.
«Грозное» 30 задание, в котором, при ближайшем рассмотрении, можно выделить только 1 окислитель (нитрат аммония), 1 восстановитель — медь. Для перевода нитрата в азотную кислоту, с которой будет реагировать медь, добавим соляную кислоту. Берем ее концентрированной, чтобы в результате реакции обмена получить концентрированную азотную кислоту (кстати, можно проводить реакцию с выделением оксида азота (2), для этого нужно взять разбавленную соляную кислоту). В результате получаем:
Данная реакция напоминает мне качественную реакцию на нитраты, в которой к нитрату добавляют медь и концентрированную серную кислоту и наблюдают образование бурого газа.
8. 32 задание.
Хорошее задание, ничего не скажешь! Реакция 2 — разрушение комплекса, достаточно типовая. Реакция 3 — окисление сульфида серебра (а еще и ртути) идет с образованием только одного оксида. Реакция достаточно редкая, но встречалась. А вот 4 реакция — меня лично ввела в ступор. Возможно ошибаюсь, но неоднократно от представителей ФИПИ на вебинарах звучало, что на ЕГЭ будут только гидроксокомплексы цинка и алюминия. Понемногу «пробрались» аммиакаты. Но цианидных комплексов до сих пор еще не было. Искренний респект составителям!
9. 33 цепочка.
Вот это задание заслуживает самого пристального внимания. С одной стороны — бруттоформулы в задании- это очень хорошо, поскольку способствует более глубокому проникновению в суть задания. С другой стороны- последняя реакция, представляющая собой введение ацетальной защиты (по мнению авторов пробника). Я бы написала здесь и альдольную конденсацию дифенилкетона с ацетальдегидом. Но этого не дают в школьной программе (или я ошибаюсь?).
Необходимо отметить, что еще одну цепочку с ацетальной защитой я нашла в сборнике
10. 34 задача.
Данную задачу в этой статье отрешивать не буду. Сделаю это позже. Но бросается в глаза новое усложнение — нахождение состава газовой смеси по плотности. Практически не встречалось такого в задачах , предназначенных для подготовки к ЕГЭ.
11. 35 задача.
Одно из заданий, которое мне очень понравилось в этом пробнике.
Решение
1. Схема реакции сгорания неизвестного соединения:
CxHySzOk+O2=CO2+H2O+SO2
2. Найдем молекулярную формулу неизвестного соединения:
а) n(C)=n(CO2)= 20,16/22,4=0,9 моль,
n(Н)=2n(Н2О)= 2*8,1 /18=0,9 моль,
n(S)=n(SO2)= 3,36/22,4=0,15 моль,
n(O)=(23,7-(12*0,9+0,9+32*0,15))/16=0,45 моль
б) Молекулярная формула неизвестного вещества-: С6Н6SO3. Это — бензолсульфокислота
3. Структурная формула —
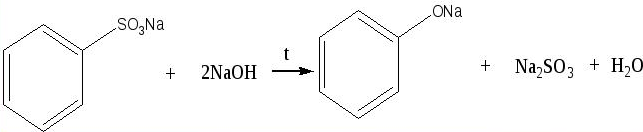
4. Уравнение реакции, происходящей при сплавлении бензолсульфоната натрия со щелочью:
Рассмотрела только первый вариант пробника, но и в нем много информации к размышлению. Резюмирую:
1. Реальный ЕГЭ по сложности раньше не всегда корреллировал со статградовскими пробниками, поэтому не факт, что задания уровня сложности рассмотренных 32-34 стоит ожидать на реальном экзамене.
2. Задания данного пробника актуализируют изучаемую, но относительно редко используемую информацию об органических и неорганических веществах (особенно — задания 4, 7, 11, 17, 27, 29, 35).
3. Для выполнения заданий 32 и 33 необходимо обладать информацией, адекватное усвоение которой возможно только в ходе изучения вузовских курса неорганической и органической химий (подчеркиваю, что это — мое субъективное мнение).
4. Великолепна задача 35. Впервые в пробниках ЕГЭ: серосодержащая органика и практически не используемый ранее при составлении заданий способ получения фенола.
5. В целом — еще раз — респект составителям, но — детей жалко. Без хорошего репетитора до уровня такого пробника не подняться.
Всего доброго!
Тренировочный вариант по химии №7, №8 решу ЕГЭ 2023. Новые тренировочные варианты Добротина ЕГЭ 2023 по химии для 11 класса вариант 7 и вариант 8 в формате реального экзамена ЕГЭ, пробные варианты с ответами и решением для подготовки ФИПИ.
Скачать вариант №7
Скачать вариант №8
Вариант №7 Добротин ЕГЭ 2023 по химии с ответами
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- 1) O
- 2) Si
- 3) Cr
- 4) Sc
- 5) Cl
1. Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат ровно один неспаренный электрон.
2. Из указанных в ряду химических элементов выберите три элемента, которые в находятся в малых периодах. Расположите выбранные элементы в порядке увеличения электроотрицательности. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3. Из числа указанных в ряду элементов выберите два элемента, у каждого из которых значение высшей степени окисления численно совпадает со значением низшей степени окисления.
4. Из предложенного перечня выберите два вещества, для каждого из которых характерны высокая температура плавления, хорошая растворимость в воде и наличие ковалентной полярной связи.
- 1) SiO2
- 2) HCl
- 3) NaOH
- 4) KBr
- 5) Na2SO4
5. Среди предложенных веществ, расположенных в пронумерованных ячейках, выберите:
- А) соль серной кислоты,
- Б) щелочь,
- В) комплексную соль
6. К одной из пробирок с раствором гидроксида кальция добавили раствор соли X, а через другую пропустили газ Y. В результате в каждой из пробирок наблюдалось выпадение белого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1) CuCl2
- 2) NH3
- 3) FeCl3
- 4) CO2
- 5) NaHCO3
11. Из предложенного перечня выберите два вещества, в которых все атомы углерода находятся в состоянии sp2-гибридизации.
- 1) щавелевая кислота
- 2) толуол
- 3) стирол
- 4) ацетон
- 5) пропен
12. Из предложенного перечня выберите все вещества, из которых в одну стадию может быть получен алкин.
- 1) карбид кальция
- 2) 2,3-дибром-2,3-диметилбутан
- 3) бензол
- 4) хлорэтен
- 5) этиленгликоль
13. Из предложенного перечня выберите два продукта гидролиза метилового эфира аминоуксусной кислоты в солянокислой среде.
- 1) CH3Cl
- 2) CH3OH
- 3) CH3COONH4
- 4) NH2CH2COOH
- 5) [HOOC–CH2–NH3]Cl
17. Из предложенного перечня выберите все вещества, термическое разложение которых относится к окислительно-восстановительным реакциям:
- 1) гидрокарбонат калия
- 2) перманганат калия
- 3) карбонат магния
- 4) нитрит аммония
- 5) гидроксид алюминия
18. Из предложенного перечня выберите все воздействия, которые не влияют на скорость реакции, протекающей по схеме: Cuଶା + Zn = Cu + Z
- 1) понижение давления
- 2) понижение температуры
- 3) уменьшение концентрации ионов цинка
- 4) добавление металлической меди
- 5) добавление воды в реакционную колбу
23. В реактор постоянного объема поместили оксид серы (IV) и оксид серы (VI). В результате протекания обратимой реакции 2SO3 (г) ⇆ O2 (г) + 2SO2 (г) в системе установилось химическое равновесие. Исходная концентрация оксида серы (VI) равна 2 моль/л, а равновесные концентрации кислорода и оксида серы (IV) равны 0,5 моль/л и 1,8 моль/л соответственно. Определите равновесную концентрацию оксида серы (VI) (X) и исходную концентрацию оксида серы (IV) (Y). Выберите из списка номера правильных ответов:
- 1) 0,2 моль/л
- 2) 0,5 моль/л
- 3) 0,8 моль/л
- 4) 1,0 моль/л
- 5) 1,3 моль/л
- 6) 2,8 моль/л
26. Вычислите массу соли (в граммах), которую нужно добавить к 182 г 5% раствора этой же соли, чтобы получить 13,55%-ный раствор. Ответ запишите с точность до целых.
27. При сгорании 8,4 г этилена выделяется 423,3 кДж теплоты. Вычислите количество теплоты, которое выделится при сгорании 0,896 м3 (при н.у.) этилена. Ответ запишите с точностью до целых.
28. Вычислите массу угля, содержащего 4% негорючих примесей, необходимую для полного восстановления 116 г железной окалины. Примите, что в ходе реакции образуется угарный газ. Ответ дайте в граммах с точностью до целых.
29. Из предложенного перечня выберите два вещества, между которыми протекает окислительно-восстановительная реакция. В ходе этой реакции образуется белый осадок, а окислитель принимает один электрон (в расчете на один атом). Запишите уравнение реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30. Из предложенного перечня веществ выберите два вещества, принадлежащих к одинаковой группе веществ, между которыми протекает реакция ионного обмена. Раствор одного из реагентов окрашен. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с использованием выбранных веществ.
31. На концентрированную соляную кислоту подействовали бихроматом натрия. Образовавшееся при этом простое вещество прореагировало с кремнием при нагревании. Продукт реакции добавили к необходимому количеству раствора гидроксида калия. Через полученный раствор пропустили избыток углекислого газа и наблюдали образование осадка. Составьте уравнения четырех описанных реакций.
33. Для полного сжигания порции некоторого органического вещества Х необходимо 7,39 л (н. у.) кислорода, при этом образуется углекислый газ, 1,46 г хлороводорода и 1,8 г воды. Известно, что вещество Х может быть получено при взаимодействии углеводорода Y симметричного строения с избытком хлороводорода. На основании данных задачи:
- 1. Проведите необходимые вычисления и установите молекулярную формулу органического вещества Х;
- 2. Составьте структурную формулу вещества Х, которая однозначно отражает порядок связи атомов в его молекуле;
- 3. Напишите уравнение реакции вещества Y с подкисленным серной кислотой раствором перманганата калия, используя структурную формулу вещества.
34. 66,1 г смеси медного купороса (CuSO4 · 5H2O) и десятиводного сульфата натрия, содержащую 2,0408 · 1025 протонов, внесли в дистиллированную воду и получили раствор, в котором массовая концентрация ионов меди равна 4%. От этого раствора отобрали порцию массой 64 г и добавили к ней 3,92 г железных опилок. Вычислите массовые доли веществ в полученном растворе после окончания реакций.
Вариант №8 ЕГЭ 2023 по химии с ответами
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- 1) С
- 2) F
- 3) O
- 4) Sn
- 5) Ge
Задание 1. Определите, в атомах каких из указанных в ряду элементов общее число p-электронов не превышает общее число s-электронов.
Задание 2. Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одной группе. Расположите выбранные элементы в порядке уменьшения основных свойств соответствующих им высших оксидов. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Задание 3. Из числа указанных в ряду элементов выберите два элемента, высшая степень окисления которых численно не совпадает с номером группы.
Задание 4. Из предложенного перечня выберите два элемента, атомы которых образуют с водородом более длинную ковалентную связь по сравнению с остальными.
- 1) O
- 2) Se
- 3) I
- 4) F
- 5) Br
Задание 6. К одной из пробирок, содержащей раствор гидроксида натрия, добавили раствор вещества Х, а к другой – раствор соли Y. В результате в первой пробирке выделился газ с резким запахом, а во второй выпал белого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1) BaCl2
- 2) H2SO4
- 3) Ca(HCO3)2
- 4) K2S
- 5) NH4Cl
Задание 7. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 11. Из предложенного перечня веществ выберите два вещества, в молекулах которых содержится система сопряженных связей.
- 1) ацетилен
- 2) толуол
- 3) циклопентан
- 4) изопрен
- 5) пентадиен-1,4
Задание 12. Из предложенного перечня выберите все вещества, которые взаимодействуют с пропеновой кислотой, но не взаимодействуют с этиленгликолем.
- 1) водород
- 2) гидроксид меди (II)
- 3) метанол
- 4) бромная вода
- 5) гидрокарбонат калия
Задание 13. Из предложенного перечня выберите два вещества, которые не вступают в реакцию этерификации.
- 1) целлюлоза
- 2) фенилаланин
- 3) глюкоза
- 4) метиламин
- 5) анилин
Задание 14. Установите соответствие между органическими веществами и органическими продуктами их взаимодействия с подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 17. Выберите все пары веществ, между которыми протекает окислительновосстановительная реакция.
- 1) хромат калия и ацетат серебра
- 2) сероводород и бром ная вода
- 3) оксид азота (IV) и вода
- 4) оксид меди (II) и азотная кислота (конц.)
- 5) оксид меди (II) и иодоводород
Задание 18. Выберите все металлы, которые при комнатной температуре реагируют с водой со значительной скоростью:
- 1) Ca
- 2) Ag
- 3) Fe
- 4) Rb
- 5) Li
Задание 19. Установите соответствие между формулой иона и свойством, которое он может проявлять в окислительно-восстановительных реакциях: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 20. Установите соответствие между формулами солей и продуктами, которые выделятся на графитовом катоде при электролизе их водных растворов: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 23. В реактор постоянного объема поместили аммиак и нагрели его в присутствии катализатора. В результате протекания обратимой реакции в системе установилось химическое равновесие. Известно, что исходная концентрация аммиака равна 0,8 моль/л, а в равновесной смеси количество вещества аммиака составляет 60% от суммарного количества веществ газов. Определите равновесные концентрации азота (X) и водорода (Y). Выберите из списка номера правильных ответов:
- 1) 0,10 моль/л
- 2) 0,24 моль/л
- 3) 0,30 моль/л
- 4) 0,48 моль/л
- 5) 0,60 моль/л
- 6) 0,80 моль/л
Задание 26. К 400 г 12%-го раствора соли добавили раствор этой же соли и получили 520 г 18%-го раствора. Вычислите массовую долю соли в добавленном растворе. Ответ запишите с точностью до целых.
Задание 27. Вычислите тепловой эффект реакции 2CH3OH + 3O2 = 4H2O + 2CO2 + Q, если при сгорании некоторого количества метанола образовалось 63,84 л (н. у.) углекислого газа и выделилось 2069,1 кДж теплоты. Ответ запишите с точностью до целых.
Задание 28. В ходе спиртового брожения глюкозы массой 72 г получено 12,096 л (н. у.) углекислого газа. Вычислите долю выхода углекислого газа в процентах от теоретического. Ответ дайте в процентах с точностью до десятых.
Задание 29. Из предложенного перечня выберите вещества, между которыми в щелочной среде протекает окислительно-восстановительная реакция. В ходе этой реакции наблюдается образование раствора желтого цвета. Запишите уравнение реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Задание 30. Из предложенного перечня веществ выберите кислую соль и вещество, между которыми протекает реакция ионного обмена без видимых признаков. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с использованием выбранных веществ.
Задание 31. Серебро растворили в концентрированной азотной кислоте при нагревании. Выделившийся газ пропустили над нагретым цинком. Полученное твердое вещество обработали раствором гидроксида калия. Через полученный раствор пропустили избыток сероводорода и наблюдали выпадение осадка. Составьте уравнения четырех описанных реакций.
Задание 32.
Задание 33. При сгорании бескислородного органического вещества Х массой 31,79 г получено 7,62 л (н.у.) углекислого газа, 1,53 мл воды и бромоводород. Продукт гидролиза вещества Х в присутствии избытка щелочи содержит две функциональные группы, находящиеся на максимальном расстоянии друг от друга, и не взаимодействует с гидроксидом меди (II). На основании данных в задаче:
- 1. Проведите необходимые вычисления и установите молекулярную формулу органического вещества Х;
- 2. Составьте структурную формулу вещества Х, которая однозначно отражает порядок связи атомов в его молекуле;
- 3. Напишите уравнение реакции гидролиза вещества Х в присутствии избытка гидроксида натрия, используя структурную формулу вещества.
Задание 34. 186,25 г 16%-го раствора хлорида калия подвергли электролизу (с инертными электродами). Процесс прекратили, когда на катоде выделилось 13,44 л (при н. у.) газа. Через оставшийся раствор пропустили сероводород, при этом в конечном растворе общее число атомов калия и серы оказалось равным 3,311 · 1023. Вычислите массовые доли веществ в конечном растворе.
Смотрите также на нашем сайте:
ЕГЭ по химии 11 класс 2023. Новый тренировочный вариант №5 — №221107 (задания и ответы)
Метки: 11 класс ЕГЭ химия
SuperEGE.ru
- 34
- 36
- 37
- 38
- 39
- 40
- 41
- 42
- 43
- 44
- 45
- 46
- 47
- 48
- 49
- 50
- 51
- 52
- 53
- 54
- 55
- 56
- 57
- 58
- 59
- 60
- 61
- 62
- 63
- 64
- 65
- 66
- 67
- 68
- 81
- 527
- 528
- 529
- 530
- 531
- 532
- 533
- 534
- 535
- 536
- 537
- 538
- 539
- 540
- 541
- 542
- 543
- 544
- 545
- 546
- 547
- 548
- 549
- 550
- 551
- 552
- 553
- 554
- 555
- 556
- 557
- 558
- 559
- 560
- 561
- 562
- 563
- 564
- 565
- 566
- 567
- 568
- 569
- 570
- 571
- 572
- 573
- 574
- 575
- 576
- 577
- 578
- 579
- 580
- 581
- 582
- 583
- 584
- 585
- 586
- 587
- 588
- 589
- 590
- 591
- 592
- 593
- 594
- 595
- 596
- 597
- 598
- 599
- 600
- 601
- 602
- 603
- 604
- 605
- 606
- 607
- 608
- 609
- 610
- 611
- 612
- 613
- 614
- 615
- 616
- 617
- 618
- 619
- 620
- 621
- 622
- 623
- 624
- 625
- 626
- 627
- 628
- 629
- 630
- 631
- 667
- 668
- 669
- 670
- 671
- 672
- 673
- 674
- 675
- 676
- 677
- 678
- 679
- 680
- 681
- 682
- 683
- 684
- 685
- 686
- 687
- 688
- 689
- 690
- 691
- 692
- 693
- 694
- 695
- 696
- 697
- 698
- 699
- 700
- 701
- 702
- 703
- 704
- 705
- 706
- 707
- 708
- 709
- 710
- 711
- 712
- 713
- 714
- 715
- 716
- 717
- 718
- 719
- 720
- 721
- 722
- 723
- 724
- 725
- 726
- 727
- 728
- 729
- 730
- 731
- 732
- 733
- 734
- 735
- 736
- 737
- 738
- 739
- 740
- 741
- 742
- 743
- 744
- 745
- 746
- 747
- 748
- 749
- 750
- 751
- 752
- 753
- 754
- 755
- 756
- 757
- 758
- 759
- 760
- 761
- 762
- 763
- 764
- 765
- 766
- 767
- 768
- 769
- 770
- 771
- 772
- 773
- 774
- 776
- 777
- 778
- 779
- 780
- 781
- 782
- 783
- 784
- 785
- 786
- 787
- 788
- 789
- 790
- 791
- 792
- 793
- 794
- 795
- 796
- 797
- 798
- 799
- 800
- 801
- 802
- 803
- 804
- 805
- 806
- 807
- 808
- 809
- 810
- 811
- 812
- 813
- 814
- 815
- 816
- 817
- 818
- 819
- 820
- 821
- 822
- 823
- 824
- 825
- 826
- 827
- 828
- 829
- 830
- 831
- 832
- 833
- 834
- 835
- 836
- 837
- 838
- 839
- 840
- 841
- 842
- 843
- 844
- 845
- 846
- 847
- 848
- 849
- 850
- 851
- 852
- 853
- 854
- 855
- 856
- 857
- 858
- 859
- 860
- 861
- 862
- 863
- 864
- 865
- 866
- 867
- 868
- 869
- 870
- 871
- 872
- 873
- 874
- 875
- 876
- 877
- 878
- 879
- 880
- 881
- 882
- 883
- 884
- 885
- 886
- 887
- 888
- 889
- 890
- 891
- 892
- 893
- 894
- 895
- 896
- 897
- 898
- 899
- 900
- 901
- 902
- 903
- 904
- 905
- 906
- 907
- 908
- 909
- 910
- 911
- 912
- 913
- 914
- 915
- 916
- 917
- 918
- 919
- 920
- 921
- 922
- 923
- 924
- 925
- 926
- 927
- 928
- 929
- 930
- 931
- 932
- 933
- 934
- 935
- 936
- 937
- 938
- 939
- 940
- 941
- 942
- 943
- 944
- 945
- 946
- 947
- 948
- 949
- 950
- 951
- 952
- 953
- 954
- 955
- 956
- 957
- 958
- 959
- 960
- 961
- 962
- 963
- 964
- 965
- 966
- 967
- 968
- 969
- 970
- 971
- 972
- 973
- 974
- 975
- 976
- 977
- 978
- 979
- 980
- 981
- 982
- 983
- 984
- 985
- 986
- 987
- 988
- 989
- 990
- 991
- 992
- 993
- 994
- 995
- 996
- 997
- 998
- 999
- 1000
- 1001
- 1002
- 1003
- 1004
- 1005
- 1006
- 1007
- 1008
- 1009
- 1010
- 1011
- 1012
- 1013
- 1014
- 1015
- 1016
- 1017
- 1018
- 1019
- 1020
- 1021
- 1022
- 1023
- 1024
- 1025
- 1026
- 1027
- 1028
- 1029
- 1030
- 1031
- 1032
- 1033
- 1034
- 1035
- 1036
- 1037
- 1038
- 1039
- 1040
- 1041
- 1042
- 1043
- 1044
- 1045
- 1046
- 1047
- 1048
- 1049
- 1050
- 1051
- 2918
- 2919
- 2920
- 2921
- 2922
- 2923
- 2924
- 2925
- 2926
- 2927
- 2928
- 2929
- 2930
- 2931
- 2932
- 2933
- 2934
- 2935
- 2936
- 2937
- 2938
- 2939
- 2940
- 2941
- 2942
- 2943
- 2944
- 2945
- 2946
- 2947
- 2948
- 2949
- 2950
- 2951
- 2952
- 2953
- 2954
- 2955
- 2956
- 2957
- 2958
- 2959
- 2960
- 2961
- 2962
- 2963
- 2964
- 2965
- 2966
- 2967
- 2968
- 2969
- 2970
- 2971
- 2972
- 2973
- 2974
- 2975
- 2976
- 2977
- 2978
- 2979
- 2980
- 2981
- 2982
- 2983
- 2984
- 2985
- 2986
- 2987
- 3026
- 3027
- 3028
- 3029
- 3030
- 3031
- 3032
- 3033
- 3034
- 3035
- 3036
- 3037
- 3038
- 3039
- 3040
- 3041
- 3042
- 3043
- 3044
- 3045
- 3046
- 3047
- 3048
- 3049
- 3050
- 3051
- 3052
- 3053
- 3054
- 3055
- 3056
- 3057
- 3058
- 3059
- 3060
- 3841
- 3876
- 3905
- 3954
- 3989
- 4124
- 4159
- 4194
- 4229
- 4264
- 4369
- 4524
- 4559
- 4594
- 4805
- 4806
- 4807
- 4808
- 4809
- 4810
- 4811
- 4812
- 4813
- 4814
- 4815
- 4816
- 4817
- 4818
- 4819
- 4820
- 4821
- 4822
- 4823
- 4824
- 4825
- 4826
- 4827
- 4828
- 4829
- 4830
- 4831
- 4832
- 4833
- 4834
- 4835
- 4836
- 4837
- 4838
- 4839
- 4841
- 4842
- 4843
- 4844
- 4845
- 4846
- 4847
- 4848
- 4849
- 4850
- 4851
- 4852
- 4853
- 4854
- 4855
- 4856
- 4857
- 4858
- 4859
- 4860
- 4861
- 4862
- 4863
- 4864
- 4865
- 4866
- 4867
- 4868
- 4869
- 4870
- 4871
- 4872
- 4873
- 4874
- 4875
- 4876
- 4877
- 4878
- 4879
- 4880
- 4881
- 4882
- 4883
- 4884
- 4885
- 4886
- 4887
- 4888
- 4889
- 4890
- 4891
- 4892
- 4893
- 4894
- 4895
- 4896
- 4897
- 4898
- 4899
- 4900
- 4901
- 4902
- 4903
- 4904
- 4905
- 4906
- 4907
- 4908
- 4909
- 4910
- 4946
- 4947
- 4948
- 4949
- 4950
- 4951
- 4952
- 4953
- 4954
- 4955
- 4956
- 4957
- 4958
- 4959
- 4960
- 4961
- 4962
- 4963
- 4964
- 4965
- 4966
- 4967
- 4968
- 4969
- 4970
- 4971
- 4972
- 4973
- 4974
- 4975
- 4976
- 4977
- 4978
- 4979
- 4980
- 4981
- 4982
- 4983
- 4984
- 4985
- 4986
- 4987
- 4988
- 4989
- 4990
- 4991
- 4992
- 4993
- 4994
- 4995
- 4996
- 4997
- 4998
- 4999
- 5000
- 5001
- 5002
- 5003
- 5004
- 5005
- 5006
- 5007
- 5008
- 5009
- 5010
- 5011
- 5012
- 5013
- 5014
- 5015
- 5016
- 5017
- 5018
- 5019
- 5020
- 5021
- 5022
- 5023
- 5024
- 5025
- 5026
- 5027
- 5028
- 5029
- 5030
- 5031
- 5032
- 5033
- 5034
- 5035
- 5036
- 5037
- 5038
- 5039
- 5040
- 5041
- 5042
- 5043
- 5044
- 5045
- 5046
- 5047
- 5048
- 5049
- 5050
- 5051
- 5052
- 5053
- 5054
- 5055
- 5056
- 5057
- 5058
- 5059
- 5060
- 5061
- 5062
- 5063
- 5064
- 5065
- 5066
- 5067
- 5068
- 5069
- 5070
- 5071
- 5072
- 5073
- 5074
- 5075
- 5076
- 5077
- 5078
- 5079
- 5080
- 5081
- 5082
- 5083
- 5084
- 5085
- 5086
- 5087
- 5088
- 5089
- 5090
- 5091
- 5092
- 5093
- 5094
- 5095
- 5096
- 5097
- 5098
- 5099
- 5100
- 5101
- 5102
- 5103
- 5104
- 5105
- 5106
- 5107
- 5108
- 5109
- 5110
- 5111
- 5112
- 5113
- 5114
- 5115
- 5116
- 5117
- 5118
- 5119
- 5120
- 5123
- 5124
- 5125
- 5126
- 5127
- 5128
- 5129
- 5130
- 5131
- 5132
- 5133
- 5134
- 5135
- 5136
- 5137
- 5138
- 5139
- 5140
- 5141
- 5142
- 5143
- 5144
- 5145
- 5146
- 5147
- 5148
- 5149
- 5150
- 5151
- 5152
- 5153
- 5154
- 5155
- 5156
- 5157
- 5158
- 5159
- 5160
- 5161
- 5162
- 5163
- 5164
- 5165
- 5166
- 5167
- 5168
- 5169
- 5170
- 5171
- 5172
- 5173
- 5174
- 5175
- 5176
- 5177
- 5178
- 5179
- 5180
- 5181
- 5182
- 5183
- 5184
- 5185
- 5186
- 5187
- 5188
- 5189
- 5190
- 5191
- 5192
- 5275
- 5277
- 5279
- 5280
- 5281
- 5282
- 5283
- 5284
- 5285
- 5286
- 5287
- 5288
- 5289
- 5290
- 5291
- 5292
- 5293
- 5294
- 5295
- 5296
- 5297
- 5298
- 5299
- 5300
- 5301
- 5302
- 5303
- 5304
- 5305
- 5306
- 5307
- 5310
- 5312
- 5314
- 5315
- 5316
- 5317
- 5318
- 5319
- 5320
- 5321
- 5322
- 5323
- 5324
- 5325
- 5326
- 5327
- 5328
- 5329
- 5330
- 5331
- 5332
- 5333
- 5334
- 5335
- 5336
- 5337
- 5338
- 5339
- 5340
- 5341
- 5342
- 5345
- 5347
- 5349
- 5350
- 5351
- 5352
- 5353
- 5354
- 5355
- 5356
- 5357
- 5358
- 5359
- 5360
- 5361
- 5362
- 5363
- 5364
- 5365
- 5366
- 5367
- 5368
- 5369
- 5370
- 5371
- 5372
- 5373
- 5374
- 5375
- 5376
- 5377
- 5440
- 5442
- 5444
- 5445
- 5446
- 5447
- 5448
- 5449
- 5450
- 5451
- 5452
- 5453
- 5454
- 5455
- 5456
- 5457
- 5458
- 5459
- 5460
- 5461
- 5462
- 5463
- 5464
- 5465
- 5466
- 5467
- 5468
- 5469
- 5470
- 5471
- 5472
- 5475
- 5477
- 5479
- 5480
- 5481
- 5482
- 5483
- 5484
- 5485
- 5486
- 5487
- 5488
- 5489
- 5490
- 5491
- 5492
- 5493
- 5494
- 5495
- 5496
- 5497
- 5498
- 5499
- 5500
- 5501
- 5502
- 5503
- 5504
- 5505
- 5506
- 5507
- 5510
- 5512
- 5514
- 5515
- 5516
- 5517
- 5518
- 5519
- 5520
- 5521
- 5522
- 5523
- 5524
- 5525
- 5526
- 5527
- 5528
- 5529
- 5530
- 5531
- 5532
- 5533
- 5534
- 5535
- 5536
- 5537
- 5538
- 5539
- 5540
- 5541
- 5542
- 5876
- 5877
- 5878
- 5879
- 5880
- 5881
- 5882
- 5883
- 5884
- 5885
- 5886
- 5887
- 5888
- 5889
- 5890
- 5891
- 5892
- 5893
- 5894
- 5895
- 5896
- 5897
- 5898
- 5899
- 5900
- 5901
- 5902
- 5903
- 5904
- 5905
- 5906
- 5907
- 5908
- 5909
- 5910
- 5941
- 5945
- 5946
- 5947
- 5948
- 5949
- 5950
- 5951
- 5952
- 5953
- 5954
- 5955
- 5956
- 5957
- 5958
- 5959
- 5960
- 5961
- 5962
- 5963
- 5964
- 5965
- 5966
- 5967
- 5968
- 5969
- 5970
- 5976
- 5980
- 5981
- 5982
- 5983
- 5984
- 5985
- 5986
- 5987
- 5988
- 5989
- 5990
- 5991
- 5992
- 5993
- 5994
- 5995
- 5996
- 5997
- 5998
- 5999
- 6000
- 6001
- 6002
- 6003
- 6004
- 6005
- 6011
- 6015
- 6016
- 6017
- 6018
- 6019
- 6020
- 6021
- 6022
- 6023
- 6024
- 6025
- 6026
- 6027
- 6028
- 6029
- 6030
- 6031
- 6032
- 6033
- 6034
- 6035
- 6036
- 6037
- 6038
- 6039
- 6040
- 6046
- 6050
- 6051
- 6052
- 6053
- 6054
- 6055
- 6056
- 6057
- 6058
- 6059
- 6060
- 6061
- 6062
- 6063
- 6064
- 6065
- 6066
- 6067
- 6068
- 6069
- 6070
- 6071
- 6072
- 6073
- 6074
- 6075
- 6081
- 6085
- 6086
- 6087
- 6088
- 6089
- 6090
- 6091
- 6092
- 6093
- 6094
- 6095
- 6096
- 6097
- 6098
- 6099
- 6100
- 6101
- 6102
- 6103
- 6104
- 6105
- 6106
- 6107
- 6108
- 6109
- 6110
- 6116
- 6120
- 6121
- 6122
- 6123
- 6124
- 6125
- 6126
- 6127
- 6128
- 6129
- 6130
- 6131
- 6132
- 6133
- 6134
- 6135
- 6136
- 6137
- 6138
- 6139
- 6140
- 6141
- 6142
- 6143
- 6144
- 6145
- 6151
- 6155
- 6156
- 6157
- 6158
- 6159
- 6160
- 6161
- 6162
- 6163
- 6164
- 6165
- 6166
- 6167
- 6168
- 6169
- 6170
- 6171
- 6172
- 6173
- 6174
- 6175
- 6176
- 6177
- 6178
- 6179
- 6180
- 6186
- 6190
- 6191
- 6192
- 6193
- 6194
- 6195
- 6196
- 6197
- 6198
- 6199
- 6200
- 6201
- 6202
- 6203
- 6204
- 6205
- 6206
- 6207
- 6208
- 6209
- 6210
- 6211
- 6212
- 6213
- 6214
- 6215
- 6221
- 6225
- 6226
- 6227
- 6228
- 6229
- 6230
- 6231
- 6232
- 6233
- 6234
- 6236
- 6237
- 6238
- 6239
- 6240
- 6241
- 6242
- 6243
- 6244
- 6245
- 6246
- 6247
- 6248
- 6249
- 6250
- 6256
- 6260
- 6261
- 6262
- 6263
- 6264
- 6265
- 6266
- 6267
- 6268
- 6269
- 6270
- 6271
- 6272
- 6273
- 6274
- 6275
- 6276
- 6277
- 6278
- 6279
- 6280
- 6281
- 6282
- 6283
- 6284
- 6285
- 6373
- 6377
- 6378
- 6379
- 6380
- 6381
- 6382
- 6383
- 6384
- 6385
- 6386
- 6387
- 6388
- 6389
- 6390
- 6391
- 6392
- 6393
- 6394
- 6395
- 6396
- 6397
- 6398
- 6399
- 6400
- 6401
- 6402
- 6408
- 6412
- 6413
- 6414
- 6415
- 6416
- 6417
- 6418
- 6419
- 6420
- 6421
- 6422
- 6423
- 6424
- 6425
- 6426
- 6427
- 6428
- 6429
- 6430
- 6431
- 6432
- 6433
- 6434
- 6435
- 6436
- 6437
- 6443
- 6447
- 6448
- 6449
- 6450
- 6451
- 6452
- 6453
- 6454
- 6455
- 6456
- 6457
- 6458
- 6459
- 6460
- 6461
- 6462
- 6463
- 6464
- 6465
- 6466
- 6467
- 6468
- 6469
- 6470
- 6471
- 6472
- 6478
- 6482
- 6483
- 6484
- 6485
- 6486
- 6487
- 6488
- 6489
- 6490
- 6491
- 6492
- 6493
- 6494
- 6495
- 6496
- 6497
- 6498
- 6499
- 6500
- 6501
- 6502
- 6503
- 6504
- 6505
- 6506
- 6507
- 6513
- 6517
- 6518
- 6519
- 6520
- 6521
- 6522
- 6523
- 6524
- 6525
- 6526
- 6527
- 6528
- 6529
- 6530
- 6531
- 6532
- 6533
- 6534
- 6535
- 6536
- 6537
- 6538
- 6539
- 6540
- 6541
- 6542
- 6581
- 6582
- 6583
- 6584
- 6585
- 6586
- 6587
- 6588
- 6589
- 6590
- 6591
- 6592
- 6593
- 6594
- 6595
- 6596
- 6597
- 6598
- 6599
- 6600
- 6601
- 6602
- 6603
- 6604
- 6605
- 6606
- 6607
- 6608
- 6609
- 6610
- 6611
- 6612
- 6613
- 6614
- 6996
- 7001
- 7002
- 7030
- 7035
- 7064
- 7069
- 7098
- 7103
- 7132
- 7137
- 7166
- 7171
- 7200
- 7205
- 7234
- 7239
- 7268
- 7273
- 7302
- 7307
- 7336
- 7341
- 7370
- 7375
- 7404
- 7409
- 7438
- 7443
- 7502
- 7503
- 7506
- 7511
- 7519
- 7524
- 7527
- 7528
- 7530
- 7601
- 7602
- 7603
- 7604
- 7605
- 7606
- 7607
- 7608
- 7609
- 7610
- 7611
- 7612
- 7613
- 7614
- 7615
- 7616
- 7617
- 7618
- 7619
- 7620
- 7621
- 7622
- 7623
- 7624
- 7625
- 7626
- 7627
- 7628
- 7629
- 7630
- 7631
- 7632
- 7633
- 7634
- Войти в свой аккаунт
-
Химия
-
Биология
-
Русский язык
-
Математика базовая
-
Математика профильная