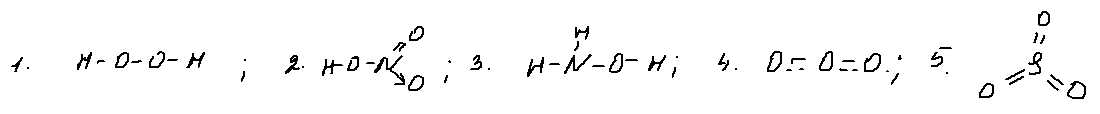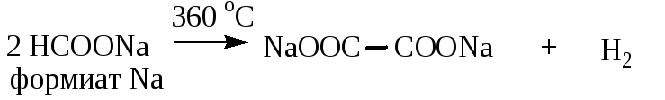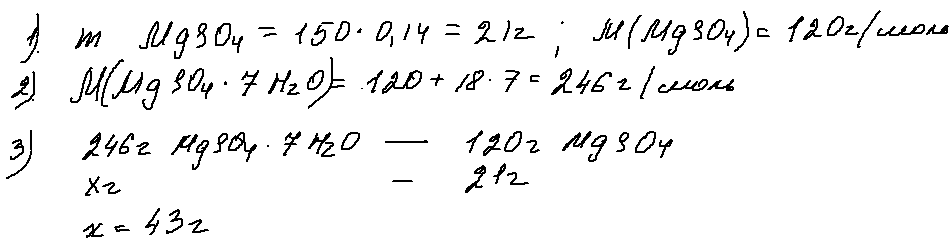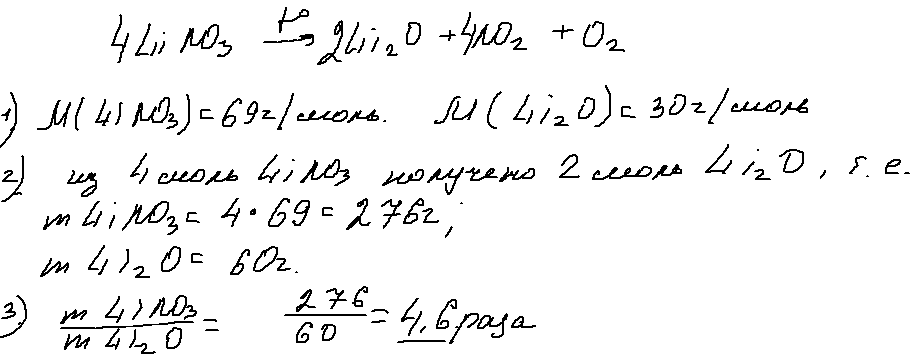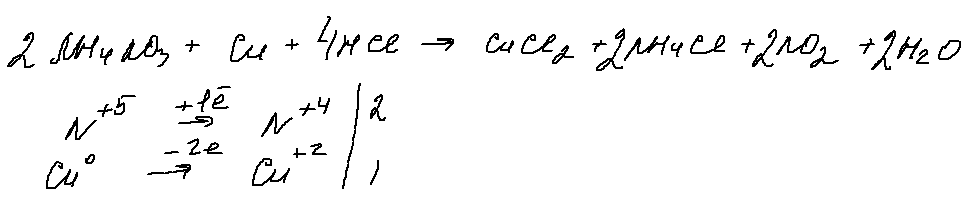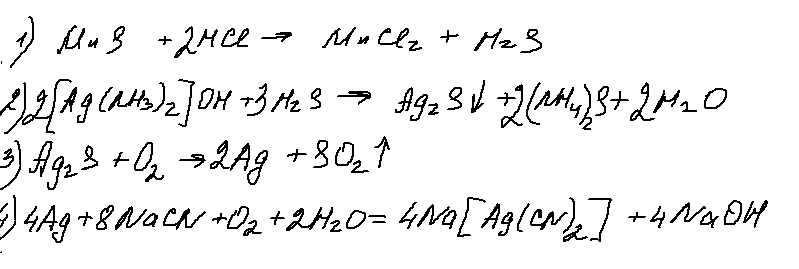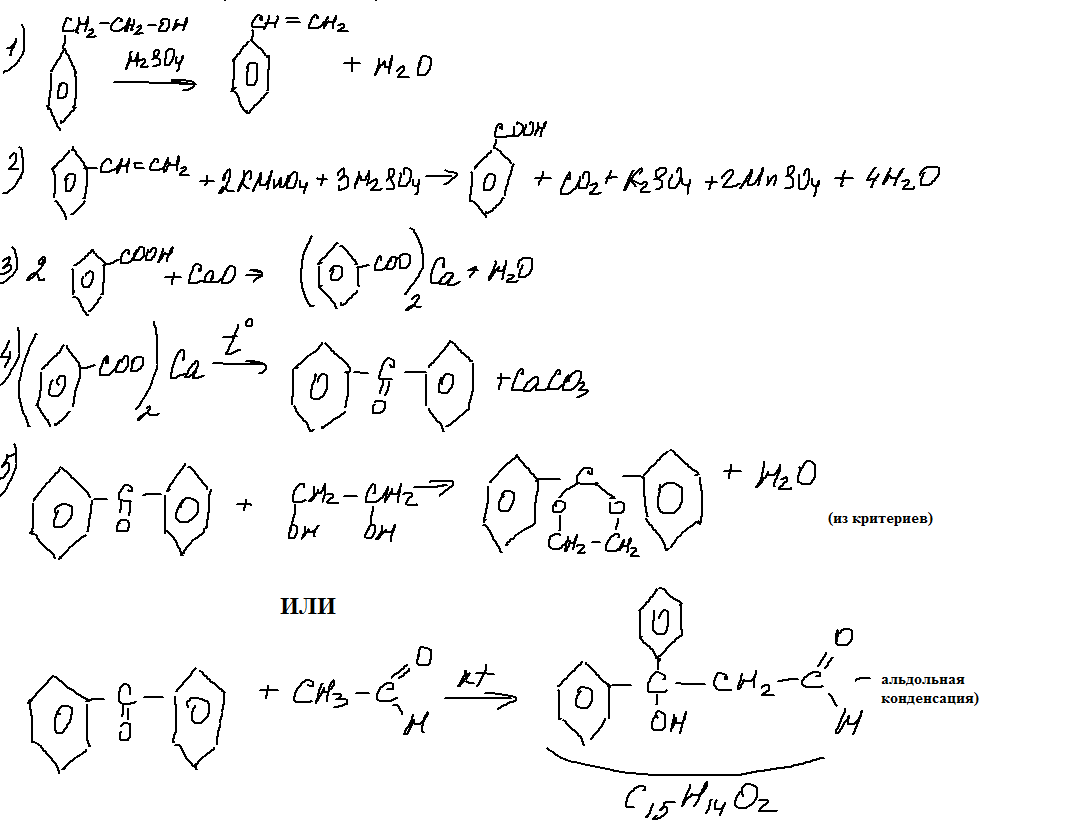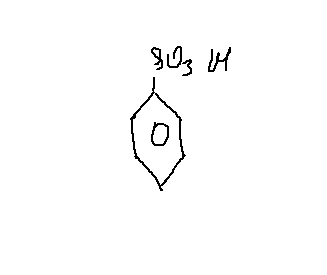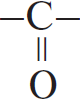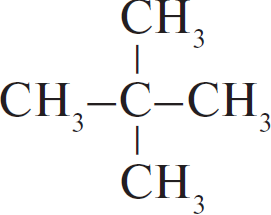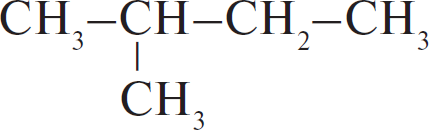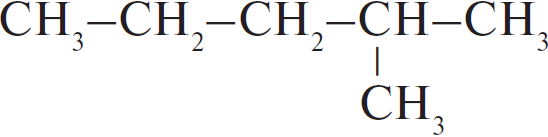Задания
Версия для печати и копирования в MS Word
Из предложенного перечня выберите два вещества, которые не имеют структурных изомеров.
1) бутанол-1
2) пропанол-2
3) пропан
4) этаналь
5) этин
Запишите в поле ответа номера выбранных веществ.
Спрятать решение
Решение.
У пропана и этина, в отличие от других представленных соединений, не может быть структурных изомеров.
Ответ: 35.
Источник: РЕШУ ЕГЭ
Спрятать решение
·
·
Иван Карбышев 18.11.2016 20:50
Какой структурный изомер у этаналя???
Александр Иванов
эпоксиэтан
7583. Серу сплавили с железом. Продукт реакции обработали соляной кислотой. Выделившийся при этом газ сожгли в избытке кислорода. Продукты горения поглотили водным раствором сульфата железа(III).
Напишите уравнения четырёх описанных реакций.

1) Fe + S = (t°) FeS
2) FeS + 2HCl = FeCl2 + H2S↑
3) 2H2S + 3O2 = (t°) 2SO2↑ + 2H2O
4) Fe2(SO4)3 + SO2 + 2H2O = 2FeSO4 + 2H2SO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7583.
7548. Некоторое количество сульфида цинка разделили на две части. Одну из них обработали разбавленной серной кислотой, а другую подвергли обжигу на воздухе. При взаимодействии выделившихся газов образовалось простое вещество. Это вещество нагрели с концентрированной азотной кислотой, причём выделился бурый газ.
Напишите уравнения четырёх описанных реакций.

1) ZnS + H2SO4 = ZnSO4 + H2S↑
2) 2ZnS + 3O2 = 2ZnO + 2SO2↑
3) 2H2S + SO2 = 3S↓ + 2H2O
4) S + 6HNO3 = H2SO4 + 6NO2↑ + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7548.
7513. В результате неполного сгорания угля получили газ, в токе которого нагревали оксид железа(III). Полученное простое вещество растворили в горячей концентрированной серной кислоте. Образовавшийся раствор соли прореагировал с порошком меди.
Напишите уравнения четырёх описанных реакций.

1) 2C + O2 = (t°) 2CO
2) Fe2O3 + 3CO = (t°) 2Fe + 3CO2
3) 2Fe + 6H2SO4 = (t°) Fe2(SO4)3 + 3SO2↑ + 6H2O
4) Fe2(SO4)3 + Cu = 2FeSO4 + CuSO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7513.
7478. Порошок металлического алюминия смешали с твёрдым иодом и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдали выпадение осадка.
Напишите уравнения четырёх описанных реакций.

1) 2Al + 3I2 = 2AlI3
2) AlI3 + 3NaOH = Al(OH)3↓ + 3NaI
3) Al(OH)3 + 3HCl = AlCl3 + 3H2O
4) 2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 6NaCl
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7478.
7443. Диоксид серы растворили в воде. К полученному раствору прилили бромную воду до исчезновения окраски, а затем избыток хлорида бария. Осадок отфильтровали, высушили и прокалили с углём. Выделившийся в ходе реакции газ пропустили над оксидом меди(II) при нагревании.
Напишите уравнения соответствующих реакций.

1) SO2 + Br2 + 2H2O = H2SO4 + 2HBr
2) H2SO4 + BaCl2 = BaSO4↓ + 2HCl
3) BaSO4 + 4C = (t°) BaS + 4CO↑
4) CO + CuO = (t°) Cu + CO2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7443.
7408. Оксид меди (II) нагревали в токе угарного газа. Полученное простое вещество сожгли в атмосфере хлора. Продукт реакции растворили в воде. Полученный раствор разделили на две части. К одной части добавили раствор иодида калия, ко второй — раствор нитрата серебра. И в том, и в другом случае наблюдали образование осадка.
Напишите уравнения четырёх описанных реакций

1) CuO + CO = Cu + CO2↑
2) Cu + Cl2 = CuCl2
3) 2CuCl2 + 4KI = 2CuI + I2↓ + 4KCl
4) CuCl2 + 2AgNO3 = 2AgCl↓ + Cu(NO3)2
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7408.
7373. При обработке карбида кальция избытком кипящей воды выделился газ, при пропускании которого через раствор, полученный взаимодействием оксида меди(I) с раствором аммиака, образуется осадок. Выделяющийся газ в ходе реакции пропустили через раскаленную трубку из оксида меди(II).
Напишите соответствующие уравнения реакций.

1) CaC2 + 2H2O = (t°) Ca(OH)2 + C2H2↑
2) Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH
3) C2H2 + 2[Cu(NH3)2]OH = Cu-C≡C-Cu↓ + 4NH3↑ + 2H2O
4) 3CuO + 2NH3 = (t°) 3Cu + N2 + 3H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7373.
7338. Фосфор сожгли на воздухе. Полученный оксид обработали водой. В полученный раствор поместили гидроксид кальция. Образовавшуюся среднюю соль отфильтровали и обработали концентрированной серной кислотой.
Напишите уравнения четырёх описанных реакций.

1) P (или P4) + O2 = P4O10 (или 2P2O5)
2) P4O10 + 6H2O = 4H3PO4 (или P2O5 + 3H2O = 2H3PO4)
3) 2H3PO4 + 3Ca(OH)2 = Ca3(PO4)2↓ + 6H2O
4) Ca3(PO4)2 + 3H2SO4 = 3CaSO4 + 2H3PO4
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7338.
7303. К раствору хлорида бериллия добавили по каплям раствор гидроксида калия до полного растворения первоначально выпавшего осадка. К полученному раствору по каплям добавили соляную кислоту до выпадения осадка, а затем разбавленную серную кислоту до растворения осадка.
Напишите уравнения четырёх описанных реакций.

1) BeCl2 + 2KOH = Be(OH)2↓ + 2KCl
2) Be(OH)2 + 2KOH = K2[Be(OH)4]
3) K2[Be(OH)4] + 2HCl = Be(OH)2↓ + 2KCl + 2H2O
4) Be(OH)2 + H2SO4 = BeSO4 + 2H2O
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7303.
7268. Через раствор гидроксида калия пропустили сначала недостаточное, а затем избыточное количество углекислого газа. Полученную соль обработали разбавленной азотной кислотой. Полученный раствор выпарили досуха, а остаток прокалили.
Напишите уравнения четырёх описанных реакций.

1) CO2 + 2KOH = K2CO3 + H2O
2) K2CO3 + CO2 + H2O = 2KHCO3
3) KHCO3 + HNO3 = KNO3 + CO2↑ + H2O
4) 2KNO3 = (t°) 2KNO2 + O2↑
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 7268.
Для вас приятно генерировать тесты, создавайте их почаще

Предлагаем вам ознакомиться с новыми открытыми вариантами ЕГЭ-23, здесь вы найдете новые ответы с объяснением, пошаговые решения и пояснения на новые варианты КИМ, ФИПИ и новым ФГОС на ЕГЭ-2023. Демоварианты вы сможете бесплатно скачать ответы в формате PDF или ВОРД / WORD для подготовки к экзамену и самостоятельно решать задачи и примеры. Также здесь можно скачать ответы, решения, пояснения и объяснения к заданиям экзамена. Домашняя работа. Вариант

Официальный сайт. Единый Государственный Экзамен ОГЭ 2022 — 2023 учебный год. 11 класс. ВПР. РП. ФИПИ ШКОЛЕ. ДНР. ФГОС. ОРКСЭ. МЦКО. ФИОКО. ОГЭ. ЕГЭ. ПНШ.ДОУ. УМК. Просвещение. Ответы. Школа России. Школа 21 век. Перспектива. Школа 2100. Планета знаний. Россия. Беларусь. ЛНР. Казахстан. РБ. Татарстан. Башкортостан









.
Елена Шаврак. ЕГЭ по химии: новые упражнения и цепочки превращений. вопрос — хим. связь.. вопрос.
Елена Шаврак
ЕГЭ по химии: новые упражнения и цепочки превращений
Здравствуйте, уважаемые читатели!
Сегодня я хочу рассмотреть некоторые задания из нового СтатГрадовского пробника от 3 марта 2021 года. Причина — подобные упражнения ранее мне не встречались ни в одном из пробников и пособий за последние 8 лет. Про себя я данный факт обозначила как : «СтатГрад расширяет границы», причем это расширение носит как экстенсивный, так и интенсивный характер.
Итак, по порядку. Начинаю с заданий 1 варианта.
1. 4 вопрос — хим. связь.
Для выполнения этого задания запишем структурные формулы всех веществ (не учитываю валентные углы):
Только одинарные ковалентные связи есть в молекуле пероксида водорода (1) и гидроксиламина (3).
Новизна этого задания, скорее, экстенсивного характера. Т.е., несмотря на то, что ранее подобная формулировка 4 задания не встречалась в пробниках (мое субъективное мнение), для его выполнения вполне достаточно школьной базы.
2. 7 вопрос.
Для выполнения этого задания необходимо знать, что соединения меди могут выпадать в осадок при добавлении растворов трех реагентов из предложенного списка, а именно: аммиака, сероводорода и карбоната калия. Но в избытке аммиака осадок растворится вследствие образования аммиакатного комплекса меди. Одновременное образование осадка и газа — это маркерный признак совместного (или смешанного) гидролиза, протекающего при смешении растворов соли меди и карбоната. Т.о., ответы — Х- H2S, Y- K2CO3.
Новизна этого задания также условная. Аммиакатные комплексы меди (и цинка) в 7 задании встречались и ранее, но ОЧЕНЬ редко.
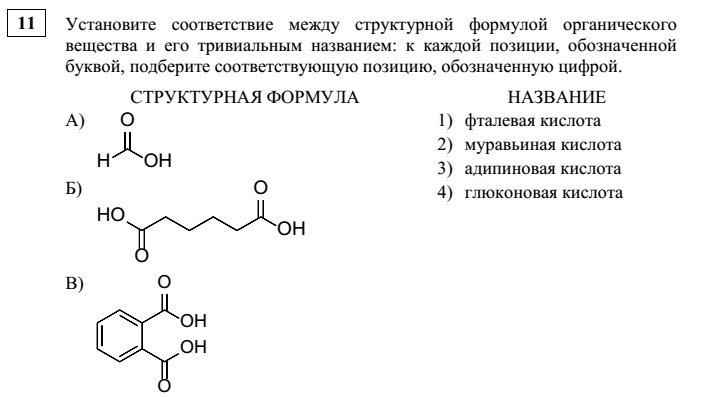
3. 11 вопрос
Практически во всех последних СтатГрадовских пробниках в 11 задании используются «скелетные» формулы органических веществ. Выскажу свою точку зрения: это хорошо, поскольку, опять же, — расширяет границы восприятия материала. Надеюсь, что, со временем, в формулировках будут использоваться классические скелетные формулы, в которых клинообразными линиями обозначаются связи, направленные вверх относительно плоскости, т.е. к наблюдателю, пунктирными линиями обозначаются связи, направленные вниз относительно плоскости, т.е. от наблюдателя.
Ответы — 231
Новизна этого задания невелика. Пожалуй, при подготовке стоит обратить внимание на отработку тривиальных названий органических соединений.
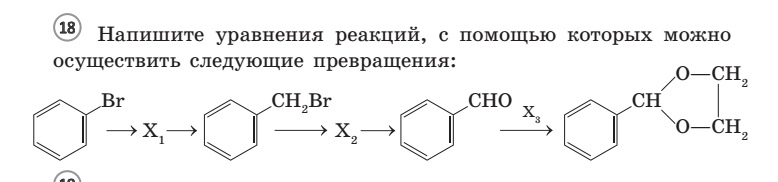
4. 17 вопрос
В 17 задании, посвященном кислородсодержащей органике, приведена практически не упоминавшаяся в пробниках и сборниках тестов реакция термического превращения формиата натрия до оксалата натрия:
Мой личный вывод: спасибо СтатГраду за актуализацию ранее невостребованной информации, относящейся, в принципе, к школьной программе (способы получения дикарбоновых кислот).
5. 27 задача.
Задача 27, в который уже раз в этом году, обращает внимание к кристаллогидратам. Решать ее можно разными способами — через моли, через пропорцию, правилом креста …
Ниже я привела один из вариантов решения., суть которого заключается в нахождении массы всей растворенной соли и последующем «заключении» ее в кристаллогидрат:
Ответ — 43 г.
6. 29 задача.
Задача 29 обращает на себя внимание формулировкой (полное отсутствие числовых данных) и «незамыленной» химией — разложением нитрата активного металла. Опять же и эту задачу можно решать несколькими способами. Ниже привожу один из них:
7. 30 задание.
«Грозное» 30 задание, в котором, при ближайшем рассмотрении, можно выделить только 1 окислитель (нитрат аммония), 1 восстановитель — медь. Для перевода нитрата в азотную кислоту, с которой будет реагировать медь, добавим соляную кислоту. Берем ее концентрированной, чтобы в результате реакции обмена получить концентрированную азотную кислоту (кстати, можно проводить реакцию с выделением оксида азота (2), для этого нужно взять разбавленную соляную кислоту). В результате получаем:
Данная реакция напоминает мне качественную реакцию на нитраты, в которой к нитрату добавляют медь и концентрированную серную кислоту и наблюдают образование бурого газа.
8. 32 задание.
Хорошее задание, ничего не скажешь! Реакция 2 — разрушение комплекса, достаточно типовая. Реакция 3 — окисление сульфида серебра (а еще и ртути) идет с образованием только одного оксида. Реакция достаточно редкая, но встречалась. А вот 4 реакция — меня лично ввела в ступор. Возможно ошибаюсь, но неоднократно от представителей ФИПИ на вебинарах звучало, что на ЕГЭ будут только гидроксокомплексы цинка и алюминия. Понемногу «пробрались» аммиакаты. Но цианидных комплексов до сих пор еще не было. Искренний респект составителям!
9. 33 цепочка.
Вот это задание заслуживает самого пристального внимания. С одной стороны — бруттоформулы в задании- это очень хорошо, поскольку способствует более глубокому проникновению в суть задания. С другой стороны- последняя реакция, представляющая собой введение ацетальной защиты (по мнению авторов пробника). Я бы написала здесь и альдольную конденсацию дифенилкетона с ацетальдегидом. Но этого не дают в школьной программе (или я ошибаюсь?).
Необходимо отметить, что еще одну цепочку с ацетальной защитой я нашла в сборнике
10. 34 задача.
Данную задачу в этой статье отрешивать не буду. Сделаю это позже. Но бросается в глаза новое усложнение — нахождение состава газовой смеси по плотности. Практически не встречалось такого в задачах , предназначенных для подготовки к ЕГЭ.
11. 35 задача.
Одно из заданий, которое мне очень понравилось в этом пробнике.
Решение
1. Схема реакции сгорания неизвестного соединения:
CxHySzOk+O2=CO2+H2O+SO2
2. Найдем молекулярную формулу неизвестного соединения:
а) n(C)=n(CO2)= 20,16/22,4=0,9 моль,
n(Н)=2n(Н2О)= 2*8,1 /18=0,9 моль,
n(S)=n(SO2)= 3,36/22,4=0,15 моль,
n(O)=(23,7-(12*0,9+0,9+32*0,15))/16=0,45 моль
б) Молекулярная формула неизвестного вещества-: С6Н6SO3. Это — бензолсульфокислота
3. Структурная формула —
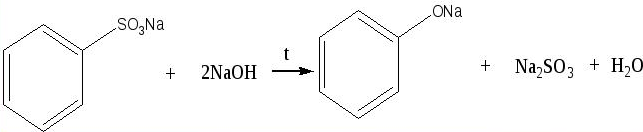
4. Уравнение реакции, происходящей при сплавлении бензолсульфоната натрия со щелочью:
Рассмотрела только первый вариант пробника, но и в нем много информации к размышлению. Резюмирую:
1. Реальный ЕГЭ по сложности раньше не всегда корреллировал со статградовскими пробниками, поэтому не факт, что задания уровня сложности рассмотренных 32-34 стоит ожидать на реальном экзамене.
2. Задания данного пробника актуализируют изучаемую, но относительно редко используемую информацию об органических и неорганических веществах (особенно — задания 4, 7, 11, 17, 27, 29, 35).
3. Для выполнения заданий 32 и 33 необходимо обладать информацией, адекватное усвоение которой возможно только в ходе изучения вузовских курса неорганической и органической химий (подчеркиваю, что это — мое субъективное мнение).
4. Великолепна задача 35. Впервые в пробниках ЕГЭ: серосодержащая органика и практически не используемый ранее при составлении заданий способ получения фенола.
5. В целом — еще раз — респект составителям, но — детей жалко. Без хорошего репетитора до уровня такого пробника не подняться.
Всего доброго!
Тренировочный вариант по химии №7, №8 решу ЕГЭ 2023. Новые тренировочные варианты Добротина ЕГЭ 2023 по химии для 11 класса вариант 7 и вариант 8 в формате реального экзамена ЕГЭ, пробные варианты с ответами и решением для подготовки ФИПИ.
Скачать вариант №7
Скачать вариант №8
Вариант №7 Добротин ЕГЭ 2023 по химии с ответами
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- 1) O
- 2) Si
- 3) Cr
- 4) Sc
- 5) Cl
1. Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат ровно один неспаренный электрон.
2. Из указанных в ряду химических элементов выберите три элемента, которые в находятся в малых периодах. Расположите выбранные элементы в порядке увеличения электроотрицательности. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3. Из числа указанных в ряду элементов выберите два элемента, у каждого из которых значение высшей степени окисления численно совпадает со значением низшей степени окисления.
4. Из предложенного перечня выберите два вещества, для каждого из которых характерны высокая температура плавления, хорошая растворимость в воде и наличие ковалентной полярной связи.
- 1) SiO2
- 2) HCl
- 3) NaOH
- 4) KBr
- 5) Na2SO4
5. Среди предложенных веществ, расположенных в пронумерованных ячейках, выберите:
- А) соль серной кислоты,
- Б) щелочь,
- В) комплексную соль
6. К одной из пробирок с раствором гидроксида кальция добавили раствор соли X, а через другую пропустили газ Y. В результате в каждой из пробирок наблюдалось выпадение белого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1) CuCl2
- 2) NH3
- 3) FeCl3
- 4) CO2
- 5) NaHCO3
11. Из предложенного перечня выберите два вещества, в которых все атомы углерода находятся в состоянии sp2-гибридизации.
- 1) щавелевая кислота
- 2) толуол
- 3) стирол
- 4) ацетон
- 5) пропен
12. Из предложенного перечня выберите все вещества, из которых в одну стадию может быть получен алкин.
- 1) карбид кальция
- 2) 2,3-дибром-2,3-диметилбутан
- 3) бензол
- 4) хлорэтен
- 5) этиленгликоль
13. Из предложенного перечня выберите два продукта гидролиза метилового эфира аминоуксусной кислоты в солянокислой среде.
- 1) CH3Cl
- 2) CH3OH
- 3) CH3COONH4
- 4) NH2CH2COOH
- 5) [HOOC–CH2–NH3]Cl
17. Из предложенного перечня выберите все вещества, термическое разложение которых относится к окислительно-восстановительным реакциям:
- 1) гидрокарбонат калия
- 2) перманганат калия
- 3) карбонат магния
- 4) нитрит аммония
- 5) гидроксид алюминия
18. Из предложенного перечня выберите все воздействия, которые не влияют на скорость реакции, протекающей по схеме: Cuଶା + Zn = Cu + Z
- 1) понижение давления
- 2) понижение температуры
- 3) уменьшение концентрации ионов цинка
- 4) добавление металлической меди
- 5) добавление воды в реакционную колбу
23. В реактор постоянного объема поместили оксид серы (IV) и оксид серы (VI). В результате протекания обратимой реакции 2SO3 (г) ⇆ O2 (г) + 2SO2 (г) в системе установилось химическое равновесие. Исходная концентрация оксида серы (VI) равна 2 моль/л, а равновесные концентрации кислорода и оксида серы (IV) равны 0,5 моль/л и 1,8 моль/л соответственно. Определите равновесную концентрацию оксида серы (VI) (X) и исходную концентрацию оксида серы (IV) (Y). Выберите из списка номера правильных ответов:
- 1) 0,2 моль/л
- 2) 0,5 моль/л
- 3) 0,8 моль/л
- 4) 1,0 моль/л
- 5) 1,3 моль/л
- 6) 2,8 моль/л
26. Вычислите массу соли (в граммах), которую нужно добавить к 182 г 5% раствора этой же соли, чтобы получить 13,55%-ный раствор. Ответ запишите с точность до целых.
27. При сгорании 8,4 г этилена выделяется 423,3 кДж теплоты. Вычислите количество теплоты, которое выделится при сгорании 0,896 м3 (при н.у.) этилена. Ответ запишите с точностью до целых.
28. Вычислите массу угля, содержащего 4% негорючих примесей, необходимую для полного восстановления 116 г железной окалины. Примите, что в ходе реакции образуется угарный газ. Ответ дайте в граммах с точностью до целых.
29. Из предложенного перечня выберите два вещества, между которыми протекает окислительно-восстановительная реакция. В ходе этой реакции образуется белый осадок, а окислитель принимает один электрон (в расчете на один атом). Запишите уравнение реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30. Из предложенного перечня веществ выберите два вещества, принадлежащих к одинаковой группе веществ, между которыми протекает реакция ионного обмена. Раствор одного из реагентов окрашен. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с использованием выбранных веществ.
31. На концентрированную соляную кислоту подействовали бихроматом натрия. Образовавшееся при этом простое вещество прореагировало с кремнием при нагревании. Продукт реакции добавили к необходимому количеству раствора гидроксида калия. Через полученный раствор пропустили избыток углекислого газа и наблюдали образование осадка. Составьте уравнения четырех описанных реакций.
33. Для полного сжигания порции некоторого органического вещества Х необходимо 7,39 л (н. у.) кислорода, при этом образуется углекислый газ, 1,46 г хлороводорода и 1,8 г воды. Известно, что вещество Х может быть получено при взаимодействии углеводорода Y симметричного строения с избытком хлороводорода. На основании данных задачи:
- 1. Проведите необходимые вычисления и установите молекулярную формулу органического вещества Х;
- 2. Составьте структурную формулу вещества Х, которая однозначно отражает порядок связи атомов в его молекуле;
- 3. Напишите уравнение реакции вещества Y с подкисленным серной кислотой раствором перманганата калия, используя структурную формулу вещества.
34. 66,1 г смеси медного купороса (CuSO4 · 5H2O) и десятиводного сульфата натрия, содержащую 2,0408 · 1025 протонов, внесли в дистиллированную воду и получили раствор, в котором массовая концентрация ионов меди равна 4%. От этого раствора отобрали порцию массой 64 г и добавили к ней 3,92 г железных опилок. Вычислите массовые доли веществ в полученном растворе после окончания реакций.
Вариант №8 ЕГЭ 2023 по химии с ответами
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
- 1) С
- 2) F
- 3) O
- 4) Sn
- 5) Ge
Задание 1. Определите, в атомах каких из указанных в ряду элементов общее число p-электронов не превышает общее число s-электронов.
Задание 2. Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одной группе. Расположите выбранные элементы в порядке уменьшения основных свойств соответствующих им высших оксидов. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Задание 3. Из числа указанных в ряду элементов выберите два элемента, высшая степень окисления которых численно не совпадает с номером группы.
Задание 4. Из предложенного перечня выберите два элемента, атомы которых образуют с водородом более длинную ковалентную связь по сравнению с остальными.
- 1) O
- 2) Se
- 3) I
- 4) F
- 5) Br
Задание 6. К одной из пробирок, содержащей раствор гидроксида натрия, добавили раствор вещества Х, а к другой – раствор соли Y. В результате в первой пробирке выделился газ с резким запахом, а во второй выпал белого осадка. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
- 1) BaCl2
- 2) H2SO4
- 3) Ca(HCO3)2
- 4) K2S
- 5) NH4Cl
Задание 7. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 11. Из предложенного перечня веществ выберите два вещества, в молекулах которых содержится система сопряженных связей.
- 1) ацетилен
- 2) толуол
- 3) циклопентан
- 4) изопрен
- 5) пентадиен-1,4
Задание 12. Из предложенного перечня выберите все вещества, которые взаимодействуют с пропеновой кислотой, но не взаимодействуют с этиленгликолем.
- 1) водород
- 2) гидроксид меди (II)
- 3) метанол
- 4) бромная вода
- 5) гидрокарбонат калия
Задание 13. Из предложенного перечня выберите два вещества, которые не вступают в реакцию этерификации.
- 1) целлюлоза
- 2) фенилаланин
- 3) глюкоза
- 4) метиламин
- 5) анилин
Задание 14. Установите соответствие между органическими веществами и органическими продуктами их взаимодействия с подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 17. Выберите все пары веществ, между которыми протекает окислительновосстановительная реакция.
- 1) хромат калия и ацетат серебра
- 2) сероводород и бром ная вода
- 3) оксид азота (IV) и вода
- 4) оксид меди (II) и азотная кислота (конц.)
- 5) оксид меди (II) и иодоводород
Задание 18. Выберите все металлы, которые при комнатной температуре реагируют с водой со значительной скоростью:
- 1) Ca
- 2) Ag
- 3) Fe
- 4) Rb
- 5) Li
Задание 19. Установите соответствие между формулой иона и свойством, которое он может проявлять в окислительно-восстановительных реакциях: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 20. Установите соответствие между формулами солей и продуктами, которые выделятся на графитовом катоде при электролизе их водных растворов: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задание 23. В реактор постоянного объема поместили аммиак и нагрели его в присутствии катализатора. В результате протекания обратимой реакции в системе установилось химическое равновесие. Известно, что исходная концентрация аммиака равна 0,8 моль/л, а в равновесной смеси количество вещества аммиака составляет 60% от суммарного количества веществ газов. Определите равновесные концентрации азота (X) и водорода (Y). Выберите из списка номера правильных ответов:
- 1) 0,10 моль/л
- 2) 0,24 моль/л
- 3) 0,30 моль/л
- 4) 0,48 моль/л
- 5) 0,60 моль/л
- 6) 0,80 моль/л
Задание 26. К 400 г 12%-го раствора соли добавили раствор этой же соли и получили 520 г 18%-го раствора. Вычислите массовую долю соли в добавленном растворе. Ответ запишите с точностью до целых.
Задание 27. Вычислите тепловой эффект реакции 2CH3OH + 3O2 = 4H2O + 2CO2 + Q, если при сгорании некоторого количества метанола образовалось 63,84 л (н. у.) углекислого газа и выделилось 2069,1 кДж теплоты. Ответ запишите с точностью до целых.
Задание 28. В ходе спиртового брожения глюкозы массой 72 г получено 12,096 л (н. у.) углекислого газа. Вычислите долю выхода углекислого газа в процентах от теоретического. Ответ дайте в процентах с точностью до десятых.
Задание 29. Из предложенного перечня выберите вещества, между которыми в щелочной среде протекает окислительно-восстановительная реакция. В ходе этой реакции наблюдается образование раствора желтого цвета. Запишите уравнение реакции с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Задание 30. Из предложенного перечня веществ выберите кислую соль и вещество, между которыми протекает реакция ионного обмена без видимых признаков. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с использованием выбранных веществ.
Задание 31. Серебро растворили в концентрированной азотной кислоте при нагревании. Выделившийся газ пропустили над нагретым цинком. Полученное твердое вещество обработали раствором гидроксида калия. Через полученный раствор пропустили избыток сероводорода и наблюдали выпадение осадка. Составьте уравнения четырех описанных реакций.
Задание 32.
Задание 33. При сгорании бескислородного органического вещества Х массой 31,79 г получено 7,62 л (н.у.) углекислого газа, 1,53 мл воды и бромоводород. Продукт гидролиза вещества Х в присутствии избытка щелочи содержит две функциональные группы, находящиеся на максимальном расстоянии друг от друга, и не взаимодействует с гидроксидом меди (II). На основании данных в задаче:
- 1. Проведите необходимые вычисления и установите молекулярную формулу органического вещества Х;
- 2. Составьте структурную формулу вещества Х, которая однозначно отражает порядок связи атомов в его молекуле;
- 3. Напишите уравнение реакции гидролиза вещества Х в присутствии избытка гидроксида натрия, используя структурную формулу вещества.
Задание 34. 186,25 г 16%-го раствора хлорида калия подвергли электролизу (с инертными электродами). Процесс прекратили, когда на катоде выделилось 13,44 л (при н. у.) газа. Через оставшийся раствор пропустили сероводород, при этом в конечном растворе общее число атомов калия и серы оказалось равным 3,311 · 1023. Вычислите массовые доли веществ в конечном растворе.
Смотрите также на нашем сайте:
ЕГЭ по химии 11 класс 2023. Новый тренировочный вариант №5 — №221107 (задания и ответы)
Метки: 11 класс ЕГЭ химия
Тренировочная работа №3 статград ЕГЭ 2022 по химии 11 класс задания и ответы для вариантов ХИ2110301, ХИ2110302, ХИ2110303, ХИ2110304. Официальная дата проведения работы: 21.01.2022 (21 января 2022 год).
Скачать варианты ХИ2110301-ХИ2110302
Скачать варианты ХИ2110303-ХИ2110304
Все ответы (решения) и задания (без водяного знака)
Работа статград по химии состоит из двух частей, включающих в себя 34 задания. Часть 1 содержит 28 заданий с кратким ответом, часть 2 содержит 6 заданий с развёрнутым ответом.
Тренировочные варианты статград ХИ2110301 и ХИ2110302 ЕГЭ 2022 по химии 11 класс:
Решать варианты ХИ2110303 и ХИ2110304:
Сложные задания и ответы с 1 варианта:
Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) K, 2) Cl, 3) Li, 4) Be, 5) P Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1)У каких из указанных элементов ровно треть от общего числа электронов находится на внешнем уровне (в основном состоянии)? Запишите номера выбранных элементов в порядке возрастания.
Правильный ответ: 35
2)Из указанного ряда выберите три металла. Расположите их в порядке уменьшения радиуса атома. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Правильный ответ: 134
3)Из указанного ряда выберите два элемента, которые в соединениях могут проявлять степень окисления +3. Запишите в поле ответа номера выбранных элементов в порядке возрастания.
Правильный ответ: 25
4)Сколько всего электронов участвуют в образовании химических связей в молекуле NH3 и в ионе NH4 +? Запишите два выбранных ответа в порядке возрастания. 1) 0 2) 2 3) 4 4) 6 5) 8
Правильный ответ: 45
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) кислотного оксида; Б) щёлочи; В) двойной соли.
Правильный ответ: 264
6)В двух пробирках находился оксид меди(II). В первую пробирку добавили раствор вещества Х, а во вторую – избыток концентрированного раствора вещества Y. В обеих пробирках осадок полностью растворился. В первой пробирке раствор приобрёл голубой цвет, а во второй – зелёный. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции. 1) NaOH 2) Na2CO3 3) HCl 4) AgNO3 5) H2SO4
Правильный ответ: 53
11)Из предложенного перечня выберите две пары изомеров. 1) пентан и циклопентан 2) гексан и 2,3-диметилбутан 3) фенол и бензиловый спирт 4) уксусная кислота и метилформиат 5) метиламин и диметиламин.
Правильный ответ: 24
12)Из предложенного перечня выберите все вещества, при гидролизе которых в кислой среде образуется уксусная кислота. 1) CH3CN 2) CH3OC2H5 3) CH3CHCl2 4) CH3C(O)Cl 5) CH3COOC2H5
Правильный ответ: 145
13)Из предложенного перечня выберите два вещества, которые не вступают в реакцию гидролиза. 1) глицилаланин 2) фенилаланин 3) целлюлоза 4) дезоксирибоза 5) трипальмитат глицерина
Правильный ответ: 24
17)Из предложенного перечня выберите все реакции элиминирования (отщепления). 1) нагревание пропанола с концентрированной серной кислотой 2) нагревание бензола с концентрированной серной кислотой 3) нагревание 1,2-дихлорэтана с магнием 4) взаимодействие 1,2-дихлорэтана со спиртовым раствором щёлочи 5) взаимодействие метилацетата с водным раствором щёлочи
Правильный ответ: 134
18)Укажите все факторы, от которых зависит скорость разложения пероксида водорода в водном растворе. 1) температура 2) объём раствора 3) давление кислорода над раствором 4) концентрация пероксида водорода 5) действие света на раствор
Правильный ответ: 145
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих концентрацию 0.1 моль/л. Расположите эти вещества в порядке возрастания pH водного раствора. Запишите номера веществ в правильном порядке. 1) NH3 2) NH4Cl 3) KCl 4) KOH
Правильный ответ: 2314
23)В реакторе постоянного объёма смешали азот и водород в мольном соотношении 1:3. Смесь нагрели и добавили катализатор. Через некоторое время установилось равновесие: N2(г) + 3H2(г) ←→ 2NH3(г) Используя данные таблицы, найдите исходную концентрацию H2 (X) и равновесную концентрацию N2 (Y)
Правильный ответ: 62
26)Растворимость нитрата калия в воде при 60 о С составляет 110 г на 100 г воды. Сколько граммов нитрата калия содержится в 170 г насыщенного раствора при этой температуре? (Запишите число с точностью до целых.)
Правильный ответ: 89
27)Термохимическое уравнение сгорания ацетилена имеет вид: 2C2H2 + 5O2 = 4CO2 + 2H2O(ж) + 2600 кДж. Сколько теплоты (в кДж) выделится при сжигании 5,6 л (н. у.) ацетилена? (Запишите число с точностью до целых.)
Правильный ответ: 325
28)Сколько литров аммиака (н. у.) потребуется для получения 90 г карбамида (NH2)2CO по реакции с углекислым газом, если выход продукта составляет 60 %? (Запишите число с точностью до целых.)
Правильный ответ: 112
29)Для выполнения заданий 29 и 30 используйте следующий перечень веществ: хлорид хрома(III), гидрокарбонат калия, пероксид водорода, гидроксид калия, сульфат аммония, магний. Допустимо использование водных растворов веществ и воды в качестве среды для протекания реакций. Из предложенного перечня выберите вещества, между которыми протекает окислительно-восстановительная реакция, приводящая к изменению цвета раствора, но без образования осадка. В ответе запишите уравнение реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите два вещества, которые вступают в реакцию ионного обмена, при этом выделяется газ, но не выпадает осадок. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31)Газ, полученный при действии концентрированной соляной кислоты на твёрдый перманганат калия, пропустили через горячий крепкий раствор карбоната калия, в процессе реакции из раствора выделялся газ. При охлаждении полученного раствора из него выделились кристаллы, которые отфильтровали и высушили на воздухе. Кристаллы нагрели с красным фосфором, а продукты реакции растворили в воде и получили раствор, имеющий кислую среду. Напишите молекулярные уравнения четырёх описанных реакций.
33)Навеску сульфида железа(II) массой 14,08 г сожгли в атмосфере кислорода. Твёрдый остаток растворили в строго необходимом количестве 10%-й соляной кислоты, а в полученный раствор добавили порошок железа массой 20 г, нерастворившийся порошок отфильтровали. Рассчитайте массу полученного раствора и массовую долю соли в нем. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
34)Органическое вещество представляет собой летучую жидкость с характерным приятным запахом. При сжигании 11,1 г этого вещества было получено 10,08 л углекислого газа (н. у.) и 8,1 г воды. Установите молекулярную формулу вещества и определите его строение, если известно, что оно даёт реакцию «серебряного зеркала» и гидролизуется с образованием двух органических соединений. Напишите уравнение реакции вещества с аммиачным раствором оксида серебра (в уравнении используйте структурные формулы органических веществ).
Сложные задания и ответы с 2 варианта:
Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) Ca, 2) O, 3) F, 4) Cr, 5) S Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1)У каких из указанных элементов число электронов на внешнем уровне (в основном состоянии) больше числа внутренних электронов? Запишите номера выбранных элементов в порядке возрастания.
Правильный ответ: 23
2)Из указанного ряда выберите три неметалла. Расположите их в порядке увеличения радиуса атома. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Правильный ответ: 325
3)Из указанного ряда выберите два элемента, которые в соединениях могут проявлять степень окисления +6. Запишите в поле ответа номера выбранных элементов в порядке возрастания.
Правильный ответ: 45
4)Сколько всего электронов участвуют в образовании химических связей в молекуле H2O и в ионе H3O+? Запишите два выбранных ответа в порядке возрастания. 1) 0 2) 2 3) 4 4) 6 5) 8
Правильный ответ: 34
6)В двух колбах находился раствор карбоната калия. В первую колбу добавили раствор вещества Х, а во вторую – раствор вещества Y. В обеих колбах выпал осадок, но в первой колбе также выделился газ. Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
Правильный ответ: 24
11)Из предложенного перечня выберите две пары изомеров. 1) бензол и гексадиин-1,5 2) уксусная кислота и метилацетат 3) гексен-2 и гексин-2 4) пиридин и анилин 5) пропиламин и триметиламин
Правильный ответ: 15
12)Из предложенного перечня выберите все вещества, при взаимодействии которых с водой в соответствующих условиях образуется уксусный альдегид. 1) C2H2 2) CH3CN 3) CH3CHCl2 4) CH3CCl3 5) CH3C(O)OCH=CH2
Правильный ответ: 135
13)Из предложенного перечня выберите два вещества, которые вступают в реакцию гидролиза. 1) сахароза 2) тристеарат глицерина 3) рибоза 4) цистеин 5) олеиновая кислота
Правильный ответ: 12
17)Из предложенного перечня выберите все реакции замещения. 1) взаимодействие пропена с хлором при сильном нагревании 2) взаимодействие пропена с бромоводородом 3) взаимодействие толуола с азотной кислотой 4) взаимодействие водорода с бензолом 5) взаимодействие этанола с уксусной кислотой в присутствии серной кислоты
Правильный ответ: 135
18)Укажите все факторы, от которых зависит скорость реакции порошка диоксида марганца с концентрированной соляной кислотой. 1) давление хлора над раствором 2) форма реакционного сосуда 3) pH в растворе кислоты 4) степень измельчения порошка 5) температура
Правильный ответ: 345
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих концентрацию 0.01 моль/л. Расположите эти вещества в порядке уменьшения pH водного раствора. Запишите номера веществ в правильном порядке. 1) MgCl2 2) Ca(OH)2 3) Ca(NO3)2 4) HClO4
Правильный ответ: 2314
26)В 115 г насыщенного при определённой температуре раствора карбоната калия содержится 62 г соли. Чему равна растворимость карбоната калия при этой температуре (в г соли на 100 г воды)? (Запишите число с точностью до целых.)
Правильный ответ: 117
27)Термохимическое уравнение сгорания этана имеет вид: 2C2H6 + 7O2 = 4CO2 + 6H2O(ж) + 3115 кДж. Сколько литров этана (н. у.) вступило в реакцию, если в результате выделилось 445 кДж теплоты? (Запишите число с точностью до десятых.)
Правильный ответ: 6,4
28)Из смеси 1 м3 угарного газа и 2 м3 водорода получен 1 кг метанола. Чему равен выход метанола (в %)? Объёмы газов даны при нормальных условиях. (Запишите число с точностью до целых.)
Правильный ответ: 70
29)Для выполнения заданий 29 и 30 используйте следующий перечень веществ: серная кислота, оксид магния, карбонат натрия, хлорид меди(I), аммиачная вода, ацетат свинца(II). Допустимо использование водных растворов веществ и воды в качестве среды для протекания реакций. Из предложенного перечня выберите вещества, между которыми протекает окислительно-восстановительная реакция с выделением газа. В ответе запишите уравнение реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня выберите вещества, которые вступают в реакцию ионного обмена с образованием осадка, но без выделения газа. В ответ запишите уравнение только одной из возможных реакций. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31)Белый фосфор подожгли на воздухе в условиях недостатка кислорода. Полученное твёрдое вещество растворили в воде. Раствор разделили на две части. К первой добавили подкисленный раствор перманганата калия и наблюдали обесцвечивание. Вторую часть раствора выпарили и полученное вещество сильно нагрели, при этом выделился газ. Напишите молекулярные уравнения четырёх описанных реакций.
33)Навеску сульфида меди(II) массой 14,4 г сожгли в атмосфере кислорода. Твёрдый остаток растворили в строго необходимом количестве 10 %-й серной кислоты, а полученный раствор подвергли электролизу с инертным анодом, в результате чего на аноде выделилось 1,12 л газа (н. у.). Рассчитайте массу полученного после электролиза раствора и массовые доли веществ в нём. Примите Ar(Cu) = 64. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
34)Органическое вещество представляет собой нелетучую, высококипящую жидкость со слабым характерным запахом, с водой смешивается в любых соотношениях. Его используют в качестве антифриза при противогололёдной обработке самолётов. При сжигании 11,4 г этого вещества было получено 10,08 л углекислого газа (н. у.) и 10,8 г воды. Установите молекулярную формулу вещества и определите его строение, если известно, что оно реагирует с натрием, а при дегидратации под действием серной кислоты превращается в соединение, содержащее шестичленный цикл. Напишите уравнение дегидратации (в уравнении используйте структурные фформулы органических веществ).
Другие тренировочные пробные варианты ЕГЭ по химии 11 класс:
Варианты ХИ2110201-ХИ2110204 ЕГЭ 2022 статград по химии 11 класс задания и ответы
Статград работы по химии задания и ответы
Share the post «Варианты ХИ2110301-ХИ2110304 ЕГЭ 2022 работа статград химия 11 класс с ответами»
- VKontakte
Метки: ЕГЭ 2022заданияответыстатградтренировочная работахимия 11 класс
За это задание ты можешь получить 1 балл. На решение дается около 2 минут. Уровень сложности: базовый.
Средний процент выполнения: 51.7%
Ответом к заданию 11 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Задача 1
Из предложенного перечня выберите два класса веществ, в молекулах которых присутствует функциональная группа
- спирты
- кетоны
- простые эфиры
- фенолы
- пептиды
Запишите в поле ответа номера выбранных классов веществ.
Решение
Функциональная группа -С(О)- (карбонильная группа) присутствует в кетонах в составе кетогруппы, в альдегидах в составе альдегидной группы -СНО и в кислотах в составе карбоксильной группы -СООН. Среди предложенных классов есть кетоны а также пептиды — производные аминокислот, тоже несущие карбонильную группу — в составе пептидной связи -С(О)-NH-.
Ответ: 25
Задача 2
Из предложенного перечня выберите два вещества, которые имеют общую формулу $С_{n}H_{2n}$.
- бензол
- циклогексан
- гексан
- гексен
- гексин
Запишите в поле ответа номера выбранных веществ.
Решение
Такая формула характерна для алкенов и циклоалканов, так как они теряют по два атома водорода относительно алканов благодаря двойной связи или циклизации.
Ответ: 24
Задача 3
Из предложенного перечня выберите два типа гибридизации орбиталей атома углерода, которые имеются в молекуле 2-метилбутена-2.
- $sp^3$
- $sp^2$
- sp
- $sp^3$ и sp
- $sp^2$ и sp
Запишите в поле ответа номера выбранных типов гибридизации.
Решение
Тип гибридизации атома углерода зависит от количества атомов, с которыми он связан. В молекуле 2-метилбутена-2 $СН_3-С(СН_3)=СН-СН_3$ присутствуют атомы углерода, образующие связи с 4 атомами, например первый, они имеют $sp^3$-гибридизацию, и образующий связь с тремя атомами — второй, он имеет $sp^2$-гибридизацию.
Ответ: 12
Задача 4
Из предложенного перечня выберите два ряда веществ, которые являются гомологами.
- $CH_3NO_2$ и $CH_3NH_2$
- $CH_3OH$ и $CH_3COOH$
- $CH_3CH_2CH_2OH$ и $CH_3OH$
- $CH_3Cl$ и $CH_3Br$
- $CH_3CHO$ и $C_2H_5CHO$
Запишите в поле ответа номера выбранных рядов веществ.
Решение
Гомологическим рядом называют ряд веществ, которые имеют общую формулу, похожее строение, закономерно изменяющиеся физические свойства, общие способы получения и общие химические свойства и отличаются по составу на одну или несколько групп $CH_2$, которая называется гомологической разностью. Гомологи — вещества, принадлежащие к одному гомологическому ряду.
1) $CH_3NO_2$ — нитрометан, класс нитросоединений; $CH_3NH_2$ — метиламин (аминометан), класс предельных первичных аминов. Вещества принадлежат к разным классам.
2) $CH_3OH$ — метанол (метиловый спирт), класс предельных одноатомных спиртов; $CH_3COOH$ — уксусная кислота. Вещества принадлежат к разным классам.
3) $CH_3CH_2CH_2OH$ — пропанол-1, $CH_3OH$ — метанол. Оба вещества относятся к классу спиртов, отличаются по составу на две группы $–CH_2$, имеют похожее строение (линейная цепь углеродных атомов, группа –OH находится у крайнего атома углерода) и общую формулу $C_{n}H_{2n+2}O (C_{n}H_{2n+1}OH$), т. е. являются гомологами.
4) $CH_3Cl$ — хлорметан и $CH_3Br$ — бромметан. Вещества отличаются качественным составом.
5) $CH_3CHO$ — этаналь, класс альдегидов предельного ряда; $C_2H_5CHO$ — пропаналь, класс альдегидов предельного ряда. Оба вещества относятся к классу альдегидов, отличаются по составу на группу $–CH_2$, имеют похожее строение (линейная цепь углеродных атомов) и общую формулу $C_{n}H_{2n}O$, т. е. являются гомологами.
Ответ: 35
Задача 5
Из предложенного перечня выберите два вещества, в молекулах которых имеется две π-связи.
- акриловая кислота
- пропен
- бутан
- бутен
- ацетилен
Запишите в поле ответа номера выбранных веществ.
Решение
Двойная связь состоит из одной σ-связи и одной π-связи.
Тройная связь состоит из одной σ-связи и двух π-связей.
1) Акриловая (пропеновая) кислота $CH_2=CH–C(O)–OH$. В молекуле имеется одна двойная C=C связь и одна двойная C=O связь. Ответ правильный.
2) Пропен $CH_2=CH–CH_3$. В молекуле имеется одна двойная С=С связь. Ответ неверный.
3) Бутан $CH_3–CH_2–CH_2–CH_3$. В молекуле нет двойных С=С связей. Ответ неверный.
4) Бутен, $CH_2=CH–CH_2–CH_3$ или $CH_3–CH=CH–CH_3$. В молекуле любого из бутенов имеется только одна двойная C=C связь. Ответ неверный.
5) Ацетилен, или этин, H–C≡C–H. В молекуле имеется тройная C≡C связь. Ответ правильный.
Ответ: 15
Задача 6
Из предложенного перечня выберите два вещества, которые относятся к тем же гомологическим рядам, что и вещества, имеющие молекулярную формулу $С_5Н_{10}$.
- метан
- этилен
- бензол
- циклопропан
- ацетилен
Запишите в поле ответа номера выбранных веществ.
Решение
Общую формулу гомологического ряда $C_nH_{2n}$ имеют алкены и циклоалканы. В предложенном списке веществ есть алкен – этилен, и циклоалкан – циклопропан.
Ответ: 24
Задача 7
Из предложенного перечня выберите два вещества, которые являются изомерами 2-метилбутана.
- $CH_3–CH_2–CH_2–CH_2–CH_3$
- $CH_3–CH_2–CH_2–CH_3$
Запишите в поле ответа номера выбранных веществ.
Решение
Изомеры — вещества, имеющие одинаковый состав, то есть одинаковую молекулярную формулу, но разное строение. 2-метилбутан $СН_3-СН(СН_3)-СН_2-СН_3$ имеет молекулярную формулу $С_5Н_{12}$. Такую же молекулярную формулу имеют все алканы с пятью атомами углерода, в том числе представленный под номером 1 н-пентан и представленный под номером 2 1,2-диметилпропан.
Ответ: 12
Задача 8
Из предложенного перечня выберите два вещества, которые являются структурными изомерами пентена-1.
- циклопентан
- пентадиен-1,3
- 2-метилбутан
- 2-метилбутен-2
- 3-метилбутин-1
Запишите в поле ответа номера выбранных веществ.
Решение
Пентен-1 – алкен, то есть имеет 5 атомов углерода и 10 атомов водорода, его изомерами являются циклопентан, который также теряет два атома водорода из-за кольцевой связи, а также 2-метилбутен-2, который теряет 2 атома водорода в той же двойной связи.
Ответ: 14
Задача 9
Из предложенного перечня выберите две пары веществ, которые являются гомологами.
- этилен и метан
- пропен и этен
- циклобутан и бутан
- пропан и бутан
- этин и этен
Запишите в поле ответа номера выбранных пар веществ.
Решение
Гомологи — вещества, принадлежащие к одному классу. В первой паре представлен алкен и алкан, во второй — два алкена, в третьей — циклоалкан и алкан, в четвёртой — два алкана, в пятой — алкин и алкен. Таким образом, гомологи представлены в парах номер 2 и 4.
Ответ: 24
Задача 10
Из предложенного перечня выберите два класса органических веществ, к которым может относиться вещество, формула которого $C_4H_{10}O$.
- спирты
- альдегиды
- простые эфиры
- сложные эфиры
- кетоны
Запишите в поле ответа номера выбранных классов веществ.
Решение
Общей формулой гомологического ряда спиртов является $С_{n}H_{2n+1}ОH$, что как раз соответствует данному веществу (его можно переписать как $C_{4}H_{9}OH$). Общей формулой гомологического ряда простых эфиров является $С_{n}H_{2n+2}О$, что также соответствует данному веществу.
Ответ: 13
Задача 11
Из предложенного перечня выберите два вещества, между молекулами которых образуются водородные связи.
- этанол
- этан
- этаналь
- ацетон
- этановая кислота
Запишите в поле ответа номера выбранных веществ.
Решение
Водородные связи образуются между молекулами веществ, содержащих атом водорода непосредственно связанным с атомом кислорода. Из органических веществ это спирты, фенолы, карбоновые кислоты, аминокислоты. Среди представленных веществ есть спирт — этанол и карбоновая кислота — этановая.
Ответ: 15
Задача 12
Из предложенного перечня выберите два вещества, которые имеют систему сопряжённых связей.
- фенол
- бутадиен-1,3
- циклогексен
- 2-метилбутан
- бутин-1
Запишите в поле ответа номера выбранных веществ.
Решение
Систему сопряжённых связей имеют, прежде всего, сопряжённые диены (две двойных связи разделены одинарной). Но помимо них сопряжённые двойные связи формально присутствуют в бензольном кольце, что наглядно отражает формула Кекуле. Среди предложенных веществ есть сопряжённый диен — бутадиен-1,3 $CH_2=CH-CH=CH_2$ и соединение, имеющее в составе бензольное кольцо — фенол $С_6Н_5ОН$.
Ответ: 12
Задача 13
Из предложенного перечня выберите две пары веществ, каждое из которых содержит функциональную группу –ОН.
- фенол и рибоза
- диэтиловый эфир и глюкоза
- сахароза и формальдегид
- фенол и толуол
- пропанол и крезол
Запишите в поле ответа номера выбранных пар веществ.
Решение
Функциональную группу –ОН содержат спирты, фенолы и углеводы. Из предложенных пар веществ эту группу имеют фенол и рибоза (углевод) — номер 1, пропанол (спирт) и крезол (метилфенол).
Ответ: 15
Задача 14
Из предложенного перечня выберите два вещества, которые имеют общую формулу СnH2n.
- бензол
- циклогексан
- гексан
- гексен
- гексин
Запишите в поле ответа номера выбранных веществ.
Решение
Общая формула $С_nH_{2n}$ соответствует классу алкенов, а также их изомеров — циклоалканов. Среди предложенных веществ есть циклоалкан — циклогексан ($С_6Н_{12}$) и алкен — гексен ($С_6Н_{12}$).
Ответ: 24
Задача 15
Из предложенного перечня выберите два вещества, которые относятся к кетонам.
- формалин
- ацетон
- этилацетат
- бутанон
- фруктоза
Запишите в поле ответа номера выбранных веществ.
Решение
О принадлежности к классу кетонов в названии вещества свидетельствует суффикс -он-. По этому принципу выбираем бутанон, а ацетон — это тривиальное название диметилкетона (пропанона).
Ответ: 24
Задача 16
Из предложенного перечня выберите два вещества, которые являются гомологами глицина.
- $CH_3CH_2CONH_2$
- $CH_3CH(NH_2)COOH$
- $CH_3CH_2COOH$
- $CH_3CH_2CH(NH_2)COOH$
- $CH_3CH_2NH_2$
Запишите в поле ответа номера выбранных веществ.
Решение
Гомологи — вещества, относящиеся к одному классу. Глицин $NH_2-СН_2-СООН$ — аминокислота. К этому же классу относятся вещества, имеющие в составе карбоксильну группу -СООН и аминогруппу $-NH_2$. Подходят соединения под номерами 2 и 4.
Ответ: 24
Задача 17
Из предложенного перечня выберите два вещества, которые являются гомологами бензола.
- циклогексан
- толуол
- ацетилен
- винилбензол
- фенилэтан
Запишите в поле ответа номера выбранных веществ.
Решение
Гомологи — вещества, принадлежащие одному классу соединений. Безол — ароматический углеводород, то есть содержит бензольное кольцо и состоит только из углерода и водорода. Его гомологами являются толуол (метилбензол) и фенилэтан. Винилбензол не является гомологом, так как содержит непредельный радикал.
Ответ: 25