в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 260 … 141–160 | 161–180 | 181–200 | 201–220 | 221–240 | 241–260
Добавить в вариант
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
В уравнениях приведите структурные формулы органических веществ.
Источник: СтатГрад: Тренировочная работа 28.11.2018. Вариант ХИ10202.
Установите соответствие между веществом и основным способом его промышленного производства: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) железо
Б) водород
В) хлор
СПОСОБ ПРОМЫШЛЕННОГО ПРОИЗВОДСТВА
1) паровая конверсия природного газа
2) восстановление оксида углеродом
3) перегонка воздуха
4) электролиз раствора соли
Запишите в таблицу выбранные цифры под соответствующими буквами.
Гашёную известь сплавили с твёрдым хлоридом аммония, образовавшийся при этом газ пропустили над нагретым оксидом меди (II). Получившееся при этом твёрдое вещество обработали разбавленной азотной кислотой (при этом выделился бесцветный газ), а оставшийся раствор подвергли электролизу. Напишите уравнения четырёх указанных реакций.
Источник: ЕГЭ по химии 2019. Основная волна. Вариант 1
Установите соответствие между реагирующими веществами и углеводородом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) хлорметан и натрий
Б) ацетат натрия и гидроксид натрия
В) пропионат натрия и вода, электролиз
Г) 1,2-дихлорэтан и спиртовой раствор гидроксида натрия
ПРОДУКТ РЕАКЦИИ — УГЛЕВОДОРОД
1) метан
2) этан
3) пропан
4) н-бутан
5) ацетилен
6) этилен
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Сколько граммов хлорида натрия требуется для получения 6,72 л газообразного хлора (н. у.) методом электролиза? Примите Ответ запишите с точностью до десятых.
Установите соответствие между реагирующими веществами и продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТ РЕАКЦИИ
1) пропан
2) бутан
3) этан
4) этен
5) пропен
6) уксусная кислота
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по химии 2020. Основная волна. Вариант 2
Дана схема превращений:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Кристаллогидрат сульфата алюминия, в котором массовая доля серы меньше массовой доли кислорода в 5 раз, растворили в воде с образованием раствора массой 722,4 г. Полученный раствор подвергли электролизу до выделения на аноде 35,84 л (н. у.) газа. К образовавшемуся раствору добавили 424 г 10%-го раствора карбоната натрия, после всех реакций его массовая доля уменьшилась в 10 раз. Определите массу растворенного кристаллогидрата сульфата алюминия. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Источник: ЕГЭ по химии 2021. Основная волна. Вариант 2
Электролиз 522 г 10 %-го раствора нитрата бария проводили до тех пор, пока на катоде не образовалось 94,08 л газа (н. у.). Полученный раствор смешали с насыщенным при комнатной температуре раствором сульфата меди(II), приготовленным при добавлении воды к медному купоросу массой 100 г. После окончания всех реакций массовая доля сульфата меди(II) уменьшилась в 4 раза. Вычислите растворимость безводного сульфата меди(II) при комнатной температуре (в г на 100 г воды). В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Источник: Задания 34 ЕГЭ–2021 по химии
При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите молекулярные уравнения четырех описанных реакций.
Источник: Демонстрационная версия ЕГЭ—2022 по химии, Демонстрационная версия ЕГЭ—2023 по химии
Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Бромоводородную кислоту нейтрализовали карбонатом натрия. Полученный раствор подвергли электролизу. Газ, выделившийся на катоде, пропустили при нагревании над оксидом меди(II). Образовавшееся твёрдое вещество поместили в концентрированный раствор азотной кислоты. Напишите уравнения четырёх описанных реакций.
Источник: ЕГЭ по химии 2022. Досрочная волна
Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Установите соответствие между схемой реакции и веществом X, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Установите соответствие между названием газа и основным способом его получения в промышленности: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ
1) перегонка нефти
2) пиролиз нефти
3) перегонка жидкого воздуха
4) электролиз раствора хлорида натрия
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: СтатГрад: Тренировочная работа 09.11.2022. Вариант ХИ2210201.
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) этан
2) бутан
3) гексан
4) гексин-3
5) гексадиен-2,4
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Источник: СтатГрад: Тренировочная работа 09.11.2022. Вариант ХИ2210202.
Навеску сульфида меди(II) массой 14,4 г сожгли в атмосфере кислорода. Твёрдый остаток растворили в строго необходимом количестве 10 %-й серной кислоты, а полученный раствор подвергли электролизу с инертным анодом, в результате чего на аноде выделилось 1,12 л газа (н. у.). Рассчитайте массу полученного после электролиза раствора и массовые доли веществ в нём. Примите В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
Задания Д26 № 945
Процесс переработки каменного угля в промышленности получил название
1) коксования
2) дегидрирования
3) электролиза
4) ректификации
Провели электролиз раствора хлорида натрия. К полученному раствору добавили хлорид железа (III). Выпавший осадок отфильтровали и прокалили. Твёрдый остаток растворили в иодоводородной кислоте.
Напишите уравнения четырёх описанных реакций.
Источник: ЕГЭ по химии 10.06.2013. Основная волна. Дальний Восток. Вариант 5
Всего: 260 … 141–160 | 161–180 | 181–200 | 201–220 | 221–240 | 241–260
ЕГЭ ПО ХИМИИ ЗАДАНИЕ 9
пЛАН
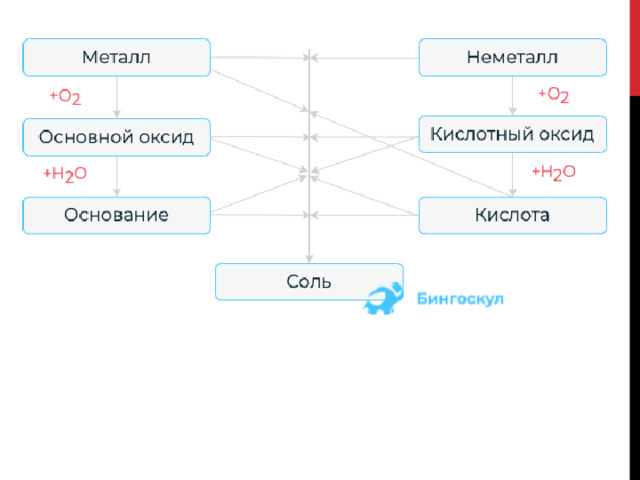
Взаимосвязь различных классов неорганических веществ
Как уже известно, существует четыре класса неорганических соединений. К ним относятся оксиды, основания, кислоты и соли. При подробном изучении способов получения каждого класса соединений можно проследить определенную взаимосвязь между всеми классами. Например, из кислот можно получить соли, из оксидов основания и так далее. Такая связь называется генетической .
Следовательно, генетическая связь – это связь между классами неорганических соединений, которая основана на получении веществ одного класса из веществ другого класса, а также их химических свойств.
На основании данной связи составляют генетические ряды , которые включают в себя представителей разных классов, но состоящие из одного элемента.
Генетическую связь можно представить в виде схемы.
Из данной схемы видно, что существует определенная взаимосвязь между классами. Основополагающими элементами генетического ряда являются либо металл, либо неметалл.
- Для получения оксида необходимо осуществить взаимодействие металла либо неметалла с кислородом.
- При взаимодействии с водой из основного оксида можно получить основание, а из кислотного – кислоту.
- Соль образуется при различных реакциях между всеми классами неорганических соединений. Например, металл + неметалл, основный оксид + кислотный оксид, основание + кислота и так далее.
Можно выделить два типа генетических рядов, которые мы и рассмотрим.
1. Генетический ряд металла
Металл → Основный оксид → Основание → Соль
Ряд кальция: Ca → CaO → Ca(OH) 2 → Ca Cl 2 ;
Ряд натрия: Na → Na 2 O → NaOH → Na 3 PO 4 ;
Ряд магния: Mg → MgO → Mg(OH) 2 → Mg(NO 3 ) 2 ;
Ряд железа: Fe → FeO → Fe(OH) 2 → FeSO4.
Рассмотрим взаимосвязь в данных рядах на примере магния.
Для получения оксида магния из чистого металла, осуществим реакцию взаимодействия с кислородом.
Mg + O 2 → MgO
При взаимодействии основного оксида с водой, в частности оксида магния, получим основание – гидроксид магния.
MgO + H2O → Mg(OH) 2
Для получения соли из нерастворимого основания, необходимо добавить кислоту.
Mg(OH) 2 + HNO 3 → Mg(NO 3 ) 2 + H 2 O
2. Генетический ряд неметалла
Неметалл → Кислотный оксид → Кислота → Соль
Ряд фосфора: P → P 2 O 5 →H 3 PO 4 → Na 3 PO 4 ;
Ряд углерода: C → CO 2 → H 2 CO 3 → CaCO 3 ;
Ряд серы: S → SO 2 → H 2 SO 3 → MgSO 3 ;
Ряд кремния: Si → SiO 2 → H 2 SiO 3 → K 2 SiO 3 .
Рассмотрим взаимосвязь в данных рядах на примере углерода.
Для получения оксида углерода осуществим реакцию взаимодействия с кислородом – горение. Протекает с выделением энергии.
C + O 2 → CO 2
При взаимодействии кислотного оксида с водой, в частности оксида углерода, получим угольную кислоту.
CO + H 2 O → H 2 CO 3
Для получения соли из кислоты, необходимо добавить основание.
Ca(OH) 2 + H 2 CO 3 → CaCO 3 ↓ + 2H 2 O
Важно!!!
Для составления генетических цепочек необходимо знать химические свойства каждого класса неорганических соединений, а также валентные возможности того элемента, который лежит в основе генетического ряда.
Задания для подготовки к егэ
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
Ответ: 43.
Пояснение
Вещества X и Y — различны. При этом Y — гидрокарбонат натрия, значит, из оставшихся веществ гидроксид натрия в карбонат натрия можно перевести только по реакции с углекислым газом.
Задания для подготовки к егэ
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
Ответ: 23.
пояснение
В первой реакции происходит окисление железа. Окислить железо могут азотная кислота, кислород и серная кислота. Но кислоты превратят железо не в оксид, а в соль. Поэтому веществом является кислород.
Во второй реакции происходит восстановление железа из степени окисления +3 до степени окисления +2. Единственным восстановителем из представленных веществ является водород. Вещество У — это водород.
Домашняя работа
Вариант № 5509109
Ссылка — https:// chem-ege.sdamgia.ru/test?id=5509109
Задания 32 из реального ЕГЭ по химии-2021, все задачи на неорганическую химию (мысленный эксперимент) из реального экзамена ЕГЭ по химии, задания 32 из реального ЕГЭ 2021 (основная волна и резервные дни — 30 мая 2021 года) с текстовыми решениями и ответами.
1. Фосфид алюминия растворили в бромоводородной кислоте. К полученному при этом раствору добавили избыток раствора гидроксида натрия. Через получившийся раствор пропустили газ с резким запахом, образовавшийся в результате полного растворения сульфида железа(II) в концентрированной серной кислоте. Напишите уравнения четырех описанных реакций.
AlP + 3HBr = AlBr3 + PH3
AlBr3 + 4NaOH = Na[Al(OH)4] + 3NaBr (допустимо образование Na3[Al(OH)6])
2FeS + 10H2SO4 = Fe2(SO4)3 + 9SO2 + 10H2O
SO2 + 2Na[Al(OH)4] = Na2SO3 + 2Al(OH)3 + H2O (возможно образование NaHSO3)
2. Кристаллический иодид аммония нагрели с твёрдым гидроксидом натрия. Получившуюся соль растворили в воде и поместили в раствор нитрата меди(II). Выпавшую в осадок соль отделили и поместили в концентрированный раствор серной кислоты, при этом происходило выделение газа с резким запахом и образование окрашенного простого вещества. Полученное простое вещество отделили и поместили в горячий раствор гидроксида натрия. Напишите уравнения четырех описанных реакций.
NH4I + NaOH = NaI + NH3 + H2O
4NaI + 2Cu(NO3)2 = 2CuI + 4NaNO3 + I2
2CuI + 4H2SO4 = 2CuSO4 + I2 + 2SO2 + 4H2O
3I2 + 6NaOH → 5NaI + NaIO3 + 3H2O
3. Оксид кремния при нагревании прореагировал с избытком магния. Одно из получившихся при этом соединений магния поместили в воду. Выделившийся при этом газ полностью поглотили раствором, содержащим перманганат калия и гидроксид калия. Из полученного раствора зелёного цвета выделили соединение кремния и поместили его в раствор бромоводородной кислоты. Напишите уравнения четырех описанных реакций.
SiO2 + 4Mg → Mg2Si + 2MgO
Mg2Si + 4H2O = 2Mg(OH)2 + SiH4
SiH4 + 8KMnO4 + 10KOH = 8K2MnO4 + K2SiO3 + 7H2O
2HBr + K2SiO3 = 2KBr + H2SiO3
4. Сульфид алюминия растворили в избытке раствора гидроксида калия. Полученное в результате соединение серы выделили и поместили в раствор сульфата хрома(III). Образовавшийся осадок отделили и нагрели с перхлоратом калия и гидроксидом калия. Полученную соль хрома отделили, растворили в воде и поместили в раствор нитрата серебра. Напишите уравнения четырех описанных реакций.
Al2S3 + 8KOH = 2K[Al(OH)4] + K2S
Cr2(SO4)3 + 3K2S + 6H2O → 2Cr(OH)3 + 3H2S + 3K2SO4
8Cr(OH)3 + 3KClO4 + 16KOH →(tº) 8K2CrO4 + 3KCl + 20H2O
K2CrO4 + 2AgNO3 = Ag2CrO4 + 2KNO3
5. Нитрат железа(II) прокалили. Полученный твёрдый остаток растворили в растворе иодоводородной кислоты. Образовавшуюся соль железа поместили в раствор азотной кислоты и наблюдали образование окрашенного простого вещества и выделение бурого газа. Простое вещество отделили, а к оставшемуся раствору соли прилили раствор карбоната калия. Напишите уравнения четырех описанных реакций.
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2
Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O
FeI2 + 6HNO3(конц.) = Fe(NO3)3 + I2 + 3NO2 + 3H2O
2Fe(NO3)3 + 3K2CO3 + 3H2O = 2Fe(OH)3 + 3CO2 + 6KNO3
6. Фосфид алюминия растворили в соляной кислоте. К полученному при этом раствору добавили избыток раствора гидроксида калия. Через получившийся раствор пропустили газ с резким запахом, образовавшийся в результате полного растворения сульфида меди(I) в концентрированной серной кислоте. Напишите уравнения четырех описанных реакций.
AlP + 3HCl = AlCl3 + PH3
AlCl3 + 4KOH = K[Al(OH)4] + 3KCl (допустимо образование K3[Al(OH)6])
Cu2S + 6H2SO4 = 2CuSO4 + 5SO2 + 6H2O
SO2 + 2K[Al(OH)4] = K2SO3 + 2Al(OH)3 + H2O (возможно образование KHSO3)
7. Хлорид кремния(IV) поместили в воду. Выделившийся при этом осадок отделили, а в оставшийся раствор внесли фосфид цинка. Образовавшийся при этом газ пропустили через раствор, содержащий дихромат натрия и серную кислоту. Полученную при этом соль хрома выделили, растворили в воде и к полученному раствору добавили раствор карбоната калия. Напишите уравнения четырех описанных реакций.
SiCl4 + 3H2O = H2SiO3 + 4HCl
Zn3P2 + 6HCl = 3ZnCl2 + 2PH3
3PH3 + 4Na2Cr2O7 + 16H2SO4 = 4Cr2(SO4)3 + 4Na2SO4 + 3H3PO4 + 16H2O
Cr2(SO4)3 + 3K2CO3 + 3H2O = 2Cr(OH)3 + 3CO2 + 3K2SO4
8. Кристаллический иодид аммония нагрели с твёрдым гидроксидом калия. Получившуюся соль растворили в воде и поместили в раствор сульфата меди(II). Выпавшую в осадок соль отделили и поместили в концентрированный раствор азотной кислоты, при этом наблюдали выделение бурого газа и образование окрашенного простого вещества. Полученное простое вещество отделили и поместили в горячий раствор гидроксида калия. Напишите уравнения четырех описанных реакций.
NH4I + KOH = KI + NH3 + H2O
4KI + 2CuSO4 = 2CuI + 2K2SO4 + I2
2CuI + 8HNO3 = 2Cu(NO3)2 + I2 + 4NO2 + 4H2O
3I2 + 6KOH → 5KI + KIO3 + 3H2O
9. Нитрат железа(III) прокалили. Полученный твёрдый остаток растворили в растворе иодоводородной кислоты. Образовавшуюся соль железа поместили в концентрированный раствор серной кислоты и наблюдали образование окрашенного простого вещества и выделение газа с резким запахом. Простое вещество отделили, а к оставшемуся раствору соли прилили раствор карбоната натрия. Напишите уравнения четырех описанных реакций.
4Fe(NO3)3 → 2Fe2O3 + 12NO2 + 3O2
Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O
2FeI2 + 6H2SO4(конц.) = Fe2(SO4)3 + 2I2 + 3SO2 + 6H2O
Fe2(SO4)3 + 3Na2CO3 + 3H2O = 2Fe(OH)3 + 3CO2 + 3Na2SO4
10. Сульфид алюминия растворили в избытке раствора гидроксида натрия. Полученное в результате соединение серы выделили и поместили в раствор нитрата хрома(III). Образовавшийся осадок отделили и нагрели с перхлоратом натрия и гидроксидом натрия. Полученную соль хрома отделили, растворили в воде и поместили в раствор ацетата серебра. Напишите уравнения четырех описанных реакций.
Al2S3 + 8NaOH = 2K[Al(OH)4] + Na2S
2Cr(NO3)3 + 3Na2S + 6H2O → 2Cr(OH)3 + 3H2S + 6NaNO3
8Cr(OH)3 + 3NaClO4 + 16NaOH → 8Na2CrO4 + 3NaCl + 20H2O
Na2CrO4 + 2CH3COOAg = Ag2CrO4 + 2CH3COONa
11. Железную окалину растворили в разбавленной серной кислоте. Полученный раствор обработали иодидом калия. Образовавшуюся соль бескислородной кислоты поместили в раствор азотной кислоты и наблюдали образование окрашенного простого вещества и выделение бурого газа. Простое вещество отделили, а к оставшемуся раствору соли прилили раствор карбоната калия. Напишите уравнения четырех описанных реакций.
Fe3O4 + 4H2SO4 = FeSO4 + Fe2(SO4)3 + 4H2O
Fe2(SO4)3 + 6KI = 2FeI2 + I2 + 3K2SO4
FeI2 + 6HNO3(конц.) = Fe(NO3)3 + 2I2 + 3NO2 + 3H2O
2Fe(NO3)3 + 3K2CO3 + 3H2O = 2Fe(OH)3 + 3CO2 + 6KNO3
12. Фосфор смешали с магнием и нагрели. Полученное при этом вещество поместили в воду. Выделившийся газ пропустили через раствор, содержащий перманганат калия и гидроксид калия, в результате раствор приобрёл зелёную окраску. Через полученный раствор пропустили хлор, при этом наблюдали изменение цвета раствора. Напишите уравнения четырех описанных реакций.
3Mg + 2P = Mg3P2
Mg3P2 + 6H2O = 2PH3 + 3Mg(OH)2
PH3 + 8KMnO4 + 11KOH = K3PO4 + 8K2MnO4 + 7H2O
2K2MnO4 + Cl2 = 2KMnO4 + 2KCl
13. Иодид калия прореагировал с нитритом калия в присутствии серной кислоты. Образовавшийся при этом газ собрали в колбу и наблюдали, как при стоянии на воздухе газ в колбе постепенно окрасился в бурый цвет. Полученный бурый газ смешали с кислородом и пропустили через воду, при этом образовалась кислота. В полученный концентрированный раствор кислоты внесли пирит, при этом наблюдали его полное растворение и выделение бурого газа. Напишите уравнения четырех описанных реакций.
2KI + 2KNO2 + 2H2SO4 = I2 + 2NO + 2K2SO4 + 2H2O
2NO + O2 = 2NO2
4NO2 + O2 + H2O = 4HNO3
FeS2 + 18HNO3 = Fe(NO3)3 + 2H2SO4 + 15NO2 + 7H2O
14. Сульфид натрия прореагировал с нитритом натрия в присутствии серной кислоты. Образовавшийся при этом газ собрали в колбу и наблюдали, как при стоянии на воздухе газ в колбе постепенно окрасился в бурый цвет. Полученный бурый газ смешали с кислородом и пропустили через воду, при этом образовалась кислота. В полученный концентрированный раствор кислоты внесли сульфид меди(I), при этом наблюдали его полное растворение и выделение бурого газа. Напишите уравнения четырех описанных реакций.
Na2S + 2NaNO2 + 2H2SO4 = S + 2NO + 2Na2SO4 + 2H2O
2NO + O2 = 2NO2
4NO2 + O2 + H2O = 4HNO3
Cu2S + 14HNO3 = 2Cu(NO3)2 + H2SO4 + 10NO2 + 6H2O
15. Фосфид цинка растворили в соляной кислоте. Полученный газ разделили на две части, одну часть поглотили раствором, содержащим перманганат калия и гидроксид калия, в результате раствор приобрёл зелёную окраску. Другую часть газа поглотили раствором дихромата калия, подкисленным серной кислотой. Полученную при этом соль хрома выделили, растворили в воде и к полученному раствору добавили раствор карбоната натрия. Напишите уравнения четырех описанных реакций.
Zn3P2 + 6HCl = 3ZnCl2 + 2PH3
PH3 + 8KMnO4 + 11KOH = K3PO4 + 8K2MnO4 + 7H2O
3PH3 + 4K2Cr2O7 + 16H2SO4 = 4Cr2(SO4)3 + 4K2SO4 + 3H3PO4 + 16H2O
Cr2(SO4)3 + 3Na2CO3 + 3H2O = 2Cr(OH)3 + 3CO2 + 3Na2SO4
Время урока: 7 Марта 17:00
Дедлайн д/з: Сегодня в 23:55
На занятии по теме «Задача 34 на электролиз» мы разберем:
📌как писать уравнения электролиза;
📌задачу 34 на электролиз;
📌задачу 34 на неполный электролиз.
Домашнее задание
еще не выдано
Заглядывай сюда после окончания урока 😉
-
Рабочая тетрадь 2 урок
.pdf

Нужно авторизоваться
Нужно авторизоваться
Введите больше 6 символов
На почту 12345@mail.ru отправлена ссылка для сброса пароля.
Пожалуйста, подтвердите ваш номер телефона
Нужно авторизоваться
Нужно авторизоваться
Нужно авторизоваться
Введите больше 6 символов
На почту 12345@mail.ru отправлена ссылка для сброса пароля.
Пожалуйста, подтвердите ваш номер телефона
Пополнение
счёта
Курс заблокирован
К сожалению, данный курс заблокирован. Необходимо внести доплату
Вывод
средств
Ваше задание
подтверждено!
успешно
Теперь вы можете приступить
к следующему уроку
курса по математике
Перейти к уроку
Подтверждение
замены
Для смены номера телефона
мы отправили Вам код по СМС,
введите его в поле ниже.
Подтвердить
Ты включаешь автопродление — 25-го числа каждого месяца доступ к купленным курсам будет автоматически продлеваться. Деньги будут списываться с одной из привязанных к учетной записи банковских карт. Управлять автопродлением можно из раздела «Финансы»
Для активации регулярного платежа мы спишем небольшую сумму с карты и сразу её вернем
Вы дествительно хотите отменить автопродление?
Благодарим за покупку!
В ближайшее время курс будет доступен в разделе Моё обучение
Материалы будут доступны за сутки до начала урока
Чат будет доступен после выдачи домашнего задания
Укажите вашу электронную почту
Мы используем cookie. Это позволяет нам анализировать взаимодействие посетителей с сайтом и делать его лучше. Продолжая пользоваться сайтом, вы соглашаетесь с использованием файлов cookie. Для лучшей работоспособности сайта просим вас отключить AdBlock.
OK
Задания
для подготовки
1. Задание 25 № 3666
Установите соответствие между двумя
веществами и реактивом, с помощью которого можно различить эти вещества: к
каждой позиции, обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
ВЕЩЕСТВА
РЕАКТИВ
А) Бензол и гексен 1)
Бромная вода
Б) Бутин–1 и бутин–2 2)
Фенолфталеин
В) Глюкоза и сорбит
3) Соляная кислота
Г)
Пропионовая кислота и пропанол 4)
Раствор карбоната натрия
5)
Аммиачный раствор оксида серебра
Запишите в ответ цифры, расположив их
в порядке, соответствующим буквам:
Решение.
Установим соответствие.
А) Бензол и гексен. Гексен реагирует с
бромной водой (1).
Б) Бутин–1 и бутин–2. Бутин–1
реагирует с аммиачным
раствором оксида серебра (5).
В) Глюкоза и сорбит. Глюкоза
реагирует с аммиачным раствором
оксида серебра (5).
Г) Пропионовая
кислота и пропанол. Кислота реагирует с
карбонатом натрия (4).
Ответ: 1554.
1/31
2. 3668
признаками
качественной химической реакции и веществами, кото‐
рые дают эту реакцию: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.
ПРИЗНАКИ
РЕАКЦИИ ВЕЩЕСТВА
А)
Исчезновение окраски раствора
и 1) Водный раствор
перманганата калия и выпадение
белого осадка этилен
Б)
Исчезновение окраски раствора
и 2) Фенол и бромная вода выпадение
бурого осадка 3) Раствор лакмуса и
уксусная кислота
В)
Обесцвечивание раствора без
выпа‐ 4)
Пропен и бромная вода
дения осадка 5)
Этиленгликоль и гидроксид меди (II)
Г)
Образование раствора с
интенсивной синей окраской
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А) При взаимодействии фенола с бромной
водой обесцвечивается бромная вода (исчезает окраска раствора) и
выпадает белый осадок 2,4,6-трибромфенола (2).
Б) При
окислении алкенов (этилен) водным раствором перманганата калия он
обесцвечивается
(исчезает окраска
раствора) и образуется бурый осадок
оксида марганца (IV) (1). В) Алкены (пропен)
обесцвечивают бромную воду (4).
Г) Многоатомные спирты (этиленгликоль)
взаимодействуют с гидроксидом меди(II), образуя с ним раствор
интенсивной синей окраски (5).
Ответ: 2145.
2/31
3. 3669
веществом
и качественной реакцией на вещества этого класса: к
каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
ВЕЩЕСТВА
КАЧЕСТВЕННЫЕ РЕАКЦИИ
А) Ацетальдегид 1)
Фиолетовое окрашивание
раствора хлорида железа (III)
Б) Сорбит 2)
Осадок с аммиачным раствором
оксида серебра
В) Фенол 3)
Образование
фиолетового раствора с
гидроксидом меди
Г) Ацетилен (II)
4)
Образование раствора с
интенсивной синей окраской
сгидроксидом меди (II)
5)
Реакция «серебряного зеркала»
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А)
Качественная реакция на альдегиды (ацетальдегид) — реакция «серебряного
зеркала»
(образование налёта серебра на стенках
пробирки) с аммиачным раствором
оксида серебра.
Б) Сорбит — многоатомный спирт
(гексангексаол). Качественная реакция на многоатомные спирты —
образование васильково-синего
раствора с гидроксидом меди (II).
В) Фенол при взаимодействии с
хлоридом железа (III) даёт
фиолетовое окрашивание.
Г) Ацетилен вступает в реакцию с
аммиачным раствором оксида серебра, в которой происходит
образование осадка
ацетиленида серебра.
Ответ: 5412.
3/31
4. 3670
реактивом
и веществами которые можно различить с его помощью:
к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
РЕАКТИВ
ВЕЩЕСТВА
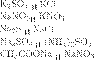
Б)
Раствор при нагревании 2)
В) Раствор 3)
Г) Раствор 4)
5)
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А) Реакция с медью при участии
концентрированной серной кислоты — качественная реакция на нитрат-ион. В кислой
среде нитрат-ион окисляет медь. Признак реакции — образование бурого газа :
(5).
Б) При нагревании щёлочи с солями аммония
выделяется аммиак (качественная реакция на соли аммония):
(4).
В) С помощью растворимых солей бария
можно обнаружить в растворе сульфат-ион, образующий с
катионом бария нерастворимый в
азотной кислоте белый осадок:
Осадки хлорида и сульфата
свинца имеют белый цвет.
Ответ: 5413.
4/31
5. 3677
соответствие , которые необходимо
различить, и реактивом, с помощью которого можно это сделать: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ВЕЩЕСТВА |
РЕАКТИВ |
|
|
А) Бутен–1 и бутан Б) Растворы В) Растворы Г) Уксусная и |
1) Бромная вода 2) Фенолфталеин 3) Гидроксид 4) Раствор 5) Аммиачный |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А) Бутен–1 и бутан — бутен
реагирует с бромной водой.
Б) Растворы глицерина и пропанола —
глицерин образует окрашенный ярко-синий комплекс при реакции с
гидроксидом меди (II).
В) Растворы глюкозы и этаналя — глюкоза,
как многоатомный спирт, образует окрашенный яркосиний комплекс при
реакции с гидроксидом меди (II).
Г) Уксусная и муравьиная кислоты —
муравьиная кислота реагирует с аммиачным раствором оксида серебра (реакция
серебряного зеркала).
Ответ: 1335.
5/31
6.
3678
веществами,
которые необходимо различить, и реактивом, с помо‐
щью которого можно это сделать: к каждой позиции, обозначенной
буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
РЕАКТИВ
А) Бензол и толуол 1)
Лакмус
Б) Ацетилен и этилен 2)
Бромная вода
В) Глюкоза и фруктоза 3)
Соляная кислота
Г)
Растворы фенола и пропанола 4)
Аммиачный раствор оксида серебра
5)
Подкисленный раствор
перманганата калия
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А) Бензол и толуол —
толуол может быть окислен
подкисленным раствором
перманганата калия.
Б) Ацетилен и этилен —
ацетилен реагирует с
аммиачным раствором оксида
серебра.
В) Глюкоза и фруктоза —
глюкоза реагирует с с
аммиачным раствором оксида
серебра.
Г) Растворы фенола и
пропанола — фенол дает осадок с бромной
водой.
Ответ: 5442.
7.
Задание 25 № 3978
Установите соответствие между веществами
и реактивом, с помощью которого их можно отличить: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
Вещества |
Реактивы |
|
|
А) карбонат натрия и Б) хлорид алюминия и хлорид В) сульфат аммония и Г) карбонат натрия и |
1) гидроксид меди (II) 2) натрий 3) соляная кислота 4) бромная вода 5) гидроксид калия |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Карбонат натрия при взаимодействии с
соляной кислотой выделит углекислый газ, хлорид алюминия образует нерастворимый
гидроксид в реакции с гидроксидом калия.
Сульфат аммония перейдет в водный раствор аммиака при
взаимодействии с гидроксидом калия.
Силикат натрия образует нерастворимую
кремниевую кислоту при взаимодействии с соляной кислотой.
Ответ: 3553.
6/31
8. 3982
и
реактивом с помощью которого можно различить эти
вещества: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.
|
Вещества |
Реактив |
|
|
А) сульфид натрия и Б) сульфат калия и В) хлорид алюминия и Г) гидроксид |
1) гидроксид 2) соляная 3) нитрат бария 4) гидроксид 5) фосфат натрия |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
В реакции сульфида натрия с соляной
кислотой пойдет неприятный запах. Сульфат анионы связываются с катионами бария
образуя нерастворимую соль. После реакции хлорида алюминия с гидроксидом натрия
образуется нерастворимый гидроксид алюминия, который растворится в избытке
щелочи (в отличие от гидроксида магния). Фосфат ионы образуют единственную
нерастворимую соль лития — фосфат лития.
Ответ: 2315.
9. Задание 25 № 3983
Установите соответствие между веществами
и реактивом, с помощью которого их можно отличить: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
Вещества |
Реактив |
|
|
А) метан и этилен Б) этаналь и метанол В) бензол и Г) этанол и фенол |
1) оксид 2) гидрокарбонат 3) фенолфталеин 4) бромная вода 5) хлороводородная |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Этилен — ненасыщенный углеводород,
вступает в реакции бромирования, этаналь вступает в реакции серебряного
зеркала. Уксусная кислота взаимодействует с гидрокарбонатом натрия. Фенол
участвует в реакции бромирования.
Ответ: 4124.
7/31
10.
3985
веществами
и с помощью которого их можно отличить: к
каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
|
Вещества |
Реактив |
|
|
А) уксусная кислота и Б) метанол и диэтиловый В) этаналь и диметилкетон Г) этилен и этан |
1) фенолфталеин 2) оксид серебра (аммиачный 3) бромная вода 4) гидрокарбонат натрия 5) калий |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Уксусная кислота реагирует с
гидрокарбонатом натрия, спирт не реагирует. Метанол взаимодействует с металлом.
Этаналь вступает в реакцию серебряного зеркала. Этилен подвергается
галогенированию (в данном случае — бромированию).
Ответ: 4523.
11.
Задание 25 № 3987
Установите соответствие между веществами
и реактивом, с помощью которого их можно отличить: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Вещества
Реактив
А) уксусная и муравьиная кислота 1)
фенолфталеин
Б) пропанол и пропанон 2)
гидроксид натрия
В) этаналь и пропанон
3) бромная вода
Г)
этилен и этан 4) оксид серебра
(аммиачный раствор)
5)
калий
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Муравьиная кислота, в силу своих
особенностей, как и альдегиды, вступает в реакцию серебряного зеркала с оксидом
серебра, калий реагирует со спиртом, этаналь — альдегид, тоже вступает в
реакцию серебряного зеркала, этилен — ненасыщенный углеводород, вступает в
реакцию бромирования.
Ответ: 4543.
8/31
12. 3989
соответствия и признаком протекающей
между ними реакции: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
|
Реагирующие вещества |
Признак реакции |
|
|
А) сульфит калия (р-р) и Б) гидроксид алюминия и (избыток) В) хлорид аммония и Г) нитрат бария (р-р) и |
1) растворение 2) без видимых 3) образование 4) выделение 5) обесцвечивание |
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Сульфит калия образован слабой сернистой
кислотой, при образовании нитрата калия сернистая кислота распадется на воду и
оксид серы(IV), в реакции с щелочью гидроксид алюминия будет проявлять
амфотерность, образовывать растворимый комплекс. В реакции хлорида аммония с
гидроксидом кальция будет образовываться неустойчивый гидроксид аммония,
который будет выделять аммиак. При реакции растворимой соли нитрата бария и
соляной кислоты будет образовываться растворимая соль — хлорид бария (а
точнее раствор ионов), а значит, никаких видимых
изменений мы не увидим.
Ответ: 4142.
13. Задание 25 № 3990
Установите соответствие между веществами
и признаком протекающей между ними реакции: к каждой позиции, обозначенной
буквой, подберите соответствующую позицию, обозначенную цифрой.
Реагирующие
вещества Признак реакции
А) бутадиен и бром (р-р) 1)
растворение осадка
Б) уксусная кислота и гидроксид меди (II) 2)
образование кирпично-красного осадка
В) этилен и перманганат калия (кислая
3) обесцвечивание раствора
среда) 4)
появление фиолетовой окраски раствора
Г)
белок и азотная кислота 5) жёлтое окрашивание
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Бутадиен присоединяет бром по месту
разрыва двойных связей. Уксусная кислота реагирует с основаниями, образуется
растворимая соль. Раствор перманганата калия имеет малиновый цвет, разрывает
двойную связь алкенов, раствор обесцвечивается. Взаимодействие белка и азотной
кислоты окрашивает раствор в желтый цвет.
Ответ: 3135.
9/31
14. 7240
между
ионом и использующимся для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
A) силикатный анион 1)
соляная кислота
Б) катион бария 2)
гидроксид натрия
В) катион меди (II)
3) сульфат натрия
Г) катион алюминия 4)
хлорид калия
5)
ацетат аммония
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
A) силикатный анион
определяется по
образованию
нерастворимой кремниевой
кислоты при реакции с более сильными
кислотами (1).
Б) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с сульфатами (3).
В) катион меди (II) определяется по
образованию нерастворимого гидроксида меди (II) при реакции с
щелочами (2).
Г) катион алюминия определяется по
образованию нерастворимого гидроксида алюминия,
растворяющегося в избытке
щелочи (2).
Ответ: 1322.
10/31
15. 7241
ионом
и реактивом, использующимся для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
A) катион аммония 1)
сульфат натрия
Б) катион кальция 2)
бромид калия
В) катион железа (II)
3) нитрат железа (III)
Г) катион бария 4)
ацетат меди (II)
5)
гидроксид калия
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
A) катион аммония определяется по выделению аммиака при
реакции с щелочами (5).
Б) катион кальция определяется по
образованию нерастворимого сульфата кальция при реакции с сульфатами (1).
В) катион железа (II) определяется по образованию
нерастворимого гидроксида железа (II) при реакции с щелочами (5).
Г) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с сульфатами (1).
Ответ: 5151.
11/31
16. 7245
между
ионом и использующимся для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
A) катион серебра 1)
ацетат натрия
Б) катион кальция 2)
фторид калия
В) катион хрома(III)
3) сульфат аммония
Г) катион бария 4)
йодид свинца
5)
нитрат стронция
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
A) катион серебра определяется по
образованию нерастворимого сульфата серебра при реакции с сульфатами (3).
Б) катион кальция определяется по
образованию нерастворимого фторида кальция при реакции с фторидами (2).
В) катион хрома(III) определяется по
образованию нерастворимого фторида хрома(III) при реакции с фторидами (2).
Г) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с сульфатами (3).
Ответ: 3223.
12/31
17. 7374
веществами
и реагентом, с помощью которого их можно отличить
друг от друга: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
ВЕЩЕСТВА
РЕАГЕНТ
А) ацетилен и этилен 1)
Б) этилен и этан 2)
В) этандиол-1,2 и этанол
3)
Г) фенол и этанол
4)
5)
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) ацетилен и этилен — только
ацетилен прореагирует с 2) , при этом выпадет осадок.
Б) этилен и этан — только
этилен прореагирует с бромной водой ((1) ), раствор при этом обесцветится.
В) этандиол-1, 2 и этанол — только
этиленгликоль прореагирует с 5) , образуется синефиолетовый раствор.
Г) фенол и этанол — только фенол
прореагирует с бромной водой ((1) ), раствор при этом обесцветится, и выпадет
осадок трибромфенола.
Ответ: 2151.
13/31
18. 7400
веществами
и реагентом с помощью которого их можно отличить
друг от друга: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
РЕАГЕНТ
А) (p-p) 1)
дистиллированная вода
Б) 2)
В) (тв.)
3) фенолфталеин
Г) (p-p) 4)
5)
ацетальдегид
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А ) (p-p) и (p-p) — кислоту и щелочь
можно различить кислотно-основным индикатором, например, 3) фенолфталеином.
Б ) (тв.) и (тв.) — бромид
кальция растворим в воде, а фторид — малорастворим. 1) дистиллированная вода.
В ) (тв.) и (тв.) — хлорид алюминия
растворим в воде, а гидроксид — нет. 1) дистиллированная вода.
Г) (p-p) и (p-p) — сульфид
серебра черного цвета, а фосфат — желтого. 2) .
Ответ: 3112.
14/31
19. 7429
веществами
и реагентом, с помощью которого их можно отличить
друг от друга: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
РЕАГЕНТ
А) 1)
(разб.)
Б)
2) (разб.)
В) 3)
Г) 4)
5)
(конц.)
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А)
и 5) (конц.) вытеснит слабую фосфорную
кислоту из фосфата кальция.
Б ) и 1) (разб.) будет
образовывать белый кристаллический осадок сульфата бария. С хлоридом магния
либо не будет реакции, либо будет образовываться осадок в объеме пробирки. В)
и 2) (разб.) — образует белый осадок только при реакции с солью серебра.
Г) и 3) — оксид
натрия будет реагировать с водой, а оксид магния — нет.
Ответ: 5123.
15/31
20. 7465
признаками соответствующую
цифрой.
ВЕЩЕСТВА
ПРИЗНАКИ РЕАКЦИИ
А) 1)
растворение осадка Б) 2)
образование осадка
В) 3)
изменение окраски раствора
Г) 4)
выделение газа
5)
видимых признаков реакции нет
Запишите в ответ цифры,
расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
—
реакция нейтрализации, без использования индикатора — 5) видимых
Б) — (р-р) 1)
растворение осадка гидроксида цинка.
В ) — 3) изменение
окраски раствора — фиолетовый раствор перманганата калия
— 2) образование осадка
хлорида серебра.
Ответ: 5132.
16/31
21. 7499
реагирующими
веществами и реагентом, с помощью которого их
можно отличить друг от друга: к каждой позиции, обозначенной
буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
РЕАГЕНТ
A) этаналь и ацетон 1)
метилоранж (р-р)
Б) пропанол-1 и этиленгликоль 2) B)
метиламин и пропан 3)
Г)
этанол и глицерин 4) (р-р)
5)
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
A) этаналь
и ацетон — альдегиды окисляются до карбоновых кислот под действием даже мягких
окислителей, например, 2) .
Б) пропанол-1 и
этиленгликоль — 2) — гликоли при взаимодействии со свежеосажденным гидроксидом
меди образуют сине-фиолетовые растворы.
B) метиламин
и пропан — 1) метилоранж (р-р) — метиламин имеет щелочную реакцию среды.
Г) этанол и глицерин — 2) — гликоли при
взаимодействии со свежеосажденным гидроксидом меди образуют сине-фиолетовые
растворы.
Ответ: 2212.
17/31
22. 7530
признаками соответствующую
цифрой.
ВЕЩЕСТВА
ПРИЗНАКИ РЕАКЦИИ
A)
1) выделение бесцветного газа Б) 2) образование черного
осадка
B)
3) образование белого осадка
Г) 4) изменение окраски раствора
5)
видимых признаков не наблюдается
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
— 1)
выделение бесцветного углекислого
газа.
— 3) образование
белого осадка карбоната кальция.
— 3) образование
белого осадка карбоната кальция.
— 3) образование
белого осадка карбоната кальция.
Ответ: 1333.
18/31
23.
7561
реагирующими
веществами и признаками протекающей между ними
реакции: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
ПРИЗНАКИ РЕАКЦИИ
A)
1) выделение бурого газа
Б) 2) образование белого осадка B) 3) образование
синего осадка
Г) 4) образование черного осадка
5)
растворение осадка
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
24.
7592
признаком соответствующую цифрой.
ВЕЩЕСТВА
ПРИЗНАКИ РЕАКЦИИ
A)
1) изменение окраски осадка
Б) 2)
растворение осадка
B)
3) выделение бурого газа
4)
изменение окраски раствора
Г)
5)
видимых признаков реакции нет
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
—
3) образование синего осадка
гидроксида меди (II). — 4) изменение окраски раствора — окисление зеленого
гидроксокомплекса
— 4) образование
черного осадка сульфида меди (II).
—
5) растворение осадка гидроксида меди (II). Б)
— 1) изменение окраски осадка — окисление зеленого гидроксида железа (II) до
— 5) растворение осадка
гидроксида меди (II).
B)
— 2) растворение осадка гидроксида железа (II) с получением сульфата
Ответ: 3455. железа
(II).
Г ) — 2) растворение осадка
гидроксида железа (II) с получением нитрата железа (III).
Ответ:
4122.
19/31 20/31
25. 7623
веществами
и реагентом, с помощью которого их можно отличить
друг от друга: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
|
ВЕЩЕСТВА |
РЕАГЕНТ |
|
А) пентанол и фенол Б) пропанол-1 и глицерин В) муравьиная кислота и Г) стеариновая и олеиновая |
1) бромная вода 2) аммиачный р-р оксида 3) раствор питьевой соды 4) гидроксид меди (II) 5) натрий |
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) пентанол и фенол — фенол реагирует с
1) бромной водой с образованием осадка 2,4,6трибромфенола.
Б) пропанол-1 и глицерин — гликоли с 4)
гидроксидом меди (II) образуют сине-фиолетовые растворы.
В) муравьиная кислота и уксусная кислота
— муравьиная кислота окисляется 2) аммиачным р-ром оксида
серебра (I).
Г) стеариновая и олеиновая кислота — 1)
бромная вода — непредельные кислоты будут окисляться бромной водой.
Ответ: 1421.
21/31
26. 9096
ионом
и реактивом, использующимся для его качественного опреде‐
ления: к позиции,
обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион бария 1)
соляная кислота
Б) катион
железа (II) 2)
глицерин
В)
катион меди (II) 3)
гексацианоферрат (III) калия
Г) катион
кобальта 4)
сульфат натрия
5)
роданид аммония
Запишите в ответ цифры,
расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
A) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с сульфатами.
Б) катион железа (II) определяется по образованию синего
осадка .
В) катион меди (II) определяется по
образованию сине-фиолетового комплекса при реакции с многоатомными спиртами.
Г) катион кобальта определяется по образованию синего
раствора из-за комплексного аниона
.
Ответ: 4325.
Примечение.
Отметим, что за качественную реакцию
можно было бы принять образование аммиакатов меди (синий) и кобальта (бурый,
окисляющийся со временем до красного). Но этот способ подошёл бы, если бы
использовался водный раствор аммиака. Из представленных же вариантов есть
только аммониевая соль, которая является донором катиона аммония ,
но не лиганда .
22/31
27. 9099
использующимся
для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион аммония 1)
серная кислота
Б) катион алюминия 2)
сульфат бария
В) катион железа (III)
3) нитрат железа (III)
Г) катион бария 4)
ацетат меди (II)
5)
гидроксид калия
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) катион аммония определяется по выделению аммиака при
реакции с щелочами.
Б) катион алюминия определяется по
образованию нерастворимого гидроксида алюминия, растворяющегося в избытке
щелочи.
В) катион железа (III) определяется по
образованию нерастворимого гидроксида железа (II) при реакции с щелочами.
Г) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с серной кислотой.
Ответ: 5551.
23/31
28. 9130
между
ионом и реактивом, использующимся для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион бария 1)
серная кислота
Б) катион алюминия 2)
соляная кислота
В) катион железа (III)
3) нитрат железа (III)
Г) катион аммония 4)
ацетат меди (II)
5)
гидроксид калия
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с серной кислотой.
Б) катион алюминия определяется по
образованию нерастворимого гидроксида алюминия, растворяющегося в избытке
щелочи.
В) катион железа (III) определяется по
образованию нерастворимого гидроксида железа (II) при реакции с щелочами.
Г) катион аммония определяется по выделению аммиака при
реакции со щелочами.
Ответ: 1555.
24/31
29. 9151
использующимся
для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион меди 1)
серная кислота
Б) катион бария 2)
хлорид натрия
В) катион железа (III)
3) нитрат серебра
Г) анион йода 4)
ацетат меди (II)
5)
гидроксид калия
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) катион меди определяется по выпадению синего осадка при
реакции с гидроксидом калия.
Б) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с серной кислотой.
В) катион железа (III) определяется по
образованию нерастворимого гидроксида железа (II) при реакции с щелочами.
Г) анион йода определяется по образованию
нерастворимого йодида серебра при реакции с нитратом серебра.
Ответ: 5153.
25/31
30. 9154
Установите соответствие между классом
органических соединений и реактивом, который может быть использован для их
обнаружения: к каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
РЕАКТИВ ДЛЯ
ВЕЩЕСТВО
ОБНАРУЖЕНИЯ
А)
карбоновые кислоты 1) раствор
перманганата калия
Б) 1,2-диолы 2)
гидрокарбонат натрия
В) фенолы
3) хлорид железа (III)
Г) непредельные углеводороды 4)
кислород
5)
(в изб. )
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) карбоновые кислоты реагируют с гидрокарбонатами с
выделением газа.
Б) многоатомные спирты проявляют васильковое окрашивание
при реакции со свежеосажденным
В) фенолы дают фиолетовое окрашивание с солями железа
(III).
Г) непредельные углеводороды обесцвечивают водный раствор
перманганата калия.
Ответ: 2531.
26/31
31. 9167
использующимся
для его обнаружения: к
позиции, обозначенной буквой, подберите позицию, обозначенную
цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион стронция 1)
серная кислота
Б) сульфат анион 2)
сероводород
В) катион железа (III)
3) жёлтая кровяная соль
Г) катион свинца 4)
ацетат меди (II)
5)
нитрат бария
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) катион стронция определяется по
образованию нерастворимого сульфата стронция при реакции с серной кислотой.
Б) сульфат анион определяется по
образованию нерастворимого сульфата бария при реакции с нитратом бария.
В) катион железа (III)
образует темно-синий комплекс с жёлтой кровяной солью
(гексацианоферратом (2) калия).
Г) катион свинца определяется по
образованию черного осадка сульфида свинца при реакции с сероводородом.
Ответ: 1532.
Примечание.
Сульфат свинца тоже нерастворим, но он
белый, как и большинство других нерастворимых соединений, поэтому наиболее
характеристичной реакцией на катион свинца является именно реакция с
сульфид-ионом, в ходе которой образуется вещество черного цвета.
27/31
32. 9169
Установите соответствие между классом
органических соединений и реактивом, который может быть использован для их
качественного определения: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ВЕЩЕСТВО
ОПРЕДЕЛЕНИЯ
А) алкадиены 1)
аммиачный раствор оксида серебра
Б) одноатомные спирты 2)
гидрокарбонат натрия
В) карбоновые кислоты
3) оксид меди (II)
Г) алкены 4)
бромная вода
5)
(в изб. )
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) алкадиены обесцвечивают бромную воду.
Б) одноатомные спирты окисляются оксидом меди (II).
В) карбоновые кислоты реагируют с гидрокарбонатом натрия.
Г) алкены обесцвечивают бромную воду.
Ответ: 4324.
28/31
33. 9182
использующимся
для его качественного
определения: к позиции, обозначенной буквой, подберите
позицию, обозначенную цифрой.
РЕАКТИВ
ДЛЯ КАЧЕСТВЕННОГО
ИОН
ОПРЕДЕЛЕНИЯ
А) катион железа (III) 1)
серная кислота
Б) катион меди 2)
хлорид натрия
В) катион бария
3) нитрат серебра
Г) анион хлора 4)
ацетат меди (II)
5)
гидроксид калия
Запишите в ответ цифры, расположив их в порядке,
соответствующем буквам:
Решение.
Установим соответствие.
А) катион железа (III) определяется по
образованию нерастворимого гидроксида железа (II) при реакции с щелочами.
Б) катион меди определяется по выпадению синего осадка
гидроксида меди.
В) катион бария определяется по
образованию нерастворимого сульфата бария при реакции с серной кислотой.
Г) анион хлора определяется по
образованию нерастворимого хлорида серебра при реакции с нитратом серебра.
Ответ: 5513.
29/31
34. 9679
Установите соответствие между формулами
газов и реагентом, с помощью которого их можно различить: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛЫ
ГАЗОВ РЕАГЕНТ
A) 1) лакмус
Б)
2) (водн.)
В) 3)
Г)
4) крахмал
5)
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
А) Озон реагирует с водным раствором
йодида калия, в ходе реакции образуется йод, окрашивающий крахмал в синий цвет.
Б) Сернистый газ обесцвечивает бромную воду, образуя
бромоводород и серную кислоту.
В) Аммиак имеет основную среду, поэтому окрасит лакмус в
синий цвет.
Г) — непредельный углеводород, в
отличие от ,
поэтому обесцветит бромную воду.
Ответ: 4212.
30/31
35. 9747
формулами
газов и реагентом, с помощью которого их можно
различить: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ФОРМУЛЫ
ГАЗОВ РЕАГЕНТ
A) 1) фенолфталеин
Б) 2)
В)
3) (водн.)
Г)
4) крахмал
5)
Запишите в ответ цифры, расположив их
в порядке, соответствующем буквам:
Решение.
Установим соответствие.
1) При
реакции сероводорода с бромной водой произойдет обесцвечивание раствора и
выпадет в видеосадка сера.
2) Хлор
вытесняет йод и бром из соответствующих солей, поэтому при реакции с йодидом
калия выделится йод и окрасит крахмал в синий цвет.
3) Аммиак
имеет основную среду, поэтому окрасит фенолфталеин в малиновый цвет.
4) —
непредельный углеводород, в отличие от , поэтому
обесцветит бромную воду.
Ответ: 3413.
31/31
Чтобы поделиться, нажимайте
Реальный ЕГЭ по химии 2020. Задание 32
Представляем вашему вниманию задание 32 из реального ЕГЭ 2020 (основная волна и резервные дни — 16 июля 2020 года, 24 июля 2020) с подробными текстовыми решениями и ответами.
Реальный ЕГЭ 2020. Задание 32. Вариант 1
- Дигидрофосфат кальция растворили в избытке раствора гидроксида калия. Полученное соединение кальция отделили и высушили, а затем сплавили с оксидом кремния (IV) и углеродом. Полученное простое вещество прореагировало с хлоратом калия. Образовавшуюся соль растворили в воде и провели электролиз полученного раствора. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) 3Ca(H2PO4)2 + 12KOH = 4K3PO4 + Ca3(PO4)2↓ + 12H2O
2) Ca3(PO4)2 + 5C + 3SiO2 = 2P + 3CaSiO3 + 5CO (сплавление)
или 2Ca3(PO4)2 + 10C + 6SiO2 = P4 + 6CaSiO3 + 10CO (сплавление)
3) 5KClO3 + 6P = 5KCl + 3P2O5
или 10KClO3 + 12P = 10KCl + 3P4O10
или 10KClO3 + 3P4 = 3P4O10 + 10KCl
или 10KClO3 + 3P4 = 6P2O5 + 10KCl
4) 2KCl + 2H2O = H2↑ + Cl2↑ + 2KOH (электролиз)
Реальный ЕГЭ 2020. Задание 32. Вариант 2
- К раствору сульфата хрома (III) прилили раствор сульфита натрия. В результате реакции выделился газ и выпал осадок. Полученный газ пропустили через раствор перманганата калия. А осадок, полученный в первой реакции, отделили и добавили к раствору пероксида водорода подщелоченного гидроксидом натрия. Затем к образовавшемуся раствору прилили избыток раствора разбавленной серной кислоты. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Cr2(SO4)3 + 3Na2SO3 + 3H2O = 2Cr(OH)3↓ + 3SO2↑ + 3Na2SO4
2) 5SO2 + 2KMnO4 + 2H2O = 2MnSO4 + K2SO4 + 2H2SO4
3) 2Cr(OH)3 + 3H2O2 + 4NaOH = 2Na2CrO4 + 8H2O
4) 2Na2CrO4 + H2SO4 = Na2SO4 + Na2Cr2O7 + H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 3
- Железную окалину растворили в разбавленной серной кислоте. В полученный раствор добавили раствор дихромата калия, подкисленный серной кислотой. Хромосодержащее вещество, полученное в результате реакции, выделили и добавили его к раствору карбоната натрия. Полученный осадок отделили и растворили в горячем растворе хлората калия и гидроксида калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Fe3O4 + 4H2SO4 = FeSO4 + Fe2(SO4)3 + 4H2O
2) 6FeSO4 + K2Cr2O7 + 7H2SO4 = 3Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 + 7H2O
3) Cr2(SO4)3 + 3Na2CO3 + 3H2O = 2Cr(OH)3↓ + 3CO2↑ + 3Na2SO4
4) 2Cr(OH)3 + KClO3 + 4KOH = KCl + 2K2CrO4 + 5H2O (нагревание)
Реальный ЕГЭ 2020. Задание 32. Вариант 4
- Натрий нагрели с кислородом. Полученное твёрдое вещество обработали подкисленным серной кислотой раствором перманганата калия. Газ, образовавшийся в ходе реакции, прореагировал с пиритом при нагревании. Полученное твёрдое вещество растворили в растворе иодоводорода. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) 2Na + O2 = Na2O2
2) 5Na2O2 + 2KMnO4 + 8H2SO4 = 5Na2SO4 + K2SO4 + 2MnSO4 + 5O2↑ + 8H2O
3) 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 (нагревание)
4) Fe2O3 + 6HI = 2FeI2 + I2↓ + 3H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 5
- Провели электролиз раствора нитрата серебра (I). Полученный на аноде газ прореагировал с раскалённым железом. Образовавшееся твёрдое вещество чёрного цвета растворили в растворе иодоводородной кислоты. Полученное простое вещество отделили и растворили при нагревании в растворе гидроксида натрия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) 4AgNO3 + 2H2O = 4Ag↓ + O2↑ + 4HNO3 (электролиз)
2) 3Fe + 2O2 = Fe3O4 (нагревание)
3) Fe3O4 + 8HI = 3FeI2 + I2↓ + 4H2O
4) 3I2 + 6NaOH = NaIO3 + 5NaI + 3H2O (нагревание)
Реальный ЕГЭ 2020. Задание 32. Вариант 6
- К фосфиду алюминия добавили соляную кислоту. Затем к получившемуся раствору добавили раствор сульфита калия, в результате чего образовался белый осадок и бесцветный газ. Выделившийся газ разделили на две части. Первую часть пропустили через раствор дихромата натрия, подкисленный серной кислотой. Вторую часть газа пропустили через концентрированную азотную кислоту. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) AlP + 3HCl = AlCl3 + PH3↑
2) 2AlCl3 + 3K2SO3 + 3H2O = 2Al(OH)3↓ + 3SO2↑ + 6KCl
3) Na2Cr2O7 + 3SO2 + H2SO4 = Na2SO4 + Cr2(SO4)3 + H2O
4) SO2 + 2HNO3 = H2SO4 + 2NO2↑
Реальный ЕГЭ 2020. Задание 32. Вариант 7
- Смешали растворы хлорной кислоты и гидроксида натрия. Полученную соль выделили и сплавили с оксидом хрома (III) и гидроксидом натрия. Соль, содержащую хром, отделили и добавили к избытку разбавленного раствора серной кислоты. Затем через полученный кислый раствор пропустили сероводород. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) HClO4 + NaOH = NaClO4 + H2O
2) 3NaClO4 + 4Cr2O3 + 16NaOH = 8Na2CrO4 + 3NaCl + 8H2O (сплавление)
3) 2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
4) 3H2S + Na2Cr2O7 + 4H2SO4 = 3S + Cr2(SO4)3 + Na2SO4 + 7H2O
или 3H2S + 4Na2Cr2O7 + 13H2SO4 = 4Cr2(SO4)3 + 4Na2SO4 + 16H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 8
- К раствору сульфата цинка добавили избыток раствора гидроксида калия. Через образовавшийся раствор пропустили сероводород, образовавшийся белый осадок растворили в концентрированной азотной кислоте и наблюдали выделение бурого газа. Выделившийся бурый газ пропустили через раствор гидроксида бария. Запишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) ZnSO4 + 4KOH = K2SO4 + K2[Zn(OH)4]
2) K2[Zn(OH)4] + 3H2S = ZnS↓ + 2KHS + 4H2O
или K2[Zn(OH)4] + 2H2S = ZnS↓ + K2S + 4H2O
3) ZnS + 8HNO3 = ZnSO4 + 8NO2↑ + 4H2O
или ZnS + 10HNO3 = Zn(NO3)2 + 8NO2↑ + H2SO4 + 4H2O
или ZnS + 4HNO3 = Zn(NO3)2 + S↓ + 2NO2↑ +2H2O
4) 4NO2 + 2Ba(OH)2 = Ba(NO2)2 + Ba(NO3)2 + 2H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 9
- Алюминий добавили к раствору гидроксида калия. Через полученный прозрачный раствор пропустили газ, получившийся при взаимодействии магния с концентрированной серной кислотой. Образовавшийся осадок отделили, а в оставшийся раствор добавили раствор перманганата калия, в результате чего в осадок перешло простое вещество. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) 2Al + 2KOH + 6H2O = 2K[Al(OH)4] + 3H2↑
2) 4Mg + 5H2SO4 (конц.) = 4MgSO4 + H2S↑ + 4H2O
3) 2K[Al(OH)4] + H2S = 2Al(OH)3↓ + K2S + 2H2O
или K[Al(OH)4] + H2S → KHS + Al(OH)3↓ + H2O
4) 3K2S + 2KMnO4 + 4H2O = 3S↓ + 2MnO2↓ + 8KOH
или 3KHS + 2KMnO4 + H2O = 5KOH + 2MnO2↓ + 3S↓
Реальный ЕГЭ 2020. Задание 32. Вариант 10
- Оксид хрома (VI) обработали избытком раствора гидроксида натрия. К полученному жёлтому раствору прилили серную кислоту. Затем раствор снова подкислили серной кислотой и пропустили через него фосфин. Полученную соль хрома выделили и добавили к ней раствор карбоната калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) CrO3 + 2NaOH = Na2CrO4 + H2O
2) 2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
3) 4Na2Cr2O7 + 16H2SO4 + 3PH3 = 4Cr2(SO4)3 + 4Na2SO4 + 3H3PO4 + 16H2O
4) Cr2(SO4)3 + 3K2CO3 + 3H2O = 2Cr(OH)3↓ + 3CO2↑ + 3K2SO4
Реальный ЕГЭ 2020. Задание 32. Вариант 11
- Оксид меди (I) растворили в концентрированной азотной кислоте. Образовавшуюся соль выделили, высушили и прокалили. Через полученный твёрдый остаток при нагревании пропустили газ, полученный при сливании известковой воды и раствора гидрофосфата аммония. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Cu2O + 6HNO3 (конц.) = 2Cu(NO3)2 + 2NO2 + 3H2O
2) 2Cu(NO3)2 = 2CuO + 4NO2↑ + O2↑ (прокаливание)
3) 3Ca(OH)2 + 2(NH4)2HPO4 = Ca3(PO4)3↓ + 4NH3↑ + 6H2O
или Ca(OH)2 + (NH4)2HPO4 = CaHPO4↓ + 2NH3↑ + 2H2O
4) 3CuO + 2NH3 = 3Cu + N2 + 3H2O (нагревание)
Реальный ЕГЭ 2020. Задание 32. Вариант 12
- Дихромат аммония прокалили до постоянной массы. Твёрдый остаток растворили в растворе пероксида водорода с гидроксидом калия. К образовавшемуся раствору жёлтого цвета прилили избыток концентрированной бромоводородной кислоты. Полученную соль хрома выделили и добавили к раствору карбоната калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) (NH4)2Cr2O7 = N2↑ + Cr2O3 + 4H2O (прокаливание)
2) Cr2O3 + 4KOH + 3H2O2 = 2K2CrO4 + 5H2O
3) 2K2CrO4 + 16HBr = 4KBr + 2CrBr3 + 3Br2 + 8H2O
4) 2CrBr3 + 3K2CO3 + 3H2O = 6KBr + 2Cr(OH)3↓ + 3CO2↑
Реальный ЕГЭ 2020. Задание 32. Вариант 13
- Карбид алюминия сожгли. Полученное твёрдое вещество поместили в раствор гидроксида натрия. Через образовавшийся прозрачный раствор пропустили газ, полученный при действии на магний концентрированной серной кислоты. При пропускании газа происходило выпадение белого осадка и образование соли бескислородной кислоты.
Развернуть/свернуть решение
1) Al4C3 + 6O2 = 3CO2 + 2Al2O3
2) Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
3) 4Mg + 5H2SO4 (конц.) = 4MgSO4 + H2S↑ + 4H2O
4) H2S + 2Na[Al(OH)4] = 2Al(OH)3 ↓+ Na2S + 2H2O (допустимо образование NaHS)
Реальный ЕГЭ 2020. Задание 32. Вариант 14
- Натрий растворили в воде. Образовавшееся газообразное вещество при нагревании пропустили через железную окалину. Получившееся простое вещество при нагревании растворили в необходимом количестве концентрированной серной кислоты, при этом образовался бесцветный газ с резким запахом. К полученному раствору добавили раствор карбоната калия.
Развернуть/свернуть решение
1) 2Na + 2H2O = 2NaOH + H2↑
2) Fe3O4 + 4H2 = 3Fe + 4H2O
3) 2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2↑ + 6H2O
4) Fe2(SO4)3 + 3K2CO3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 3K2SO4
Реальный ЕГЭ 2020. Задание 32. Вариант 15
- Оксид меди (I) растворили в концентрированном растворе азотной кислоты. Полученный в результате бурый газ поглотили холодным раствором гидроксида натрия. К образовавшемуся раствору добавили подкисленный серной кислотой раствор дихромата натрия. Образовавшееся соединение хрома выделили и поместили в раствор карбоната калия.
Развернуть/свернуть решение
1) Cu2O + 6HNO3 = 2Cu(NO3)2 + 2NO2↑ + 3H2O
2) 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
3) 3NaNO2 + Na2Cr2O7 + 4H2SO4 = 3NaNO3 + Cr2(SO4)3 + Na2SO4 + 4H2O
4) Cr2(SO4)3 + 3K2CO3 + 3H2O = 2Cr(OH)3↓ + 3CO2↑ + 3K2SO4
Реальный ЕГЭ 2020. Задание 32. Вариант 16
- К раствору дигидрофосфата калия добавили избыток раствора гидроксида кальция. Образовавшийся осадок отделили, высушили и нагрели с кремнезёмом и углём. Полученное простое вещество вступило в реакцию с хлоратом калия. Полученный при этом оксид поместили в избыток раствора гидроксида натрия.
Развернуть/свернуть решение
1) 2KH2PO4 + 3Ca(OH)2 = Ca3(PO4)2↓ + 2KOH + 4H2O
2) Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3 + 5CO + 2P
3) 6P + 5KClO3 = 3P2O5 + 5KCl
4) P2O5 + 6NaOH = 2Na3PO4 + 3H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 17
- Нитрат хрома (III) прокалили. Образовавшееся при этом твёрдое вещество нагрели с хлоратом натрия и гидроксидом натрия. Одно из полученных веществ прореагировало с концентрированным раствором хлороводородной кислоты. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната натрия.
Развернуть/свернуть решение
1) 4Cr(NO3)3 = 2Cr2O3 + 12NO2↑ + 3O2↑
2) Cr2O3 + NaClO3 + 4NaOH = 2Na2CrO4 + NaCl + 2H2O
3) 2Na2CrO4 + 16HCl = 2CrCl3 + 3Cl2↑ + 4NaCl + 8H2O
4) 2CrCl3 + 3Na2CO3 + 3H2O = 2Cr(OH)3↓ + 3CO2↑ + 6NaCl
Реальный ЕГЭ 2020. Задание 32. Вариант 18
- Перхлорат натрия сплавили с оксидом хрома (III) и гидроксидом натрия. Полученное соединение хрома поместили в разбавленный раствор серной кислоты. В образовавшийся раствор добавили серную кислоту и поместили иодид натрия. Образовавшееся простое вещество при нагревании прореагировало с гидроксидом калия.
Развернуть/свернуть решение
1) 3NaClO4 + 4Cr2O3 + 16NaOH = 8Na2CrO4 + 3NaCl + 8H2O
2) 2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
3) Na2Cr2O7 + 6NaI + 7H2SO4 = 3I2↓ + Cr2(SO4)3 + 4Na2SO4 + 7H2O
4) 3I2 + 6KOH = KIO3 + 5KI + 3H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 19
- Пероксид натрия поместили в раствор, содержащий перманганат калия и серную кислоту. Полученное простое вещество при нагревании прореагировало с железом. Образовавшееся при этом твёрдое вещество черного цвета поместили в раствор иодоводородной кислоты. Образовавшуюся при этом соль железа выделили, растворили в воде и полученный раствор прилили к раствору карбоната натрия.
Развернуть/свернуть решение
1) 5Na2O2 + 2KMnO4 + 8H2SO4 = 5O2↑ + 2MnSO4 + 5Na2SO4 + K2SO4 + 8H2O
2) 2O2 + 3Fe = Fe3O4
3) Fe3O4 + 8HI = 3FeI2 + I2↓ + 4H2O
4) FeI2 + Na2CO3 = FeCO3↓ + 2NaI
Реальный ЕГЭ 2020. Задание 32. Вариант 20
- Оксид железа (III) поместили в раствор бромоводородной кислоты. Через получившийся раствор пропустили аммиак. Образовавшийся при этом осадок отделили и прокалили. Полученное бурое вещество сплавили с твёрдым гидроксидом калия.
Развернуть/свернуть решение
1) Fe2O3 + 6HBr = 2FeBr3 + 3H2O
2) FeBr3 + 3NH3 + 3H2O = Fe(OH)3↓ + 3NH4Br
3) 2Fe(OH)3 = Fe2O3 + 3H2O
4) Fe2O3 + 2KOH = 2KFeO2 + H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 21
- Через раствор силиката калия пропустили углекислый газ. Полученный при этом осадок отделили, а оставшийся раствор смешали с раствором сульфата железа (III). Выпавший при этом осадок отделили и прокалили. Полученное бурое вещество сплавили с твёрдым карбонатом натрия.
Развернуть/свернуть решение
1) K2SiO3 + CO2 + H2O = H2SiO3↓ + K2CO3 (допустимо образование KHCO3)
2) 3K2CO3 + Fe2(SO4)3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 3K2SO4
3) 2Fe(OH)3 = Fe2O3 + 3H2O
4) Fe2O3 + Na2CO3 = 2NaFeO2 + CO2↑
Реальный ЕГЭ 2020. Задание 32. Вариант 22
- Алюминат натрия растворили в серной кислоте. К полученному при этом раствору добавили раствор сульфида натрия. Выделившийся газ разделили на две части, одну часть поглотили раствором дихромата натрия, подкисленным серной кислотой. Другую часть газа поглотили бромной водой.
Развернуть/свернуть решение
1) 2NaAlO2 + 4H2SO4 = Na2SO4 + Al2(SO4)3 + 4H2O
2) Al2(SO4)3 + 3Na2S + 6H2O = 2Al(OH)3↓ + 3H2S↑ + 3Na2SO4
3) 3H2S + Na2Cr2O7 + 4H2SO4 = 3S↓ + Cr2(SO4)3 + Na2SO4 + 7H2O
4) H2S + Br2 = S↓ + 2HBr
Реальный ЕГЭ 2020. Задание 32. Вариант 23
- Цинк сплавили с твёрдым гидроксидом калия. Полученное в результате твёрдое вещество растворили в необходимом количестве раствора серной кислоты. В образовавшийся раствор добавили сульфид калия, в результате чего образовался белый осадок. Осадок отделили и при нагревании растворили в концентрированной серной кислоте, при этом образовался бесцветный газ с резким запахом.
Развернуть/свернуть решение
1) Zn + 2KOH = K2ZnO2 + H2↑
2) K2ZnO2 + 2H2SO4 = K2SO4 + ZnSO4 + 2H2O
3) ZnSO4 + K2S = ZnS↓ + K2SO4
4) ZnS + 4H2SO4 (конц.) = ZnSO4 + 4SO2↑ + 4H2O
Реальный ЕГЭ 2020. Задание 32. Вариант 24
- Нитрат железа (II) прокалили. Полученное твердое вещество сплавили с твердым гидроксидом калия. Образовавшийся твердый продукт растворили в необходимом количестве бромоводородной кислоты. Через полученный раствор пропустили аммиак.
Развернуть/свернуть решение
1) 4Fe(NO3)2 = 2Fe2O3 + 8NO2↑ + O2↑
2) Fe2O3 + 2KOH = 2KFeO2 + H2O
3) KFeO2 + 4HBr = KBr + FeBr3 + 2H2O
4) FeBr3 + 3NH3 + 3H2O = Fe(OH)3↓ + 3NH4Br
Реальный ЕГЭ 2020. Задание 32. Вариант 25
- Нитрат цинка прокалили. Полученное простое вещество прореагировало с оксидом азота (II). Полученный продукт прореагировал с холодным раствором гидроксида натрия. К образовавшемуся раствору прилили раствор, содержащий дихромат натрия и серную кислоту.
Развернуть/свернуть решение
1) 2Zn(NO3)2 = 2ZnO + 4NO2↑ + O2↑
2) 2NO + O2 = 2NO2
3) 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
4) 3NaNO2 + Na2Cr2O7 + 4H2SO4 = 3NaNO3 + Cr2(SO4)3 + Na2SO4 + 4H2O
Резерв
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 1
- Гидросульфит бария растворили в водном растворе пероксида водорода. Полученную соль отделили и нагрели с водородом. Полученное вещество добавили в раствор сульфата алюминия. К образовавшемуся нерастворимому основанию, которое отделили от раствора, добавили раствор гидроксида натрия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Ba(HSO3)2 + 2H2O2 = BaSO4↓ + H2SO4 + 2H2O
2) BaSO4 + 4H2 = BaS + 4H2O (нагревание) (очень спорная реакция)
3) 3BaS + Al2(SO4)3 + 6H2O = 3BaSO4↓ + 3H2S↑ + 2Al(OH)3↓
4) Al(OH)3 + NaOH = Na[Al(OH)4]
или Al(OH)3 + 3NaOH = Na3[Al(OH)6]
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 2
- Прокалили смесь карбоната калия и оксида цинка. Полученный в результате реакции газ прореагировал с избытком твёрдой щёлочи при нагревании. В результате реакции образовалась соль, которую растворили в воде и к образовавшемуся раствору добавили хлорид алюминия. Полученный осадок отделили и растворили в растворе гидроксида калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) K2CO3 + ZnO = K2ZnO2 + CO2↑ (прокаливание)
2) CO2 + 2NaOH = Na2CO3 + H2O
3) 2Na2CO3 + 2AlCl3 + 3H2O = 2Al(OH)3↓ + 3CO2↑ + 6NaCl
4) Al(OH)3 + KOH = K[Al(OH)4]
или Al(OH)3 + 3KOH = K3[Al(OH)6]
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 3
- Металюминат калия растворили в серной кислоте. В полученный раствор добавили сульфит натрия. В результате реакции выделился газ, который разделили на две части. Одну часть полученного газа пропустили через бромную воду, а вторую – через подкисленный серной кислотой раствор дихромата натрия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) 2KAlO2 + 4H2SO4 = K2SO4 + Al2(SO4)3 + 4H2O
2) Al2(SO4)3 + 3Na2SO3 + 3H2O = 2Al(OH)3↓ + 3Na2SO4 + 3SO2↑
3) 3SO2 + Na2Cr2O7 + H2SO4 = Na2SO4 + Cr2(SO4)3 + H2O
4) SO2 + Br2 + 2H2O = 2HBr + H2SO4
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 4
- Оксид меди (II) нагрели с медью. Образовавшееся вещество растворили в концентрированной азотной кислоте. Выделившийся бурый газ поглотили раствором гидроксида калия. К образовавшемуся раствору добавили подкисленный серной кислотой раствор дихромата калия. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) CuO + Cu = Cu2O (нагревание)
2) Cu2O + HNO3 (конц.) = 2Cu(NO3)2 + 2NO2↑ + 3H2O
3) 2NO2 + 2KOH = KNO2 + KNO3 + H2O
4) 3KNO2 + K2Cr2O7 + 4H2SO4 = 3KNO3 + K2SO4 + Cr2(SO4)2 + 4H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 5
- Через избыток раствора силиката натрия пропустили углекислый газ. Образовавшуюся соль отделили и растворили в растворе хлорида железа (III). Образовавшийся осадок отфильтровали и прокалили до постоянной массы. Образовавшийся твёрдый остаток растворили в растворе иодоводородной кислоты. Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Na2SiO3 + CO2 + H2O = H2SiO3↓ + Na2CO3 (допустимо образование NaHCO3)
2) 3Na2CO3 + 2FeCl3 + 3H2O = 2Fe(OH)3↓ + 6NaCl + 3CO2↑
3) 2Fe(OH)3 = Fe2O3 + 3H2O (прокаливание)
4) Fe2O3 + 6HI = I2↓ + 2FeI2 + 3H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 6
- Прокалили смесь карбоната калия и оксида цинка. Выделившийся газ пропустили через раствор силиката натрия. Образовавшийся осадок отделили, а оставшийся раствор смешали с раствором хлорида железа(III), при этом наблюдали образование осадка и выделение газа. Полученный осадок отделили и поместили в раствор иодоводородной кислоты.Напишите уравнения четырёх описанных реакций.
Развернуть/свернуть решение
1) Na2CO3 + ZnO = Na2ZnO2 + CO2↑ (прокаливание)
2) Na2SiO3 + CO2 + H2O = H2SiO3↓ + Na2CO3 (допустимо образование NaHCO3)
3) 2Na2CO3 + 2FeCl3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 6NaCl
4) 2Fe(OH)3 + 6HI = 2FeI2 + I2↓ + 6H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 7
- К раствору сульфата цинка добавили избыток раствора гидроксида натрия. Через полученный раствор пропустили сероводород. Образовавшийся при этом осадок при нагревании растворили в концентрированной серной кислоте, при этом образовался бесцветный газ с резким запахом. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой.
Развернуть/свернуть решение
1) ZnSO4 + 4NaOH = Na2[Zn(OH)4] + Na2SO4
2) Na2[Zn(OH)4] + 2H2S = ZnS↓ + Na2S + 4H2O (допустимо образование NaHS)
3) ZnS + 4H2SO4 = ZnSO4 + 4SO2↑ + 4H2O
4) 5SO2 + 2KMnO4 + 2H2O = 2MnSO4 + K2SO4 + 2H2SO4
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 8
- К раствору нитрата алюминия добавили раствор сульфида натрия. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой, при этом наблюдали образование осадка. Осадок отделили и обработали горячим концентрированным раствором гидроксида калия. Полученную при этом кислородосодержащую соль добавили в раствор, содержащий дихромат калия и серную кислоту.
Развернуть/свернуть решение
1) 2Al(NO3)3 + 3Na2S + 6H2O = 2Al(OH)3↓ + 3H2S↑ + 6NaNO3
2) 5H2S + 2KMnO4 + 3H2SO4 = 5S↓ + 2MnSO4 + K2SO4 + 8H2O
3) 3S + 6KOH = 2K2S + K2SO3 + 3H2O
4) 3K2SO3 + K2Cr2O7 + 4H2SO4 = 4K2SO4 + Cr2(SO4)3 + 4H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 9
- Оксид хрома (VI) поместили в раствор гидроксида калия. В полученный при этом раствор добавили раствор серной кислоты. Образовавшийся раствор дополнительно подкислили серной кислотой и пропустили через этот раствор сероводород. Образовавшийся при этом осадок отделили и поместили в горячий концентрированный раствор гидроксида калия.
Развернуть/свернуть решение
1) CrO3 + 2KOH = K2CrO4 + H2O
2) 2K2CrO4 + H2SO4 = K2Cr2O7 + K2SO4 + H2O
3) 3H2S + K2Cr2O7 + 4H2SO4 = 3S↓ + Cr2(SO4)3 + K2SO4 + 7H2O
4) 3S + 6KOH = 2K2S + K2SO3 + 3H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 10
- Фосфид цинка растворили в соляной кислоте. Полученный газ поглотили концентрированным раствором азотной кислоты при нагревании, при этом наблюдали выделение бурого газа. Бурый газ пропустили через раствор гидроксида натрия. К полученному раствору добавили раствор, содержащий дихромат натрия и серную кислоту.
Развернуть/свернуть решение
1) Zn3P2 + 6HCl = 3ZnCl2 + 2PH3↑
2) PH3 + 8HNO3 = H3PO4 + 8NO2↑ + 4H2O
3) 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
4) 3NaNO2 + Na2Cr2O7 + 4H2SO4 = 3NaNO3 + Cr2(SO4)3 + Na2SO4 + 4H2O
Реальный ЕГЭ 2020 (резервные дни). Задание 32. Вариант 11
- Алюминий добавили к раствору гидроксида натрия. Через образовавшийся прозрачный раствор пропустили газ, полученный при растворении серы в концентрированной серной кислоте. Образовавшийся осадок отделили, а к полученному раствору добавили раствор перманганата калия.
Развернуть/свернуть решение
1) 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 ↑
2) S + 2H2SO4 = 3SO2↑ + 2H2O
3) SO2 + 2Na[Al(OH)4] = 2Al(OH)3↓ + Na2SO3 + H2O (допустимо образование NaHSO3)
4) 3Na2SO3 + 2KMnO4 + H2O = 3Na2SO4 + 2MnO2↓ + 2KOH
Также предлагаем вам плейлист видео-уроков и видео-объяснений заданий на эту тему:
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку
В результате выполнения задания 19 ЕГЭ по химии проверяются следующие требования/умения:
Коды проверяемых требований к уровню подготовки (по кодификатору):
Читать подробнее…
Коды проверяемых элементов содержания (по кодификатору):
Уровень сложности задания:
Максимальный балл за выполнение задания:
Примерное время выполнения задания выпускником, изучавшим предмет:
Установите соответствие между веществом, которое вступает в реакцию с этанолом, и преимущественно образующимся углеродсодержащим продуктом этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) СuО
Б) KMnO4(H+)
В) Н2SO4 (конц. 180)
Г) K
ПРОДУКТ РЕАКЦИИ
1) ацетат калия
2) этилат калия
3) ацетальдегид
4) уксусная кислота
5) диметиловый эфир
6) этилен
Установите соответствие между схемой реакции и органическим веществом, которое является продуктом этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) CH3CHO → Cu(OH)2
Б) CH3CHO →H2
В) CH3CH2OH→CuO
Г) CH3CH2OH →H2SO4 t
ПРОДУКТ РЕАКЦИИ
1) этанол
2) ацетат калия
3) ацетальдегид
4) диэтиловый эфир
5) ацетат меди(II)
6) этановая кислота
Установите соответствие между схемой реакции и веществом X, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СХЕМА РЕАКЦИИ
А) бутанол-2 —X→ бутен-2
Б) бутанол-2 —X→ 2-бромбутан
В) бутанол-2 —X→ бутанон
Г) бутанол-1 —X→ бутаналь
ВЕЩЕСТВО X
1) бром
2) H2SO4(конц.)
3) вода
4) СuО (t)
5) NaBr
6) бромоводород
Установите соответствие между веществом и углеродсодержащими продуктом реакции, который преимущественно образуется при взаимодействии этого вещества с оксидом меди(II): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) уксусная кислота
Б) этанол
В) метанол
Г) пропанол-2
ПРОДУКТ РЕАКЦИИ
1) ацетон
2) ацетальдегид
3) формальдегид
4) пропаналь
5) формиат меди(II)
6) ацетат меди(II)
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) фенол и натрий
Б) фенол и сода
В) фенол и бромная вода
Г) уксусная кислота и сода
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) трибромфенол
2) ацетат натрия
3) формиат натрия
4) фенолят натрия
5) монобромфенол
6) бензоат натрия
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CH3COOK и КОН
Б) СН3СООН и СН3ОН
В) СН3ОН и К
Г) СН3ОН и H2SO4
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) диэтиловый эфир
2) метилацетат
3) метилат калия
4) метан
5) диметиловый эфир
6) метаналь
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) пропанол-1 и оксид меди(II)
Б) пропанол-2 и оксид меди(II)
В) пропанол-2 и муравьиная кислота
Г) пропин и вода
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) пропаналь
2) ацетон
3) пропен
4) изопропанол
5) пропилацетат
6) изопропилформиат
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) этанол и оксид меди(II)
Б) уксусная кислота и оксид меди(II)
В) этанол и натрий
Г) этанол и гидроксид натрия
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) ацетат меди(I)
2) ацетат меди(II)
3) этилат натрия
4) этилнатрий
5) этаналь
6) не взаимодействуют
Установите соответствие между реагирующими веществами и органическим веществом, которое является продуктом взаимодействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) фенол и гидроксид калия
Б) фенол и калий
В) фенолят калия и углекислый газ
Г) фенолят калия и бромметан
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) трибромфенол
2) фенолят калия
3) фенол
4) метилфениловый эфир
5) монобромфенол
6) бензоат натрия
Из предложенного перечня выберите два типа реакций, к которым можно отнести взаимодействие этанола с пропионовой кислотой.
1) присоединения
2) окисления
3) нейтрализации
4) этерификации
5) обратимая