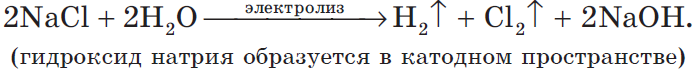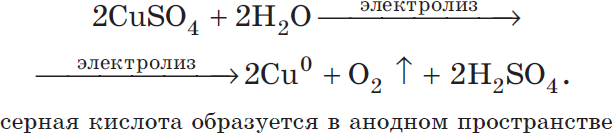Скачать:
в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 263 … 141–160 | 161–180 | 181–200 | 201–220 | 221–240 | 241–260 | 261–263
Добавить в вариант
При электролизе раствора сульфата меди(II) на аноде выделилось 3,36 л (н. у.) кислорода. Сколько граммов металла выделилось на катоде? Примите Ответ запишите с точностью до десятых.
При электролизе раствора нитрата серебра на аноде выделилось 1,12 л (н. у.) кислорода. Сколько граммов металла выделилось на катоде? Ответ запишите с точностью до десятых.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
В уравнениях приведите структурные формулы органических веществ.
Источник: СтатГрад: Тренировочная работа 28.11.2018. Вариант ХИ10202.
Установите соответствие между веществом и основным способом его промышленного производства: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) железо
Б) водород
В) хлор
СПОСОБ ПРОМЫШЛЕННОГО ПРОИЗВОДСТВА
1) паровая конверсия природного газа
2) восстановление оксида углеродом
3) перегонка воздуха
4) электролиз раствора соли
Запишите в таблицу выбранные цифры под соответствующими буквами.
Гашёную известь сплавили с твёрдым хлоридом аммония, образовавшийся при этом газ пропустили над нагретым оксидом меди (II). Получившееся при этом твёрдое вещество обработали разбавленной азотной кислотой (при этом выделился бесцветный газ), а оставшийся раствор подвергли электролизу. Напишите уравнения четырёх указанных реакций.
Источник: ЕГЭ по химии 2019. Основная волна. Вариант 1
Установите соответствие между реагирующими веществами и углеводородом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) хлорметан и натрий
Б) ацетат натрия и гидроксид натрия
В) пропионат натрия и вода, электролиз
Г) 1,2-дихлорэтан и спиртовой раствор гидроксида натрия
ПРОДУКТ РЕАКЦИИ — УГЛЕВОДОРОД
1) метан
2) этан
3) пропан
4) н-бутан
5) ацетилен
6) этилен
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Сколько граммов хлорида натрия требуется для получения 6,72 л газообразного хлора (н. у.) методом электролиза? Примите Ответ запишите с точностью до десятых.
Установите соответствие между реагирующими веществами и продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТ РЕАКЦИИ
1) пропан
2) бутан
3) этан
4) этен
5) пропен
6) уксусная кислота
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по химии 2020. Основная волна. Вариант 2
Дана схема превращений:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Кристаллогидрат сульфата алюминия, в котором массовая доля серы меньше массовой доли кислорода в 5 раз, растворили в воде с образованием раствора массой 722,4 г. Полученный раствор подвергли электролизу до выделения на аноде 35,84 л (н. у.) газа. К образовавшемуся раствору добавили 424 г 10%-го раствора карбоната натрия, после всех реакций его массовая доля уменьшилась в 10 раз. Определите массу растворенного кристаллогидрата сульфата алюминия. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Источник: ЕГЭ по химии 2021. Основная волна. Вариант 2
Электролиз 522 г 10 %-го раствора нитрата бария проводили до тех пор, пока на катоде не образовалось 94,08 л газа (н. у.). Полученный раствор смешали с насыщенным при комнатной температуре раствором сульфата меди(II), приготовленным при добавлении воды к медному купоросу массой 100 г. После окончания всех реакций массовая доля сульфата меди(II) уменьшилась в 4 раза. Вычислите растворимость безводного сульфата меди(II) при комнатной температуре (в г на 100 г воды). В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Источник: Задания 34 ЕГЭ–2021 по химии
При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите молекулярные уравнения четырех описанных реакций.
Источник: Демонстрационная версия ЕГЭ—2022 по химии, Демонстрационная версия ЕГЭ—2023 по химии
Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Бромоводородную кислоту нейтрализовали карбонатом натрия. Полученный раствор подвергли электролизу. Газ, выделившийся на катоде, пропустили при нагревании над оксидом меди(II). Образовавшееся твёрдое вещество поместили в концентрированный раствор азотной кислоты. Напишите уравнения четырёх описанных реакций.
Источник: ЕГЭ по химии 2022. Досрочная волна
Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Установите соответствие между схемой реакции и веществом X, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Установите соответствие между названием газа и основным способом его получения в промышленности: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ
1) перегонка нефти
2) пиролиз нефти
3) перегонка жидкого воздуха
4) электролиз раствора хлорида натрия
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: СтатГрад: Тренировочная работа 09.11.2022. Вариант ХИ2210201.
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) этан
2) бутан
3) гексан
4) гексин-3
5) гексадиен-2,4
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Источник: СтатГрад: Тренировочная работа 09.11.2022. Вариант ХИ2210202.
Навеску сульфида меди(II) массой 14,4 г сожгли в атмосфере кислорода. Твёрдый остаток растворили в строго необходимом количестве 10 %-й серной кислоты, а полученный раствор подвергли электролизу с инертным анодом, в результате чего на аноде выделилось 1,12 л газа (н. у.). Рассчитайте массу полученного после электролиза раствора и массовые доли веществ в нём. Примите В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
Всего: 263 … 141–160 | 161–180 | 181–200 | 201–220 | 221–240 | 241–260 | 261–263
В течение последних лет все более широкое
применение получает электрохимический
метод в синтезе органических соединений.
Здесь используется важное преимущество
электрохимического метода, возможность
точного дозирования и быстрого
регулирования окислительно-восстановительных
процессов, что обеспечивает получение
чистых продуктов и их высокий выход.
Впервые электролиз органического
вещества был осуществлен Кольбе в 1951
году. Он погрузил два платиновых электрода
в щелочной раствор валериановой кислоты
(C4H9COOH)
и в результате пропускания тока получил
жидкое вещество, состоящее только их
водорода и углерода. Кольбе предполагал,
что получил бутил:
.
Позднее выяснилось, что это не бутил, а
октан C8H18и схему реакции нужно дополнить уравнением
завершающей стадии сдваивания
.
Как правило, вещества, подвергающиеся
электролизу, до пропускания электрического
тока не реагирует между собой, а для
того чтобы прекратить идущую реакцию,
нужно отключить ток. Поэтому один из
способов сделать реакцию управляемой
– это проводить ее с помощью электросинтеза.
Хлор и бром часто реагируют с органическими
соединениями очень бурно, даже если их
подают в зону реакции очень осторожно.
А если хлор и бром не подавать извне, а
получать в реакторе с помощью электролиза,
то тогда их концентрация будет определяться
величиной подаваемого тока.
Если, например, в реактор загрузить
водный раствор NaClи
пропускать через него этилен, который
ни сNaCl, ни сH2Oне взаимодействует, затем включить ток
(в реакторе есть пара графитовых
электродов), то на аноде начинает
выделяться хлор.
Дальнейший ход реакции зависит от
величины тока. Если ток достаточный, то
образуется дихлорэтан – широко
применяемый растворитель:
CH2=CH2
+ 2Cl–
– 2ē → Cl–CH2–CH2–Cl.
При других условиях в реакцию вступает
вода и образуется другой продукт реакции
– этиленхлоргидрин – важный полупродукт
химического синтеза:
CH2=CH2
+ Cl–
+H2O
Cl–CH2–CH2–OH
+ H+.
На катоде одновременно происходит
восстановление ионов водорода
2H+ + 2e
→ H2.
По мере убывания концентрации ионов
водорода среда становится более щелочной,
при этом этиленхлоргидрин превращается
в окись этилена:
Cl–CH2–CH2–OH
+ NaOH →
+
H2O
+ NaCl.
С помощью электросинтеза получают окись
пропилена. Реакция происходит в
электролизере с диафрагмой. Электролизу
подвергается раствор хлорида натрия.
В анодное пространство электролизера
подается пропилен, который, взаимодействия
с образовавшимся на аноде хлором,
превращается в пропиленхлоргидрин.
Последний фильтруется через диафрагму
в катодное пространство электролизера,
где омыляется образовавшейся на катоде
щелочью и превращается в окись пропилена.
Электросинтез является основным
промышленным способом получения
фторорганических соединений, применяемых
в качестве диэлектриков и поверхностно-активных
веществ.
С помощью электролизера можно осуществить
реакцию алкилирования.
При проведения электролиза раствора
уксусной кислоты (CH3COOH)
под давлением насыщенным этиленом
наряду с этаном – обычным продуктом
электролиза уксусной кислоты – был
получен бутан.
CH3COO–
– ē → [CH3COO]
2
→ CH3–CH3
2
+ CH2=CH2
→ CH3–CH2–CH2–CH3.
Метильные радикалы присоединяются к
двойной связи молекулы этилена. При
проведении этой реакции нужно поддерживать
определенное соотношение между молекулами
этилена и метильными радикалами – это
осуществляется с помощью электрического
тока.
Электрохимия позволяет также изменять
потенциал электрода, на котором происходит
изучаемая реакция, или поддерживать
его строго постоянным. Такой электрод
с управляемым потенциалом можно
использовать взамен целого набора
реагентов.
Если, например, восстановление ацетона
происходит на цинковом катоде, то при
низком потенциале в присутствии ацетата
натрия образуется изопропиловый спирт
,
в щелочной среде ацетон на 60% превращается
в цинакон
,
а при высоком потенциале основным
продуктом становится пропан.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Электролиз расплавов и растворов (солей, щелочей)
Если в раствор или расплав электролита опустить электроды и пропустить постоянный электрический ток, то ионы будут двигаться направленно: катионы к катоду (отрицательно заряженному электроду), анионы к аноду (положительно заряженному электроду).
На катоде катионы принимают электроны и восстанавливаются, на аноде анионы отдают электроны и окисляются. Этот процесс называют электролизом.
Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита.
Электролиз расплавленных солей
Рассмотрим процесс электролиза расплава хлорида натрия. В расплаве идет процесс термической диссоциации:
$NaCl→Na^{+}+Cl^{-}.$
Под действием электрического тока катионы $Na^{+}$ движутся к катоду и принимают от него электроны:
$Na^{+}+ē→{Na}↖{0}$ (восстановление).
Анионы $Cl^{-}$ движутся к аноду и отдают электроны:
$2Cl^{-}-2ē→{Cl_2}↖{0}↑$ (окисление).
Суммарное уравнение процессов:
$Na^{+}+ē→{Na}↖{0}|2$
$2Cl^{-}-2ē→{Cl_2}↖{0}↑|1$
$2Na^{+}+2Cl^{-}=2{Na}↖{0}+{Cl_2}↖{0}↑$
или
$2NaCl{→}↖{text»электролиз»}2Na+Cl_2↑$
На катоде образуется металлический натрий, на аноде — газообразный хлор.
Главное, что вы должны помнить: в процессе электролиза за счет электрической энергии осуществляется химическая реакция, которая самопроизвольно идти не может.
Электролиз водных растворов электролитов
Более сложный случай — электролиз растворов электролитов.
В растворе соли, кроме ионов металла и кислотного остатка, присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие в электролизе.
Для определения продуктов электролиза водных растворов электролитов существуют следующие правила:
1. Процесс на катоде зависит не от материала, из которого сделан катод, а от положения металла (катиона электролита) в электрохимическом ряду напряжений, при этом если:
1.1. Катион электролита расположен в ряду напряжений в начале ряда по $Al$ включительно, то на катоде идет процесс восстановления воды (выделяется водород $Н_2↑$). Катионы металла не восстанавливаются, они остаются в растворе.
1.2. Катион электролита находится в ряду напряжений между алюминием и водородом, то на катоде восстанавливаются одновременно и ионы металла, и молекулы воды.
1.3. Катион электролита находится в ряду напряжений после водорода, то на катоде восстанавливаются катионы металла.
1.4. В растворе содержатся катионы разных металлов, то сначала восстанавливается катион металла, стоящий в ряду напряжений правее.
Катодные процессы
| $Li K Ca Na Mg Al$ $Li^{+} K^{+} Ca^{2+} Na^{+} Mg^{2+} Al^{3+}$ |
$Mn Zn Fe Ni Sn Pb$ $Mn^{2+} Zn^{2+} Fe^{2+} Ni^{2+} Sn^{2+} Pb^{2+}$ |
$H_2$ $2H^{+}$ |
$Cu Hg Ag Pt Au$ $Cu^{2+} Hg_2^{2+} Ag^{+} Pt^{2+} Au^{3+}$ |
| Восстанавливается вода: $2H_2O+2ē=H_2↑+2OH^{−};$ $M^{n+}$ не восстанавливается |
Восстанавливаются катионы металла и вода: $M^{n+}+nē=M^0$ $2H_2O+2ē=H_2↑+2OH^{−}$ |
Восстанавливаются катионы металла: $M^{n+}+nē=M^0$ | |
| $nē→$ Усиление окислительных свойств катионов (способности принимать электроны) |
2. Процесс на аноде зависит от материала анода и от природы аниона.
Анодные процессы
| Кислотный остаток $Ас^{m–}$ | Анод | |
| Растворимый | Нерастворимый | |
| Бескислородный | Окисление металла анода $M^{−}−nē=M^{n+}$ анод раствор |
Окисление аниона (кроме $F^{–}$) $Ac^{m−}−mē=Ac^0$ |
| Кислородсодержащий | В кислотной и нейтральной средах: $2H_2O−4ē=O_2↑+4H^{+}$ В щелочной среде: $4OH^{−}−4ē=O_2↑+4H^{+}$ |
2.1. Если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются в процессе электролиза), то окисляется металл анода, несмотря на природу аниона.
2.2. Если анод не растворяется (его называют инертным — графит, золото, платина), то:
а) при электролизе растворов солей бескислородных кислот (кроме фторидов) на аноде идет процесс окисления аниона;
б) при электролизе растворов солей кислородсодержащих кислот и фторидов на аноде идет процесс окисления воды (выделяется $О_2↑$). Анионы не окисляются, они остаются в растворе;
в) анионы по их способности окисляться располагаются в следующем порядке:
Попробуем применить эти правила в конкретных ситуациях.
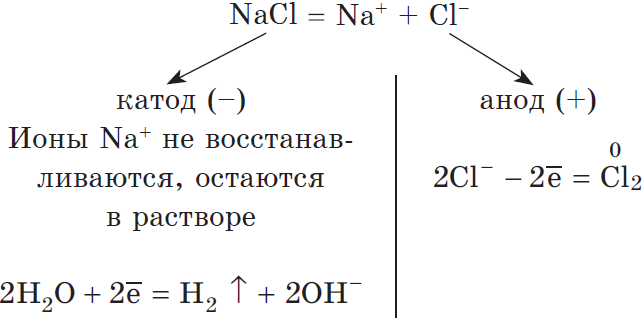
Рассмотрим электролиз раствора хлорида натрия в случае, если анод нерастворимый и если анод растворимый.
1) Анод нерастворимый (например, графитовый).
В растворе идет процесс электролитической диссоциации:
Суммарное уравнение:
$2H_2O+2Cl^{-}=H_2↑+Cl_2↑+2OH^{-}$.
Учитывая присутствие ионов $Na^{+}$ в растворе, составляем молекулярное уравнение:
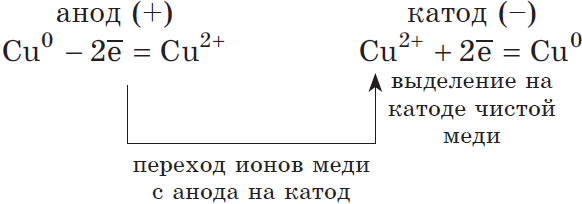
2) Анод растворимый (например, медный):
$NaCl=Na^{+}+Cl^{-}$.
Если анод растворимый, то металл анода будет окисляться:
$Cu^{0}-2ē=Cu^{2+}$.
Катионы $Cu^{2+}$ в ряду напряжений стоят после ($Н^{+}$), по этому они и будут восстанавливаться на катоде.
Концентрация $NaCl$ в растворе не меняется.
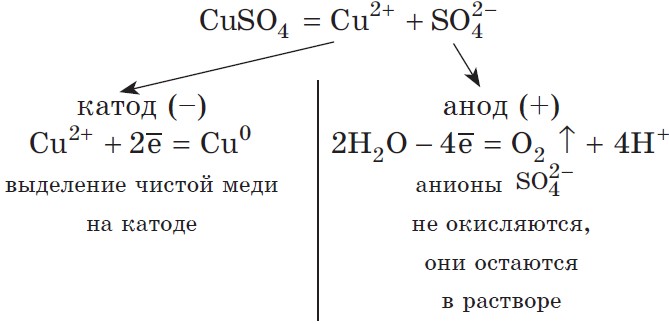
Рассмотрим электролиз раствора сульфата меди (II) на нерастворимом аноде:
$Cu^{2+}+2ē=Cu^{0}|2$
$2H_2O-4ē=O_2↑+4H^{+}|1$
Суммарное ионное уравнение:
$2Cu^{2+}+2H_2O=2Cu^{0}+O_2↑+4H^{+}$
Суммарное молекулярное уравнение с учетом присутствия анионов $SO_4^{2-}$ в растворе:
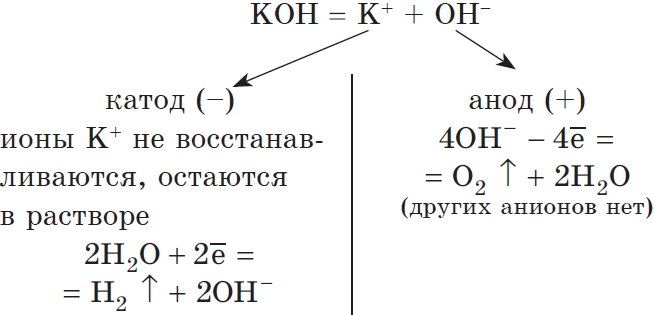
Рассмотрим электролиз раствора гидроксида калия на нерастворимом аноде:
$2H_2O+2ē=H_2↑+2OH^{-}|2$
$4OH^{-}-4ē=O_2↑+2H_2O|1$
Суммарное ионное уравнение:
$4H_2O+4OH^{-}=2H_2↑+4OH^{-}+O_2↑+2H_2O$
Суммарное молекулярное уравнение:
$2H_2O{→}↖{text»электролиз»}2H_2↑+O_2↑$
В данном случае, оказывается, идет только электролиз воды. Аналогичный результат получим и в случае электролиза растворов $H_2SO_4, NaNO_3, K_2SO_4$ и др.
Электролиз расплавов и растворов веществ широко используется в промышленности:
- Для получения металлов (алюминий, магний, натрий, кадмий получают только электролизом).
- Для получения водорода, галогенов, щелочей.
- Для очистки металлов — рафинирования (очистку меди, никеля, свинца проводят электрохимическим методом).
- Для защиты металлов от коррозии (хрома, никеля, меди, серебра, золота) — гальваностегия.
- Для получения металлических копий, пластинок — гальванопластика.
Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 20 ЕГЭ по химии) ( с ответами)
Электролиз
Химические реакции, сопровождающиеся переносом электронов (окислительно-восстановительные реакции) делятся на два типа: реакции, протекающие самопроизвольно и реакции, протекающие при прохождении тока через раствор или расплав электролита.
Раствор или расплав электролита помещают в специальную емкость — электролитическую ванну.
Электрический ток — это упорядоченное движение заряженных частиц — ионов, электронов и др. под действием внешнего электрического поля. Электрическое поле в растворе или расплаве электролита создают электроды.
Электроды — это, как правило, стержни из материала, проводящего электрический ток. Их помещают в раствор или расплав электролита, и подключают к электрической цепи с источником питания.
При этом отрицательно заряженный электрод катод — притягивает положительно заряженные ионы — катионы. Положительно заряженный электрод (анод) притягивает отрицательно заряженные частицы (анионы). Катод выступает в качестве восстановителя, а анод — в качестве окислителя.
Различают электролиз с активными и инертными электродами. Активные (растворимые) электроды подвергаются химическим превращениям в процессе электролиза. Обычно их изготавливают из меди, никеля и других металлов. Инертные (нерастворимые) электроды химическим превращениям не подвергаются. Их изготавливают из неактивных металлов, например, платины, или графита.
Электролиз растворов
Различают электролиз раствора или расплава химического вещества. В растворе присутствует дополнительное химическое вещество — вода, которая может принимать участие в окислительно-восстановительных реакциях.
Катодные процессы
В растворе солей катод притягивает катионы металлов. Катионы металлов могут выступать в качестве окислителей. Окислительные способности ионов металлов различаются. Для оценки окислительно-восстановительных способностей металлов применяют электро-химический ряд напряжений:
Каждый металл характеризуется значением электрохимического потен-циала. Чем меньше потенциал, тем больше восстановительные свойства металла и тем меньше окислительные свойства соответствующего иона этого металла. Разным ионам соответствуют разные значения этого потенциала. Электрохимический потенциал — относительная величина. Электрохимический потенциал водорода принят равным нулю.
Также около катода находятся молекулы воды Н2О. В составе воды есть окислитель — ион H+.
При электролизе растворов солей на катоде наблюдаются следующие закономерности:
1. Если металл в соли — активный (до Al3+ включительно в ряду напряжений), то вместо металла на катоде восстанавливается (разряжается) водород, т.к. потенциал водорода намного больше. Протекает процесс восстановления молекулярного водорода из воды, при этом образуются ионы OH—, среда возле катода — щелочная:
2H2O +2ē → H2 + 2OH—
Например, при электролизе раствора хлорида натрия на катоде будет вос-станавливаться только водород из воды.
2. Если металл в соли – средней активности (между Al3+ и Н+), то на катоде восстанавливается (разряжается) и металл, и водород, так как потенциал таких металлов сравним с потенциалом водорода:
Men+ + nē → Me0
2H+2O +2ē → H20 + 2OH—
Например, при электролизе раствора сульфата железа (II) на катоде будет восстанавливаться (разряжаться) и железо, и водород:
Fe2+ + 2ē → Fe0
2H+2O +2ē → H20 + 2OH—
3. Если металл в соли — неактивный (после водорода в ряду стандартных электрохимических металлов), то ион такого металла является более сильным окислителем, чем ион водорода, и на катоде восстанавливается только металл:
Men+ + nē → Me0
Например, при электролизе раствора сульфата меди (II) на катоде будет восстанавливаться медь:
Cu2+ + 2ē → Cu0
4. Если на катод попадают катионы водорода H+, то они и восстанавливаются до молекулярного водорода:
2H+ + 2ē → H20
Анодные процессы
Положительно заряженный анод притягивает анионы и молекулы воды. Анод – окислитель. В качестве восстановителей выступаю либо анионы кислотных остаток, либо молекулы воды (за счет кислорода в степени окисления -2: H2O-2).
При электролизе растворов солей на аноде наблюдаются следующие закономерности:
1. Если на анод попадает бескислородный кислотный остаток, то он окисляется до свободного состояния (до степени окисления 0):
неМеn- – nē = неМе0
Например: при электролизе раствора хлорида натрия на аноде окисляют-ся хлорид-ионы:
2Cl— – 2ē = Cl20
Действительно, если вспомнить Периодический закон: при увеличении электроотрицательности неметалла его восстановительные свойства уменьшаются. А кислород – второй по величине электроотрицательности элемент. Таким образом, проще окислить практически любой неметалл, а не кислород. Правда, есть одно исключение. Наверное, вы уже догадались. Конечно же, это фтор. Ведь электроотрицательность фтора больше, чем у кислорода. Таким образом, при электролизе растворов фторидов окисляться будут именно молекулы воды, а не фторид-ионы:
2H2O-2 – 4ē → O20+ 4H+
2. Если на анод попадает кислородсодержащий кислотный остаток, либо фторид-ион, то окислению подвергается вода с выделением молекулярно-го кислорода:
2H2O-2 – 4ē → O20 + 4H+
3. Если на анод попадает гидроксид-ион, то он окисляется и происходит выделение молекулярного кислорода:
4O-2H– – 4ē → O20 + 2H2O
4. При электролизе растворов солей карбоновых кислот окислению под-вергается атом углерода карбоксильной группы, выделяется углекислый газ и соответствующий алкан.
Например, при электролизе растворов ацетатов выделяется углекислый газ и этан:
2CH3C+3OO– –2ē → 2C+4O2+ CH3-CH3
Суммарные процессы электролиза
Рассмотрим электролиз растворов различных солей.
Например, электролиз раствора сульфата меди. На катоде восстанавливаются ионы меди:
Катод (–): Cu2+ + 2ē → Cu0
На аноде окисляются молекулы воды:
Анод (+): 2H2O-2 – 4ē → O2 + 4H+
Сульфат-ионы в процессе не участвуют. Мы их запишем в итоговом уравнении с ионами водорода в виде серной кислоты:
2Cu2+SO4 + 2H2O-2 → 2Cu0 + 2H2SO4 + O20
Электролиз раствора хлорида натрия выглядит так:
На катоде восстанавливается водород:
Катод (–): 2H+2O +2ē → H20 + 2OH–
На аноде окисляются хлорид-ионы:
Анод (+): 2Cl– – 2ē → Cl20
Ионы натрия в процессе электролиза не участвуют. Мы записываем их с гидроксид-анионами в суммарном уравнении электролиза раствора хлорида натрия:
2H+2O +2NaCl– → H20 + 2NaOH + Cl20
Следующий пример: электролиз водного раствора карбоната калия.
На катоде восстанавливается водород из воды:
Катод (–): 2H+2O +2ē → H20 + 2OH–
На аноде окисляются молекулы воды до молекулярного кислорода:
Анод (+): 2H2O-2 – 4ē → O20 + 4H+
Таким образом, при электролизе раствора карбоната калия ионы калия и карбонат-ионы в процессе не участвуют. Происходит электролиз воды:
2H2+O-2 → 2H20 + O20
Еще один пример: электролиз водного раствора хлорида меди (II).
На катоде восстанавливается медь:
Катод (–): Cu2+ + 2ē → Cu0
На аноде окисляются хлорид-ионы до молекулярного хлора:
Анод (+): 2Cl– – 2ē → Cl20
Таким образом, при электролизе раствора карбоната калия происходит электролиз воды:
Cu2+Cl2– → Cu0 + Cl20
Еще несколько примеров: электролиз раствора гидроксида натрия.
На катоде восстанавливается водород из воды:
Катод (–): 2H+2O +2ē → H20 + 2OH–
На аноде окисляются гидроксид-ионы до молекулярного кислорода:
Анод (+): 4O-2H– – 4ē → O20 + 2H2O
Таким образом, при электролизе раствора гидроксида натрия происходит разложение воды, катионы натрия в процессе не участвуют:
2H2+O-2 → 2H20 + O20
Электролиз расплавов
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na+ + ē → Na0
На аноде окисляются анионы хлора:
Анод (+): 2Cl– – 2ē → Cl20
Суммарное уравнение электролиза расплава хлорида натрия:
2Na+Cl– → 2Na0 + Cl20
Еще один пример: электролиз расплава гидроксида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na+ + ē → Na0
На аноде окисляются гидроксид-ионы:
Анод (+): 4OH– – 4ē → O20 + 2H2O
Суммарное уравнение электролиза расплава гидроксида натрия:
4Na+OH– → 4Na0 + O20 + 2H2O
Многие металлы получают в промышленности электролизом расплавов.
Например, алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na3[AlF6] плавится при более низкой температуре (1100оС), чем оксид алюминия (2050оС). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
Al2O3 = Al3+ + AlO33-
На катоде восстанавливаются катионы алюминия:
Катод (–): Al3+ + 3ē → Al0
На аноде окисляются алюминат-ионы:
Анод (+): 4AlO33– – 12ē → 2Al2O3 + 3O20
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2Al2О3 = 4Al0 + 3О20
В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C0 + О20 = C+4O2-2
Электролиз с растворимыми электродами
Если материал электродов выполнен из того же металла, который присутствует в растворе в виде соли, или из более активного металла, то на аноде разряжаются не молекулы воды или анионы, а окисляются частицы самого металла в составе электрода.
Например, рассмотрим электролиз раствора сульфата меди (II) с медными электродами.
На катоде разряжаются ионы меди из раствора:
Катод (–): Cu2+ + 2ē → Cu0
На аноде окисляются частицы меди из электрода:
Анод (+): Cu0 – 2ē → Cu2+
Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 20 ЕГЭ по химии) ( с ответами)
201
Создан на
11 января, 2022 От Admin
Электролиз
Тренажер задания 20 ЕГЭ по химии
1 / 10
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, которые образовались на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
|
А) Na2S Б) К2SO4 В) СuSO4 Г) Cu(NO3)2 |
1) Н2, O2 2) Сu, O2 3) Н2, S 4) Сu, S 5) Н2, NO2 |
2 / 10
Установите соответствие между веществом и способом его электролитического получения.
К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
ВЕЩЕСТВО |
ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ |
|
А) калий Б) фтор В) алюминий Г) водород |
1) расплава KF 2) водного раствора AgF 3) водного раствора Al2(SO4)3 4) водного раствора CuCl2 5) раствора Al2O3 в расплавленном криолите 6) водного раствора AgNO3 |
3 / 10
Установите соответствие между металлом и способом его электролитического получения.
К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
НАЗВАНИЕ МЕТАЛЛА |
СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛА |
|
А) натрий Б) алюминий В) серебро Г) медь |
1) электролиз водного раствора солей 2) электролиз водного раствора гидроксида 3) электролиз расплава поваренной соли 4) электролиз расплавленного оксида 5) электролиз раствора оксида в расплавленном криолите 6) электролиз расплавленного нитрата |
4 / 10
Установите соответствие между названием вещества и электролитическим способом получения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | ЭЛЕКТРОЛИЗ |
|
А) водород Б) алюминий В) калий Г) фтор |
1) расплава КF 2) водного раствора СuCl2 3) раствора Аl2O3 в расплавленном криолите 4) водного раствора Аl2(SO4)3 5) водного раствора АgF |
5 / 10
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
|
А) KI Б) Сu(NO3)2 В) Li2S Г) Li2SO4 |
1) металл и кислород 2) водород и кислород 3) металл и галоген 4) металл и сера 5) водород и сера 6) водород и галоген |
6 / 10
Установите соответствие между солью и продуктами электролиза водного раствора этого вещества, которые образовались на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СОЛЬ | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
| A) Nal
Б) Ca(NO3)2 B) K2SO4 |
1) металл, галоген
2) металл, кислород 3) водород, галоген 4) водород, кислород |
7 / 10
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
|
А) K3РО4 Б) Са(NО3)2 В) RbBr Г) CuCl2 |
1) металл и азот 2) металл и кислород 3) металл и галоген 4) водород и сера 5) водород и галоген 6) водород и кислород |
8 / 10
Установите соответствие между названием вещества и электролитическим способом получения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | ЭЛЕКТРОЛИЗ |
|
А) кислород Б) хлор В) водород Г) бром |
1) расплава КI 2) водного раствора КСlO3 3) расплава NaF 4) водного раствора СuBr2 5) расплава SiO2 6) водного раствора СuCl2 |
9 / 10
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
|
А) КI Б) НgCl2 В) СuSO4 Г) Са(NO3)2 |
1) металл и кислород 2) водород и кислород 3) металл и галоген 4) водород и галоген 5) металл и азот 6) водород и сера |
10 / 10
Установите соответствие между названием простого вещества и способом его электролитического получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ |
|
А) натрий Б) алюминий В) сера Г) фтор |
1) водного раствора АgF 2) водного раствора Аl2(SО4)3 3) расплава NаСl 4) расплава КF 5) раствора Аl2О3 в расплавленном криолите 6) водного раствора Na2S |
Ваша оценка
The average score is 45%
Электролиз растворов электролитов с инертными электродами
Напомним, что на катоде протекают процессы восстановления, на аноде — процессы окисления.
Процессы, протекающие на катоде:
В растворе имеются несколько видов положительно заряженных частиц, способных восстанавливаться на катоде:
1) Катионы металла восстанавливаются до простого вещества, если металл находится в ряду напряжений правее алюминия (не включая сам Al). Например:
Zn2+ +2e → Zn0.
2) В случае раствора соли или щелочи: катионы водорода восстанавливаются до простого вещества, если металл находится в ряду напряжений металлов до H2:
2H2O + 2e → H20 + 2OH–.
Например, в случае электролиза растворов NaNO3 или KOH.
3) В случае электролиза раствора кислоты: катионы водорода восстанавливаются до простого вещества:
2H+ +2e → H2.
Например, в случае электролиза раствора H2SO4.
Процессы, протекающие на аноде:
На аноде легко окисляются кислотные остатки не содержащие кислород. Например, галогенид-ионы (кроме F–), сульфид-анионы, гидроксид-анионы и молекулы воды:
1) Галогенид-анионы окисляются до простых веществ:
2Cl– – 2e → Cl2.
2) В случае электролиза раствора щелочи в гидроксид-анионах кислород окисляется до простого вещества. Водород уже имеет степень окисления +1 и не может быть окислен дальше. Также будет выделение воды — почему? Потому что больше ничего написать и не получится: 1) H+ написать не можем, так как OH– и H+ не могут стоять по разные стороны одного уравнения; 2) H2 написать также не можем, так как это был бы процесс восстановления водорода (2H+ +2e → H2), а на аноде протекают только процессы окисления.
4OH– – 4e → O2 + 2H2O.
3) Если в растворе есть анионы фтора или любые кислородсодержащие анионы, то окислению будет подвергаться вода с подкислением прианодного пространства согласно следующему уравнению:
2H2O – 4e → O2 + 4H+.
Такая реакция идет в случае электролиза растворов кислородсодержащих солей или кислородсодержащих кислот. В случае электролиза раствора щелочи окисляться будут гидроксид-анионы согласно правилу 2) выше.
4) В случае электролиза раствора соли органической кислоты на аноде всегда происходит выделение CO2 и удвоение остатка углеродной цепи:
2R-COO– – 2e → R-R + 2CO2.
Примеры:
1. Раствор NaCl
Расписываем диссоциацию на ионы:
NaCl → Na+ + Cl–
Металл Na стоит в ряду напряжений до алюминия, следовательно, восстанавливаться на катоде не будет (катионы остаются в растворе). Согласно правилу выше, на катоде восстанавливается водород. Хлорид-анионы будут окисляться на аноде до простого вещества:
К: 2Na+ (в растворе)
2H2O + 2e → H20 + 2OH–
А: 2Cl– – 2e → Cl2
Коэффициент 2 перед Na+ появился из-за наличия аналогичного коэффициента перед хлорид-ионами, так как в соли NaCl их соотношение 1:1.
Проверяем, что количество принимаемых и отдаваемых электронов одинаковое, и суммируем левые и правые части катодных и анодных процессов:
2Na+ + 2Cl– + 2H2O → H20 + 2Na+ + 2OH– + Cl2. Соединяем катионы и анионы:
2NaCl + 2H2O → H20 + 2NaOH + Cl2.
2. Раствор Na2SO4
Расписываем диссоциацию на ионы:
Na2SO4 → 2Na+ + SO42–
Натрий стоит в ряду напряжений до алюминия, следовательно, восстанавливаться на катоде не будет (катионы остаются в растворе). Согласно правилу выше, на катоде восстанавливается только водород. Сульфат-анионы содержат кислород, поэтому окисляться не будут, также оставаясь в растворе. Согласно правилу выше, в этом случае окисляются молекулы воды:
К: 2H2O + 2e → H20 + 2OH–
А: 2H2O – 4e → O20 + 4H+.
Уравниваем число принимаемых и отдаваемых электронов на катоде и аноде. Для этого необходимо умножить все коэффициенты катодного процесса на 2:
К: 4H2O + 4e → 2H20 + 4OH–
А: 2H2O – 4e → O20 + 4H+.
Складываем левые и правые части катодных и анодных процессов:
6H2O → 2H20 + 4OH– + 4H+ + O20.
4OH- и 4H+ соединяем в 4 молекулы H2O:
6H2O → 2H20 + 4H2O + O20.
Сокращаем молекулы воды, находящиеся по обе стороны уравнения, т.е. вычитаем из каждой части уравнения 4H2O и получаем итоговое уравнение гидролиза:
2H2O → 2H20 + O20.
Таким образом, гидролиз растворов кислородсодержащих солей активных металлов (до Al включительно) сводится к гидролизу воды, так как ни катионы металлов, ни анионы кислотных остатков не принимают участие в окислительно-восстановительных процессах, протекающих на электродах.
3. Раствор CuCl2
Расписываем диссоциацию на ионы:
CuCl2 → Cu2+ + 2Cl–
Медь находится в ряду напряжений металлов после водорода, следовательно, только она будет восстанавливаться на катоде. На аноде будут окисляться только хлорид-анионы.
К: Cu2+ + 2e → Cu0
A: 2Cl– – 2e → Cl2
Записываем суммарное уравнение:
CuCl2 → Cu0 + Cl2.
4. Раствор CuSO4
Расписываем диссоциацию на ионы:
CuSO4 → Cu2+ + SO42–
Медь находится в ряду напряжений металлов после водорода, следовательно, только она будет восстанавливаться на катоде. На аноде будут окисляться молекулы воды, так как кислородсодержащие кислотные остатки в растворах на аноде не окисляются.
К: Cu2+ + 2e → Cu0
A: SO42– (в растворе)
2H2O – 4e → O2 + 4H+.
Уравниваем количество электронов на катоде и аноде. Для это умножим все коэффициенты катодного уравнения на 2. Количество сульфат-ионов также необходимо удвоить, так как в сульфате меди соотношение Cu2+ и SO42– 1:1.
К: 2Cu2+ + 4e → 2Cu0
A: 2SO42– (в растворе)
2H2O – 4e → O2 + 4H+.
Записываем суммарное уравнение:
2Cu2+ + 2SO42– + 2H2O → 2Cu0 + O2 + 4H+ + 2SO42–.
Соединив катионы и анионы, получаем итоговое уравнение электролиза:
2CuSO4 + 2H2O → 2Cu0 + O2 + 2H2SO4.
5. Раствор NiCl2
Расписываем диссоциацию на ионы:
NiCl2 → Ni2+ + 2Cl–
Никель находится в ряду напряжений металлов после алюминия и до водорода, следовательно, на катоде будут восстанавливаться и металл, и водород. На аноде будут окисляться только хлорид-анионы.
К: Ni2+ + 2e → Ni0
2H2O + 2e → H20 + 2OH–
A: 2Cl– – 2e → Cl2
Уравниваем количество электронов, принимаемых и отдаваемых на катоде и аноде. Для этого умножаем все коэффициенты анодного уравнения на 2:
К: Ni2+ + 2e → Ni0
2H2O + 2e → H20 + 2OH–
Ni2+ (в растворе)
A: 4Cl– – 4e → 2Cl2
Замечаем, что согласно формуле NiCl2, соотношение атомов никеля и хлора 1:2, следовательно, в раствор необходимо добавить Ni2+ для получения общего количества 2NiCl2. Также это необходимо сделать, так как в растворе должны присутствовать противоионы для гидроксид-анионов.
Складываем левые и правые части катодных и анодных процессов:
Ni2+ + Ni2+ + 4Cl– + 2H2O → Ni0 + H20 + 2OH– + Ni2+ + 2Cl2.
Соединяем катионы и анионы для получения итогового уравнения электролиза:
2NiCl2 + 2H2O → Ni0 + H20 + Ni(OH)2 + 2Cl2.
6. Раствор NiSO4
Расписываем диссоциацию на ионы:
NiSO4 → Ni2+ + SO42–
Никель находится в ряду напряжений металлов после алюминия и до водорода, следовательно, на катоде будут восстанавливаться и металл, и водород. На аноде будут окисляться молекулы воды, так как кислородсодержащие кислотные остатки в растворах на аноде не окисляются.
К: Ni2+ + 2e → Ni0
2H2O + 2e → H20 + 2OH–
A: SO42– (в растворе)
2H2O – 4e → O2 + 4H+.
Проверяем, что количество принятых и отданных электронов совпадает. Также замечаем, что в растворе есть гидроксид-ионы, но в записи электродных процессов для них нет противоионов. Следовательно, нужно добавить в раствор Ni2+. Так как удвоилось количество ионов никеля, необходимо удвоить и количество сульфат-ионов:
К: Ni2+ + 2e → Ni0
2H2O + 2e → H20 + 2OH–
Ni2+ (в растворе)
A: 2SO42– (в растворе)
2H2O – 4e → O2 + 4H+.
Складываем левые и правые части катодных и анодных процессов:
Ni2+ + Ni2+ + 2SO42– + 2H2O + 2H2O → Ni0 + Ni2+ + 2OH– + H20 + O20 + 2SO42– + 4H+.
Соединяем катионы и анионы и записываем итоговое уравнение электролиза:
2NiSO4 + 4H2O → Ni0 + Ni(OH)2 + H20 + O20 + 2H2SO4.
В других источниках литературы также говорится об альтернативном протекании электролиза кислородсодержащих солей металлов средней активности. Разница состоит в том, что после сложения левых и правых частей процессов электролиза необходимо соединить H+ и OH– с образованием двух молекул воды. Оставшиеся 2H+ расходуются на образование серной кислоты. В этом случае не нужно прибавлять дополнительные ионы никеля и сульфат-ионы:
Ni2+ + SO42– + 2H2O + 2H2O → Ni0 + 2OH– + H20 + O20 + SO42– + 4H+.
Ni2+ + SO42– + 4H2O → Ni0 + H20 + O20 + SO42– + 2H+ + 2H2O.
Итоговое уравнение:
NiSO4 + 2H2O → Ni0 + H20 + O20 + H2SO4.
7. Раствор CH3COONa
Расписываем диссоциацию на ионы:
CH3COONa → CH3COO– + Na+
Натрий стоит в ряду напряжений до алюминия, следовательно, восстанавливаться на катоде не будет (катионы остаются в растворе). Согласно правилу выше, на катоде восстанавливается только водород. На аноде будет происходит окисление ацетат-ионов с образованием углекислого газа и удвоением остатка углеродной цепи:
К: 2Na+ (в растворе)
2H2O + 2e → H20 + 2OH–
А: 2CH3COO– – 2e → CH3-CH3 + CO2
Так как количества электронов в процессах окисления и восстановления совпадают, составляем суммарное уравнение:
2Na+ + 2CH3COO– + 2H2O → 2Na+ + 2OH– + H20 + CH3-CH3 + CO2
Соединяем катионы и анионы:
2CH3COONa + 2H2O → 2NaOH + H20 + CH3-CH3 + CO2.
8. Раствор H2SO4
Расписываем диссоциацию на ионы:
H2SO4 → 2H+ + SO42–
Из катионов в растворе присутствуют только катионы H+, они и будут восстанавливаться до простого вещества. На аноде будет протекать окисление воды, так как кислород содержащие кислотные остатки в растворах на аноде не окисляются.
К: 2H+ +2e → H2
A: 2H2O – 4e → O2 + 4H+
Уравниваем число электронов. Для этого удваиваем каждый коэффициент в уравнении катодного процесса:
К: 4H+ +4e → 2H2
A: 2H2O – 4e → O2 + 4H+
Суммируем левые и правые части уравнений:
4H+ + 2H2O → 2H2 + O2 + 4H+
Катионы H+ находятся в обеих частях реакции, следовательно, их нужно сократить. Получаем, что в случае растворов кислот, электролизу подвергаются только молекулы H2O:
2H2O → 2H2 + O2.
9. Раствор NaOH
Расписываем диссоциацию на ионы:
NaOH → Na+ + OH–
Натрий стоит в ряду напряжений до алюминия, следовательно, восстанавливаться на катоде не будет (катионы остаются в растворе). Согласно правилу, на катоде восстанавливается только водород. На аноде будут окисляться гидроксид-анионы с образованием кислорода и воды:
К: Na+ (в растворе)
2H2O + 2e → H20 + 2OH–
А: 4OH– – 4e → O2 + 2H2O
Уравниваем число электронов, принимаемых и отдаваемых на электродах:
К: Na+ (в растворе)
4H2O + 4e → 2H20 + 4OH–
А: 4OH– – 4e → O2 + 2H2O
Суммируем левые и правые части процессов:
4H2O + 4OH– → 2H20 + 4OH– + O20 + 2H2O
Сокращая 2H2O и ионы OH–, получаем итоговое уравнение электролиза:
2H2O → 2H2 + O2.
Вывод:
При электролизе растворов 1) кислородсодержащих кислот;
2) щелочей;
3) солей активных металлов и кислородсодержащих кислот
на электродах протекает электролиз воды:
2H2O → 2H2 + O2.
Скачать материал

Скачать материал


- Сейчас обучается 111 человек из 49 регионов


- Курс добавлен 13.12.2022


- Курс добавлен 13.12.2022


Описание презентации по отдельным слайдам:
-
-
2 слайд
ЭЛЕКТРОЛИТИЧЕСКАЯ ВАННА.
Катод (-)
Анод (+)
Восстановление
Окисление
Электроды -
3 слайд
Электролиз.
Электролиз – окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через расплав или раствор электролита.
Электролиты: соли, щёлочи, кислоты. -
4 слайд
Электролиз расплавов
Расплав KOH = K+ + OH–
(–) Катод: K+ + 1ē = Ko 4
(+) Анод: 4OH– – 4ē = O2↑+ 2H2O 1
4K++ 4OH– = O2↑ + 2H2O↑+ 4K
электролиз
4KOH → 4K + O2↑ + 2H2O↑
Электролиз расплавов -
5 слайд
Электролиз расплавов
Расплав KCl = K+ + Cl–
(–) Катод: K+ + 1ē = Ko 2
(+) Анод: 2Cl– – 2ē = Cl2↑ 1
электролиз
2KCl → 2K + Cl2↑
Электролиз расплавов -
6 слайд
Электролиз Al2O3
Расплав Al2O3 в Na3AlF6 (криолит)
(–) Катод ← Al3+ AlO33- → (+) Анод(–) Катод: Al3+ + 3ē = Al0
(+) Анод: 4AlO33-– 12ē = 2Al2O3 + 3O2↑
2Al2O3 = 4Al +3O2 -
7 слайд
Процессы на катоде
Катионы активных металлов:
Li+, Cs+, Rb+, K+, Ba2+, Ca2+, Na+, Mg2+, Al3+, NH4+
Металлы не восстанавливаются, а восстанавливаются молекулы H2O:
2H2O + 2ē = H2↑ + 2OH– -
8 слайд
Процессы на катоде
Катионы металлов средней активности
Mn2+, Zn2+, Cr3+, Fe2+, Co2+, Ni2+,Sn2+,Pb2+
Катионы металлов восстанавливаются совместно с молекулами воды:
Men++ nē = Meo
2H2O + 2ē = H2↑+ 2OH– -
9 слайд
Процессы на катоде
Катионы водородаH+
Ионы H+ восстанавливаются только при электролизе растворов кислот:
2H++ 2ē = H2↑ -
10 слайд
Процессы на катоде
Катионы малоактивных металлов:
Cu2+, Hg2+, Ag+, Pt2+, Au3+
Восстанавливаются только катионы металлов:
Men++nē = Meo -
11 слайд
Процессы на аноде
1) Анионы бескислородных кислот:
I–, Br–, S2–, Cl–
Окисляются кислотные остатки
Am– – mē = Ao
2) Анионы OH–
Окисляются только при электролизе растворов щёлочей
4OH– – 4ē = O2↑+ 2H2O -
12 слайд
Процессы на аноде
3) Анионы кислородсодержащих кислот:
SO42–, NO3–, CO32–, PO43–
Окисляются молекулы воды:
2H2O – 4ē =O2↑+ 4H+
4) Анионы F–
Окисляются только молекулы воды
2H2O – 4ē = O2↑ + 4H+ -
13 слайд
Если анод растворимый
Анод растворимый (активный), изготовлен из Cu, Ag, Zn, Ni, Fe и др. металлы. Анионы не окисляются. Окисляется сам анод:
Мео – nē = Men+
Катионы Men+ переходят в раствор. Масса анода уменьшается. -
14 слайд
Электролиз раствора NaCl
Раствор NaCl
(–) Катод ← Na+ Cl– → (+) Анод
H2O H2O
(–) Катод: 2H2O + 2ē = H2↑+ 2OH–
(+) Анод: 2Cl– – 2ē = Cl2↑
2H2O + 2Cl– = H2↑ + Cl2↑ + 2OH–
2H2O+2NaCl=H2↑+Cl2↑+ 2NaOH -
15 слайд
Электролиз раствора ZnSO4
Раствор ZnSO4
(–) Катод ← Zn2+ SO42- → (+) Анод
H2O H2O
(–) Катод: 2H2O + 2ē = H2↑+ 2OH–
Zn2+ + 2ē = Zn0
(+) Анод: 2H2O — 4ē = O2↑+ 4H+
Zn2+ + 2H2O = Zn0 +H2↑ + O2↑ + 2H+
ZnSO4 + 2H2O = Zn+H2↑+O2↑+ H2SO4 -
16 слайд
Электролиз раствора CuSO4
Раствор CuSO4
(–) Катод ← Cu2+ SO42- → (+) Анод
H2O H2O
(–) Катод: Cu2+ + 2ē = Cu0
(+) Анод: 2H2O — 4ē = O2↑+ 4H+
Cu2+ + 2H2O = 2Cu0 + O2↑+ 4H+
2CuSO4 + 2H2O = 2Cu+ O2↑+ 2H2SO4 -
17 слайд
Электролиз раствора NaOH
Раствор NaOH
(–) Катод ← Na+ OH– → (+) Анод
H2O H2O
(–) Катод: 2H2O + 2ē = H2↑+ 2OH–
(+) Анод: 4OH- — 4ē = 2H2O↑+ O2↑
4H2O + 4OH– = 2H2↑ + O2↑ + 4OH– + 2H2O
2H2O = 2H2↑+O2↑ -
18 слайд
Если анод растворимый
Анод растворимый.
Электролиз раствора AgNO3
(анод растворимый – из Ag)
(–) Катод: Ag+ + 1ē = Ago
(+) Анод: Ago – 1ē = Ag+
Ago + Ag+ = Ag+ + Ago
Электролиз сводится к переносу серебра с анода на катод. -
-
20 слайд
Электролиз органических солей
(–) Катод ← Na+ СН3СОO– → (+) Анод
H2O H2O
(–) Катод: 2H2O + 2ē = H2↑+ 2OH–
(+) Анод: 2СН3СОO — 2ē = С2Н6 + 2СO2↑
электролиз
2СН3СОONa + 2H2O→ C2H6+2CO2↑ +
+2NaOH +H2Анод: для орг. в-в ( 2RСОО- — 2е = 2СО2 + R – R)
Катод: (кислая среда 2Н+ + 2е = Н2) -
21 слайд
Применение электролиза.
Для получения щёлочных, щёлочноземельных металлов, алюминия, лантаноидов
Для получения точных металлических копий, что называется гальванопластикой
Для защиты металлических изделий от коррозии и для придания декоративного вида. Отрасль прикладной электрохимии, которая занимается покрытием металлических изделий другими металлами называется ГАЛЬВАНОСТЕГИЕЙ. -
22 слайд
Законы электролиза.
Законы Фарадея.
Масса веществ, выделившегося на электроде при электролизе, пропорциональна количеству электричества, прошедшее через электролит:
где , m–масса веществ продуктов электролиза, гр.
Э – эквивалентная масса вещества, гр.
I – сила тока, А.
F – постоянная Фарадея = 96500 Кл.
t – время электролиза, сек. -
23 слайд
Эквивалентная масса (молярная масса эквивалента вещества) mэкв является одной из важнейших характеристик вещества.
По определению эквивалент вещества — это такое количество химического вещества, которая реагирует с 1 г водорода или вытесняет такое же количество водорода из его соединений.
Величина mэкв определяется или экспериментально, или, чаще всего, исходя из химической формулы вещества и его принадлежности к тому или иному классу химических соединений -
24 слайд
mэкв(оксида) = Моксида/(число атомов кислорода·2);
mэкв(основания) = Моснования/кислотность основания;
mэкв(кислоты) = Мкислоты/основность кислоты;
mэкв(соли) = Мсоли/(число атомов металла·валентность металла).
кислотность основания равна числу гидроксильных групп в формуле основания, а основность кислоты равна числу атомов водорода в формуле кислоты.
Например:
mэкв(Fe2O3) = М(Fe2O3)/(3·2) = 160/6 = 26,7 г/моль;
mэкв(H2SO4) = M(H2SO4)/2 = 98/2 = 49 г/моль;
mэкв(Ca(OH)2) = M(Ca(OH)2)/2 = 74/2 = 37 г/моль;
mэкв(Al2(SO4)3) = M(Al2(SO4)3) = 342/2 = 171 г/моль; -
25 слайд
При электролизе раствора хлорида натрия получили раствор, содержащий 20г гидроксида натрия. Газ, выделившийся на аноде в ходе электролиза, пропустили через 665мл 10%-ного водного раствора иодида калия (ρ=1,1 г/мл). Какова масса образовавшегося при этом осадка?
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 157 098 материалов в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Другие материалы
- 19.09.2016
- 959
- 5
Рейтинг:
4 из 5
- 19.09.2016
- 1413
- 3
- 19.09.2016
- 2599
- 8
Рейтинг:
4 из 5
- 19.09.2016
- 4901
- 141


Рейтинг:
4 из 5
- 19.09.2016
- 5074
- 190

- 19.09.2016
- 456
- 0
Вам будут интересны эти курсы:
-
Курс повышения квалификации «Химия окружающей среды»
-
Курс профессиональной переподготовки «Химия: теория и методика преподавания в образовательной организации»
-
Курс повышения квалификации «Нанотехнологии и наноматериалы в биологии. Нанобиотехнологическая продукция»
-
Курс повышения квалификации «Введение в сетевые технологии»
-
Курс повышения квалификации «Организация практики студентов в соответствии с требованиями ФГОС педагогических направлений подготовки»
-
Курс повышения квалификации «Применение MS Word, Excel в финансовых расчетах»
-
Курс повышения квалификации «Особенности подготовки к сдаче ОГЭ по химии в условиях реализации ФГОС ООО»
-
Курс профессиональной переподготовки «Биология и химия: теория и методика преподавания в образовательной организации»
-
Курс повышения квалификации «Основы менеджмента в туризме»
-
Курс повышения квалификации «Современные образовательные технологии в преподавании химии с учетом ФГОС»
-
Курс профессиональной переподготовки «Уголовно-правовые дисциплины: теория и методика преподавания в образовательной организации»
-
Курс профессиональной переподготовки «Техническое сопровождение технологических процессов переработки нефти и газа»
-
Курс профессиональной переподготовки «Организация системы учета и мониторинга обращения с отходами производства и потребления»