Таблицы на ЕГЭ и ОГЭ по химии
На сдаче ЕГЭ и ОГЭ по химии можно использовать три таблицы:
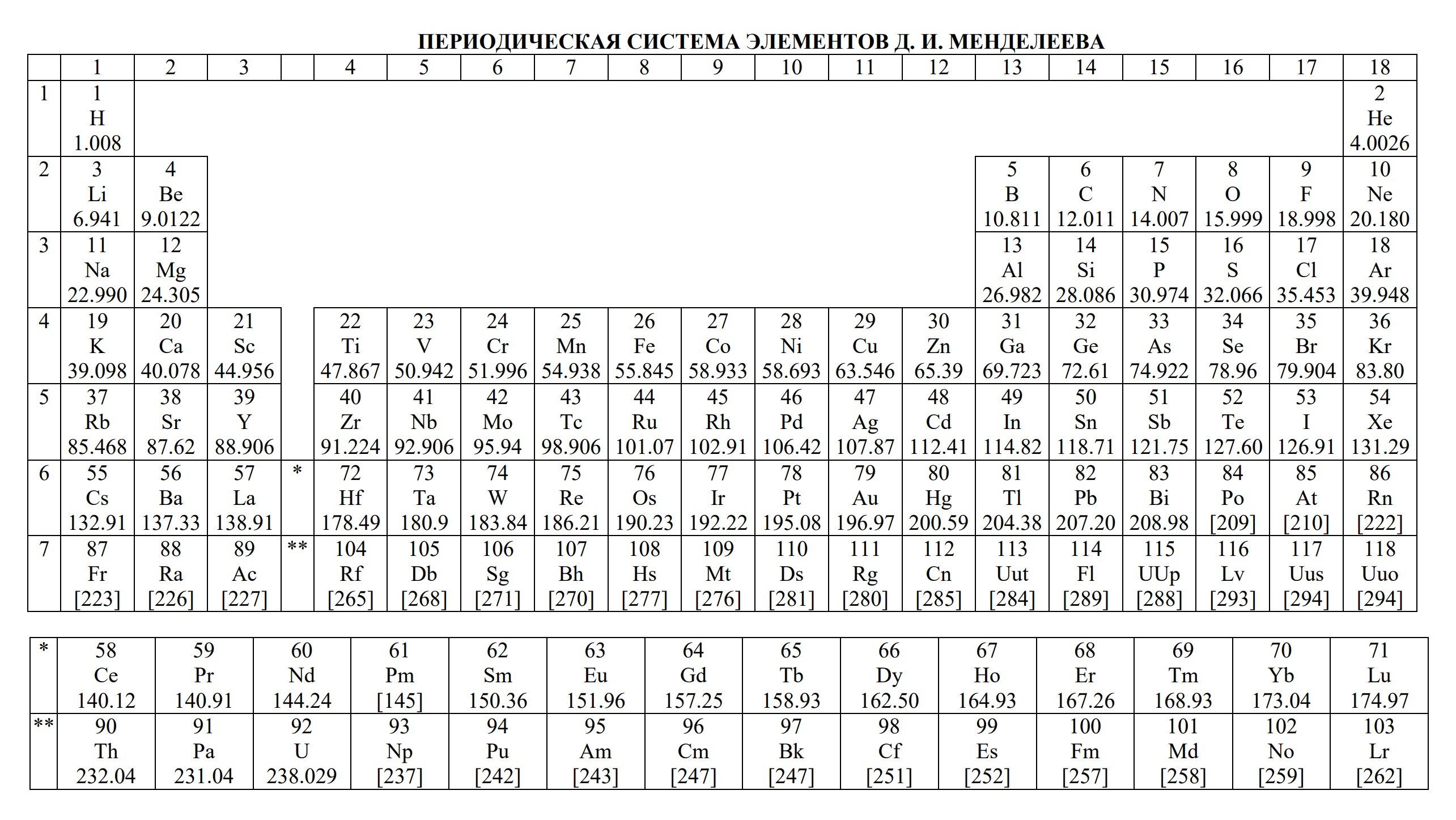
- периодическая система химических элементов Д.И. Менделеева
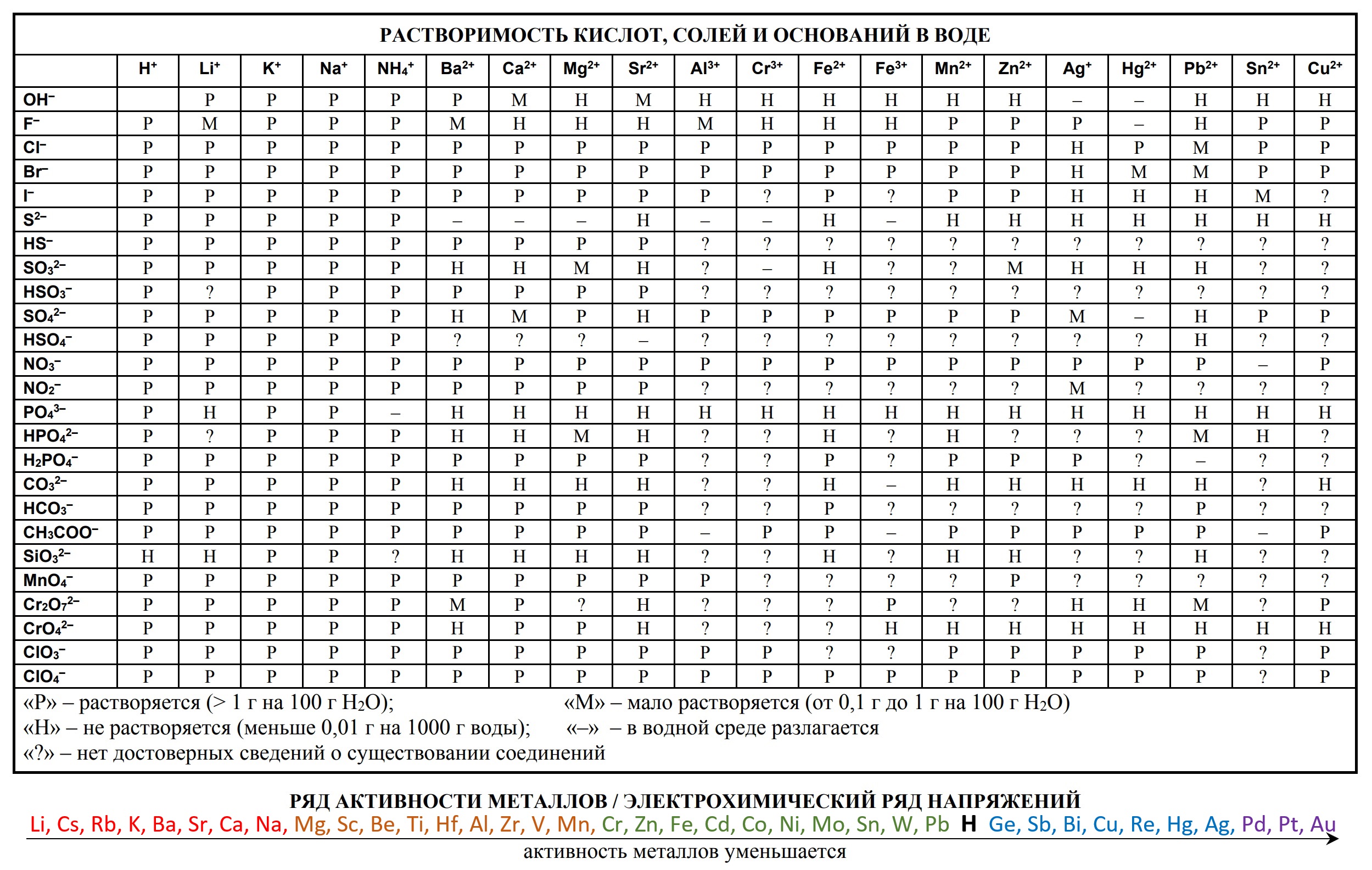
- таблица растворимости
- ряд активности металлов.
Они содержат в себе 80% информации, необходимой для решения большинства заданий.
Однако таблицы на форзацах разных учебников, продаваемые в книжных магазинах, располагающиеся на просторах интернета отличаются не только оформлением, но и содержанием. Что бы они оказались надёжно шпаргалкой, а не приятной неожиданностью, лучше с самого начала начинать работать с тем форматом, который официально разрешен на ЕГЭ твоего года.
Скачать эти таблицы можно ниже. А как сделать эти безликие таблицы наиболее информационными для тебя я расскажу на уроке.
- Таблица Д.И. Менделеева для ОГЭ и ЕГЭ
- Таблица растворимости и ряд активности для ОГЭ и ЕГЭ
- Таблица растворимости с расширенным рядом активности
- Таблица Д.И. Менделеева длиннопериодная для олимпиады
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности
Таблицы ЕГЭ по химии
Ниже приведены таблицы, идентичные используемым на ЕГЭ по химии: «Периодическая система химических элементов Д.И.Менделеева»
«Растворимость солей, кислот и оснований в воде» и «Электрохимический ряд напряжений металлов»:
Опорный конспект по теме:
Периодическая система химических элементов Д. И. Менделеева
Основные понятия:
1. Порядковый номер химического элемента — номер, данный элементу при его нумерации. Показывает общее число электронов в атоме и число протонов в ядре, определяет заряд ядра атома данного химического элемента.
2. Период – химические элементы, расположенные в строчку (периодов всего 7). Период определяет количество энергетических уровней в атоме.
Малые периоды (1 – 3) включают только s- и p- элементы (элементы главных подгрупп) и состоят из одной строчки; большие (4 – 7) включают не только s- и p- элементы (элементы главных подгрупп), но и d- и f- элементы (элементы побочных подгрупп) и состоят из двух строчек.
3. Группы – химические элементы, расположенные в столбик (групп всего 8). Группа определяет количество электронов внешнего уровня для элементов главных подгрупп, а так же число валентных электронов в атоме химического элемента.
Главная подгруппа (А) – включает элементы больших и малых периодов (только s- и p- элементы).
Побочная подгруппа (В) – включает элементы только больших периодов (только d- или f- элементы).
4. Относительная атомная масса (Ar) – показывает, во сколько раз данный атом тяжелее 1/12 части атома 12С, это безразмерная величина (для расчётов берут округлённое значение).
5. Изотопы – разновидность атомов одного и того же химического элемента, отличающиеся друг от друга только своей массой, с одинаковым порядковым номером.
Основные положения
1. В периоде слева направо:
1) Относительная атомная масса – увеличивается
2) Заряд ядра – увеличивается
3) Количество энергоуровней – постоянно
4) Количество электронов на внешнем уровне — увеличивается
5) Радиус атомов – уменьшается
6) Электроотрицательность – увеличивается
Следовательно, внешние электроны удерживаются сильнее, и металлические (восстановительные) свойства ослабевают, а неметаллические (окислительные) усиливаются.
2. В группе, в главной подгруппе сверху вниз:
1) Относительная атомная масса – увеличивается
2) Число электронов на внешнем уровне – постоянно
3) Заряд ядра – увеличивается
4) Количество энергоуровней – увеличивается
5) Радиус атомов — увеличивается
6) Электроотрицательность – уменьшается.
Следовательно, внешние электроны удерживаются слабее, и металлические (восстановительные) свойства элементов усиливаются, неметаллические (окислительные) — ослабевают.
3. Изменение свойств летучих водородных соединений:
1) в группах главных подгруппах с ростом заряда ядра прочность летучих водородных соединений уменьшается, а кислотные свойства их водных растворов усиливаются (основные свойства уменьшаются);
2) в периодах слева направо кислотные свойства летучих водородных соединений в водных растворах усиливаются (основные уменьшаются), а прочность уменьшается;
3) в группах с ростом заряда ядра в главных подгруппах валентность элемента в летучих водородных соединениях не изменяется, в периодах слева направо уменьшается от IV до I.
4. Изменение свойств высших оксидов и соответствующих им гидроксидов (кислородсодержащие кислоты неметаллов и основания металлов):
1) в периодах слева направо свойства высших оксидов и соответствующих им гидроксидов изменяются от основных через амфотерные к кислотным;
2) кислотные свойства высших оксидов и соответствующих им гидроксидов с ростом заряда ядра в периоде усиливаются, основные уменьшаются, прочность уменьшается;
3) в группах главных подгруппах у высших оксидов и соответствующих им гидроксидов с ростом заряда ядра прочность растёт, кислотные свойства уменьшаются, основные усиливаются;
4) в группах с ростом заряда ядра в главных подгруппах валентность элемента в высших оксидах не изменяется, в периодах слева направо увеличивается от I до VIII.
5. Завершенность внешнего уровня – если на внешнем уровне атома 8 электронов (для водорода и гелия 2 электрона)
6. Металлические свойства – способность атома отдавать электроны до завершения внешнего уровня.
7. Неметаллические свойства — способность атома принимать электроны до завершения внешнего уровня.
8. Электроотрицательность – способность атома в молекуле притягивать к себе электроны
9. Семейства элементов:
Щелочные металлы (1 группа «А») – Li, Na, K, Rb, Cs, Fr
Галогены (7 группа «А») – F, Cl, Br, I
Инертные газы (8 группа «А») – He, Ne, Ar, Xe, Rn
Халькогены (6 группа «А») – O, S, Se, Te, Po
Щелочноземельные металлы (2 группа «А») – Ca, Sr, Ba, Ra
10. Радиус атома – расстояние от ядра атома до внешнего уровня
Таблицы для ЕГЭ по химии
- 31.10.2020
Приводим таблицы, которые можно использовать на ЕГЭ по химии, эти таблицы можно использовать на ЕГЭ в любом году, входит в пакет разрешённых документов, т.е. то, чем можно пользоваться на ЕГЭ по химии.
Из года в год эти таблицы не меняются. В 2023 году поменялась только таблица растворимости — информацию обновили. Используйте ссылки ниже.
В состав документа входят:
- Таблица растворимости солей
- Таблица Менделеева
Добавить комментарий
Комментарии без регистрации. Несодержательные сообщения удаляются.