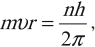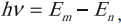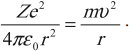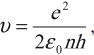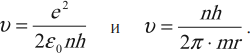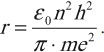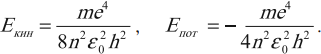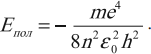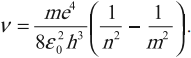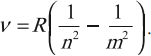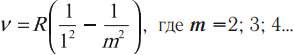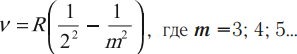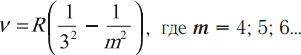Задания Д32 C3 № 3045
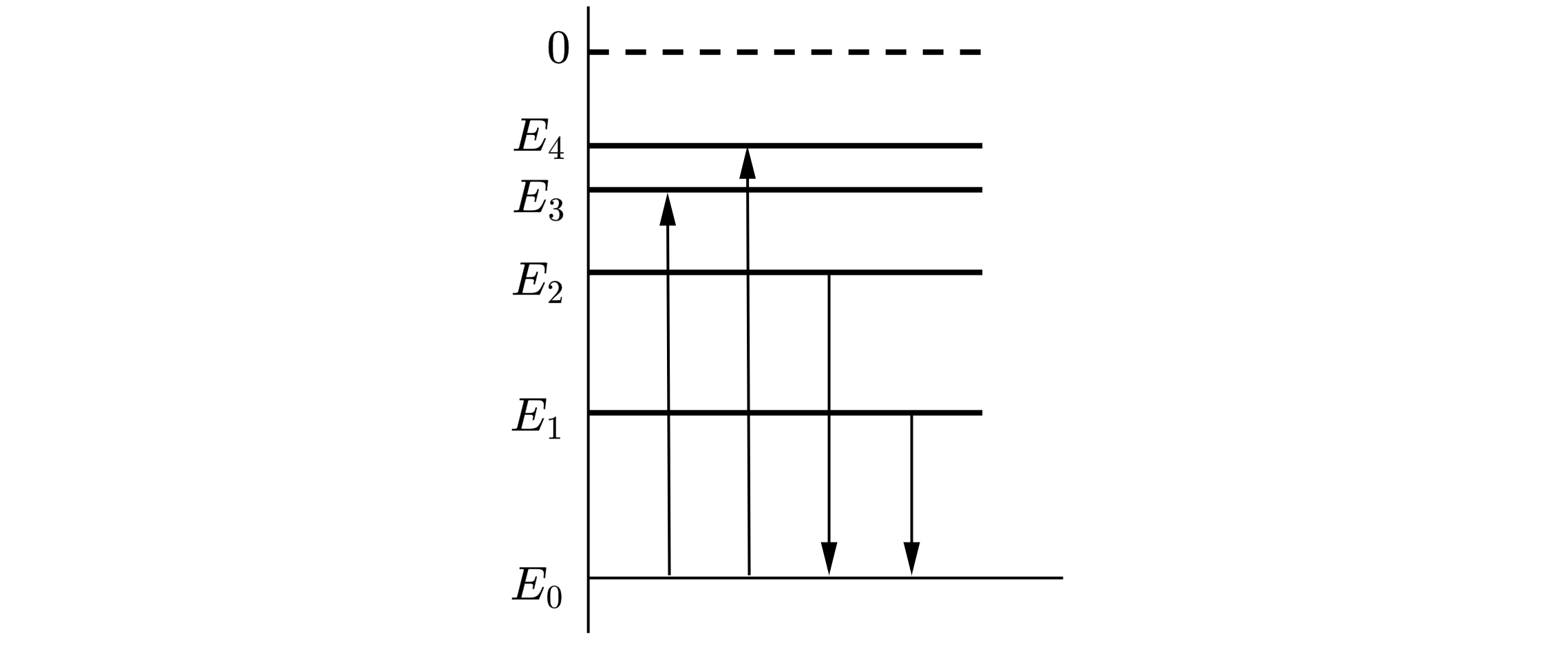
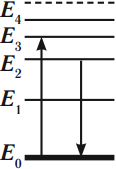
Предположим, что схема нижних энергетических уровней атомов некоего элемента имеет вид, показанный на рисунке, и атомы находятся в состоянии с энергией
Электрон, столкнувшись с одним из таких покоящихся атомов, в результате столкновения получил некоторую дополнительную энергию. Импульс электрона после столкновения с атомом оказался равным
Определите кинетическую энергию электрона до столкновения. Возможностью испускания света атомом при столкновении с электроном пренебречь. Эффектом отдачи пренебречь. Ответ дайте в джоулях, округлив до десятых число, умноженное на
Тема 19.
Основы СТО. Квантовая физика (изменение физических величин в процессах, установление соответствия)
19
.
04
Энергетические уровни
Вспоминай формулы по каждой теме
Решай новые задачи каждый день
Вдумчиво разбирай решения
ШКОЛКОВО.
Готовиться с нами — ЛЕГКО!
Подтемы раздела
основы сто. квантовая физика (изменение физических величин в процессах, установление соответствия)
19.01Фотоэффект
19.02Модель атома и атомного ядра.
19.03Радиоактивный распад
19.04Энергетические уровни
19.05Фотоны
19.06СТО
Решаем задачи
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены
некоторые возможные переходы атома между этими уровнями.
Стрелками отмечены некоторые возможные переходы атома между этими уровнями. Установите соответствие между процессами
поглощения света наименьшей длины волны и излучения света наименьшей частоты и энергией соответствующего
фотона.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные
цифры под соответствующими буквами.
Установите соответствие между физическими величинами и формулами, при помощи которых можно их рассчитать.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные
цифры под соответствующими буквами.
Показать ответ и решение
Энергия электрона определяется формулой 3, а энергия, которую нужно сообщить электрону в атоме
водорода для того, чтобы он перешел с n-го энергетического уровня на m-й энергетический уровень –
формулой 1.
При переходе электрона в атоме с (n + 1)-го энергетического уровня на n-й энергетический уровень испускается фотон. Как
изменятся следующие физические величины при уменьшении n на единицу: энергия испускаемого фотона, длина волны
испускаемого фотона.
Для каждой величины определите соответствующий характер изменения:
1) увеличилась;
2) уменьшилась;
3) не изменилась.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Показать ответ и решение
Энергия испускаемого фотона – это разница энергий между высшим и низшим уровнем
Расстояние между соседними уровнями увеличивается с уменьшением n. И, значит, с уменьшением n энергия испускаемого
фотона будет увеличиваться.
Энергия фотона обратно пропорциональна длине волны. Отсюда следует вывод, что увеличение энергии фотона (с уменьшением
n) приведет к уменьшению длины волны.
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены
некоторые возможные переходы атома между этими уровнями. Какие из этих переходов связаны с поглощением кванта света
наибольшей длины волны и излучением кванта света с наименьшей энергией? Установите соответствие между процессами
поглощения и испускания света и стрелками, обозначающими энергетические переходы атома. К каждой позиции первого столбца
подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
Демоверсия 2021
Показать ответ и решение
По второму постулату Бора энергия перехода равна:
где – энергия на начальном уровне,
– энергия на конечном уровне.
Энергия перехода можно также найти по формуле:
где – частота,
– длина волны.
А) Поглощение – переход с более низкого уровня на более высокие, при этом так как длина волны максимальна,
то
энергия поглощенного фотона минимальна, значит, уровни находятся ближе друг к другу.
Б) Излучение с наименьшей энергией от более высокого, к более низкому, при этом расстояние между уровнями
минимально
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены
некоторые возможные переходы атома между этими уровнями. Какой из этих четырёх переходов связан с поглощением света
наименьшей частоты, а какой – с излучением света наибольшей частоты?
Установите соответствие между процессами поглощения и испускания света и стрелками, указывающими энергетические
переходы атома. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу
выбранные цифры под соответствующими буквами
Демоверсия 2019
Показать ответ и решение
По второму постулату Бора энергия перехода равна:
где – энергия на начальном уровне,
– энергия на конечном уровне.
Энергия перехода можно также найти по формуле:
где – частота,
– длина волны.
А) Поглощение – переход с более низкого уровня на более высокие, при этом так как частота минимальна, то
энергия поглощенного фотона минимальна, значит, уровни находятся ближе друг к другу (3).
Б) Излучение с наименьшей энергией от более высокого, к более низкому, при этом так как частота максимальна,
то
энергия излученного фотона максимальна, значит, уровни находятся дальше друг от друга (2)
Атом Бора.
Автор — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев.
Темы кодификатора ЕГЭ: постулаты Бора.
Планетарная модель атома, успешно истолковав результаты опытов по рассеянию -частиц, в свою очередь столкнулась с очень серьёзными трудностями.
Как мы знаем, любой заряд, движущийся с ускорением, излучает электромагнитные волны. Это — неоспоримый факт классической электродинамики Максвелла, подтверждаемый многочисленными наблюдениями.
Нам также хорошо известно, что электромагнитные волны несут энергию. Стало быть, ускоренно движущийся заряд, излучая, теряет энергию, которая этим излучением уносится.
А теперь давайте возьмём произвольный электрон в планетарной модели. Он двигается вокруг ядра по замкнутой орбите, так что направление его скорости постоянно меняется. Следовательно, электрон всё время имеет некоторое ускорение (например, при равномерном движении по окружности это будет центростремительное ускорение), и поэтому должен непрерывно излучать электромагнитные волны. Расходуя свою энергию на излучение, электрон будет постепенно приближаться к ядру; в конце концов, исчерпав запас своей энергии полностью, электрон упадёт на ядро.
Если исходить из того, что механика Ньютона и электродинамика Максвелла работают внутри атома, и провести соответствующие вычисления, то получается весьма озадачивающий результат: расход энергии электрона на излучение (с последующим падением электрона на ядро) потребует совсем малого времени — порядка секунды. За это время атом должен полностью «коллапсировать» и прекратить своё существование.
Таким образом, классическая физика предрекает неустойчивость атомов, устроенных согласно планетарной модели. Этот вывод находится в глубоком противоречии с опытом: ведь на самом деле ничего такого не наблюдается. Предметы нашего мира вполне устойчивы и не коллапсируют на глазах! Атом может сколь угодно долго пребывать в невозбуждённом состоянии, не излучая при этом электромагнитные волны.
Постулаты Бора.
Оставалось признать, что внутри атомов перестают действовать известные законы классической физики. Микромир подчиняется совсем другим законам.
Первый прорыв в познании законов микромира принадлежит великому датскому физику Нильсу Бору. Он предложил три постулата, резко расходящиеся с механикой и электродинамикой, но тем не менее позволяющих правильно описать простейший из атомов — атом водорода.
Классическая физика хорошо описывает непрерывные процессы — движение материальной точки, изменение состояния идеального газа, распространение электромагнитных волн… Энергия объекта, подчиняющегося механике или электродинамике, в принципе может принимать любые значения. Однако линейчатые спектры указывают на дискретность процессов, происходящих внутри атомов. Эта дискретность должна фигурировать в законах новой теории.
Первый постулат Бора. Всякий атом (и вообще, всякая атомная система) может находиться не во всех состояниях с любым, наперёд заданным значением энергии. Возможен лишь дискретный набор избранных состояний, называемых стационарными, в которых энергия атома принимает значения Находясь в стационарном состоянии, атом не излучает электромагнитные волны.
Как видим, первый постулат Бора вопиющим образом противоречит классической физике: налагается запрет на любые значения энергии, кроме избранного прерывистого набора, и признаётся, что электроны, вроде бы движущиеся ускоренно, на самом деле не излучают.
Выглядит фантастически, не правда ли? Однако в том же 1913 году, когда Бор предложил свои постулаты, существование стационарных состояний было подтверждено экспериментально — в специально поставленном опыте немецких физиков Франка и Герца. Таким образом, стационарные состояния — это не выдумка, а объективная реальность.
Значения разрешённого набора называются уровнями энергии атома. Что происходит при переходе с одного уровня энергии на другой?
Второй постулат Бора. Если атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией
, то разность этих энергий может высвободиться в виде излучения. В таком случае излучается фотон с энергией
. (1)
Эта же формула работает и при поглощении света: в результате столкновения с фотоном атом переходит из состояния в состояние с большей энергией
, а фотон при этом исчезает.
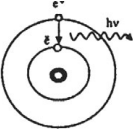
Для примера на рис. 1 показано излучение фотона при переходе атома с энергетического уровня на уровень
. Переход заключается в том, что электрон «соскакивает» с одной орбиты на другую, расположенную ближе к ядру.
Рис. 1. Излучение фотона атомом
Формула (1) даёт качественное представление о том, почему атомные спектры испускания и поглощения являются линейчатыми.
В самом деле, атом может излучать волны лишь тех частот, которые соответствуют разностям значений энергии разрешённого дискретного набора ; соответственно, набор этих частот также получается дискретным. Вот почему спектр излучения атомов состоит из отдельно расположенных резких ярких линий.
Вместе с тем, атом может поглотить не любой фотон, а только тот, энергия которого в точности равна разности
каких-то двух разрешённых значений энергии
и
. Переходя в состояние с более высокой энергией
, атомы поглощают ровно те самые фотоны, которые способны излучить при обратном переходе в исходное состояние
. Попросту говоря, атомы забирают из непрерывного спектра те линии, которые сами же и излучают; вот почему тёмные линии спектра поглощения холодного атомарного газа находятся как раз в тех местах, где расположены яркие линии спектра испускания этого же газа в нагретом состоянии.
Качественного объяснения характера атомных спектров, однако, недостаточно. Хотелось бы иметь теорию, позволяющую вычислить частоты наблюдаемых спектров. Бору удалось это сделать в самом простом случае — для атома водорода.
Атом водорода.
Атом водорода состоит из ядра с зарядом , которое называется протоном, и одного электрона с зарядом
(через
обозначена абсолютная величина заряда электрона). При построении своей теории атома водорода Бор сделал три дополнительных предположения.
1. Прежде всего, мы ограничиваемся рассмотрением только круговых орбит электрона. Таким образом, электрон движется вокруг протона по окружности радиуса с постоянной по модулю скоростью
(рис. 2).
Рис. 2. Модель атома водорода
2. Величина , равная произведению импульса электрона
на радиус орбиты
, называется моментом импульса электрона. В каких единицах измеряется момент импульса?
Смотрим:
=кг*м/с*м=(кг*м/
)*м*с=Н*м*с=Дж*с.
Это в точности размерность постоянной Планка! Именно здесь Бор увидел появление дискретности, необходимой для квантового описания атома водорода.
Правило квантования (третий постулат Бора). Момент импульса электрона может принимать лишь дискретный набор значений, кратных «перечёркнутой» постоянной Планка:
, (2)
3. Выше мы говорили, что классическая физика перестаёт работать внутри атома. Так оно в действительности и есть, но вопреки этому мы предполагаем, что электрон притягивается к протону с силой, вычисляемой по закону Кулона, а движение электрона подчиняется второму закону Ньютона:
. (3)
Эти три предположения позволяют довольно просто получить формулы для уровней энергии атома водорода. Переписываем соотношение (3) в виде:
. (4)
Из правила квантования (2) выражаем :
,
и подставляем это в (4):
.
Отсюда получаем формулу для допустимых радиусов орбит электрона:
. (5)
Теперь перейдём к нахождению энергии электрона. Потенциальная энергия кулоновского взаимодействия электрона с ядром равна:
(Она отрицательна, так как отсчитывается от бесконечно удалённой точки, в которой достигает максимального значения.)
Полная энергия электрона равна сумме его кинетической и потенциальной энергий:
.
Вместо подставим правую часть выражения (4):
. (6)
Полная энергия, как видим, отрицательна. Если на радиус орбиты никаких ограничений не накладывается, как это имеет место в классической физике, то энергия может принимать любые по модулю значения. Но согласно (5) существует лишь дискретный набор возможных значений радиуса; подставляя их в (6), получаем соответствующий набор допустимых значений энергии атома водорода:
. (7)
Основное состояние атома водорода — это состояние с наименьшей энергией . В основном состоянии атом может находиться неограниченно долго. Вычисление даёт:
Дж
эВ:
Мы видим, что если атом находится в основном состоянии, то для выбивания электрона нужно сообщить атому энергию, равную как минимум 13,6 эВ. Эта величина носит название энергии ионизации атома водорода.
По формуле (5) легко вычислить радиус орбиты основного состояния:
см.
То есть, диаметр атома оказывается равным как раз см — величине, известной из опыта. Таким образом, теория Бора впервые смогла объяснить размер атома!
Кроме того, в рамках теории Бора удаётся получить формулы для вычисления частот (или длин волн) спектра атома водорода. Так, согласно второму постулату Бора и формуле (7) имеем:
. (8)
На практике чаще имеют дело с длинами волн. Учитывая, что , формулу (8) можно переписать так:
. (9)
Константа м
называется постоянной Ридберга. Теория Бора даёт значение этой постоянной, очень хорошо согласующееся с экспериментом.
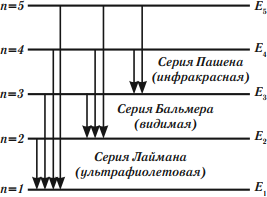
Длины волн спектра атома водорода образуют серии, характеризующиеся фиксированным значением в формуле (9). Все длины волн данной серии излучаются при переходах на уровень
с вышележащих энергетических уровней
.
Переходы в основное состояние:
образуют серию Лаймана. Длины волн этой серии описываются формулой (9) при :
.
Линии серии Лаймана лежат в ультрафиолетовом диапазоне.
Переходы на второй уровень:
образуют серию Бальмера. Длины волн этой серии подчиняются формуле (9) при :
.
Первые четыре линии серии Бальмера лежат в видимом диапазоне (рис. 3), остальные — в ультрафиолетовом.
Рис. 3. Видимый спектр атома водорода (серия Бальмера)
Переходы на третий уровень:
образуют серию Пашена. Длины волн этой серии описываются формулой (9) при :
.
Все линии серии Пашена лежат в инфракрасном диапазоне.
Имеются ещё три «именованных» серии: это серия Брэккета (переходы на уровень), серия Пфунда (переходы на уровень
) и серия Хэмпфри (переходы на уровень
). Все линии этих серий лежат в далёкой инфракрасной области.
Достоинства и недостатки теории Бора.
О достоинствах модели атома водорода, предложенной Бором, мы так или иначе уже сказали. Резюмируем их.
— Теория Бора продемонстрировала, что для описания атомных объектов принципиально недостаточно представлений классической физики. В микромире работают другие, совершенно новые законы.
Для микромира характерно квантование — дискретность изменения величин, описывающих состояние объекта. В качестве меры квантования, как показала теория Бора, может выступать постоянная Планка , которая является универсальной константой и играет фундаментальную роль во всей физике микромира (а не только в явлениях излучения и поглощения света).
— Теория Бора впервые и совершенно точно указала на факт наличия стационарных энергетических состояний атома, образующих дискретный набор. Этот факт оказался общим свойством объектов микромира.
— В рамках модели Бора удалось получить формулы для вычисления частот спектра атома водорода и объяснить размер атома. Классическая физика была не в состоянии решить эти проблемы.
Однако теория Бора, разумеется, не могла претендовать на роль общей теории, описывающей микромир. Модель Бора обладала рядом существенных недостатков.
— Теория Бора непоследовательна. С одной стороны, она отвергает описание атома на основе классической физики, так как постулирует наличие стационарных состояний и правила квантования, непонятных с точки зрения механики и электродинамики. С другой стороны, классические законы — второй закон Ньютона и закон Кулона — используются для записи уравнения движения электрона по круговой орбите.
— Теория Бора не смогла дать адекватное описание самого простого после водорода атома гелия. Подавно не могло быть и речи о распространении теории Бора на более сложные атомы.
— Даже в самом атоме водорода теория Бора смогла описать не всё. Например, дав выражения для частот спектральных линий, модель Бора не объясняла различие в их интенсивностях. Кроме того, неясен оставался механизм образования молекулы водорода из двух атомов.
Несмотря на свои недостатки, теория Бора стала важнейшим этапом развития физики микромира. Полуклассическая-полуквантовая модель Бора послужила промежуточным звеном между классической физикой и последовательной квантовой механикой , построенной десятилетием позже — в 1920-х годах.
Разберем задачи ЕГЭ на темы: «Строение атома», «Модель Резерфорда-Бора», «Энергетические уровни», «Излучение фотона».
Задача 1.
На рисунке изображена схема низших энергетических уровней атома. В начальный момент времени атом находится в состоянии с энергией Е(2). Согласно постулатам Бора, с какой энергией данный атом может излучать фотоны? (Ответ дать в 10−19 Дж.)
Решение:
Согласно постулатам Бора, атом, находящийся в стационарных состояниях, не излучает энергии. Излучение энергии возможно при переходе атома с уровня с большим значением энергии на уровень с меньшим значением энергии. Поглощение энергии, наоборот, возможно при переходе атома с меньшим уровнем энергии на больший.
С учетом представленной диаграммы, излучение атома возможно при переходе с уровня Е(2) на уровень Е(1), так как Е(2)> Е(1). Поэтому, энергия излучаемых фотонов (hv) может быть определена, как разность энергий
Подставив численные значения, рассчитаем энергию излучаемых фотонов.
(Дж).
Ответ: 3.
Задача 2.
Электрон в атоме водорода находится в основном (самом низком, с номером n = 1) энергетическом состоянии. Атом поглощает фотон с импульсом 6,8 · 10–27 кг·м/с. Найдите номер энергетического уровня, на который в результате этого перейдёт электрон.
Дано:
n1=1;
p = 6,8·10–27 кг·м/с.
Найти:
n-?
Решение:
Уровни энергии в атоме водорода определяются формулой:
(эВ), где n=1, 2, 3… и т. д. (1)
Следовательно, атом на уровне n1=1 обладает энергией, которую можно рассчитать по формуле (1).
(эВ).
Найдем связь между импульсом фотона и его энергией:
(2)
Таким образом, энергия фотона может быть определена по формуле (2).
(Дж).
С учетом, что 1 эВ, получим
(эВ).
Атом, получив энергию от фотона, переходит в стационарное состояние с большим уровнем энергии.
(эВ).
Из формулы (1) необходимо вывести номер энергетического уровня.
Ответ: 4.
Задача 3.
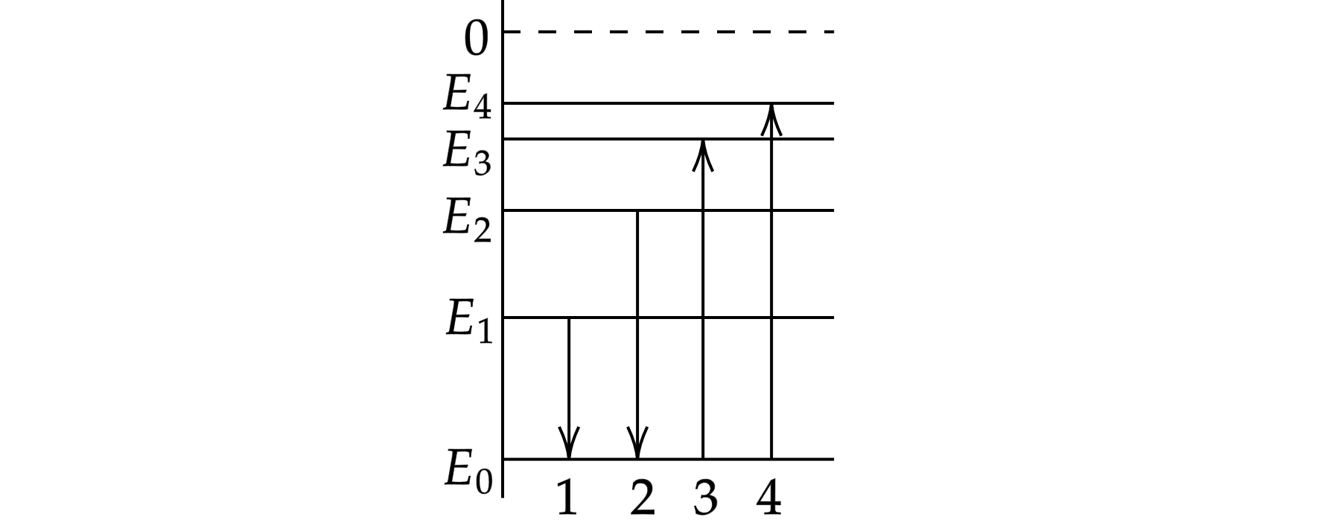
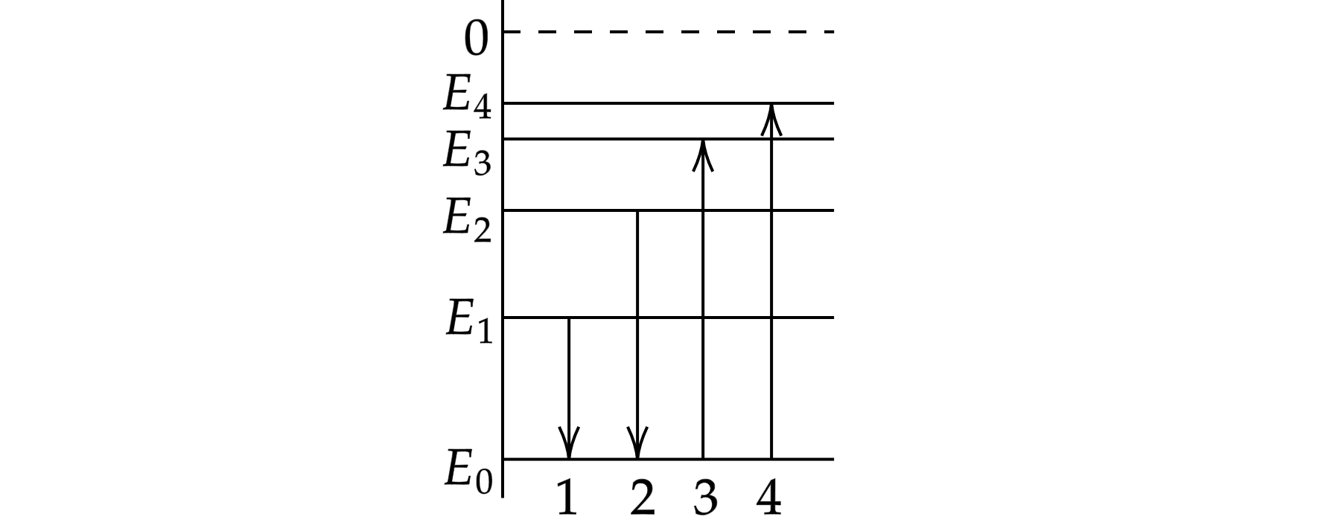
На рисунке изображена упрощенная диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Какой из этих четырех переходов связан с поглощением света наибольшей энергии, а какой — с излучением света с наибольшей длиной волны?
Установите соответствие между процессами поглощения и испускания света и стрелками, указывающими энергетические переходы атома.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕССЫ
А) поглощение света наибольшей энергии;
Б) излучение света с наибольшей длиной волны.
ЭНЕРГЕТИЧЕСКИЕ ПЕРЕХОДЫ
1) 1
2) 2
3) 3
4) 4
Ответ:
Решение:
По указанной диаграмме необходимо определить переходы, соответствующие поглощению и излучению света.
Переходы, указанные стрелками 1 и 2, соответствуют излучению энергии, так как атом переходит с большего уровня энергии на меньший.
Здесь надо учесть, что
и
Так как , то, согласно формуле Планка
, меньшая длина волны соответствует большему значению энергии излучения. Поэтому при переходе
будет излучаться большее количество энергии. Вторая стрелка будет соответствовать излучению света с наименьшей длиной волны.
Стрелки 3 и 4 соответствуют поглощению энергии, так как в этих случаях атом переходит на уровни, соответствующие большему значению энергии. Рассуждения, аналогичные первому случаю, приводят к следующему выводу:
и
Так как , то четвертая стрелка будет соответствовать поглощению света наибольшей энергии.
Ответ:
Задача 4.
Значения энергии электрона в атоме водорода задаются формулой: (эВ), где n=1, 2, 3… и т. д.
При переходах с верхних уровней энергии на нижние атом излучает фотон. Переходы с верхних уровней на уровень c n = 1 образуют серию Лаймана, на уровень c n = 2 – серию Бальмера и т. д. Найдите отношение γ максимальной длины волны фотона в серии Бальмера к максимальной длине волны фотона в серии Лаймана.
Решение:
Согласно формуле Планка , максимальная длина волны соответствует излучению света с наименьшим значением энергии. Поэтому для серии Лаймана это переход с уровня 2 на уровень 1 (см. рис. 1). Рассчитаем значение энергии, которая излучается в этом случае.
(эВ).
(эВ).
Длина волны, соответствующая этому переходу, может быть определена из формулы:
(1)
Аналогично для серии Бальмера, излучение с наибольшей длиной волны (наименьшей энергии излучения), соответствует переходу с уровня 3 на уровень 2 (см. рис. 2).
(эВ).
(эВ).
Длина волны, соответствующая этому переходу, может быть определена из формулы:
(2)
Тогда, для нахождения соотношения для длин волн
Разделим уравнение (2) на уравнение (1):
В расчетах значения энергий можно оставить в эВ, так как перевод в систему «СИ» ответа не изменит.
С учетом системы «СИ»:
(1 эВ Дж).
Ответ: 5,4.
Благодарим за то, что пользуйтесь нашими статьями.
Информация на странице «Атом Бора.» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в ВУЗ или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
08.03.2023
Современные представления о строении атома
Элемент ЕГЭ: 1.1 Современные представления о строении атома. 1.1.1 Строение электронных оболочек атомов элементов первых четырех периодов: s-, р- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояние атомов.
Современные представления о строении атома
Атом – химически неделимая электронейтральная частица, которая состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов.
Атомы не имеют заряда (нейтральны). Если атом присоединяет один или несколько электронов, он приобретает отрицательный заряд и превращается в анион. Если атом теряет один или несколько электронов, он приобретает положительный заряд и превращается в катион. Заряд иона указывают арабской цифрой и знаком после символа атома.
Состав ядра: А = Z + N, где А — массовое число; Z — протонное число (число протонов); N — число нейтронов.
Элементарные частицы
| Название | Обозначение | Масса | Заряд |
| Электрон |
ē |
≈ 0 | -1 |
| Протон |
р |
1 | +1 |
| Нейтрон |
n |
1 | 0 |
Порядковый номер элемента в периодической системе:
- Заряд ядра атома
- Число протонов в ядре атома
- Число электронов в атоме
Нуклиды – разновидности атомов с фиксированным массовым числом А, числом протонов Z и нейтронов N в ядре.
Основные положения квантовой теории строения атома:
- Дискретность энергии электрона
- Двойственная (корпускулярно-волновая) природа электрона
- Невозможность определения траектории электрона (принцип неопределенности)
Относительная атомная масса элемента (Ar)
Физическая величина, показывающая, во сколько раз средняя масса атомов данного элемента больше 1/12 части массы изотопа углерода 12С.
Атомные орбитали
Орбиталь — пространство вокруг ядра, в котором нахождение электрона наиболее вероятно (вероятность более 90%)
Порядок заполнения орбиталей в основном состоянии
1) Принцип наименьшей энергии. Электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.
2) Принцип Паули. На каждой орбитали могут находиться не более двух электронов, причём спины их противоположны.
3) Правило Хунда. Орбитали заполняются электронами так, чтобы их суммарный спин был максимальным.
Спин электрона — свойство электрона, характеризующее его способность взаимодействовать с магнитным полем. Может принимать два значения (положительное и отрицательное).
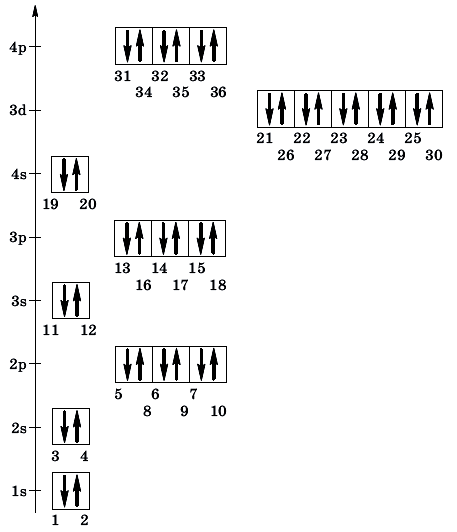
Последовательность заполнения орбиталей электронами в основном состоянии:
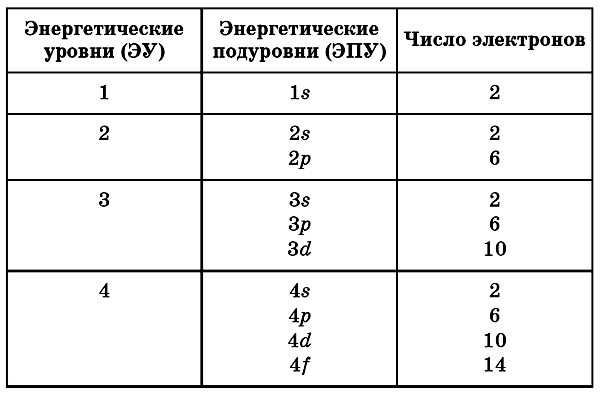
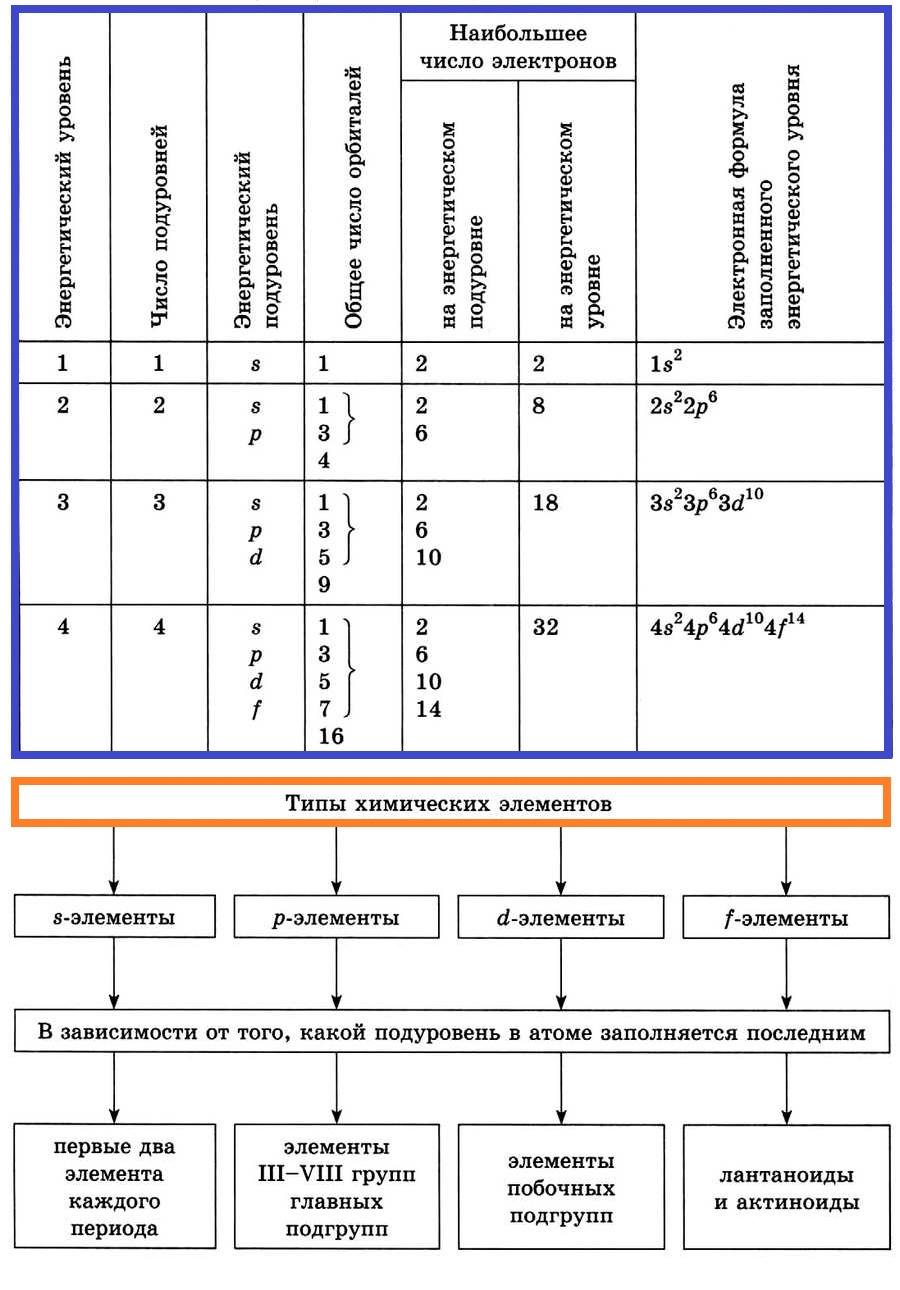
Энергетические уровни и подуровни
Элементы, у которых идет заполнение s-подуровня, называют s-элементами.
Элементы, у которых заполняется р-подуровень, называют р-элементами.
Элементы, у которых заполняется d-подуровень, называют d-элементами.
Элементы, у которых заполняется f-подуровень, называют f-элементами.
Распределение электронов в атоме по энергетическим уровням (электронным слоям) и подуровням
Электроны, относящиеся к последнему энергетическому уровню, называют внешними (валентными) электронами.
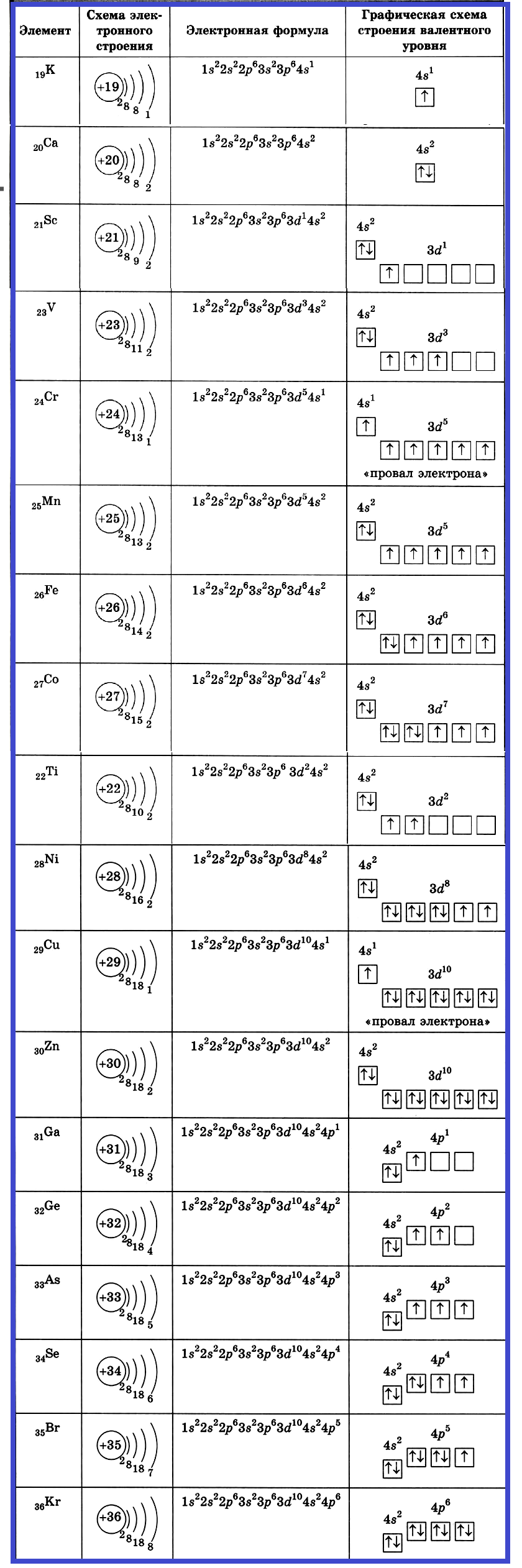
Строение электронных оболочек атомов первых четырёх периодов
Распределение электронов по орбиталям атома называют электронной конфигурацией атома, или электронной формулой.
Строение элементов первого периода
Строение элементов второго периода
Строение элементов третьего периода
Строение элементов четвёртого периода
Электронные конфигурации d5 и d10 обладают повышенной устойчивостью, поэтому в атомах хрома и меди наблюдается «перескок» электрона с 4s-подуровня на 3d-подуровень («провал электрона»).
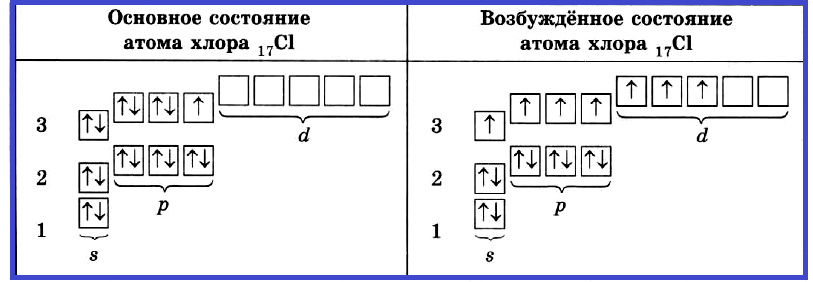
Основное и возбуждённое состояние атомов
Наиболее устойчивое состояние атома, в котором энергия его электронной оболочки минимальна, называется основным состоянием атома. Любые другие состояния атома называют возбужденными состояниями.
Для возможности перехода атома в возбуждённое состояние необходимо выполнение одновременно двух условий:
- наличие спаренных электронов;
- наличие вакантных орбиталей.
Таблица «Современные представления о строении атома. Кратко»
(с) В учебных целях использованы цитаты из пособий: «Химия / Н. Э. Варавва, О. В. Мешкова. — Москва, Эксмо (ЕГЭ. Экспресс-подготовка)» и «Химия : Новый полный справочник для подготовки к ЕГЭ / Е.В. Савинкина. — Москва, Издательство АСТ».
Вы смотрели Справочник по химии «Современные представления о строении атома». Выберите дальнейшее действие:
- Перейти к Списку конспектов по химии (по классам)
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии
- Конспект урока в 11 классе «Основные сведения о строении атома»
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
Атомные спектры. Энергетические уровни
Электрон в атоме водорода перешёл с энергетического уровня с номером m в основное энергетическое состояние с номером (n = 1). При этом был испущен фотон с импульсом (6,45cdot10^{-27}) кг(cdot)м/с. Чему равен номер (m)?
Найдем энергию испущенного фотона: [E=pc=6,45cdot 10^{-27}text{ кг·м/с}cdot 3cdot 10^{8}text{кг·м/с}=19,5cdot 10^{-19}approx 12,09text{ эВ}]
Энергетические уровни водорода находятся по формуле: [E_n=-dfrac{13,6text{ эВ}}{n^2}]
Второй постулат Бора: [E=E_M-E_n]
Подставим значения: [12,09text{ эВ}=-13,6cdot text{ эВ}left(dfrac{1}{m^2}-dfrac{1}{n^2}right)] [12,09=-13,6cdotleft(dfrac{1}{m^2}-dfrac{1}{4}right)] [12,09=-13,6cdotleft(dfrac{1}{m^2}-dfrac{1}{4}right)]
Таким образом, (m=3).
Ответ: 3
Электрон в атоме водорода переходит с энергетического уровня с номером (n = 2) на энергетический уровень с (n = 1). Чему равен модуль импульса испущенного при этом фотона? Ответ выразите в кг(cdot)м/с, умножив на (10^{-27}).
Энергетические уровни водорода находятся по формуле: [E_n=-dfrac{13,6text{ эВ}}{n^2}]
Второй постулат Бора: [E=E_2-E_1]
Получим: [E=-13,6cdotleft(1-dfrac{1}{4}right)=10,2text{ эВ}]
Импульс энергии фотона: [p=dfrac{E}{c}=dfrac{10,2cdot1,6cdot10^{-19}}{3cdot10^{8}}=5,44cdot10^{27} text{ кг $cdot$ м/с}]
Ответ: 5,44
Атомные ядра с одинаковым массовым числом, но разным количеством протонов и нейтронов, принято называть изобарами. Примером изобар могут служить ядро аргона (_{18}^{40}Ar) и ядро одного из изотопов калия (_{19}K). Сколько нейтронов содержится в указанном ядре калия? ?
Количество нейтронов равно разности атомной массы и зарядового числа, тогда в указанном ядре калия: [40-19=21]
Ответ: 21
Атомные ядра с одинаковым массовым числом, но разным количеством протонов и нейтронов, принято называть изобарами. Примером изобар могут служить ядро кадмия (_{48}^{122}Cd) и ядро одного из изотопов олова (_{50}Sn). Сколько нейтронов содержится в указанном ядре олова? ?
Количество нейтронов равно разности атомной массы и зарядового числа, тогда в указанном ядре олова: [122-50=72]
Ответ: 72
Электрон в атоме водорода находится в основном (самом низком, с номером n = 1) энергетическом состоянии. Атом поглощает фотон с импульсом 6,8(cdot)10(^{-27}) кг(cdot)м/с. Найдите номер энергетического уровня, на который в результате этого перейдёт электрон.
Энергия фотона: [E_text{фот}=hnu=pc=12,75text{ эВ}] Второй постулат Бора: [hnu=E_m-E_n Rightarrow pc = dfrac{-13,6}{n^2}+13,6 Rightarrow n=4]
Ответ: 4
В таблице приведены значения энергии для второго и четвёртого энергетических уровней атома водорода. [begin{array}{|c|c|} hline text{Номер уровня
} & text{Энергия 10$^{-19}$ Дж}\ hline text{2} & text{-
5,45} \ hline text{4} & text{-1,36} \ hline end{array}]
Какой должна быть энергия фотона, при поглощении которого атом переходит со второго уровня на четвёртый? (Ответ дать в 10(^{-19}) Дж.)
Для того, чтобы электрон перешёл со второго уровня на четвёртый под действием фотона, энергия фотона должна быть равна разности энергий четвёртого и второго энергетических уровней: [(-1,36-(-5,45))10^{-19}text{ Дж}=4,09cdot 10^{-19}text{ Дж}]
Ответ: 4,09

Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Физика атома
Для изучения атома и атомного ядра используются специальные методы наблюдения и регистрации элементарных частиц.
Принцип действия приборов для регистрации элементарных частиц
В основе методов обнаружения и изучения характеристик частиц – ионизирующее и фотохимическое действия частиц, отклонение частиц в магнитном поле. Регистрирующий прибор — это сложная макроскопическая система, которая находится в неустойчивом состоянии. При движении частицы в ней начинается процесс перехода в устойчивое состояние. Этот процесс позволяет регистрировать частицу.
Выбор регистрирующего устройства определяется целью эксперимента и условиями его проведения.
Метод сцинтилляций (сцинтилляционные счетчики частиц). В основе метода – способность частиц вызывать вспышки на экране, покрытом слоем специального вещества. Этот метод дает возможность счета частиц и позволяет фиксировать их распределение по энергиям.
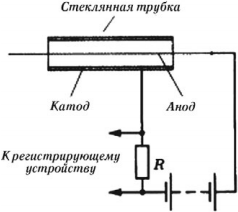
Газоразрядный счетчик Гейгера
Счетчик Гейгера применяется для регистрации электронов и ( gamma )-квантов.
Счетчик состоит из стеклянной трубки, покрытой изнутри металлическим слоем (катод), и тонкой металлической нити, идущей вдоль оси трубки (анод). Трубка заполняется инертным газом, аргоном. Действие счетчика основано на ударной ионизации. Заряженная частица, влетая в счетчик, ионизирует молекулы газа, создавая положительные ионы и электроны. Электрическое поле между анодом и катодом ускоряет электроны до энергий, при которых начинается ударная ионизация. Скорость электронов, движущихся к аноду, возрастает, и они, взаимодействуя с молекулами газа, создают лавину ионов. Ток через счетчик резко возрастает. На нагрузочном резисторе ( R ) образуется импульс напряжения, который подается в регистрирующее устройство.
Для того чтобы счетчик мог регистрировать частицу, лавинный разряд необходимо погасить. Это происходит автоматически: в момент появления импульса тока падение напряжения на нагрузочном резисторе ( R ) велико, напряжение между анодом и катодом резко уменьшается, и разряд прекращается.
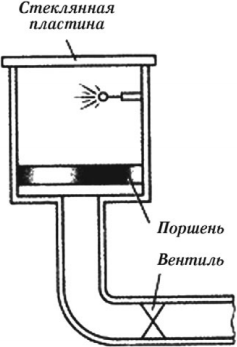
Камера Вильсона
Принцип действия камеры Вильсона основан на конденсации перенасыщенного пара на ионах с образованием капелек жидкости. Эти ионы создает вдоль своей траектории движущаяся заряженная частица. Видимый след из капелек жидкости, который оставляет заряженная частица, называется трек.
Камера Вильсона представляет собой герметически закрытый сосуд, заполненный парами воды или спирта, близкими к насыщению. При резком опускании поршня, вызванном уменьшением давления под ним, пар в камере адиабатно расширяется, охлаждается и становится перенасыщенным. Это — неустойчивое состояние пара: он легко конденсируется, если в сосуде появляются центры конденсации. Центрами конденсации становятся ионы, которые образует в рабочем пространстве камеры пролетевшая частица.
Затем камера возвращается в исходное состояние, и ионы удаляются электрическим полем. Если поместить камеру Вильсона в однородное магнитное поле, то в результате действия силы Лоренца треки частиц искривляются. Это позволяет определить удельный заряд частицы (по радиусу кривизны трека и скорости частицы). Если удельный заряд частицы известен, то по радиусу кривизны трека можно определить энергию и скорость частицы.
Пузырьковая камера
В 1952 г. американский ученый Д. Глейзер предложил использовать для обнаружения треков частиц перегретую жидкость. В такой жидкости на ионах (центрах парообразования), образующихся при движении быстрой заряженной частицы, появляются пузырьки пара, дающие видимый трек. Это устройство получило название «пузырьковая камера».
В исходном состоянии жидкость в камере находится под высоким давлением при температуре выше температуры кипения при атмосферном давлении. При резком понижении давления жидкость оказывается перегретой и будет находиться в неустойчивом состоянии. Заряженные частицы, пролетающие в это время, вызывают появление треков, состоящих из пузырьков пара. В качестве жидкости используются жидкий водород и пропан.
Преимущество пузырьковой камеры перед камерой Вильсона – большая плотность рабочего вещества. Пробеги частиц вследствие этого оказываются достаточно короткими. Это позволяет регистрировать частицы с большой энергией и наблюдать серию последовательных превращений частицы и вызываемые ею реакции.
Метод толстослойных фотоэмульсий основан на фотохимическом действии быстрых заряженных частиц, проходящих через фотоэмульсию. Толщина слоя фотоэмульсии составляет от 0,5 до 1 мм. Быстрая заряженная частица ионизирует атомы фотоэмульсии и оставляет скрытое изображение. После обработки это изображение становится видимым и может изучаться.
Содержание
- Планетарная модель атома
- Постулаты Бора
- Линейчатые спектры
- Лазер
- Основные формулы по теме «Физика атома»
Планетарная модель атома
Английский ученый Томсон в 1903 году предложил первую модель атома.
Положительный заряд атома занимает весь объем атома и распределен в этом атоме с постоянной плотностью, а внутри него находятся электроны.
Модель атома Томсона сравнивают с «булочкой с изюмом», в которой роль изюминок играют электроны.
Атом водорода, согласно этой модели, представляет собой положительно заряженный шар радиусом 10-8 м, внутри которого находится электрон. У более сложных атомов внутри положительно заряженного шара находятся несколько электронов.
Модель атома Томсона не получила экспериментального подтверждения.
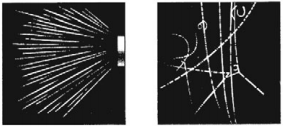
Опыт Резерфорда по рассеянию ( alpha )-частиц
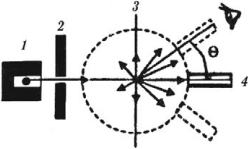
В начале ХХ века английский ученый Э. Резерфорд исследовал прохождение узкого пучка ( alpha )-частиц через золотую фольгу толщиной около 4 · 10-7 м.
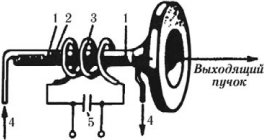
Для изучения строения атома Резерфорд предложил зондирование атома с помощью ( alpha )-частиц, которые испускались радиоактивным элементом 1, помещенным внутри свинцового цилиндра, поглощающего все ( alpha )-частицы, кроме тех, которые проходили через узкий канал 2. Узкий пучок ( alpha )-частиц попадал на фольгу из золота 3. Рассеянные после взаимодействия с золотом ( alpha )-частицы регистрировались визуально с помощью светочувствительного экрана и микроскопа 4.
В результате опыта было обнаружено, что, хотя большая часть ( alpha )-частиц проходила сквозь тонкий слой вещества, почти не отклоняясь от первоначального направления, очень небольшая доля этих частиц отклонялась на большие углы. Это возможно только под действием большой кулоновской силы, которая является результатом лобового столкновения положительно заряженной ( alpha )-частицы с положительным зарядом в атоме. Размеры этого заряда очень малы. Резерфорд назвал его «ядро атома» и в 1911 году предложил планетарную модель атома.
Планетарная модель атома
Резерфорд предположил, что атом представляет собой миниатюрную планетарную систему, в которой действуют электрические силы притяжения. В центре каждого атома находится положительно заряженное ядро. Вокруг ядра по эллиптическим орбитам вращаются отрицательно заряженные электроны.
В ядре сосредоточена практически вся масса атома, но оно занимает ничтожно малую часть его объема. Электронная оболочка занимает большую часть объема атома, но ее масса мала.
В целом атом нейтрален, т. к. суммарный отрицательный заряд электронов равен положительному заряду атомного ядра.
Планетарная модель атома Резерфорда не смогла объяснить ряд важнейших свойств атомов. В частности, атом, согласно классической механике, должен излучать электромагнитные волны, т. к. электроны движутся с ускорением (центростремительным). Это должно приводить к уменьшению энергии атома, а следовательно, к падению электрона на ядро. Однако атомы обычно не излучают электромагнитные волны и устойчивы.
Постулаты Бора
Датский ученый Н. Бор, развивая идеи Резерфорда, в 1913 году утверждал, что законы движения микрочастиц сильно отличаются от законов движения в макромире. По его мнению, законы микромира – квантовые законы, которые в то время еще не были установлены наукой. Н. Бор положил в основу своей теории следующие постулаты.
Постулаты Бора
Постулат стационарных состояний:
атом может находиться лишь в определенных стационарных состояниях, каждому из которых соответствует определенная энергия. В стационарных состояниях атом не излучает энергию.
Условие квантования круговых орбит:
каждому стационарному состоянию соответствует строго определенная энергия. Двигаясь по круговым орбитам, электроны обладают квантованными значениями момента импульса:
где ( n ) = 1; 2; 3… – номер стационарной орбиты, ( r ) – радиус стационарной орбиты, ( h ) – постоянная Планка.
Правило частот:
излучение или поглощение энергии атомом происходит при переходе электрона из одного стационарного состояния в другое. Энергия излученного или поглощенного кванта электромагнитного излучения при переходе атома из одного стационарного состояния с энергией ( E_m ) в другое стационарное состояние с энергией ( E_n ) равна разности энергий атома в этих состояниях:
где ( m ) и ( n ) – номера стационарных состояний.
Говорят, что энергия атома квантуется, а при переходе с одной стационарной орбиты на другую атом теряет или поглощает квант энергии. Поэтому теория атома Бора была названа квантовой теорией.
Стационарное состояние с минимальным запасом энергии называется основным состоянием, а все остальные стационарные состояния называются возбужденными состояниями.
Стационарные состояния представляют с помощью энергетической диаграммы. На ней состояния атома обозначаются горизонтальными линиями – энергетическими уровнями.
Переход атома из стационарного состояния с меньшей энергией в состояние с большей энергией сопровождается поглощением энергии и обозначается стрелкой, направленной вверх. Переход атома из стационарного состояния с большей энергией в состояние с меньшей энергией сопровождается выделением энергии и обозначается стрелкой, направленной вниз.
Используя постулаты и планетарную модель атома, Бор разработал количественную теорию атома водорода.
Применяя классические представления о движении электрона по круговой орбите под действием кулоновской силы притяжения между ядром и электроном, он получил выражение для радиусов орбит, соответствующих стационарным состояниям атома водорода, и для энергетических уровней.
При движении по круговой орбите кулоновская сила обеспечивает электрону центростремительное ускорение:
Для водорода ( Z ) = 1; ( frac{e^2}{4piepsilon_0r}=mv^2 ) или ( frac{e^2}{4piepsilon_0v}=mvr,,mvr=frac{nh}{2pi}. )
Скорость электрона на стационарных круговых орбитах:
где ( n ) = 1; 2; 3 … – номер стационарной круговой орбиты,
Радиус стационарных круговых орбит:
Радиус первой боровской орбиты: ( r_1 ) = 0,528·10-10 м.
Двигаясь по каждой из разрешенных стационарных круговых орбит, электрон обладает определенным запасом кинетической и потенциальной энергий:
Полная энергия электрона на стационарной орбите равна сумме кинетической и потенциальной энергий:
Согласно постулату Бора энергия излучения: ( hnu=E_m-E_n ),
( R=frac{me^4}{8varepsilon_0^2h^3}= )3,29 · 1015 с-1 – постоянная Ридберга,
Серии спектральных линий излучения, возникающих при переходе атома водорода из возбужденных состояний, принято объединять в группы.
Спектральные серии атома водорода
- Серия Лаймана
Если атом водорода перейдет с возбужденных стационарных уровней в основное состояние, то он излучит невидимые ультрафиолетовые лучи с набором соответствующих частот:
- Серия Бальмера
Если атом водорода перейдет с возбужденных стационарных уровней на второй уровень, то он излучит видимый свет с набором соответствующих частот:
- Серия Пашена
Если атом водорода перейдет с возбужденных стационарных уровней на третий уровень, то он излучит невидимые инфракрасные лучи c набором соответствующих частот:
Линейчатые спектры
Спектр – это набор частот, излучаемых нагретым телом.
Виды спектров
- Непрерывные (сплошные) спектры дают нагретые тела в твердом и жидком состоянии, а также в сжатом газообразном.
- Линейчатые спектры дают раскаленные газы в атомарном состоянии под сравнительно небольшим давлением.
- Полосатые спектры дают газы в молекулярном состоянии.
Различают линейчатые спектры испускания и поглощения.
Спектры испускания дают нагретые до высокой температуры тела. Эти спектры состоят из узких линий разного цвета.
Для получения линейчатого спектра излучения вещества, находящегося в обычных условиях в твердом состоянии, его надо нагреть до высокой температуры, при которой оно перейдет в атомарное газообразное состояние.
Спектры поглощения возникают при пропускании лучей сплошного спектра через менее нагретый газ. На фоне сплошного спектра обнаруживаются узкие темные полосы.
Линейчатый спектр у каждого химического элемента свой, не совпадающий со спектром другого химического элемента.
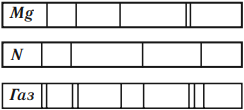
Зная линейчатые спектры различных химических элементов, можно определить химический состав неизвестного газа. Для этого необходимо сравнить линейчатый спектр данного газа со спектрами известных элементов.
По рисунку видно, что газ состоит из магния и азота, т. к. в его спектре присутствуют только линии, принадлежащие этим газам.
Линии спектра поглощения расположены в тех местах спектра, в которых находятся линии спектра излучения того же газа.
Спектральный анализ – метод определения химического состава тел по их спектру испускания или поглощения.
Спектральный анализ основывается на двух положениях:
- каждый химический элемент или химическое соединение характеризуется определенным спектром;
- интенсивность линий и полос в спектре зависит от концентрации того или иного элемента в веществе.
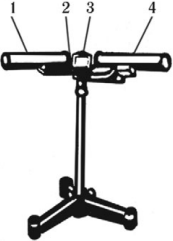
Спектроскоп – прибор для разложения сложного света и наблюдения спектров.
Спектроскоп состоит из двух труб – коллиматорной (1) и зрительной (4), укрепленных на подставке (2), и стеклянной призмы под крышкой (3).
Параллельный пучок света, выходящий из коллиматора, попадает на грань стеклянной призмы. Так как показатель преломления зависит от длины волны, то пучок света, состоящий из волн с разной длиной волны, разлагается на параллельные пучки света разного цвета. Линза зрительной трубы фиксирует каждый пучок и дает разноцветные изображения щели, образуя разноцветную полоску – спектр.
Лазер
Лазер – это оптический квантовый генератор, создающий мощные, узконаправленные, когерентные пучки монохроматического излучения.
Излучение может быть спонтанным (самопроизвольным) или индуцированным (вынужденным).
Спонтанное излучение – испускание атомом фотона в результате самопроизвольного перехода электрона из возбужденного состояния в основное.
Индуцированное излучение – переход электрона из возбужденного состояния в основное под действием электромагнитного излучения.
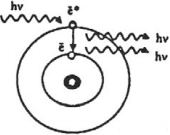
Фотон-«катализатор» попадает в возбужденный электрон и, стимулируя его переход в основное состояние, не теряет своей энергии. В результате из атома испускаются два фотона.
Основные компоненты лазера:
- активная среда – среда, в которой создаются состояния с инверсной заселенностью, т. е. заселенностью, при которой число атомов в возбужденных состояниях больше, чем их число в основном состоянии;
- система накачки – устройство для создания инверсной заселенности уровней в активной среде;
- оптический резонатор – устройство, выделяющее в пространство избирательно направленный поток фотонов и формирующее выходящий световой пучок.
Классификация лазеров
- По типу активной среды – твердотельные, газовые, полупроводниковые, жидкостные.
- По методу накачки – оптические, тепловые, химические, электроионизационные и др.
- По режиму генерации – непрерывного действия, импульсного действия.
Устройство рубинового лазера
1 – система зеркал; состоит из двух строго параллельных друг другу плоских зеркал, расположенных возле торцов рубинового стержня. Используется для того, чтобы заставить световой пучок многократно проходить через рубиновый стержень. Одно из зеркал полностью отражает свет, а другое полупрозрачно, т. е. частично отражает, а частично пропускает свет;
2 – рубиновый стержень; представляет собой цилиндр, длина которого в 8–10 раз превышает его диаметр;
3 – газоразрядная лампа; имеет вид спирали и охватывает рубиновый стержень. Ее используют для возбуждения ионов хрома в рубине;
4 – система охлаждения; охлаждает рубиновый стержень при работе лазера;
5 – батарея конденсаторов.
Принцип работы рубинового лазера
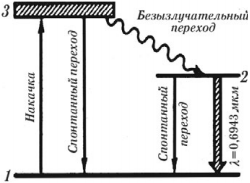
При облучении рубина сине-зеленым светом ионы хрома возбуждаются и из основного состояния (уровень 1) переходят в возбужденное состояние (уровень 3). Через короткий промежуток времени (≈10-8 с) большинство ионов хрома спонтанно переходят с уровня 3 на метастабильный энергетический уровень 2, в котором они могут находиться ≈10-3 с, т. е. в 100 тысяч раз дольше, чем на обычном возбужденном уровне. Таким образом, создается «перенаселение» уровня 2, т. е. число возбужденных электронов больше числа невозбужденных электронов. Переход ионов с энергетического уровня 3 на метастабильный уровень 2 происходит без излучения света. Высвобождающаяся при таком переходе энергия передается кристаллической решетке рубина.
Под действием электромагнитных волн, облучающих рубин, или под действием фотонов, появляющихся в самом веществе при спонтанных переходах атомов на уровень 2, происходит переход ионов хрома с метастабильного уровня 2 на уровень 1, и возникает вынужденное излучение света.
Свойства лазерного излучения:
- временная и пространственная когерентность;
- строгая монохроматичность;
- большая плотность потока энергии;
- очень малое угловое расхождение в пучке.
Применение лазеров:
- передача информации; связь (особенно в космосе);
- точное определение расстояний;
- трассировка туннелей; геологические измерения;
- определение курса и скорости кораблей, самолетов, ракет;
- в голографии для получения объемных изображений предметов;
- точечная сварка при изготовлении микросхем;
- осуществление управления термоядерными реакциями;
- в хирургии для разрезания, сшивания, стерилизации живых тканей, для приваривания отслоившейся сетчатки глаза.
Основные формулы по теме «Физика атома»
Физика атома
2.9 (58.75%) 16 votes
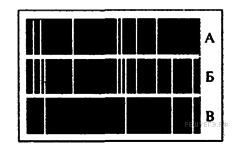
Задание 19 № 2007. На рисунках А, Б и В приведены спектры излучения атомарных газов А и В и газовой смеси Б.
На основании анализа этих участков спектров можно сказать, что смесь газа содержит
1) только газы А и В
2) газы А, В и другие
3) газ А и другой неизвестный газ
4) газ В и другой неизвестный газ
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре зависят только от свойств атомов этого вещества, но совершенно не зависят от способа возбуждения свечения атомов. Из рисунка видно, что на спектре газовой смеси Б присутствуют те и только те линии, которые есть либо на спектре газа А, либо на спектре газа В. Этот факт говорит в пользу того, что смесь газа Б содержит только газы А и В.
Правильный ответ: 1.
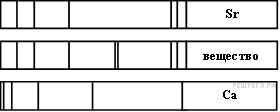
Задание 19 № 2027. На рисунке приведены спектр поглощения разреженных атомарных паров неизвестного вещества (в середине) и спектры поглощения паров известных элементов (вверху и внизу).
По анализу спектров можно утверждать, что неизвестное вещество содержит
1) только кальций (Са)
2) только стронций (Sr)
3) кальций и еще какое-то неизвестное вещество
4) стронций и еще какое-то неизвестное вещество
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре поглощения зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре поглощения разреженных атомарных паров неизвестного вещества присутствуют все линии, которые есть на спектре стронция, нет линий, свойственных кальцию, но в тоже время есть дополнительные неизвестные линии. Этот факт говорит в пользу того, что в химический состав неизвестного вещества входит стронций и еще какое-то неизвестное вещество.
Правильный ответ: 4.
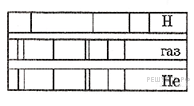
Задание 19 № 2115. На рисунке приведены фрагмент спектра поглощения неизвестного разреженного атомарного газа (в середине), спектры поглощения атомов водорода (вверху) и гелия (внизу).
В химический состав газа входят атомы
1) только водорода
2) только гелия
3) водорода и гелия
4) водорода, геля и еще какого-то вещества
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре поглощения зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре поглощения неизвестного разреженного атомарного газа присутствуют те и только те линии, которые есть на спектре гелия. Этот факт говорит в пользу того, что в химический состав неизвестного газа входит только гелий (то есть это и есть гелий).
Правильный ответ: 2.
|
Задание 19 № 2122. На рисунках А, Б, В приведены спектры излучения паров стронция, неизвестного образца и кальция. Можно утверждать, что в образце 1) не содержится ни стронция, ни кальция 2) содержится кальций, но нет стронция 3) содержатся и стронций, и кальций 4) содержится стронций, но нет кальция Решение. На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре pзависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре излучения паров неизвестного образца присутствуют все линии, которые есть на спектре стронция, нет линий, свойственных кальцию, но в тоже время есть дополнительные неизвестные линии. Этот факт говорит в пользу того, что в образце содержится стронций, но нет кальция. Правильный ответ: 4. |
Задание 19 № 2123. Длина волны фотона, излучаемого атомом при переходе из возбужденного состояния с энергией в основное состояние с энергией
, равна (c — скорость света, h — постоянная Планка)
1)
2)
3)
4)
Решение.
Частота фотона, излучаемого атомом при переходе в состояние с более низкой энергией, связана с изменением энергии атома соотношением . Принимая во внимание связь
, получаем, что длина волны фотона равна
.
Правильный ответ: 3.
Задание 19 № 2135. Каков спектр энергетических состояний атомного ядра и какие частицы испускает ядро при переходе из возбужденного состояния в нормальное?
1) cпектр линейчатый, испускает гамма-кванты
2) cпектр сплошной, испускает гамма-кванты
3) cпектр сплошной, испускает бета-частицы
4) cпектр линейчатый, испускает альфа-частицы
Решение.
Атомная система может находиться только в особых стационарных, или квантовых, состояниях, каждому из которых соответствует определенная энергия. Таким образом, спектр энергетических состояний атомного ядра линейчатый. При переходе атома из возбужденного состояния в нормальное испускаются гамма-кванты.
Правильный ответ: 1.
Задание 19 № 3243. 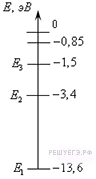
1) получить от атома энергию 3,4 эВ
2) сообщить атому энергию 3,4 эВ
3) получить от атома энергию 13,6 эВ
4) сообщить атому энергию 13,6 эВ
Решение.
Основным состоянием в атоме называется состояние с наименьшей энергии. Для водорода это уровень с энергией
. Началом отсчета энергии
является состояние, при котором ядро водорода и электрон перестают быть связанной системой. При этой энергии происходит ионизация. Таким образом, для того чтобы перевести атом водорода из основного состояния в ионизированное, необходимо сообщить ему энергию
.
|
Задание 19 № 3342. Каков заряд ядра 1) 5 2) 11 3) 16 4) 6 Решение. Числом протонов (заряд ядра в элементарных единицах заряда) записывается внизу перед наименованием элемента. Таким образом, заряд ядра Правильный ответ: 1. |
Задание 19 № 3344. Атом бора содержит
1) 8 протонов, 5 нейтронов и 13 электронов
2) 8 протонов, 13 нейтронов и 8 электронов
3) 5 протонов, 3 нейтрона и 5 электронов
4) 5 протонов, 8 нейтронов и 13 электронов
Решение.
Число электронов в нейтральном атоме совпадает с числом протонов, которое записывается внизу перед наименованием элемента. Число вверху обозначает массовое число, то есть суммарное число протонов и нейтронов. Таким образом, атом бора содержит 5 протонов, 3 нейтронов и 5 электронов.
Правильный ответ: 3.
|
Задание 19 № 3387. На рисунке приведены спектры поглощения атомарных паров неизвестного вещества и трех известных элементов. По виду спектров можно утверждать, что неизвестное вещество содержит в заметном количестве атомы 1) только стронция (Sr) и кальция (Са) 2) только натрия (Na) и стронция (Sr) 3) только стронция (Sr), кальция (Са) и натрия (Na) 4) стронция (Sr), кальция (Са), натрия (Na) и других элементов Решение. На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре поглощения зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре поглощения неизвестного вещества присутствуют все линии, которые есть на спектрах стронция, кальция и натрия. Помимо этого, на спектре есть линии, которых нет на других трех спектрах. Этот факт говорит в пользу того, что в химический состав неизвестного газа входят и стронций, и кальций, и натрий, а помимо их еще некоторые неизвестные элементы. |
Задание 19 № 3750. Линейчатые спектры поглощения и испускания характерны для
1) любых тел
2) любых нагретых тел
3) для твердых нагретых тел
4) для нагретых атомарных газов
Решение.
Спектры излучения и поглощения связаны с энергетическими переходами в веществе. Чем «сложнее» система, тем запутаннее ее спектры. Для почти свободных атомов и молекул в разрежённых газах спектры поглощения и испускания состоят из отдельных спектральных линий и потому называются линейчатым. Таким образом, линейчатые спектры поглощения и испускания характерны для атомарных газов.
Правильный ответ: 4.
Задание 19 № 3884. На рисунке схематически изображена фотография спектральных линий атомов некоторого химического элемента в ультрафиолетовой части спектра. Из этого рисунка следует, что
1) атом данного химического элемента имеет шесть электронов
2) электроны в атоме этого химического элемента могут находиться только на шести энергетических уровнях
3) электроны в атоме этого химического элемента могут находиться только на четырёх энергетических уровнях
4) только при шести переходах электронов с одного энергетического уровня на другой атом этого химического элемента испускает фотон с длиной волны, лежащей в ультрафиолетовой области спектра
Решение.
Согласно постулатам Бора, энергия излучается или поглощается атомом только при переходе электрона из одного стационарного состояния в другое, при этом частота излучения пропорциональна разности энергий стационарных состояний. Спектр изображает наблюдаемые на эксперименте частоты излучений. Поэтому из приведенного здесь схематического рисунка ультрафиолетовой части спектра можно лишь заключить, что только при шести переходах электронов с одного энергетического уровня на другой атом химического элемента испускает фотон с частотой (длиной волны), лежащей в ультрафиолетовой области спектра.
Правильный ответ: 4.
Задание 19 № 4129. 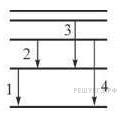
1) 1
2) 2
3) 3
4) 4
Решение.
Квант энергии излучается при переходе на более низкий уровень энергии. При этом расстояние между уровнями пропорционально импульсу излучаемого фотона: . Из диаграммы видно, что среди предложенных вариантов ответа минимальному расстоянию между уровнями, а значит, и минимальному импульсу фотона соответствует переход 2.
Правильный ответ: 2.
|
Задание 19 № 4741. Схема низших энергетических уровней атомов разреженного атомарного газа имеет вид, изображённый на рисунке. В начальный момент времени атомы находятся в состоянии с энергией 1) 0,3 эВ, 0,5эВ и1,5 эВ 2) только 1,5 эВ 3) любой в пределах от 0 до 0,5 эВ 4) только 0,3 эВ Решение. Согласно постулатам Бора, свет излучается при переходе атома на более низкие уровни энергии, при этом фотоны несут энергию, равную разности энергий начального и конечного состояний. Из приведенной здесь схемы видно, что фотон может излучиться только при переходе атома в состояние Правильный ответ: 2 |
|
Задание 19 № 4811. На рисунке указаны три низших значения энергии атома натрия. Атомы находятся в состоянии 1) произойдёт переход атомов в состояние 2) произойдёт переход атомов в состояние 3) произойдёт ионизация атомов 4) атомы не будут поглощать свет Решение. Согласно постулатам Бора, свет поглощается при переходе атома на более высокие уровни энергии, при этом фотоны должны иметь энергию, равную разности энергий конечного и начального состояний. Если атом в состоянии Из приведенной здесь схемы видно, что уровень с данной энергией действительно существует. Следовательно атомарные пары натрия будут поглощать фотоны переходить из состояния Правильный ответ: 2 |
Задание 19 № 4916. На рисунке показана схема низших энергетических уровней атома. В начальный момент времени атом находится в состоянии с энергией . Фотоны какой энергии может излучать атом?
1) только 2 эВ
2) только 2,5 эВ
3) любой, но меньшей 2,5 эВ
4) любой в пределах от 2,5 до 4,5 эВ
Решение.
Согласно постулатам Бора, свет излучается при переходе атома на более низкие уровни энергии, при этом фотоны несут энергию, равную разности энергий начального и конечного состояний. Из приведенной здесь схемы видно, что фотон может излучиться только при переходе атома в состояние , при этом его энергия будет равна .
Правильный ответ: 1
Задание 19 № 4951. На рисунке приведён спектр поглощения неизвестного газа и спектры поглощения атомарных паров известных элементов. По виду спектров можно утверждать, что неизвестный газ содержит атомы
1) азота (N), магния (Mg) и других элементов, но не калия (К)
2) только азота (N) и калия (К)
3) только магния (Mg) и азота (N)
4) магния (Mg), калия (К) и азота (N)
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре поглощения зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре поглощения паров неизвестного газа присутствуют все линии, которые есть на спектрах магния, калия и азота. Этот факт говорит в пользу того, что в химический состав неизвестного газа входят магний (Mg), калий (К) и азот (N).
Правильный ответ: 4
Задание 19 № 5161. На рисунках А, Б и В приведены спектры излучения паров кальция Са, стронция Sr и неизвестного образца. Можно утверждать, что в неизвестном образце
1) не содержится стронция
2) содержатся кальций и ещё какие-то элементы
3) не содержится кальция
4) содержится только кальций
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре излучения зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре излучения паров неизвестного газа присутствуют все линии, которые есть на спектре стронция. Этот факт говорит в пользу того, что в химический состав неизвестного газа входит стронций. С другой стороны, линий, характерных для кальция, в неизвестном спектре не наблюдается. Следовательно, неизвестный образец не содержит кальция. Таким образом, верно утверждение 3.
Правильный ответ: 3
Примечание. Можно утверждать, что в неизвестном веществе находится, например, кальций, только в том случае, если все линии кальция содержатся в спектре этого неизвестного вещества.
Задание 19 № 5196. На рисунке приведены спектры поглощения паров натрия, атомарного водорода и атмосферы Солнца.
Об атмосфере Солнца можно утверждать, что в ней
1) не содержится натрия
2) не содержится водорода
3) содержится только натрий и водород
4) содержится и натрий, и водород
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре атмосферы Солнца присутствуют все линии, которые есть на спектрах натрия водорода. Но помимо этих линий есть еще много других. Этот факт говорит в пользу того, что в химический состав атмосферы Солнца входят натрий, водород и что-то еще. Таким образом, верно утверждение 4.
Правильный ответ: 4
Задание 19 № 5231. На рисунке приведены спектр поглощения разреженных атомарных паров неизвестного вещества и спектры поглощения атомарных паров известных элементов. Проанализировав спектры, можно утверждать, что неизвестное вещество содержит
1) только водород (Н) и гелий (Не)
2) водород (Н), гелий (Не) и натрий (Na)
3) только натрий (Na) и водород (Н)
4) натрий (Na), водород (Н) и другие элементы, но не гелий (Не)
Решение.
На рисунке представлены линейчатые спектры. Главное свойство линейчатого спектра состоит в том, линии какого-либо вещества на спектре зависят только от свойств атомов этого вещества. Из рисунка видно, что на спектре поглощения паров неизвестного газа присутствуют все линии, которые есть на спектре водорода и натрия. Линии, характерные для гелия, отсутствуют. Однако присутствуют линии, соответствующие каким-то другим элементам. Все это говорит в пользу того, что в химический состав неизвестного газа входят натрий (Na), водород (Н) и другие элементы, но не гелий (Не)
Правильный ответ: 4
Задание 19 № 5616.
Схема низших энергетических уровней атома имеет вид, изображённый на рисунке. В начальный момент времени атом находится в состоянии с энергией . Согласно постулатам Бора атом может излучать фотоны с энергией
1) только 0,5 эВ
2) только 1,5 эВ
3) любой, меньшей 0,5 эВ
4) любой в пределах от 0,5 до 2 эВ
Решение.
Согласно постулатам Бора, свет излучается при переходе атома на более низкие уровни энергии, при этом фотоны несут энергию, равную разности энергий начального и конечного состояний. Единственный переход с излучением фотонов возможен на уровень с энергией равной
Правильный ответ указан под номером 2.
Задание 19 № 6090. Бета-частица представляет собой
1) нейтрон
2) электрон
3) ядро гелия
4) ион гелия
Решение.
Бета-частица — это частица с малой массой и зарядом, равным заряду электрона. Такая частица и есть электрон.
Правильный ответ указан под номером: 2.
Задание 19 № 6125. Спектр какого типа наблюдается у излучения атомарного водорода?
1) линейчатый
2) полосатый
3) сплошной
4) ответ зависит от разрешающей силы используемого спектроскопа
Решение.
Атом водорода излучает, когда его электроны переходят с более высоких энергетических уровней на более низкие, в результате чего возникают кванты света с определённой длиной волны, то есть спектр водорода — линейчатый.
Задание 19 № 6160. Спектр какого типа наблюдается у излучения атомарного гелия?
1) линейчатый
2) полосатый
3) сплошной
4) ответ зависит от разрешающей силы используемого спектроскопа
Решение.
Атом гелия излучает, когда его электроны переходят с более высоких энергетических уровней на более низкие, в результате чего возникают кванты света с определённой длиной волны, то есть спектр гелия — линейчатый.
Задание 19 № 6204. В таблице приведены значения энергии для второго и четвёртого энергетических уровней атома водорода.
|
Номер уровня |
Энергия, 10–19 Дж |
|
2 |
–5,45 |
|
4 |
–1,36 |
Какой должна быть энергия фотона, при поглощении которого атом переходит со второго уровня на четвёртый?
1) 4,09·10−19 Дж
2) 1,36·10−19 Дж
3) 5,45·10−19 Дж
4) 6,81·10−19 Дж
Решение.
Для того, чтобы электрон перешёл со второго уровня на четвёртый под действием фотона, энергия фотона должна быть равна разности энергий четвёртого и второго энергетических уровней: −1,36 − (−5,45) = 4,09·10−19 Дж.
Правильный ответ указан под номером: 1.
Задание 19 № 6239. В таблице приведены значения энергии для третьего и четвёртого энергетических уровней атома водорода.
|
Номер уровня |
Энергия, 10–19 Дж |
|
3 |
–2,42 |
|
4 |
–1,36 |
Какой должна быть энергия фотона, при поглощении которого атом переходит с третьего уровня на четвёртый?
1) 2,42·10–19 Дж
2) 1,06·10–19 Дж
3) 1,36·10–19 Дж
4) 3,78·10–19 Дж
Решение.
Для того, чтобы электрон перешёл с третьего уровня на четвёртый под действием фотона, энергия фотона должна быть равна разности энергий четвёртого и третьего энергетических уровней: −1,36 − (−2,42) = 1,06·10−19 Дж.
Правильный ответ указан под номером: 2.
Задание 19 № 6276. На рисунке приведены спектр поглощения неизвестного газа и спектры поглощения атомарных паров известных элементов. По виду спектров можно утверждать, что неизвестный газ содержит атомы
1) только азота ()
2) азота (), магния (
) и другого неизвестного вещества
3) только магния ()
4) только магния () и азота (
)
Решение.
Сравним спектры атомов и спектры неизвестного газа. Из рисунка видно, что все линии, присутствующие в спектре магния есть и в спектре неизвестного газа. Аналогично для азота. Это означает, что газ содержит, как минимум, атомы магния и азота. Кроме линий магния и азота в спектре неизвестного газа содержатся линии, не принадлежащие ни магнию, ни азоту. Следовательно, присутствуют также атомы неизвестного вещества.
Правильный ответ указан под номером: 2.
Задание 19 № 6312. На рисунке приведены спектр поглощения неизвестного газа и спектры поглощения атомарных паров известных металлов. По виду спектров можно утверждать, что неизвестный газ содержит атомы
1) только стронция ()
2) стронция (), кальция (
) и другого вещества
3) только стронция () и кальция (
)
4) только кальция ()
Решение.
Сравним спектры атомов и спектры неизвестного газа. Из рисунка видно, что все линии, присутствующие в спектре стронция есть и в спектре неизвестного газа. Аналогично для кальция. Это означает, что газ содержит, как минимум, стронция и кальция. Кроме линий стронция и кальция в спектре неизвестного газа содержатся линии, не принадлежащие ни стронцию, ни кальцию. Следовательно, присутствуют также атомы неизвестного вещества.
Правильный ответ указан под номером: 2.