Структура ЕГЭ по химии: задания, уровни сложности и другая важная информация
Несмотря на то, что химия является экзаменом по выбору, это не умаляет его важности при поступлении на медицинские, экологические, биоинженерные и другие программы. ЕГЭ по этому предмету является восьмым по популярности предметом: в этом году его сдают 95 тысяч абитуриентов, а средний балл колеблется на уровне 53−54 баллов. Рассказываем о структуре ЕГЭ по химии 2022, чтобы ты смог основательно подготовиться к экзамену.
Основная информация о ЕГЭ 2022 по химии
Экзамен по химии состоит из двух частей. Первая включает 28 заданий, на которые нужно дать краткий ответ. Задания второй части (а их 6) открытого типа, на них необходимо ответить развёрнуто. На решение всех задач отводится 210 минут. Основной этап ЕГЭ по химии 2022 запланирован на 26 мая (четверг). Заявление на участие в этом экзамене тебе нужно было подать до 1 февраля. В содержании испытания планируются следующие изменения.
Как самостоятельно подсчитать баллы ЕГЭ: раскладываем систему по полочкам
Первая часть в ЕГЭ по химии: 28 заданий
Как мы отмечали выше, в первую часть включены 28 заданий, 8 из которых повышенной сложности. В них обычно просят выбрать один либо несколько правильных ответов из пяти предложенных или установить соответствие. В этом разделе экзамена ответы записываются в виде двух-трёх цифр. В задачах повышенного уровня необходимо находить ответы на нестандартные ситуации либо устанавливать соответствия между названием органического соединения и классом/группой, к которому (-ой) оно принадлежит; названием или формулой соли и отношением этой соли к гидролизу; исходными веществами и продуктами реакции между этими веществами; названием или формулой соли и продуктами, которые образуются на инертных электродах при электролизе её водного раствора, и т. д.
За правильное выполнение первой части заданий абитуриент может получить 36 первичных баллов из максимальных 56.
Вторая часть ЕГЭ: 6 заданий
Это самая сложная часть экзамена. На шесть заданий высокого уровня сложности необходимо дать развёрнутый ответ. Таким образом проверяется комплексное усвоение знаний на углубленном уровне: выполнение расчётов в химических реакциях различного вида, установление молекулярной и структурной формулы вещества и так далее.
За правильное решение этих 6 заданий можно получить 20 первичных баллов. В этом ты убедишься, когда порешаешь демовариант ЕГЭ по химии.
Что можно брать на ЕГЭ 2022 по химии?
На экзамене разрешено пользоваться линейкой; непрограммируемым калькулятором с возможностью вычисления тригонометрических функций (cos, sin, tg); периодической системой химических элементов Д.И. Менделеева; таблицей растворимости солей, кислот и оснований в воде; электрохимическим рядом напряжений металлов. Все другие предметы следует оставить за пределами аудитории.
Как оценивают результаты ЕГЭ по химии?
Ответы на задания первой части автоматически обрабатываются компьютером, а вторую часть проверяет предметная комиссия.
За правильный ответ на задания 1−5, 9−13, 16−21, 25−28 начисляется 1 балл. Задание считается выполненным верно, если абитуриент указал правильную последовательность цифр или число с заданной степенью точности.
Задания 6−8, 14, 15, 22−24 считаются выполненными верно, если правильно указана последовательность цифр. За полный ответ на каждое из вопросов 6−8, 14, 15, 22−24 ставится 2 балла; если допущена одна ошибка — 1 балл; за неверный ответ (более одной ошибки) или его отсутствие — 0 баллов.
Задания части 2 (с развёрнутым ответом) подразумевают проверку от двух до пяти элементов ответа. Наличие каждого обязательного элемента ответа оценивается в 1 балл, поэтому максимальная оценка задания составляет от 1 до 5 баллов в зависимости от степени сложности задания. Так, за задания 29 и 30 абитуриент получает 2 балла; 31 и 33 — 4 балла; 32 — 5 баллов; 34 — 3 балла.
Таким образом, вся сумма баллов (первичный балл) переводится в тестовый. Тестовый балл и есть результат Единого государственного экзамена.
Хочешь сдать ЕГЭ на максимально возможных балл? Тогда обрати внимание на сложные задания и записывайся на онлайн-курсы от Адукар. Удачи!
Спасибо, что дочитал до конца. Мы рады, что были полезны. Чтобы получить больше информации, посмотри ещё:
Онлайн-курсы подготовки к ЕГЭ
Каталог учебных заведений Адукар
Не пропускай важные новости и подписывайся на наш YouTube, ВК, Instagram, Telegram, Facebook и уведомления на adukar.by.
***
Если хотите разместить этот текст на своём сайте или в социальной сети, свяжись с нами по адресу info@adukar.by. Перепечатка материалов возможна только с письменного согласия редакции.
Хочешь быть в курсе новостей ЦТ?
Подписывайся на Адукар в соцсетях!
Начни подготовку к ЦТ и ЦЭ прямо сейчас!

Адукар обещает крутых преподавателей и много полезной практики.
итоговые занятия перед ЦТ? Такие занятия мы проводим уже четвёртый год, и преподаватели нашего учебного центра
научились достаточно точно предсказывать, какие вопросы будут на ЦТ. На этом занятии мы прорешаем их вместе с тобой!
Регистрируйся,
если еще не сделал этого — и увеличь свои шансы на поступление!
- 31.08.2021
На этой странице мы детально разберем всё изменения, которые ожидают ЕГЭ по химии в 2022 году.
Анализ состоит из 2-х частей:
- 1 часть — официальный список изменений от ФИПИ
- 2 часть — обзоры, видеоразборы, текстовый анализ изменений.
Перед тем как начать — посмотрите демоверсию ЕГЭ 2022 по химии
- Тренировочные варианты по химии
ЧАСТЬ 1. Официальные изменения ФИПИ
В работу внесены следующие изменения.
- В экзаменационном варианте уменьшено с 35 до 34 общее количество заданий. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
— Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
— Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8. - Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
- Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
- Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
- Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).
ЧАСТЬ 2. Анализ всех изменений
И еще
Химия — один из самых сложных предметов для сдачи ЕГЭ. Задания меняются каждый год: то, что раньше казалось трудным, нынешние выпускники должны успевать за пару минут. Несмотря на это экзамен необходим будущим врачам, фармацевтам и, конечно же, химикам. Давайте обсудим, как устроен ЕГЭ по химии 2023 и что нужно выучить для успешной сдачи!
Структура ЕГЭ по химии 2023
ЕГЭ по химии состоит из двух частей. В первой выпускникам предлагают решить 28 заданий — нужен краткий ответ в виде одного числа или последовательности чисел. Во второй части — 6 заданий с развернутым ответом. В них нужно записывать уравнения химических реакций и решать сложные математические задачи. Если выполнить работу без ошибок, можно набрать 56 первичных баллов.
Нововведение ЕГЭ по химии 2023 — сокращение количества заданий и появление новых прототипов.
Изменения в ЕГЭ по химии 2023
Задание № 23. В прошлом году ребята впервые решали задание на расчет равновесных и исходных концентраций. Оно представляло собой уравнение химической реакции, а также таблицу с концентрациями каждого участника. В этом году таблицы не будет, вместо нее предлагается найти исходные данные в тексте. Советуем вам не отходить от уже отработанного алгоритма и самостоятельно составлять таблицы. Немного практики и навык владения калькулятором помогут получить за этот номер максимальные баллы даже с новым условием.
Задания № 9, 12 и 16. Эти задания не изменились на вид. В №9 и 16 предстоит разобраться с небольшими цепочками превращений – неорганической и органической соответственно. А в задании 12 выпускников вновь ожидают химические свойства органических веществ и неизвестное количество правильных ответов. Но в этом году задания станут сложнее, их переносят в разряд заданий повышенного уровня сложности. К сожалению, при неизменном 1 балле за каждый из номеров.
Задания № 33 и 34. Каждый выпускник накануне ЕГЭ по химии очень хочет знать, чему будут посвящены задачи 33 и 34. Конечно же, тайну нам не открыли, но зато эти задания поменяли местами. Теперь №33 – это задача на установление органической формулы, а №34 – сложная расчетная задача, основанная на неорганических превращениях.
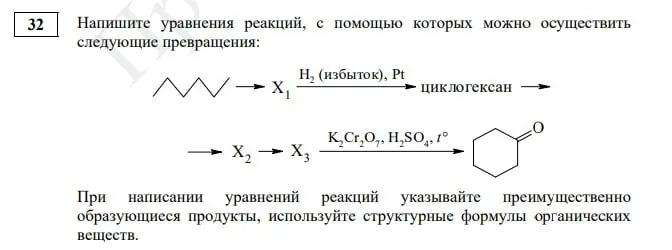
Задание № 32. Эта органическая цепочка существенно не изменилась, ребятам предстоит записать пять уравнений химических реакций. Но стоит обратить пристальное внимание на изображение гексана, с такими формулами мы в ЕГЭ еще не сталкивались, но есть вероятность, что видеть их мы теперь будем чаще.
Это главные изменения ЕГЭ по химии 2023. Но для того, чтобы получить высокий балл, просто знать о них недостаточно. Когда ФИПИ обновляет формулировки заданий, может измениться и способ их решения и критерии оценивания. Если не учитывать это во время подготовки к ЕГЭ, то можно потерять немало баллов. Обидно!
Это — лишь малая часть ловушек экзамена, которые составители расставляют выпускникам. На своих занятиях по подготовке ЕГЭ по химии я показываю ученикам их все. Мы учимся обходить каждую из них и делать такие решения заданий, к которым никто не придерется. А еще я всегда делюсь лайфхаками быстрого и правильного решения типичных задач — так можно сэкономить много времени на более сложные вещи.
Всему этому я могу научить и вас! Приходите ко мне на уроки, и я подготовлю вас к ЕГЭ по химии на 80+ 💪🤓
Какие темы есть в ЕГЭ по химии?
Чтобы успешно сдать ЕГЭ по химии 2023, нужно освоить пять разделов этой науки.
Теоретические основы химии
Этот блок включает в себя информацию о строении атомов, об их существовании в молекулах вещества. Выпускникам нужно продемонстрировать навыки работы с таблицей химических элементов Д.И. Менделеева. Этот раздел поможет решить задания 1-4, 18-20, 23 в первой части, а также задание 29 во второй части.
Неорганическая химия
Этой теме посвящены задания 5-9, 17, 21 (первая часть), 30, 31 (вторая часть). Вас ждут любые свойства неорганических соединений: от простых веществ-металлов и неметаллов до комплексных солей и кристаллогидратов. Чтобы получить высокие баллы, необходимо также знать правила номенклатуры, способы получения и основы процессов гидролиза и электролиза.
Органическая химия
В заданиях 10-16 и 32 вы столкнетесь с органической химией. Ученики, которые готовятся самостоятельно, часто стараются выучить все классы веществ по стандартному плану: название класса, номенклатура, физические и химические свойства, способы получения и применение. На самом деле можно значительно облегчить себе жизнь и начать со строения органических молекул. Как только вы поймете, что кратные связи можно разорвать одним набором реактивов, в группе –ОН замещают атом водорода, а –NH2 группа реагирует с кислотами, классы органических веществ и их реакции покажутся однотипными.
Химия и жизнь
Название этого раздела кажется простым и понятным. К сожалению, именно здесь ученики чаще всего теряют баллы. В задании 24 необходимо мысленно представить эксперимент и написать, что произойдет при смешивании заданных веществ. Например, может выпасть осадок, выделиться газ, а может вообще ничего не произойти. В задании 25 нужно определить, где используют то или иное химическое соединение. Ответом может быть химическая промышленность, медицина, сельское хозяйство и, конечно, повседневная жизнь человека.
Решение расчетных задач
Очень важная часть экзамена по химии. В заданиях 26, 27 и 28 в первой части нужно дать ответ в виде числа, не записывая решение. Обычно эти задачи решаются в одно действие — они проверяют не знания химических процессов, а навыки работы с калькулятором.
Задание 34, по мнению многих учеников — самое сложное во всем экзамене. Чтобы его решить, нужно знать химические свойства веществ, уметь составлять причинно-следственные связи в химических системах, понимать, какие вещества реагируют без остатка и почему. Кроме того, в последние годы все чаще встречаются задачи, которые необходимо решать с помощью линейных уравнений или их систем.
В задаче 32 нужно выполнить расчеты, которые позволят установить молекулярную формулу некоторого органического вещества. Далее, используя описание, необходимо представить эту формулу в структурном виде, показывая связи между атомами. Обязательно запишите в ответе уравнение реакции, о которой идет речь в условии!
Как подготовиться к ЕГЭ по химии 2023?
По структуре экзамена видно, что вам придется повторить или освоить заново весь курс химии за год. С какой темы начать? За что взяться в первую очередь?
Скачайте кодификатор по химии 2023 года. Обычно он находится вместе в демоверсией. В этом документе перечислены все темы, которые необходимо хорошо подготовить. Этот перечень охватывает все задания ЕГЭ, в нем нет ничего лишнего.
Подружитесь с таблицами. Периодическая система химических элементов Д. И. Менделеева, таблица растворимости кислот, солей и оснований, ряд активности металлов – это отличные шпаргалки, которые раздают вместе с вариантами на ЕГЭ. Если правильно ими воспользоваться, можно не только понять, протекает ли реакция между веществами, но даже установить среду раствора, силу кислоты и цвет осадка. И это еще не все!
Грамотно распределите время. Учите теорию, но и не забывайте практиковаться. Если вы не нарешаете тренировочных вариантов, время может сыграть злую шутку на реальном экзамене. 210 минут не хватает на размышления, решения, красивую запись и перепроверку. Необходимо работать в хорошем темпе!
Не оставляйте подготовку на конец года. Несмотря на распределение заданий по разделам химии, старайтесь решать их с самого начала подготовки, постепенно усложняя условия. И помните, что задачи второй части ЕГЭ оцениваются по критериям. Даже если вы не знаете, как решить задание полностью, вы всегда можете заработать 1-2 первичных балла, записав без ошибок уравнения химических реакций и проведя простейшие расчеты.
Прорешивайте как можно больше заданий. Это, пожалуй, самый главный совет. Чем больше вы будете тренироваться и решать типовые задачи, тем выше шансы получить на экзамене высокий балл. Все потому, что вы поймете алгоритм решения и сможете находить правильный ответ намного быстрее, чем другие выпускники.
Когда я готовлю к ЕГЭ по химии в MAXIMUM Education, мы посвящаем немало времени решению всех заданий экзамена. Мы разбираем все части экзамена и учимся правильно оформлять ответы, чтобы не потерять ни одного балла. Чтобы проверить, все ли понятно ученикам, я провожу срезы знаний и даже пробный экзамен. После него я разбираю ошибки с каждым учеником отдельно, и дополнительно объясняю сложные темы.
После такой подготовки мои выпускники пишут настоящий экзамен уверенно и получают высокие баллы. Точно выше среднего балла по стране 🙃 Хотите так же? Приходите на мои занятия, и я научу вас всему, что знаю!
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности
Экзамены по предметам каждый год совершенствуются и становятся либо легче, либо сложнее. Все эти коррективы, которые вносят составители ЕГЭ, заставляют выпускников менять свою подготовку, чтобы получить максимальное количество баллов. Прямо сейчас у нынешних десятиклассников есть возможность узнать все изменения в ЕГЭ по химии, которые будут ждать их на экзамене в следующем году.
Проект нового экзамена ЕГЭ по химии
Прежде всего стоит сказать, что перспективные модели — не окончательные изменения в ЕГЭ по химии. Это лишь идея того, что хотят ввести или убрать, но, в большинстве случаев, именно изменения из перспективных моделей переезжают в официальные демоверсии. Так что нужно готовиться, что большинство изменений примут.
Ознакомиться с полной перспективной моделью можно на сайте ФИПИ, но проще это сделать, если нажать сюда.
Скачать модели по другим предметам можно здесь.
Разбор заданий ЕГЭ по химии: что изменилось
Если вы не хотите искать изменения в ЕГЭ по химии самостоятельно, давайте вместе разберемся, каких номеров они коснулись и что именно изменилось.
Задание №5
В 2022 году под номером 5 появится задача, которая в вариантах 2021-го года находится в №26.
Пример:
Задание №12
Изменения в ЕГЭ по химии появились и здесь. Двенадцатый номер объединил в себе целых два номера из прошлогоднего КИМа:
- №13;
- №14.
В этом задании ученикам придется выбрать подходящие варианты ответа, опираясь лишь на свои знания, а не на минимальное или максимальное количество правильных ответов. Ответ может состоять как из одной, так и из пяти цифр. Но такое маловероятно, поэтому лучше ориентироваться на количество ответов от 2 до 4.
Задание №20
В КИМе 2022-го года вы увидите задачу на гидролиз. Только будет он не под номером 23, а на три номера раньше. С ним справятся ученики, которые умеют определять среду водных растворов.
Задание №24
Номер 24 обновили полностью, так что стоит обратить внимание на него, чтобы не встать в ступор при решении КИМа на экзамене. Оно сложное, но хорошая подготовка и практика решают эту проблему. Выглядит задание так:
Задание №25
В 25-м номере тоже изменения, но приятные: теперь здесь только задания с термохимическим уравнением. Готовиться придется меньше, а решается это просто, так что заработать балл здесь легко.
Задание №26
Этот номер в версии 2022-го года — усложненный номер 29 из КИМа 2021-го. Решив его, вы получите один балл.
Задание №29
А вот это — новинка. Так как старая версия перекочевала в номер 26, двадцать девятую задачу сделали на расчет по химическому равновесию. Оно сложное, так что для двух баллов, которые вы можете заработать, придется постараться.
Задание №33
Последнее изменение в ЕГЭ по химии коснулось задания из второй части, и оно состоит в том, что теперь это усложненная версия №35. Внимательно проверяйте свой ответ, чтобы не потерять баллы, так как задача не из простых.
Вывод
Как вы могли заметить, изменения в ЕГЭ по химии 2022 коснулись многих заданий. Но нужно пользоваться тем, что это стало известно сейчас. Ведь это значит, что у выпускников есть много времени для подготовки. При правильном распределении времени и сил можно научиться решать эти задачи так, чтобы заработать все 100 баллов за экзамен. Остается только начать идти к этому.
Рассмотрим изменения в ЕГЭ 2022 года по химии, представленных ФИПИ:
-
В экзаменационном варианте общее количество заданий уменьшено с 35 до 34. Это достигнуто в результате объединения контролируемых элементов содержания, имеющих близкую тематическую принадлежность или сходные виды деятельности при их выполнении.
-
Элементы содержания «Химические свойства углеводородов» и «Химические свойства кислородсодержащих органических соединений» (в 2021 г. – задания 13 и 14) будут проверяться заданием 12. В обновлённом задании будет снято ограничение на количество элементов ответа, из которых может состоять полный правильный ответ.
-
Исключено задание 6 (по нумерации 2021 г.), так как умение характеризовать химические свойства простых веществ и оксидов проверяется заданиями 7 и 8.
-
Изменён формат предъявления условий задания 5, проверяющего умение классифицировать неорганические вещества, и задания 21 (в 2021 г. – задание 23), проверяющего умение определять среду водных растворов: в текущем году потребуется не только определить среду раствора, но и расставить вещества в порядке уменьшения/увеличения кислотности среды (рН).
-
Включено задание (23), ориентированное на проверку умения проводить расчёты на основе данных таблицы, отражающих изменения концентрации веществ.
-
Изменён вид расчётов в задании 28: требуется определить значение «выхода продукта реакции» или «массовой доли примеси».
-
Изменена шкала оценивания некоторых заданий в связи с уточнением уровня их сложности и количеством мыслительных операций при их выполнении. В результате этого максимальный балл за выполнение работы в целом составит 56 баллов (в 2021 г. – 58 баллов).
Изменение содержания заданий ЕГЭ-2022 по химии
Единый государственный экзамен (ЕГЭ) является одной из форм государственной итоговой аттестации учащихся и проводится в соответствии с Федеральным законом об образовании Российской федерации. Общее содержание экзаменационной работы соответствует федеральному государственному образовательному стандарту. В 2022 году будут сдавать ЕГЭ учащиеся, которые, начиная с первого класса, обучались в соответствии с ФГОС. По этой причине по всем предметам, в том числе и по химии, происходит изменение содержания экзаменационных материалов; это изменение будет осуществлено в 2022 и 2023 годах.
Общая характеристика работы
Экзаменационная работа состоит из двух частей.
Первая часть содержит 28 заданий с кратким ответом, среди них 20 заданий базового уровня сложности, каждое из которых при правильном выполнении оценивается в 1 первичный тестовый балл (задания 1-5, 9-13, 16-21, 25-28), и 8 заданий повышенного уровня сложности, каждое из которых максимально может быть оценено в 2 балла (задания 6-8, 14, 15, 22-24, 26).
Вторая часть включает 6 заданий с развёрнутым ответом высокого уровня сложности.
Таблица 1
|
Уровень сложности |
Номера заданий |
Максимальный первичный балл / % от максимального первичного балла за работу |
|
1-я часть
|
||
| Базовый | 1-5, 9-13, 16-21, 25-28 | 20 / 35,7 |
| Повышенный | 6-8, 14, 15, 22-24, 26 | 16 / 28,6 |
| Всего: | 36 / 64,3 | |
|
2-я часть |
||
| Высокий | 29 | 2 / 3,6 |
| 30 | 2 / 3,6 | |
| 31 | 4 / 7,1 | |
| 32 | 5 / 8,9 | |
| 33 | 4 / 7,1 | |
| 34 | 3 / 5,4 | |
| Всего: | 20 / 35,7 | |
| Итого: | 56 |
Распределение заданий и максимальный первичный балл за выполнение задания
В таблице 2 проводится сопоставление формата заданий теста ЕГЭ-2022 по химии по сравнению с 2021 г.
|
Номер вопроса в ЕГЭ-2022 |
Номер вопроса в ЕГЭ-2021 |
Комментарий |
| 1-4 | 1-4 | Совпадение по форме и содержанию |
| 5 | 5 | Новая форма вопроса |
| 6 | 7 | Совпадение |
| 7 | 8 | Совпадение |
| 8 | 9 | Совпадение |
| 9 | 10 | Совпадение |
| 10 | 11 | Совпадение |
| 11 | 12 | Совпадение |
| 12 | 13, 14 | Новая форма вопроса |
| 13 | 15 | Совпадение |
| 14 | 16 | Совпадение |
| 15 | 17 | Совпадение |
| 16 | 18 | Совпадение |
| 17 | 19 | Совпадение |
| 18 | 20 | Совпадение |
| 19 | 21 | Совпадение |
| 20 | 22 | Изменение формы вопроса |
| 21 | — | Новая форма вопроса |
| 22 | 24 | Совпадение |
| 23 | — | Новая форма вопроса |
| 24 | 25 | Совпадение |
| 25 | 26 | Совпадение |
| 26 | 27 | Совпадение |
| 27 | 28 | Совпадение |
| 28 | Новая форма вопроса | |
| 29 | 30 | Совпадение |
| 30 | 31 | Совпадение |
| 31 | 32 | Совпадение |
| 32 | 33 | Совпадение |
| 33 | 34 | Совпадение |
| 34 | 35 | Совпадение |
Выводы
-
Уменьшилось число вопросов с 35 до 34. Это произошло в результате исключения вопроса 6 (ЕГЭ-2021) и объединения вопросов 13 и 14 в один вопрос и добавления вопроса 23.
-
Уменьшился максимальный первичный балл с 58 до 56. Это произошло в результате исключения вопроса 6 (базовый уровень сложности, уменьшение на 1 балл), объединения вопросов 13 и 14 (базовый уровень сложности, уменьшение на 1 балл), снижения уровня сложности вопросов 20 и 21 с повышенного на базовый (уменьшение на1 балл каждого).
-
Принципиально изменились вопросы 5 (классификация неорганических веществ), 12 (свойства углеводородов и их функциональных производных), 21 (понятие о кислотности среды), 23 (расчёт характеристики химического равновесия с использованием табличной формы представления данных), 28 (расчётная задача базового уровня сложности).
Пособие «Химия. ЕГЭ-2022. Тематический тренинг. Задания базового и повышенного уровней сложности» от издательства Легион разработано с учетом изменений ФИПИ 2022 года.
Примеры новых заданий в егэ по химии 2022 года
Вопрос 5:
Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная).
Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) двухоснóвной кислоты; Б) средней соли; В) амфотерного гидроксида
1
NaH2PO42
Zn(OH)23
HNO24
H2SO35
H3P6
ZnO7
Zn8
NH4NO39
Fe(OH)2
Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.

Базовые знания
Гидроксидами называются вещества, которые соответствуют оксидам. Оснóвным оксидам соответствуют оснóвные гидроксиды (основания), амфотерным – амфотерные гидроксиды, кислотным – кислородсодержащие кислоты.
Амфотерным оксидам соответствуют амфотерные гидроксиды. Амфотерные оксиды образуют атомы металлов в степенях окисления +3 или +4; амфотерными являются оксиды ZnO, BeO, Al2O3, Cr2O3, Fe2O3 и оксиды некоторых других металлов.
Zn(OH)2 = ZnO + H2O2Fe(OH)3 = Fe2O3 + 3H2O
Кислотами называются сложные вещества, состоящие из атомов водорода и кислотного остатка. По составу кислотного остатка кислоты классифицируют на кислородсодержащие (H2SO4, HNO3) и бескислородные (HCl, H2S, HCN), по числу атомов водорода — на одноосно́вные (HF, HCl, HCNS) и многоосно́вные (H2CO3, H3PO4).
Солями называются продукты полного или частичного замещения атомов водорода в кислотах на катионы металла или группы NH4+ или, другими словами, соли – электролиты, при диссоциации которых образуются катионы металла (или аммония) и анионы кислотного остатка.
Соли классифицируют на:
а) средние, например: К2SO3 – сульфит калия, CuCl2 – хлорид меди(II);
б) оснóвные, например: CuOHCl – гидроксохлорид меди(II), FeOH(NO3)2 – гидроксонитрат железа(III);
в) кислые, например: NaHSO4 – гидросульфат натрия, Ca(HCO3)2 – гидрокарбонат кальция;
г) комплексные, в состав которых входит сложный катион или анион, состоящий из атома металла-комплексообразователя и лигандов, например: Na[Al(OH)4] – тетрагидроксоалюминат натрия, [Ag(NH3)2]ОН – гидроксид диамминсеребра(I).
Анализ и решение
Необходимо, во-первых, определить класс каждого из предложенных в задании веществ и, во-вторых, правильно записать ответ.
- NaH2PO4 – состоит из атомов натрия и остатка фосфорной кислоты H3PO4, класс солей. В кислотном остатке имеются атомы водорода, следовательно, соль – кислая. Ответ неверный.
- Zn(OH)2 – состоит из атомов цинка (металл) и гидроксильных групп, класс гидроксидов. Гидроксид цинка – амфотерный гидроксид (обязан знать). Ответ В – 2.
- HNO2 – азотистая кислота (обязан знать). Одноосно́вная кислородсодержащая кислота. Ответ неверный.
- H2SO3 – сернистая кислота (обязан знать). Двухосно́вная кислородсодержащая кислота. Ответ А – 4.
- H3P – летучее водородное соединение (фосфин). Ответ неверный.
- ZnO – оксид цинка, амфотерный оксид. Ответ неверный.
- Zn – металл. Ответ неверный.
- NH4NO3 – состоит из групп NH4 и остатка азотной кислоты HNO3. Соль средняя. Ответ Б – 8.
Вывод: правильные ответы найдены. Оставшийся вариант рассматривать не будем.
Ответ: 428.
Вопрос 12:
Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Основные способы получения углеводородов (в лаборатории). Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Основные способы получения кислородсодержащих органических соединений (в лаборатории).
Из предложенного перечня выберите все вещества, при взаимодействии которых с раствором перманганата калия в кислой среде образуется карбоновая кислота.
- гексен-1
- бензол
- метилбензол
- этилацетат
- уксусный альдегид
Запишите номера выбранных ответов.
Ответ: _______ .
Базовые знания
В кислой среде раствор перманганата калия KMnO4 способен окислять спирты, альдегиды, непредельные углеводороды (алкены, алкины, диены) и их производные, боковые цепи ароматических углеводородов.
Анализ и решение
Необходимо, во-первых, определить класс каждого из предложенных в задании веществ, во-вторых, проверить возможность протекания реакции и, в третьих, правильно записать ответ.
Необходимо, во-первых, определить класс каждого из предложенных в задании веществ, во-вторых, проверить возможность протекания реакции и, в третьих, правильно записать ответ.
1) Гексен-1 – алкен, должен реагировать с подкислённым раствором перманганата калия с разрывом кратной связи и образованием углекислого газа и валериановой кислоты.
CH3(CH2)3–CH=CH2 + KMnO4 + H2SO4 → CH3(CH2)3–COOH + CO2 + K2SO4 + MnSO4 + H2O
Вывод: ответ 1 – правильный.
2) Бензол. Не окисляется раствором KMnO4.
C6H6 + KMnO4 ≠
Вывод: ответ 2 – неверный.
3) Метилбензол, или толуол, — C6H5–CH3. Возможно окисление группы CH3.
C6H5–CH3 + KMnO4 → C6H5–COOH + K2SO4 + MnSO4 + H2O
Вывод: ответ 3 – правильный.
4) Этилацетат CH3COOC2H5 – сложный эфир. Не должен окисляться раствором KMnO4/
CH3COOC2H5 + KMnO4 ≠
Вывод: ответ неверный.
5) Уксусный альдегид CH3CHO, должен окисляться раствором KMnO4.
CH3CHO + KMnO4 + H2SO4 → CH3COOH + K2SO4 + MnSO4 + H2O
Ответ: 135.
Вопрос 21:
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
- Na2SO4
- Fe(NO3)2
- K2SO3
- НClO3
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
Базовые знания
При растворении электролита в воде происходит его взаимодействие с молекулами воды. В результате происходит диссоциация электролита, смещается положение равновесия диссоциации воды и изменяется кислотность среды.
При растворении кислот в результате их диссоциации образуются катионы H+ и среда становится кислой, pH < 7. В растворах сильных кислот концентрация катионов H+ больше, чем в растворах более слабых кислот, и величина pH меньше. Например, в растворах с концентрацией 0,1 моль/л для соляной кислоты pH ≈ 1, для уксусной кислоты рН ≈ 2,9.
При растворении щелочей образуется большое количество гидроксид-ионов OH–, pH > 7.
При диссоциации солей образующие их катионы и анионы будут взаимодействовать с молекулами воды. Гидролизом называется реакция обменного взаимодействия соли и воды, в результате протекания которой смещается положение равновесия диссоциации воды и изменяется кислотность среды. Степень гидролиза, как правило, составляет доли процента и только в отдельных случаях достигает заметных значений. Наиболее выражены процессы гидролиза солей, в состав которых входят катионы слабых оснований и/или анионы слабых кислот. В растворах солей, в состав которых входят катионы слабых оснований, среда кислая, pH < 7. В растворах солей, в состав которых входят анионы слабых кислот, среда щелочная, pH > 7. Чем более слабым является основание или кислота, образующие соль, тем больше будет степень гидролиза и больше изменение кислотности среды и величины pH. Например, для раствора AlCl3 с молярной концентрацией 0,1 моль/л рН ≈ 3,1, раствора NH4Cl ≈ 5.
Вывод:
- необходимо определить классы веществ и возможность протекания гидролиза по формулам веществ;
- в растворах растворимых оснований среда щелочная, в растворах кислот – кислая, причем концентрация катионов H+ в растворах более слабых кислот будет меньше, а величина рН – больше;
- определить относительную силу катионов, взаимодействующих с водой: кислотность среды будет тем больше отклоняться от нейтральной в кислую сторону (следовательно, рН меньше), чем более слабым основанием образована соль;
- определить относительную силу анионов, взаимодействующих с водой: кислотность среды будет тем больше отклоняться от нейтральной в щелочную сторону (следовательно, рН больше), чем более слабой кислотой образована соль;
- для солей, которые образованы сильными основаниями и сильными кислотами условно будем считать среду нейтральной.
Решение
- Na2SO4 – сульфат натрия. Средняя соль, образована сильным основанием NaOH и сильной средней кислотой, гидролизу не подвергается. Среда – приблизительно нейтральная
- Fe(NO3)2 – нитрат железа(II). Средняя соль, образован слабым основанием Fe(OH)2 и сильной азотной кислотой HNO3. Гидролиз по катиону Fe2+, среда – кислая.
- K2SO3 – сульфит калия. Средняя соль, образована сильным основанием KOH и кислотой средней силы H2SO3. Гидролиз по кислотному остатку (по аниону), среда – щелочная.
- НClO3 – хлорноватая кислота. Сильная кислота. Среда – кислая.
Понятно, что концентрация катионов H+ будет наибольшей в растворе HClO3, следовательно, pH этого раствора будет иметь наименьшее значение.
Кислотность раствора Fe(NO3)2 будет меньше, чем раствора HClO3, потому что степень гидролиза редко бывает большой.
В растворе K2SO3, имеющем щелочную среду, величина pH будет наибольшей.
Вывод: величина рН будет увеличиться в последовательности
HClO3 < Fe(NO3)2 < Na2SO4 < K2SO3
Ответ: 4213.
Вопрос 23:
Обратимые и необратимые химические реакции. Химическое равновесие. Расчёты количества вещества, массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ.
В реактор постоянного объёма поместили некоторое количество оксида серы(IV) и кислорода. В результате протекания обратимой реакции в реакционной системе
2SO2(г) + O2(г) ⇄ 2SO3(г)
установилось химическое равновесие.
Используя данные, приведённые в таблице, определите серы (X) и исходную концентрацию кислорода (Y).
Реагент SO2(г) O2(г) SO3(г) Исходная концентрация, моль/л 0,6 Равновесная концентрация, моль/л 0,3 0,4
Выберите из списка номера правильных ответов.
Анализ и решение
Пусть объём системы V = 1 л, тогда изменение концентрации численно равно изменению количества вещества.
1) Вычисляем изменение количества вещества одного из реагентов (SO3):
∆n(SO3) = 0,4 – 0 = 0,4 моль
2) По изменению концентрации SO3 по уравнению реакции вычисляем количество вещества, вступившее в реакцию, других реагентов (SO2 и O2):

3) Вычисляем количество вещества оксида серы(IV) в состоянии равновесия и исходное количество кислорода:
n(SO2)равн. = 0,6 – 0,4 = 0,2 моль
n(O2)исх. = 0,3 + 0,2 = 0,5 моль
и переносим в таблицу (показаны полужирным шрифтом).
Вывод: X = 0,2 моль/л (2), Y = 0,5 моль/л (5).
Ответ: 25.
Вопрос 28:
Расчёты массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ. Расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного. Расчёты массовой доли (массы) химического соединения в смеси.
Из 150 кг природного известняка при взаимодействии с азотной кислотой был получен нитрат кальция массой 196,8 кг. Вычислите массовую долю (%) примесей в указанном известняке. (Запишите число с точностью до целых.)
Ответ: ____ %.
Базовые знания
Решение любой расчётной задачи по химии подчиняется достаточно строгому алгоритму.
1) Составить уравнение реакции.
2) Понять главный вопрос задачи.
3) Установить логическую связь: количество какого из веществ необходимо найти, по количеству какого вещества производим расчёт.
4) Произвести расчёты и ответить на главный вопрос задачи.
Решение:
1) Составляем уравнение реакции:
CaCO3 + 2HNO3 = Ca(NO3)2 + H2O + CO2↑
2) Главный вопрос задачи – найти массовую долю примесей в известняке.
Массовая доля вычисляется по формуле
ω = mчасти/mвсего образца
Массовая доля примесей
ω(примеси) = 100% — ω(CaCO3),
Вывод: необходимо найти количество CaCO3, расчёт производим по Ca(NO3)2.
3) Производим расчёт и находим количество и массу CaCO3.

а) находим количество Ca(NO3)2
M(Ca(NO3)2) = 164 г/моль
n(Ca(NO3)2) = m/M = 196,8/164 = 1,2 моль
б) находим количество и массу CaCO3
x = 1∙1,2/1 = 1,2 моль CaCO3
M(CaCO3) = 100 г/моль, m(CaCO3) = 1,2∙100 = 120 г
4) Находим массовую долю примесей.
ω(CaCO3) = 120/150 = 0,8, или 80%
ω(примеси) = 100 – 80% = 20%.
Ответ: 20.