Фейерверк
Да, фейерверк по праву может считаться самым ярким изобретением. Он не перевернул мир – он сделал его прекраснее. Небо взрывается яркими огнями, шарами, цветами, звезды падают и летят прямо на наблюдающих за этим потрясающим зрелищем… Расцвеченный огнями, играющий переливами небосвод в эти минуты показывает нам, как прекрасна Вселенная где-то там, в космосе, с ее звездами и взрывами, туманностями и астероидами. Поистине великолепная картина, созданная руками человека.

Огонь был «в почете» у многих древних народов и использовался на праздниках. Сначала украшение праздников огнем было примитивным: разводили костры, использовали маленькие огоньки, создавая подобие иллюминации. В Древней Греции и Риме был праздник Лампадарио, на котором чествовали богиню Минерву и бога Вулкана. А поблагодарить Прометея, по преданию, давшего человечеству огонь, было просто необходимо! Поэтому греки и римляне в этот праздник сжигали огромное количество светильников и надеялись на милость богов. Подобный праздник под названием «светильники» был и у египтян.
Древний Китай – родина фейерверков. Ученые считают, что именно китайцы времен династии Хань (206 – 220 гг. до н. э.) впервые заметили странное свойство бамбука: подожженный, он начинал потрескивать, а затем громко взрывался. Этот взрыв устрашающе воздействовал на суеверных китайцев, поэтому последние решили использовать его для защиты от темных сил: считалось, что злые духи тоже боятся громких звуков, значит, таким образом их можно отпугнуть… Так горящий бамбук стал обязательной частью важных событий в Китае: свадеб, похорон, религиозных обрядов.
Добавить порох
Горящий бамбук был только предтечей современного фейерверка, который смог полноценно «народиться» на свет только с изобретением пороха. Хотя есть в китайской культуре несколько легенд, связанных с фейерверком. Одна из них гласит, что он был изобретен случайно одним из поваров китайской армии, который смешал селитру, серу и древесный уголь, а затем случайно уронил смесь в огонь. Пламя окрасилось в яркие цвета, которые, как ни странно, повара не испугали, а подвигли на эксперименты: он решил начинить смесью бамбук и поджечь его. Взрыв был устрашающим. Смесь из трех ингредиентов назвали «Хо Яо» («химический пожар»), и именно она, по преданию, явилась основой первого фейерверка.
Предание преданием, а все-таки великое изобретение китайских алхимиков порох дало жизнь фейерверку. Принято считать, что порох был изобретен во времена династий Суи и Танг (581 – 907 годы). Новая смесь открыла перед экспериментаторами новые возможности. И новаторы не преминули ими воспользоваться: они начинили бамбук порохом и подожгли его. Мы можем только догадываться, какой огромной впечатляющей силой обладали экспериментальные взрывы! Рационализаторы оценили способности пороха по достоинству и решили, что бамбук – не совсем подходящий материал для устройства шоу, поэтому заменили его трубками из бумаги и дополнили тканевыми фитилями.
Для войны и развлечений
Пытливые умом китайцы к ХIII веку разработали новый вариант светового представления. «Земляная крыса» — такое непоэтическое название носила модификация. И немудрено: ее предполагалось использовать в военных целях.
Конструкция была проста: один конец трубки фейерверка поджигался, а второй оставался открытым. В результате нововведения взрыва не получалось, зато выходящий из открытого конца газ толкал конструкцию, заставляя ее двигаться по земле с безумными маневрами. Армия противника приходила в замешательство; лошади пугались, сбрасывали всадников, поворачивали назад, а китайцы шли в атаку.
«Земляная крыса» стала не только достоянием военных, но и простого люда. В «крысу» поместили заряд взрывчатого вещества, направили вверх, добавили огня и… о, чудо! Фейерверк покорил небо!
Итальянская роскошь
Долгое время фейерверк радовал своим великолепием только жителей Азии. Но в 1292 году из путешествия по Востоку вернулся в Италию небезызвестный Марко Поло. Помимо ярких впечатлений и наблюдений, итальянец привез на родину секрет фейерверка. Можно сказать, что именно с его почина фейерверк начал свое триумфальное шествие по миру.
Горячие итальянцы проявили интерес к новинке. Они не только заимствовали у китайцев технологию запуска фейерверка в воздух, но и привнесли новые технологии. В частности, в результате экспериментов с взрывчатыми смесями итальянцы получили множество новых видов фейерверочного взрыва – «фонтан», «вертушка», «конус», «колесо», «римская свеча» и такой привычный для нас «бенгальский огонь». Искусство фейерверка стало для Италии настолько значимым, что «повелители огня» даже устраивали соревнования на самое красочное шоу. В XIV – XV веках итальянские мастера считались лучшими среди устроителей огненного зрелища.
Особенно красивой фигурой фейерверочного искусства периода 1500 – 1700 годов был «дракон». Он представлял собой каркас из дерева, покрытый папье-маше и набитый зарядами. Когда заряды поджигали, создавалась иллюзия огненного дыхания чудовища. Часто двух драконов ставили друг пред другом и веселили народ своеобразной «битвой» мифических существ.
Конечно, производство фейерверков не было дешевым, поэтому баловали народ подобными развлечениями нечасто. Фейерверки запускали в воздух только по особым случаям: коронация царствующих особ, их дни рождения и большие религиозные праздники.
Короли и шутихи
От Италии потянулись огненные нити по всей Европе. Фейерверк быстро завоевал популярность среди знатных особ, которые показывали свое богатство и власть, устраивая на праздники грандиозные шоу. В Англии достижения пиротехнического искусства были впервые продемонстрированы в 1486 году в честь женитьбы короля Генриха VII. А Елизавета I была настолько очарована разлетающимися огнями, что во времена своего правления ввела новый титул – «Повелитель Огня Англии», которым награждали отличившихся пиротехников.
В Россию огненное искусство пришло раньше, вместе с использованием пороха для артиллерийских орудий – в конце XIV века. При Иване Грозном существовала должность «порохового заведующего», который отвечал и за фейерверки. Позже царь Михаил Федорович (1596 – 1645 гг.) учредил Потешную палату, заседатели которой отвечали и за организацию «огненных потех». Расцвет искусства фейерверка в России пришелся на время правления Петра I. Вернее, не столько пришелся, сколько пришел вместе с царем.
При Петре I огненные потехи стали делом государственной важности. Есть мнение, что ни до, ни после Петра фейерверочное искусство в России не переживало подобного взлета. Например, известно, что именно Петр I «закатил» самый яркий фейерверк, который продолжался целую неделю (поводом стало наступление нового века). В 1680 году в Москве было учреждено специальное ракетное заведение, а для устройства красочного зрелища при российском дворе не единожды привлекались иностранные мастера.
Работа специального ракетного заведения позволила усовершенствовать качество и состав фейерверочных зарядов. Теперь при изготовлении праздничных изделий стали использовать искристые, искристо-форсовые, серные, селитро-серные составы с добавлением окрашивающих солей. Производство фейерверков в России в петровское время было значительным по своим масштабам, и такую потеху могли позволить себе не только царские особы, но и просто зажиточные люди – знать, купцы, дворяне, служилые.
Искусство химии
Фейерверк стал неотъемлемой частью любого торжества. В начале XIX века при запуске фейерверков стали использовать ракеты с парашютом и боевые ракеты. Оба новшества сыграли на усиление зрелищности взрывов: во-первых, теперь огни дольше находились в воздухе, во-вторых, боевые ракеты дали возможность сделать огни мощнее за счет увеличения начинки.
Между прочим, вплоть до 1830 года огни фейерверка не могли похвастать цветовой гаммой – они были только белыми и оранжевыми. Открытие бертолетовой соли в корне поменяло ситуацию.
Итальянские мастера фейерверков выяснили, что ее соединение с солями металлов окрашивают пламя в разные цвета: селен – в голубой, натрий – в желтый, калий дает фиолетовый цвет, а магний горит в чистом виде, и его используют при запуске фейерверочных ракет.
Вчера и сегодня
Во второй половине XIX века количество фабрик, занимавшихся производством фейерверков, резко возросло. Это было связано с тем, что красочные снопы огня в небе завоевали популярность, спрос на фейерверки был массовым, и его нужно было удовлетворить. Уже в начале ХХ века небольшие огненные представления не были редкостью и устраивались как организациями, так и частным лицами.
Первый военный салют в СССР был дан 5 августа 1943 года в Москве в честь освобождения Красной Армией Орла и Белгорода. Потом это стало традицией – отмечать победы салютами. И, конечно, самый большой из них был дан 9 мая 1945 года.
Самым крупным изготовителем пиротехники на сегодняшний день является Китай. Производители постоянно работают над улучшением составов, разработкой новых конструкций и улучшениями зрелищного эффекта и обмениваются опытом. Что ж, скажем им «спасибо» за маленькое чудо в небе и… ждем новогоднего представления!
Обыкновенная История — Фейерверк
Поделиться в соцсетях
Участник Всероссийкой олимпиады «Металлы и Неметаллы»
| ФИО участника: | Сахабиева Алиса Маратовна |
| Учебное заведение: | Гимназия 22 |
| Результат: | 9/10 |
| Диплом: |

Скачать PDF |
Результат:
| № | Вопрос | Варианты ответа | Ответ | Правильный ответ | Баллы |
|---|---|---|---|---|---|
| 1. | Фейерверк по праву может считаться самым ярким изобретением. Поистине великолепная картина, созданная руками человека. Фейерверк стал неотъемлемой частью любого торжества. До 1830 года огни фейерверка не могли похвастать цветовой гаммой – они были только белыми и оранжевыми. Какой металл академик А. Е. Ферсман назвал «металлом красных огней»? |
|
Стронций | ДА | 1 |
| 2. | Известный «автомобильный король» Форд сказал «Если бы не было …, — не было бы автомобиля». О каком металле говорил Форд? |
|
Ванадий | ДА | 1 |
| 3. | Чистое золото – довольно мягкий металл, его можно согнуть или поцарапать даже голыми руками, поэтому золотые ювелирные украшения изготавливают не из чистого золота, а из его сплавов с другими металлами. В любом золоте 585 пробы (в каратной системе проб она обозначается как 14 карат) содержится 58,5% чистого золота, остальное – лигатура (сплав). Как называется сплав золота с серебром, платиной и палладием. |
|
Белое золото | ДА | 1 |
| 4. | Император Наполеон III на банкете велел подать для почётных гостей приборы из очень дорогого серебристо белого металла. А всем прочим было обидно до слёз: им пришлось пользоваться обычной золотой и серебряной посудой. Из чего были изготовлены вилки? |
|
Алюминий | ДА | 1 |
| 5. | Известно, что падение Рима вызвано многими социальными, политическими и экономическими причинами. Но американские учёные – токсикологи считают, что в падении Рима повинен металл. Он входил в состав посуды, косметических красок, а также из него были сделаны трубы водопроводов. Люди вымирали и обнаруженные останки древних римлян содержали большое количество этого метала. Какой металл, по мнению учёных США, повинен в гибели Рима? |
|
Свинец | ДА | 1 |
| 6. | Какой элемент сыграл роковую роль в жизни Наполеона Бонапарта? |
|
Ртуть | НЕТ | 0 |
| 7. | В 1827 году немецкий ученый Ф. Велер получил металл, внешне похожий на серебро, но легче его в 4 раза. В 1889 г в Лондоне Д.И. Менделееву в знак признания его заслуг в качестве особо ценного подарка были вручены весы, сделанные из золота и этого металла. Назовите этот металл? |
|
Алюминий | ДА | 1 |
| 8. | Этот элемент был открыт в XIX веке Французским химиком Б. Куртуа в золе морских водорослей, а помог ему в этом его любимый кот, который разбил бутылки с суспензией золы морских водорослей и серной концентрированной кислоты. Какой галоген помог открыть ученому кот? |
|
Йод | ДА | 1 |
| 9. | При Петре I вручалась медаль за пьянство введенная в 1714 году, цель которого была борьба против пьянства. |
|
Из чугуна | ДА | 1 |
| 10. | Никель широко используют при изготовлении различной химической аппаратуры, в кораблестроении, в электротехнике, при изготовлении щелочных аккумуляторов, для многих других целей, находит широкое применение как катализатор самых разных химических реакций. Кто впервые стал применять никель? |
|
Ювелиры | ДА | 1 |
| Результат: | 9/10 |

Ответственность за размещаемый пользователями контент касающийся конкурсов, для педагогов и детей, Всероссийских конкурсов, а также конкурсов, для детей и дошкольников, полностью лежит на них. Администрация сайта, оказывает помощь в проблемах связанных с работой и содержанием сайта. Вы обнаружили, что на нашем сайте используется чужой контент, пожалуйста сообщите о данном факте администрации сайта, заполнив специальную форму!

Приветствую всех участников и зрителей на еженедельном 2D MiniComps
Задание: Нарисовать новогодний фейерверк
Тема: Фейерверк
Условия:
Фейерверк по праву может считаться самым ярким изобретением. Он не перевернул мир – он сделал его прекраснее. Небо взрывается яркими огнями, шарами, цветами, звезды падают и летят прямо на наблюдающих за этим потрясающим зрелищем… Расцвеченный огнями, играющий переливами небосвод в эти минуты показывает нам, как прекрасна Вселенная где-то там, в космосе, с ее звездами и взрывами, туманностями и астероидами. Поистине великолепная картина, созданная руками человека.
Для участия в конкурсе каждый художник должен представить:
1) финальную картинку
2) один лист с нарезкой этапов создания этой картинки.
Правила участия и обсуждение конкурса — здесь.
Как загрузить работу?
Знание правил обязывает каждого, потому соблюдаем 
Обратите внимание на наше нововведение: теперь каждый желающий может на протяжении конкурсной недели выставлять этапы в общем ВИПе, где можно обсуждать, делиться мнениями и советами при необходимости. Повторяю, что это не обязательный пункт для участия в конкурсе и создается ВИП исключительно для удобства участников.
Общий WIP — здесь.
В этой теме выкладываем конкурсные работы до дедлайна, 29 декабря, в 24.00 по Москве
Удачи всем участникам!
Дата сообщения: 23.12.2013 21:16 [#] [@]
С Новым Годом!!!
Прикрепленное изображение (вес файла 375.7 Кб)
Прикрепленное изображение (вес файла 219.3 Кб)
Дата сообщения: 03.01.2014 18:51 [#] [@]
С новым годом, друзья и коллеги по перу!)))) 
заставила себя нарисовать *все-как-положено*. черно-белое, потом покраска. поэтому наверно слегка зашкалила контрастность.
Прикрепленное изображение (вес файла 498.6 Кб)
Прикрепленное изображение (вес файла 332.9 Кб)
Прикрепленное изображение (вес файла 235 Кб)
Прикрепленное изображение (вес файла 165 Кб)
Прикрепленное изображение (вес файла 133.4 Кб)
Дата сообщения: 03.01.2014 22:51 [#] [@]
Всех с новым годом и рождеством
Прикрепленное изображение (вес файла 598.8 Кб)
Прикрепленное изображение (вес файла 378.9 Кб)
Дата сообщения: 06.01.2014 09:59 [#] [@]
всех с наступившим! 
фейерверка творчества всем в наступившем году!
Прикрепленное изображение (вес файла 573 Кб)
Прикрепленное изображение (вес файла 430.7 Кб)
Дата сообщения: 06.01.2014 21:31 [#] [@]
Happy new year!
Прикрепленное изображение (вес файла 168.3 Кб)
Прикрепленное изображение (вес файла 137.5 Кб)
Дата сообщения: 08.01.2014 03:36 [#] [@]
фейерверк глазами лемура
Прикрепленное изображение (вес файла 575.5 Кб)
Прикрепленное изображение (вес файла 505 Кб)
Прикрепленное изображение (вес файла 229.2 Кб)
Дата сообщения: 13.01.2014 12:15 [#] [@]
Стартовало голосование, через неделю будут известны результаты!!!
Всем спасибо, и надеемся, что вы присоединитесь к нам в новых конкурсах
Дата сообщения: 13.01.2014 07:06 [#] [@]
2D MiniComps №122 «Фейерверк»
1-е место Gaudi — 7 баллов рейтинга + нашивка победителя на арене
2-е место ЮК — 6 баллов рейтинга
3-е место NJ — 5 баллов рейтинга
Поздравляем участников и ждём на следующем 2D MiniComps!
Дата сообщения: 21.01.2014 11:14 [#] [@]
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ПАЛИТРА ОГНЯ
Городская научно-практическая конференция
«Фестиваль научных идей»
Выполнили:
Иващенко Евгений
Стулов Виктор
Ученики 10а класса
МОУ СОШ №3 г. Лыткарино
Руководитель: Филина Н.В.
учитель химии
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ВВЕДЕНИЕ
Фейерверк по праву может считаться самым ярким изобретением. Он не
перевернул мир – он сделал его прекраснее. Небо взрывается яркими огнями,
шарами, цветами, звезды падают и летят прямо на наблюдающих за этим
потрясающим зрелищем. Расцвеченный огнями, играющий переливами небосвод
в эти минуты показывает нам, как прекрасна Вселенная где-то там, в космосе, с
ее звездами и взрывами, туманностями и астероидами. Поистине великолепная
картина, созданная руками человека.
Наша тема исследований актуальна, потому что научно-технический процесс в
наше время не стоит на месте, он идёт вперёд семимильными шагами, и чтобы
идти с ним в ногу надо познавать новое то, что происходит в сфере науки.
Сейчас во всем мире очень популярно изучение металлов и их соединений. Ведь
в наше время почти всё, что нас окружает, состоит из металла, и открытие новых
его свойств и их изучение – важнейшая тема столетия.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Исходя из вышеизложенного, сформулирована цель исследовательской работы: опытным
путём определить, какие химические вещества в ходе горения образуют необычный для
пламени цвет.
Задачи исследования:
Изучить литературные источники по теме;
Выяснить, горение каких химических веществ способно образовывать цветное пламя;
Изучить методику получения цветного пламени;
Провести химический эксперимент с исследуемыми образцами химических веществ;
Найти практическое применение цветному пламени;
Проанализировать полученные результаты и сделать выводы.
Объект исследования: пламя огня.
Предмет исследования: процесс горения химических веществ, в пламени огня.
Методы исследования:
Теоретические: изучение литературы, обобщение, анализ;
Эмпирические: наблюдение, фотографирование, сравнение;
Экспериментальные: химический эксперимент, лабораторные опыты, анализ результатов.
Гипотеза: предполагаю, что цвет пламени зависит от химических веществ, которые в
Практическая значимость работы: результаты, полученные в ходе эксперимента
можно использовать для определения химического состава горных пород и минералов.
нём сгорают.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ИСТОРИЯ ФЕЙЕРВЕРКА
Фейерверк (немецкого слова Feuerwerk, от Feuer —
огонь и Werk — дело, работа) — декоративные огни
разнообразных цветов и форм, получаемые при
сжигании пиротехнических составов.
Фейерверк представляет собой красочные и
яркие огни, разлетающиеся в воздухе при сжигании
специальных пороховых составов. Чаще всего
фейерверк используют во время праздников или
торжеств. В древнем Китае, примерно в 210 году до
нашей эры, были впервые изобретены фейерверки.
Китайцы обратили внимание на то, как
потрескивают и громко взрываются зажженные
палочки бамбука. Этот громкий звук сильно пугал
людей, и тогда они решили использовать горящий
бамбук в ритуалах, отпугивающих злые духи.
Позднее, в 400-500 годах до н.э., Южные и
Северные правящие династии стали применять
фейерверки в религиозных церемониях.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ФЕЙЕРВЕРК В
РОССИИ
Первый документально подтвержденный
российский фейерверк был устроен в 1674
году в городе Устюг во время царствования
отца Петра I. Именно при Петре появилась
традиция новогоднего фейерверка — только
при нем этот праздник стал официальным. Он
усовершенствовал искусство фейерверков,
лично создавая сложнейшие пиротехнические
фигуры. Скоро салюты стали частью
празднований Нового года, побед в битвах,
религиозных действий.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ВЕЩЕСТВА, ИСПОЛЬЗУЕМЫЕ
ДЛЯ СОЗДАНИЯ ФЕЙЕРВЕРКОВ
«Звезды», содержащиеся в составе пиротехники содержат
металлический порошок или соли металлов, которые дают
фейерверк красок.
Алюминий (Al) – это основной компонент для создания белых и
серебряных искр и огней.
Барий (Ba) – создает зеленый цвет в фейерверках и может
дополнить любой другой цвет и помочь стабилизировать другие
летучие элементы.
Медь (Cu) производит сине-зеленый цвет в фейерверке, а
галогениды меди используются для создания оттенков синего.
Кальций (Ca). Используется для создания глубоких оттенков
оранжевого цвета фейерверка
Хлор (Cl) является важным компонентом для многих
окислителей в фейерверках. Некоторые из солей металлов,
создающих цвет содержат хлор. Присутствие ионов хлора в
продуктах горения цветных составов с вышеуказанными
цветообразующими компонентами — обязательное условие. Без
хлора может обойтись только желтый огонь на основе натрия, так
как он и без того дает насыщенное окрашивание, в остальных
случаях в отсутствие хлора цвета пламени получаются блеклыми и
невыразительными.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
ПРАКТИЧЕСКАЯ
ЧАСТЬ
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Опыт 1
ПОЛУЧЕНИЕ ЦВЕТНОГО ПЛАМЕНИ
Цель: опытным путём получить цветное пламя, используя соли металлов и металлы
(магний, медь).
Оборудование: мерные стаканы, мерный цилиндр, воронка, стеклянные палочки, весы,
разновесы, спиртовка, спички, нихромовая проволока, медная проволока, весы, разновесы,
магний, растворы: дистиллированная вода; соляная кислота, соли: фторид лития (I); хлорид
натрия (I); хлорид калия (I); хлорид кальция (II); хлорид бария (II); хлорид меди (II).
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Результат
ы
Борная кислота
Сульфат меди
Хлорид
лития
Хлорид
натрия
Хлорид
кальция
Хлорид калия
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Опыт 2
Горение медной проволоки
Загибаем конец медной проволоки, делая петлю, увеличивая площадь соприкосновения
веществ. Смачиваем её в соляной кислоте и вносим в пламя спиртовки. Наблюдаем
окрашивание пламени в голубой цвет с зеленоватым оттенком.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Опыт 3
Горение магния
Стружку магния, удерживая пинцетом, вносим в пламя спиртовки. Наблюдаем
окрашивание пламени в ярко белый цвет.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Опыт 4
ОПРЕДЕЛЕНИЕ ИОНОВ МЕТАЛЛОВ, ВХОДЯЩИХ В ХИМИЧЕСКИЙ СОСТАВ МИНЕРАЛОВ
Цель: Определить ион металла, входящий в химический состав минерала, используя пламя
спиртовки.
Оборудование: спиртовка, сухое горючее, спички, пинцет, фарфоровые чашки,
минералы: магнезит, сильвин, галит
Ход работы
Измельчаем минералы. В фарфоровые чашки раскладываем сухое горючее, поджигаем и
вносим соответствующий измельчённый минерал.
Mg+2
K+
Na+
Магнезит
Сильви
н
Гали
т
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
Заключение
В ходе исследования мы узнали много интересных фактов о пламени и различных металлах.
Проделанная нами работа позволила определить на собственном опыте, в какие цвета
окрашивают металлы и ионы металлов, входящие в состав солей, пламя при горении.
Доказано, цвет пламени огня зависит от веществ, которые в нем сгорают. Метод по
обнаружению некоторых химических элементов по различному окрашиванию пламени можно
применять при исследовании химического состава минералов.
Окраска пламени зависит от наличия раскаленных паров свободных металлов, получающихся в
результате термического разложения солей.
Реакции окрашивания пламени удаются хорошо только с летучими солями (хлоридами).
Цветной огонь используются для снаряжения фейерверочных изделий
Огонь очень опасен! Его всегда нужно контролировать, нельзя оставлять без присмотра. Он
способен и очень навредить. При выполнении опытов с применением огня, необходимо
соблюдать технику безопасности при работе в лаборатории.
Научно-исследовательская работа учащихся 10 класса «Палитра огня» (химия)
СПАСИБО ЗА ВНИМАНИЕ
Фейерверк по праву может считаться самым ярким изобретением человечества, которое, конечно, не перевернуло мир, но сделало его прекраснее
Слово “фейерверк” имеет немецкие корни: от das Feuer — “огонь”, das Werk — “дело”, “огнедействие”. Но пришел он в современный мир совсем не из Германии, а из Древнего Китая. Ученые считают, что именно китайцы времен династии Хань (206 год до н.э. — 220 год н.э.) впервые заметили интересное свойство бамбука: подожженный, он начинал потрескивать, а затем громко взрывался. Изначально его использовали для отпугивания злых духов.
Добавить порох
Первый снаряд, отдаленно напоминающий современный вариант фейерверка, как гласит легенда, был изобретен случайно одним из оружейников китайской армии, имя которого затерялось в веках, как это частенько и случается с гениальными людьми. По каким-то своим надобностям он смешал селитру, серу и древесный уголь, а затем случайно уронил все это в плавильную печь. Пламя тут же окрасилось в яркие цвета, а оружейник решил поэкспериментировать дальше — набил аналогичным составом стебель бамбука и поджег его. Смесь из трех ингредиентов назвали “Хо Яо” (“химический пожар”).
Предание преданием, а все-таки современную жизнь фейерверку дал порох. Принято считать, что он был изобретен во времена династий Суи и Танг (581—907 годы). Рационализаторы тут же оценили возможности взрывчатого вещества, но решили, что бамбук — не совсем подходящий материал для устройства шоу, поэтому заменили его трубками из бумаги и дополнили тканевыми фитилями.
Для войны и развлечений
В ХIII веке был разработан новый вариант светового представления, носивший весьма непоэтическое название — “земляная крыса”. Причем изначально она предназначалась для военных действий. Бороться с вражеской армией при помощи фейерверков глупо, скажете вы. И однозначно ошибетесь. Но обо всем по порядку.
Конструкция “крысы” была проста: один конец трубки фейерверка поджигался, а второй оставался открытым. В отсутствие замкнутого пространства взрыва не получалось, но выходящий из открытого конца снаряда газ толкал конструкцию, заставляя ее двигаться по земле и выписывать непредсказуемые кренделя. Учитывая, что основной ударной силой в то время была конница, эффект от применения “земляной крысы” был весьма впечатляющим. Лошади пугались искр, бесились, вставали на дыбы и сбрасывали всадников. Тем не менее очень быстро применение “земляной крысе” нашли и в сфере развлечений. Снаряд просто укрепляли на подставке, чтобы не дергался, и направляли вверх.
Итальянская роскошь
Долгое время фейерверк радовал своим великолепием только жителей Азии. Но в 1292 году из путешествия по Востоку вернулся в Италию небезызвестный Марко Поло. Помимо ярких впечатлений и наблюдений, итальянец привез на родину секрет фейерверка. Можно сказать, что именно с его почина фейерверк начал свое триумфальное шествие по миру.
В Италии и Германии даже формировались пиротехнические школы, которые соперничали между собой. Но все же победа осталась за жителями Средиземноморья. Итальянцы не только позаимствовали у китайцев технологию запуска фейерверка в воздух, но и привнесли свои изменения в конструкцию. Так появилось множество видов фейерверочного взрыва — “фонтан”, “вертушка”, “конус”, “колесо”, “римская свеча” и такой привычный для нас “бенгальский огонь”.
Особенно красивой фигурой фейерверочного искусства был “дракон”. Он представлял собой каркас из дерева, покрытый папье-маше и набитый зарядами. Когда их поджигали, создавалась иллюзия огненного дыхания чудовища. Часто двух драконов ставили друг пред другом и веселили народ своеобразной битвой мифических существ.
В XIV—XV веках именно итальянские мастера считались лучшими пиротехниками в мире. Любопытный факт: на самом деле многие из современных ведущих американских компаний, которые выпускают фейерверки или занимаются фейерверк-шоу, принадлежат потомкам древних мастеров — это семьи Груччи, Роцци и Дзамбелли. Не мафия, но все же…
Короли и шутихи
От Италии “огненные нити” протянулись по всей Европе. В Англии достижения пиротехнического искусства были впервые продемонстрированы в 1486 году в честь женитьбы короля Генриха VII. Его сын Генрих VIII также отпраздновал фейерверком свою свадьбу с Анной Болейн. Дочь Генриха VIII и Анны Болейн королева Елизавета I так любила огненные забавы, что учредила специальную должность при дворе — повелитель огня.
В Россию фейерверки пришли в конце XIV века. При Иване Грозном существовала должность “порохового”, который отвечал и за пиротехнику. Позже царь Михаил Федорович учредил с этими же целями Потешную палату. Но настоящий расцвет пришелся на время правления Петра I, который был просто без ума от таких мероприятий. Более того, огненные потехи стали делом государственной важности. Однажды они продолжались целую неделю. Страшно даже представить, сколько денег в буквальном смысле слова вылетело в трубу.
В 1680 году в Москве было учреждено специальное ракетное заведение, работа которого позволила усовершенствовать качество и состав фейерверочных зарядов. При их изготовлении стали использовать фосфорные, серные, селитро-серные составы с добавлением окрашивающих солей. Производство фейерверков фактически поставили на поток. И это сделало их доступными по цене не только для дворянства.
При последующих российских монархах традиции крепли и развивались. Причем, начиная с Елизаветы Петровны, в создании сценария светового шоу обязательно участвовала Академия наук. В частности, химик Михаил Ломоносов и его ученик Василий Клементьев. Фейерверки, которые устраивали для императорской семьи и знатных особ, были столь грандиозными, что вгоняли иностранцев в самый настоящий ступор. В представления обязательно вкладывался замысловатый сюжет (как правило, прославляющий правящую династию и силу государства). А чтобы суть происходящего была доступна каждому, издавались пригласительные с подробными разъяснениями действий и аллегорий — нечто вроде современных театральных программок. Накануне шоу информация публиковалась отдельными изданиями с гравюрами и даже дублировалась в “Санкт-Петербургских ведомостях”.
В начале XIX века при запуске фейерверков стали использовать ракеты с парашютом и боевые ракеты. Оба новшества сыграли на усиление зрелищности: во-первых, теперь огни дольше находились в воздухе, во-вторых, сами взрывы стали мощнее за счет увеличения объема порохового заряда.
Химия цветов
Вплоть до 1830 года огни фейерверка не могли похвастать цветовой гаммой — они были либо белыми, либо оранжевыми. В корне поменяло ситуацию открытие бертолетовой соли. Итальянские мастера выяснили, что ее соединение с солями металлов окрашивает пламя в разные цвета: селен — в голубой, натрий — в желтый, калий — в фиолетовый.
Современные фейерверки отличаются еще большим цветовым разнообразием. Для получения красных огней используются соли стронция и лития, для оранжевых — соли кальция. Золотой оттенок дает железная окалина вкупе с углеродом и древесным углем, желтый — соединения натрия. Многообразие зеленого — заслуга хлора и бария, а за голубой окрас отвечает медь. Кстати, во всем многообразии цветов вы до сих пор не встретите синий. К сожалению, даже после тысячи лет существования фейерверков никто не нашел идеального состава для его создания.
ЛЮБОПЫТНО
Самым масштабным признано новогоднее шоу в честь встречи 2014 года в Дубае — оно даже попало в Книгу рекордов Гиннесса. Одновременно было запущено 450 тысяч фейерверков. Залпы производились из 400 точек, расположенных на протяжении 100 километров вдоль береговой линии административного центра эмирата.
bebenina@sb.by
Подборка по базе: Студенттік конференция 2023.pdf, Турмуханова Нурсауле РЯЛ 301 конференция.docx, Ядова К. 05.06. Инженерные сети. Городская водопроводная сеть, к, Реферат Понятие «устойчивое развитие». Конференция ООН по устойч, Он-лайн Конференция.docx, Международная научно-практическая конференция молодых ученных ст, Информационное письмо Конференция 30.11.2021.doc, Сценарий Городская боль 2.docx, Б.Толкын,И.Азиза Конференция.docx, Положение конференция ЦАТТ.docx
Городская научно-практическая конференция
«В мир поиска, мир творчества, мир науки»
Палитра огня
Выполнил:
Рымарев Ефим
ученик 8а класса
МОУ «СОШ №2 г. Свирска»
Руководитель: Полетанская Е.В.
учитель химии и биологии
МОУ «СОШ №2 г. Свирска»
Свирск, 2017
ОГЛАВЛЕНИЕ
| Стр. | ||
| Введение…………………………………………………………… | 3 | |
| 1. | Теоретическая часть……………………………………………… | 5 |
| 1.1. | История фейерверков……………………………………………… | 5 |
| 1.2. | Вещества, используемые для создания фейерверков………….. | 10 |
| 1.3. | Пламя: строение, описание, схема, температура……………… | 14 |
| 2. | Практическая часть………………………………………………. | 19 |
| 2.1. | Изучение строения пламени…………………………………….. | 19 |
| 2.2. | Получение цветного пламени…………………………………… | 22 |
| 2.3. | Определение ионов металлов, входящих в химический состав горных пород и минералов………………………………………. | 24 |
| Заключение………………………………………………………… | 26 | |
| Список литературы……………………………………………….. | 27 |
ВВЕДЕНИЕ
Фейерверк по праву может считаться самым ярким изобретением. Он не перевернул мир – он сделал его прекраснее. Небо взрывается яркими огнями, шарами, цветами, звезды падают и летят прямо на наблюдающих за этим потрясающим зрелищем. Расцвеченный огнями, играющий переливами небосвод в эти минуты показывает нам, как прекрасна Вселенная где-то там, в космосе, с ее звездами и взрывами, туманностями и астероидами. Поистине великолепная картина, созданная руками человека.
Это небесное представление всегда заставляет людей замирать и устремлять вверх восторженные взгляды. Сотни ярких светящихся точек взмывают вверх и расходятся сферой, вслед за ними вспыхивают багряные искры, и тут же — тысяча сине-фиолетовых звезд рассыпается над головой, и они будто бы несутся прямо на тебя. Кажется, нет зрелища более завораживающего, чем фейерверк. Он способен придать торжественность и особую чарующую атмосферу любому событию. [3]
XXI век – век научно-технического прогресса. Нынешний этап развития общества и, собственно, самого научно-технического прогресса назван учеными научно технической революцией. Одним из примеров такого резкого толчка в развитии человечества является расширение области распространения и применения химических элементов, соединений, да, впрочем, всей химической промышленности. Однако нам хотелось бы остановиться на производстве и использовании цветных химических соединений. Что же это такое?
Наша тема исследований актуальна для нас, потому что научно-технический процесс в наше время не стоит на месте, он идёт вперёд семимильными шагами, и чтобы идти с ним в ногу надо познавать новое то, что происходит в сфере науки. Сейчас во всем мире очень популярно изучение металлов и их соединений. Ведь в наше время почти всё, что нас окружает, состоит из металла, и открытие новых его свойств и их изучение – важнейшая тема столетия.
Исходя из вышеизложенного, сформулирована цель исследовательской работы: опытным путём определить, какие химические вещества в ходе горения образуют необычный для пламени цвет.
Задачи исследования:
- Изучить литературные источники по теме;
- Выяснить, горение, каких химических веществ, способно образовывать цветное пламя;
- Изучить методику получения цветного пламени;
- Провести химический эксперимент с исследуемыми образцами химических веществ;
- Найти практическое применение цветному пламени;
- Проанализировать полученные результаты и сделать выводы.
Объект исследования: пламя огня.
Предмет исследования: процесс горения химических веществ, в пламени огня.
Методы исследования:
- Теоретические: изучение литературы, обобщение, анализ;
- Эмпирические: наблюдение, фотографирование, сравнение;
- Экспериментальные: химический эксперимент, лабораторные опыты, анализ результатов.
Гипотеза: предполагаю, что цвет пламени зависит от химических веществ, которые в нём сгорают.
Практическая значимость работы: результаты, полученные в ходе эксперимента можно использовать для определения химического состава горных пород и минералов.
- ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
- ИСТОРИЯ ФЕЙЕРВЕРКА
Фейерверк (немецкого слова Feuerwerk, от Feuer — огонь и Werk — дело, работа) — декоративные огни разнообразных цветов и форм, получаемые при сжигании пиротехнических составов. [4]
Фейерверк представляет собой красочные и яркие огни, разлетающиеся в воздухе при сжигании специальных пороховых составов. Чаще всего фейерверк используют во время праздников или торжеств. В древнем Китае, во времена правления знаменитой династии Хань, несколько тысяч лет назад, примерно в 210 году до нашей эры, были впервые изобретены фейерверки. Китайцы обратили внимание на то, как потрескивают и громко взрываются зажженные палочки бамбука. Этот громкий звук сильно пугал людей, и тогда они решили использовать горящий бамбук в ритуалах, отпугивающих злые духи. Позднее, в 400-500 годах до н.э., Южные и Северные правящие династии стали применять фейерверки в религиозных церемониях.
Начало первых современных фейерверков зародилось во времена правления династии Суи и Танг в 500-900 года до н.э., после открытия китайцами пороха. Великие изобретатели тех времен наполнили стебли бамбука изобретенными летучими смесями и стали поджигать их на костре (рис. 1). Первооткрыватели пришли в ужасный шок от увиденного зрелища и мощных оглушающих взрывов. Осознав весь потенциал своего изобретения, древние алхимики, те, кто придумал фейерверк, стали подбирать альтернативные бамбуку корпуса. Вскоре на замену бамбуку пришли бумажные трубки наполненные порохом и фитили из ткани. [5]
Рисунок 1. Поджигание стеблей бамбука наполненными летучими смесями
Позже китайские умельцы стали создавать разноцветные фейерверки путем добавления в порох различных веществ. Позже, когда были придуманы составы, которые при горении имеют определенный цвет, размер и форму пламени, с помощью разноцветных вспышек высшую силу стали не просто отгонять, но уже и общаться с нею.
Что касается пороха, который является основой всех современных фейерверков – его случайно изобрели даосские монахи, пытаясь создать эликсир бессмертия (рис. 2).
Рисунок 2. Китайцы использовали порох для устройства фейерверков начиная примерно с 1025 года.
В дальнейшем искусство фейерверков становилось все более совершенным. Китайские мастера придумывали различные смеси и составы, начиняли ими разнообразные емкости, и вскоре научились делать праздничные салюты всех оттенков и форм — в небо взлетали разноцветные птицы, и с оглушительным треском распадались на тысячи ярких огней. [6]
В 1292 году путешественник Марко Поло впервые привез фейерверки в Италию. Вскоре итальянцы начали проявлять интерес к искусству пиротехники, и в эпоху Европейского Резонанса, у них появились новые изобретения в виде снарядов, разрывающихся высоко в небе. Это открытие привело к изобретению современных фейерверков. Кроме этого, итальянцам удалось сконструировать такие виды фейерверков, как «фонтан», «конус», «бенгальские огни», «римские свечи». [5]
История российского фейерверка начинается ещё задолго до того, как появились сами фейерверки. Наши предки, славяне, многие праздники связывали с огнём – это игрища, посвящённые чествованию Купалы, бога солнца Ярилы и многих других (рис. 3).
Рисунок 3. Празднования на Руси, связанные с огнём
Первый документально подтвержденный российский фейерверк был устроен в 1674 году в городе Устюг во время царствования отца Петра I – Алексея Михайловича. Устойчивую моду отмечать праздники «потешными огнями» ввел лично Петр I. В небе «выжигали» картины с дворцами, водопадами и фонтанами, воплощали в огне библейские сюжеты и сцены военных баталий. Пётр I, который сам занимался изготовлением «потешных огней» и целых фейерверочных композиций, сделал огненное искусство общегосударственной задачей, когда пиротехникой занимались учёные академии наук.
Царь участвовал во всех стадиях создания фейерверка: от работ в пиротехнических лабораториях по приготовлению фейерверочного состава до разработки сюжета фейерверка и его управления.
Роскошные, дорогостоящие фейерверки устраивались, как правило, в особо торжественных случаях, таких, как коронация царствующих особ, их дни рождения, в дни главных религиозных праздников. Таким образом, уже начиная с XIV века о фейерверках можно говорить, как о виде зрелищного искусства (рис. 4,5,6). [7]
Рисунок 4. Изображение фейерверка 7 мая 1724 г. в Москве в день коронации Екатерины I. Гравер: И.Ф. Зубов.
Рисунок 5. Изображение V-го акта фейерверка
26 декабря 1770 г. в Санкт-Петербурге в честь победы России над Турцией: «Блистание трона российского мудрым правлением Екатерины II».
Рисунок 6. Фейерверк в честь окончания торжественного бракосочетания их Императорских высочеств [Петра Федоровича и Екатерины Алексеевны] августа 1745 г. Гравер: Г.А. Качалов.
Изготовление и запуск фейерверков оставалось достаточно дорогим удовольствием — в небо улетали тысячи рублей. Но полученное удовольствие того, наверно, стоило. По воспоминаниям очевидцев, фейерверки петровских времен представляли собой просто произведение искусства.
С помощью огней на небе рисовали целые художественные картины — изображения дворцов, людей, библейские сюжеты, военные баталии… Например, один из самых первых, еще достаточно скромных фейерверков, устроенный в начале царствования Петра, представлял собой картину на мифологический сюжет — Геркулес, борющийся со львом…
Именно при Петре появилась традиция новогоднего фейерверка — только при нем этот праздник стал праздником. Новый год начали отмечать согласно веденному юлианскому календарю — 1 января. По указу царя предписывалось праздновать Новый год 7 дней, празднично украшать ворота домов еловыми и можжевеловыми ветвями, а по ночам зажигать праздничную иллюминацию.
На Красной площади, а затем и в Петербурге, на стрелке Васильевского острова, 1-ого января устраивались грандиозные фейерверки. Они были так красочны и великолепны, что Петр повелевал запечатлевать их на гравюрах.
После Петра искусство фейерверков уже не достигало столь грандиозного размаха, но праздничная иллюминация и салюты обязательно присутствовали на любых важных государственных мероприятиях.
Тем временем искусство производства разного рода фейерверочных приспособлений шло вперед. Была открыта бертолетова соль, позволявшая создавать очень яркие и красочные огни, появились разнообразные ракеты.
В XIX веке фейерверки были не столь красочно-художественны, как при Петре, зато распространились повсеместно. Любой помещик считал своим долгом устроить шумный и яркий фейерверк в своем имении. В результате появилось множество фабрик и лавочек, торгующих всем необходимым для украшения праздников.
После революции фейерверочные традиции были разрушены – фейерверки практически не устраивались. Но во время Отечественной войны эта традиция приобрела новое звучание – каждая победа Красной армии отмечалась салютом. Самый красочный и большой салют был дан 9 мая 1945 года.
Долгое время только праздничными салютами — на 7 ноября и на 9 мая практически и ограничивалось все отечественное фейерверочное искусство.
Но в последнее время наблюдается повышение интереса к праздничным фейерверкам. Конечно, им еще далеко до петровских живых картин, но обилие разного рода «потешных огней» на прилавках может удовлетворить самого требовательного покупателя. И в новогоднюю ночь небо наших городов теперь расцвечивается миллионами огней — к радости многочисленных зрителей.[8]
- ВЕЩЕСТВА, ИСПОЛЬЗУЕМЫЕ ДЛЯ СОЗДАНИЯ ФЕЙЕРВЕРКОВ
Основными составными частями фейерверков являются:
- корпус (из картона, бумаги, алюминия, пластмасс)
- заряды (вышибные, воспламенительно-разрывные и звуковые) из дымных порохов, бездымных порохов и пиротехнических составов типа фотосмесей
- пироэлементы в виде звёздочек, факелов, таблеток из световых, дымовых и звуковых пиротехнических составов
- средства воспламенения – огнепроводный шнур, электровоспламенители
При горении пиротехнические составы могут развивать высокую температуру (до 3000 °C). [4]
Горение – это химическая реакция окисления, сопровождающаяся выделением тепла.
Для возникновения горения необходимо наличие трёх условий горючего вещества, окислителя и источника зажигания:
- Горючее вещество – это всякое твёрдое, жидкое или газообразное
вещество, способное окисляться с выделением тепла.
- Окислители – вещества и материалы, обладающие способностью
вступать в реакцию с горючими веществами, вызывая их горение, а также увеличивать его интенсивность. Окислителем чаще всего являетсякислород воздуха (могут быть также хлор, пары брома, серы и т.д.).
- Источник зажигания – средство энергетического воздействия,
возникновение горения. Источники зажигания принято делить на открытые (светящиеся) – молния, пламя, искры, накалённые предметы, световое излучение; и скрытые (несветящиеся) – тепло химических реакций, микробиологические процессы, адиабатическое сжатие, трение, удары и т. п. Они имеют различную температуру пламени и нагрева. Всякий источник зажигания должен иметь достаточный запас теплоты или энергии, передаваемой реагирующим веществам. Поэтому на процесс возникновения горения влияет и продолжительность воздействия источника зажигания. После начала процесса горения оно поддерживается тепловым излучением из его зоны. [10]
Наиболее важным компонентом фейерверков является, конечно, взрывчатая смесь. Она была обнаружена случайно китайскими алхимиками, которых в действительности больше волновало открытие эликсир жизни. Они обнаружили, что сочетание мёда, серы и селитры (нитрат калия) вдруг воспламенялось при нагревании.
К сочетанию серы и нитрата калия позднее присоединили уголь вместо мёда. Современный порох имеет селитру, древесный уголь и серу по весу в соотношении 75:15:10. Это соотношение остается неизменным с 1781 года.
«Звезды», содержащиеся в составе пиротехники содержат металлический порошок или соли металлов, которые дают фейерверк красок. [9]
Алюминий (Al) – это основной компонент для создания белых и серебряных искр и огней.
Барий (Ba) – создает зеленый цвет в фейерверках и может дополнить любой другой цвет и помочь стабилизировать другие летучие элементы.
Углерод (С) – это черный порошок, который используется в качестве пропеллента в фейерверках (разжигателя). В некоторые формулы также могут входить сажа, сахар и крахмал.
Кальций (Ca). Используется для создания глубоких оттенков оранжевого цвета фейерверка
Хлор (Cl) является важным компонентом для многих окислителей в фейерверках. Некоторые из солей металлов, создающих цвет содержат хлор. Присутствие ионов хлора в продуктах горения цветных составов с вышеуказанными цветообразующими компонентами — обязательное условие. Без хлора может обойтись только желтый огонь на основе натрия, так как он и без того дает насыщенное окрашивание, в остальных случаях в отсутствие хлора цвета пламени получаются блеклыми и невыразительными.
Цезий (Cs) помогает окислять смеси фейерверков, а также создает в эффектах цвет индиго.
Медь (Cu) производит сине-зеленый цвет в фейерверке, а галогениды меди используются для создания оттенков синего.
Железо (Fe) используется для получения искры. Чем жарче разогревается металл, тем ярче в итоге получается искра.
Калий (К). Создает фиолетово-розовый цвет искры, а его соединения, такие как: нитрат калия, хлорат калия, перхлорат калия и другие не менее важные окислители, помогают окислять смеси фейерверков.
Литий (Li) – это металл, который используется для создания красного цвета фейерверков. В частности, карбонат лития, является одним из главных красителей.
Магний (Mg) — горит очень ярким белым цветом, поэтому используется для создания белых искр или придания общего блеска фейерверкам.
Натрий (Na) – используется для создания желтого цвета в эффектах. Однако, бывает горит настолько ярким желтым цветом, что его маскируют другими менее интенсивными цветами.
Кислород (О). Это окислители, которые выделяют кислород для лучшего горения фейерверка. Окислителями, как правило, выступают нитраты, хлораты или перхлораты. Иногда используется для обеспечения цвета.
Фосфор (P). Фосфор спонтанно горит в воздухе и отвечает за некоторые эффекты, которые светятся в темноте. Это один из компонентов топлива фейерверка.
Рубидий (Rb). Соединения рубидия производят фиолетово-красный цвет фейерверка. Также, они помогают окислять смеси фейерверков.
Сера (S) – компонент дымного пороха и используется как один из основных элементов толкающих фейерверк в воздух.
Сурьма (Sb) – используется для создания эффекта “Блеск”.
Стронций (Sr) – придает эффектам красный цвет. Его соединения также стабилизируют смеси в фейерверке.
Титан (Ti) – используется для создания серебряных искр.
Цинк (Zn) – создает голубовато-белый цвет эффекта, который используется для создания дымовых эффектов и для других эффектов фейерверков. [10]
- ПЛАМЯ: СТРОЕНИЕ, ОПИСАНИЕ, СХЕМА, ТЕМПЕРАТУРА
Определение
Пламя представляет собой раскаленную газообразную среду, состоящую в значительной степени из частично ионизированных частиц,
В пламени осуществляются преобразования физического и химического типа, сопровождающиеся свечением, выделением тепловой энергии и разогревом. Наличие же в газообразной среде ионных и радикальных частичек характеризует его электрическую проводимость и особое поведение в электромагнитном поле. [11]
Пламя: строение и структура
Горение свечи
Горение свечи подобно горению спички или зажигалки. А строение пламени свечи напоминает раскаленный газовый поток, который вытягивается вверх за счет выталкивающих сил. Процесс начинается с нагревания фитиля, за которым следует испарение парафина. Самую нижнюю зону, находящуюся внутри и прилегающую к нити, называют первой областью. Она обладает небольшим свечением синего цвета из-за большого количества топлива, но малого объема кислородной смеси. Здесь осуществляется процесс неполного сгорания веществ с выделением угарного газа, который в дальнейшем окисляется (рис. 7).
Рисунок 7. Горение свечи
Схема пламени включает:
— Первую или темную область (рис. 8 (1));
— Вторую светящуюся зону (рис. 8 (2));
— Третью прозрачную оболочку (рис. 8 (3)).
Нить свечи не подвергается горению, а только происходит обугливание загнутого конца. [11]
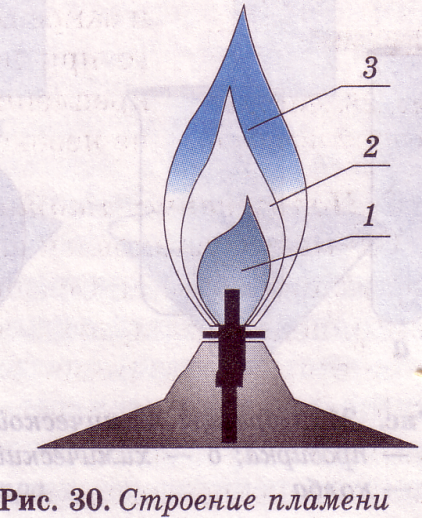
Рисунок 8. Схема строения пламени
Горение спиртовки
Для химических экспериментов часто используют небольшие резервуары со спиртом. Их называют спиртовками. Фитиль горелки пропитывается залитым через отверстие жидким топливом. Этому способствует давление капиллярное. При достижении свободной верхушки фитиля, спирт начинает испаряться. В парообразном состоянии он поджигается и горит при температуре не более 900 °C. Пламя спиртовки имеет обычную форму, оно практически бесцветное, с небольшим оттенком голубого цвета (рис.9). Его зоны не так четко видны, как у свечки. [11]
Рисунок 9. Горение спиртовки
Цветовая характеристика пламени
Окраска пламени взаимосвязана с температурными показателями, с наличием в нем ионных частиц, которые относятся к определенному эмиссионному или оптическому спектру. Так, горение некоторых элементов приводит к изменению цвета огня в горелке. Отличия в окрашивании факела связаны с расположением элементов в разных группах периодической системы. Огонь на наличие излучений, относящихся к видимому спектру, изучают спектроскопом. При этом было установлено, что простые вещества из общей подгруппы оказывают и подобное окрашивание пламени. Для наглядности используют горение натрия в качестве теста на данный металл. При внесении его в пламя, языки становятся ярко-желтыми. [11]
Температурные показатели пламени
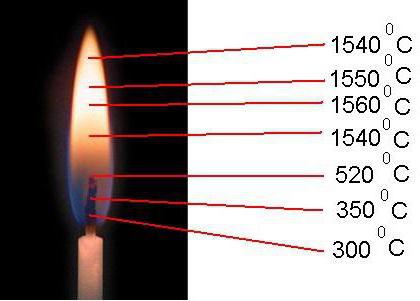
Каждая зона огня свечи или горелки имеет свои значения, обусловленные поступлением кислородным молекул. Температура открытого пламени в разных его частях колеблется от 300 °C до 1600 °C (рис 10.)
Рисунок 10. Температурные показатели пламени
Окраска пламени взаимосвязана с температурными показателями, с наличием в нем ионных частиц, которые относятся к определенному оптическому спектру. Так, горение некоторых элементов приводит к изменению цвета огня в горелке. Отличия в окрашивании факела связаны с расположением элементов в разных группах периодической системы. [11]
Вывод:
Фейерверк – декоративные огни разнообразных цветов и форм, получаемые при сжигании пиротехнических составов.
Ещё в древние времена огню придавали большое значение. У многих народов существуют традиции, связанные с использованием костров (в России — это Масленица, праздник Ивана Купалы), свечей, факелов и т. п. Это были прообразы первых фейерверков.
Фейерверки были изобретены в Китае в 12 веке н. э. Существует предположение, что первыми фейерверками были куски зелёного бамбука, который взрывался, когда его бросали в костёр
Ключевую роль в распространении фейерверка сыграл Марко Поло, который после долгих странствий привёз порох из Китая. Уже к XV веку каждая европейская страна имела свои традиции фейерверка. В Италии и Германии даже формировались пиротехнические школы
В начале XIX века развитие фейерверка вступило в новую стадию. Теперь пиротехники задумались не только над технической стороной, но и над варьированием цветов фейерверка. Палитра значительно расширилась, также появились новые спецэффекты.
Петр Великий усовершенствует искусство фейерверков, лично создавая сложнейшие пиротехнические фигуры. Скоро салюты стали частью празднований Нового года, побед в битвах, религиозных действий.
В России первый фейерверк был устроен в городе Устюг в 1674 году, после фейерверки стали традицией.
В последние годы фейерверки в России интенсивно развиваются. Сейчас они включают в себя не только так называемые «бомбы», но и различные фонтаны, горящие надписи/логотипы, статические и динамические фигуры, дневные фейерверки и спецэффекты для помещений
Пиротехники используют в своей работе разнообразные горючие вещества. Широко представлены неметаллические элементы. Многие смеси включают органические углеродсодержащие материалы. Используются химически активные металлы, чье горение при высокой температуре дает яркий свет. Цвета в фейерверках исходят из широкого спектра металлических соединений – особенно металлических солей.
В процессе горения образуется пламя, строение которого обусловлено реагирующими веществами. Его структура поделена на области в зависимости от температурных показателей.
- ПРАКТИЧЕСКАЯ ЧАСТЬ
- ИЗУЧЕНИЕ СТРОЕНИЯ ПЛАМЕНИ
Цель работы: Изучить строение пламени.
Оборудование: спички, стеклянная трубка, фарфоровая чашка, деревянная лучинка, пинцет, химический стакан, парафиновая свеча, известковая вода.
Ход работы
Соблюдая технику безопасности при работе в лаборатории, приступаем к выполнению опытов
Опыт 1. Изучение строения пламени
Зажигаем свечу и внимательно рассматриваем ее пламя (рис. 11). Мы видим, что оно неоднородно. Около самого фитиля пламя почти не светится, а вот средняя широкая часть его светится ярче всего. Наружная часть пламени опять более бледная, а над ней можно иногда заметить идущую вверх, струйку сажи.
При рассмотрении пламени можно различить три его зоны (рис. 11):
- Нижняя более тёмная часть пламени голубого цвета – в ней находятся пары горючего вещества – парафина, смешанные с воздухом;
- Средняя наиболее яркая часть пламени красно-оранжевого цвета. Это объясняется тем, что здесь под влиянием высокой температуры происходит разложение углеродсодержащих соединений, и частицы угля раскаляются, излучая свет;
- Верхняя наиболее светлая часть пламени бледно жёлтого цвета. В ней происходит полное сгорание продуктов разложения с образованием оксида углерода (IV) и воды.[1]

Рисунок 11. Изучение строения пламени
Опыт 2. Исследование состава внутренней части пламени
При исследовании тёмной (нижней) части пламени мы вносим в него при помощи пинцета конец стеклянной трубки, держа её под углом 45-50° (рис.12). К другому концу трубки подносим горящую лучинку. Из-за недостатка воздуха горение здесь почти не происходит, так как нижняя часть пламени представляет собой газообразный парафин, смешанный с воздухом.
Рисунок 12. Состав внутренней части пламени
При исследовании средней части пламени (самой яркой), вносим в неё холодный предмет, фарфоровую чашку. Наблюдаем образование сажи, продукта горения раскалённых частиц угля. Средняя часть пламени состоит из раскалённых частиц угля (рис. 13).

Рисунок 13. Состав средней части пламени
Для исследования состава внешней части пламени, вносим в неё на 2-3 с. опрокинутый, смоченный известковой водой химический стакан. Наблюдаем образование помутнения на стенках стакана, это свидетельствует о том, что во внешней части пламени находятся вода и углекислый газ (рис. 14).

Рисунок 14. Состав верхней части пламени
Опыт 3. Исследование температуры пламени.
Для опыта нам понадобятся свеча и тонкая деревянная лучинка. Вносим лучинку на 2-3 с. в пламя, как бы разрезая его лучинкой поперек (рис. 15). После рассмотрения лучинки замечаем, что она обуглилась в двух местах, соответствующих наружной части пламени. Это значит, что самая высокая температура в верхней части пламени, самая низкая – в нижней части пламени.

Рисунок 15. Исследование температуры пламени
- ПОЛУЧЕНИЕ ЦВЕТНОГО ПЛАМЕНИ
Цель: опытным путём получить цветное пламя, используя соли металлов и металлы (магний, медь).
Оборудование: мерные стаканы, мерный цилиндр, воронка, стеклянные палочки, весы, разновесы, спиртовка, спички, нихромовая проволока, медная проволока, весы, разновесы, магний, растворы: дистиллированная вода; соляная кислота, соли: фторид лития (I); хлорид натрия (I); хлорид калия (I); хлорид кальция (II); хлорид бария (II); хлорид меди (II).
Ход работы:
Опыт 1. Приготовление растворов солей с определённой массовой долей растворённого вещества.
Цель: приготовить 20%-ный раствор соответствующей соли для химического эксперимента.
Расчёт массы соли:
Для приготовления раствора соли нам понадобиться дистиллированная вода 5 мл, отмеренная с помощью мерного цилиндра. По формуле (1):
m=V*, (1)
где m – масса вещества;
V – объём вещества;
— плотность вещества,
Находим массу дистиллированной воды m=5 мл * 1 г/мл =5 г.
Массовая доля воды в 20%-ном растворе соли составит 80% (100% — 20% =80%)
Составляя пропорцию, находим массу соли, необходимую для приготовления 20%-ного раствора соли. Предварительно обозначив её за х.
5 г – 80%
х г – 20%
х = (5 г * 20%)/80% = 1,25 г
Для приготовления 20%-ного раствора соответствующей соли: 1,25 г растворяем в 5 мл воды.
Нами были приготовлены 20%-ные растворы фторида лития (I); хлорида натрия (I); хлорида калия (I); хлорида кальция (II); хлорида бария (II); хлорида меди (II).
Опыт 2. Окрашивание пламени солями металлов
Предварительно нихромовую проволочку тщательно очищаем. Для этого её смачиваем раствором соляной кислоты, вносим в пламя спиртовки (обычно пламя окрашивается в интенсивно жёлтый цвет примесями солей натрия). Затем на проволочку наносим анализируемый раствор и вносим в пламя спиртовки. [2] В присутствии катионов Li+, Na+, K+, Cа2+, Ba+2, Cu2+ пламя приобретает характерную окраску. Результаты опыта представлены в таблице 1.
Таблица 1. Окрашивание пламени в присутствии катионов металлов входящих в химический состав солей
| Катион | Воздействие | Наблюдения |
| Li+ | Пламя | Красное окрашивание |
| Na+ | Пламя | Желтое окрашивание |
| К+ | Пламя | Фиолетовое окрашивание |
| Са2+ | Пламя | Кирпично-красное окрашивание |
| Ва2+ | Пламя | Жёлто-зелёное окрашивание |
| Сu2+ | Пламя | Зеленовато-голубое окрашивание |
Химические вещества сгорают, окрашивая огонь отдельными своими ионами, которые высвобождаются под воздействием высокой температуры.
Опыт 3. Горение медной проволоки
Загибаем конец медной проволоки, делая петлю, увеличивая площадь соприкосновения веществ. Смачиваем её в соляной кислоте и вносим в пламя спиртовки. Наблюдаем окрашивание пламени в голубой цвет с зеленоватым оттенком.
Опыт 4. Горение магния
Стружку магния, удерживая пинцетом, вносим в пламя спиртовки. Наблюдаем окрашивание пламени в ярко белый цвет.
- ОПРЕДЕЛЕНИЕ ИОНОВ МЕТАЛЛОВ, ВХОДЯЩИХ В ХИМИЧЕСКИЙ СОСТАВ МИНЕРАЛОВ
Цель: Определить ион металла, входящий в химический состав минерала, используя пламя спиртовки.
Оборудование: спиртовка, сухое горючее, спички, пинцет, фарфоровые чашки, минералы: магнезит, сильвин, галит
Ход работы
Измельчаем минералы. В фарфоровые чашки раскладываем сухое горючее, поджигаем и вносим соответствующий измельчённый минерал.
Результаты опыта представлены в таблице 2.
Таблица 2. Практическое определение химических элементов по различному окрашиванию пламени
| Реагент | Воздействие | Наблюдение | Вывод |
| Магнезит | Пламя | Серебристо белое окрашивание | Содержит ионы магния |
| Сильвин | Пламя | Фиолетовый оттенок | Содержит ионы калия |
| Галит | Пламя | Жёлтое окрашивание | Содержит ионы натрия |
Вывод:
Пламя по своему строению неоднородно. В нём различают три зоны: нижнюю, среднюю, верхнюю. Каждая зона пламени имеет характерный цвет и температуру. Самая горячая часть пламени – наружная и что наиболее эффективный нагрев веществ будет проходить именно в ней. В результате горения свечи, образуются продукты горения парафина. Химические элементы медь, магний и соли в присутствии катионов металлов Li+, Na+, K+, Cа 2+, Ba+2 , Cu2+ способны окрашивать пламя в характерный цвет. Результаты, полученные в ходе исследования можно использовать для определения содержания катионов металлов Li+, Na+, K+, Cа 2+, Ba+2 , Cu2+ в минералах.
ЗАКЛЮЧЕНИЕ
В ходе исследования мы узнали много интересных фактов о пламени и различных металлах. Проделанная нами работа позволила определить на собственном опыте, в какие цвета окрашивают металлы и ионы металлов, входящие в состав солей, пламя при горении. Доказано, цвет пламени огня зависит от веществ, которые в нем сгорают. Гипотеза подтвердилась.
Благодаря нашим опытам мы проверили это явление на практике, что
позволяет найти пути применения этого явления. Метод по обнаружению некоторых химических элементов по различному окрашиванию пламени можно применять при исследовании химического состава минералов.
Окраска пламени зависит от наличия раскаленных паров свободных металлов, получающихся в результате термического разложения солей.
Реакции окрашивания пламени удаются хорошо только с летучими солями (хлоридами).
Цветной огонь используются для снаряжения фейерверочных изделий
Также выяснили: пламя по своему строению неоднородно. В нём различают три зоны: нижнюю, среднюю, верхнюю. Каждая зона пламени имеет характерный цвет и температуру.
Огонь очень опасен! Его всегда нужно контролировать, нельзя оставлять без присмотра. Он способен и очень навредить. При выполнении опытов с применением огня, необходимо соблюдать технику безопасности при работе в лаборатории.
Конечно, мы исследовали не всё о таком удивительном явлении как огонь. Поэтому, в дальнейшем, возможно, исследовать такие вопросы: как люди научились разжигать огонь, каковы были первые способы? Какие вещества не горят и почему? Как делают фокусы с огнем? Также интересна тема “Огонь и оружие”.
СПИСОК ЛИТЕРАТУРЫ
- Габриелян О.С., Купцова А.В. Химия 8 кл.: Тетрадь для лабораторных и практических работ к учебнику О.С. Габриеляна – М.: Дрофа, 2015.
- Прохоров Г.В. Качественный химический анализ: практикум для школьника под ред. проф. Т.Н. Шеховцовой – М.: Московский государственный университет им. М.В. Ломоносова, 2006
- https://shkolazhizni.ru/culture/articles/11729 Как и когда изобрели фейерверк
- https://ru.wikipedia.org/wiki Фейерверк
-
http://retrobazar.com/journal/interesting/1020_istorija-fejerverka.html История фейерверка
-
http://surwiki.admsurgut.ru/wiki/index.php 300 лет Петровским огненным потехам.
- http://www.ras.ru/lomonosov М.В. Ломоносов и его время
- http://www.chronoton.ru/past/thing/firework Фейерверки — история «потешных огней»
- http://v-nayke.ru/?p=8572 Из чего делают фейерверки
- http://fire-work.com.ua/articles/24-vewchestva-ispolzyemue-dlja-sozdanija-fejerverkov Вещества, используемые для создания фейерверков
- http://fb.ru/article/241852/plamya-stroenie-opisanie-shema-temperatura Пламя: строение, описание, схема, температура
Отзыв
научного руководителя об исследовательской работе Рымарева Ефима
«Палитра огня
Исследовательская работа Рымарева Ефима представляет собой исследование, направленное на определение химических веществ в ходе горения, которые образуют необычный для пламени цвет. Актуальность работы заключается в том, что научно-технический процесс в наше время не стоит на месте, он идёт вперёд семимильными шагами, и чтобы идти с ним в ногу надо познавать новое то, что происходит в сфере науки. Сейчас во всем мире очень популярно изучение металлов и их соединений. Ведь в наше время почти всё, что нас окружает, состоит из металла, и открытие новых его свойств и их изучение – важнейшая тема столетия.
Содержание работы соответствует заявленной теме.
Текст работы изложен на 27 листах печатного текста, что представляется достаточным для написания проекта.
Работа включает в себя введение, основную часть из двух глав, заключение, список литературы. Во введении указывается актуальность исследования, ставятся цель и задачи, объект и предмет исследования, методы, выдвигается гипотеза.
В первой главе ведётся обзор литературы по данной теме. Во второй главе описывается исследование, а результаты оформлены в виде таблицы. Каждая глава завершается выводами. В заключении излагаются результаты исследования и подтверждение гипотезы.
Работу Ефим выполнял самостоятельно, используя интернет источники и литературу, рекомендованную ему для исследования. При выполнении работы проявил: самостоятельность, творчество, инициативу, способность решать соответствующие исследовательские проблемы. Чётко выполнял все рекомендации научного руководителя, и вовремя устранял замечания в процессе доработки исследовательской работы.
Можно сделать вывод, что у данного ученика сформированы элементарные навыки исследовательской деятельности. Работа заслуживает внимания и высокой оценки.
Научный руководитель: Полетанская Е.В.