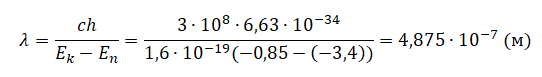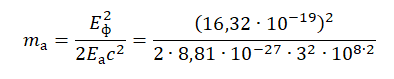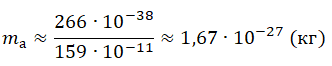Атом Бора.
Автор — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев.
Темы кодификатора ЕГЭ: постулаты Бора.
Планетарная модель атома, успешно истолковав результаты опытов по рассеянию -частиц, в свою очередь столкнулась с очень серьёзными трудностями.
Как мы знаем, любой заряд, движущийся с ускорением, излучает электромагнитные волны. Это — неоспоримый факт классической электродинамики Максвелла, подтверждаемый многочисленными наблюдениями.
Нам также хорошо известно, что электромагнитные волны несут энергию. Стало быть, ускоренно движущийся заряд, излучая, теряет энергию, которая этим излучением уносится.
А теперь давайте возьмём произвольный электрон в планетарной модели. Он двигается вокруг ядра по замкнутой орбите, так что направление его скорости постоянно меняется. Следовательно, электрон всё время имеет некоторое ускорение (например, при равномерном движении по окружности это будет центростремительное ускорение), и поэтому должен непрерывно излучать электромагнитные волны. Расходуя свою энергию на излучение, электрон будет постепенно приближаться к ядру; в конце концов, исчерпав запас своей энергии полностью, электрон упадёт на ядро.
Если исходить из того, что механика Ньютона и электродинамика Максвелла работают внутри атома, и провести соответствующие вычисления, то получается весьма озадачивающий результат: расход энергии электрона на излучение (с последующим падением электрона на ядро) потребует совсем малого времени — порядка секунды. За это время атом должен полностью «коллапсировать» и прекратить своё существование.
Таким образом, классическая физика предрекает неустойчивость атомов, устроенных согласно планетарной модели. Этот вывод находится в глубоком противоречии с опытом: ведь на самом деле ничего такого не наблюдается. Предметы нашего мира вполне устойчивы и не коллапсируют на глазах! Атом может сколь угодно долго пребывать в невозбуждённом состоянии, не излучая при этом электромагнитные волны.
Постулаты Бора.
Оставалось признать, что внутри атомов перестают действовать известные законы классической физики. Микромир подчиняется совсем другим законам.
Первый прорыв в познании законов микромира принадлежит великому датскому физику Нильсу Бору. Он предложил три постулата, резко расходящиеся с механикой и электродинамикой, но тем не менее позволяющих правильно описать простейший из атомов — атом водорода.
Классическая физика хорошо описывает непрерывные процессы — движение материальной точки, изменение состояния идеального газа, распространение электромагнитных волн… Энергия объекта, подчиняющегося механике или электродинамике, в принципе может принимать любые значения. Однако линейчатые спектры указывают на дискретность процессов, происходящих внутри атомов. Эта дискретность должна фигурировать в законах новой теории.
Первый постулат Бора. Всякий атом (и вообще, всякая атомная система) может находиться не во всех состояниях с любым, наперёд заданным значением энергии. Возможен лишь дискретный набор избранных состояний, называемых стационарными, в которых энергия атома принимает значения Находясь в стационарном состоянии, атом не излучает электромагнитные волны.
Как видим, первый постулат Бора вопиющим образом противоречит классической физике: налагается запрет на любые значения энергии, кроме избранного прерывистого набора, и признаётся, что электроны, вроде бы движущиеся ускоренно, на самом деле не излучают.
Выглядит фантастически, не правда ли? Однако в том же 1913 году, когда Бор предложил свои постулаты, существование стационарных состояний было подтверждено экспериментально — в специально поставленном опыте немецких физиков Франка и Герца. Таким образом, стационарные состояния — это не выдумка, а объективная реальность.
Значения разрешённого набора называются уровнями энергии атома. Что происходит при переходе с одного уровня энергии на другой?
Второй постулат Бора. Если атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией
, то разность этих энергий может высвободиться в виде излучения. В таком случае излучается фотон с энергией
. (1)
Эта же формула работает и при поглощении света: в результате столкновения с фотоном атом переходит из состояния в состояние с большей энергией
, а фотон при этом исчезает.
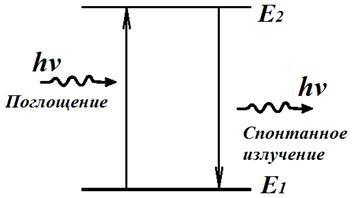
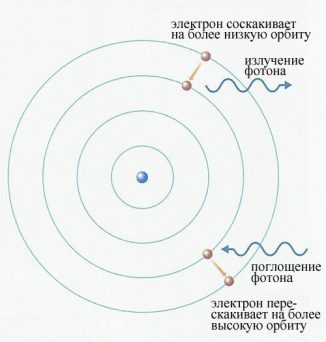
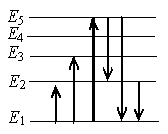
Для примера на рис. 1 показано излучение фотона при переходе атома с энергетического уровня на уровень
. Переход заключается в том, что электрон «соскакивает» с одной орбиты на другую, расположенную ближе к ядру.
Рис. 1. Излучение фотона атомом
Формула (1) даёт качественное представление о том, почему атомные спектры испускания и поглощения являются линейчатыми.
В самом деле, атом может излучать волны лишь тех частот, которые соответствуют разностям значений энергии разрешённого дискретного набора ; соответственно, набор этих частот также получается дискретным. Вот почему спектр излучения атомов состоит из отдельно расположенных резких ярких линий.
Вместе с тем, атом может поглотить не любой фотон, а только тот, энергия которого в точности равна разности
каких-то двух разрешённых значений энергии
и
. Переходя в состояние с более высокой энергией
, атомы поглощают ровно те самые фотоны, которые способны излучить при обратном переходе в исходное состояние
. Попросту говоря, атомы забирают из непрерывного спектра те линии, которые сами же и излучают; вот почему тёмные линии спектра поглощения холодного атомарного газа находятся как раз в тех местах, где расположены яркие линии спектра испускания этого же газа в нагретом состоянии.
Качественного объяснения характера атомных спектров, однако, недостаточно. Хотелось бы иметь теорию, позволяющую вычислить частоты наблюдаемых спектров. Бору удалось это сделать в самом простом случае — для атома водорода.
Атом водорода.
Атом водорода состоит из ядра с зарядом , которое называется протоном, и одного электрона с зарядом
(через
обозначена абсолютная величина заряда электрона). При построении своей теории атома водорода Бор сделал три дополнительных предположения.
1. Прежде всего, мы ограничиваемся рассмотрением только круговых орбит электрона. Таким образом, электрон движется вокруг протона по окружности радиуса с постоянной по модулю скоростью
(рис. 2).
Рис. 2. Модель атома водорода
2. Величина , равная произведению импульса электрона
на радиус орбиты
, называется моментом импульса электрона. В каких единицах измеряется момент импульса?
Смотрим:
=кг*м/с*м=(кг*м/
)*м*с=Н*м*с=Дж*с.
Это в точности размерность постоянной Планка! Именно здесь Бор увидел появление дискретности, необходимой для квантового описания атома водорода.
Правило квантования (третий постулат Бора). Момент импульса электрона может принимать лишь дискретный набор значений, кратных «перечёркнутой» постоянной Планка:
, (2)
3. Выше мы говорили, что классическая физика перестаёт работать внутри атома. Так оно в действительности и есть, но вопреки этому мы предполагаем, что электрон притягивается к протону с силой, вычисляемой по закону Кулона, а движение электрона подчиняется второму закону Ньютона:
. (3)
Эти три предположения позволяют довольно просто получить формулы для уровней энергии атома водорода. Переписываем соотношение (3) в виде:
. (4)
Из правила квантования (2) выражаем :
,
и подставляем это в (4):
.
Отсюда получаем формулу для допустимых радиусов орбит электрона:
. (5)
Теперь перейдём к нахождению энергии электрона. Потенциальная энергия кулоновского взаимодействия электрона с ядром равна:
(Она отрицательна, так как отсчитывается от бесконечно удалённой точки, в которой достигает максимального значения.)
Полная энергия электрона равна сумме его кинетической и потенциальной энергий:
.
Вместо подставим правую часть выражения (4):
. (6)
Полная энергия, как видим, отрицательна. Если на радиус орбиты никаких ограничений не накладывается, как это имеет место в классической физике, то энергия может принимать любые по модулю значения. Но согласно (5) существует лишь дискретный набор возможных значений радиуса; подставляя их в (6), получаем соответствующий набор допустимых значений энергии атома водорода:
. (7)
Основное состояние атома водорода — это состояние с наименьшей энергией . В основном состоянии атом может находиться неограниченно долго. Вычисление даёт:
Дж
эВ:
Мы видим, что если атом находится в основном состоянии, то для выбивания электрона нужно сообщить атому энергию, равную как минимум 13,6 эВ. Эта величина носит название энергии ионизации атома водорода.
По формуле (5) легко вычислить радиус орбиты основного состояния:
см.
То есть, диаметр атома оказывается равным как раз см — величине, известной из опыта. Таким образом, теория Бора впервые смогла объяснить размер атома!
Кроме того, в рамках теории Бора удаётся получить формулы для вычисления частот (или длин волн) спектра атома водорода. Так, согласно второму постулату Бора и формуле (7) имеем:
. (8)
На практике чаще имеют дело с длинами волн. Учитывая, что , формулу (8) можно переписать так:
. (9)
Константа м
называется постоянной Ридберга. Теория Бора даёт значение этой постоянной, очень хорошо согласующееся с экспериментом.
Длины волн спектра атома водорода образуют серии, характеризующиеся фиксированным значением в формуле (9). Все длины волн данной серии излучаются при переходах на уровень
с вышележащих энергетических уровней
.
Переходы в основное состояние:
образуют серию Лаймана. Длины волн этой серии описываются формулой (9) при :
.
Линии серии Лаймана лежат в ультрафиолетовом диапазоне.
Переходы на второй уровень:
образуют серию Бальмера. Длины волн этой серии подчиняются формуле (9) при :
.
Первые четыре линии серии Бальмера лежат в видимом диапазоне (рис. 3), остальные — в ультрафиолетовом.
Рис. 3. Видимый спектр атома водорода (серия Бальмера)
Переходы на третий уровень:
образуют серию Пашена. Длины волн этой серии описываются формулой (9) при :
.
Все линии серии Пашена лежат в инфракрасном диапазоне.
Имеются ещё три «именованных» серии: это серия Брэккета (переходы на уровень), серия Пфунда (переходы на уровень
) и серия Хэмпфри (переходы на уровень
). Все линии этих серий лежат в далёкой инфракрасной области.
Достоинства и недостатки теории Бора.
О достоинствах модели атома водорода, предложенной Бором, мы так или иначе уже сказали. Резюмируем их.
— Теория Бора продемонстрировала, что для описания атомных объектов принципиально недостаточно представлений классической физики. В микромире работают другие, совершенно новые законы.
Для микромира характерно квантование — дискретность изменения величин, описывающих состояние объекта. В качестве меры квантования, как показала теория Бора, может выступать постоянная Планка , которая является универсальной константой и играет фундаментальную роль во всей физике микромира (а не только в явлениях излучения и поглощения света).
— Теория Бора впервые и совершенно точно указала на факт наличия стационарных энергетических состояний атома, образующих дискретный набор. Этот факт оказался общим свойством объектов микромира.
— В рамках модели Бора удалось получить формулы для вычисления частот спектра атома водорода и объяснить размер атома. Классическая физика была не в состоянии решить эти проблемы.
Однако теория Бора, разумеется, не могла претендовать на роль общей теории, описывающей микромир. Модель Бора обладала рядом существенных недостатков.
— Теория Бора непоследовательна. С одной стороны, она отвергает описание атома на основе классической физики, так как постулирует наличие стационарных состояний и правила квантования, непонятных с точки зрения механики и электродинамики. С другой стороны, классические законы — второй закон Ньютона и закон Кулона — используются для записи уравнения движения электрона по круговой орбите.
— Теория Бора не смогла дать адекватное описание самого простого после водорода атома гелия. Подавно не могло быть и речи о распространении теории Бора на более сложные атомы.
— Даже в самом атоме водорода теория Бора смогла описать не всё. Например, дав выражения для частот спектральных линий, модель Бора не объясняла различие в их интенсивностях. Кроме того, неясен оставался механизм образования молекулы водорода из двух атомов.
Несмотря на свои недостатки, теория Бора стала важнейшим этапом развития физики микромира. Полуклассическая-полуквантовая модель Бора послужила промежуточным звеном между классической физикой и последовательной квантовой механикой , построенной десятилетием позже — в 1920-х годах.
Разберем задачи ЕГЭ на темы: «Строение атома», «Модель Резерфорда-Бора», «Энергетические уровни», «Излучение фотона».
Задача 1.
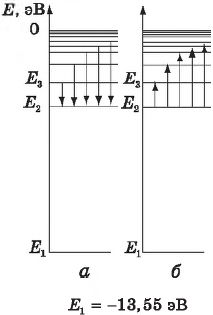
На рисунке изображена схема низших энергетических уровней атома. В начальный момент времени атом находится в состоянии с энергией Е(2). Согласно постулатам Бора, с какой энергией данный атом может излучать фотоны? (Ответ дать в 10−19 Дж.)
Решение:
Согласно постулатам Бора, атом, находящийся в стационарных состояниях, не излучает энергии. Излучение энергии возможно при переходе атома с уровня с большим значением энергии на уровень с меньшим значением энергии. Поглощение энергии, наоборот, возможно при переходе атома с меньшим уровнем энергии на больший.
С учетом представленной диаграммы, излучение атома возможно при переходе с уровня Е(2) на уровень Е(1), так как Е(2)> Е(1). Поэтому, энергия излучаемых фотонов (hv) может быть определена, как разность энергий
Подставив численные значения, рассчитаем энергию излучаемых фотонов.
(Дж).
Ответ: 3.
Задача 2.
Электрон в атоме водорода находится в основном (самом низком, с номером n = 1) энергетическом состоянии. Атом поглощает фотон с импульсом 6,8 · 10–27 кг·м/с. Найдите номер энергетического уровня, на который в результате этого перейдёт электрон.
Дано:
n1=1;
p = 6,8·10–27 кг·м/с.
Найти:
n-?
Решение:
Уровни энергии в атоме водорода определяются формулой:
(эВ), где n=1, 2, 3… и т. д. (1)
Следовательно, атом на уровне n1=1 обладает энергией, которую можно рассчитать по формуле (1).
(эВ).
Найдем связь между импульсом фотона и его энергией:
(2)
Таким образом, энергия фотона может быть определена по формуле (2).
(Дж).
С учетом, что 1 эВ, получим
(эВ).
Атом, получив энергию от фотона, переходит в стационарное состояние с большим уровнем энергии.
(эВ).
Из формулы (1) необходимо вывести номер энергетического уровня.
Ответ: 4.
Задача 3.
На рисунке изображена упрощенная диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Какой из этих четырех переходов связан с поглощением света наибольшей энергии, а какой — с излучением света с наибольшей длиной волны?
Установите соответствие между процессами поглощения и испускания света и стрелками, указывающими энергетические переходы атома.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕССЫ
А) поглощение света наибольшей энергии;
Б) излучение света с наибольшей длиной волны.
ЭНЕРГЕТИЧЕСКИЕ ПЕРЕХОДЫ
1) 1
2) 2
3) 3
4) 4
Ответ:
Решение:
По указанной диаграмме необходимо определить переходы, соответствующие поглощению и излучению света.
Переходы, указанные стрелками 1 и 2, соответствуют излучению энергии, так как атом переходит с большего уровня энергии на меньший.
Здесь надо учесть, что
и
Так как , то, согласно формуле Планка
, меньшая длина волны соответствует большему значению энергии излучения. Поэтому при переходе
будет излучаться большее количество энергии. Вторая стрелка будет соответствовать излучению света с наименьшей длиной волны.
Стрелки 3 и 4 соответствуют поглощению энергии, так как в этих случаях атом переходит на уровни, соответствующие большему значению энергии. Рассуждения, аналогичные первому случаю, приводят к следующему выводу:
и
Так как , то четвертая стрелка будет соответствовать поглощению света наибольшей энергии.
Ответ:
Задача 4.
Значения энергии электрона в атоме водорода задаются формулой: (эВ), где n=1, 2, 3… и т. д.
При переходах с верхних уровней энергии на нижние атом излучает фотон. Переходы с верхних уровней на уровень c n = 1 образуют серию Лаймана, на уровень c n = 2 – серию Бальмера и т. д. Найдите отношение γ максимальной длины волны фотона в серии Бальмера к максимальной длине волны фотона в серии Лаймана.
Решение:
Согласно формуле Планка , максимальная длина волны соответствует излучению света с наименьшим значением энергии. Поэтому для серии Лаймана это переход с уровня 2 на уровень 1 (см. рис. 1). Рассчитаем значение энергии, которая излучается в этом случае.
(эВ).
(эВ).
Длина волны, соответствующая этому переходу, может быть определена из формулы:
(1)
Аналогично для серии Бальмера, излучение с наибольшей длиной волны (наименьшей энергии излучения), соответствует переходу с уровня 3 на уровень 2 (см. рис. 2).
(эВ).
(эВ).
Длина волны, соответствующая этому переходу, может быть определена из формулы:
(2)
Тогда, для нахождения соотношения для длин волн
Разделим уравнение (2) на уравнение (1):
В расчетах значения энергий можно оставить в эВ, так как перевод в систему «СИ» ответа не изменит.
С учетом системы «СИ»:
(1 эВ Дж).
Ответ: 5,4.
Благодарим за то, что пользуйтесь нашими статьями.
Информация на странице «Атом Бора.» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в ВУЗ или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
08.03.2023
Всего: 46 1–20 | 21–40 | 41–46
Добавить в вариант
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома водорода (Е0 = 13,6 эВ). Стрелками отмечены некоторые возможные переходы атома между этими уровнями.
Установите соответствие между показанными на рисунке процессами поглощения фотона наибольшей частоты и излучения фотона наименьшей длины волны и энергией соответствующего фотона. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕСС
А) поглощение фотона наименьшей длины волны
Б) излучение фотона наибольшей частоты
Установите соответствие между названиями постулатов и их формулировками. К каждой позиции первого столбца подберите нужную позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
ИХ ФОРМУЛИРОВКИ
1) переходя из одного состояния в другое, атом излучает (поглощает) половину раз-ности энергий в начальном и конечном состояниях
2) переходя из одного состояния в другое, атом излучает (поглощает) квант энергии, равный разности энергий в начальном и конечном состояниях
3) атом может находиться только в одном из двух возможных состояний
4) атом может находиться только в одном из состояний с определенным значением энергии
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
В атоме водорода уровни энергии описываются формулой Наибольшая длина волны излучаемого фотона при переходе на второй уровень энергии равна 650 нм. Чему будет равна наибольшая длина волны излучаемого фотона при переходе на уровень энергии 4.
Источник: ЕГЭ по физике 01.04.2019. Досрочная волна. (Часть С)
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Какие из этих переходов связаны с поглощением кванта света наибольшей длины волны и излучением кванта света с наименьшей энергией? Установите соответствие между процессами поглощения и испускания света и стрелками, обозначающими энергетические переходы атома. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕССЫ
А) поглощение кванта света наибольшей длины волны
Б) излучение кванта света с наименьшей энергией
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2021 по физике
В атоме водорода уровни энергии описываются формулой Наибольшая длина волны излучаемого фотона при переходе на второй уровень энергии равна 655 нм. Найдите E0.
Источник: ЕГЭ по физике 01.04.2019. Досрочная волна. Вариант 1
На рисунке изображена схема низших энергетических уровней атома. В начальный момент времени атом находится в состоянии с энергией
Согласно постулатам Бора с какой энергией данный атом может излучать фотоны? (Ответ дать в 10−19 Дж.)
Источник: ЕГЭ по физике 06.06.2013. Основная волна. Дальний Восток. Вариант 1.
В первом эксперименте атомы водорода облучают потоком фотонов такой частоты, что электроны в атомах переходят с энергетического уровня с номером n > 1 на энергетический уровень с номером n + 1. При постановке второго эксперимента частоту фотонов подбирают такой, что электроны в атомах переходят с энергетического уровня с номером n − 1 на энергетический уровень с номером n. Определите, как изменяются во втором эксперименте по сравнению с первым длина волны падающего на атом фотона и приращение энергии атома в результате поглощения фотона.
Для каждой величины определите соответствующий характер изменения:
1) увеличивается
2) уменьшается
3) не изменяется
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Длина волны падающего
на атом фотона |
Приращение энергии атома в результате поглощения фотона |
В первом эксперименте атомы водорода облучают потоком фотонов такой частоты, что электроны в атомах переходят с энергетического уровня с номером n > 1 на энергетический уровень с номером n + 1. При постановке второго эксперимента частоту фотонов подбирают такой, что электроны в атомах переходят с энергетического уровня с номером n + 2 на энергетический уровень с номером n + 1. Определите, как изменяются во втором эксперименте по сравнению с первым длина волны падающего на атом фотона и приращение энергии атома в результате поглощения фотона.
Для каждой величины определите соответствующий характер изменения:
1) увеличивается
2) уменьшается
3) не изменяется
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Длина волны падающего
на атом фотона |
Приращение энергии атома в результате поглощения фотона |
На рисунке изображена упрощённая диаграмма нижних энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Какие из этих четырёх переходов связаны с излучением света с наибольшей длиной волны и поглощением света с наименьшей энергией?
Установите соответствие между процессами поглощения и излучения света и энергетическими переходами атома, указанными стрелками.
К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕССЫ
А) излучение света с наибольшей длиной волны
Б) поглощение света с наименьшей энергией
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2023 по физике
Источник: Демонстрационная версия ЕГЭ—2014 по физике.
На рисунке изображена упрощённая диаграмма энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Какие из этих переходов связаны с поглощением света наименьшей длины волны и излучением кванта света с наибольшей энергией?
Установите соответствие между процессами поглощения и испускания света и стрелками, указывающими энергетические переходы атома.
К каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕСС
А) поглощение света наименьшей длины волны
Б) излучение кванта света с наибольшей энергией
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Атом водорода переходит из возбужденного состояния в основное. При этом испускается фотон, который уносит энергию. Установите соответствие между уносимой фотоном энергией и номером энергетического уровня, с которого осуществляется переход электрона. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ЭНЕРГИЯ, УНОСИМАЯ ФОТОНОМ
НОМЕР N УРОВНЯ, С КОТОРОГО
ОСУЩЕСТВЛЯЕТСЯ ПЕРЕХОД ЭЛЕКТРОНА
1) n = 2
2) n = 3
3) n = 4
4) n = 5
Атом водорода переходит из возбужденного состояния в основное. При этом испускается фотон, который уносит энергию. Установите соответствие между уносимой фотоном энергией и номером энергетического уровня, с которого осуществляется переход электрона. К каждой позиции первого столбца подберите соответствующую позицию из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ЭНЕРГИЯ, УНОСИМАЯ ФОТОНОМ
НОМЕР N УРОВНЯ, С КОТОРОГО
ОСУЩЕСТВЛЯЕТСЯ ПЕРЕХОД ЭЛЕКТРОНА
1) n = 2
2) n = 3
3) n = 4
4) n = 5
Задания Д32 C3 № 3059
На рисунке изображены несколько энергетических уровней атома и указаны длины волн фотонов, излучаемых и поглощаемых при переходах с одного уровня на другой.
Экспериментально установлено, что минимальная длина волны для фотонов, излучаемых при переходах между этими уровнями, равна Какова величина
если
?
На рисунке изображена упрощённая диаграмма энергетических уровней атома. Нумерованными стрелками отмечены некоторые возможные переходы атома между этими уровнями. Установите соответствие между процессами поглощения света наибольшей длины волны и испускания света наибольшей длины волны и стрелками, указывающими энергетические переходы атома. К каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
ПРОЦЕСС
А) поглощение света наибольшей длины волны
Б) излучение света наибольшей длины волны
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2013 по физике.
Источник: ЕГЭ по физике 06.06.2013. Основная волна. Сибирь. Вариант 1.
Источник: ЕГЭ по физике 06.06.2013. Основная волна. Сибирь. Вариант 3.
Задания Д32 C3 № 4898
Источник: ЕГЭ по физике 06.06.2013. Основная волна. Сибирь. Вариант 5., ЕГЭ по физике 06.06.2013. Основная волна. Сибирь. Вариант 6.
Всего: 46 1–20 | 21–40 | 41–46
Постулаты Бора
Основу квантовой теории атома Бора составляют два постулата.
Первый постулат Бора гласит: атомная система может находиться только в особых стационарных, или квантовых, состояниях, каждому из которых соответствует определенная энергия $Е_n$; в стационарном состоянии атом не излучает энергию.
Этот постулат противоречит классической механике, согласно которой энергия движущихся электронов может быть любой. Он противоречит также и электродинамике Максвелла, так как допускает возможность ускоренного движения электронов без излучения электромагнитных волн.
Второй постулат Бора: излучение света происходит при переходе атома из стационарного состояния с большей энергией $Е_k$ в стационарное состояние с меньшей энергией $Е_n$. Энергия излученного фотона равна разности энергий стационарных состояний:
$hν_{kn}=E_k-E_n$
Отсюда можно получить частоту излучения:
$ν_{kn}={E_k-E_n}/{h}={E_k}/{h}-{E_n}/{h}$
При поглощении света атом переходит из стационарного состояния с меньшей энергией в стационарное состояние с большей энергией.
Модель атома водорода Бора
Для построения модели простейшей системы — атома водорода — Бор постулировал также правило определения стационарных значений энергии атома (уровней энергии) — так называемое правило квантования.
Правило квантования орбит Бора заключается в следующем.
Стационарным состояниям атома соответствуют разрешенные дискретные значения энергии электрона, такие, что при движении по стационарным круговым орбитам электрон должен иметь дискретные значения момента количества движения:
$m_{e}υr=n{h}/{2π}, n=1,2,3…,$
где $m_{e}$ — масса электрона, $υ$ — его скорость, $r$ — радиус орбиты, $h$ — постоянная Планка, $n$ называется главным квантовым числом (является номером орбиты в спектре атома водорода, в частности).
Используя законы механики Ньютона и правило квантования, Бор вычислил допустимые радиусы орбит и значения энергии стационарных состояний. Минимальный радиус орбиты определяет размер атома (он оказался равным $0.53·10^{-10}$м). Значения энергий стационарных состояний в электронвольтах отложены на вертикальной оси. (В атомной физике энергию выражают в электронвольтах, сокращенно — эВ. $1$ эВ — это энергия, приобретаемая электроном при прохождении разности потенциалов $1$ В. $1$ эВ$ = 1.6·10^{-19}$ Дж.)
Правило квантования орбит и постулаты Бора позволили ему самому и другим ученым объяснить наблюдавшиеся закономерности в оптическом спектре излучения атома водорода, а также в рентгеновских спектрах, и дать физическое истолкование Периодического закона элементов.
Поглощение света
Поглощение света — процесс, обратный излучению, при котором атом с нижних энергетических уровней переходит на верхние уровни. При этом он поглощает излучение тех же частот, которые излучает при переходе с верхних энергетических уровней на нижние.
Гипотеза Планка о квантах
Гипотеза Планка — предположение, что атомы испускают электромагнитную энергию (свет) не непрерывно, а отдельными порциями — квантами.
Энергия каждой порции пропорциональна частоте излучения:
$E=hν,$
где $h=6.63·10^{-34}$ $Дж·с$ — постоянная Планка, $ν$ — частота света.
Постоянная Планка (квант действия) — фундаментальная физическая константа. Введена М. Планком в 1900 г. Наиболее точное значение постоянной Планка $h = 6.626176(36) · 10^{-34}$ $Дж·с$. Чаще пользуются постоянной $h={h}/{2π}=1.0545887(57)·10^{-34}$ $Дж·с$, также называемой постоянной Планка. Формула $p↖{→}={mυ↖{→}}{√{1-{υ^2}/{c^2}}$ — это вторая из простых великих формул физики (первая — формула Эйнштейна, связывающая энергию покоя тела с его массой). После открытия Планка начала развиваться квантовая теория.
Инфоурок
›
Физика
›Презентации›Презентация Постулаты Бора. Подготовка к ЕГЭ
Презентация Постулаты Бора. Подготовка к ЕГЭ
Скачать материал

Скачать материал


- Сейчас обучается 63 человека из 37 регионов


- Сейчас обучается 46 человек из 28 регионов


- Сейчас обучается 97 человек из 42 регионов


Описание презентации по отдельным слайдам:
-
1 слайд
Постулаты Бора. Задания ЕГЭ
-
-
-
-
-
-
-
-
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 156 989 материалов в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Другие материалы
- 08.11.2022
- 70
- 0
- 08.11.2022
- 66
- 0



- 08.11.2022
- 65
- 0


Вам будут интересны эти курсы:
-
Курс повышения квалификации «Информационные технологии в деятельности учителя физики»
-
Курс повышения квалификации «Подростковый возраст — важнейшая фаза становления личности»
-
Курс повышения квалификации «Организация научно-исследовательской работы студентов в соответствии с требованиями ФГОС»
-
Курс повышения квалификации «Основы управления проектами в условиях реализации ФГОС»
-
Курс повышения квалификации «История и философия науки в условиях реализации ФГОС ВО»
-
Курс повышения квалификации «ЕГЭ по физике: методика решения задач»
-
Курс повышения квалификации «Мировая экономика и международные экономические отношения»
-
Курс профессиональной переподготовки «Метрология, стандартизация и сертификация»
-
Курс профессиональной переподготовки «Гостиничный менеджмент: организация управления текущей деятельностью»
-
Курс профессиональной переподготовки «Информационная поддержка бизнес-процессов в организации»
-
Настоящий материал опубликован пользователем Гудкова Вера Германовна. Инфоурок является
информационным посредником и предоставляет пользователям возможность размещать на сайте
методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них
сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайтЕсли Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.Удалить материал
-
- На сайте: 6 лет и 1 месяц
- Подписчики: 0
- Всего просмотров: 2562
-
Всего материалов:
12
Планетарная модель атома, предложенная Резерфордом, – это попытка применения классических представлений о движении тел к явлениям атомных масштабов. Она оказалась несостоятельной. Классический атом неустойчив. Электроны, движущиеся по орбите с ускорением, должны неизбежно упасть на ядро, растратив всю энергию на излучение электромагнитных волн (см. рисунок ниже). При этом спектр излучения атома должен быть непрерывным, а не линейчатым. Это никак не вязалось с тем, что ученые наблюдали на практике.
Следующий шаг в развитии представлений об устройстве атома в 1913 году сделал выдающийся датский физик Н. Бор. Проанализировав всю совокупность опытных фактов, Бор пришел к выводу, что при описании поведения атомных систем следует отказаться от многих представлений классической физики. Он сформулировал постулаты, которым должна удовлетворять новая теория о строении атомов.
Квантовые постулаты Бора – предположения (утверждения), сделанные Н. Бором для того, чтобы модель строения атома Резерфорда соответствовала реальному поведению атомов водорода.
Первый постулат Бора
Первый постулат Бора также носит название постулата стационарных состояний:
Атомная система может находиться только в стационарных, или квантовых, состояниях, каждому из которых соответствует определенная энергия En. В стационарном состоянии атом не излучает электромагнитные волны.
Этот постулат находится в явном противоречии с классической механикой, согласно которой энергия движущегося электрона может быть любой. Он находится в противоречии и с электродинамикой, так как допускает возможность ускоренного движения электронов без излучения электромагнитных волн.
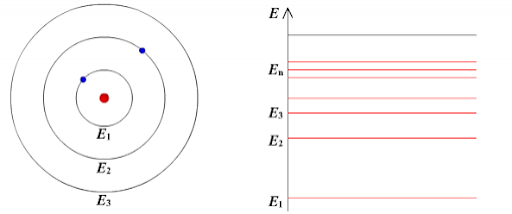
Согласно первому постулату Бора, атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию (см. рисунок ниже). Механическая энергия электрона, движущегося по замкнутой траектории вокруг положительно заряженного ядра, отрицательна. Поэтому всем стационарным состояниям соответствуют значения энергии En < 0. При En ≥ 0 электрон удаляется от ядра, т. е. происходит ионизация. Величина |E1| называется энергией ионизации.
Второй постулат Бора
Второй постулат Бора также носит название правила частот:
Излучение света происходит при переходе атома из стационарного состояния с большей энергией Ek в стационарное состояние с меньшей энергией En. Энергия излученного фотона равна разности энергий стационарных состояний.
Разность энергий стационарных состояний можно вычислить по формуле:
E=hν
hνkn=Ek−En
Внимание! В квантовой физике энергию принято измерять не в Джоулях, а в электрон-вольтах, обозначаемых «эВ». 1 эВ равен энергии, приобретаемой электроном при прохождении разницы потенциалов 1 В. 1 эВ = 1,6∙10–19 Дж.
Отсюда можно выразить частоту излучения:
νkn=Ek−Enh
Наименьшей энергии En соответствует состояние атома, которое называется основным, а наибольшей энергии Ek — возбужденное состояние атома. В основном состоянии электрон может находиться неограниченно долго, а в остальных состояниях не более 10-8 с.
Если атом переходит из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией (Ek > En), происходит излучение фотона. Если атом переходит из стационарного состояния с меньшей энергией в стационарное состояние с большей энергией (Ek < En), происходит поглощение фотона.
Второй постулат Бора позволил объяснить линейчатую структуру атомных спектров. Ведь атом, как оказалось, может поглощать и излучать свет только определенных частот.
Этот постулат Бора также противоречит электродинамике Максвелла, так как частота излучения определяется только изменением энергии атома и никак не зависит от характера движения электрона.
Пример №1. Определите длину волны света, испускаемого атомом водорода при его переходе из стационарного состояния с энергией E4 = –0,85 эВ (k = 4) в состояние с энергией E2 = –3,4 эВ (n = 2).
Длина волны определяется формулой:
λ=cν
Частоту найдем по формуле:
νkn=Ek−Enh
Следовательно, длина волны равна:
Теория Бора при описании поведения атомных систем не отвергла полностью законы классической физики. В ней сохранились представления об орбитальном движении электронов в кулоновском поле ядра. Классическая ядерная модель атома Резерфорда в теории Бора была дополнена идеей о квантовании электронных орбит. Поэтому теорию Бора иногда называют полуклассической.
Задание EF17570
Ответ:
а) с уровня 1 на уровень 5
б) с уровня 5 на уровень 2
в) с уровня 5 на уровень 1
г) с уровня 2 на уровень 1
Алгоритм решения
- Сформулировать второй постулат Бора.
- Определить, при переходе с какого на какой уровень выделяется фотон с максимальной энергией.
Решение
Излучение света происходит при переходе атома из стационарного состояния с большей энергией Ek в стационарное состояние с меньшей энергией En. Энергия излученного фотона равна разности энергий стационарных состояний.
Причем чем на более высоком уровне находится электрон, тем с более высокой энергией фотон он испускает при переходе на 1 уровень. Поэтому на рисунке нам подходит переход с уровня 5 на уровень 1.
Ответ: в
pазбирался: Алиса Никитина | обсудить разбор | оценить
Задание EF17650
В сосуде находится разреженный атомарный водород. Атом водорода в основном состоянии (Е1 = – 13,6 эВ) поглощает фотон частотой 3,7⋅1015 Гц. С какой скоростью υ движется вдали от ядра электрон, вылетевший из атома в результате ионизации? Энергией теплового движения атомов водорода пренебречь.
Ответ:
а) 80 км/с
б) 380 км/с
в) 760 км/с
г) 1530 км/с
Алгоритм решения
1.Записать исходные данные.
2.Записать второй постулат Бора в математической форме.
3.Выполнить решение в общем виде.
4.Подставить известные данные и вычислить искомую величину.
Решение
Запишем исходные данные:
• Энергия стационарного состояния: En = –13,6 эВ.
• Частота поглощенного фотона: νkn = 3,7∙1015 Гц.
Запишем второй постулат Бора в математической форме:
hνkn=Ek−En
Скорость электрона мы можем посчитать, если примем энергию электрона в возбужденном состоянии за его кинетическую энергию. Тогда формула примет вид:
hνkn=mv22−En
Сделаем несколько преобразований, чтобы выразить скорость электрона:
mv22=hνkn+En
v2=2(hνkn+En)m
v=√2(hνkn+En)m
Учтем, что:
• Масса электрона: m = 9,1∙10–31 кг.
Тогда:
Ответ: в
pазбирался: Алиса Никитина | обсудить разбор | оценить
Задание EF17726
Покоящийся атом излучает фотон с энергией 16,32·10–19 Дж в результате перехода электрона из возбуждённого состояния в основное. Атом в результате отдачи начинает двигаться поступательно в противоположном направлении с кинетической энергией 8,81·10–27 Дж. Найдите массу атома. Скорость атома считать малой по сравнению со скоростью света.
Алгоритм решения
1.Записать исходные данные.
2.Записать закон сохранения импульса.
3.Выполнить решение в общем виде.
4.Подставить известные данные и вычислить искомую величину.
Решение
Запишем исходные данные:
• Энергия излученного фотона: Eф = 16,32∙10–19 Дж.
• Кинетическая энергия атома после излучения фотона: Eа = 8,81∙10–27 Дж.
Так как до излучения фотона атом покоился, то его импульс был равен нулю. Поэтому после излучения фотона суммарный импульс согласно закону сохранения импульса тоже должен быть равен нулю. Поэтому импульс атома равен по модулю импульсу излученного фотона:
pа=pф
Импульс тела и его кинетическая энергия — связанные величины. Но скорость атома много меньше скорости света. Поэтому для атома связь импульса с кинетической энергией будет описываться нерелятивистским выражением:
Eа=p2а2mа
Отсюда импульс, обретенный атомом, равен:
pа=√2mаEа
Фотон двигается со скоростью света, и его импульс может быть выражен из следующей его связи с энергией:
Eф=pфc
Тогда импульс фотона равен:
pф=Eфc
Приравняем импульсы атома и фотона:
√2mаEа=Eфc
Возведем обе части выражения в квадрат, выразим и посчитаем массу атома:
2mаEа=E2фc2
pазбирался: Алиса Никитина | обсудить разбор | оценить
Алиса Никитина | Просмотров: 3.1k