Подготовка к ЕГЭ
Фтор
F2 – фтор.
Галоген. Газ светло –зелёного цвета, с характерным резким запахом — в жидком
состоянии- светло – жёлтый. Растворяется в жидком фтороводороде.
Физические
характеристики фтора:
Плотность 1,7 г/л.
Температура
плавления 53,53 К.
Температура
кипения 85,03 К.
Как и многие
элементы, фтор сначала был «предсказан» теоретически, как атом плавиковой
кислоты (которую открыл в 1771 году Карл Шееле) в 1810 году, и только в конце
XIX столетия Анри Муассан выделил фтор в свободном виде. Своим названием фтор обязан
древнегреческому слову φθόρος которое переводится как разрушение.
Физиологическое
действие фтора
·
укрепляет
иммунитет, костный скелет и зубную эмаль,
·
обеспечивает
рост волос и ногтей,
·
стимулирует
процессы кроветворения,
·
выводит
радикалы и тяжёлые металлы,
·
предупреждает
развитие остеопороза,
·
предотвращает
развитие кариеса.
Суточная
потребность во фторе
Суточная
норма во фторе увеличивается по мере роста человека, от 0,5 до 0,9 мг у детей и
1,5-4 мг у взрослых женщин и мужчин.
Продукты питания
богатые фтором
Основной
источник фтора – питьевая вода, далее идут зелёный и чёрный чай, грецкие орехи, морепродукты, молоко, яйца, репчатый лук, чечевица, овсянка, гречка и рис, картофель, зелёные листовые
овощи и говяжья печень.
Основными
признаками нехватки фтора являются заболевания зубов и дёсен – пародонтоз и
кариес.
Признаками
переизбытка фтора в организме человека являются замедление обмена веществ,
поражение эмали зубов, деформация костей скелета, тошнота и рвота.
Промышленное
применение
В атомарном и
молекулярном состоянии фтор используется для плазменного травления в
производстве полупроводников, плоских дисплеев и микроэлектромеханических
систем. Плавиковая кислота применяется для травления стекла в лампах и других
изделиях. Наряду с некоторыми из его соединений, фтор – это важная составляющая
производства фармацевтических препаратов, агрохимикатов, горюче-смазочных
материалов и текстиля. Химический элемент необходим для получения
галогенированных алканов (галоны), которые, в свою очередь, широко
использовались в системах кондиционирования воздуха и охлаждения. Позже такое
применение хлорфторуглеродов было запрещено, поскольку они способствуют
разрушению озонового слоя в верхних слоях атмосферы. Соединения фтора, в том
числе NaF, используются в зубных пастах для предотвращения кариеса. Эти
вещества добавляются в системы муниципального водоснабжения для фторирования
воды, однако из-за воздействия на здоровье человека эта практика считается
спорной. При более высоких концентрациях NaF используются в качестве
инсектицида, особенно для борьбы с тараканами.
Получение
В
лабораторных условиях фтор можно получать с помощью электролиза. В медный сосуд
1, заполненный расплавом KF·3HF помещают медный сосуд 2, имеющий отверстия в
дне. В сосуд 2 помещают толстый никелевый анод. Катод помещается в сосуд 1.
Таким образом, в процессе электролиза, газообразный фтор выделяется из трубки
3, а водород из трубки 4. Важным требованием является обеспечение герметичности
системы, для этого используют пробки из фторида кальция со смазкой из оксида
свинца (II) и глицерина. В 1986 году, во время подготовки к конференции по
поводу празднования 100-летия открытия фтора, Карл Кристе открыл способ чисто
химического получения фтора с использованием реакции во фтороводородном
растворе K2MnF6 и SbF5 при 150 °C:
K2MnF6 + 2SbF5 = 2KSbF6 +
MnF3 + F2
Хотя этот метод не имеет практического применения, он демонстрирует, что
электролиз необязателен.
Промышленное производство фтора осуществляется электролизом расплава кислого
фторида калия KF·3HF (часто с добавлениями фторида лития) при температуре около
100°С в стальных электролизёрах со стальным катодом и угольным анодом.
Химические свойства фтора
Сильнейший
окислитель, при обычных условиях энергично взаимодействует с металлами,
неметаллами (кроме гелия, неона и аргона), водой, кислотами, щелочами и
аммиаком. Образует многочисленные соединения с другими галогенами. Фтор,
взаимодействуя с водородом, взрывается даже при низкой температуре и в темноте.
Он бурно реагирует с водой, образуя плавиковую кислоту и газообразный кислород.
Различные материалы, в том числе мелкодисперсные металлы и стекла, в струе
газообразного фтора горят ярким пламенем. Кроме того, данный химический элемент
образует соединения с благородными газами криптоном, ксеноном и радоном. Однако
непосредственно с азотом и кислородом он не реагирует (только при электрических
разрядах)
F2 + H2O (холод,
лёд) = HOF + HF
F2 + H2O = 2HF + O0
4F2 + 6NaOH (разбавленный)=
OF2 +6NaF + O2 + 3H2O
F2 + H2 = 2 HF (в
темноте)
5F2 + CI2 = 2CIF5 (CI2 и Br2
при 2000 C, I2 при
комнатной температуре)
3F2 + S = SF6
F2+ О2
= О2F2
(электрический разряд)
3F2 + N2 = 2NF6 (при
электрическом разряде)
5F2 +2 P (красный)
= 2PF5
F2 + Xe = XeF2
F2 + 8NH3 (газ) = N2 + 5NH4F (горение
аммиака в атмосфере фтора при 1300 C)
2
F2 + SiO2 = SiF4 + O2
2
F2 + 2Na2CO3 = 4NaF +2CO2 +O2
Горят
в атмосфере фтора и металлы: натрий, калий, кальций, магний, алюминий, даже
золота и платина при нагревании до 3000 С. Однако следует отметить,
что некоторые металлы (Fe, Сu, Al, Ni, Mg, Zn) реагируют с фтором с
образованием защитной плёнки фторидов, препятствующей дальнейшей реакции
F2 +Na = 2NaF
В
азотной кислота фтор замещает водород и образует триоксифторид азота
2
F2 + 2HNO3 = 2NO3F + H2F2
F2
сильнейший окислитель
F2
+ NaBrO3 + 2NaOH = 2NaF + NaBrO4 + H2O
1 Br+5 – 2e → Br+7
1 F2 + 2e → 2F—
Литература:
1. Хомченко
Г.П., Цитович И.Н. Неорганическая химия. Москва, Высшая школа, 1978 год
2. Химия.
Справочник (под редакцией В.Д. Орлова). Харьков: Фолио; Ростов на Дону; Феникс,
1997 год
3. Лидин
Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ,
Москва, «Химия», 200 год
1. Положение галогенов в периодической системе химических элементов
2. Электронное строение галогенов
3. Физические свойства и нахождение в природе
4. Соединения галогенов
5. Способы получения галогенов
6. Химические свойства
6.1. Взаимодействие с простыми веществами
6.1.1. Взаимодействие с кислородом
6.1.2. Взаимодействие с серой
6.1.3. Взаимодействие с серой и фосфором
6.1.4. Взаимодействие с металлами
6.1.5. Взаимодействие с водородом
6.1.6. Взаимодействие с галогенами
6.2. Взаимодействие со сложными веществами
6.2.1. Взаимодействие с водой
6.2.2. Взаимодействие с щелочами
6.2.3. Взаимодействие с солями и галогеноводородами
6.2.4. Взаимодействие с восстановителями
Галогеноводороды
1. Строение молекулы и физические свойства
2. Способы получения
3. Химические свойства
3.1. Кислотные свойства
3.2. Диссоциация
3.3. Взаимодействие с солями
3.4. Восстановительные свойства
3.5. Взаимодействие с оксидом кремния (IV)
Соли-галогениды
Способы получения галогенидов
Химические свойства галогенидов
Кислородсодержащие кислоты галогенов
1. Хлорноватистая кислота и ее соли
2. Хлористая кислота и ее соли
3. Хлорноватая кислота и ее соли
4. Хлорная кислота и ее соли
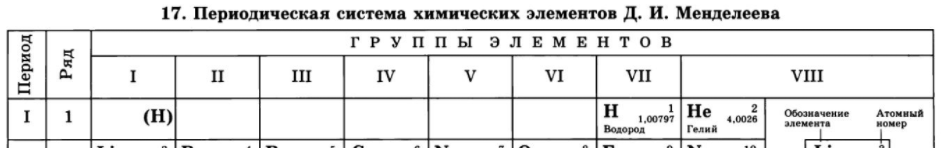
Галогены
Положение в периодической системе химических элементов
Галогены расположены в главной подгруппе VII группы (или в 17 группе в современной форме ПСХЭ) периодической системы химических элементов Д.И. Менделеева.
Электронное строение галогенов
Электронная конфигурация галогенов в основном состоянии соответствует формуле ns2np5.
Например, электронная конфигурация фтора:
Электронная концигурация хлора:
Атомы галогенов содержат на внешнем энергетическом уровне 1 неспаренный электрон и три неподеленные электронные пары в основном энергетическом состоянии. Следовательно, в основном состоянии атомы галогенов могут образовывать 1 связи по обменному механизму.
При этом у фтора возбужденного состояния нет, т.е. максимальная валентность фтора в соединения равна I.
Однако, в отличие от фтора, за счет вакантной d-орбитали атомы хлора, брома и йода могут переходить в возбужденное энергетическое состояние.
Таким образом, максимальная валентность галогенов (кроме фтора) в соединениях равна VII. Также для галогенов характерны валентности I, III, V.
Степени окисления атома галогенов – от -1 до +7. Характерные степени окисления -1, 0, +1, +3, +5, +7. Для фтора характерная степень окисления -1 и валентность I.
Физические свойства и закономерности изменения свойств
Галогены образуют двухатомные молекулы состава Hal2. В твёрдом состоянии имеют молекулярную кристаллическую решетку. Плохо растворимы в воде, все имеют запах, летучи.
| Галоген | F | Cl | Br | I |
| Электронная формула | … 2s22p5 | … 3s23p5 | … 4s24p5 | … 5s25p5 |
| Электроотрицательность | 4,0 | 3,0 | 2,8 | 2,5 |
| Степени окисления | -1 | -1, +1, +3, +5, +7 | -1, +1, +3, +5, +7 | -1, +1, +3, +5, +7 |
| Агрегатное состояние | Газ | Газ | Жидкость | Твердые кристаллы |
| Цвет | Светло-желтый | Жёлто-зелёный | Буровато-коричневый | Тёмно-серый с металлическим блеском |
| Запах | Резкий | Резкий, удушливый | Резкий, зловонный | Резкий |
| T плавления | –220оС | –101оС | –7оС | 113,5оС |
| Т кипения | –188оС | –34оС | 58оС | 185оС |
Внешний вид галогенов:
Фтор
Хлор
Бром
Йод
В природе галогены встречаются в виде соединений, в основном, в виде галогенидов.
Соединения галогенов
Типичные соединения хлора:
| Степень окисления | Типичные соединения |
| +7 | Хлорная кислота HClO4
Перхлораты MeClO4 |
| +5 | Хлорноватая кислота HClO3
Хлораты MeClO3 |
| +3 | Хлористая кислота HClO2 |
| +1 | Хлорноватистая кислота HClO
Гипохлориты MeClO |
| –1 | Хлороводород HCl, Хлориды MeCl |
Бром и йод образуют подобные соединения.
Способы получения галогенов
1. Получение хлора.
В промышленности хлор получают электролизом расплава или раствора хлорида натрия.
Электролиз расплава хлорида натрия.
В расплаве хлорид натрия диссоциирует на ионы:
NaCl → Na+ + Cl−
На катоде восстанавливаются ионы натрия:
K(–): Na+ +1e → Na0
На аноде окисляются ионы хлора:
A(+): 2Cl− ̶ 2e → Cl20
Ионное уравнение электролиза расплава хлорида натрия:
2Na+ + 2Cl− → 2Na º + Cl2º
Суммарное уравнение электролиза расплава хлорида натрия:
2NaCl → 2Na + Cl2
Электролиз раствора хлорида натрия.
В растворе хлорид натрия диссоциирует на ионы:
NaCl → Na+ + Cl−
На катоде восстанавливаются молекулы воды:
K(–): 2H2O + 2e → H2° + 2OH−
На аноде окисляются ионы хлора:
A(+): 2Cl− ̶ 2e → Cl20
Ионное уравнение электролиза раствора хлорида натрия:
2H2O + 2Cl− → H2°↑ + 2OH− + Cl2°↑
Суммарное уравнение электролиза раствора хлорида натрия:
2NaCl + 2H2O → H2↑ + 2NaOH + Cl2↑
В лаборатории хлор получают взаимодействием концентрированной соляной кислоты с сильными окислителями.
Например, взаимодействием соляной кислоты с оксидом марганца (IV)
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
Или перманганатом калия:
2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2↑ + 8H2O
Бертолетова соль также окисляет соляную кислоту:
KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O
Бихромат калия окисляет соляную кислоту:
K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2↑ + 7H2O
2. Получение фтора.
Фтор получают электролизом расплава гидрофторида калия.
2KHF2 → 2K + H2 + 2F2
3. Получение брома.
Бром можно получить окислением ионов Br– сильными окислителями.
Например, бромоводород окисляется хлором:
2HBr + Cl2 → Br2 + 2HCl
Соединения марганца также окисляют бромид-ионы.
Например, оксид марганца (IV):
MnO2 + 4HBr → MnBr2 + Br2 + 2H2O
4. Получение йода.
Йод получают окислением ионов I– сильными окислителями.
Например, хлор окисляет йодид калия:
2KI + Cl2 → I2 + 2KCl
Соединения марганца также окисляют йодид-ионы.
Например, оксид марганца (IV) в кислой среде окисляет йодид калия:
2KI + MnO2 + 2H2SO4 → I2 + K2SO4 + MnSO4 + 2H2O
Химические свойства галогенов
Химическая активность галогенов увеличивается снизу вверх – от астата к фтору.
1. Галогены проявляют свойства окислителей. Галогены реагируют с металлами и неметаллами.
1.1. Галогены не горят на воздухе. Фтор окисляет кислород с образованием фторида кислорода:
2F2 + O2 → 2OF2
1.2. При взаимодействии галогенов с серой образуются галогениды серы:
S + Cl2 → SCl2 (S2Cl2)
S + 3F2 → SF6
1.3. При взаимодействии фосфора и углерода с галогенами образуются галогениды фосфора и углерода:
2P + 5Cl2 → 2PCl5
2P + 3Cl2 → 2PCl3
2F2 + C → CF4
1.4. При взаимодействии с металлами галогены проявляют свойства окислителей, образуя галогениды.
Например, железо реагирует с галогенами с образованием галогенидов. При этом фтор, хлор и бром образуются галогениды железа (III), а c йодом — соединение железа (II):
3Cl2 + 2Fe → 2FeCl3
I2 + Fe → FeI2
Аналогичная ситуация с медью: фтор, хлор и бром окисляют медь до галогенидов меди (II),а йод до йодида меди (I):
Cl2 + Cu → 2CuCl2
I2 + 2Cu → 2CuI
Активные металлы бурно реагируют с галогенами, особенно с фтором и хлором (горят в атмосфере фтора или хлора).
Еще пример: алюминий взаимодействует с хлором с образованием хлорида алюминия:
3Cl2 + 2Al → 2AlCl3
1.5. Водород горит в атмосфере фтора:
F2 + H2 → 2HF
С хлором водород реагирует только при нагревании или освещении. При этом реакция протекает со взрывом:
Cl2 + H2 → 2HCl
Бром также реагирует с водородом с образованием бромоводорода:
Br2 + H2 → 2HBr
Взаимодействие йода с водородом происходит только при сильном нагревании, реакция протекает обратимо, с поглощением теплоты (эндотермическая):
I2 + H2 ↔ 2HI
1.6. Галогены реагируют с галогенами. Более активные галогены окисляют менее активные.
Например, фтор окисляет хлор, бром и йод:
Cl2 + F2 → 2ClF
2. Со сложными веществами галогены реагируют, также проявляя преимущественно окислительные свойства. Галогены охотно диспропорционируют при растворении в воде или в щелочах.
2.1. При растворении в воде хлор и бром частично диспропорционируют, повышая и понижая степень окисления. Фтор окисляет воду.
Например, хлор при растворении в холодной воде диспропорционирует до ближайших стабильных степеней окисления (+1 и -1), образует при этом соляную кислоту и хлорноватистую кислоту (хлорная вода):
Cl2 + H2O ↔ HCl + HClO
При растворении в горячей воде хлор диспропорционирует до степеней окисления -1 и +5, образуя соляную кислоту и хлороватую кислоту:
Cl2 + 6H2O ↔ 5HCl + HClO3
Фтор реагирует с водой со взрывом:
2F2 + 2H2O → 4HF + O2
2.2. При растворении в щелочах хлор, бром и йод диспропорционируют с образованием различных солей. Фтор окисляет щелочи.
Например, хлор реагирует с холодным раствором гидроксидом натрия:
Сl2 + 2NaOH (хол.) → NaCl + NaClO + H2O
При взаимодействии с горячим раствором гидроксида натрия образуются хлорид и хлорат:
3Cl2 + 6NaOH (гор.) → 5NaCl + NaClO3 + 3H2O
Еще пример: хлор растворяется в холодном растворе гидроксида кальция:
2Сl2 + 2Са(OH)2(хол.) → СaCl2 + Сa(ClO)2 + 2H2O
2.3. Более активные галогены вытесняют менее активные галогены из солей и галогеноводородов.
Например, хлор вытесняет йод и бром из раствора йодида калия и бромида калия соответственно:
Cl2 + 2NaI → 2NaCl + I2
Cl2 + 2NaBr → 2NaCl + Br2
Еще одно свойство: более активные галогены окисляют менее активные.
Например, фтор окисляет хлор с образованием фторида хлора (I):
Cl2 + F2 → 2Cl+F–
В свою очередь, хлор окисляет йод. При этом в растворе образуется соляная кислота и йодная кислота:
Cl2 + I2 + H2O → HCl + HIO3
2.4. Галогены проявляют окислительные свойства, взаимодействуют с восстановителями.
Например, хлор окисляет сероводород:
Cl2 + H2S → S + 2HCl
Хлор также окисляет сульфиты:
Cl2 + H2O + Na2SO3 → 2HCl + Na2SO4
Также галогены окисляют пероксиды:
Cl2 + H2O2 → 2HCl + O2
Или, при нагревании или на свету, воду:
2Cl2 + 2H2O → 4HCl + O2 (на свету или кип.)
Галогеноводороды
Строение молекулы и физические свойства
Галогеноводороды HHal – это бинарные соединения водорода с галогенами, которые относятся к летучим водородным соединениям. Галогеноводороды – бесцветные ядовитый газы, с резким запахом, хорошо растворимые в воде.
В ряду HCl – HBr – HI увеличивается длина связи и ковалентности связи уменьшается полярность связи H – Hal.
Растворы галогеноводородов в воде (за исключением фтороводорода) – сильные кислоты. Водный раствор фтороводорода – слабая кислота.
Способы получения галогеноводородов
В лаборатории галогеноводороды получают действием нелетучих кислот на хлориды металлов.
Например, действием концентрированной серной кислоты на хлорид натрия:
H2SO4(конц.) + NaCl(тверд.) → NaHSO4 + HCl↑
Галогеноводороды получают также прямым взаимодействием простых веществ:
Cl2 + H2 → 2HCl
Химические свойства галогеноводородов
1. В водном растворе галогеноводороды проявляют кислотные свойства. Взаимодействуют с основаниями, основными оксидами, амфотерными гидроксидами, амфотерными оксидами. Кислотные свойства в ряду HF – HCl – HBr – HI возрастают.
Например, хлороводород реагирует с оксидом кальция, оксидом алюминия, гидроксидом натрия, гидроксидом меди (II), гидроксидом цинка (II), аммиаком:
2HCl + CaO → CaCl2 + H2O
6HCl + Al2O3 → 2AlCl3 + 3H2O
HCl + NaOH → NaCl + H2O
2HCl + Cu(OH)2 → CuCl2 + 2H2O
2HCl + Zn(OH)2 → ZnCl2 + 2H2O
HCl + NH3 → NH4Cl
Как типичные минеральные кислоты, водные растворы галогеноводородов реагируют с металлами, расположенными в ряду активности металлов до водорода. При этом образуются соль металла и водород.
Например, соляная кислота растворяет железо. При этом образуется водород и хлорид железа (II):
Fe + 2HCl → FeCl2 + H2
2. В водном растворе галогеноводороды диссоциируют, образуя кислоты. Водный раствор фтороводорода (плавиковая кислота) – слабая кислота:
HF ↔ H+ + F–
Водные растворы хлороводорода (соляная кислота), бромоводорода и йодоводорода – сильные кислоты, в разбавленном растворе диссоциируют практически полностью:
HCl ↔ H+ + Cl–
3. Водные растворы галогеноводородов взаимодействуют с солями более слабых кислот и с некоторыми растворимыми солями (если образуется газ, осадок, вода или слабый электролит).
Например, соляная кислота реагирует с карбонатом кальция:
2HCl + CaCO3 → CaCl2 + 2H2O + CO2
Качественная реакция на галогенид-ионы – взаимодействие с растворимыми солями серебра.
При взаимодействии соляной кислоты с нитратом серебра (I) образуется белый осадок хлорида серебра:
HCl + AgNO3 = AgCl↓ + HNO3
Осадок бромида серебра – бледно-желтого цвета:
HBr + AgNO3 = AgBr↓ + HNO3
Осадок иодида серебра – желтого цвета:
HI + AgNO3 = AgI↓ + HNO3
Фторид серебра – растворимая соль, поэтому реакция плавиковой кислоты и ее солей с нитратом серебра не является качественной.
Видеоопыты качественных реакций на хлорид-, бромид- и йодид-ионы (взаимодействие с нитратом серебра) можно посмотреть здесь.
4. Восстановительные свойства галогеноводородов усиливаются в ряду HF – HCl – HBr – HI.
Галогеноводороды реагируют с галогенами. При этом более активные галогены вытесняют менее активные.
Например, бром вытесняет йод из йодоводорода:
Br2 + 2HI → I2 + 2HBr
А вот хлор не может вытеснить фтор из фтороводорода.
Фтороводород практически невозможно окислить.
Концентрированная соляная кислота окисляется соединениями марганца с валетностью выше II или соединениями хрома (VI).
Например: концентрированная соляная кислота окисляется оксидом марганца (IV):
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
Бромоводород – сильный восстановитель и окисляется соединениями марганца, хрома (VI), концентрированной серной кислотой и другими сильными окислителями:
Например, бромоводород окисляется концентрированной серной кислотой:
2HBr + H2SO4(конц.) → Br2 + SO2 + 2H2O
Бромоводород реагирует с бихроматом калия с образованием молекулярного брома:
14HBr + K2Cr2O7 → 2KBr + 2CrBr3 + 3Br2 + 7H2O
Или с оксидом марганца (IV):
4HBr + MnO2 → MnBr2 + Br2 + 2H2O
Пероксид водорода также окисляет бромоводород до молекулярного брома:
2HBr + H2O2 → Br2 + 2H2O
Йодоводород – еще более сильный восстановитель, и окисляется другими неметаллами и даже такими окислителями, как соединения железа (III) и соединения меди (II).
Например, йодоводород реагирует с хлоридом железа (III) с образованием молекулярного йода:
2HI + 2FeCl3 → I2 + 2FeCl2 + 2HCl
или с сульфатом железа (III):
2HI + Fe2(SO4)3 → 2FeSO4 + I2 + H2SO4
Йодоводород легко окисляется соединениями азота, например, оксидом азота (IV):
2HI + NO2 → I2 + NO + H2O
или молекулярной серой при нагревании:
2HI + S → I2 + H2S
5. Плавиковая кислота реагирует с оксидом кремния (IV) (растворяет стекло):
SiO2 + 4HF → SiF4 + 2H2O
SiO2 + 6HF(изб) → H2[SiF6] + H2O
Галогениды металлов
Галогениды – это бинарные соединения галогенов и металлов или некоторых неметаллов, соли галогеноводородов.
Способы получения галогенидов
1. Галогениды металлов получают при взаимодействии галогенов с металлами. При этом галогены проявляют свойства окислителя.
Например, хлор взаимодействует с магнием и кальцием:
Cl2 + Mg → MgCl2
Cl2 + Ca → CaCl2
При взаимодействии железа с хлором образуется хлорид железа (III):
3Cl2 + 2Fe → 2FeCl3
2. Галогениды металлов можно получить при взаимодействии металлов с галогеноводородами.
Например, соляная кислота реагирует с железом с образованием хлорида железа (II):
Fe + 2HCl → FeCl2 + H2
3. Галогениды металлов можно получить при взаимодействии основных и амфотерных оксидов с галогеноводородами.
Например, при взаимодействии оксида кальция и соляной кислоты:
2HCl + CaO → CaCl2 + H2O
Еще пример: взаимодействие оксида алюминия с соляной кислотой:
6HCl + Al2O3 → 2AlCl3 + 3H2O
4. Галогениды металлов можно получить при взаимодействии оснований и амфотерных гидроксидов с галогеноводородами.
Например, при взаимодействии гидроксида натрия и соляной кислоты:
HCl + NaOH → NaCl + H2O
Или при взаимодействии гидроксида меди (II) с соляной кислотой:
2HCl + Cu(OH)2 → CuCl2 + 2H2O
Гидроксид цинка (II) также взаимодействует с соляной кислотой:
2HCl + Zn(OH)2 → ZnCl2 + 2H2O
5. Некоторые соли взаимодействуют с галогеноводородами с образованием галогенидов металлов.
Например, гидрокарбонат натрия реагирует с бромоводородом с образованием бромида натрия:
HBr + NaHCO3 → NaBr + CO2↑ + H2O
Взаимодействие с нитратом серебра – качественная реакция на соляную кислоту, бромодоводород и йодоводород:
HCl + AgNO3 → AgCl↓ + HNO3
HBr + AgNO3 → AgBr↓ + HNO3
HI + AgNO3 → AgI↓ + HNO3
Химические свойства галогенидов
1. Растворимые галогениды вступают в обменные реакции с растворимыми солями, кислотами и основаниями, если образуется осадок, газ или вода.
Например, бромиды, йодиды и хлориды реагируют с нитратом серебра с образованием желтого, желтого и белого осадков соответственно.
NaCl + AgNO3 → AgCl↓ + NaNO3
Фторид серебра – растворимая соль, поэтому реакция фторидов с нитратом серебра не является качественной.
Видеоопыты качественных реакций на хлорид-, бромид- и йодид-ионы (взаимодействие с нитратом серебра) можно посмотреть здесь.
2. Галогениды тяжелых металлов реагируют с более активными металлами. При этом более активные металлы вытесняют менее активные.
Например, магний вытесняет медь из расплава хлорида меди (II):
Mg + CuCl2 → MgCl2 + Cu
Обратите внимание! В растворе более активные металлы вытесняют менее активные только если более активные металлы не взаимодействуют с водой (металлы, расположенные в ряду активности до магния). Если добавляемый металл слишком активен, то он провзаимодействует с водой, а не с солью.
Например, натрий не вытесняет цинк из раствора хлорида цинка. Т.к. натрий реагирует с водой, а реакция с хлоридом цинка не идет.
Na + ZnCl2(раствор) ≠
3. Галогениды подвергаются электролизу в растворе или расплаве. При этом на аноде образуются галогены.
Например, при электролизе расплава бромида калия на катоде образуется клий, а на аноде – бром:
2KBr → 2K + Br2
При электролизе раствора бромида калия на катоде выдялется водород, а на аноде также образуется бром:
2KBr + 2H2O → H2↑ + 2KOH + Br2↑
4. Галогениды металлов проявляют восстановительные свойства. Хлориды окисляются только сильными окислителями, а вот йодиды уже являются очень сильными восстановителями. В целом, восстановительные свойства галогенидов аналогичны свойствам галогеноводородов.
Например, бромид калия окисляется концентрированной серной кислотой:
2KBr + 2H2SO4 (конц.) → 4K2SO4 + 4Br2 + SO2 + 2H2O
Еще пример: йодид калия окисляется соединениями меди (II) и соединениями железа (III):
4KI + 2CuCl2 → 2CuI↓ + I2↓ + 4KCl
2KI + 2FeCl3 → I2↓ + 2FeI2 + 2KCl
Еще несколько примеров восстановительных свойств галогенидов:
8KI + 5H2SO4 (конц.) → 4K2SO4 + 4I2 + H2S + 4H2O или
8KI + 9H2SO4 (конц.) → 4I2↓ + H2S↑ + 8KHSO4 + 4H2O
KI + 3H2O + 3Cl2 → HIO3 + KCl + 5HCl
10KI + 8H2SO4 + 2KMnO4 → 5I2 + 2MnSO4 + 6K2SO4 + 8H2O
6KI + 7H2SO4 + K2Cr2O7 → Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O
2KI + H2SO4 + H2O2 → I2 + K2SO4 + 2H2O
2KI + Fe2(SO4)3 → I2 + 2FeSO4 + K2SO4
2KI + 2CuSO4 + K2SO3 + H2O → 2CuI + 2K2SO4 + H2SO4
Более активные галогены вытесняют менее активные из солей.
При этом галогениды металлов не горят в кислороде.
5. Нерастворимые галогениды металлов растворяются под действием избытка аммиака.
Например, хлорид серебра (I) растворяется под действием избытка раствора аммиака:
AgCl + NH3 → [Ag(NH3)2]Cl
6. Нерастворимые галогениды под действием света разлагаются на галоген и металл.
Например, хлорид серебра разлагается под действием ультрафиолета:
2AgCl → 2Ag + Cl2
Кислородсодержащие кислоты галогенов
Рассмотрим кислородсодержащие кислоты галогенов на примере хлора:
| Степень окисления галогена | +1 | +3 | +5 | +7 |
| Формула | HClO | HClO2 | HClO3 | HClO4 |
| Название кислоты | Хлорноватистая | Хлористая | Хлорноватая | Хлорная |
| Устойчивость и сила | Существует только в растворах, слабая кислота | Существует только в растворах, слабая кислота | Существует только в растворах, сильная кислота | Сильная кислота |
| Название соответствующей соли | Гипохлориты | Хлориты | Хлораты | Перхлораты |
Хлорноватистая кислота и ее соли
Хлорноватистая кислота HClO устойчива только в разбавленном водном растворе.
Cпособ получения хлорноватистой кислоты:
1. Диспропорционирование хлора в холодной воде:
Cl2 + H2O ↔ HCl + HClO
Химические свойства хлорноватистой кислоты:
Хлорноватистая кислота HClO – это слабая кислота, но сильный окислитель.
1. Под действием ультрафиолета (на свету) хлорноватистая кислота разлагается:
2HClO → 2HCl + O2
2. Как кислота, хлорноватистая кислота реагирует с сильными основаниями.
Например, с гидроксидом калия:
HClO + KOH → KClO + H2O
3. Ярко выражены окислительные свойства хлорноватистой кислоты за счет атома хлора в степени окисления +1. При взаимодействии с восстановителями хлор, как правило, восстанавливается до степени окисления -1.
Например, хлорноватистая кислота окисляет йодоводород:
HClO + 2HI → HCl + I2 + H2O
Хлорноватистая кислота также окисляет, например, пероксид водорода:
HClO + H2O2 → HCl + H2O + O2
4. Хлорноватистая кислота диспропорционирует:
3HClO → 2HCl + НСlO3
Химические свойства солей хлорноватистой кислоты (гипохлоритов):
1. Более сильные кислоты вытесняют гипохлориты из солей.
Например, соляная кислота реагирует с гипохлоритом натрия:
NaClO + 2HCl → NaCl + Cl2 + H2O
Серная кислота реагирует с гипохлоритом кальция при нагревании или под действием излучения:
Ca(ClO)2 + H2SO4 → CaSO4 + 2HCl + O2
Даже угольная кислота вытесняет гипохлориты:
Ca(ClO)2 + CO2 + H2O → CaCO3 + 2HClO
2. Гипохлориты вступают в обменные реакции с другими солями, если образуется слабый электролит.
Например, гипохлорит кальция реагирует с растворимыми карбонатами:
Ca(ClO)2 + Na2CO3 → CaCO3 + 2NaClO
3. При нагревании гипохлориты разлагаются:
Ca(ClO)2 → CaCl2 + O2
Хлористая кислота и ее соли
Хлористая кислота HClO2 – существует только в водных растворах.
Способы получения:
Хлористую кислоту можно получить окислением оксида хлора пероксидом водорода:
2ClO2 + H2O2 → 2HClO2 + O2
Химические свойства хлористой кислоты:
1. Хлористая кислота является также слабой. Реагирует с щелочами с образованием хлоритов:
HClO2 + KOH → KClO2 + H2O
2. При длительном хранении разлагается:
4HClO2 → HCl + HClO3 + 2ClO2 + H2O
Хлорноватая кислота и ее соли
Хлорноватая кислота HClO3 – также существует только в водных растворах.
Способы получения:
Хлорноватую кислоту можно получить из солей хлорноватой кислоты – хлоратов.
Например, из хлората бария под действием серной кислоты:
Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4
Химические свойства хлорноватой кислоты:
1. Хлорноватая кислота – сильная кислота. Реагирует с щелочами с образованием хлоратов:
HClO3 + KOH → KClO3 + H2O
2. Хлорноватая кислота – сильный окислитель.
Например, хлорноватая кислота окисляет фосфор:
6P + 5HClO3 → 3P2O5 + 5HCl
Химические свойства солей хлорноватой кислоты – хлоратов:
1. Хлораты – сильные окислители.
Например, хлорат калия (бертолетова соль) при нагревании разлагается. При этом без катализатора хлорат диспропорционирует:
4KClO3 → 3KClO4 + KCl
В присутствии катализатора (оксид марганца (IV)) хлорат калия разлагается, окисляя кислород:
2KClO3 → 2KCl + 3O2↑
Еще пример: хлорат калия окисляет серу и фосфор:
2KClO3 + 3S → 2KCl + 3SO2
5KClO3 + 6P → 5KCl + 3P2O5
Хлорная кислота и ее соли
Хлорная кислота HClO4 – это бесцветная жидкость, хорошо растворимая в воде.
Способы получения:
Хлорную кислоту можно получить из солей хлорной кислоты – перхлоратов.
Например, из перхлората натрия под действием серной кислоты:
2NaClO4 + H2SO4 → 2HClO4 + Na2SO4
Химические свойства хлорной кислоты:
1. Хлорная кислота – сильная кислота. Реагирует с щелочами с образованием перхлоратов:
HClO4 + KOH → KClO4 + H2O
2. Хлорная кислота – сильный окислитель.
Например, хлорная кислота окисляет углерод:
8HClO4 + 14C → 14CO2 + 4Cl2 + 4H2O
3. При нагревании хлорная кислота разлагается:
4HClO4 → 4ClO2 + 3O2 + 2H2O
Химические свойства солей хлорной кислоты – перхлоратов:
1. Перхлораты – сильные окислители.
Например, перхлорат калия при нагревании разлагается. При этом хлор окисляет кислород:
KClO4 → KCl + 2O2↑
Еще пример: перхлорат калия окисляет алюминий:
3KClO4 + 8Al → 3KCl + 4Al2O3
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством
других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.

Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств.
Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns2np5:
- F — 2s22p5
- Cl — 3s23p5
- Br — 4s24p5
- I — 5s25p5
- At — 6s26p5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов
в возбужденном состоянии.

Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит

Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают
электролизом водного раствора хлорида натрия.
NaCl + H2O → (электролиз) NaOH + H2↑ + Cl2↑
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
HF → F2 + H2
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
Cl2 + KBr → Br2 + KCl
Cl2 + KI → I2 + KCl

В лабораторных условиях галогены могут быть получены следующими реакциями.
HCl + MnO2 → MnCl2 + Cl2 + H2O
HCl + KMnO4 → MnCl2 + Cl2 + KCl + H2O
Химические свойства
- Реакции с металлами
- Реакции с неметаллами
- Реакции с водой
- Реакции с щелочами
- Окислительные способности
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере
фтора самовоспламеняются.
Al + F2 → AlF3
Cu + Cl2 → CuCl2
Na + Br2 → NaBr
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
Cl2 + Si → SiCl4
Cl2 + H2 → HCl (на свету)

F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F—)
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br—)
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
H2O + F2 → HF + O2
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Cl2 + H2O → HCl + HClO
H2O + Br2 → HBr + HBrO

Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при
нагревании.
Cl2 + NaOH → NaCl + NaClO + H2O
Cl2 + NaOH → (t) NaCl + NaClO3 + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KCl + F2 → KF + Cl2
KBr + Cl2 → KCl + Br2
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
Получение
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
H2 + Cl2 → HCl
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
NaCl + H2SO4 → NaHSO4 + HCl↑
CaF2 + H2SO4 → CaSO4 + HF
PBr3 + H2O → HBr↑ + H3PO3
H2S + I2 → S + HI
Химические свойства
- Кислотные свойства
- С солями
- Восстановительные свойства
- Реакция с оксидом кремния
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить
водород из кислоты.
Mg + HBr → MgBr2 + H2↑
Zn + HCl → ZnCl2 + H2↑

Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
Na2O + HCl → NaCl + H2O
ZnO + HI → ZnI2 + H2O
KOH + HCl → KCl + H2O (реакция нейтрализации)

Cr(OH)3 + HCl → CrCl3 + H2O
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
AgNO3 + HCl → AgCl + HNO3
Li2CO3 + HBr → LiBr + H2CO3
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
HI + MnO2 → I2 + MnI2 + H2O
HI + H2SO4 → I2 + H2S + H2O
HI + O2 → H2O + I2
HI + Br2 → HBr + I2
HBr + H2SO4 → Br2 + SO2 + H2O

В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с
плавиковой кислотой.
SiO2 + HF → SiF4 + H2O
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 121 1–20 | 21–40 | 41–60 | 61–80 …
Добавить в вариант
Из предложенного перечня выберите две пары веществ, в которых расположены только соединения с ковалентной неполярной связью.
1) азот и кислород
2) вода и аммиак
3) медь и азот
4) бром и метан
5) фтор и сера
Запишите в поле ответа номера выбранных пар веществ.
Источник: РЕШУ ЕГЭ
Задания Д3 № 321
Из перечисленных элементов наиболее электроотрицательным является
1) азот
2) кислород
3) хлор
4) фтор
Установите соответствие между формулой вещества и продуктами электролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) металл и галоген
3) металл, вода и кислород
4) водород и галоген
5) металл, углекислый газ и углеводород
6) водород, углекислый газ и углеводород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород, галоген
2) металл, кислород
3) металл, галоген
4) водород, кислород
5) металл, галоген, кислород
6) металл, водород, кислород
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: ЕГЭ по химии 2021. Основная волна. Вариант 1
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) водород и галоген
3) металл и кислород
4) металл и галоген
5) водород и оксид азота
6) металл, водород и кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и хлор
2) водород и кислород
3) металл и кислород
4) водород и хлор
5) водород, металл и кислород
6) водород, металл и хлор
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: ЕГЭ по химии 2021. Основная волна. Вариант 2
Установите соответствие между формулой вещества и продуктами электролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и кислород
2) металл и галоген
3) металл, вода и кислород
4) водород и кислород
5) металл, углекислый газ и углеводород
6) водород, углекислый газ и углеводород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и кислород
2) водород и галоген
3) металл и кислород
4) металл и галоген
5) водород и оксид азота
6) металл, водород и кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл, водород, кислород
2) водород, кислород
3) металл, водород, галоген
4) металл, галоген
5) водород, галоген
6) металл, кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по химии 2021. Досрочная волна. Вариант 1
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород и сернистый газ
2) металл и сероводород
3) водород и кислород
4) водород и галоген
5) металл и кислород
6) металл и галоген
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и продуктами электролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) (расплав)
Б) (расплав)
В) (раствор)
Г) (раствор)
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и кислород
2) металл и водород
3) металл, вода и кислород
4) водород и сернистый газ
5) металл, водород и кислород
6) водород и кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород, углекислый газ и этан
2) водород и кислород
3) водород и галоген
4) металл и кислород
5) металл и галоген
6) металл и углекислый газ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и галоген
2) водород и кислород
3) металл и кислород
4) водород и галоген
5) металл и водород
6) кислород и галоген
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по химии 2020. Основная волна. Вариант 2
Установите соответствие между формулой вещества и продуктами электролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ВЕЩЕСТВА
А) (расплав)
Б) (расплав)
В) (раствор)
Г) (раствор)
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и кислород
2) металл и водород
3) металл, вода и кислород
4) металл и хлор
5) водород и хлор
6) водород и кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой соли и продуктами электролиза водного раствора этого вещества, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл, кислород
2) металл, галоген
3) водород, кислород
4) водород, галоген
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2022 по химии
Установите соответствие между солью и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СОЛЬ
А) бромид лития
Б) сульфат калия
В) хлорид алюминия
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) водород, галоген
2) металл, кислород
3) металл, галоген
4) водород, кислород
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: ЕГЭ по химии 2022. Досрочная волна
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и хлор
2) водород и кислород
3) водород и азот
4) водород и хлор
5) металл и кислород
6) водород и углекислый газ
Запишите в таблицу выбранные цифры под соответствующими буквами.
Источник: ЕГЭ по химии 2019. Досрочная волна
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и хлор
2) водород и кислород
3) водород и азот
4) водород и хлор
5) металл и кислород
6) водород и углекислый газ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2020 по химии
Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) металл и хлор
2) водород и кислород
3) водород и азот
4) водород и хлор
5) металл и кислород
6) водород и углекислый газ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и продуктом(-ами) электролиза водного раствора этого вещества, образовавшим(и)ся на инертном аноде: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ПРОДУКТ(Ы) НА АНОДЕ
1) кислород
2) галоген
3) диоксид азота
4) углекислый газ и углеводород
Запишите в таблицу выбранные цифры под соответствующими буквами.
Всего: 121 1–20 | 21–40 | 41–60 | 61–80 …
Теория по химии на тему «Фтор»
- 14.09.2016
Очень полезная теория для подготовки к ЕГЭ по химии. В файле представлена очень интересная и нужная информация на тему «Фтор».
Смотреть в PDF:
Или прямо сейчас: cкачать в pdf файле.
Сохранить ссылку:
Комментарии (0)
Добавить комментарий
Добавить комментарий
Комментарии без регистрации. Несодержательные сообщения удаляются.
Имя (обязательное)
E-Mail
Подписаться на уведомления о новых комментариях
Отправить
2.3.1. Химические свойства водорода и галогенов.
Химические свойства водорода
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s1. С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Взаимодействие водорода с простыми веществами
с металлами
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
с неметаллами
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Взаимодействие водорода со сложными веществами
с оксидами металлов
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
c оксидами неметаллов
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
Смесь CO и H2 даже имеет свое собственное название – «синтез-газ», поскольку из нее в зависимости от условий могут быть получены такие востребованные продукты промышленности как метанол, формальдегид и даже синтетические углеводороды:
c кислотами
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
c солями
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
Галоген |
Физические свойства |
| F2 | Светло-желтый газ с резким раздражающим запахом |
| Cl2 | Желто-зеленый газ с резким удушливым запахом |
| Br2 | Красно-бурая жидкость с резким зловонным запахом |
| I2 | Твердое вещество с резким запахом, образующее черно-фиолетовые кристаллы |
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns2np5, где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
F2 > Cl2 > Br2 > I2
Взаимодействие галогенов с простыми веществами
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
Взаимодействие галогенов с неметаллами
водородом
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
фосфором
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
серой
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Взаимодействие галогенов с металлами
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Реакции галогенов со сложными веществами
Реакции замещения с галогенами
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром вытесняет серу из растворов сульфидов и сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Взаимодействие галогенов с водой
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Взаимодействие галогенов с растворами щелочей
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
В отличие от фтора, остальные галогены в растворах щелочей диспропорционируют, то есть одновременно и повышают и понижают свою степень окисления. При этом, в случае хлора и брома в зависимости от температуры возможно протекание по двум разным направлениям. В частности, на холоду реакции протекают следующим образом:
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду:
…
К элементам главной подгруппы VII группы периодической таблицы Менделеева относятся элементы с общим названием «галогены»:
- Фтор F
- Хлор Cl
- Бром Br
- Йод I
- Астат At
Общая характеристика галогенов
От F к At (сверху вниз в
периодической таблице)
Увеличивается
- атомный радиус,
Уменьшается
- электроотрицательность,
- энергия ионизация,
- сродство к электрону.
Электронные конфигурации
у данных элементов схожи, они содержат 7 электронов на внешнем слое ns2np5:
F – 2s2 2p5;
Cl – 3s23p5;
Br – 3d10 4s2 4p5;
I — 4d10 5s2 5p5;
At – 4f14 5d10 6s2 6p5
Электронная конфигурация фтора и хлора
Электронная конфигурация брома и йода
Нахождение в природе галогенов
Галогены являются химически активными веществами, в связи с чем, в природе
они встречаются только в виде соединений. Их распространённость в земной
коре снижается при увеличении атомного
радиуса (от фтора к иоду). Например, содержание астата в
земной коре исчисляется граммами.
Наиболее распространённые соединения фтора — флюорит CaF2, криолит Na3AlF6 и др., хлора — каменная соль (галит) NaCl, сильвин KCl и сильвинит KCl⋅NaCl.
Бром и иод не образуют
индивидуальных минералов, но их соединения содержатся в морской воде и могут
накапливаться водорослями.
Фтор
Способы получения фтора
Фтор
получают методом электролиза расплава гидрофторида калия (смеси
HF и KF):
2KHF2 → 2K + H2 + 2F2
Физические свойства фтора
Фтор при обычной
температуре — зеленовато-жёлтый ядовитый газ, с резким запахом, очень
реакционноспособный, хорошо растворим в жидких водороде и
кислороде.
Химические свойства фтора
Фтор является самым сильным окислителем из всех простых веществ. Непосредственно он не взаимодействует только с N2, Не, Ne, Аr, а при нормальных условиях также и с O2.
Взаимодействие с
простыми веществами
С кислородом
Реакция протекает при электрическом разряде (2100-2400 В, 25-30 мА), температуре от -196°C до -183°C и давлении 12 мм рт.ст. с образованием дифторида трикислорода (триоксодифторид, фторид озона) или фторида кислорода:
3O2 + 2F2 → 2O3F2
O2 + 2F2 → 2OF2
С галогенами (Cl, Br, I)
Фтор вступает в
реакции с другими галогенами:
Hal2 + F2 = HalFx
Например, Cl2 + F2 → 2ClF
С водородом
Взаимодействует с водородом со взрывом даже в темноте:
H2 + F2 = 2HF
С серой
Реакция с
серой протекает легко даже при сильном охлажлении:
S + 3F2 = SF6
С углеродом
Реакция окисления порошкообразного
углерода сопровождается самовоспламенением последнего:
C + 2F2→ CF4
С азотом
При нагревании фтор реагирует и с азотом:
N2 + 3F2 → 2NF
С фосфором
Фтор взаимодействует с P энергично (со взрывом) на свету и в темноте, даже при охлаждении жидким N2:
2Р + 5F2 = 2PF5
С кремнием
Взаимодействует
с кремнием с образованием фторида кремния
Si + 2F2→ SiF4
C инертными газами
Окисляет
ксенон, образуя фторид ксенона:
Xe + 3F2 = XeF6
С металлами
При взаимодействии с металлами
образуются фториды:
Ме + F2 = Me+xF-1x
- К, Na, Pb, Fe загораются при обычной температуре на свету. С щелочными металлами реакция протекает со взрывом:
K + F2 = KF
- Mg, Zn, Sn, Al, Ag, Cu и др. загораются на свету при слабом нагревании:
Mg + F2 = MgF2
- с малоактивными металлами – Au, Pt реагирует при нагревании до 300-400°С
2Au+3F2=2AuF3.
Взаимодействие со сложными веществами
С водой
Фтор активно разлагает воду с образованием таких соединений, как фториды кислорода OF2, O2F2; пероксид водорода Н2O2; кислород, озон, фтороводород:
2F2 + Н2O = OF2 + 2HF
2F2 + 2Н2О = O2 + 4HF
С кислотами
- Взаимодействует с безводной азотной кислотой при комнатной температуре с образованием диоксида-гипофторита азота и фтороводорода:
F2 + HNO3 → NO2FO + HF
или
F2 + HNO3 → FONO2 + HF
- С серной кислотой образует гексафторид серы, фтороводород и кислород:
H2SO4 + 4F2 = 2HF + SF6 + 2O2
С щелочами и аммиаком
Фтор окисляет щелочи:
2F2 + 2NaOH = OF2 + 2NaF + H2O
Реагирует с газообразным аммиаком:
2NH3(г) +
3F2(г) = 6HF(г) + N2(г),
2NH3(г) +
6F2(г) = 6HF(г) + 2NF3(г)
С солями
Не взаимодействует
Взаимодействие
фтора с водными растворами солей невозможны, т.к. он ступает в реакцию с водой.
С оксидами
Реагирует с оксидом кремния, который загорается в атмосфере F2:
2F2 + SiO2 = SiF4 + O2
Хлор
Способы получения хлора
Промышленный способ
Электролиз расплавов или водных растворов хлоридов, чаще – NaCl.
- Электролиз расплава хлорида натрия:
NaCl → Na+ + Cl−
K(–): Na+ +1e → Na0
A(+): 2Cl− ̶ 2e → Cl20
2Na+ + 2Cl− → 2Na º + Cl2º
Таким образом, получаем:
2NaCl → 2Na + Cl2
- Электролиз раствора хлорида натрия.
NaCl → Na+ + Cl−
K(–): 2H2O + 2e → H2° + 2OH−
A(+): 2Cl− ̶ 2e → Cl20
2H2O + 2Cl− → H2°↑ + 2OH− + Cl2°↑
Таким образом, получаем:
2NaCl + 2H2O → H2↑ + 2NaOH + Cl2↑
Лабораторный способ
Окисление концентрированной HCI сильными окислителями:
4HCI + MnO2 = Cl2↑ + МпCl2 + 2Н2O
16НСl + 2КМпО4 = 5Cl2↑ + 2MnCl2 + 2KCl + 8Н2O
6HCl + КСlO3 = ЗCl2↑ + KCl + 3Н2O
14HCl + К2Сr2O7 = 3Cl2↑ + 2CrCl3 + 2KCl + 7Н2O
Физические свойства хлора
Хлор Cl2 при обычной температуре – тяжелый, желто-зеленый
газ с резким удушающим запахом.
Cl2 в 2,5 раза тяжелее воздуха, малорастворим в воде (~
6,5 г/л); хорошо растворим в неполярных органических растворителях. В свободном
состоянии встречается только в вулканических газах.
Химические свойства хлора
Хлор — очень сильный окислитель. Окисляет металлы, неметаллы и сложные вещества, с образованием в устойчивые хлорид-ионы:
Cl20+ 2e— = 2Cl—
Взаимодействие с простыми веществами
С кислородом
Непосредственно не взаимодействует
С галогенами
Хлор взаимодействует с другими галогенами – более активные галогены окисляют менее активные. В зависимости от условий могут получиться различные соединения:
F2 + Cl2 = 2ClF
3F2 + Cl2 =
2ClF3
Br2 + Cl2 =
2BrCl
Br2 + 5Cl2 +
6H2O = 2HBrO3 + 10HCl
I2 + Cl2 =
2ICl
I2 + 3Cl2 =
2ICl3
I2 +
5Cl2 + 6H2O = 2HIO3 + 10HCl
С водородом
Реакция с водородом при обычных условиях не протекает. Однако, при нагревании, УФ — освещении или электрическом разряде реакция протекает со взрывом:
Cl2 + Н2 =2НСl
С серой
Cl2 + 2S (расплав) = S2Cl2
С азотом
Непосредственно не взаимодействует
С фосфором
ЗCl2 + 2Р = 2РCl3 (или РCl5 — в избытке Cl2)
С углеродом
Непосредственно не взаимодействует
С кремнием
2Cl2 + Si = SiCl4 (при нагревании)
С металлами
- Активные металлы самовоспламеняются и горят в атмосфере сухого газообразного хлора:
Cl2+
2Na = 2NaCl
3Cl2 + 2Fe = 2FeCl3
- Окисление малоактивных металлов происходит легче влажным хлором или его водными растворами:
Cl2 + Сu = CuCl2
3Cl2 + 2Аu = 2AuCl3
Взаимодействие со сложными веществами
Окислительно-восстановительные реакции
Окисляет сложные вещества:
ЗСl2 + 2NH3 = N2 + 6HCl
Cl2 + H2S = S + 2HCl
Cl2 + H2O + Na2SO3 → 2HCl + Na2SO4
Cl2 + 3H2O2 → 2HCl + 2H2O + O2
2Cl2 + 2H2O → 4HCl + O2 (на свету или кипячении)
Cl2 + 2HI = I2 + 2HCl
С водой
При растворении хлора в воде вступает в реакцию диспропорционирования (самоокисления-самовосстановления), с образованием хлорноватистой кислоты:
Cl2 + Н2O = HCl + НClO
С водными растворами щелочей
При взаимодействии с щелочами хлор диспропорционирует с образованием солей,
состав которых зависит от условий проведения реакции:
- с холодным раствором щелочи образуются хлорид и гипохлорит:
Сl2 + 2NaOH (хол.) → NaCl + NaClO + H2O
- с горячим раствором щелочи образуются хлорид и хлорат:
3Cl2 + 6NaOH (гор.) → 5NaCl + NaClO3 + 3H2O
- Хлор также растворяется в холодном растворе гидроксида кальция:
2Сl2 + 2Са(OH)2(хол.) → СaCl2 + Сa(ClO)2 + 2H2O
Эти реакции
имеют важное практическое значение, приводят к получению гипохлоритов — КClO3 и Са(ClO)2; хлората калия
(бертолетова соль) — КClO3
С солями
Более активные галогены вытесняют менее активные галогены из солей и галогеноводородов:
Cl2 + 2KBr = Br2 + 2KCl
Cl2 + 2KI = I2 + 2KCl
С органическими соединениями
- замещение атомов водорода в молекулах органических соединений:
- присоединение молекул Cl2 по месту разрыва кратных углерод-углеродных связей
H2C = CH2 + Cl2 → Cl — H2C — CH2 — Cl 1,2-дихлорэтан
HC ≡ CH + 2Cl2 → Cl2HC — CHCl2 1,1,2,2-тетрахлорэтан
Бром
Способы получения брома
Промышленный способ
- Исходное сырьё для
получения брома — морская вода, озёрные и подземные рассолы и щелока калийного
производства, содержащие бром в виде бромид-иона Br-
Бром втесняют при помощи хлора:
2Вг— + Cl2 = Br2 + 2Сl—
Далее бром отгоняют из раствора водяным паром или воздухом.
Лабораторный способ
- В лаборатории для получения брома используют сильные окислители:
2NaBr + МnO2 + 2H2SO4 = Br2↓ + MnSO4 + Na2SO4 + 2Н2O
MnO2 + 4HBr → MnBr2 + Br2 + 2H2O
НВг + 2H2SO4 = 3Br2↓ + S↓ + 4Н2O
2HBr + Cl2 → Br2 + 2HCl
Физические свойства брома
В обычных
условиях бром – красно-бурая жидкость с резким зловонным запахом. При Т=-7,2°C
жидкий бром застывает, образуя красно-коричневые игольчатые кристаллы.
Пары брома жёлто-бурого цвета, Ткип = 58,78°C.
В воде бром растворяется лучше других галогенов
(3,58 г брома в 100 г H2O при 20°C). Хорошо растворим во многих
органических растворителях.
Бромная вода имеет желто-бурую окраску, быстро исчезающую, при взаимодействии растворенного Br2 с каким-либо веществом. «Обесцвечивание бромной воды» — широко используется в качестве теста на обнаружение в растворе многих неорганических и органических веществ.
Химические свойства брома
Химические
свойства брома сходны с хлором. Различаются только условия протекания реакций.
Взаимодействие с простыми веществами
С металлами
Жидкий бром сильный окислитель. Например, железо и алюминий самовозгораются при соприкосновении с бромом даже при обычной температуре.
Al(тв) + 3/2Br2(ж) = AlBr3(тв), ΔH°298 = -513
кДж/моль
Al(тв) + 3/2Cl2(г) = AlBr3(тв), ΔH°298 = -704
кДж/моль
Fe(тв) + 3/2Br(тв) = FeBr3(тв), ΔH°298 = -269
кДж/моль
Fe(тв) + 3/2Cl2(г) = FeBr3(тв), ΔH°298 = -399 кДж/моль
С водородом
Взаимодействие брома с водородом происходит лишь при повышенной температуре. Реакция эндотермической и обратимой.
Br2 + H2 ↔ 2HBr
С азотом, углеродом, кислородом и благородными газами
Непосредственно не взаимодействует
С галогенами
Бром окисляется более активными галогенами:
5Cl2 + Br2 + 6H2O = 2HBrO3 + 10HCl
Взаимодействие со сложными веществами
- Бром окисляет сложные соединения:
Na2SO3 + Br2 + H2O = Na2SO4 + 2HBr
BaS
+ 4Br2 + 4H2O = BaSO4 + 8HBr
- диспропорционирует в водном растворе:
3BrO— ↔ BrO3— + 2Br—
4BrO— ↔ BrO4— + 3Br—
Обесцвечивание
бромной воды
Обесцвечивание бромной воды – качественная реакция на многие неорганические и органические соединения:
- в воде SO2 и H2S в газообразном и растворенном виде, а также растворимые сульфиты и сульфиды реагируют с бромной водой, обесцвечивая ее:
Br2 + SO2 + 2Н2O = 2НВr + H2SO4
Br2 + Na2SO3 + Н2O = 2HBr +
Na2SO4
Br2 + H2S = 2НВr + S↓
3Br2 + Na2S + ЗН2O = 6HBr +
Na2SO3
- Обесцвечивание бромной воды непредельными органическими соединениями:
R-CH=CH-R’ + Br2 → R-CHBr-CHBr-R’
- Фенол и анилин также легко взаимодействуют с бромной водой:
С6Н5ОН + ЗBr2 → С6Н2Вг3ОН↓ + ЗНВr
С6Н5NH2 + ЗВr2 → С6H2Br3NH2↓ + ЗНВr
Йод
Способы получения йода
Промышленный способ
- Йод, также как и бром, извлекают из морской воды, соленых озер, подземных рассолов и буровых вод, где он содержится в виде I—.
- Получение свободного йода с помощью различных окислителей, чаще всего газообразного хлора:
2 КI + СI2 = 2 КCl + I2
Лабораторный способ
- Йод можно получить также как и хлор или бром действием различных окислителей (КМnО4, МnО2, КСlO3, КВrО3, FеСl3 и СuSO4) на иодоводородную кислоту:
2 КМnО4 + 16 НI = 2 КI + 2 MnI2 + 5I2 + 8 Н2О
КВrО3 + 6 НI = КВr + 5 I2 + 3 Н2О
2 FеC3 + 2 НI = 2 FeCl2 +
I2 + 2 НСl
2 СuSO4 + 4 НI = 2 СuI + 2 Н2SO4 + I2
H2SO4 + 2HI = I2↓ + SO2↑ + 2Н2O
Физические свойства йода
Свободный йод I2 при обычной температуре — черно-серое с фиолетовым
оттенком кристаллическое вещество с металлическим блеском. Легко возгоняется. Пары
йода имеют своеобразный запах и очень ядовиты.
Среди галогенов I2 обладает самой меньшей растворимостью
в воде, однако он хорошо растворим в спирте и других органических
растворителях.
Химические свойства йода
Химическая активность йода – наименьшая по
сравнению с другими галогенами. Со многими элементами йод непосредственно не
взаимодействует, а с некоторыми реагирует только при повышенных температурах
(водород, кремний, многие металлы).
Йод-крахмальная реакция
Обнаружить I2 даже в самой минимальной концентрации можно с помощью раствора крахмала, который при наличии I2 окрашивается в грязно-синий цвет.
Йод-крахмальная реакция используется при качественном обнаружении йода, а также его количественного анализа
Взаимодействие с простыми веществами
С водородом
Реакция обратима и возможна только
при высокой температуре:
H2(г)+
I2(кр)↔ 2HI(г), ΔH298= +53,1 кДж/моль
С
металлами
При добавлении капли воды в качестве катализатора цинк, железо и алюминий в смеси с порошком йода горят, образуя йодиды:
Zn + I2 = ZnI2
С азотом, углеродом, кислородом
Непосредственно не взаимодействует
Взаимодействие со сложными веществами
С водой
Частично реагирует с водой (реакция
диспропорционирования):
I2 + H2O = HI + HIO
С щелочью
Диспропорционирует в водном растворе щелочи:
NaOH + I2 ↔ NaI + NaIO + H2O
C аммиаком
C аммиаком образует
аддукт нитрид трииодида:
3I2 + 5NH3 = 3NH4I +
NH3∙NI3$
С иодидами щелочных металлов
Молекулы галогенов присоединяются к
иодидам щелочных металлов с образованием полииодидов (периодидов):
I2 + KI = KI3
С окислителями
Йод проявляет восстановительные свойства в реакциях с сильными окислителями:
I2 + I0HNO3 = 2НIO3 + 10NO2 + 4Н2O
I2 + 5Н2O2 = 2НIO3 + 4Н2O
I2 + 5Cl2 + 6Н2O = 2НIO3 + 10HCl
C восстановителями
Иод менее сильный окислитель, чем фтор, хлор и бром. Восстановители, такие как H2S, Na2S2O3 и др. восстанавливают его до иона I−:
I2 + H2S
= S + 2HI
I2 + 2Na2S2O3 = 2NaI + Na2S4O6