|
Строение и функции белков |
Краткий конспект в схемах и таблицах
Подробный конспект
Конспект включает подробное текстовое описание строения, свойств и функций белков в формате ЕГЭ по биологии.
перейти…
Термины по теме
Основные термины по теме «Строение и функции белков».
перейти…
Тестовые задания
Раздел содержит тесты по теме «Строение и функции белков» в формате ЕГЭ для тренировки
перейти…
Список использованных источников
- Биология 11 класс. В.Б. Захаров, С.Г. Мамонтов, Н.И. Сонин, Е.Т. Захарова; Дрофа, 2010
- Биология. Общая биология. Базовый уровень: учебник для 10-11 классов. В.И. Сивоглазов, И.Б. Агафонова, Е.Т. Захарова; Дрофа, 2010
- Биология 10-11 класс. Сухорукова Л.Н., Кучменко В.С., Иванова Т.В.; Сфера, Просвещение
- Использованные рисунки, находящиеся в свободном доступе в Интернете
В видео-уроке использовались фрагменты:
https://www.youtube.com/watch?v=RCGTZw7E7tE
Справочная таблица.
f-b.docx
f-b.pdf
|
Название функции |
Примеры белков |
Где содержатся |
Характеристика функции |
|
1. Строительная (структурная) |
Кератин |
Волосяной покров, кости, ногти |
Участие в образовании всех клеточных мембран и органоидов клетки. |
|
Коллаген |
Соединительная ткань, железы насекомых, кости |
Образование нитей натурального шелка. |
|
|
2. Регуляторная |
Инсулин |
Поджелудочная железа |
Регулирует поступление и уровень глюкозы в крови. |
|
Гистоны |
В крови |
||
|
3. Транспортная |
Гемоглобин |
Эритроциты крови |
Переносит О2, питательные вещества и СО2. |
|
Альбумины |
Кровь |
Транспорт жирных кислот. |
|
|
4. Каталитическая |
Б-ферменты |
Во всех клетках и тканях животных и растений |
Ускоряют химические реакции, способствуют расщеплению питательных веществ и вредных соединений. |
|
5. Защитная |
Антитела крови |
Кровеносная система (лейкоциты) |
Иммунная защита организмов. Свертывание крови. Подавляет развитие вирусов. |
|
6. Сократительная |
Актин |
Мышечные волокна. Структура ресничек и жгутиков простейших |
Сокращение мышц. Движение простейших. Все виды движений. |
|
7. Энергетическая |
Все белки |
Клетки всех организмов |
Источник энергии для клеток (1г белка – 17,6 кДж энергии) |
|
8. Запасная (питательная) |
Казеин |
Молоко |
Запас питательных веществ. |
|
Альбумин |
Яйца |
||
|
Клейковина |
Пшеница |
||
|
Зеин |
Кукуруза |
Автор: Кистайкин Н.В.
Химический состав живых организмов
Химический состав живых организмов можно выразить в двух видах — атомном и молекулярном.
Атомный (элементный) состав характеризует соотношение атомов элементов, входящих в живые организмы.
Молекулярный (вещественный) состав отражает соотношение молекул веществ.
Элементарный состав
По относительному содержанию элементы, входящие в состав живых организмов, делят на три группы.
Группы элементов по их содержанию в живых организмах
| Группа элементов | Элементы | Суммарное содержание в клетке, % |
| Макроэлементы | O, C, H, N (основные, или органогены) Ca, K, Si, Mg, P, S, Na, Cl, Fe |
98–99 1–2 |
| Микроэлементы | Mn, Co, Zn, Cu, B, I, F, Mo и др. | 0,1 |
| Ультрамикроэлементы | Se, U, Hg, Ra, Au, Ag и др. менее | 0,01 |
Макроэлементы составляют основную массу процентного состава живых организмов.
Содержание некоторых химических элементов в природных объектах
| Элемент | В живых организмах, % от сырой массы | В земной коре, % | В морской воде, % |
| Кислород | 65–75 | 49,2 | 85,8 |
| Углерод | 15–18 | 0,4 | 0,0035 |
| Водород | 8–10 | 1,0 | 10,67 |
| Азот | 1,5–3,0 | 0,04 | 0,37 |
| Фосфор | 0,20–1,0 | 0,1 | 0,003 |
| Сера | 0,15–0,2 | 0,15 | 0,09 |
| Калий | 0,15–0,4 | 2,35 | 0,04 |
| Хлор | 0,05–0,1 | 0,2 | 0,06 |
| Кальций | 0,04–2,0 | 3,25 | 0,05 |
| Магний | 0,02–0,03 | 2,35 | 0,14 |
| Натрий | 0,02–0,03 | 2,4 | 1,14 |
| Железо | 0,01–0,015 | 4,2 | 0,00015 |
| Цинк | 0,0003 | < 0,01 | 0,00015 |
| Медь | 0,0002 | < 0,01 | < 0,00001 |
| Йод | 0,0001 | < 0,01 | 0,000015 |
| Фтор | 0,0001 | 0,1 | 2,07 |
Химические элементы, которые входят в состав живых организмов и при этом выполняют биологические функции, называются биогенными. Даже те из них, которые содержатся в клетках в ничтожно малых количествах, ничем не могут быть заменены и совершенно необходимы для жизни. В основном это макро- и микроэлементы. Физиологическая роль большинства микроэлементов не раскрыта.
Роль биогенных элементов в живых организмах
| Название элемента | Символ элемента | Роль в живых организмах |
| Углерод | С | Входит в состав органических веществ, в форме карбонатов входит в состав раковин моллюсков, коралловых полипов, покровов тела простейших, бикарбонатной буферной системы (HCO3-, Н2CO3) |
| Кислород | О | Входит в состав воды и органических веществ |
| Водород | Н | Входит в состав воды и органических веществ |
| Азот | N | Входит в состав всех аминокислот, нуклеиновых кислот, АТФ, НАД, НАДФ, ФАД |
| Фосфор | Р | Входит в состав нуклеиновых кислот, АТФ, НАД, НАДФ, ФАД, фосфолипидов, костной ткани, эмали зубов, фосфатной буферной системы (HPO4, H2PO4-) |
| Сера | S | Входит в состав серосодержащих аминокислот (цистина, цистеина, метионина), инсулина, витамина В1, кофермента А, многих ферментов, участвует в формировании третичной структуры белка (образование дисульфидных связей), в бактериальном фотосинтезе (сера входит в состав бактериохлорофилла, H2S является источником водорода), окисление соединений серы — источник энергии в хемосинтезе |
| Хлор | Cl | Преобладающий отрицательный ион в организме, участвует в создании мембранных потенциалов клеток, осмотического давления для поглощения растениями воды из почвы и тургорного давления для поддержания формы клетки, процессах возбуждения и торможения в нервных клетках, входит в состав соляной кислоты желудочного сока |
| Натрий | Na | Главный внеклеточный положительный ион, участвует в создании мембранных потенциалов клеток (в результате работы натрий-калиевого насоса), осмотического давления для поглощения растениями воды из почвы и тургорного давления для поддержания формы клетки, в поддержании сердечного ритма (вместе с ионами K+ и Ca2+) |
| Калий | K | Преобладающий положительный ион внутри клетки, участвует в создании мембранных потенциалов клеток (в результате работы натрий-калиевого насоса), поддержании сердечного ритма (вместе с ионами Na+ и Ca2+), активирует ферменты, участвующие в синтезе белка |
| Кальций | Ca | Входит в состав костей, зубов, раковин, участвует в регуляции избирательной проницаемости клеточной мембраны, процессах свёртывания крови; поддержании сердечного ритма (вместе с ионами K+ и Na2+), образовании желчи, активирует ферменты при сокращении поперечно-полосатых мышечных волокон |
| Магний | Mg | Входит в состав хлорофилла, многих ферментов |
| Железо | Fe | Входит в состав гемоглобина, миоглобина, некоторых ферментов |
| Медь | Cu | Входит в состав некоторых ферментов |
| Цинк | Zn | Входит в состав некоторых ферментов |
| Марганец | Mn | Входит в состав некоторых ферментов |
| Молибден | Mo | Входит в состав некоторых ферментов |
| Кобальт | Co | Входит в состав витамина В12 |
| Фтор | F | Входит в состав эмали зубов, костей |
| Йод | I | Входит в состав гормона щитовидной железы — тироксина |
| Бром | Br | Входит в состав витамина В1 |
| Бор | В | Влияет на рост растений |
Молекулярный состав
Химические элементы входят в состав клеток в виде ионов и молекул неорганических и органических веществ. Важнейшие неорганические вещества в клетке — вода и минеральные соли, важнейшие органические вещества — углеводы, липиды, белки и нуклеиновые кислоты.
Содержание в клетке химических веществ
| Вещество | Содержание, % от сырой массы |
| Вода | 75–85 |
| Белки | 10–15 |
| Жиры | 1–5 |
| Углеводы | 0,2–2,0 |
| Нуклеиновые кислоты | 1–2 |
| Низкомолекулярные органические соединения | 0,1–0,5 |
| Неорганические соединения | 1,0–1,5 |
Неорганические вещества
Вода
Вода — преобладающее вещество всех живых организмов. Она обладает уникальными свойствами благодаря особенностям строения: молекулы воды имеют форму диполя и между ними образуются водородные связи. Среднее содержание воды в клетках большинства живых организмов составляет около 70%. Вода в клетке присутствует в двух формах: свободной (95% всей воды клетки) и связанной (4–5% связаны с белками). Функции воды представлены в таблице.
Функции воды
| Функция | Характеристика |
| Вода как растворитель | Вода является лучшим из известных растворителей, в ней растворяется больше веществ, чем в любой другой жидкости. Многие химические реакции в клетке являются ионными, поэтому протекают только в водной среде. Молекулы воды полярны, поэтому вещества, молекулы которых также полярны, хорошо растворяются в воде, а вещества, молекулы которых не полярны, нерастворяются (плохо растворяются) в воде. Вещества, растворяющиеся в воде, называются гидрофильными (спирты, сахара, альдегиды, аминокислоты), нерастворяющиеся — гидрофобными (жирные кислоты, целлюлоза). |
| Вода как реагент | Вода участвует во многих химических реакциях: реакциях гидролиза, полимеризации, в процессе фотосинтеза и т. д. |
| Транспортная | Передвижение по организму вместе с водой растворённых в ней веществ к различным его частям и выведение ненужных продуктов из организма. |
| Вода как термостабилизатор и терморегулятор | Эта функция обусловлена такими свойствами воды, как высокая теплоёмкость (благодаря наличию водородных связей): смягчает влияние на организм значительных перепадов температуры в окружающей среде; высокая теплопроводность (вследствие небольших размеров молекул) позволяет организму поддерживать одинаковую температуру во всем его объёме; высокая теплота испарения (благодаря наличию водородных связей): вода используется для охлаждения организма при потоотделении у млекопитающих и транспирации у растений. |
| Структурная | Цитоплазма клеток содержит обычно от 60 до 95% воды, и именно она придаёт клеткам их нормальную форму. У растений вода поддерживает тургор (упругость эндоплазматической мембраны), у некоторых животных служит гидростатическим скелетом (медузы, круглые черви). Это возможно благодаря такому свойству воды, как полная несжимаемость. |
Минеральные соли
Минеральные соли в водном растворе клетки диссоциируют на катионы и анионы.
Наиболее важные катионы — K+, Ca2+, Mg2+, Na+, NH4+,
Наиболее важные анионы — Cl—, SO42-, HPO42-, H2PO4—, HCO3—, NO3—.
Существенным является не только концентрация, но и соотношение отдельных ионов в клетке.
Функции минеральных веществ представлены в таблице.
Функции минеральных веществ
| Функция | Характеристика |
| Поддержание кислотно- щелочного равновесия | Наиболее важные буферные системы млекопитающих — фосфатная и бикарбонатная. Фосфатная буферная система (HPO4 2-, H2PO4—) поддерживает рН внутриклеточной жидкости в пределах 6,9–7,4. Бикарбонатная система (HCO3—, Н2CO3) сохраняет рН внеклеточной среды (плазмы крови) на уровне 7,4. |
| Участие в создании мембранных потенциалов клеток | В составе наружной клеточной мембраны клетки имеются так называемые ионные насосы. Один из них — натрий-калиевый насос — белок, пронизывающий плазматическую мембрану, накачивает ионы натрия внутрь клетки и выкачивает из неё ионы натрия. При этом на каждые два поглощённых иона калия выводятся три иона натрия. В результате образуется разность зарядов (потенциалов) внешней и внутренней поверхностей мембраны клетки: внутренняя сторона заряжена отрицательно, наружная — положительно. Разность потенциалов необходима для передачи возбуждения по нерву или мышце. |
| Активация ферментов | Ионы Ca, Mg, Fe, Zn, Cu, Mn, Co и других металлов являются компонентами многих ферментов, гормонов и витаминов. |
| Создание осмотического давления в клетке | Более высокая концентрация ионов солей внутри клетки обеспечивает поступление в неё воды и создание тургорного давления. |
| Строительная (структурная) | Соединения азота, фосфора, серы и другие неорганические вещества служат источником строительного материала для синтеза органических молекул (аминокислот, белков, нуклеиновых кислот и др.) и входят в состав ряда опорных структур клетки и организма. Соли кальция и фосфора входят в состав костной ткани животных. |
Кроме того, соляная кислота входит в состав желудочного сока животных и человека, ускоряя процесс переваривания белков пищи. Остатки серной кислоты способствуют выведению чужеродных веществ из организма. Натриевые и калиевые соли азотистой и фосфорной кислот, кальциевая соль серной кислоты служат важными компонентами минерального питания растений, их вносят в почву в качестве удобрений.
Органические вещества
Полимер — многозвеньевая цепь, в которой звеном является какое-либо относительно простое вещество — мономер. Полимеры бывают линейные и разветвленные, гомополимеры (все мономеры одинаковые — остатки глюкозы в крахмале) и гетерополимеры (мономеры разные — остатки аминокислот в белках), регулярные (группа мономеров в полимере периодически повторяется) и нерегулярные (в молекулах нет видимой повторяемости мономерных звеньев).
Биологические полимеры — это полимеры, входящие в состав клеток живых организмов и продуктов их жизнедеятельности. Биополимерами являются белки, нуклеиновые кислоты, полисахариды. Свойства биополимеров зависят от числа, состава и порядка расположения составляющих их мономеров. Изменение состава и последовательности мономеров в структуре полимера приводит к значительному числу вариантов биологических макромолекул.
Углеводы
Углеводы — органические соединения, состоящие из одной или многих молекул простых сахаров. Содержание углеводов в животных клетках составляет 1–5 %, а в некоторых клетках растений достигает 70 %.
Выделяют три группы углеводов: моносахариды, олигосахариды (состоят из 2–10 молекул простых сахаров), полисахариды (состоят более чем из 10 молекул сахаров). Соединяясь с липидами и белками, углеводы образуют гликолипиды и гликопротеины.
Характеристика углеводов
| Группа | Строение | Характеристика |
| Моносахариды (или простые сахара) | Это кетонные или альдегидные производные многоатомных спиртов. | В зависимости от числа атомов углерода различают триозы, тетрозы, пентозы (рибоза, дезоксирибоза), гексозы (глюкоза, фруктоза) и гептозы. В зависимости от функциональной группы сахара разделяют на альдозы, имеющие в составе альдегидную группу (глюкоза, рибоза, дезоксирибоза), и кетозы, имеющие в составе кетонную группу (фруктоза). Моносахариды — бесцветные твёрдые кристаллические вещества, легко растворимые в воде, имеющие, как правило, сладкий вкус. Моносахариды могут существовать в ациклических и циклических формах, которые легко превращаются друг в друга. Олиго- и полисахариды образуются из циклических форм моносахаридов. |
| Олигосахариды | Состоят из 2–10 молекул простых сахаров. В природе в большей степени представлены дисахаридами, состоящими из двух моносахаридов, связанных друг с другом с помощью гликозидной связи. | Наиболее часто встречаются мальтоза, или солодовый сахар, состоящий из двух молекул глюкозы; лактоза, входящая в состав молока и состоящая из галактозы и глюкозы; сахароза, или свекловичный сахар, включающий глюкозу и фруктозу. Дисахариды, как и моносахариды, растворимы в воде и обладают сладким вкусом. |
| Полисахариды | Состоят более чем из 10 молекул сахаров. В полисахаридах простые сахара (глюкоза, галактоза и др.) соединены между собой гликозидными связями. Если присутствуют только 1–4, гликозидные связи, то образуется линейный, неразветвлённый полимер (целлюлоза), если присутствуют и 1–4, и 1–6 связи, полимер будет разветвлённым (крахмал, гликоген). Полисахариды утрачивают сладкий вкус и способность растворяться в воде. | Целлюлоза — линейный полисахарид, состоящий из молекул β-глюкозы, соединённых 1–4 связями. Целлюлоза является главным компонентом клеточной стенки растений. Она нерастворима в воде и обладает большой прочностью. У жвачных животных целлюлозу расщепляют ферменты бактерий, постоянно обитающих в специальном отделе желудка. Крахмал и гликоген являются основными формами запасания глюкозы у растений и животных соответственно. Остатки α-глюкозы в них связаны 1–4 и 1–6 гликозидными связями. Хитин образует у членистоногих наружный скелет (панцирь), у грибов придаёт прочность клеточной стенке. |
Функции углеводов представлены в таблице.
Функции углеводов
| Функция | Характеристика |
| Энергетическая | При окислении простых сахаров (в первую очередь глюкозы) организм получает основную часть необходимой ему энергии. При полном расщеплении 1 г глюкозы высвобождается 17,6 кДж энергии. |
| Запасающая | Крахмал (у растений) и гликоген (у животных, грибов и бактерий) играют роль источника глюкозы, высвобождая её по мере необходимости. |
| Строительная (структурная) | Целлюлоза (у растений) и хитин (у грибов) придают прочность клеточным стенкам. Рибоза и дезоксирибоза входят в состав нуклеиновых кислот. Рибоза также входит в состав АТФ, ФАД, НАД, НАДФ. |
| Рецепторная | Функция узнавания клетками друг друга обеспечивается гликопротеинами, входящими в состав клеточных мембран. Утрата способности узнавать друг друга характерна для клеток злокачественных опухолей. |
| Защитная | Хитин образует покровы (наружный скелет) тела членистоногих. |
Липиды
Липиды — жиры и жироподобные органические соединения, практически нерастворимые в воде. Их содержание в разных клетках сильно варьируется от 2–3 (в клетках семян растений) до 50–90% (в жировой ткани животных). В химическом отношении липиды, как правило, сложные эфиры жирных кислот и ряда спиртов
Они делятся на несколько классов. Наиболее распространены в живой природе нейтральные жиры, воска, фосфолипиды, стероиды. В состав большинства липидов входят жирные кислоты, молекулы которых содержат гидрофобный длинноцепочечный углеводородный «хвост» и гидрофильную карбоксильную группу.
Жиры — сложные эфиры трёхатомного спирта глицерина и трёх молекул жирных кислот. Воска — это сложные эфиры многоатомных спиртов и жирных кислот. Фосфолипиды имеют в молекуле вместо остатка жирной кислоты остаток фосфорной кислоты. Стероиды не содержат жирных кислот и имеют особую структуру. Также для живых организмов характерны липопротеины — соединения липидов с белками без образования ковалентных связей и гликолипиды — липиды, в которых помимо остатка жирной кислоты содержится одна или несколько молекул сахара.
Функции липидов представлены в таблице.
Функции липидов
| Функция | Характеристика |
| Строительная (структурная) | Фосфолипиды вместе с белками являются основой биологических мембран. Стероид холестерин — важный компонент клеточных мембран у животных. Липопротеины и гликолипиды входят в состав мембран клеток некоторых тканей. Воск входит в состав пчелиных сот. |
| Гормональная (регуляторная) | Многие гормоны по химической природе являются стероидами. Например, тестостерон стимулирует развитие полового аппарата и вторичных половых признаков, характерных для мужчин; прогестерон (гормон беременности) способствует имплантации яйцеклетки в матке, задерживает созревание и овуляцию фолликулов, стимулирует рост молочных желёз; кортизон и кортикостерон влияют на обмен углеводов, белков, жиров, обеспечивая адаптацию организма к большим мышечным нагрузкам. |
| Энергетическая | При окислении 1 г жирных кислот высвобождается 38,9 кДж энергии и синтезируется в два раза больше АТФ, чем при расщеплении такого же количества глюкозы. У позвоночных половина энергии, потребляемой в состоянии покоя, образуется за счёт окисления жирных кислот. |
| Запасающая | В виде жиров хранится значительная часть энергетических запасов организма: твёрдые жиры у животных, жидкие жиры (масла) у растений, например, у подсолнечника, сои, клещевины. Кроме того, жиры служат источником воды (при сгорании 1 г жира образуется 1,1 г воды). Это особенно ценно для пустынных и арктических животных, испытывающих дефицит свободной воды. |
| Защитная | У млекопитающих подкожный жир выступает в качестве термоизолятора (защита от охлаждения) и амортизатора (защита от механических воздействий). Воск покрывает эпидермис растений, кожу, перья, шерсть, волосы животных, предохраняя от смачивания. |
Белки
Белки представляют собой самый многочисленный и наиболее разнообразный класс органических соединений клетки. Белки — это биологические гетерополимеры, мономерами которых являются аминокислоты.
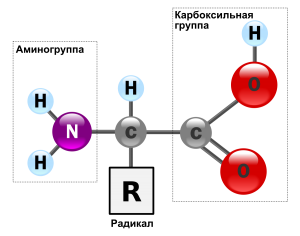
По химическому составу аминокислоты — это соединения, содержащие одну карбоксильную группу (—СООН) и одну аминную (—NH2), связанные с одним атомом углерода, к которому присоединена боковая цепь — какой-либо радикал R. Именно радикал придаёт аминокислоте её неповторимые свойства.
В образовании белков участвуют только 20 аминокислот. Они называются фундаментальными, или основными: аланин, метионин, валин, пролин, лейцин, изолейцин, триптофан, фенилаланин, аспарагин, глутамин, серин, глицин, тирозин, треонин, цистеин, аргинин, гистидин, лизин, аспарагиновая и глутаминовая кислоты. Некоторые из аминокислот не синтезируются в организмах животных и человека и должны поступать с растительной пищей. Они называются незаменимыми: аргинин, валин, гистидин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин.
Аминокислоты, соединяясь друг с другом ковалентными пептидными связями, образуют различной длины пептиды
Пептидной (амидной) называется ковалентная связь, образованная карбоксильной группой одной аминокислоты и аминной группой другой.
Белки представляют собой высокомолекулярные полипептиды, в состав которых входят от ста до нескольких тысяч аминокислот.
Выделяют 4 уровня организации белков:
Уровни организации белков
| Уровень | Характеристика |
| Первичная структура | Последовательность аминокислот в полипептидной цепи. Она образуется за счёт ковалентных пептидных связей между аминокислотными остатками. Первичная структура определяется последовательностью нуклеотидов в участке молекулы ДНК, кодирующем данный белок. Первичная структура любого белка уникальна и определяет его форму, свойства и функции. Молекулы белков могут принимать различные пространственные формы (конформации). Существуют вторичная, третичная и четвертичная пространственные структуры белковой молекулы. |
| Вторичная структура | Образуется укладкой полипептидных цепей в α-спираль или β-структуру. Она поддерживается за счёт водородных связей между атомами водорода групп NH— и атомами кислорода групп СО—. α-спираль формируется в результате скручивания полипептидной цепи в спираль с одинаковыми расстояниями между витками. Она характерна для глобулярных белков, имеющих сферическую форму глобулы. β-структура представляет собой продольную укладку трёх полипептидных цепей. Она характерна для фибриллярных белков, имеющих вытянутую форму фибриллы. |
| Третичная структура | Образуется при сворачивании спирали в клубок (глобулу, домен). Домены — глобулоподобные образования с гидрофобной сердцевиной и гидрофильным наружным слоем. Третичная структура формируется за счёт связей, образующихся между радикалами (R) аминокислот, за счёт ионных, гидрофобных и дисперсионных взаимодействий, а также за счёт образования дисульфидных (S — S) связей между радикалами цистеина. |
| Четвертичная структура | Характерна для сложных белков, состоящих из двух и более полипептидных цепей (глобул), не связанных ковалентными связями, а также для белков, содержащих небелковые компоненты (ионы металлов, коферменты). Четвертичная структура поддерживается в основном силами межмолекулярного притяжения и в меньшей степени водородными и ионными связями. |
Конфигурация белка зависит от последовательности аминокислот, но на неё могут влиять и конкретные условия, в которых находится белок.
Утрата белковой молекулой своей структурной организации называется денатурацией.
Денатурация может быть обратимой и необратимой. При обратимой денатурации разрушается четвертичная, третичная и вторичная структуры, но благодаря сохранению первичной структуры при возвращении нормальных условий возможна ренатурация белка — восстановление нормальной (нативной) конформации. При необратимой денатурации происходит разрушение первичной структуры белка. Денатурация может быть вызвана высокой температурой (выше 45 °C), обезвоживанием, ионизирующим излучением и другими факторами. Изменение конформации (пространственной структуры) белковой молекулы лежит в основе ряда функций белков (сигнальные, антигенные свойства и др.).
По химическому составу различают простые и сложные белки. Простые белки состоят только из аминокислот (фибриллярные белки, антитела — иммуноглобулины). Сложные белки содержат белковую часть и небелковую — простетические группы. Различают липопротеины (содержат липиды), гликопротеины (углеводы), фосфопротеины (одну или несколько фосфатных групп), металлопротеины (различные металлы), нуклеопротеины (нуклеиновые кислоты). Простетические группы обычно играют важную роль при выполнении белком его биологической функции.
Функции белков представлены в таблице.
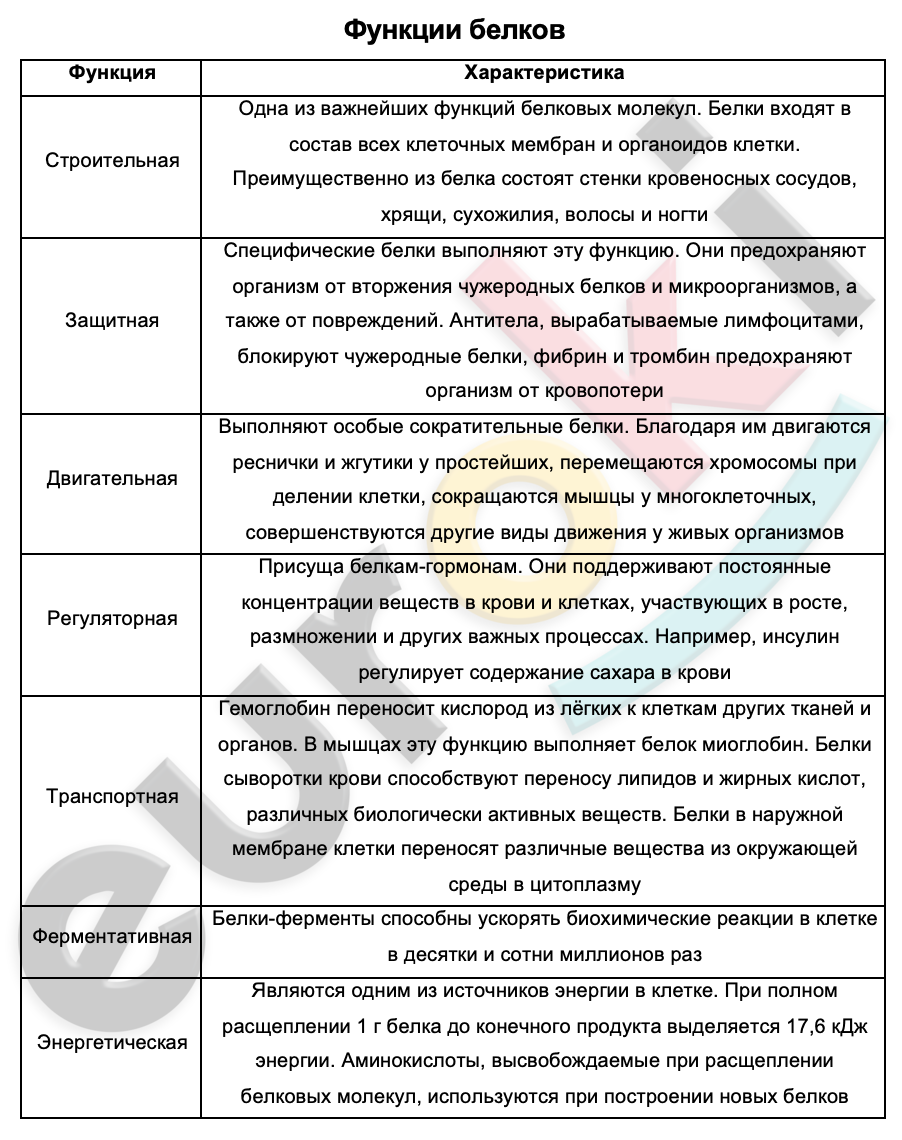
Функции белков
| Функция | Характеристика |
| Каталитическая (ферментативная) | Все ферменты являются белками. Белки-ферменты катализируют протекание в организме химических реакций. Например, каталаза разлагает перекись водорода, амилаза гидролизует крахмал, липаза — жиры, трипсин — белки, нуклеаза — нуклеиновые кислоты, ДНК-полимераза катализирует удвоение ДНК. |
| Строительная (структурная) | Её осуществляют фибриллярные белки. Например, кератин содержится в ногтях, волосах, шерсти, перьях, рогах, копытах; коллаген — в костях, хрящах, сухожилиях; эластин — в связках и стенках кровеносных сосудов. |
| Транспортная | Ряд белков способен присоединять и переносить различные вещества. Например, гемоглобин переносит кислород и углекислый газ, белки-переносчики осуществляют облегчённую диффузию через плазматическую мембрану клетки. |
| Гормональная (регуляторная) | Многие гормоны являются белками, пептидами, гликопептидами. Например, соматропин регулирует рост; инсулин и глюкагон регулируют уровень глюкозы в крови: инсулин повышает проницаемость клеточных мембран для глюкозы, что усиливает её расщепление в тканях, отложение гликогена в печени, глюкагон способствует превращению гликогена печени в глюкозу. |
| Защитная | Например, иммуноглобулины крови являются антителами; интерфероны — универсальные противовирусные белки; фибрин и тромбин участвуют в свёртывании крови. |
| Сократительная (двигательная) | Например, актин и миозин образуют микрофиламенты и осуществляют сокращение мышц, тубулин образует микротрубочки и обеспечивает работу веретена деления. |
| Рецепторная (сигнальная) | Например, гликопротеины входят в состав гликокаликса и воспринимают информацию из окружающей среды; опсин — составная часть светочувствительных пигментов родопсина и йодопсина, находящихся в клетках сетчатки глаза. |
| Запасающая | Например, альбумин запасает воду в яичном желтке, миоглобин содержит запас кислорода в мышцах позвоночных, белки семян растений бобовых — запас питательных веществ для зародыша. |
| Энергетическая | При расщеплении 1 г белков высвобождается 17,6 кДж энергии. |
Ферменты. Белки-ферменты катализируют протекание в организме химических реакций. Эти реакции, в силу энергетических причин, сами по себе либо вообще не протекают в организме, либо протекают слишком медленно.
Ферментативную реакцию можно выразить общим уравнением:
Е+S → [ES] → E+P,
где субстрат (S) обратимо реагирует с ферментом (Е) с образованием фермент-субстратного комплекса (ES), который затем распадается с образованием продукта реакции (Р). Фермент не входит в состав конечных продуктов реакции.
В молекуле фермента имеется активный центр, состоящий из двух участков — сорбционного (отвечает за связывание фермента с молекулой субстрата) и каталитического (отвечает за протекание собственно катализа). В ходе реакции фермент связывает субстрат, последовательно изменяет его конфигурацию, образуя ряд промежуточных молекул, дающих в конечном итоге продукты реакции.
Отличие ферментов от катализаторов неорганической природы:
1. Один фермент катализирует только один тип реакций.
2. Активность ферментов ограничена довольно узкими температурными рамками (обычно 35–45оС).
3. Ферменты активны при определенных значениях рН (большинство в слабощелочной среде).
Нуклеиновые кислоты
Мононуклеотиды. Мононуклеотид состоит из одного азотистого основания — пуринового (аденин — А, гуанин — Г) или пиримидинового (цитозин — Ц, тимин — Т, урацил — У), сахара-пентозы (рибоза или дезоксирибоза) и 1–3 остатков фосфорной кислоты.
В зависимости от числа фосфатных групп различают моно-, ди- и трифосфаты нуклеотидов, например, аденозинмонофосфат — АМФ, гуанозиндифосфат — ГДФ, уридинтрифосфат — УТФ, тимидинтрифосфат — ТТФ и т. д.
Функции мононуклеотидов представлены в таблице.
Функции мононуклеотидов
| Функция | Характеристика |
| Строительная (структурная) | Наиболее важная роль нуклеотидов состоит в том, что они служат строительными блоками для сборки полинуклеотидов: ДНК и РНК (дезоксирибонуклеиновых и рибонуклеиновых кислот). |
| Энергетическая | АТФ является универсальным переносчиком и хранителем энергии в клетке, участвует как источник энергии почти во всех внутриклеточных реакциях. |
| Транспортная | Производные нуклеотидов служат переносчиками некоторых химических групп, например, НАД (никотинамидадениндинуклеотид) и ФАД (флавинадениндинуклеотид) — переносчики атомов водорода. |
Полинуклеотиды. Нуклеиновые кислоты (полинуклеотиды) — полимеры, мономерами которых являются нуклеотиды. Существуют два типа нуклеиновых кислот: ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота).
Нуклеотиды ДНК и РНК состоят из следующих компонентов:
- Азотистое основание (в ДНК: аденин, гуанин, цитозин и тимин; в РНК: аденин, гуанин, цитозин и урацил).
- Сахар-пентоза (в ДНК — дезоксирибоза, в РНК — рибоза).
- Остаток фосфорной кислоты.
ДНК (дезоксирибонуклеиновая кислота) — линейный полимер, состоящий из четырёх типов мономеров: нуклеотидов А, Т, Г и Ц, связанных друг с другом ковалентной связью через остатки фосфорной кислоты.
Молекула ДНК состоит из двух спирально закрученных цепей (двойная спираль). При этом между аденином и тимином образуются две водородные связи, а между гуанином и цитозином — три. Эти пары азотистых оснований называют комплементарными. В молекуле ДНК они всегда расположены друг напротив друга. Цепи в молекуле ДНК противоположно направлены. Пространственная структура молекулы ДНК была установлена в 1953 г. Д. Уотсоном и Ф. Криком.
Связываясь с белками, молекула ДНК образует хромосому. Хромосома — комплекс одной молекулы ДНК с белками. Молекулы ДНК эукариотических организмов (грибов, растений и животных) линейны, незамкнуты, связаны с белками, образуя хромосомы. У прокариот (бактерий) ДНК замкнута в кольцо, не связана с белками, не образует линейную хромосому.
Функция ДНК: хранение, передача и воспроизведение в ряду поколений генетической информации. ДНК определяет, какие белки и в каких количествах необходимо синтезировать.
РНК (рибонуклеиновые кислоты) в отличие от ДНК вместо дезоксирибозы содержат рибозу, а вместо тимина — урацил. РНК, как правило, имеют лишь одну цепь, более короткую, чем цепи ДНК. Двуцепочечные РНК встречаются у некоторых вирусов.
Существует 3 вида РНК.
Виды РНК
| Вид | Характеристика | Доля в клетке, % |
| Информационная РНК (иРНК), или матричная РНК (мРНК) | Имеет незамкнутую цепь. Служит в качестве матриц для синтеза белков, перенося информацию об их структуре с молекулы ДНК к рибосомам в цитоплазму. | Около 5 |
| Транспортная РНК (тРНК) | Доставляет аминокислоты к синтезируемой молекуле белка. Молекула тРНК состоит из 70–90 нуклеотидов и благодаря внутрицепочечным комплементарным взаимодействиям приобретает характерную вторичную структуру в виде «клеверного листа». 1 — 4 — участки комплементарного соединения внутри одной цепочки РНК; 5 — участок комплементарного соединения с молекулой мРНК; 6 — участок (активный центр) соединения с аминокислотой |
Около 10 |
| Рибосомная РНК (рРНК) | В комплексе с рибосомными белками образует рибосомы — органоиды, на которых происходит синтез белка. | Около 85 |
Функции РНК: участие в биосинтезе белков.
Самоудвоение ДНК. Молекулы ДНК обладают способностью, не присущей ни одной другой молекуле, — способностью к удвоению. Процесс удвоения молекул ДНК называется репликацией.
В основе репликации лежит принцип комплементарности — образование водородных связей между нуклеотидами А и Т, Г и Ц.
Репликацию осуществляют ферменты ДНК-полимеразы. Под их воздействием цепи молекулы ДНК разделяются на небольшом отрезке молекулы. На цепи материнской молекулы достраиваются дочерние цепи. Затем расплетается новый отрезок, и цикл репликации повторяется.
В результате образуются дочерние молекулы ДНК, ничем не отличающиеся друг от друга и от материнской молекулы. В процессе деления клетки дочерние молекулы ДНК распределяются между образующимися клетками. Так осуществляется передача информации из поколения в поколение.
Под воздействием различных факторов внешней среды (ультрафиолетового излучения, различных химических веществ) молекула ДНК может повреждаться. Происходят разрывы цепей, ошибочные замены азотистых оснований нуклеотидов и др. Кроме того, изменения в ДНК могут происходить самопроизвольно, например, в результате рекомбинации — обмена фрагментами ДНК. Произошедшие изменения в наследственной информации также передаются потомству.
В некоторых случаях молекулы ДНК способны «исправлять» возникающие в её цепях изменения. Эта способность называется репарацией. В восстановлении исходной структуры ДНК участвуют белки, которые узнают изменённые участки ДНК и удаляют их из цепи, тем самым восстанавливая правильную последовательность нуклеотидов, сшивая восстановленный фрагмент с остальной молекулой ДНК.
Сравнительная характеристика ДНК и РНК представлена в таблице.
Сравнительная характеристика ДНК и РНК
| Признаки | ДНК | РНК |
| Местонахождение в клетке | Ядро, митохондрии, пластиды. Цитоплазма у прокариот | Ядро, рибосомы, цитоплазма, митохондрии, хлоропласты |
| Местонахождение в ядре | Хромосомы | Кариоплазма, ядрышко (рРНК) |
| Строение макромолекулы | Двуцепочечный (как правило) линейный полинуклеотид, свёрнутый правозакрученной спиралью, с водородными связями между двумя цепями | Одноцепочечный (как правило) полинуклеотид. Некоторые вирусы имеют двуцепочечную РНК |
| Мономеры | Дезоксирибонуклеотиды | Рибонуклеотиды |
| Состав нуклеотида | Азотистое основание (пуриновое — аденин, гуанин, пиримидиновое — тимин, цитозин); углевод (дезоксирибоза); остаток фосфорной кислоты | Азотистое основание (пуриновое — аденин, гуанин, пиримидиновое — урацил, цитозин); углевод (рибоза); остаток фосфорной кислоты |
| Типы нуклеотидов | Адениловый (А), гуаниловый (Г), тимидиловый (Т), цитидиловый (Ц) | Адениловый (А), гуаниловый (Г), уридиловый (У), цитидиловый (Ц) |
| Свойства | Способна к самоудвоению (репликации) по принципу комплементарности: А=Т, Т=А, Г=Ц, Ц=Г. Стабильна | Не способна к самоудвоению. Лабильна. Генетическая РНК вирусов способна к репликации |
| Функции | Химическая основа хромосомного генетического материала (гена); синтез ДНК; синтез РНК; информация о структуре белков | Информационная (иРНК) — переносит информацию о структуре белка с молекулы ДНК к рибосомам в цитоплазму; транспортная (тРНК) — переносит аминокислоты к рибосомам; рибосомальная (рРНК) — входит в состав рибосом; митохондриальная и пластидная — входят в состав рибосом этих органелл |
Строение клетки
Клеточная теория
Становление клеточной теории:
- Роберт Гук в 1665 году обнаружил клетки в срезе пробки и впервые применил термин клетка.
- Антони ван Левенгук открыл одноклеточные организмы.
- Маттиас Шлейден в 1838 году и Томас Шванн в 1839 году сформулировали основные положения клеточной теории. Однако они ошибочно считали, что клетки возникают из первичного неклеточного вещества.
- Рудольф Вирхов в 1858 году доказал, что все клетки образуются из других клеток путём клеточного деления.
Основные положения клеточной теории:
- Клетка является структурной единицей всего живого. Все живые организмы состоят из клеток (исключение составляют вирусы).
- Клетка является функциональной единицей всего живого. Клетка проявляет весь комплекс жизненных функций.
- Клетка является единицей развития всего живого. Новые клетки образуются только в результате деления исходной (материнской) клетки.
- Клетка является генетической единицей всего живого. В хромосомах клетки содержится информация о развитии всего организма.
- Клетки всех организмов сходны по химическому составу, строению и функциям.
Типы клеточной организации
Среди живых организмов только вирусы не имеют клеточного строения. Все остальные организмы представлены клеточными формами жизни. Различают два типа клеточной организации: прокариотический и эукариотический. К прокариотам относятся бактерии и цианобактерии (сине-зелёные), к эукариотам — растения, грибы и животные.
Прокариотические клетки устроены сравнительно просто. Они не имеют ядра, область расположения ДНК в цитоплазме называется нуклеоид, единственная молекула ДНК кольцевая и не связана с белками, клетки меньше эукариотических, в состав клеточной стенки входит гликопептид — муреин, мембранные органоиды отсутствуют, их функции выполняют впячивания плазматической мембраны (мезосомы), рибосомы мелкие, микротрубочки отсутствуют, поэтому цитоплазма неподвижна, а реснички и жгутики имеют особую структуру.
Эукариотические клетки имеют ядро, в котором находятся хромосомы — линейные молекулы ДНК, связанные с белками, в цитоплазме расположены различные мембранные органоиды.
Растительные клетки отличаются наличием толстой целлюлозной клеточной стенки, пластид, крупной центральной вакуоли, смещающей ядро к периферии. Клеточный центр высших растений не содержит центриоли. Запасным углеводом является крахмал.
Клетки грибов имеют клеточную стенку, содержащую хитин, в цитоплазме имеется центральная вакуоль, отсутствуют пластиды. Только у некоторых грибов в клеточном центре встречается центриоль. Главным резервным углеводом является гликоген.
Животные клетки не имеют клеточной стенки, не содержат пластид и центральной вакуоли, для клеточного центра характерна центриоль. Запасным углеводом является гликоген.
В зависимости от количества клеток, из которых состоят организмы, их делят на одноклеточные и многоклеточные. Одноклеточные организмы состоят из одной-единственной клетки, выполняющей функции целостного организма. Одноклеточными являются все прокариоты, а также простейшие, некоторые зелёные водоросли и грибы. Тело многоклеточных организмов состоит из множества клеток, объединённых в ткани, органы и системы органов. Клетки многоклеточного организма специализированы для выполнения определённой функции и могут существовать вне организма лишь в микросреде, близкой к физиологической (например, в условиях культуры тканей). Клетки в составе многоклеточного организма различаются по размерам, форме, структуре и выполняемым функциям. Несмотря на индивидуальные особенности, все клетки построены по единому плану и имеют много общих черт.
Характеристика структур эукариотической клетки
| Название | Строение | Функции |
| I. Поверхностный аппарат клетки | Плазматическая мембрана, надмембранный комплекс, субмембранный комплекс | Взаимодействие с внешней средой; обеспечение клеточных контактов; транспорт: а) пассивный (диффузия, осмос, облегченная диффузия через поры); б) активный; в) экзоцитоз и эндоцитоз (фагоцитоз, пиноцитоз) |
| 1. Плазматическая мембрана | Два слоя липидных молекул, в которые встроены молекулы белка (интегральные, полуинтегральные и периферические) | Структурная |
| 2. Надмембранный комплекс: | ||
| а) гликокаликс | Гликолипиды и гликопротеины | Рецепторная |
| б) клеточная стенка у растений и грибов | Целлюлоза у растений, хитин у грибов | Структурная; защитная; обеспечение тургора клетки |
| 3. Субмембранный комплекс | Микротрубочки и микрофиламенты | Обеспечивает механическую устойчивость плазматической мембраны |
| II. Цитоплазма | ||
| 1. Гиалоплазма | Коллоидный раствор неорганических и органических веществ | Протекание ферментативных реакций; синтез аминокислот, жирных кислот; формирование цитоскелета; обеспечение движения цитоплазмы (циклоза) |
| 2. Одномембранные органеллы: | ||
| а) эндоплазматический ретикулум: | Система мембран, образующих цистерны, канальцы | Транспорт веществ внутри и вне клетки; разграничение ферментных систем; место образования одномембранных органелл: комплекса Гольджи, лизосом, вакуолей |
| гладкий | Рибосом нет | Синтез липидов и углеводов |
| шероховатый | Рибосомы есть | Синтез белков |
| б) аппарат Гольджи | Плоские цистерны, крупные цистерны, микровакуоли | Образование лизосом; секреторная; накопительная; укрупнение белковых молекул; синтез сложных углеводов |
| в) первичные лизосомы | Пузырьки, ограниченные мембраной, содержащие ферменты | Участие во внутриклеточном пищеварении; защитная |
| г) вторичные лизосомы: | ||
| пищеварительные вакуоли | Первичная лизосома + фагосома | Эндогенное питание |
| остаточные тельца | Вторичная лизосома, содержащая непереваренный материал | Накопление нерасщеплённых веществ |
| аутолизосомы | Первичная лизосома + разрушенные органеллы клеток | Аутолиз органелл |
| д) вакуоли | В клетках растений мелкие пузырьки, отделённые от цитоплазмы мембраной; полость заполнена клеточным соком | Поддержание тургора клетки; запасающая |
| е) пероксисомы | Мелкие пузырьки, содержащие ферменты, нейтрализующие перекись водорода | Участие в реакциях обмена; защитная |
| 3. Двумембранные органеллы: | ||
| а) митохондрии | Внешняя мембрана, внутренняя мембрана с кристами, матрикс, содержащий ДНК, РНК, ферменты, рибосомы | Клеточное дыхание; синтез АТФ; синтез белков митохондрий |
| б) пластиды: | Внешняя и внутренняя мембраны, строма | |
| хлоропласты | В строме мембранные структуры — ламеллы, образующие диски — тилакоиды, собранные в стопки — граны, содержащие пигмент хлорофилл. В строме — ДНК, РНК, рибосомы, ферменты | Фотосинтез; определение окраски листьев, плодов |
| хромопласты | Содержат жёлтые, красные, оранжевые пигменты | Определение окраски листьев, плодов, цветов |
| лейкопласты | Не содержат пигментов | Накопление запасных питательных веществ |
| 4. Немембранные органеллы: | ||
| а) рибосомы | Имеют большую и малую субъединицы | Синтез белка |
| б) микротрубочки | Трубочки диаметром 24 нм, стенки образованы тубулином | Участие в образовании цитоскелета, делении ядра |
| в) микрофиламенты | Нити диаметром 6 нм из актина и миозина | Участие в образовании цитоскелета; образование кортикального слоя под плазматической мембраной |
| г) клеточный центр | Участок цитоплазмы и две центриоли, перпендикулярные друг другу, каждая образована девятью триплетами микротрубочек | Участие в делении клетки |
| д) реснички и жгутики | Выросты цитоплазмы; в основании находятся базальные тельца. На поперечном срезе ресничек и жгутиков по периметру расположено девять пар микротрубочек и одна пара в центре | Участие в передвижении |
| 5. Включения | Капли жира, гранулы гликогена, гемоглобин эритроцитов | Запасающая; секреторная; специфическая |
| III. Ядро | Имеет двумембранную оболочку, кариоплазму, ядрышко, хроматин | Регуляция активности клетки; хранение наследственной информации; передача наследственной информации |
| 1. Ядерная оболочка | Состоит из двух мембран. Имеет поры. Связана с эндоплазматическим ретикулумом | Отделяет ядро от цитоплазмы; регулирует транспорт веществ в цитоплазму |
| 2. Кариоплазма | Раствор белков, нуклеотидов и других веществ | Обеспечивает нормальное функционирование генетического материала |
| 3. Ядрышки | Мелкие тельца округлой формы, содержат рРНК | Синтез рРНК |
| 4. Хроматин | Неспирализованная молекула ДНК, связанная с белками (мелкозернистые гранулы) | Образуют хромосомы при делении клетки |
| 5. Хромосомы | Спирализованная молекула ДНК, связанная с белками. Плечи хромосомы соединены центромерой, может быть вторичная перетяжка, отделяющая спутник, плечи оканчивают стеломерами | Передача наследственной информации |
Основные различия клеток прокариот и эукариот
| Признак | Прокариоты | Эукариоты |
| Организмы | Бактерии и цианобактерии (сине-зелёные водоросли) | Грибы, растения, животные |
| Ядро | Имеется нуклеоид — часть цитоплазмы, где содержится ДНК, не окружённая мембраной | Ядро имеет оболочку из двух мембран, содержит одно или несколько ядрышек |
| Генетический материал | Кольцевая молекула ДНК, не связанная с белками | Линейные молекулы ДНК, связанные с белками, организованы в хромосомы |
| Ядрышко (и) | Нет | Есть |
| Плазмиды (нехромосомные кольцевые молекулы ДНК) | Есть | В составе митохондрий и пластид |
| Организация генома | До 1,5 тыс. генов. Большинство представлены в единственной копии | От 5 до 200 тыс. генов. До 45% генов представлены несколькими копиями |
| Клеточная стенка | Есть (у бактерий прочность придает муреин, у цианобактерий — целлюлоза, пектиновые вещества, муреин) | Есть у растений (целлюлоза) и грибов (хитин), у животных нет |
| Мембранные органоиды: эндоплазматический ретикулум, аппарат Гольджи, вакуоли, лизосомы, митохондрии и др. | Нет | Есть |
| Мезосома (впячивание плазматической мембраны в цитоплазму) | Есть | Нет |
| Рибосомы | Мельче, чем у эукариот | Крупнее, чем у прокариот |
| Жгутики | если есть, то не имеют микротрубочек и не окружены плазматической мембраной | если есть, то имеют микротрубочки, окружены плазматической мембраной |
| Размеры | диаметр в среднем 0,5–5 мкм | диаметр обычно до 40 мкм |
Основные различия животной и растительной клеток
| Признак | Растительная клетка | Животная клетка |
| Клеточная стенка | Есть | Нет |
| Пластиды | Есть | Нет |
| Вакуоли | Есть крупные, занимают до 70–95% объёма клетки, оттесняя остальные органоиды к периферии клетки, поддерживают тургорное давление | Есть небольшие пищеварительные и сократительные вакуоли, не аналогичные вакуолям растительных клеток |
| Гликокаликс | Нет | Есть |
| Микроворсинки | Нет | Есть |
| Клеточный центр | Есть только у низших растений | Есть |
| Гранулы гликогена | Нет | Есть |
| Гранулы крахмала | Есть | Нет |
Белки – наиболее важные органические соединения клетки. Их содержание колеблется от 50% до 80% в разных клетках организма.
Строение белков
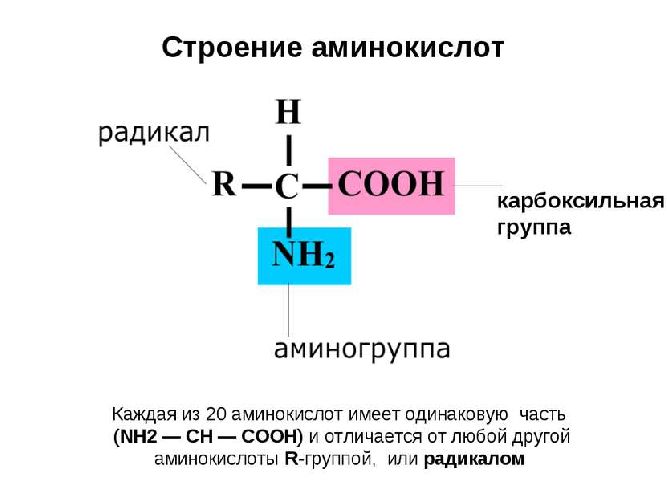
В состав белков, кроме 4 основных химических элементов (углерод, кислорода, водород, азот), могут входит фосфор, сера, железо. Белки – сложные высокомолекулярные соединения, которые составлены из аминокислотных последовательностей. Аминокислоты состоят из двух частей: аминогруппы -NH2 и карбоксильной группы -COOH. Первая несет в себе основные свойства, а вторая – кислотные, что обуславливает активности и амфотерность этих соединений (Амфотерность – проявление кислотных или основных свойств в зависимости от реакции). Аминокислоты отличаются радикалами.
Строение аминокислоты
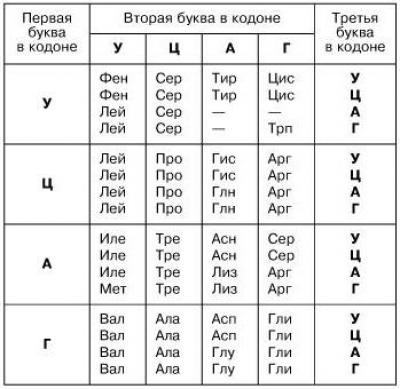
Аминокислоты ассоциируются с генетическим кодом, так как последовательности нуклеотидов кодируют триплеты нуклеотидов. Такие задачи изучаются в школе и встречаются в ЕГЭ. Всем, кто сталкивался с генетикой, хорошо знакома таблица аминокислот:
Таблица аминокислот
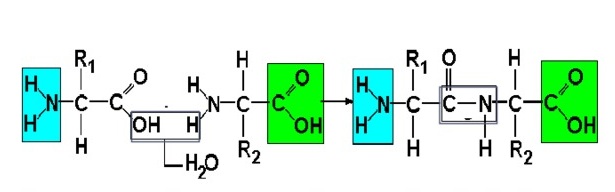
В один белок может входить много аминокислот. Они соединяются в цепь посредством образования пептидных связей: азот одной аминокислоты связывается с углеродом другой аминокислоты:
Строение белка. Зеленым цветом обозначена карбоксильная группа аминокислоты, голубым цветом – аминогруппа аминокислоты
В состав белка может входить даже несколько аминокислотных цепей. Всего аминокислот насчитывается около 170, однако основное разнообразие задают 20 аминокислот, что связано с тем, что одна аминокислота может кодироваться различными последовательностями кодонов, или другими словами, аминокислота может кодироваться разными триплетами нуклеотидов. Это одно из свойств генетического кода (свойство избыточности).
Некоторые аминокислоты животный организм синтезирует самостоятельно, но, как можно догадаться, не все. Такие аминокислоты называются незаменимыми аминокислотами, их следует употреблять с пищей. Например, лейцин используется не просто как биологическая добавка, что достаточно распространено среди фармакологических компаний, но и применяется при лечении заболеваний печени, а также анемии, она же малокровие.
Классификация белков
Протеины – белки, в состав которых входят только белковые молекулы.
Протеиды – белки, в состав которых, кроме белковых молекул, входят небелковые молекулы.
- Гликопротеиды (белок + углевод)
- Липопротеиды (белок + липид)
- Нуклеопротеиды (белок + нуклеиновые кислоты)
Для того чтобы не путаться в понятиях, нужно вспомнить, что принимают спортсмены для того, чтобы скорее нарастить мышечную массу, то есть протеиновые коктейли, батончики и т.д. Именно протеиновые, это слово на слуху, пусть теперь оно ассоциируется с этой классификацией.
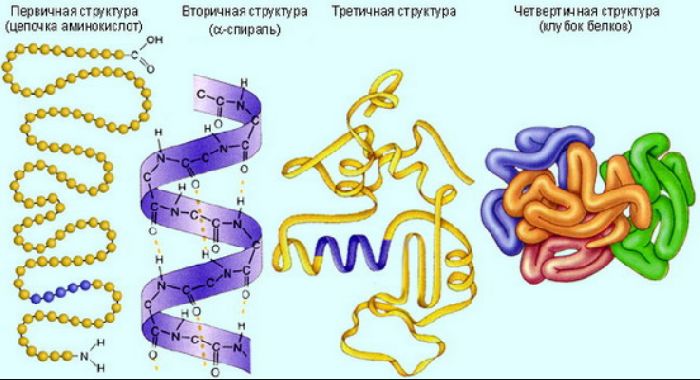
Уровни организации белковой молекулы
Структура белка именуется просто по счету, в зависимости от сложности укладки.
Первичная структура белка представляет собой прямую цепь из аминокислот. Она является главной и определяющей свойства, форму и функции белка.
Вторичная структура белка – уже две цепи. Однако эти цепи не идут параллельно друг другу. Они скручены в спираль и связаны водородными связями, которые их удерживают за счет того, что их много. ДНК была обнаружена именно в форме двойной спирали. В этом виде она наиболее известна.
Третичная структура белка – глобула. Глобула означает шар, что и является описанием структуры белка. В этом случае прочность обусловлена тремя видами связей: водородными, ионными и дисульфидными.
Четвертичная структура белка – это как бы глобула из глобул. Она встречается не у всех белков. Белок крови гемоглобин состоит из 4х субъединиц четвертичной структуры.
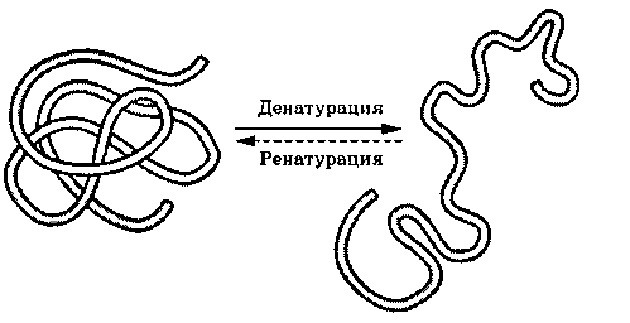
Денатурация – утрата белковой молекулой своей природной структуры. Это обратимый процесс, похожий на сохранение в игре. Если белок денатурировал, но его природная структура не нарушена, то он восстановится. Причин разрушения белка может быть много: высокая температура, химические повреждения, радиация, обезвоживание и т.д. Так что когда мы варим яйца или мясо, то происходит денатурация белка. Как мы видим, к исходному состояния он уже не возвращается (не ренатурирует). Денатурацию и ренатурацию просто запомнить по похожим словам: денатурация – деградация – разрушение; ренатурация – регенерация – восстановление.
Денатурация и ренатурация
Функции белков
1.Структурная функция
Белки входят в состав всего в клетке: мембраны и органоиды. Кроме того, есть белки, которые очень важно знать:
- Коллаген – входит в состав соединительной ткани. Коллаген можно запомнить по кремам, которые обещают продлить молодость и расправить морщины.
- Кератин – известен всем, кто когда-либо смотрел рекламу шампуня для волос. Кератин входит в структуру волос и прочих производных нашего и животного тела: шерсть, перья, ногти, когти, копыта, рога.
- Эластин – как понятно из названия, отвечает за эластичность. Она важна а) в связках, так как они должны растягиваться для совершения движений и возвращаться в исходное состояние. Кстати, в том числе и голосовые связки; б) в сосудах, по которым течет кровь порой под большим давлением, с высоким давлением и скоростью.
2.Ферментативная функция
Ферменты – катализаторы (= ускорители химических реакций) белковой природы. С ферментами происходит тесное знакомство в разделе «пищеварение». Есть одно важное правило, которое нужно обязательно запомнить: все ферменты – белки, но не все белки – ферменты.
3.Транспортная функция
Белки-транспортеры осуществляют перенос веществ через мембрану клетки. Очень наглядным примером транспорта белками является белок-переносчик гемоглобин, благодаря которому мы дышим. В мышцах существует аналог этого белка – миоглобин (приставка мио- означает «сокращение», тем самым называя месторасположение белка).
4.Защитная функция
Изучая иммунитет, ученики и студенты знакомятся с антителами – специфическими белками крови, которые вырабатываются иммунными клетками лимфоцитами для борьбы с чужеродными организмами или вредными соединениями. Так антитела сражаются за нас, когда мы хватаем где-то микробов, так же эти белки воюют, когда человеку переливают кровь неподходящей группы или пересаживают орган, который его организм отторгает. Переливание крови неподходящей группы может привести к летальному исходу, так как произойдет агглютинация – склеивание эритроцитов.
Некоторые растения и животные вырабатывают яды или токсины для того, чтобы защитить себя от нападения и поедания. Поэтому не следует есть незнакомые ягоды, грибы и ловить где-нибудь в тропиках лягушек. Это может закончиться плачевно.
Кроме оборонительной и атакующей функции во благо защиты организма, есть и латающая. При порезе и кровопотере молекулы белка тромбина объединяются для того, чтобы закрыть поврежденный сосуд, а тем временем, тонкие нити белка фибрина переплетаются на поверхности раны, образуя тоненькую пленочку. Если порез был несерьезным, то кровотечение успешно остановлено.
5.Регуляторная функция
Некоторые белки являются гормонами. Они отвечают за регуляцию физиологических процессов организма. Наиболее известным примером белкового гормона является инсулин.
6.Энергетическая функция
Как и углеводы с жирами, белки тоже могут быть расщеплены для получения энергии. Однако, чаще всего, аминокислоты, полученные в результате распада белка, снова используются организмом для построения других белков. Это делает для экономии энергии и биологического материала, ведь в случае повторного использования, не нужно тратиться на синтез новых соединений. При расщеплении 1 г белка высвобождается 17,6 кДж энергии.
Задание EB11693
Установите соответствие между классами органических веществ и выполняемыми ими функциями в клетке.
| ОСОБЕННОСТИ СТРОЕНИЯ И СВОЙСТВ ВЕЩЕСТВА | ВЕЩЕСТВА |
|
A) запасание энергии Б) сигнальная B) хранение генетической информации Г) перенос энергии Д) входит в состав клеточных стенок и мембран Е) реализация генетической информации (синтез белка) |
1) углеводы 2) нуклеиновые кислоты (ДНК, РНК) |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
| А | Б | В | Г | Д | Е |
Для начала вспомним какие вообще есть классы органических веществ в клетке.
Это белки, жиры, углеводы и нуклеиновые кислоты. Белки, жиры и углеводы являются источниками энергии, но у них есть и более локальные функции:
| Белки | Жиры | Углеводы | Нуклеиновые кислоты | |
| Структурная | + | + | ||
| Энергетическая | + | + | + | |
| Защитная | + | + | ||
| Ферментативная | + | |||
| Двигательная | + | |||
| Транспортная | + | |||
| Регуляторная | + | |||
| Рецепторная | + | |||
| Хранение и передача ген.информации | + | |||
| Биосинтез белка | + |
Выберем вначале то,что относится к нуклеиновым кислотам: биосинтез белка и хранение генетической информации.
Остальное — углеводы.
PS: сигнальная и рецепторная функция — одно и то же.
Ответ: 112112
pазбирался: Ксения Алексеевна | обсудить разбор | оценить
Задание EB21891
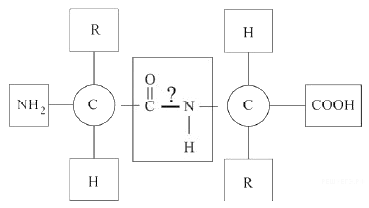
Рассмотрите предложенную схему реакции между аминокислотами. Запишите в ответ понятие, обозначающее название химической связи, отмеченной на схеме знаком вопроса.
На данной схеме изображена реакция между двумя аминокислотами, что известно из вопроса. Между ними действуют пептидные связи.
Пептидная связь — это химическая связь, возникающая между двумя молекулами в результате реакции конденсации между карбоксильной группой (-СООН) одной молекулы и аминогруппой (-NH2) другой молекулы, при выделении одной молекулы воды (H2O).
Ответ: пептидная
pазбирался: Ксения Алексеевна | обсудить разбор | оценить
Ксения Алексеевна | Просмотров: 5.5k
Задумайтесь! Мы с вами состоит из миллиардов атомов. Все атомы находятся в круговороте, и
все атомы, которыми мы обладаем, в ком-то и где-то находились те 4,5 млрд. лет, которые существует Земля. Они были частями
животных, растений, грибов и бактерий — а сейчас принадлежат нам на короткое время.

С химической точки зрения ответ на вопрос «Жив ли изучаемый объект?» — не представляется возможным. Понятию «жизнь» дано
колоссальное количество определений. Жизнь — это самовоспроизведение с изменением, способ существования белковых тел,
постоянный обмен веществ с внешней средой.
Мы приступаем к изучению неорганических и органических веществ клетки. Начнем с неотъемлемого компонента клетки,
благодаря которому жизнь на Земле в принципе стала возможна — вода.
Вода
Составляет 60-80% массы клетки. Молекула воды обладает уникальным свойством — полярностью, которое возникает из-за
разницы в электроотрицательности (ЭО) между атомами кислорода и водорода (у кислорода ЭО больше).

Поскольку молекула воды полярна, ее называют диполь. Между молекулами воды возникают непрочные водородные связи:
водородная связь начинается от отрицательно заряженного атома кислорода (2δ—) одной молекулы воды и
тянется до положительно заряженного атома водорода другой молекулы воды (δ+)
По отношению к воде все вещества можно подразделить на два типа:
- Гидрофильные (греч. hydro — вода и philéo — люблю) — вещества, которые хорошо растворяются в воде. Гидрофильными
веществами являются сахара, соли, альдегиды, спирты, аминокислоты. - Гидрофобные (греч. hydro — вода и phobos — страх) — вещества, которые не растворяются в воде. Гидрофобными
веществами являются жиры.
Роль воды в клетке трудно переоценить. Ее функции и свойства крайне важны:
- Вода — универсальный растворитель
- Вода — терморегулятор
- Вода — реагент
- Транспортная функция
- Структурная функция
Большинство реакций, которые протекают в клетке, идут в растворе (водной среде). Полярность молекулы воды позволяет
ей быть отличным растворителем для других гидрофильных (полярных) веществ.
Вода может поглощать теплоту при минимальном изменении температуры. Это настоящее «спасение» для клеток: чуть только
температура меняется, вода начинает поглощать избыток тепла, защищая клетку от перегревания. Выделяясь на поверхность
кожи с потом, вода испаряется, поверхность кожи при этом охлаждается.
Она не только создает среду для реакций в клетке, но и сама активно участвует во многих из них. Расщепление питательных
веществ, попавших в клетку, происходит за счет реакции гидролиза (греч. hydro — вода и lysis — расщепление).
Питательные вещества, газы перемещаются по организму с током крови. Вода составляет 90-92% плазмы крови, является ее основным
компонентом. С помощью воды происходит не только доставка веществ к клеткам, но и удаление из организма побочных продуктов
обмена веществ.

Вода придает тканям тургор (лат. turgor — наполнение) — внутреннее осмотическое давление в живой клетке, создающее
напряжение оболочек клеток. Вода составляет от 60 до 95% цитоплазмы, придает клеткам форму. Изменение тургора клеток растений
приводит к перемещениям их частей, раскрытию устьиц, цветков.
Осмотическое давление — избыточное гидростатическое давление на раствор, отделенный от чистого растворителя с
помощью полупроницаемой мембраны.
Главное — понимать суть: если мы поместим живую клетку в гипертонический раствор, то
вода (растворитель) устремится из клетки в раствор (в сторону большей концентрации соли) — это приведет к сморщиванию
клеток.
Если же клетка окажется
в гипотоническом растворе, то вода извне устремится внутрь клетки (опять-таки в сторону большей концентрации солей),
приводя при этом к разбуханию (и возможному разрыву) клетки.

Элементы
Живая клетка — кладезь элементов таблицы Менделеева. Процент содержания различных элементов отличается, в связи с чем все они делятся на
3 группы:
- Биогенные (основные) — C, H, O, N. Входят в состав органических соединений, составляют основную часть клетки
- Макроэлементы (греч. makrós — большой) — составляют десятые и сотые доли в клетке: K, Na, Ca, Mg, Cl, P, S
- Микроэлементы (греч. mikrós — маленький) — составляют тысячные доли в клетке: Zn, Cu, I, Co, Mn, Fe
Процентное содержание элемента не коррелирует с его важностью и биологической значимостью. Так, к примеру, микроэлемент
I играет важную роль в синтезе гормонов щитовидной железы: тироксина, трийодтиронина. За нормальные рост и развитие
организмов отвечают Zn, Mn, Cu.
Благоприятно влияют на сперматозоиды Zn, Ca, Mg, защищая их от оксидативного стресса (окисления). Невозможным становится
нормальное образование эритроцитов без должного уровня Fe и Cu.

Соли
В водной среде клетки соли диссоциируют (распадаются) на положительно заряженные ионы — катионы (Na+, K+,
Ca2+, Mg2+) и отрицательно заряженные — анионы (Cl—, SO42-,
HPO42-, H2PO4—).
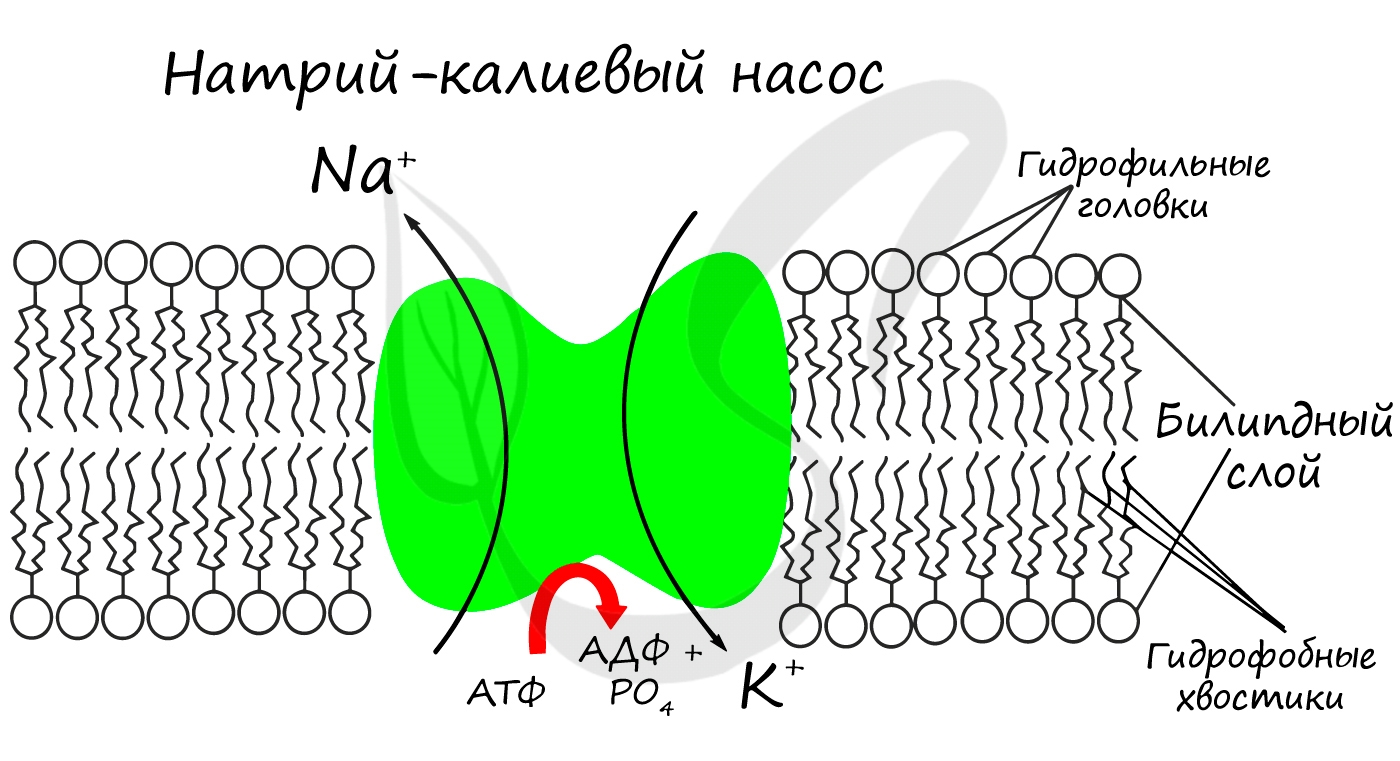
Для процессов возбуждения клетки (нейрона, миоцита — мышечной клетки) внутри клетки должна поддерживаться низкая концентрация ионов Na+ и высокая концентрация ионов K+. В окружающей клетку среде все наоборот: много Na и мало K. В мембране существует
специальный натрий-калиевый насос, который поддерживает необходимое равновесие. Если это
соотношение нарушится, то нейрон не сможет сгенерировать нервный импульс, а клетка мышцы — сократиться.
Соли в клетке и организме выполняют ряд важных функций:
- Участвуют в активации ферментов
- Создают буферные системы (бикарбонтаную, фосфатную, белковую)
- Поддерживают кислотно-щелочное состояние (КЩС)
- Создают осмотическое давление клетки
- Создают мембранный потенциал клеток (натрий-калиевый насос)
- Являются основным минеральным составляющим скелета внутреннего и наружного (у моллюсков)

Мы переходим к органическим компонентам клетки, к которым относятся: жиры, углеводы, белки и нуклеиновые кислоты.
Белки, или пептиды (греч. πεπτος — питательный)
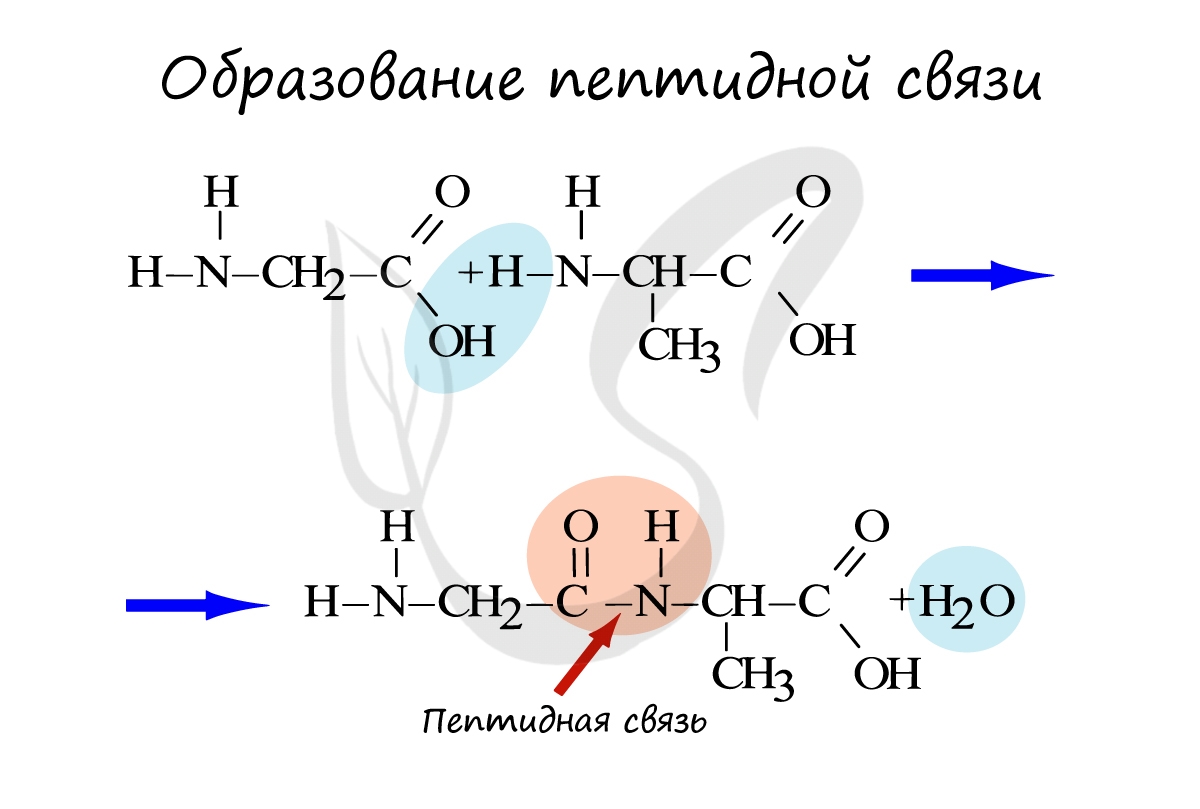
Белки — полимеры, мономерами которых являются аминокислоты. Белки представляют линейную структуру, образованную из
длинной цепи аминокислот, между которыми возникают пептидные связи. Пептидная связь образуется между карбоксильной
группой (COOH) одной аминокислоты и аминогруппой другой аминокислоты (NH2).
Между понятиями пептиды и белки существует определенная разница. Белки состоят из сотен тысяч аминокислот. Пептидами
называют небольшие белки, содержащие до 10 аминокислот. Ими являются некоторые гормоны: окситоцин,
вазопрессин, тиреолиберин — эти пептиды выполняют регуляторную функцию.
Выделяется несколько уровней пространственной организации белка:
- Первичная — полипептидная цепь, в которой аминокислоты расположены линейно
- Вторичная — полипептидная цепь закручивается в спираль, формируется α или β структура
- Третичная — спирали скручиваются в глобулу (лат. globulus — шарик)
- Четвертичная — образуется у сложных белков путем соединения нескольких глобул

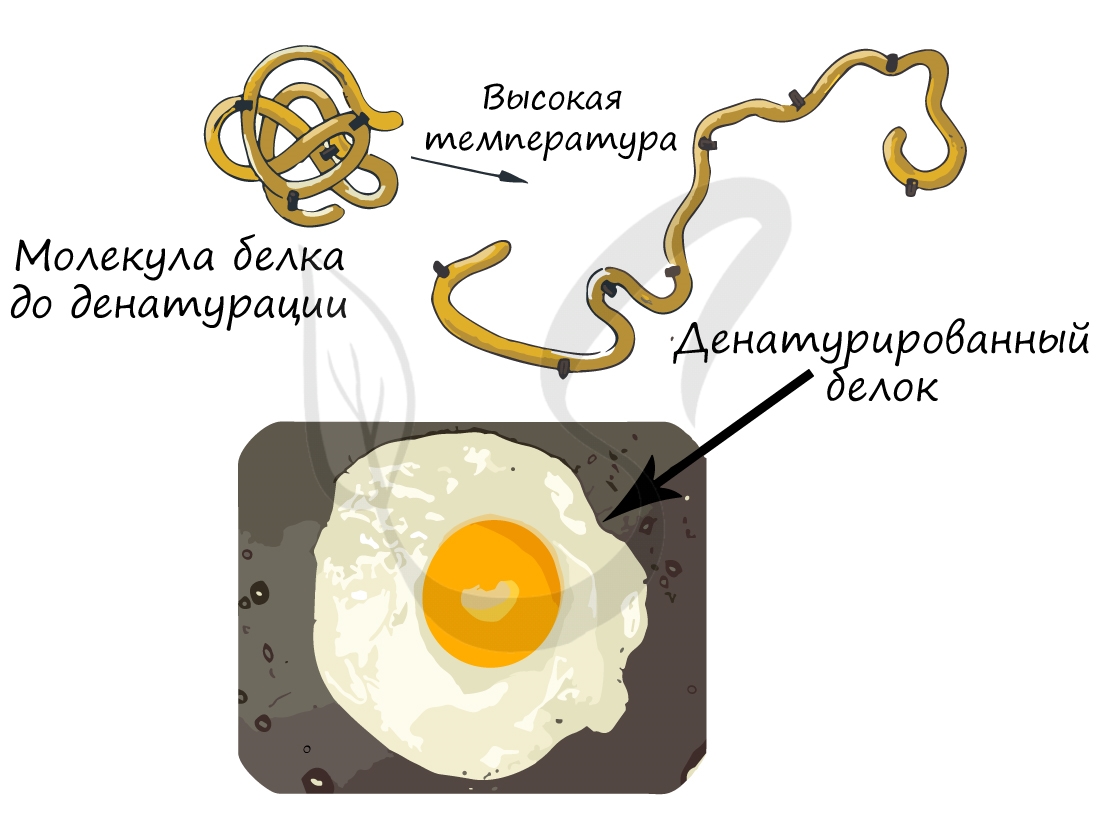
При резком изменении оптимальных для белка условий он подвергается денатурации: при этом происходит переход от
высших структур организации к низшим, или «раскручивание белка». Важно заметить, что аминокислотная последовательность (первичная структура белка) при этом не меняется, однако свойства белка меняются кардинально (теряется его гидрофильность).
Осмелюсь сделать заявление: вы часто начинаете свой день с денатурации белка. Простейший способ провести такой
эксперимент — пожарить яичницу. Заметьте, что изначально яичный белок прозрачный и текучий, но по итогу жарки эти свойства
утрачиваются: он становится непрозрачным и вязким.
Завершаем тему о белках изучением их функций:
- Каталитическая (греч. katalysis — разрушение)
- Строительная
- Регуляторная
- Защитная
- Энергетическая
- Транспортная
- Сократительная
- Рецепторная
Белки — природные катализаторы, ускоряющие реакции в организме в десятки и сотни тысяч раз. Эту роль главным образом
выполняют белки-ферменты (энзимы).
Иногда в состав белков входят так называемые ко-факторы — небелковые соединения,
которые необходимы ферменту для его биологической активности (в роли ко-факторов могут выступать Zn2+,
Mg2+).
Белки входят в состав клеточных мембран. Сложные белки: коллаген, эластин — входят в состав соединительных тканей организма,
придавая им некоторую прочность и эластичность.
Некоторые гормоны, регулирующие обменные процессы в организме, имеют белковое происхождение: инсулин, глюкагон,
адренокортикотропный гормон (АКТГ).
Говоря об этой функции, прежде всего, стоит вспомнить об антителах — иммуноглобулинах, которые синтезируют B-лимфоциты.
Антитела нейтрализуют чужеродные организму антигены (разрушают бактерии).

Помимо антител, защитную функцию выполняют
также белки свертывающей системы крови (тромбин и фибриноген): они предохраняют организм от кровопотери.
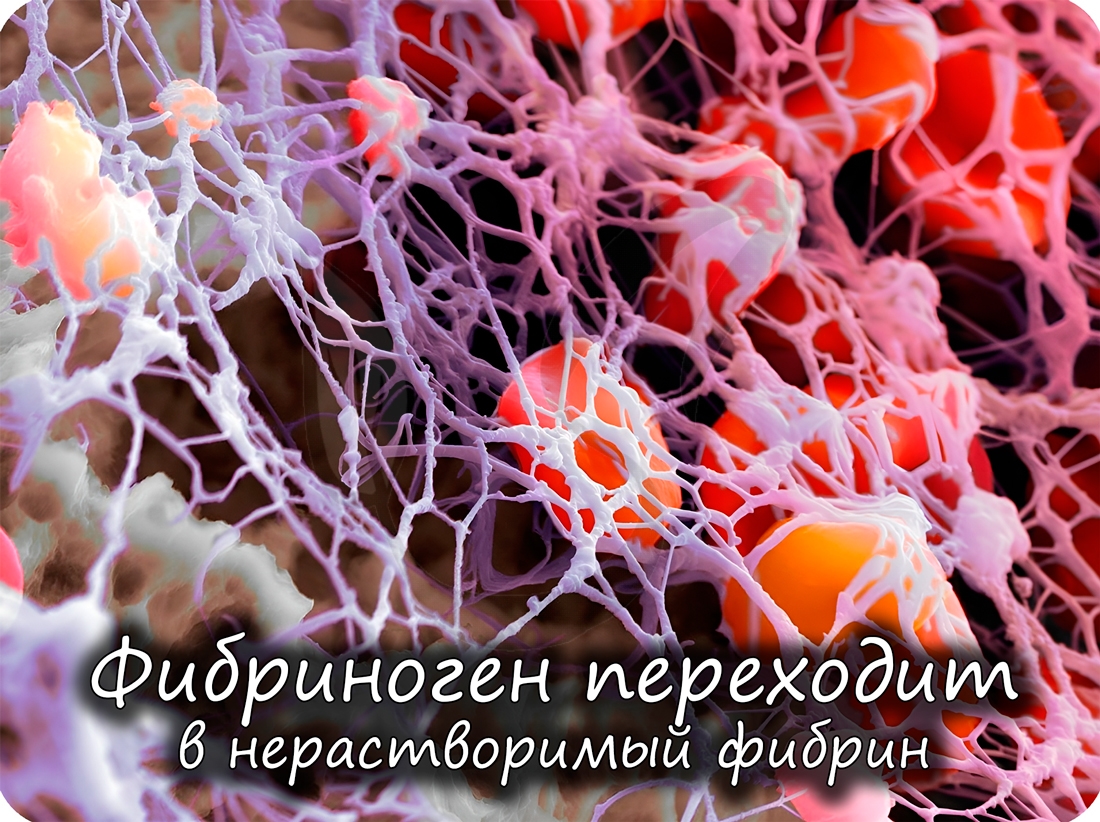
При недостаточном питании в организме начинают окисляться молекулы белков. При расщеплении 1 г белков выделяется 17,6 кДж энергии.
Некоторые белки крови способны присоединять к себе и переносить различные молекулы. Альбумины участвуют в транспорте
жирных кислот, глобулины — гормонов и некоторых ионов (Fe, Cu). Основной белок эритроцитов — гемоглобин — способен
переносить кислород, углекислый и угарный газы (угарный конечно нежелательно ему переносить, будет отравление)
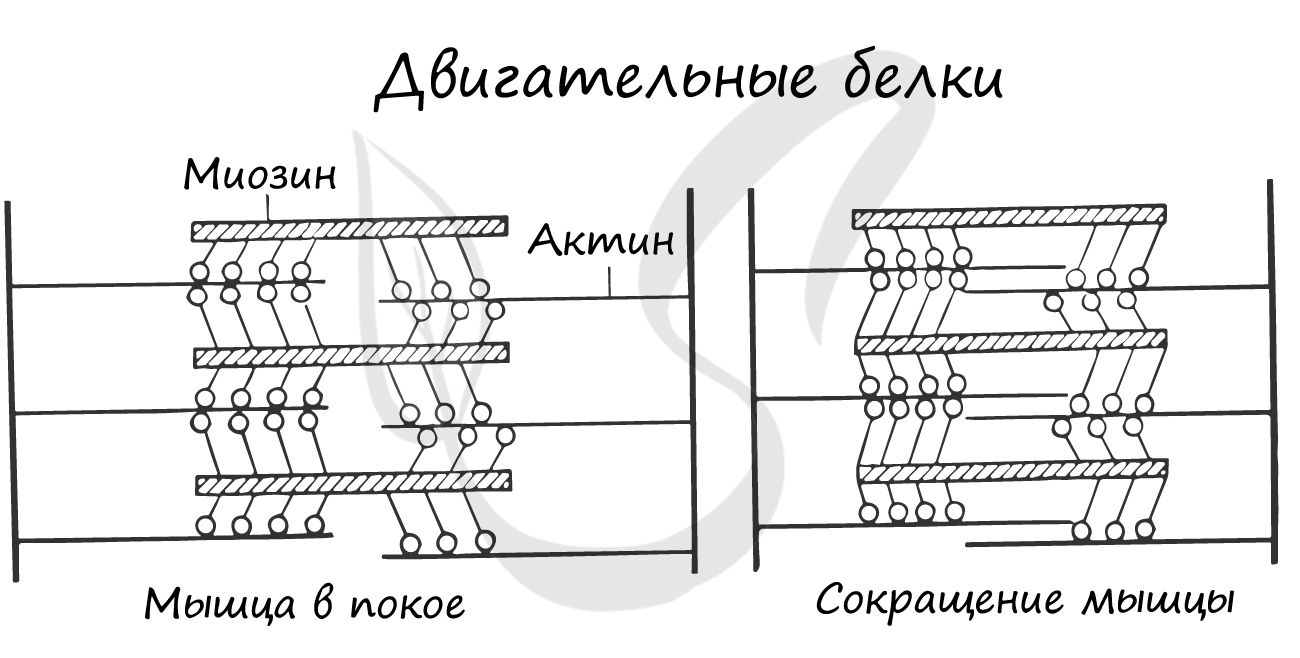
Двигательные белки, актин и миозин, на уровне саркомера обеспечивают сокращение мышц. При возбуждении мышечной
ткани тонкие нити актина начинают тереться о толстые нити миозина, приводя к сокращению.
На поверхности мембраны белки образуют многочисленные рецепторы, которые, соединяясь с гормонами, приводят к
изменению обмена веществ в клетке. Таким образом, гормоны реализуют воздействие на клетки органов-мишеней.
Жиры, или липиды (греч. lipos — жир)
С химической точки зрения жиры являются сложными эфирами, образованными трехатомным спиртом глицерином и высшими
карбоновыми кислотами (жирными кислотами). Среди их свойств надо выделить то, что они практически нерастворимы
в воде. Вспомните, как тяжело смыть жир с рук водой.
Почему именно мыло смывает жир с рук? Дело в том, что молекула мыла повторяет свойства жира: одна часть ее гидрофобна,
а другая гидрофильна. Мыло соединяется с молекулой жира гидрофобной частью, и вместе они легко смываются водой.
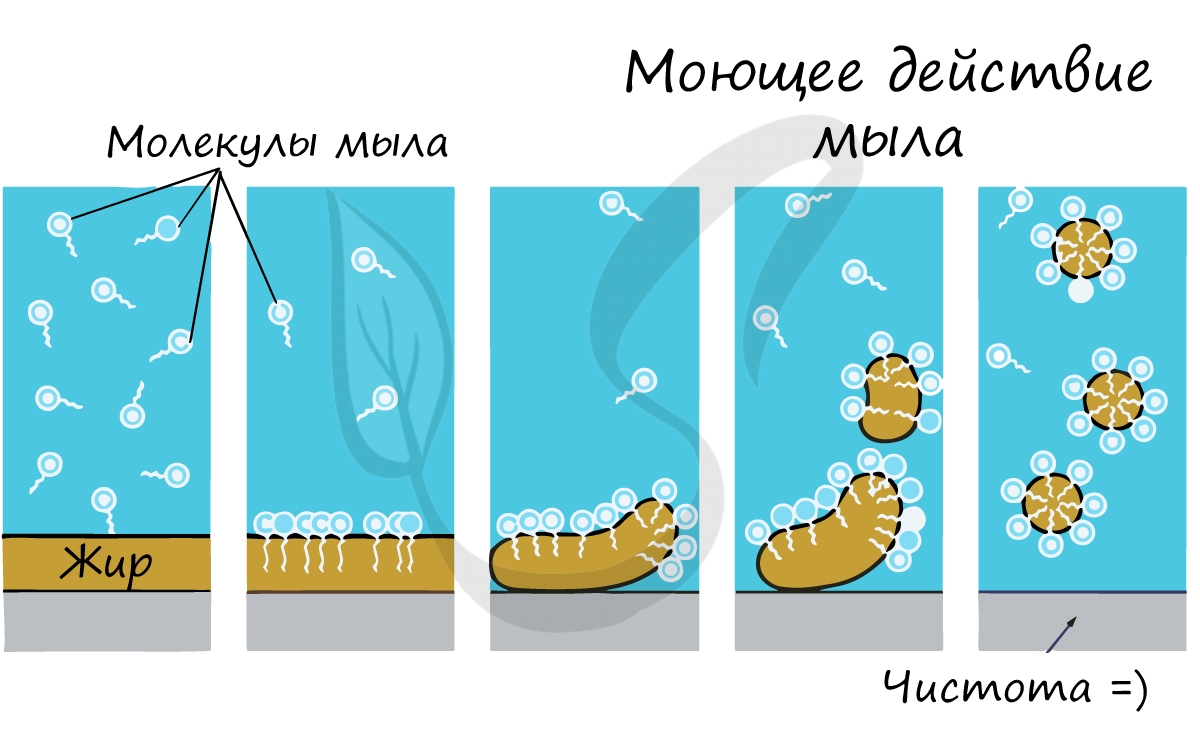
Приступим к изучению функций жиров:
- Энергетическая
- Запасающая
- Структурная
- Терморегуляция
- Гормональная
- Участие в обмене веществ (метаболизме)
При окислении жиров выделяется много энергии: 1 г — 38,9 кДж. Это вдвое больше выделяющейся энергии при расщеплении
1г углеводов.
Жиры имеют способность накапливаться в клетках, расположенных в подкожно-жировой клетчатке, внутренних органах.
Эти запасы являются резервом организма на случай голодания или при недостаточном питании.
В жирах также запасается вода: в 100 г жира содержится 107 мл воды. Многим пустынным животным (верблюдам)
жировые запасы помогают длительное время обходиться без воды.
Жиры входят в состав биологических мембран клеток человека вместе с белками. Из фосфолипидов построены мембраны всех
клеток органов и тканей!
Так, к примеру, холестерин — обязательный компонент мембраны, придает ей определенную жесткость и совершенно необходим
для нормальной жизнедеятельности (заболевания возникают только при нарушении липидного обмена).

Жиры обладают плохой теплопроводностью. Располагаясь в подкожно-жировой клетчатке, они образуют термоизолирующий слой.
Особенно хорошо он развит у ластоногих (моржи и тюлени), китов, защищает их от переохлаждения.
Некоторые гормоны по строению относятся к жирам: половые (андрогены — мужские и эстрогены — женские), гормон
беременности (прогестерон), кортикостероиды.
Производное жира — витамин D — принимает важное участие в обмене кальция и фосфора в организме. Он образуется
в коже под действием ультрафиолетового излучения (солнечного света). При недостатке витамина D возникает заболевание —
рахит.

Углеводы
Представляют собой органические соединения, состоящие из одной или нескольких молекул простых сахаров. Выделяется три основных
класса углеводов:
- Моносахариды (греч. monos — единственный)
- Олигосахариды (греч. ὀλίγος — немногий)
- Полисахариды
Простые сахара, легко растворяющиеся в воде и имеющие сладкий вкус. Моносахариды подразделяются на гексозы (имеют 6 атомов углерода)
— глюкоза, фруктоза, и пентозы (имеют 5 атомов углерода) — рибоза и дезоксирибоза, входящие в состав нуклеиновых кислот.
При гидролизе олигосахариды распадаются на моносахариды. В состав олигосахаридов может входить от 2 до 10 моносахаридных остатков.
Если в состав олигосахарида входят 2 остатка моносахарида, то его называют дисахарид. К дисахаридам относятся сахароза, лактоза,
мальтоза. При гидролизе сахароза распадается на глюкозу и фруктозу.
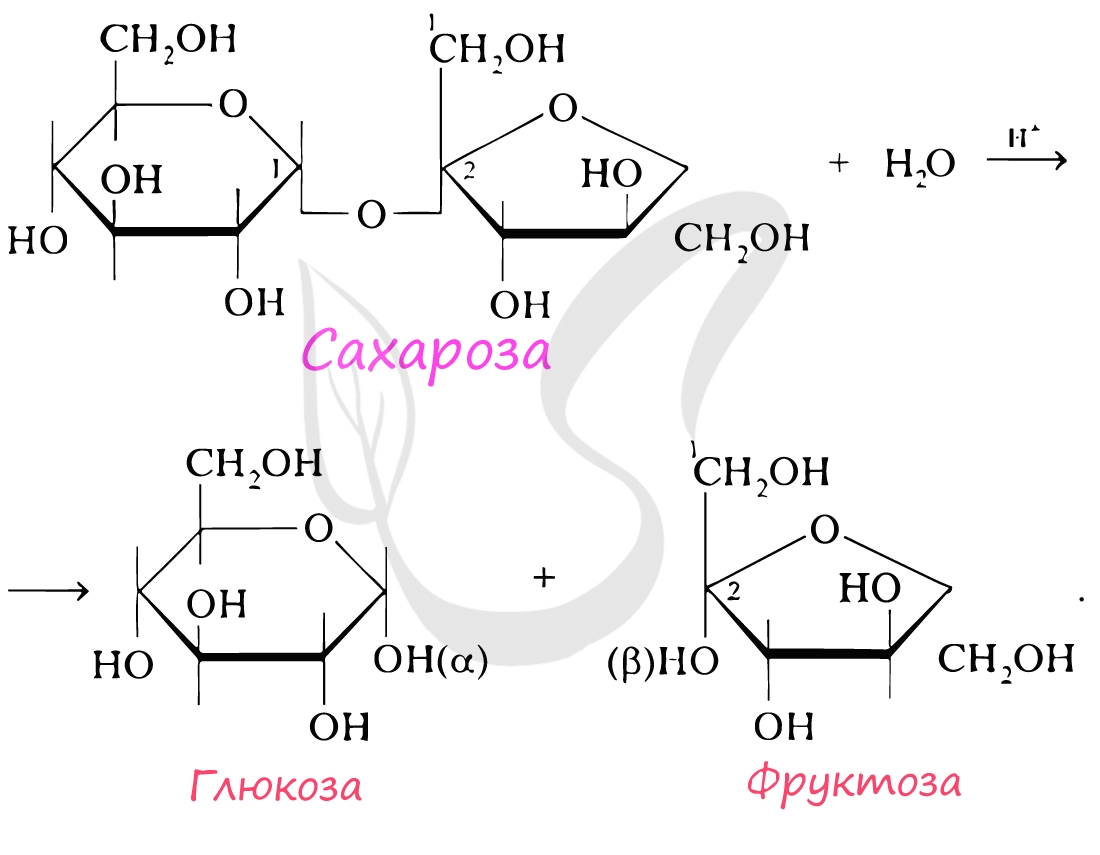
Это биополимеры, в состав которых входят сотни тысяч моносахаридов. Они обладают высокой молекулярной массой,
нерастворимы в воде, на вкус несладкие.
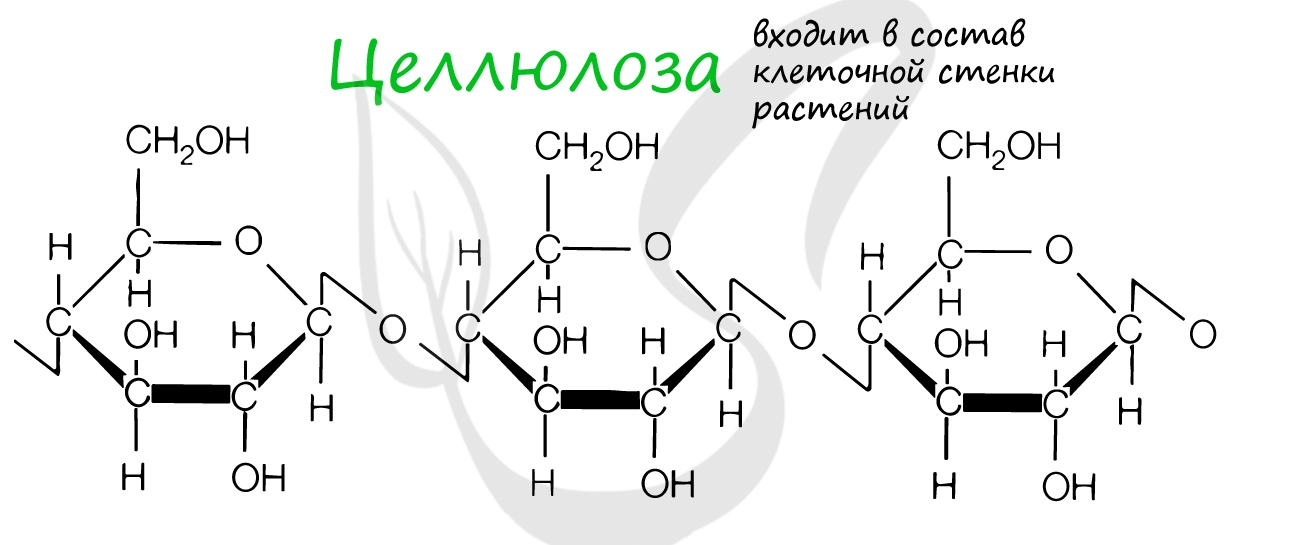
Крахмал, целлюлоза, гликоген, хитин и муреин — все это биополимеры. Давайте вспомним, где они находятся.
Клеточная стенка образована: у растений — целлюлозой, у грибов — хитином, у бактерий — муреином. Запасным питательным
веществом растений является крахмал, животных — гликоген.
Перечислим функции, которые выполняют углеводы:
- Энергетическая
- Запасающая
- Структурная (опорная)
В результате расщепления 1 г углеводов высвобождается 17,6 кДж энергии.
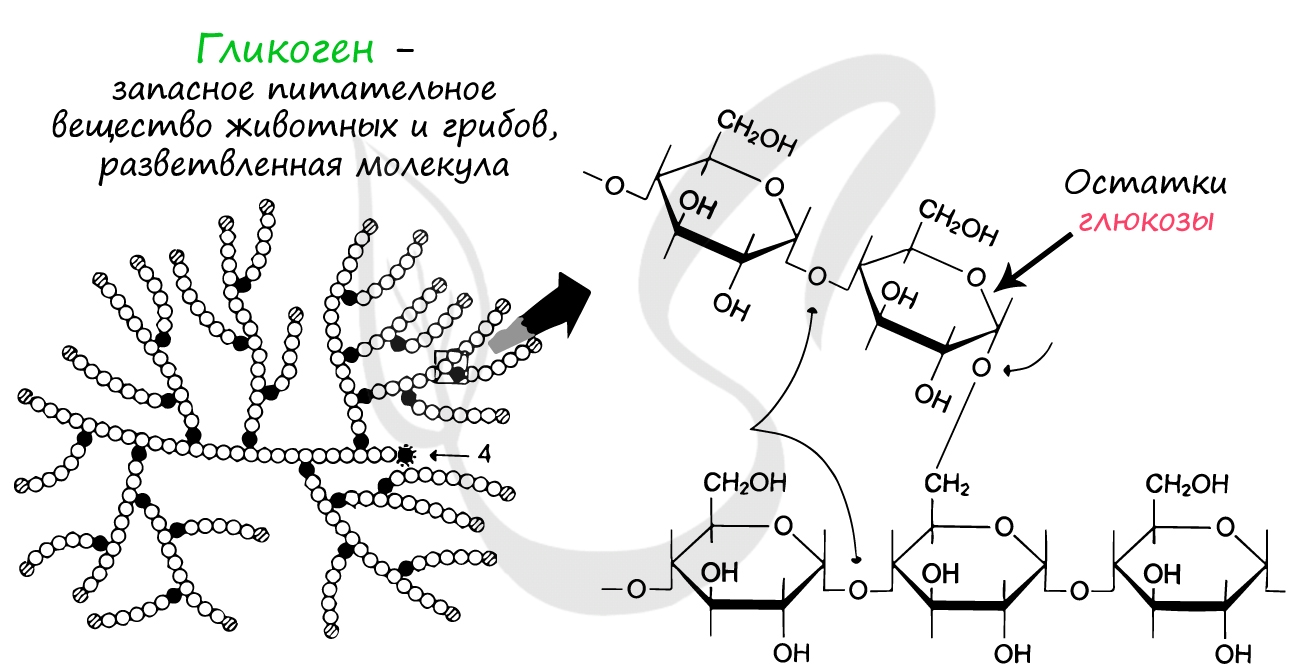
Запасным питательным веществом растений и животных соответственно являются крахмал и гликоген. Расщепление гликогена позволяет
нам оставаться в сознании и быть активными между приемами пищи.
Гликоген представляет собой разветвленную молекулу, состоящую
из остатков глюкозы. За счет больших размеров такая молекула хорошо удерживается в клетке, а ее разветвленность позволяет ферментам
быстро отщеплять множество молекул глюкозы одновременно.
Существуют заболевания, при которых распад
гликогена нарушается: в результате нейроны не получают глюкозы (источника энергии, соответственно не синтезируются и молекулы АТФ). Из-за этого становятся возможны частые потери сознания.
Целлюлоза входит в состав клеточных стенок растений, придавая им необходимую твердость. Хитин образует клеточную стенку
грибов и наружный скелет членистоногих.

Нуклеиновые кислоты (от лат. nucleus — ядро)
Высокомолекулярные органические соединения, представленные двумя видами: ДНК (дезоксирибонуклеиновые кислоты) и РНК
(рибонуклеиновые кислоты). ДНК и РНК — биополимеры, мономером которых является нуклеотид. Запомните, что нуклеотид
состоит из 3 компонентов:
- Азотистое основание
- Остаток сахара
- Остаток фосфорной кислоты — фосфат
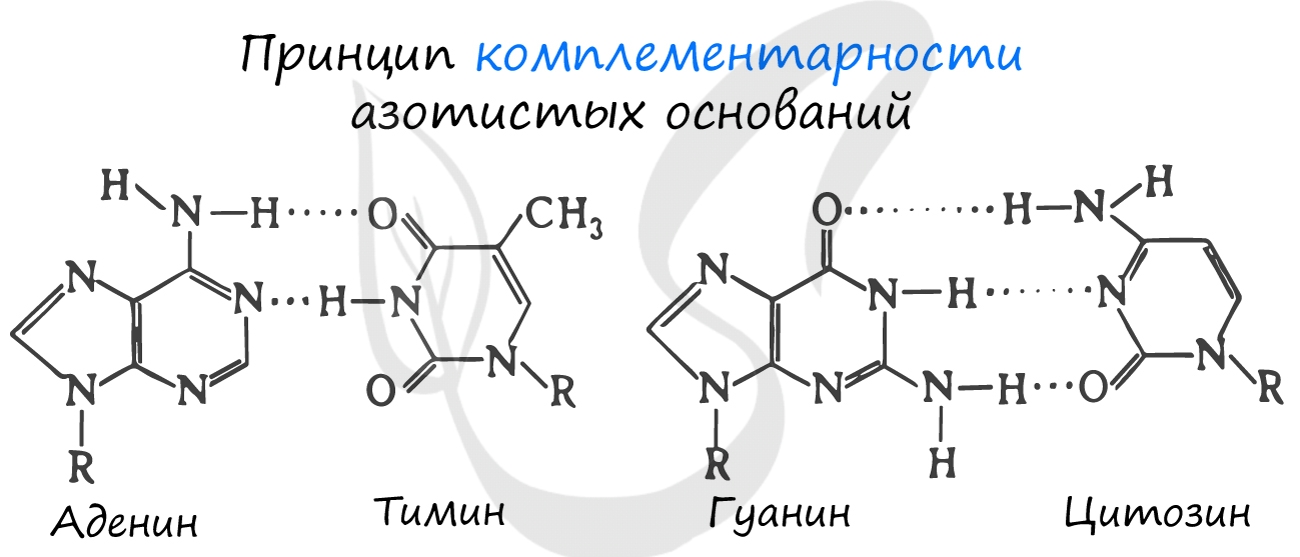
Для ДНК характерны следующие азотистые основания: аденин — тимин, гуанин — цитозин; для РНК: аденин — урацил,
гуанин — цитозин. Исходя из принципа комплементарности, данные основания соответствуют друг другу, в результате
чего между ними образуются связи.
Между аденином и тимином образуется 2 водородные связи, а между гуанином и цитозином — 3.
Именно по этой причине количество аденина в молекуле ДНК всегда совпадает с количеством тимина. К примеру, если
в ДНК 20% аденина, то с уверенностью можно сказать, что в ней 20% тимина. Выходит на оставшиеся основания — цитозин
и гуанин — остается 60%, значит, цитозин и гуанин составляют в ДНК 30% каждый. Таким нехитрым образом, зная процент
содержания одного основания, можно подсчитать все остальные.
В ДНК остаток сахара — дезоксирибоза, в РНК — рибоза.
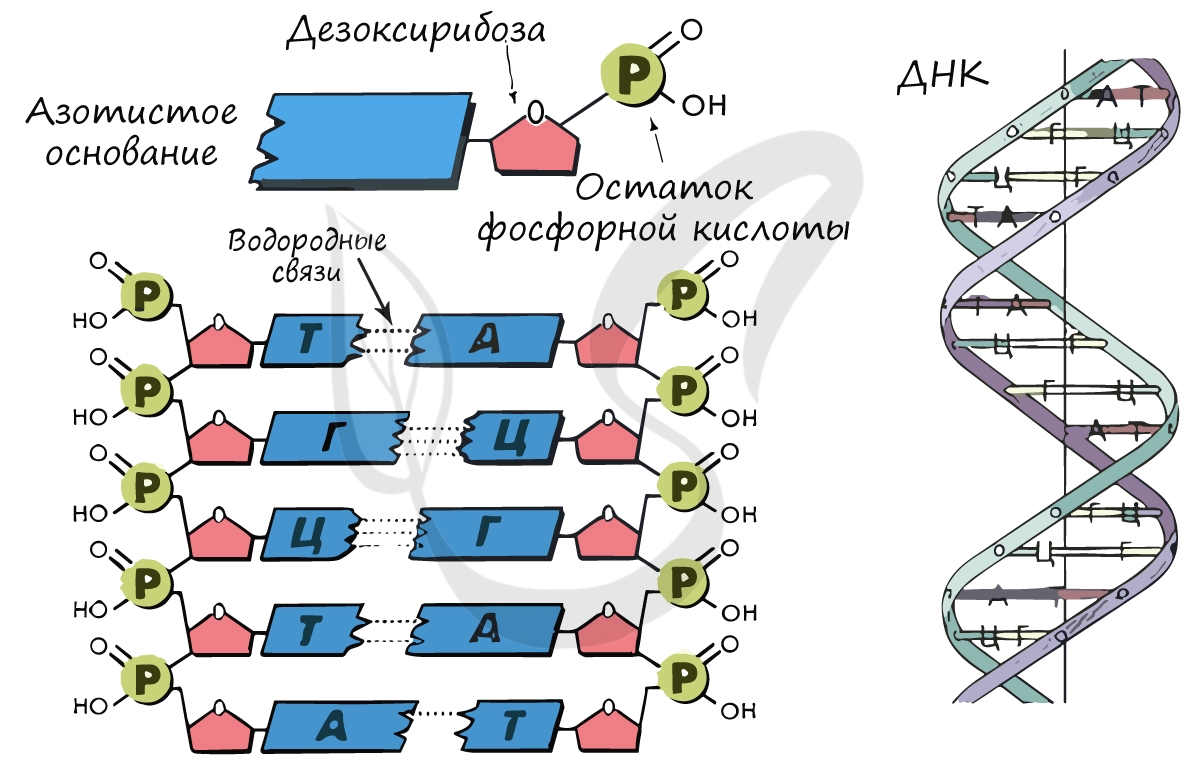
Мы подробно изучили структуру ДНК (дезоксирибонуклеиновой кислоты) — двойной правозакрученной спиральной молекулы. Теперь
настало время детально поговорить об РНК (рибонуклеиновой кислоте). Все виды РНК синтезируются на матрице — ДНК, различают
три вида РНК:
- Рибосомальная РНК (рРНК)
- Информационная РНК (иРНК, син. — матричная РНК, мРНК)
- Транспортная РНК (тРНК)
Синтезируется в ядрышке. рРНК входит в состав
малых и больших субъединиц рибосом. В процентном отношении рРНК составляет 80-90% всей РНК клетки.
Синтезируется в ядре в ходе процесса транскрипции (лат. transcriptio — переписывание).
Фермент РНК-полимераза строит цепь иРНК по принципу комплементарности с ДНК. Исходя из данного принципа,
гуанин (Г) в молекуле ДНК соединяется с цитозином (Ц) в РНК. Далее соответственно: цитозин (Ц) — гуанин (Г),
аденин (А) — урацил (У), тимин (Т) — аденин (А).
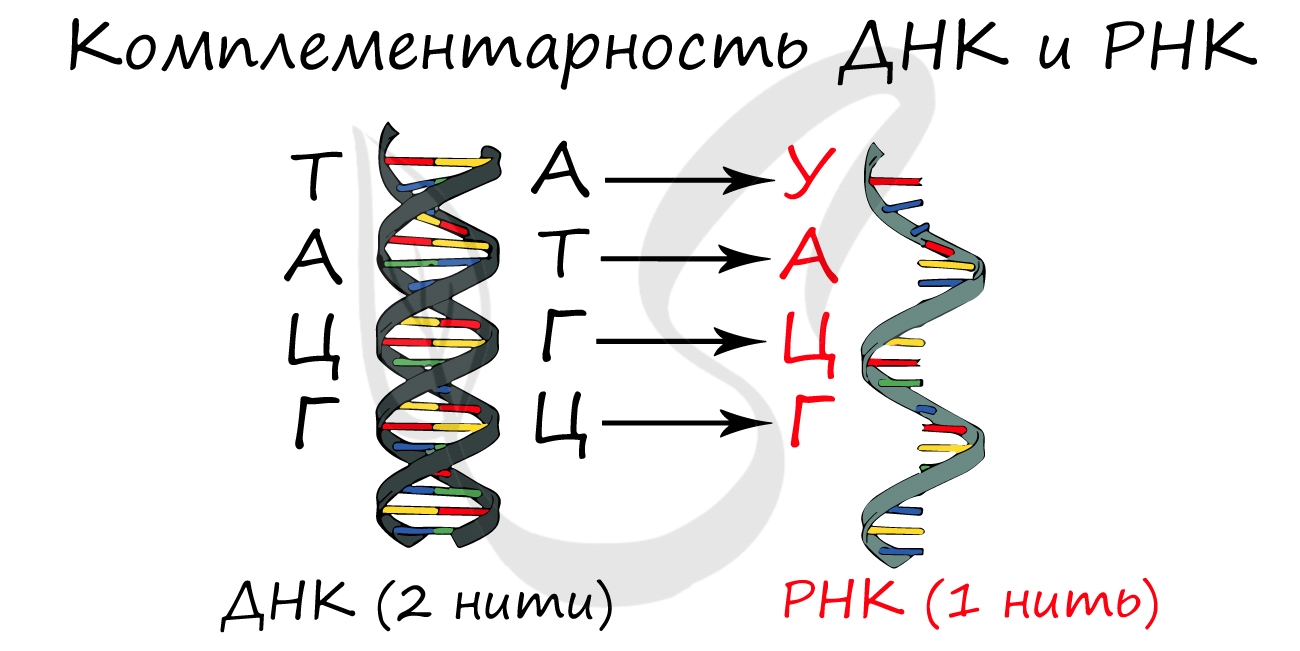
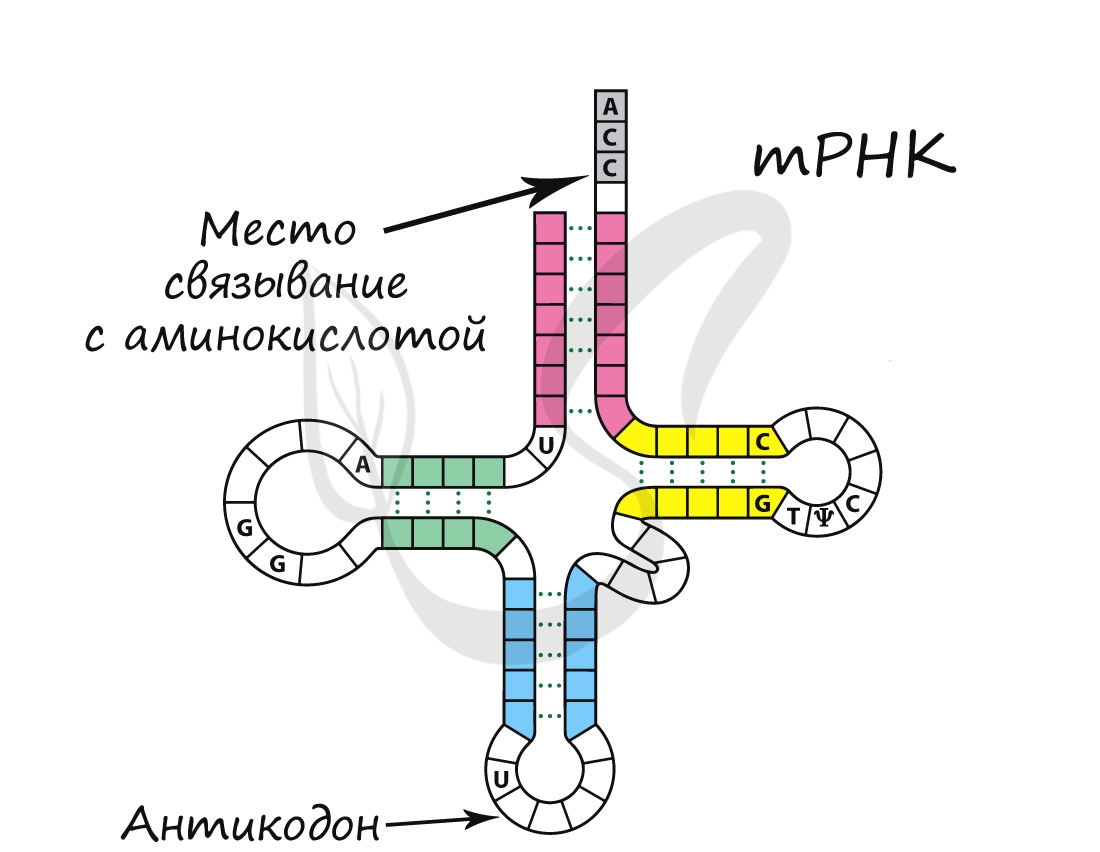
Обеспечивает транспорт аминокислоты к рибосоме во время синтеза белка. Благодаря этому становится возможным
соединение аминокислот друг с другом, образуется белок. тРНК имеет характерную форму клеверного листа.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Таблица “Функции белков”
4.7
Средняя оценка: 4.7
Всего получено оценок: 1242.
4.7
Средняя оценка: 4.7
Всего получено оценок: 1242.
Белки – сложные органические соединения, необходимые для нормального функционирования и построения организма. В зависимости от функций выделяют несколько видов белков. Значение белков в организме представлено в общей таблице «Функции белков».
Опыт работы учителем биологии — 23 лет.
Что такое белок?
Белки – полимеры, состоящие из аминокислот – многочисленных мономеров.
Каждая аминокислота включает:
- аминную группу (-NH2);
- карбоксильную группу (-СООН);
- радикал.
Различаются аминокислоты радикалами. Не все аминокислоты образуются внутри организма. Такие аминокислоты называются незаменимыми и должны поступать вовнутрь организма вместе с пищей.
Выделяют четыре уровня в организации белковой молекулы в зависимости от сложности:
- первичная структура – последовательность из аминокислот;
- вторичная структура – цепь, закрученная в спираль, или складчатый слой;
- третичная структура – плотно упакованные глобулы (глобулярные белки) и нитевидные структуры (фибриллярные белки);
- четвертичная структура – несколько глобул, образующих надмолекулярный комплекс.
Под действием температуры, облучения, химических веществ структура белка может нарушаться. Разрушение природной структуры белка называется денатурацией. Если воздействие фактора было непродолжительным и первичная структура сохранена,то белок может восстановить утраченную структуру, происходит ренатурация. Разрушение первичной структуры приводит к необратимой денатурации белка.
Роль белков
Большинство биологически активных веществ (гормоны, ферменты) являются белками. Основные биологические функции белков описаны в таблице.
| Функция | Описание | Примеры белков |
| Структурная | Являются «строительным материалом». Входят в состав клеточных мембран, органелл, хрящей, сухожилий, волос, кровеносных сосудов | Кератин, коллаген, эластин |
| Двигательная | Сокращают мышцы, обеспечивают движение жгутиков, хромосом при митозе, органов растений | Актин, миозин |
| Транспортная | Переносят молекулы веществ при дыхании и метаболизме, обеспечивают взаимосвязь каждой клетки с внешней средой | Гемоглобин, миоглобин, транскортин |
| Защитная | Обеспечивают свёртываемость крови, предохраняют организм от инфекций и чужеродных частиц, поддерживают иммунитет | Иммуноглобулины, тромбин, фибриноген |
| Рецепторная | Принимают, задерживают и передают сигналы из внешней среды в клетку | Опсин, фитохром, протеинкиназа |
| Регуляторная | Регулируют обмен веществ, контролируют рост, развитие, размножение | Глюкагон, тироксин, соматотропин |
| Ферментативная | Участвуют в биохимических реакциях, ускоряя их протекание | Трипсин, пепсин, амилаза, липаза, каталаза |
| Запасающая | Запасают в организме различные жизненно важные элементы – железо, кислород и т.д. | Альбумин, глютен, ферритин |
| Энергетическая | При длительном голодании могут использоваться в качестве энергии. Расщепление грамма белка даёт 17,6 кДж энергии | Любой белок организма |
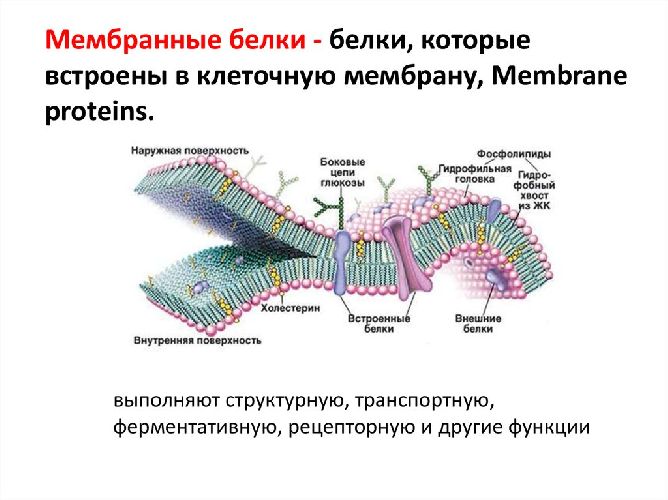
Белки, в зависимости от выполняемой функции, могут быть встроенными, поверхностными, свободными. Например, глобулярные белки, интегрированные в клеточную мембрану, выполняют транспортную или рецепторную функцию.
Что мы узнали?
Из урока биологии 10 класса кратко узнали о строении и основных функциях белка. Белки состоят из аминокислот. В зависимости от назначения выделяют рецепторные, структурные, регуляторные, ферментативные, двигательные и другие белки.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Алексей Беляев
5/5
-
Михаил Захаров
5/5
-
Пётр Гришаев
5/5
-
Женя Игушкин
4/5
ТОП-1 статья
которые читают вместе с этой
Оценка доклада
4.7
Средняя оценка: 4.7
Всего получено оценок: 1242.
А какая ваша оценка?
| Функция | Характеристика |
|---|---|
| Строительная | Одна из важнейших функций белковых молекул. Белки входят в состав всех клеточных мембран и органоидов клетки. Преимущественно из белка состоят стенки кровеносных сосудов, хрящи, сухожилия, волосы и ногти |
| Защитная | Специфические белки выполняют эту функцию. Они предохраняют организм от вторжения чужеродных белков и микроорганизмов, а также от повреждений. Антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки, фибрин и тромбин предохраняют организм от кровопотери |
| Двигательная | Выполняют особые сократительные белки. Благодаря им двигаются реснички и жгутики у простейших, перемещаются хромосомы при делении клетки, сокращаются мышцы у многоклеточных, совершенствуются другие виды движения у живых организмов |
| Регуляторная | Присуща белкам-гормонам. Они поддерживают постоянные концентрации веществ в крови и клетках, участвующих в росте, размножении и других важных процессах. Например, инсулин регулирует содержание сахара в крови |
| Транспортная | Гемоглобин переносит кислород из лёгких к клеткам других тканей и органов. В мышцах эту функцию выполняет белок миоглобин. Белки сыворотки крови способствуют переносу липидов и жирных кислот, различных биологически активных веществ. Белки в наружной мембране клетки переносят различные вещества из окружающей среды в цитоплазму |
| Ферментативная | Белки-ферменты способны ускорять биохимические реакции в клетке в десятки и сотни миллионов раз |
| Энергетическая | Являются одним из источников энергии в клетке. При полном расщеплении 1 г белка до конечного продукта выделяется 17,6 кДж энергии. Аминокислоты, высвобождаемые при расщеплении белковых молекул, используются при построении новых белков |
Скачать решение
Таблицa на схожие темы
-
Белки и нуклеиновые кислоты
-
Роль белков, жиров, углеводов, минеральных солей и воды
-
Строение и функции отделов уха
-
Функции желёз внутренней секреции
-
Функции липидов
-
Функции углеводов
© 2021 Copyright. Все права защищены. Правообладатель SIA Ksenokss.
Адрес: 1069, Курземес проспект 106/45, Рига, Латвия.
Тел.: +371 29-851-888 E-mail: [email protected]