Проанализируйте таблицу «Классификация липидов». Заполните пустые ячейки таблицы, используя термины и понятия, приведённые в списке. Для каждой ячейки, обозначенной буквой, выберите соответствующий термин из предложенного списка.
| Группа липидов | Особенности строения | Функция в организме
человека |
|---|---|---|
| триглицериды | ____________(Б) | запасание энергии |
| фосфолипиды | эфир глицерина,
жирных кислот и остатка фосфорной кислоты |
____________(В) |
| ____________(А) | спирт на основе
стероидного ядра |
компонент клеточных
мембран и основа для синтеза стероидных гормонов |
Список терминов и понятий:
1) жирные кислоты
2) полисахариды
3) холестерин
4) выделение энергии при окислении
5) компонент клеточных мембран
6) смазывающее вещество в суставах
7) эфир глицерина и жирных кислот
8) соединение аденина, рибозы и трёх остатков фосфорной кислоты
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Статья на конкурс «Био/Мол/Текст»: Задумывались ли вы когда-нибудь о том, что клетки общаются между собой? Ведь клеточный мир настолько многообразен и велик, что в нем без языка не обойтись! Всем известные гормоны — только один из диалектов такого «языка»! В этой статье мы расскажем о том, как липиды помогают клеткам «общаться». Почему такой, казалось бы, простой химический процесс, как окисление липидов, может приводить к гибели клетки? Как клетки понимают, когда пора заканчивать фазу воспаления и переходить к восстановлению? Что такое ферроптоз?.. Вы все еще читаете аннотацию? Давайте скорее окунемся в удивительный мир редокс-липидомики и взглянем на липиды по-новому!
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Давно известно, что без липидов человеческий организм не может существовать. Эта обширная группа природных органических соединений, включающая жиры и жироподобные вещества, необходима для построения клеточных мембран и регуляции обмена веществ. Изучением липидов занимается липидомика, а появление раздела «редокс-липидомика» (окислительно-восстановительная липидомика, часть липидомики, занимающаяся характеристикой окисленных липидов) позволило по-новому взглянуть на роль продуктов окисления липидов и оценить их влияние на ключевые процессы, происходящие в клетках.
О липидах в составе клеточных мембран читайте в статье «Липидный фундамент жизни» [1]. — Ред.
В дополнение к природному липидому (совокупности всех липидов организма), существуют виды липидов, полученные в результате ферментативных и неферментативных модификаций (эпилипидом), что делает общую картину еще более сложной, поскольку их функции все еще в значительной степени неизвестны. Окисленные липиды представляют собой фракцию эпилипидома, которая привлекла большое внимание ученых из-за их роли в возникновении и развитии многих заболеваний человека. Однако основной проблемой редокс-липидомики остается отсутствие оптимальных вычислительных инструментов для надежной, точной и специфической идентификации уже открытых и еще неизвестных модифицированных липидов. В настоящее время жидкостная хроматография и масс-спектрометрия являются основными методами, позволяющими определить количество липидов в клетке, оценить их участие в ряде физиологических механизмов и даже изучить структуру продуктов окисления этих веществ [2].
Знакомство с липидами
Молекулы липидов чрезвычайно разнообразны, их насчитывают более миллиона вариантов [3]! Впечатляющее количество, по сравнению с 70 000 выявленных белков и 30 000 генов! Для удобства химики разделили все липиды на две большие группы:
- омыляемые, которые легко гидролизуются в воде под действием щелочей;
- неомыляемые, которые не гидролизуются в щелочной среде.
К первой группе относятся простые липиды, состоящие исключительно из спирта и жирных кислот (воски, триацилглицеролы, эфиры холестерола), и сложные липиды, в состав которых входят и другие компоненты (фосфолипиды, гликолипиды, сфинголипиды). К неомыляемым липидам относится большая группа стероидов, включающая холестерин и его производные: стероидные гормоны, витамины, желчные кислоты.
Большая роль маленьких молекул
Липиды, содержащие полиненасыщенные жирные кислоты (ПНЖК — кислоты, содержащие две и более двойных связей), являются важными сигнальными молекулами, регулирующими многие метаболические процессы и клеточные реакции, включая воспаление. Для выполнения этих функций они подвергаются реакциям окисления, то есть присоединяют кислородсодержащие группы.
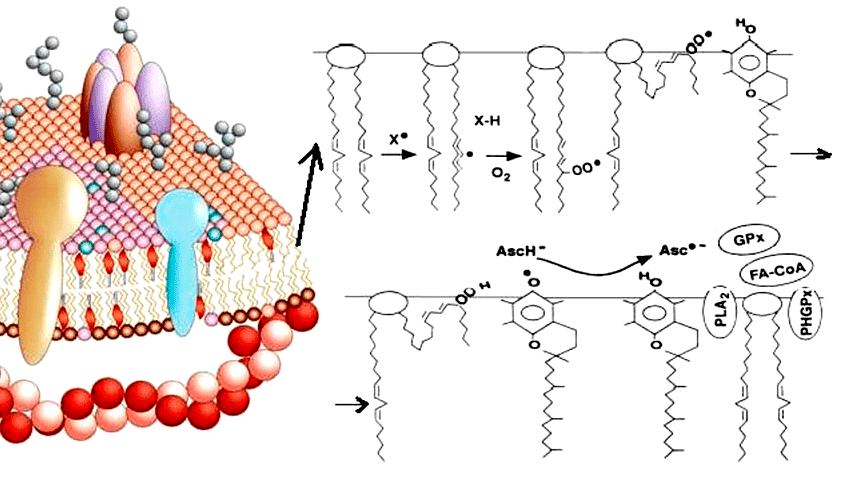
Окисление липидов происходит с помощью двух основных механизмов. Первый способ — неферментативное перекисное окисление. При этом липиды взаимодействуют с активными формами кислорода (АФК), в результате чего происходит накопление гидроперекисей липидов (LOOH) (рис. 1). В норме процессы перекисного окисления необходимы для поддержания структуры клеточных мембран, функционирования ионных каналов, рецепторов и ферментных систем. Их роль велика и в синтезе липидных медиаторов — биорегуляторов (простагландинов, тромбоксанов, лейкотриенов и др.). Однако неконтролируемое свободнорадикальное окисление липидов может приводить к изменению проницаемости мембраны, нарушению ее целостности, а это прямая угроза гибели клетки [3]!
Рисунок 1. Зарождение цепной реакции перекисного окисления липидов. Фосфолипиды клеточных мембран, взаимодействуя со свободными радикалами, превращаются в гидроперекиси липидов, что может влиять на функции мембраны клетки.
Второй путь окисления — ферментативные изменения, отличающиеся высокой селективностью и специфичностью. Ферментативное окисление происходит под действием металлопротеинов: липоксигеназы, циклооксигеназы, цитохрома Р450, пероксидазы. Продукты реакций окисления ПНЖК, выступая в качестве сигнальных молекул, координируют метаболизм и другие физиологические процессы, иными словами, управляют судьбой клетки [4]! Такие вещества носят название эйкозаноидов. Они принимают участие во многих важнейших процессах: росте мышечной ткани, реакциях иммунитета на токсины и патогены, выступают в роли нейромедиаторов и даже гормонов!
К сожалению, человеческий организм не научился синтезировать все необходимые ПНЖК. Возникает вопрос: можно ли их получить извне? Разумеется! Пищевыми источниками полиненасыщенных жирных кислот являются растительные масла, рыбий жир и препараты омега-3-жирных кислот. Таким образом, казалось бы невкусный рыбий жир — просто лакомство для наших клеток!
Из липидов — в дирижеры клеточных реакций
Исследования редокс-липидомики, проведенные при помощи масс-спектрометрии в сочетании с обращенно-фазовой хроматографией, выявили удивительный факт: липиды контролируют активность иммунной системы [4]! При попадании в организм чужеродных агентов, желающих нанести вред и повредить ткани, развивается воспаление, цель которого — устранить патоген. Иммунные клетки, встав на защиту организма, в зоне повреждения вырабатывают «провоспалительные» производные ПНЖК (лейкотриены, липоксины, гипоксины и т.д.), которые усиливают воспаление и таким образом избавляют организм от патогена (рис. 2).
Рисунок 2. Провоспалительные производные арахидоновой кислоты: простагландины, тромбоксаны и лейкотриены
рисунок авторов статьи
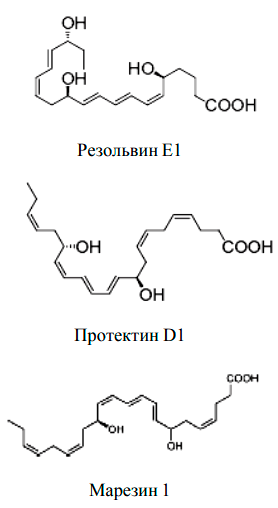
Рисунок 3. Противовоспалительные медиаторы: резолвины, протектины, марезины
Но воспаление — патологический процесс, и при удалении повреждающего фактора важно вовремя остановиться и прекратить воспалительный ответ. Здесь на помощь приходят противовоспалительные липидные медиаторы — резолвины, протектины, марезины (рис.3). Они останавливают образование «провоспалительных» медиаторов и обеспечивают защиту клеток от повреждающих факторов.
Кроме того, собственные поврежденные клетки, не способные восстановиться, для перехода воспаления в завершающую фазу и сохранения постоянства внутренней среды должны подвергнуться уничтожению, чему также способствуют липидные медиаторы. Как это возможно? Оказалось, что липидные молекулы фосфатидилсерина (фосфолипида клеточной мембраны) выставляются на мембрану поврежденных клеток и «помечают» их. Фосфатидилсерин на поверхности клеток является сигналом для их поглощения макрофагами и клетками микроглии [5]. В исследованиях также была продемонстрирована значимость этого медиатора: наличие даже одной молекулы фосфатидилсерина уже достаточно для активации фагоцитоза!
Две стороны одной медали
Оказалось, что роль липидов велика не только в уничтожении старых или поврежденных клеток, но и их компонентов, или органелл. Например, для удаления митохондрий, безвозвратно утративших свои функции, на поверхности ее внешней мембраны появляется кардиолипин — фосфолипид, который в норме присутствует только на внутренней мембране органелл. Именно он и служит сигналом митофагии, или уничтожения митохондрий [5]. Удаление исключительно ненужных организму структур без повреждения нормальных клеток требует точной передачи сигналов и имеет решающее значение для поддержания постоянства внутренней среды.
Однако данный процесс может стать опасным для организма. Чрезмерная митофагия описана при многих острых и хронических заболеваниях центральной нервной системы. Так, при болезни Паркинсона она может привести к гибели нейронов [6]. Контроль качества митохондрий с целью избежания излишнего уничтожения имеет центральное значение для функционирования и благополучия нейронов. Это открывает новые возможности для исследований в области лечения нейродегенеративных заболеваний!
Как липиды «помогают» клетке погибнуть?
Что же делать со старыми клетками, честно отслужившими свой срок? Безусловно, оставлять их на своем месте нельзя, иначе новым здоровым клеткам будет некуда деться. Остается один вариант — аккуратно разобрать и удалить из организма те из них, которые не способны более функционировать. Данный процесс носит названия апоптоза. Валериан Каган и его соавторы доказали, что для осуществления этого процесса необходимо окислить ПНЖК кардиолипина [7]. При необратимых изменениях в клетке знакомый нам кардиолипин образует комплекс с белком дыхательной цепи — цитохромом c — и превращает его в фермент пероксидазу. Пероксидаза тотчас окисляет ПНЖК кардиолипина, и он перемещается на внешнюю мембрану митохондрий, увеличивая ее проницаемость (рис.4). Это приводит к высвобождению других проапоптотических факторов клетки, действие которых приводит к клеточной гибели.
Рисунок 4. Окисление кардиолипина как фактор апоптоза. На рисунке представлена клеточная мембрана, состоящая из бислоя липидов, один из которых — кардиолипин (показан желтым цветом). При взаимодействии с белком цитохромом c (cyt c) кардиолипин превращает его в пероксидазу, которая, в свою очередь, окисляет ПНЖК кардиолипина (на рисунке — cardiolipin hydroperoxide, CL-OOH). Гидроперекись кардиолипина выходит на внешнюю мембрану митохондрии, изменяя ее проницаемость, что приводит к апоптозу.
Новый взгляд на клеточную смерть
Одним из важнейших достижений редокс-липидомики является открытие уникального варианта неапоптотической программируемой гибели клетки — ферроптоза [8]. По сравнению с другими формами этот путь клеточной гибели неповторим. В чем же его особенность? Оказалось, что, в отличие от апоптоза, при котором происходит аккуратная разборка клетки, ферроптоз приводит к клеточному коллапсу, в котором железо и АФК принимают активное участие. Давайте разберемся, как это происходит!
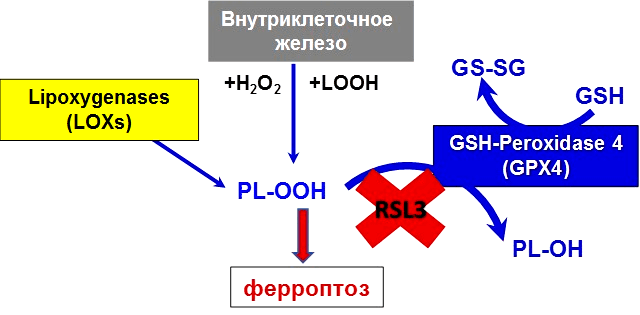
Ферроптоз назван так неспроста. Железо (Fe от лат. ferrum) — основной элемент, необходимый для осуществления ключевого звена данного пути гибели клетки: перекисного окисления липидов (рис. 5) [9], [10]. Перекисное окисление может происходить под действием свободного двухвалентного железа (через реакцию Фентона), а также посредством фермента липоксигеназы, содержащей железо.
Рисунок 5. Ионы железа в организме находятся под строгим метаболическим контролем. Нарушение баланса ионов железа в клетке и возникновение окислительного стресса приводит к цепной реакции окисления липидов и формированию избытка гидроперекисей. Накопление гидроперекисей липидов приводит к развитию ферроптоза. Гидроперекиси фосфолипидов (PL-OOH) образуются внутри клетки с участием различных форм низкомолекулярного внутриклеточного железа и железосодержащих ферментов. Активная GPX4 восстанавливает гидроперекиси липидов до спиртов. В случае ингибирования фермента, например, специфическим ингибитором RSL3, PL-OOH накапливаются в клетках, усиливая развитие окислительного стресса.
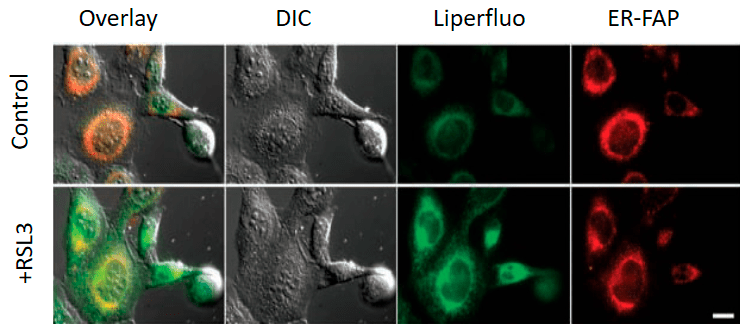
Конкретные механизмы редокс-модификации липидов, задействованные в выполнении программы ферроптоза, на сегодняшний день остаются тайной. Но, окрасив клетку различными флуоресцентными красителями, можно увидеть, насколько удивительные очертания они приобретают при ферроптозе (рис. 6) [11]!
Рисунок 6. Снимок конфокальной микроскопии эмбриональных фибробластов мыши, обработанных индуктором ферроптоза RSL3 (100 nM, 6h). Control — необработанные клетки. Liperfluo — флуоресцентный зонд, который после взаимодействия с гидроперекисями липидов способен флуоресцировать, если он встроен в плазматическую мембрану клеток. ER-FAP (ER-targeted fluorogen-activating protein) — флуоресцентный белок, чья флуоресценция активируется при связывании метки с эндоплазматическим ретикулумом.
В клетках организма существуют механизмы, препятствующие неконтролируемому перекисному окислению. Одним из ключевых ферментов здесь является глутатионпероксидаза 4 (GPX4), которая восстанавливает гидроперекиси липидов до спиртов за счет окисления глутатиона (GSH). Далее окисленная молекула глутатиона (GS-SG) восстанавливается с помощью фермента глутатион-редуктазы. В случае инактивации клеточного глутатиона и GSH-зависимой антиоксидантной защиты происходит накопление токсичных липидных АФК и запуск ферроптоза [12].
Две крайности одной и той же сущности. Как ферроптоз реализуется в целом организме и можно ли обернуть его в свою пользу?
Проведенные исследования показывают, что ферроптоз осуществляется во многих типах тканей человека. Так, при отравлении парацетамолом в организме накапливается N-ацетил-p-бензохинонимин, при этом наблюдается истощение глутатиона, в результате чего происходит массивная гибель клетки по механизму ферроптоза [13].
Имеющиеся данные указывают на то, что ферроптоз может выступать одним из ключевых механизмов развития некоторых нейродегенеративных заболеваний, а также является одной из возможных причин гибели клеток в условиях глутаматной эксайтотоксичности [14].
Ионы железа могут играть ключевую роль в гибели эпителиальных клеток почечных канальцев в условиях острой почечной недостаточности [13]. Данный механизм обусловлен нарушением гломерулярной фильтрации и накоплением ионов железа как внутриклеточно, так и в полости канальца, что приводит к реализации клеточной смерти.
Ферроптоз, как механизм регулируемой клеточной смерти, имеет и терапевтическую ценность. Существует ряд потенциальных молекул, ингибирующих Xc– — транспортную систему (эрастин, RSL3), которые, воздействуя на культуру опухолевых клеток, вызывают их гибель по механизму ферроптоза [12], [13]. Как доказать, что это происходит благодаря ферроптозу, а не случайному совпадению? При добавлении к клеткам веществ, связывающих железо, оно становится «неподвижным» и не может участвовать в химических процессах. В этом случае процессы ферроптоза значительно замедляются. Однако не все так просто и радужно! Эти молекулы не обладают высокой специфичностью, и при более высоких дозах клеточная гибель может происходить по механизму апоптоза!
Вывод
Благодаря редокс-липидомике стало известно, что кислородсодержащие липиды играют огромную роль в сохранении постоянства внутренней среды, запуская апоптоз, ферроптоз и контролируя воспаление. Однако стоит принять во внимание, что, несмотря на очевидное значение в регуляции множества биологических функций, содержание окисленных липидов в организме крайне мало (0,03–3,0 моль% от всего липидома организма) [4]. Кроме того, трудности анализа окисленных липидов заключаются в их химической нестабильности, термолабильности и неоднородности окисленных продуктов. Не зря их сравнивают с иголкой в стоге сена!
- Липидный фундамент жизни;
- Zhixu Ni, Laura Goracci, Gabriele Cruciani, Maria Fedorova. (2019). Computational solutions in redox lipidomics – Current strategies and future perspectives. Free Radical Biology and Medicine. 144, 110-123;
- Yulia Y. Tyurina, Claudette M. St. Croix, Simon C. Watkins, Alan M. Watson, Michael W. Epperly, et. al.. (2019). Redox (phospho)lipidomics of signaling in inflammation and programmed cell death. J Leukoc Biol;
- Yulia Y. Tyurina, Vladimir A. Tyurin, Tamil Anthonymuthu, Andrew A. Amoscato, Louis J. Sparvero, et. al.. (2019). “Redox lipidomics technology: Looking for a needle in a haystack”. Chemistry and Physics of Lipids. 221, 93-107;
- V.E. Kagan, Y.Y. Tyurina, W.Y. Sun, I.I. Vlasova, H. Dar, et. al.. (2020). Redox phospholipidomics of enzymatically generated oxygenated phospholipids as specific signals of programmed cell death. Free Radical Biology and Medicine. 147, 231-241;
- Charleen T Chu, Hülya Bayır, Valerian E Kagan. (2014). LC3 binds externalized cardiolipin on injured mitochondria to signal mitophagy in neurons. Autophagy. 10, 376-378;
- Valerian E. Kagan, Hülya Bayır, Yulia Y. Tyurina, Sergey B. Bolevich, John J. Maguire, et. al.. (2017). Elimination of the unnecessary: Intra- and extracellular signaling by anionic phospholipids. Biochemical and Biophysical Research Communications. 482, 482-490;
- Scott J. Dixon, Kathryn M. Lemberg, Michael R. Lamprecht, Rachid Skouta, Eleina M. Zaitsev, et. al.. (2012). Ferroptosis: An Iron-Dependent Form of Nonapoptotic Cell Death. Cell. 149, 1060-1072;
- Wan Seok Yang, Brent R. Stockwell. (2016). Ferroptosis: Death by Lipid Peroxidation. Trends in Cell Biology. 26, 165-176;
- Власова И.И., Владимиров Г.К., Каган В.Е. Глава 3. Процессы гибели клеток // Введение в регенеративную медицину: лабораторный курс: учебное пособие / П.С. Тимашев, А.И. Шпичка. Издательство Сеченовского университета, 2020. 348 с.;
- Valerian E Kagan, Gaowei Mao, Feng Qu, Jose Pedro Friedmann Angeli, Sebastian Doll, et. al.. (2017). Oxidized arachidonic and adrenic PEs navigate cells to ferroptosis. Nat Chem Biol. 13, 81-90;
- Jennifer Yinuo Cao, Scott J. Dixon. (2016). Mechanisms of ferroptosis. Cell. Mol. Life Sci.. 73, 2195-2209;
- Marcus Conrad, Valerian E. Kagan, Hülya Bayir, Gabriela C. Pagnussat, Brian Head, et. al.. (2018). Regulation of lipid peroxidation and ferroptosis in diverse species. Genes Dev.. 32, 602-619;
- Leslie Magtanong, Scott J. Dixon. (2018). Ferroptosis and Brain Injury. Dev Neurosci. 40, 382-395;
- Куликов В.А. и Гребенников И.Н. (2012). Резольвины, протектины и марезины: новые медиаторы воспаления. «Вестник Витебского государственного медицинского университета». 1, 25–30.
Жиры или липиды плохо растворимы в воде, но растворимы в органических растворителях. Термин «жир» чаще всего используется для обозначения пищи и липидного обмена. Около 90% жиров в пище — триглицериды. Другие типы жиров включают холестерин, фосфолипиды, стерины и каротиноиды
Жиры содержат три типа жирных кислот: насыщенные, мононенасыщенные и полиненасыщенные. Именно их соотношение определяет диетическую ценность.
Что такое липиды
Липиды — это различные классы соединений, таких как стероиды, жиры, сфинголипиды и т.п. Липиды включены в биологические мембраны и, следовательно, от них зависит проводимость мембраны, передача нервных импульсов и образование межклеточных связей.
Они образуют основные запасы энергии клеток. Также липиды — источник эндогенной воды. Они делятся на гидролизуемые и негидролизуемые. К последним относятся терпены и стероиды.
Классификация гидролизуемых липидов намного сложнее. Они делятся на:
- обычные, включающие триглицериды (сложные эфиры глицерина и жирных кислот);
- воски — сложные эфиры длинноцепочечных жирных кислот и длинноцепочечных одноатомных спиртов.
К сложным липидам относятся соединения, которые помимо жирных кислот и спирта содержат молекулы других веществ.
Функции жира в организме
Липиды являются концентрированными источниками энергии. В сутки при нормальном питании потребляется около 100 г липидов. Основные пищевые липиды — триглицериды. С пищей организму необходимо получать липиды животного и растительного происхождения — полиненасыщенные жирные кислоты.
Жир это:
- источник энергии – 1 грамм жира выделяет 9 ккал;
- источник незаменимых жирных кислот;
- переносчик жирорастворимых витаминов A, D, E и K;
- улучшитель вкуса и внешнего вида пищи.
Некоторые типы жиров важны для производства стероидных гормонов, интерлейкинов, тромбоксанов и простагландинов.
Холестерин необходим для производства желчных кислот, которые переваривают жиры.
Триглицериды
Триглецириды — это нейтральные жиры — сложные эфиры глицерина и жирных кислот. Это резервные жиры, которые являются основным источником эндогенной энергии. В жировой ткани триглицериды составляют 60-85% ее массы.
Триглицерид — это сложный эфир, состоящий из глицерина, связанного с тремя жирными кислотами, которые могут быть насыщенными или ненасыщенными. В организме человека преобладают насыщенные пальмитиновая и олеиновая (омега-9) кислоты.
Триглицериды попадают с пищей или синтезируются в самом организме (печень, жировая ткань, слизистая тонкого кишечника, мышцы). Триглицериды, поступающие с пищей, гидролизуются в желудочно-кишечном тракте ферментом липазой. Скорость синтеза зависит от количества жирных кислот, полученных с пищей.
Триглицериды попадают в кровь в виде хиломикронов (липопротеин, несущий триглицериды). Произведенные жирные кислоты потребляются в тканях или повторно синтезируются из них, а триглицериды сохраняются.
Фосфолипиды
Состоят из двух групп соединений. Это глицерофосфолипиды (спирт-глицерин) и сфингомиелины (спиртовой сфингозин). Фосфолипиды имеют повышенную гидрофильную часть по сравнению с триглицеридами, состоящую из фосфатной группы и определенного аминоспирта, такого как холин. Из-за этой повышенной гидрофильной части фосфолипиды характеризуются полярностью и поэтому также называются полярными липидами.
Фосфолипиды являются основными липидами мембран. Их очень много в нервных клетках. Фосфолипиды образуют миелиновую оболочку нервных волокон и активно участвуют в энергетическом обмене.
Жирные кислоты
- Насыщенные жирные кислоты. Они имеют высокую температуру плавления и поэтому сохраняют твердую консистенцию при комнатной температуре. Насыщенные жирные кислоты получают из животных источников. В растительных маслах (жирах) преобладают ненасыщенные жирные кислоты, за исключением кокосового и пальмового масел. Некоторые промышленные маргарины и спреды содержат много насыщенных жирных кислот.
- Мононенасыщенные жирные кислоты. Эти жирные кислоты находятся в жидкой форме при комнатной температуре. Оливковое и рапсовое масла — лучший источник мононенасыщенных жирных кислот.
- Полиненасыщенные жирные кислоты (PNRR). PNRR находятся в жидкой форме при комнатной температуре. Они легко окисляются в пище и в организме. PNRR участвуют в процессе метаболизма холестерина и входят в состав фосфолипидов клеточных мембран. Кроме того, они являются предшественниками таких активных биологических веществ, как простагландины, интерлейкины, тромбоксаны, играющих решающую роль в формировании иммунного ответа, регулировании свертывания крови и уменьшении воспаления.
Полиненасыщенные RR делятся на:
- Омега-3 (альфа-линоленовые) – содержатся в льняном, тыквенном, грецком, рапсовом и соевом маслах и зеленых листовых овощах;
- Эйкозапантан, докозагексаен — содержатся в масле морских рыб, масле морских водорослей.
Линоленовые жиры, арахидон — их производные. Они присутствуют в молочном жире, особенно летом, потому что в организме животных они состоят из линолевой кислоты, полученной с кормом.
Более длинные цепи RR: арахидон (AA), докозагексаеновая кислота (DHR), эйкозапентаеновая кислота (EPR) не считаются незаменимыми, но при отсутствии RR омега-3 и омега-6 в пище их выработка в организме может достигать критических уровней. Прямое поступление АК, ЭПК и ДГК с пищей позволяет избежать метаболизма линолевой и альфа линоленовой кислоты.
DHR и EPR очень важны для неврологического развития плода и ребенка. Дефицит DHR связан с болезнью Альцгеймера, синдромом дефицита внимания, фенилкетонурией, муковисцидозом и другими заболеваниями. Растительный α-линоленовый RR омега-3 может быть преобразован ферментами в физиологически важные EPR и DHR или соединения класса гормоноподобных эйкозаноидов.
Жирные кислоты омега-3 активно участвуют в клеточном метаболизме, в регуляции холестерина в организме человека: они снижают количество холестерина липопротеидов низкой плотности (так называемый плохой холестерин) в организме, а также вероятность сердечных заболеваний. Они также очень важны для функционирования клеток мозга, нейронных синапсов, сетчатки глаза, а также для выработки половых гормонов.
Оптимальное соотношение жирных кислот омега-6 к омега-3 составляет 5:1. В современном рационе это соотношение превышает 15 раз и более. Неправильное соотношение Омега-3 и Омега-6 опасно для здоровья.
Трансизомерные кислоты
Трансизомерные кислоты в небольших количествах содержатся в натуральных жирах, в желудках коров и овец, баранине, говядине, молоке и сыре. Важнейшим источником транс-изомерных кислот являются гидрогенизированные спреды PNRR, маргарины.
В процессе нагревания растительного масла ненасыщенные кислоты становятся насыщенными, а жидкие жиры становятся твердыми. Гидратированные диетические жиры имеют ряд преимуществ. Они дешевле, портятся медленнее, чем животные жиры, более устойчивы к окислению и высоким температурам.
Транс-изомерные кислоты, образующиеся во время гидрогенизации, связаны с увеличением холестерина ЛПНП и снижением холестерина ЛПВП, что увеличивает риск сердечно-сосудистых заболеваний, ожирения, диабета, а высокие уровни которых могут быть канцерогенными.
Стерины
Производные стероидов — это стероидные спирты, состоящие из четырех конденсированных колец атомов углерода, которые отличаются друг от друга функциональными группами (например, тестостерон, холестерин). Содержится в растениях, мясе и вырабатывается в организме.
В организме человека могут содержаться свободные стерины или сложные эфиры (стериды), образованные с жирными кислотами. Существует множество стеринов и стероидов, включая желчные кислоты, половые гормоны и гормоны коры надпочечников, витамины группы D, сердечные гликозиды, растительные фитостерины и некоторые алкалоиды.
В растениях есть стерины (эргостерин, стигмастерин и т. д.), но эти стерины не очень хорошо усваиваются организмом и, как считается, блокируют всасывание холестерина.
Самый распространенный стерол — это воскоподобный холестерин, который содержится только в продуктах животного происхождения. Фитостерины содержатся в растительной пище.
Холестерин является предшественником желчных кислот, стероидных гормонов и витамина D и представляет собой пергидрофенантреновое производное циклопентана. Это циклический ненасыщенный одноатомный спирт, имеющий полярную гидроксигруппу. Из холестерина в организме синтезируются другие стероиды: гормоны надпочечников, кортикостероиды, половые гормоны, желчные кислоты. Он синтезируется во многих клетках организма, но наиболее интенсивно в эндоплазматическом ретикулуме и цитоплазме эпителиальных клеток печени и кишечника. Холестерин синтезируется из ацетил-КоА. Выводится из организма с желчью или в виде солей желчных кислот.
Пищевой холестерин слабо влияет на уровень холестерина в плазме крови, поскольку большая его часть имеет эндогенное происхождение. Однако уменьшение количества насыщенных жиров в пище также резко снижает уровень холестерина в крови.
Животные и растительные жиры в диете
Животные жиры содержат много насыщенных жирных кислот. Они повышают уровень холестерина в крови и, следовательно, способствуют развитию атеросклероза, сердечно-сосудистых заболеваний и рака. Чрезмерное потребление насыщенных жирных кислот может привести к раку легких, кишечника, прямой кишки, груди и простаты.
Единственное исключение составляет один вид животного жира — жир морской рыбы, такой как скумбрия, сельдь, лосось, треска. Рекомендуется есть их как можно чаще из-за наличия полиненасыщенных жирных кислот омега-3.
Пищевая ценность масла определяется соотношением содержащихся в нем жирных кислот и количества жирорастворимых витаминов. В растительных маслах ненасыщенные жирные кислоты, то есть олеиновая, линолевая и α-линоленовая кислоты, составляют значительную часть всех жирных кислот. Особенно важны группы PNRR омега-6 и омега-3.
- Считается, что дефицит производных омега-6 RR может быть одним из факторов риска, связанных с развитием рака.
- Омега-3 PNRR снижает агрегацию тромбоцитов, а также риск образования тромбов, влияет на электрическую активность сердечной мышцы, тормозит возникновение аритмий. Они снижают уровень триглицеридов в крови, а также частоту ишемической болезни сердца.
Соотношение RR омега-6 и омега-3 в пищевых продуктах, рекомендованных Всемирной организацией здравоохранения (ВОЗ), должно составлять от 1:1 до 5:1. В последние десятилетия стала очевидной искаженная тенденция в этой рекомендации: растет потребление масел с высоким содержанием омега-6 и слишком низким содержанием омега-3 RR. Например, подсолнечное масло.
Соотношение этих кислот в различных продуктах питания колеблется от 10:1 до 20:1. Превышение омега-6 снижает уровень холестерина ЛПВП и увеличивает холестерин ЛПНП. Арахидон, производимый из кислот омега-6 и его метаболиты вызывают сужение сосудов и агрегацию тромбоцитов.
Более насыщенных транс-изомерных кислот, образующихся при гидрогенизации растительных масел, то есть при их затвердевании, увеличивают риск дислипидемии, CD типа II, а также попадания канцерогенов в клетки.
Качество растительного масла определяется его химическим составом, способом экстракции, технологией рафинирования и сохраняемыми при нем естественными физиологически активными веществами. Рекомендуется употреблять не менее 2-3 столовых ложек ненагретого масла в день с различными блюдами или салатами.