Установите соответствие между исходными веществами и продуктами, которые преимущественно образуются в ходе реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Спрятать решение
Решение.
Установим соответствие.
A) — вытеснение растворимой кислотой нерастворимой кислоты, образуется кремниевая кислота и гидрокарбонат калия, вариант: 5.
Б) — вытеснение более сильной кислотой более слабой, получится кремниевая кислота и хлорид калия, вариант: 4.
B) — формально при реакции обмена должен был бы получиться карбонат алюминия, однако данная соль является солью слабого основания и слабой кислоты что усиливает её гидролиз, при этом при её гидролизе получается осадок (гидроксид алюминия) и газ (углекислый), что также усиливает гидролиз, поэтому он становится необратимым. Вариант: 2.
Г) — в зависимости от количества щелочи получится либо гидроксид алюминия и хлорид калия, либо (поскольку алюминий амфотерен) тетрагидроксоалюминат калия. Последнего варианта нет, поэтому выбираем гидроксид алюминия и хлорид калия, вариант: 1.
Ответ: 5421.
Постила
- Внешность
- Дети
- Еда и напитки
- Знаменитости
- Маникюр
- Причёски
- Разное
- Сад и огород
- Спорт и фитнес
- Вязание
- Диеты и похудение
- Животные
- Компьютеры и телефоны
- Музыка
- Психология
- Ремонт
- Саморазвитие
- Фотография и искусство
- Кусочек Постилы
- Гороскопы и эзотерика
- Дом и уют
- Здоровье
- Литература
- Покупки
- Путешествия
- Рукоделие
- Свадьба
- Цветы
- Блог Постилы
Русский
English (US)
Espanol
-
Вход / Регистрация
- Кнопка Пост!
- Правила
Главная
/
Саморазвитие
-
- Встроить
- Пожаловаться
sun7-14.userapi.com
3 недели 5 дней назад
rKakZnvo97Y.jpg (762×1080)
Сохранено в ЕГЭ.ХИМИЯ.
Саморазвитие
ольга майорова
2277 подписчиков
Нет комментариев
Подборка тренировочных вариантов ЕГЭ 2022 по химии с ответами.
Тренировочные варианты ЕГЭ 2022 по химии
| vk.com/repetitor_po_himii_i_biologii | |
| Вариант 1 | Ответы |
| vk.com/chem4you | |
| скачать вариант 1 | ответы |
| скачать вариант 2 | ответы |
| скачать вариант 3 | ответы |
| скачать вариант 4 | ответы |
| скачать вариант 5 | ответы |
| скачать вариант 6 | ответы |
| скачать вариант 7 | ответы |
| скачать вариант 8 | ответы |
| скачать вариант 9 | ответы |
| скачать вариант 10 | ответы |
| скачать вариант 11 | ответы |
| скачать вариант 12 | ответы |
| скачать вариант 13 | ответы |
| скачать вариант 14 | ответы |
| ЕГЭ 100 баллов (с решениями) | |
| Вариант 1 | скачать |
| Вариант 2 | скачать |
| Вариант 3 | скачать |
| Вариант 4 | скачать |
| Вариант 5 | скачать |
| Вариант 6 | скачать |
| Вариант 7 | скачать |
| Вариант 8 | скачать |
| Вариант 9 | скачать |
| Вариант 10 | скачать |
| Вариант 12 | скачать |
| Вариант 13 | скачать |
| Вариант 14 | скачать |
| Широкопояс (Источник: vk.com/naukadljatebja) | |
| Variant 1 | скачать |
| Variant 2 | скачать |
| Variant 3 | скачать |
| Variant 4 | скачать |
| Variant 5 | скачать |
| Variant 6 | скачать |
| Variant 7 | скачать |
| Variant 8 | скачать |
| Variant 9 | скачать |
| Variant 10 | скачать |
| Variant 11 | скачать |
| Variant 12 | скачать |
| Variant 13 | скачать |
| Variant 14 | скачать |
| Variant 15 | скачать |
| Variant 16 | скачать |
| Variant 17 | скачать |
| Variant 18 | скачать |
| Variant 19 | скачать |
| Variant 20 | скачать |
| Variant 21 | скачать |
| Variant 22 | скачать |
| Variant 23 | скачать |
| Variant 24 | скачать |
| Variant 25 | скачать |
| Variant 26 | скачать |
| Variant 27 | скачать |
| Variant 28 | скачать |
| Variant 29 | скачать |
| Variant 30 | скачать |
| vk.com/shkolkovo_him | |
| вариант 1 | разбор |
| вариант 2 | разбор |
| вариант 3 | ответы |
| вариант 4 | ответы |
| вариант 5 | ответы |
| vk.com/repetitor_korsakova | |
| variant 1 | otvet |
| variant 2 | otvet |
| variant 3 | otvet |
| СтатГрад | |
| Вариант 1-2 | критерии оценивания |
| Вариант 3-4 | критерии оценивания |
| vk.com/schoolzhukova | скачать вариант
ответы |
| → купить сборники типовых вариантов ЕГЭ по химии |
Варианты в соответствии с новой демоверсией ЕГЭ 2022 по химии.
→ Тренировочные варианты ЕГЭ 2021 по химии
Подходы к отбору содержания, разработке структуры КИМ ЕГЭ
Отбор содержания заданий КИМ для проведения ЕГЭ по химии в 2022 г. в целом осуществляют с сохранением установок, на основе которых формировались экзаменационные модели предыдущих лет. В числе этих установок наиболее важными с методической точки зрения являются следующие.
КИМ ориентированы на проверку усвоения системы знаний и умений, формирование которых предусмотрено действующими программами по химии для общеобразовательных организаций. Во ФГОС эта система знаний и умений представлена в виде требований к предметным результатам освоения учебного предмета. С данными требованиями соотносится уровень предъявления в КИМ проверяемых элементов содержания.
Экзаменационные варианты по химии содержат задания, различные по форме предъявления условия и виду требуемого ответа, по уровню сложности, а также по способам оценки их выполнения. Как и в предыдущие годы, задания КИМ ЕГЭ 2022 г. построены на материале основных разделов школьного курса химии: общей, неорганической и органической, изучение которых обеспечивает овладение учащимися системой химических знаний.
К числу главных составляющих этой системы относятся: ведущие понятия о химическом элементе, веществе и химической реакции; основные законы и теоретические положения химии; знания о системности и причинности
химических явлений, генезисе веществ, способах познания веществ.
В стандарте эта система знаний представлена в виде требований к уровню подготовке выпускников. В целях обеспечения возможности дифференцированной оценки учебных достижений выпускников КИМ ЕГЭ осуществляют проверку освоения основных образовательных программ по химии на трёх уровнях сложности: базовом, повышенном и высоком.
При разработке КИМ особое внимание было уделено реализации требований к конструированию заданий различного типа. Каждое задание строилось таким образом, чтобы его содержание соответствовало требованиям к уровню усвоения учебного материала и формируемым видам учебной деятельности.
Учебный материал, на основе которого строились задания, отбирался по признаку его значимости для общеобразовательной подготовки выпускников средней школы. Большое внимание при конструировании заданий было уделено усилению деятельностной и практико-ориентированной составляющей их содержания. Данный подход позволяет усилить дифференцирующую способность экзаменационной модели, так как требует от обучающихся последовательного выполнения нескольких мыслительных операций с опорой на понимание причинно- следственных связей, умений обобщать знания, применять ключевые понятия и др.
Смотрите также:
Материал по химии
- Какие реакции нужно знать, чтобы решить ЕГЭ по химии?
- 1) Взаимодействие металлов с кислородом
- 2) Взаимодействие металлов с водой
- 3) Амфотерные металлы
- 4) Амфотерные оксиды и гидроксиды
- 5) Комплексные соли
- 6) Амфотерные соли
- 7) Углерод на ЕГЭ
-
Азот на ЕГЭ
- 9) Фосфор на ЕГЭ
- 10) Сера на ЕГЭ
- 11) Замещение неметаллов
- 12) Взаимодействие неметаллов с другими неметаллами
- 13) Медь и её соединения
- 14) Серебро и его соединения
- 15) Хром и его соединения
- 16) Железо и его соединения
- 17) Соединения марганца
- 18) Неметаллы с щелочами
- 19) Кислотные оксиды с щелочами
- 20) Гидриды, фосфиды, нитриды, сульфиды, карбиды
- 21) Гидролиз бинарных соединений с ковалентной полярной связью
- 22) Взаимный гидролиз
В данном материале мы рассмотрим только те реакции неорганической химии, что выходят за пределы свойств классов (солей, кислот, оксидов, оснований) и часто встречаются в 8 задании. В материале Вы познакомитесь с самыми популярными реакциями, которые встречаются на экзамене.
Какие реакции нужно знать, чтобы решить ЕГЭ по химии?
1) Взаимодействие металлов с кислородом
- Натрий, как и другие щелочные металлы (кроме лития), а также барий, при взаимодействии с кислородом образуют пероксиды или надпероксиды:
2Na + O2 = Na2O2
Причем, для натрия более характерен пероксид, а для калия – надпероксид:
K + O2 = KO2
- Пероксиды реагируют с холодной и горячей водой по-разному: с холодной водой происходит реакция обмена:
Na2O2 + 2H2O = 2NaOH + H2O2
В горячей воде происходит окислительно-восстановительная реакция:
2Na2O2 + H2O = 4NaOH + O2↑
2) Взаимодействие металлов с водой
Основные продукты при взаимодействии металлов с водой можно представить в виде следующей схемы:
Задание 8 ЕГЭ по химии
- Активные металлы, такие как натрий, калий, кальций, легко реагируют с водой, вытесняя водород. Реакции относятся к экзотермическим (проходят с выделением большого количества тепла), натрий и калий так активно реагируют с водой, что при контакте происходит их возгорание.
2Na + 2H2O = 2NaOH + H2↑
- Магний и алюминий тоже образуют гидроксиды, но для реакции необходимо нагревание. Алюминий берут в виде амальгамы.
Mg + 2H2O = Mg(OH)2 + H2↑
- Металлы средней активности требуют нагревания для взаимодействия с водой, при этом образуется оксид, а не гидроксид:
Zn + H2O = ZnO + H2↑
- Железо при взаимодействии с водой образует окалину (смесь оксида железа II и оксида железа III):
3Fe + 4H2O = Fe3O4 + 4H2
- На влажном воздухе железо превращается в бурый гидроксид железа III:
2Fe + 3H2O + 3O2 = 2Fe(OH)3
Задание в формате ЕГЭ с ответом:
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- K + H2O →
- K2O + H2O →
- K + O2 →
- K2O2 + H2Oхолод. →
- KOH
- K2O
- KOH + H2O2
- KOH + H2
- KO2
Пример задания из КИМ ЕГЭ:
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Ba + O2 →
- BaO + H2O →
- Ba + H2O →
- BaO2 + H2O (горяч.) →
- Ba(OH) 2 + O2
- BaO2
- Ba(OH) 2
- BaO
- Ba(OH) 2 + H2
От активности металла зависит продукт реакции
3) Амфотерные металлы
Алюминий, цинк и бериллий отличаются от других металлов тем, что могут вступать во взаимодействие с концентрированными растворами щелочей, понятие «амфотерные металлы» использовано для облегчения поиска, такое понятие не совсем верно.
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2
4) Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды реагируют с концентрированными растворами щелочей, причем продукт зависит от агрегатного состояния исходной щелочи: если она твердая, то применяют сплавление и образуется средняя соль, если же щелочь дана в растворенном виде, то образуется комплексная соль. Эти различия очень часто встречаются в задании 8 на ЕГЭ по химии!
- При сплавлении:
Al2O3 + 2NaOH = 2NaAlO2 + H2O↑
Al(OH)3 + NaOH = NaAlO2 + 2H2O↑
- При растворении в концентрированной щелочи:
BeO + 2KOH + H2O = K2[Be(OH)4]
Be(OH)2 + 2KOH = K2[Be(OH)4]
Можно брать любую щелочь и любой амфотерный оксид или гидроксид.
- Амфотерные оксиды, при сплавлении с солями, вытесняют летучие кислотные оксиды:
Na2CO3 + Al2O3 = 2NaAlO2 + CO2↑
K2SO3 + ZnO = K2ZnO2 + SO2↑
Задание по образцу ФИПИ:
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Be + KOH р-р →
- BeO + KOH р-р →
- BeO + KOH тв. →
- Be(OH) 2 + KOH тв. →
- K2 [Be(OH) 4] + H2O
- K2 [Be(OH) 4] + H2
- K2O + Be(OH) 2
- K2 [Be(OH) 4]
- K2BeO2 + H2O
5) Комплексные соли
- Комплексные соли разлагаются при нагревании с потерей воды:
Na[Al(OH)4] = NaAlO2 + 2H2O
K2[Zn(OH)4] = K2ZnO2 + 2H2O
- Комплексные соли реагируют с сильными кислотами в двух вариантах (при избытке и при недостатке кислоты):
Na[Al(OH)4] + HCl = NaCl + H2O + Al(OH)3↓ (при недостатке кислоты)
Na[Al(OH)4] + 4HCl = NaCl + AlCl3 + 4H2O (при избытке кислоты)
- Комплексные соли реагируют со слабыми кислотами и летучими кислотными оксидами, получаемые сульфиды, карбонаты, сульфиты алюминия неустойчивы, поэтому вместо них записывают гидроксид амфотерного металла:
2Na[Al(OH)4] + H2S = Na2S + 2Al(OH)3 + 2H2O (при недостатке сероводородной кислоты)
Na[Al(OH)4] + H2S = NaHS + Al(OH)3 + H2O (при избытке сероводородной кислоты)
2Na[Al(OH)4] + CO2 = Na2CO3 + 2Al(OH)3 + H2O (при недостатке углекислого газа)
Na[Al(OH)4] + CO2 = NaHCO3 + Al(OH)3 (в условиях избытка углекислого газа)
Попробуйте решить задание ЕГЭ:
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Na2 [Zn(OH) 4] нагревание →
- Na2 [Zn(OH) 4] + H2S изб. →
- Na2 [Zn(OH) 4] + H2S нед. →
- NaOH тв. + Zn(OH) 2 →
- NaHS + ZnS + H2O
- Na2S + Zn(OH) 2 + H2O
- Na2ZnO2 + H2O
- Na2S + Zn + H2O
- Na2ZnO2 + H2
6) Амфотерные соли
Термин «амфотерные соли» некорректен, однако за последний месяц было более четырех тысяч запросов с таким сочетанием слов, под амфотерными солями школьник понимает соли, в анионе которого стоит амфотерный металл, а также комплексные соли, описанные выше. На самом деле, соли в которых амфотерный металл принадлежит аниону следует относить к самым обычным средним солям. Рассмотрим свойства некоторых из них, например, цинката натрия (Na2ZnO2) и алюмината калия (KAlO2).
- Реагируют с сильными кислотами:
Na2ZnO2 + 4HCl = 2NaCl + ZnCl2 + 2H2O
2KAlO2 + 4H2SO4 = K2SO4 + Al2(SO4)3 + 4H2O
Б) Растворяются в воде с образованием соответствующей комплексной соли:
KAlO2 + 2H2O = K[Al(OH)4]
- Также под амфотерными солями школьники подразумевают соли, содержащие в катионе металл в третьей валентности (что тоже является неверным, это средние соли) или цинк и бериллий, такие соли могут по-разному реагировать с растворами щелочей, например:
AlCl3 + 3NaOH = 3NaCl + Al(OH)3 (недостаток щелочи, разбавленный раствор щелочи)
AlCl3 + 4NaOH = NaCl + Na[Al(OH)4] (избыток щелочи, концентрированный раствор щелочи)
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Na2BeO2 + H2SO4 →
- Na2 [Be(OH) 4] + H2SO4 изб. →
- Na2 [Be(OH) 4] + H2SO4 нед. →
- Na2BeO2 + H2O →
- Na2SO4 + BeSO4 + H2O
- Na2SO4 + Be(OH) 2
- Na2SO4 + Be(OH) 2 + H2O
- Na2 [Be(OH) 4]
- NaOH + BeSO4 + H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- AlCl3 + KOH разб. →
- AlCl3 + K2CO3 р-р →
- AlCl3 + KOH конц. →
- Al2O3 + K2CO3 тв. →
- Al(OH) 3 + KCl
- KCl + KAlO2 + H2O
- KAlO2 + CO2
- K[Al(OH) 4] + KCl
- Al(OH) 3 + KCl + CO2
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Ba(OH) 2 нед. + AlCl3 →
- Ba(OH) 2 изб. + AlCl3 →
- Ba(AlO2)2 + HCl →
- Ba[Al(OH) 4]2 + HCl изб. →
- Ba(OH) 2 + AlCl3 + H2O
- BaCl2 + Ba[Al(OH) 4]2
- BaCl2 + AlCl3 + H2O
- BaCl2 + Al(OH) 3 + H2O
- BaCl2 + Al(OH) 3
7) Углерод на ЕГЭ
В задании 8 часто встречаются гидрокарбонаты, рассмотрим их важнейшие свойства на примере гидрокарбоната кальция.
Гидрокарбонаты, как и другие кислые соли, при взаимодействии с щелочами, оксидами, солями, кислотами и при нагревании часто превращаются в средние соли.
- Разложение при нагревании:
Ca(HCO3)2 → CaCO3 + CO2 + H2O
- Взаимодействие с щелочами:
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O
Ca(HCO3)2 + 2NaOH → CaCO3 + Na2CO3 + 2H2O
- Взаимодействие с кислотами:
Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 + 2H2O
- Реакция с карбонатами. Эти реакции идут с образованием кислых солей, необходимый для их образования водород поступает из воды, поэтому составители используют такие обозначения как CO2 р-р или CaCO3 влажн., реакция идет по следующей схеме:
CaCO3 + CO2 + H2O → Ca(HCO3)2
- Углекислый газ
Восстановление углерода активными металлами и углеродом:
CO2 + 2Mg → 2MgO + C
CO2 + C → 2CO
- Реакции с монооксидом углерода:
- CO или угарный газ – хороший восстановитель, реагирует с окислителями:
CO + CuO = CO2 + Cu
CO + Cl2 = COCl2
CO + Br2 = COBr2
2CO + O2 = 2CO2
- Монооксид углерода проявляет и окислительные свойства:
СO + H2 = CH3OH
- Вступает в реакции без изменения степени окисления:
CO + NaOHтв. = HCOONa (при сплавлении)
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- KHCO3 + Ca(OH) 2 →
- Mg(HCO3)2 + H2CrO4 →
- MgCO3 + H2CrO4 →
- Ca(HCO3)2 + KOH →
- Cr2O3 + MgCO3 + H2O
- KOH + Ca(HCO3)2
- CaCO3 + K2CO3 + H2O
- MgCrO4 + H2O + CO2
- CaO + K2CO3 + H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Mg + CO2 →
- MgO + CO2 →
- Mg(HCO3)2 + NaOH →
- MgCl2 + Na2CO3 →
- MgO + C
- MgCO3
- Mg + CO
- MgCO3 + Na2CO3 + H2O
- MgCO3 + NaCl
 Азот на ЕГЭ
Азот на ЕГЭ
Очень популярной в заданиях ЕГЭ по химии является азотная кислота, в отличие от обычных кислот, в качестве окислителя выступает не протон водорода, а азот в высшей степени окисления.
В общем, схему реакции кислоты с металлами можно представить в следующем виде:
HNO3 + Me → Me+x(NO3)x + H2O + особый продукт
Особые продукты зависят от характера металла, приведем из в виде таблицы:
Таблица – свойства азотной кислоты
|
Реагент |
HNO3 концентрированная |
HNO3 разбавленная |
|
Активные металлы (металлы IA и IIА-группы в таблице Менделеева) |
N2O (редко NO) |
NH4NO3 (редко N2 или NH3) |
|
Неактивные металлы Cu, Ag, Hg |
NO2 |
NO |
|
Cr, Al, Fe |
На холоде реакция не идёт в следствие пассивации, При нагревании образуется NO2, а металл приобретает степень окисления +3 |
NO (редко N2, N2O) |
|
Металлы средней активности (все остальные металлы, например, Zn, Ni, Co) |
NO2 |
NO (редко N2, N2O) |
|
Au, Pt |
Реакция не идет |
Реакция не идет |
- Примеры реакций металлов с азотной кислотой:
4HNO3 разб. + Al = Al(NO3)3 + NO + 2H2O (при любой температуре)
6HNO3 конц. + Al = Al(NO3)3 + 3NO2 + 3H2O (реакция идет только при нагревании)
10HNO3 разб. + 4Mg = 4Mg(NO3)2 + NH4NO3 + 3H2O
10HNO3 конц. + 4Mg = 4Mg(NO3)2 + N2O + 5H2O
- C другими восстановителями азотные кислоты ведут себя аналогичным образом: у концентрированной продуктом является NO2, а у разбавленной – NO:
FeO + 4HNO3 конц. = Fe(NO3)3 + NO2 + 2H2O
3FeO + 10HNO3 разб. = 3Fe(NO3)3 + NO + 5H2O
- Азотная кислота реагирует и с неметаллами, например, с серой и углеродом:
6HNO3 конц. + S = H2SO4 + 6NO2 + 2H2O
4HNO3 конц. + С = CO2 + 4NO2 + 2H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- CuO + HNO3 конц. →
- CuO + HNO3 разб. →
- Cu + HNO3 конц. →
- Cu + HNO3 разб. →
- Cu(NO3)2 + H2O + NO2
- CuO + NO2 + O2
- Cu(NO3)2 + H2O
- Cu(NO3)2 + H2O + NO
- CuNO3 + H2O + NO
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- FeO + HNO3 конц. →
- Fe + HNO3 конц. tºC →
- Fe(NO3)2 + HNO3 конц. →
- FeO + HNO3 разб. →
- Fe(NO3)2 + H2O + NO2
- Fe(NO3)3 + H2O + NO2
- Fe(NO3)2 + H2O + NO
- Fe(NO3)3 + H2O + NO
- Fe(NO3)2 + H2O
9) Фосфор на ЕГЭ
- Фосфор выступает в роли окислителя и восстановителя в реакции с щелочами:
4P + 3NaOH + 3H2O → 3NaH2PO2 + PH3↑
Это одна из самых популярных окислительно-восстановительных реакций с фосфором на ЕГЭ по химии.
- оксид фосфора III реагирует с холодными растворами щелочей и водой без изменения степени окисления:
P2O3 + 2KOH + H2O → 2KH2PO3
P2O3 + 3H2O → 2H3PO3 (или HPO2)
- Соединения фосфора III – хорошие восстановители, стремятся превратиться в соединения фосфора V:
P2O3 + окислитель → PO43‒ + продукты восстановления
P2O3 + 4KMnO4 + 10KOH → 2K3PO4 + 4K2MnO4 + 5H2O
P2O3 + 4HNO3 + H2O → 2H3PO4 + 4NO2
- Оксид фосфора V реагирует с водой, образуя ряд кислот:
P2O5 + H2O → 2HPO3 – метафосфорная (в сильном недостатке воды)
P2O5 + 2H2O → H4P2O7 – пирофосфорная (в небольшом недостатке воды)
P2O5 + 3H2O → 2H3PO4 – ортофосфорная (в избытке воды)
- Фосфаты могут образовывать кислые соли, при взаимодействии с фосфорной кислотой:
2K3PO4 + H3PO4 → 3K2HPO4
K3PO4 + 2H3PO4(большой избыток) → 3KH2PO4
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- NaH2PO4 + NaOH нед. →
- NaH2PO4 + NaOH изб. →
- NaH2PO4 изб. + NaOH →
- NaH2PO4 нед. + NaOH →
- Na3PO4 + H2O
- NaH2PO3 + H2O
- Na3PO4 + P2O5
- NaH2PO2 + H2O
- Na2HPO4 + H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- P2O5 + H2O нед. →
- P2O3 + KOH →
- P + KOH →
- P2O5 нед. + H2O →
- K2HPO3 + H2O
- KH2PO2 + PH3
- HPO3
- H3PO4
- HPO2
10) Сера на ЕГЭ
Таблица ‒ Серная кислота
|
Свойства |
Разбавленная H2SO4 |
Концентрированная H2SO4 |
|
Окислительные свойства |
Окислитель за счет протона водорода |
Окислитель за счет серы |
|
Активные металлы |
2Na + H2SO4 = Na2SO4 + H2 |
8Na + 5H2SO4 = 4Na2SO4 + 4H2O + H2S↑ |
|
Металлы средней активности |
Zn + H2SO4 = ZnSO4 + H2 |
3Zn + 4H2SO4 = 3ZnSO4 + 4H2O + S↓ (в зависимости от концентрации кислоты может выделиться SO2 или H2S) |
|
Al, Cr, Fe |
Как с другими металлами до водорода: Fe + H2SO4 = FeSO4 + H2 |
На холоде реакция не идет (пассивация), при нагревании: 2Fe + 6H2SO4 = Fe2(SO4)3 + 6H2O + 3SO2 |
|
Металлы средней активности |
Реакция не идет, так как эти металлы не могут вытеснить водород |
Cu + 2H2SO4 = CuSO4 + 2H2O + SO2 |
- Обменная реакция с концентрированной серной кислотой:
NaCl + H2SO4 конц. = NaHSO4 + HCl↑ (при сильном нагревании)
Остальные обменные реакции стандартны и в этом материале рассмотрены не будут.
- Сероводород:
SO2 + 2H2S = 3S↓ + 2H2O
2H2S + 3O2 = 2H2O + 2SO2 (кислород в избытке)
2H2S + O2 = 2H2O + 2S↓ (кислород в недостатке)
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- KCl тв. + H2SO4 конц. →
- KI + H2SO4 конц. →
- Fe + H2SO4 конц. tºC →
- FeO + H2SO4 конц. →
- Cl2 + K2SO4 + H2O
- KHSO4 + HI
- KHSO4 + HCl
- I2 + K2SO4 + H2S
- Fe2 (SO4)2 + H2O + SO2
- FeSO4 + H2O
11) Замещение неметаллов
Часто в задании 8 ЕГЭ по химии встречается замещение брома на хлор, или йода на хлор или бром. Галогены могут вытеснять друг друга и другие неметаллы из соединений. Чтобы понимать, какие неметаллы могут вытеснить другие неметаллы, нужно помнить о том, что в ПС Д.И. Менделеева элементы стоят таким образом, что чем правее и выше стоит элемент, тем сильнее проявляются его неметаллические свойства, и тем выше его электроотрицательность. Более электроотрицательные неметаллы могут вытеснять менее электроотрицательные. Так, хлор и бром стоят выше в таблице Менделеева, чем йод, поэтому могут вытеснить его из соединений:
2NaI + Br2 = 2NaBr + I2
2KI + Cl2 = 2KCl + I2
Хлор может вытеснить бром:
2NaBr + Cl2 = 2NaCl + Br2
Йод не может вытеснить другие галогены, так как расположен в ПС ниже хлора, брома и фтора, но йод может вытеснить те элементы-неметаллы, что стоят левее в Периодической системе, например, серу:
H2S + I2 = 2HI + S
Можно использовать ряд электроотрицательности неметаллов, на реальном ЕГЭ его не будет, легче запомнить Периодический закон, тем более что эти знания также нужны для выполнения задания 2 ЕГЭ по химии.
12) Взаимодействие неметаллов с другими неметаллами
Более электроотрицательные неметаллы могут окислить менее электроотрицательные неметаллы. То есть те элементы, которые стоят в ПС выше и правее отнимают электроны у тех неметаллов, которые стоят ниже и левее.
Например, хлор, бром и фтор могут окислить йод, серу, фосфор (наиболее популярные на ЕГЭ реакции). В таблице представлены наиболее популярные продукты:
Таблица – взаимодействие неметаллов
|
Восстановители |
Окислители |
|||||
|
F2 |
Cl2 |
Br2 |
I2 |
O2 |
S |
|
|
I2 |
IF7 IF5 |
ICl5 ICl3 ICl |
IBr5 IBr3 IBr |
‒ |
‒ |
‒ |
|
S |
SF6 |
SCl4 |
SBr4 |
‒ |
SO2 |
‒ |
|
P |
PF5 |
PCl5 PCl3 |
PBr5 PBr3 |
PI3 |
P2O3 P2O5 |
P2S3 P2S5 |
|
Si |
SiF4 |
SiCl4 |
SiBr4 |
SiI4 |
SiO2 |
SiS2 |
|
H2 |
HF |
HCl |
HBr |
HI |
H2O |
H2S |
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- S + O2 →
- SO2 + O2 →
- H2S + SO2 →
- S + P →
- S + H2O
- SO2
- P2S3
- SO3
- S3P2
13) Медь и её соединения
2CuCl2 + 4KI = 2CuI↓ + I2 + 4KCl
Cu(OH)2 + 4NH3 = [Cu(NH3)4](OH)2 – темно-синий комплекс
Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH – прозрачный раствор
3CuO + 2NH3 = 3Cu + N2 + 3H2O
14) Серебро и его соединения
AgCl + 2NH3 = [Ag(NH3)2]Cl
8AgNO3 + PH3 + 4H2O = H3PO4 + 8Ag + 8HNO3
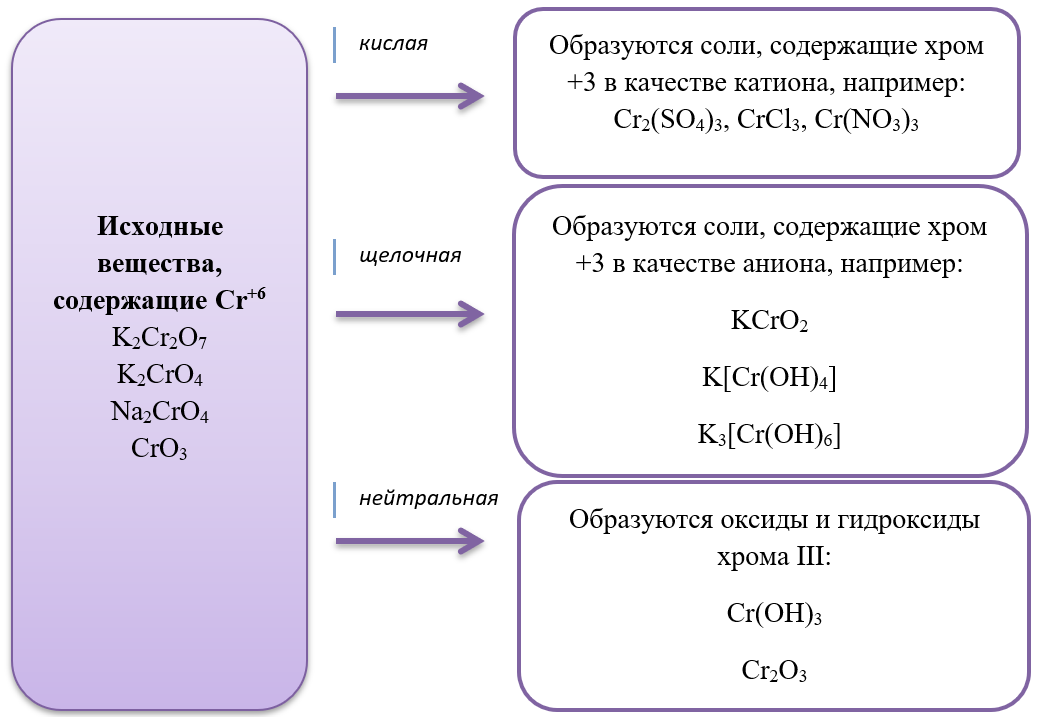
15) Хром и его соединения
- Соединения хрома II – хорошие восстановители, при взаимодействии с окислителями превращаются в соединения хрома III
4CrO + O2 = 2Cr2O3
CrO + 4HNO3 = Cr(NO3)3 + 2H2O + NO2
- соединения хрома III проявляют как окислительные, так и восстановительные свойства:
2Na3[Cr(OH)6] + 3Br2 + 4NaOH = 6NaBr + 8H2O + 2Na2CrO4 (хром в степени окисления +3 является восстановителем)
2CrCl3 + H2 = 2CrCl2 + 2HCl (хром в степени окисления +3 является восстановителем)
- Дихроматы – соли, окрашивающие растворы в оранжевый цвет и хроматы – соли желтого цвета устойчивы в разных средах: в кислой среде устойчивы оранжевые дихроматы, а в щелочной – желтые хроматы. В зависимости от среды, они могут взаимно превращаться:
Хромат превращается в дихромат в кислой среде, раствор меняет цвет с желтого на оранжевый.
2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
Дихромат превращается в хромат в щелочной среде, раствор меняет цвет с оранжевого на желтый.
K2Cr2O7 + 2KOH = 2K2CrO4 + H2O
В ЕГЭ по химии стали уже традиционными задания с соединениями хрома, особенно с дихроматами, в основном встречается их окислительно-восстановительные свойства:
16) Железо и его соединения
- Железо реагирует с концентрированной азотной и серной кислотой только при нагревании, с разбавленными кислотами реагирует при нормальных условиях, например:
Fe + 6HNO3 конц = Fe(NO3)3 + 3NO2 + 3H2O (при нагревании)
- Взаимодействие железа с галогенами и галогенводородами:
Таблица – Железо с галогенами и галогеноводородами
|
С галогенами |
С галогенводородом |
|
2Fe + 3Cl2 = 2FeCl3 |
Fe + 2HCl = FeCl2 + H2 |
|
2Fe + 3Br2 = 2FeBr3 |
Fe + 2HBr = FeBr2 + H2 |
|
Fe + I2 = FeI2 |
Fe + 2HI = FeI2 + H2 |
- Соединения двухвалентного железа – хорошие восстановители, с окислителями превращаются в соединения трехвалентного железа:
FeO + 4HNO3 конц = Fe(NO3)3 + NO2 + 2H2O
2FeCl2 + Cl2 = 2FeCl3
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
- Железная окалина – двойной оксид Fe3O4 или FeO·Fe2O3, проявляет как окислительные (за счет оксида железа III), так и восстановительные (за счет железа II) свойства, а также растворяется в кислотах, образуя две соли (железа II и железа III)
Fe3O4 + 4H2SO4 разб. = FeSO4 + Fe2(SO4)3 + 4H2O (оксиды железа растворились в разбавленной серной кислоте без изменения степени окисления)
Fe3O4 + 8KI + 4H2SO4 = 3FeI2 + 4K2SO4 + I2 + 4H2O (железная окалина проявляет окислительные свойства за счет наличия железа III)
Fe3O4 + 10HNO3конц = 3Fe(NO3)3 + NO2 + 5H2O (железная окалина проявляет восстановительные свойства за счет железа II)
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Fe + I2 →
- Fe + Cl2 →
- Fe + HCl →
- Fe + O2 →
- FeI3
- FeCl2
- FeI2
- FeCl3
- FeO
- Fe3O4
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- Fe + CuSO4 →
- Fe + H2SO4 р-р →
- Fe + H2SO4 конц. tºC →
- Fe + H2O + O2 →
- FeSO4 + Cu
- FeSO4 + H2
- Fe2(SO4)3 + Cu
- Fe2 (SO4)3 + H2
- Fe2(SO4)3 + SO2 + H2O
- Fe(OH) 3
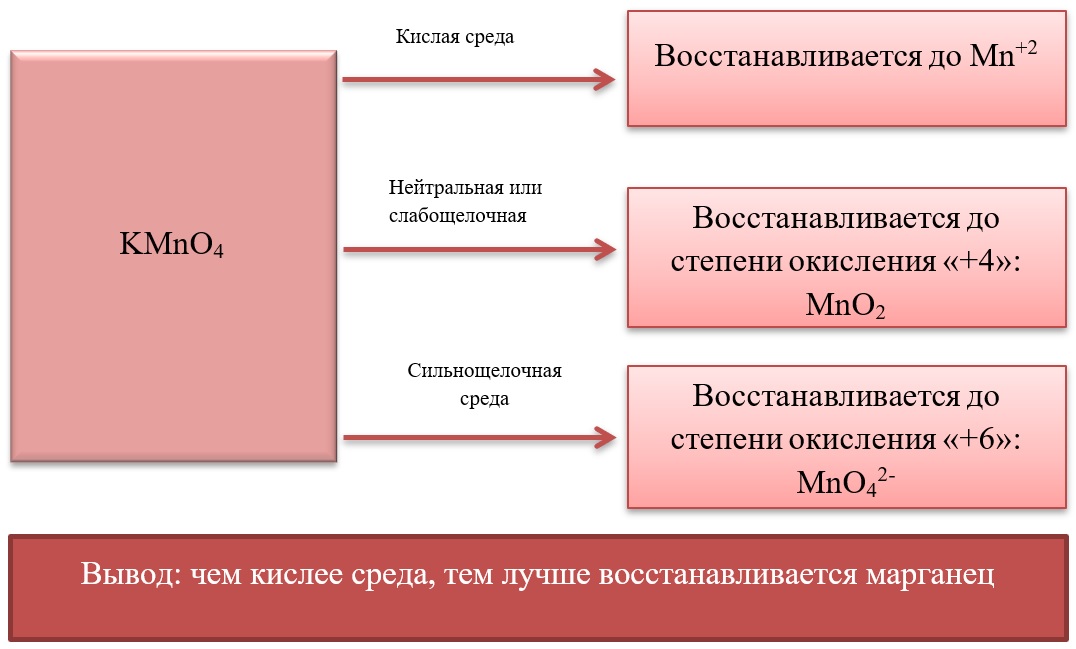
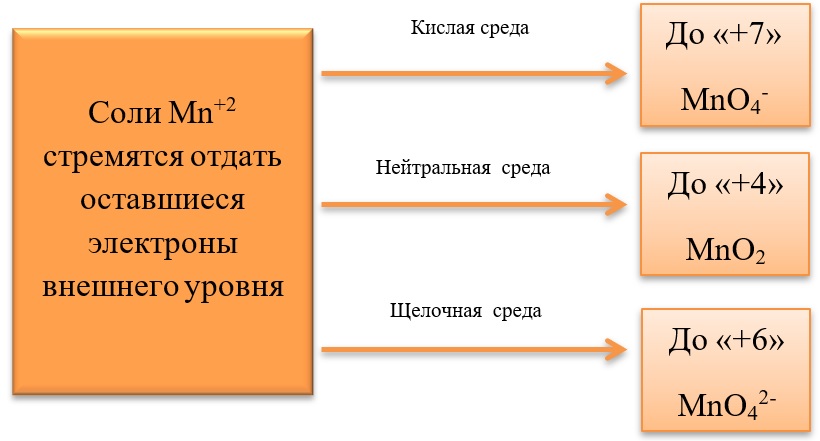
17) Соединения марганца
- Марганец в степени окисления +7 проявляет окислительные свойства. Продукты его восстановления зависят от среды:
Примеры реакция перманганата калия:
2KMnO4 + 5Na2SO3 + 3H2SO4 = 2MnSO4 + 5Na2SO4 + K2SO4 + 3H2O
2KMnO4 + 6KI + 4H2O = 2MnO2 + 3I2 + 8KOH
2KMnO4 + SO2 + 4KOH = K2SO4 + 2K2MnO4 + 2H2O
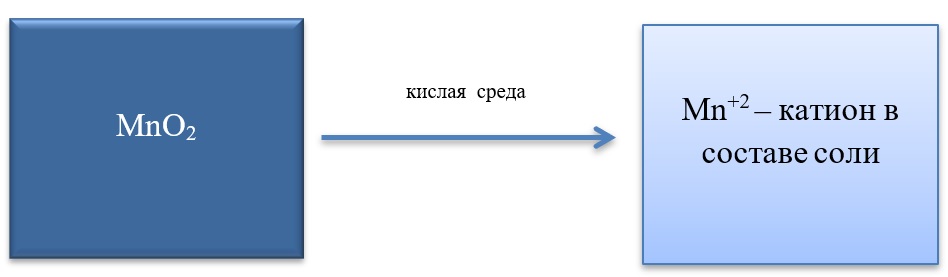
- Марганец в степени окисления +4 проявляет как окислительные. Так и восстановительные свойства.
Окислительные свойства чаще проявляет в кислой среде, восстанавливаясь до катиона +2.
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O
MnO2 + 2KI + 2H2SO4 = MnSO4 + I2 + K2SO4 + 2H2O
MnO2 + H2O2 + H2SO4 → O2 + MnSO4 + 2H2O
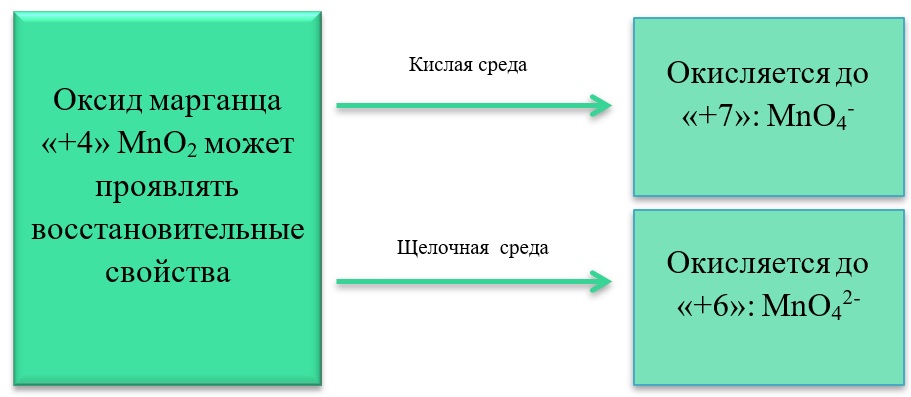
В) Марганец в степени окисления +4 проявляет и восстановительные свойства, окисляясь до +6 в щелочной среде, и до +7 в кислой:
MnO2 + Br2 + 4KOH = K2MnO4 + 2KBr + 2H2O
- Соединения марганца II, например, MnSO4 проявляет как окислительные, так и восстановительные свойства.
Окислительные свойства проявляет в реакциях с более активными металлами, например, с алюминием:
3MnSO4 + 2Al = 3Mn + Al2(SO4)3
Восстановительные свойства проявляет при взаимодействии с типичными окислителями.
2MnSO4 + 5PbO2 + 3H2SO4 = 2HMnO4 + 5PbSO4 + 2H2O
3MnSO4 + 2KMnO4 + 2H2O = 5MnO2 + K2SO4 + 2H2SO4
3MnSO4 + 2KClO3 + 12KOH = 3K2MnO4 + 2KCl + 3K2SO4 + 6H2O
18) Неметаллы с щелочами
- Галогены с щелочами:
Хлор, бром и йод реагируют с щелочами при разных условиях. На холоде окисления галогена происходит чаще до степени окисления +1 (восстановление в любых условиях происходит до степени окисления ‒1). Описать данную реакцию можно уравнением:
Г2 + 2NaOH = NaГ + NaГO + H2O (вместо гидроксида натрия можно взять любую щелочь, содержащую одновалентный металл: K, Cs, Rb)
2Г2 + 2Ca(OH)2 = CaГ2 + Ca(ГO)2 + 2H2O (вместо гидроксида кальция можно брать гидроксид бария и стронция).
Где Г = I, Cl, Br
Например:
Cl2 + 2NaOH = NaCl + NaClO + H2O
2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
При нагревании окисление галогена часто проходит до степени окисления +5:
3Г2 + 6NaOH = 5NaГ + NaГO3 + 3H2O
6Г2 + 6Ca(OH)2 = 5CaГ2 + Ca(ГO3)2 + 6H2O
Например:
3Cl2 + 6NaOH = 5NaCl + NaClO3 + 3H2O
6Cl2 + 6Ca(OH)2 = 5CaCl2 + Ca(ClO3)2 + 6H2O
Обращайте внимание на температуру, от Вашей внимательности зависят Ваши баллы на ЕГЭ по химии!
- Сера, селен и теллур тоже реагируют с щелочами по одной схеме:
3Э + 6NaOH = 2Na2Э + Na2ЭO3 + 3H2O
3Э + 3Ca(OH)2 = 2CaЭ + CaЭO3 + 3H2O
Например:
3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
3S + 3Ca(OH)2 = 2CaS + CaSO3 + 3H2O
- Фосфор с щелочами:
4P + 3NaOH + 3H2O = 3NaH2PO2 + PH3↑
- Кремний с щелочами:
Si + 2NaOH + H2O = Na2SiO3 + 2H2
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- S + NaOH →
- SO2 + NaOH →
- SO3 + NaOH →
- H2S + NaOH →
- NaHS + S + H2O
- Na2SO4 + H2O
- Na2S + Na2SO3 + H2O
- Na2SO3 + H2O
- Na2S + H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- P + NaOH →
- P2O3 + NaOH →
- P2O5 + NaOH изб. →
- P2O5 + NaOH нед. →
- NaH2PO2
- NaH2PO3
- Na3P
- Na3PO4
- NaH2PO4
19) Кислотные оксиды с щелочами
Кислотные оксиды реагируют с щелочами, образуя соль и воду, к нестандартным реакциям относят взаимодействие диоксида азота с щелочами, продукты которого зависят от наличия в среде кислорода:
2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
4NO2 + 4NaOH + O2 = 4NaNO3 + 2H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- NaOH + Cl2O →
- NaOH + NO2 + O2 →
- NaOH + Cl2O3 →
- NaOH + HNO3 →
- NaClO + H2O
- NaCl + HCl
- NaClO2 + H2O
- NaNO3 + H2O
- NaNO2 + NaNO3 + H2O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- NaOH + SO2 →
- NaOH + SO3 →
- NaOH + NO2 →
- NaOH + P2O5 →
- NaNO3 + NaNO2 + H2O
- Na2SO4 + H2O
- NaNO2 + H2O
- NaH2PO4
- NaH2PO3
- Na2SO3 + H2O
20) Гидриды, фосфиды, нитриды, сульфиды, карбиды
Многие неметаллы реагируют с активными металлами, образуя соли или солеподобные вещества, легко гидролизующиеся в воде или кислотах.
Для начала рассмотрим схемы образования этих веществ. В них неметалл часто проявляет низшую степень окисления (значение низшей степени окисления легко определяется по номеру группы: для этого от номера группы нужно отнять 8, например, для азота это будет 5 ‒ 8 = ‒3)
Таблица – Степени окисления, которые принимают неметаллы при взаимодействии с активными металлами:
|
С |
Si |
N и P |
S, Se, Te |
F, Cl, Br, I |
|
‒4 (с Na, K, Al) ‒1 (с Ca, Mg) |
‒4 |
‒3 |
‒2 |
‒1 |
|
Карбиды |
Силициды |
Нитриды и фосфиды |
Сульфиды, селениды, теллуриды |
Фториды, хлориды, бромиды, йодиды |
Степени окисления активных металлов равны номеру группы, в которой они стоят в ПС.
4Na + C = Na4C
4Al + 3C = Al4C3
Ca + 2C = CaC2
4K + Si = K4Si
3Ca + N2 = Ca3N2
3K + P = K3P
2Al + 3S = Al2S3
Ba + Cl2 = BaCl2
Практически все эти вещества, за исключением некоторых сульфидов и галогенидов (хлоридов, бромидов, йодидов, фторидов) неустойчивы в растворах и подвергаются мгновенному гидролизу, который стоит рассматривать как обычную обменную реакцию с водой:
K3P + 3HOH = 3KOH + PH3↑
Na4Si + 4HOH = 4NaOH + SiH4↑
Ca3N2 + 6HOH = 3Ca(OH)2 + 2NH3↑
Продукт гидролиза карбидов зависит от степени окисления углерода в исходном веществе: если она равна ‒1, то образуется ацетилен (C2H2), а если ‒4, то метан (CH4).
Al4C3 + 12HOH = 4Al(OH)3 + 3CH4↑
CaC2 + 2HOH = Ca(OH)2 + C2H2↑
Так же происходит их кислотный гидролиз:
Al4C3 + 12HCl = 4AlCl3 + 3CH4↑
Ba3P2 + 3H2SO4 = 3BaSO4 + 2PH3↑
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- MgC2 + H2O →
- Na4C + H2O →
- Mg3P2 + H2O →
- Na3P + H2O →
- NaOH + C2H2
- Mg(OH) 2 + CH4
- Mg(OH) 2 + PH3
- NaOH + CH4
- Mg(OH) 2 + C2H2
- NaOH + PH3
21) Гидролиз бинарных соединений с ковалентной полярной связью
При гидролизе бинарных соединений неметаллов важно помнить, что степень окисления неметаллов не изменяется, из неметалла с положительной степенью окисления образуется кислотный гидроксид (кислородсодержащая кислота), из отрицательно заряженного неметалла образуется бескислородная кислота:
PCl5 + 4H2O = H3PO4 + 5HCl
SF6 + 4H2O = H2SO4 + 6HF
ICl3 + 2H2O = HIO2 + 3HCl
Для образования гидроксидов неметаллов можно воспользоваться следующей таблицей:
|
Степень окисления неметалла |
Э+1 |
Э+3 |
Э+4 |
Э+5 |
Э+6 |
Э+7 |
|
Соответствующая кислота (кислотный гидроксид) |
НЭО |
HЭO2 Или H3ЭO3 |
H2ЭO3 |
HЭO3 Или H3ЭO4 |
H2ЭO4 |
HЭO4 |
|
Примеры |
HClO |
HClO2 H3PO3 |
H2SO3 |
HIO3 H3PO4 |
H2SO4 |
HClO4 |
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- ICl + H2O →
- ICl3 + H2O →
- ICl5 + H2O →
- ICl7 + H2O →
- HClO3 + HI
- HIO + HCl
- HIO4 + HCl
- HIO2 + HCl
- HIO3 + HCl
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- PCl3 + H2O →
- SCl4 + H2O →
- SiCl4 + H2O →
- PCl5 + H2O →
- H2SO4 + HCl
- H2SiO3 + HCl
- H3PO3 + HCl
- SO2 + HCl
- HPO3 + HCl
22) Взаимный гидролиз
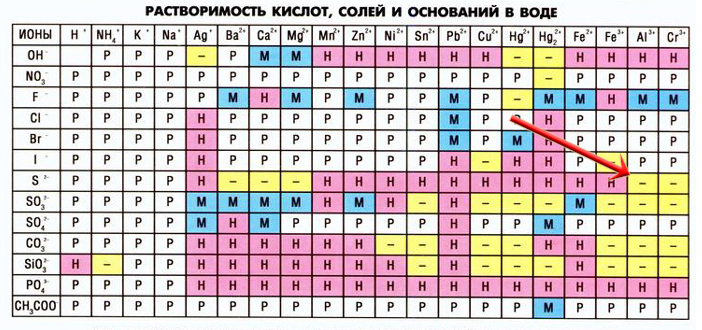
При взаимодействии некоторых солей могут образоваться новые соли, неустойчивые в растворах, в таких случаях в таблице растворимости на пересечении катиона и аниона мы видим прочерк (не существует или необратимо разлагается водой), например, сульфид алюминия:
Сульфид алюминия образуется в реакциях между растворимыми сульфидами и солями алюминия:
3Na2S + 2AlCl3 = 6NaCl + Al2S3
Но данная запись неверна, так как сульфида алюминия не существует в растворах, записываем уравнение гидролиза этой соли:
Al2S3 + 6HOH = 2Al(OH)3↓ + 3H2S↑
Объединим первое уравнение со вторым(левую часть первого уравнение соединяем с левой частью второго уравнения, а правую с правой, все коэффициенты сохраняем):
3Na2S + 2AlCl3 + Al2S3 + 6H2O = 6NaCl + Al2S3 + 2Al(OH)3↓ + 3H2S↑
Сокращаем сульфид алюминия, так как он есть и в правой части реакции, и в левой:
3Na2S + 2AlCl3 + 6H2O = 6NaCl + 2Al(OH)3↓ + 3H2S↑ — так выглядит реакция взаимодействия растворов сульфида натрия и хлорида алюминия.
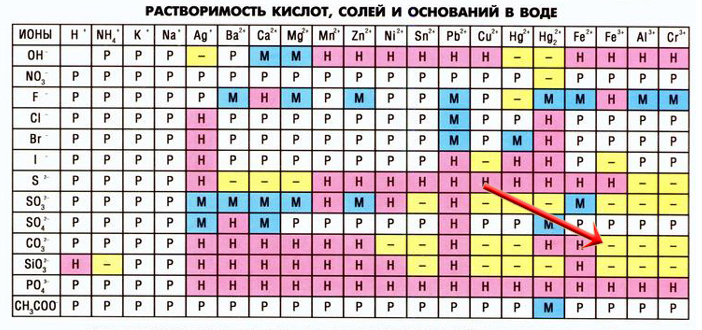
Рассмотрим еще один пример — взаимодействие карбоната калия и нитрата железа III:
3K2CO3 + 2Fe(NO3)3 = Fe2(CO3)3 + 6KNO3
Образовавшийся карбонат железа III разлагается в воде:
Fe2(CO3)3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑
Соединяем два уравнения:
3K2CO3 + 2Fe(NO3)3 + Fe2(CO3)3 + 3H2O = Fe2(CO3)3 + 6KNO3 + 2Fe(OH)3↓ + 3CO2↑
Сокращаем карбонат железа III с обеих сторон:
3K2CO3 + 2Fe(NO3)3 + 3H2O = 6KNO3 + 2Fe(OH)3↓ + 3CO2↑
Взаимный гидролиз попался мне на реальном досрочном ЕГЭ по химии 2022 во второй части!
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- CrCl3 + NaOH изб. →
- CrCl3 + NaOH нед. →
- CrCl3 + Na2S р-р →
- Cr2O3 + Na2SO3 →
- Cr(OH) 3 + NaCl + SO2
- NaCl + Cr(OH) 3
- Cr(OH) 3 + NaCl + H2S
- NaCrO2 + SO2
- Na3 [Cr(OH) 6] + NaCl
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- AlCl3 + K2CO3 р-р →
- AlCl3 + KOH изб. →
- AlCl3 + KOH нед. →
- Al2O3 + K2CO3 →
- KCl + K[Al(OH) 4]
- Al(OH) 3 + KCl + CO2
- Al2 (CO3)3 + KCl
- KAlO2 + CO2
- Al(OH) 3 + KCl
Типовые (тематические) тесты в формате ЕГЭ по химии по каждому заданию. Тренировочные тесты, которые соответствуют заданиям ЕГЭ-2023 по химии по темам КИМ ЕГЭ по химии.
Хотите видеть больше интересных материалов? Вы можете поддержать работу сайта:
Обратите внимание! Форма выше — это форма для сбора донатов на работу сайта.
Полные тренировочные варианты ЕГЭ по химии с автопроверкой первой части
Спецификация ЕГЭ по химии-2023
| Номер задания | Тематические тесты по теме |
| 1 | Строение электронных оболочек атомов элементов первых четырёх периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояния атомов |
| 2 | Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов. Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов |
| 3 | Электроотрицательность. Степень окисления и валентность химических элементов |
| 4 | Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения |
| 5 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная) |
| 6 | Характерные химические свойства простых веществ – металлов: щелочных, щёлочноземельных, магния, алюминия; переходных металлов: меди, цинка, хрома, железа. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния. Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот. Характерные химические свойства солей: средних, кислых, оснóвных; комплексных (на примере гидроксосоединений алюминия и цинка). Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена |
| 7 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная). Характерные химические свойства неорганических веществ: – простых веществ – металлов: щелочных, щёлочноземельных, магния, алюминия, переходных металлов (меди, цинка, хрома, железа); – простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния; – оксидов: оснóвных, амфотерных, кислотных; – оснований и амфотерных гидроксидов; – кислот; – солей: средних, кислых, оснóвных; комплексных (на примере гидроксосоединений алюминия и цинка) |
| 8 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная); Характерные химические свойства неорганических веществ: – простых веществ – металлов: щелочных, щёлочноземельных, магния, алюминия, переходных металлов (меди, цинка, хрома, железа); – простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния; – оксидов: оснóвных, амфотерных, кислотных; – оснований и амфотерных гидроксидов; – кислот; – солей: средних, кислых, оснóвных; комплексных (на примере гидроксосоединений алюминия и цинка) |
| 9 | Взаимосвязь неорганических веществ |
| 10 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) |
| 11 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа |
| 12 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Основные способы получения углеводородов (в лаборатории). Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Основные способы получения кислородсодержащих органических соединений (в лаборатории) |
| 13 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки |
| 14 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола). Важнейшие способы получения углеводородов. Ионный (правило В.В. Марковникова) и радикальные механизмы реакций в органической химии |
| 15 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, карбоновых кислот, сложных эфиров. Важнейшие способы получения кислородсодержащих органических соединений |
| 16 | Взаимосвязь углеводородов, кислородсодержащих и азотсодержащих органических соединений |
| 17 | Классификация химических реакций в неорганической и органической химии |
| 18 | Скорость реакции, её зависимость от различных факторов |
| 19 | Реакции окислительно-восстановительные |
| 20 | Электролиз расплавов и растворов (солей, щелочей, кислот) |
| 21 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная |
| 22 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов |
| 23 | Обратимые и необратимые химические реакции. Химическое равновесие. Расчёты количества вещества, массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ |
| 24 | Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений |
| 25 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ. Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки |
| 26 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе» |
| 27 | Расчёты теплового эффекта (по термохимическим уравнениям) |
| 28 | Расчёты массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ. Расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного. Расчёты массовой доли (массы) химического соединения в смеси |
| 29 | Окислитель и восстановитель. Реакции окислительно-восстановительные
Задания 29 (ранее 30) из реального ЕГЭ по химии 2021 Задания 29 (ранее 30) из реального ЕГЭ по химии 2020 |
| 30 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена
Задания 30 (ранее 31) из реального ЕГЭ по химии 2021 Задания 30 (ранее 31) из реального ЕГЭ по химии 2020 |
| 31 | Тренажер задания 31 по химии железа
Тренажер задания 31 ЕГЭ по химии щелочных металлов Тренажер задания 31 ЕГЭ по химии щелочноземельных металлов Тренажер задания 31 по химии азота Тренажер задания 31 по химии алюминия Тренажер задания 31 по химии галогенов Тренажер задания 31 по химии марганца Тренажер задания 31 по химии меди Тренажер задания 31 по химии серы Тренажер задания 31 по химии углерода и кремния Тренажер задания 31 по химии цинка Тренажер задания 31 по химии хрома Задания 31 (ранее 32) из реального ЕГЭ по химии 2021 Задания 31 (ранее 32) из реального ЕГЭ по химии 2020 |
| 32 | Реакции, подтверждающие взаимосвязь органических соединений
Органические цепочки (задания 32, ранее 33) из реального ЕГЭ по химии 2021 Органические цепочки (задания 32, ранее 33) из реального ЕГЭ по химии 2020 |
| 33 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе». Расчёты массы (объёма, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси).Расчёты массы (объёма, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определённой массовой долей растворённого вещества.Расчёты массовой доли (массы) химического соединения в смесиРасчетные задачи по неорганике (задания 33, ранее 34) из реального ЕГЭ по химии 2021Расчетные задачи по неорганике (задания 33, ранее 34) из реального ЕГЭ по химии 2020 |
| 34 | Установление молекулярной и структурной формул вещества
Расчетные задачи, органическая химия (задания 34, ранее 35) из реального ЕГЭ по химии 2021 Расчетные задачи, органическая химия (задания 34, ранее 35) из реального ЕГЭ по химии 2020 |
Чтобы поделиться, нажимайте
Реальный ЕГЭ по химии
Вашему вниманию представлены задания реального ЕГЭ (их видео-объяснения, решения и ответы), которые представлялись в разных регионах и в разные годы. Также на этой странице вы найдёте задания и видео-объяснения из досрочных ЕГЭ, демо ЕГЭ всех лет, начиная с первого ЕГЭ 2002 года. А ещё тренировочные и пробные варианты ЕГЭ от разных авторов, и, конечно, всю литературу для подготовки к ЕГЭ.
В общем, на этой странице есть ВСЁ для вашей подготовки к ЕГЭ. Листайте до конца!
Варианты с видео-объяснением:
- Возможные варианты задания 33 в ЕГЭ 2022
- Возможные варианты задания 34 в ЕГЭ 2022
- Реальный ЕГЭ по химии 2021. Задание 34 (в ЕГЭ 2022 будет заданием 33)
- Открытый вариант ЕГЭ по химии 2021 от ФИПИ (досрочная волна)
- Реальный ЕГЭ по химии 2020. Задание 34 (в ЕГЭ 2022 будет заданием 33)
- Реальный ЕГЭ по химии 2020. Задание 35 (в ЕГЭ 2022 будет заданием 34)
- Новинка ЕГЭ 2020: задачи на «атомистику»
- Досрочный ЕГЭ 2020. Вариант 1
- Досрочный ЕГЭ 2020. Вариант 2
- Демо 2020. Часть 1 и Демо 2020. Часть 2
- Задачи ЕГЭ 2020
- Реальный ЕГЭ 2019 (основная волна, 31 мая 2019 года)
- Задания из резервных дней ЕГЭ 2019 (20 июня 2019 года и 1 июля 2019 года)
- Досрочный ЕГЭ 2019 (досрочная волна, 25 марта 2019 года)
- Досрочный ЕГЭ 2019 (текстовые условия ФИПИ, вариант 101)
- Демо 2019. Часть 1 и Демо 2019. Часть 2
- Реальный ЕГЭ 2018 (Задание 30, Задание 31, Задание 32, Задание 33, Задание 34, Задание 35)
- Досрочный ЕГЭ 2018 (Часть 1, Часть 2, Текстовые услововия досрочного ЕГЭ по химии)
- Реальный ЕГЭ 2017
- Досрочный ЕГЭ 2017 (Часть 1-1, Часть 1-2 и Часть 2)
Варианты без видео-объяснения:
- Задания по темам (по номерам заданий)
- Задачи 33 реального ЕГЭ по химии всех лет (бывшее задание 34)
- Задачи 34 реального ЕГЭ по химии всех лет (бывшее задание 35)
2022
- ЕГЭ 2022, Демонстрационный вариант
- ЕГЭ 2022, Кодификатор
- ЕГЭ 2022, Спецификация
- Рекомендации от ФИПИ (анализ ошибок ЕГЭ 2021)
Материалы из группы ЕГЭ на 100 баллов
- Тренировочный вариант №1
- Тренировочный вариант №2
- Тренировочный вариант №3
- Тренировочный вариант №4
- Тренировочный вариант №5
- Тренировочный вариант №6
- Тренировочный вариант №7
Материалы из группы в контакте ЕГЭ-2022 с Химическим Котом ★ Степенин и Дацук
- Вариант 1 ЕГЭ-2022 химия с ответами
- Вариант 2 ЕГЭ-2022 химия с ответами
- Вариант 3 ЕГЭ-2022 химия с ответами
- Вариант 4 ЕГЭ-2022 химия с ответами
- Вариант 5 ЕГЭ-2022 химия с ответами
- Вариант 6 ЕГЭ-2022 химия с ответами
- Вариант 7 ЕГЭ-2022 химия с ответами
- Вариант 8 ЕГЭ-2022 химия с ответами
Материалы из группы в контакте Широкопояс. Химия ЕГЭ. Вебинары.
- Тренировочный КИМ №1
- Тренировочный КИМ №2
- Тренировочный КИМ №3
- Тренировочный КИМ №4
- Тренировочный КИМ №5
- Тренировочный КИМ №6
- Тренировочный КИМ №7
- Тренировочный КИМ №8
- Тренировочный КИМ №9
- Тренировочный КИМ №10
- Тренировочный КИМ №31
- Тренировочный КИМ №32
- Тренировочный КИМ №33
- Тренировочный КИМ №34
2021
- Реальный вариант ЕГЭ по химии 2021. Центр
- Реальный вариант ЕГЭ по химии 2021. Сибирь
- Реальный вариант ЕГЭ по химии 2021. Урал
- Реальный ЕГЭ по химии 2021. Задание 34
- Открытый вариант ЕГЭ по химии 2021 от ФИПИ (досрочная волна)
- ЕГЭ 2021, Демонстрационный вариант
- ЕГЭ 2021, Кодификатор
- ЕГЭ 2021, Спецификация
Новые варианты пробных вариантов выходят в начале каждого месяца.
- Пробный ЕГЭ по химии 2021. Вариант 1
- Пробный ЕГЭ по химии 2021. Вариант 2
- Пробный ЕГЭ по химии 2021. Вариант 3
- Пробный ЕГЭ по химии 2021. Вариант 4
- Пробный ЕГЭ по химии 2021. Вариант 5
- Пробный ЕГЭ по химии 2021. Вариант 6
- Пробный ЕГЭ по химии 2021. Вариант 7
- Пробный ЕГЭ по химии 2021. Вариант 8
- Пробный ЕГЭ по химии 2021. Вариант 9
- Пробный ЕГЭ по химии 2021. Вариант 10
Материалы из группы ЕГЭ ПО ХИМИИ НА МАКСИМУМ
- Тренировочный вариант №1
- Тренировочный вариант №2
- Тренировочный вариант №3
- Тренировочный вариант №4
- Тренировочный вариант №5
- Тренировочный вариант №6
- Тренировочный вариант №7
- Тренировочный вариант №8
- Тренировочный вариант №9
- Тренировочный вариант №10
- Тренировочный вариант №11
- Тренировочный вариант №12
- Тренировочный вариант №13
- Тренировочный вариант №14
- Тренировочный вариант №15
- Тренировочный вариант №16
- Тренировочный вариант №17
- Тренировочный вариант №18
- Тренировочный вариант №19
Материалы из группы в контакте Химия: ЕГЭ, олимпиады и школьный курс
- Вариант 1 ЕГЭ-2021 химия с ответами
- Вариант 2 ЕГЭ-2021 химия с ответами
- Вариант 3 ЕГЭ-2021 химия с ответами
- Вариант 4 ЕГЭ-2021 химия с ответами
- Вариант 5 ЕГЭ-2021 химия с ответами
- Вариант 6 ЕГЭ-2021 химия с ответами
- Вариант 7 ЕГЭ-2021 химия с ответами
- Вариант 8 ЕГЭ-2021 химия с ответами
- Вариант 9 ЕГЭ-2021 химия с ответами
- Вариант 10 ЕГЭ-2021 химия с ответами
- Вариант 11 ЕГЭ-2021 химия с ответами
- Вариант 12 ЕГЭ-2021 химия с ответами
- Вариант 13 ЕГЭ-2021 химия с ответами
- Вариант 14 ЕГЭ-2021 химия с ответами
- Вариант 15 ЕГЭ-2021 химия с ответами
- Вариант 16 ЕГЭ-2021 химия с ответами
- Вариант 17 ЕГЭ-2021 химия с ответами
- Вариант 18 ЕГЭ-2021 химия с ответами
- Вариант 19 ЕГЭ-2021 химия с ответами
- Вариант 20 ЕГЭ-2021 химия с ответами
- Вариант 21 ЕГЭ-2021 химия с ответами
- Вариант 22 ЕГЭ-2021 химия с ответами
Материалы из группы в контакте
- Тренировочный КИМ №23
- Тренировочный КИМ №24
- Тренировочный КИМ №25
- Тренировочный КИМ №26
- Тренировочный КИМ №27
- Тренировочный КИМ №28
- Тренировочный КИМ №29
- Тренировочный КИМ №30
Материалы из группы в контакте ХИМИЯ | ЕГЭ 2021 | ВЕБИУМ
- Пробный вариант 1
2020
- ЕГЭ 2020, Демонстрационный вариант
- ЕГЭ 2020, Кодификатор
- ЕГЭ 2020, Спецификация
- Новинка ЕГЭ 2020: задачи на «атомистику»
Новые варианты пробных вариантов выходят в начале каждого месяца.
- Пробный ЕГЭ по химии 2020. Вариант 1
- Пробный ЕГЭ по химии 2020. Вариант 2
- Пробный ЕГЭ по химии 2020. Вариант 3
- Пробный ЕГЭ по химии 2020. Вариант 4
- Пробный ЕГЭ по химии 2020. Вариант 5
- Пробный ЕГЭ по химии 2020. Вариант 6
- Пробный ЕГЭ по химии 2020. Вариант 7
- Пробный ЕГЭ по химии 2020. Вариант 8
- Пробный ЕГЭ по химии 2020. Вариант 9
- Пробный ЕГЭ по химии 2020. Вариант 10
Материалы из группы ЕГЭ ПО ХИМИИ НА МАКСИМУМ
- Тренировочный вариант №1
- Тренировочный вариант №2
- Тренировочный вариант №3
- Тренировочный вариант №4
- Тренировочный вариант №5
- Тренировочный вариант №6
- Тренировочный вариант №7
- Тренировочный вариант №8
- Тренировочный вариант №9
- Тренировочный вариант №10
- Тренировочный вариант №11
- Тренировочный вариант №12
- Тренировочный вариант №13
- Тренировочный вариант №14
- Тренировочный вариант №15
- Тренировочный вариант №16
- Тренировочный вариант №17
- Тренировочный вариант №18
- Тренировочный вариант №19
- Тренировочный вариант №20
- Тренировочный вариант №21
- Тренировочный вариант №22
- Тренировочный вариант №23
- Тренировочный вариант №24
- Тренировочный вариант №25
- Тренировочный вариант №26
Материалы из группы в контакте Химия: ЕГЭ, олимпиады и школьный курс
- Вариант 1 ЕГЭ-2020 химия с ответами
- Вариант 2 ЕГЭ-2020 химия с ответами
- Вариант 3 ЕГЭ-2020 химия с ответами
- Вариант 4 ЕГЭ-2020 химия с ответами
- Вариант 5 ЕГЭ-2020 химия с ответами
- Вариант 6 ЕГЭ-2020 химия с ответами
- Вариант 7 ЕГЭ-2020 химия с ответами
- Вариант 8 ЕГЭ-2020 химия с ответами
- Вариант 9 ЕГЭ-2020 химия с ответами
- Вариант 10 ЕГЭ-2020 химия с ответами
- Вариант 11 ЕГЭ-2020 химия с ответами
- Вариант 12 ЕГЭ-2020 химия с ответами
- Вариант 13 ЕГЭ-2020 химия с ответами
- Вариант 14 ЕГЭ-2020 химия с ответами
- Вариант 15 ЕГЭ-2020 химия с ответами
- Вариант 16 ЕГЭ-2020 химия с ответами
- Вариант 17 ЕГЭ-2020 химия с ответами
- Вариант 18 ЕГЭ-2020 химия с ответами
- Вариант 19 ЕГЭ-2020 химия с ответами
- Вариант 20 ЕГЭ-2020 химия с ответами
Материалы из группы в контакте Химия ЕГЭ. Вебинары. ДВИ МГУ. Наука для тебя.
- Тренировочный КИМ №1
- Тренировочный КИМ №2
- Тренировочный КИМ №3
- Тренировочный КИМ №4
- Тренировочный КИМ №5
- Тренировочный КИМ №6
- Тренировочный КИМ №7
- Тренировочный КИМ №8
- Тренировочный КИМ №9
- Тренировочный КИМ №10
- Тренировочный КИМ №11
- Тренировочный КИМ №12
- Тренировочный КИМ №13
- Тренировочный КИМ №14
- Тренировочный КИМ №15
- Тренировочный КИМ №16
- Тренировочный КИМ №17
- Тренировочный КИМ №18
- Тренировочный КИМ №19
- Тренировочный КИМ №20
- Тренировочный КИМ №21
- Тренировочный КИМ №22
- Тренировочный КИМ №24
- Тренировочный КИМ №25
Материалы из группы в контакте ХИМИЯ | ЕГЭ 2020 | ВЕБИУМ
- Пробный вариант 1
- Пробный вариант 2
- Пробный вариант 3
- Пробный вариант 4
- Пробный вариант 5
- Пробный вариант 6
- Пробный вариант 7
- Пробный вариант 8
- Пробный вариант 9
- Пробный вариант 10
- Пробный вариант 11
- Пробный вариант 12
- Пробный вариант 13
- Пробный вариант 14
- Пробный вариант 15
- Пробный вариант 16
- Пробный вариант 17
- Пробный вариант 18
- Пробный вариант 19
Книги из интернета
- ЕГЭ 2020. Химия. Типовые тестовые задания. 14 вариантов. Медведев Ю.Н.
- Химия ЕГЭ. Курс самоподготовки. Технология решения заданий. Каверина, Медведев, Молчанова и др.
2019
Развернуть/свернуть
- ЕГЭ 2019, Демонстрационный вариант (видео-объяснения каждого задания)
- ЕГЭ 2019, Кодификатор
- ЕГЭ 2019, Спецификатор
- Досрочный ЕГЭ 2019
- Досрочный ЕГЭ 2019 (текстовые условия ФИПИ, вариант 101)
Новые варианты выходят в начале каждого месяца.
- Пробный ЕГЭ по химии 2019. Вариант 1
- Пробный ЕГЭ по химии 2019. Вариант 2
- Пробный ЕГЭ по химии 2019. Вариант 3
- Пробный ЕГЭ по химии 2019. Вариант 4
- Пробный ЕГЭ по химии 2019. Вариант 5
- Пробный ЕГЭ по химии 2019. Вариант 6
- Пробный ЕГЭ по химии 2019. Вариант 7
- Пробный ЕГЭ по химии 2019. Вариант 8
- Пробный ЕГЭ по химии 2019. Вариант 9
- Пробный ЕГЭ по химии 2019. Вариант 10
Материалы из интернета
- Тренировочный вариант №1
- Тренировочный вариант №2
- Тренировочный вариант №3
- Тренировочный вариант №4
- Тренировочный вариант №5
- Тренировочный вариант №6
- Тренировочный вариант №7
- Тренировочный вариант №8
- Тренировочный вариант №9
- Тренировочный вариант №10
- Тренировочный вариант №11
- Тренировочный вариант №12
- Тренировочный вариант №13
- Тренировочный вариант №14
- Тренировочный вариант №15
- Тренировочный вариант №16
- Тренировочный вариант №17
- Тренировочный вариант №18
- Тренировочный вариант №19
- Тренировочный вариант №20
- Тренировочный вариант №21
Материалы из группы в контакте Химия: ЕГЭ, олимпиады и школьный курс
- Вариант 1 ЕГЭ-2019 химия с ответами
- Вариант 2 ЕГЭ-2019 химия с ответами
- Вариант 3 ЕГЭ-2019 химия с ответами
- Вариант 4 ЕГЭ-2019 химия с ответами
- Вариант 5 ЕГЭ-2019 химия с ответами
- Вариант 6 ЕГЭ-2019 химия с ответами
- Вариант 7 ЕГЭ-2019 химия с ответами
- Вариант 8 ЕГЭ-2019 химия с ответами
- Вариант 9 ЕГЭ-2019 химия с ответами
- Вариант 10 ЕГЭ-2019 химия с ответами
- Вариант 11 ЕГЭ-2019 химия с ответами
- Вариант 12 ЕГЭ-2019 химия с ответами
- Вариант 13 ЕГЭ-2019 химия с ответами
- Вариант 14 ЕГЭ-2019 химия с ответами
- Вариант 15 ЕГЭ-2019 химия с ответами
- Вариант 16 ЕГЭ-2019 химия с ответами
- Вариант 17 ЕГЭ-2019 химия с ответами
- Вариант 18 ЕГЭ-2019 химия с ответами
- Вариант 19 ЕГЭ-2019 химия с ответами
- Вариант 20 ЕГЭ-2019 химия с ответами
- Вариант 21 ЕГЭ-2019 химия с ответами
- Вариант 22 ЕГЭ-2019 химия с ответами
- Вариант 23 ЕГЭ-2019 химия с ответами
- Вариант 24 ЕГЭ-2019 химия с ответами
- Вариант 25 ЕГЭ-2019 химия с ответами
- Вариант 26 ЕГЭ-2019 химия с ответами
Материалы из группы в контакте Химия ЕГЭ. Вебинары. ДВИ МГУ. Наука для тебя.
- Тренировочный КИМ №1
- Тренировочный КИМ №2
- Тренировочный КИМ №3
- Тренировочный КИМ №4
- Тренировочный КИМ №5
- Тренировочный КИМ №6
- Тренировочный КИМ №7
- Тренировочный КИМ №8
- Тренировочный КИМ №9
- Тренировочный КИМ №10
Книги из интернета
- ЕГЭ 2019. Химия. Типовые тестовые задания. 14 вариантов. Медведев Ю.Н.
- ЕГЭ 2019. Химия. 10 тренировочных вариантов экзаменационных работ. Савинкина Е.В., Живейнова О.Г. (2018)
- ЕГЭ 2019. Химия. 25 вариантов. Яшкин С.Н., Яшкина Е.А. (2019)
- ЕГЭ 2019. Химия. 50 тренировочных вариантов экзаменационных работ. Савинкина Е.В., Живейнова О.Г. (2018)
- ЕГЭ 2019. Химия. Эксперт. Краткий теоретический курс. 15 типовых вариантов ЕГЭ. Медведев Ю.Н. и др. (2019)
- ЕГЭ 2019. Химия. Готовимся к итоговой аттестации. Каверина А.А., Медведев Ю.Н. и др. (2019)
- ЕГЭ 2019. Химия. Решение задач. Антошин А.Э. (2018)
- ЕГЭ 2019. Химия. Диагностические работы. (2019)
- Химия. Алгоритмы выполнения типовых заданий. Крышилович Е.В., Мостовых В.А. (2018)
- ЕГЭ. Химия. Большой справочник для подготовки к ЕГЭ. (2018)
- ЕГЭ 2019. Химия. Методические рекомендации по результатам ЕГЭ 2018г.
2018
Развернуть/свернуть
- ЕГЭ 2018, Демонстрационный вариант (видео-объяснения каждого задания)
- ЕГЭ 2018, Кодификатор
- ЕГЭ 2018, Спецификатор
- Пробный ЕГЭ 2018 по химии №1
- Пробный ЕГЭ 2018 по химии №2
- Пробный ЕГЭ 2018 по химии №3
- Пробный ЕГЭ 2018 по химии №4
- Пробный ЕГЭ 2018 по химии №5
- Пробный ЕГЭ 2018 по химии №6
- Пробный ЕГЭ 2018 по химии №7
- Пробный ЕГЭ 2018 по химии №8
- Пробный ЕГЭ 2018 по химии №9
- Пробный ЕГЭ 2018 по химии №10
- Пробный ЕГЭ 2018 по химии №11
- Пробный ЕГЭ 2018 по химии №12
- Пробный ЕГЭ 2018 по химии №13
- Пробный ЕГЭ 2018 по химии №14
- Пробный ЕГЭ 2018 по химии №15
- Пробный ЕГЭ 2018 по химии №16
- Пробный ЕГЭ 2018 по химии №17
- Пробный ЕГЭ 2018 по химии №18
- Пробные ЕГЭ 2018 по химии №19
Материалы из группы в контакте Химия: ЕГЭ, олимпиады и школьный курс
- Вариант 26 ЕГЭ-2018 химия с ответами
- Вариант 25 ЕГЭ-2018 химия с ответами
- Вариант 24 ЕГЭ-2018 химия с ответами
- Вариант 23 ЕГЭ-2018 химия с ответами
- Вариант 22 ЕГЭ-2018 химия с ответами
- Вариант 21 ЕГЭ-2018 химия с ответами
- Вариант 20 ЕГЭ-2018 химия с ответами
- Вариант 19 ЕГЭ-2018 химия с ответами
- Вариант 18 ЕГЭ-2018 химия с ответами
- Вариант 17 ЕГЭ-2018 химия с ответами
- Вариант 16 ЕГЭ-2018 химия с ответами
- Вариант 15 ЕГЭ-2018 химия с ответами
- Вариант 14 ЕГЭ-2018 химия с ответами
- Вариант 13 ЕГЭ-2018 химия с ответами
- Вариант 12 ЕГЭ-2018 химия с ответами
- Вариант 11 ЕГЭ-2018 химия с ответами
- Вариант 10 ЕГЭ-2018 химия с ответами
- Вариант 9 ЕГЭ-2018 химия с ответами
- Вариант 8 ЕГЭ-2018 химия с ответами
- Вариант 7 ЕГЭ-2018 химия с ответами
- Вариант 6 ЕГЭ-2018 химия с ответами
- Вариант 5 ЕГЭ-2018 химия с ответами
- Вариант 4 ЕГЭ-2018 химия с ответами
- Вариант 3 ЕГЭ-2018 химия с ответами
- Вариант 2 ЕГЭ-2018 химия с ответами
- Вариант 1 ЕГЭ-2018 химия с ответами
- СтатГрад: Тренировочная работа 26.10.2017 с решениями: вариант ХИ10103
- СтатГрад: Тренировочная работа 26.10.2017 с решениями: вариант ХИ10104
- СтатГрад: Тренировочная работа ноябрь 2017: вариант ХИ10201 и ХИ10202
- ЕГЭ 2018, Химия, Типовые тестовые задания, Медведев Ю.Н.
- ЕГЭ 2018, Химия, Эксперт в ЕГЭ, Медведев Ю.Н., 2018
- ЕГЭ 2018, Химия, Типовые экзаменационные варианты, 30 вариантов, Каверина А.А., 2018
2017
Развернуть/свернуть
- ЕГЭ 2017, Демонстрационный вариант
- Досрочный ЕГЭ 2017 по химии
- Анализ ЕГЭ 2017
- Пробный ЕГЭ 2017 по химии №18 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №17 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №16 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №15 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №14 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №13 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №12 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №11 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №10 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №9 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №8 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №7 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №6 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №5 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №4 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №3 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №2 с ответами и решениями
- Пробный ЕГЭ 2017 по химии №1 с ответами и решениями
- ЕГЭ, Химия, Высший балл, Самостоятельная подготовка, Каверина А.А., Добротин Д.Ю., Медведев Ю.Н., 2017
- ЕГЭ 2017, Химия, Типовые тестовые задания, Медведев Ю.Н.
2016
Развернуть/свернуть
- ЕГЭ 2016, Демонстрационный вариант.
- ЕГЭ 2016, Досрочный экзамен, Реальный вариант №101
- ЕГЭ 2016, Химия, Тренировочный вариант №1-19.
- ЕГЭ 2016. Химия. Тренировочная работа 1. СтатГрад
- ЕГЭ 2016. Химия. Тренировочная работа 2. СтатГрад
- ЕГЭ 2016. Химия. Тренировочная работа 3. СтатГрад
- ЕГЭ 2016. Химия. Тренировочная работа 4. СтатГрад
- ЕГЭ 2016. Химия. Тренировочная работа 5. СтатГрад
- ЕГЭ 2016. Краснодарский демонстрационный вариант
- ЕГЭ по химии — 2016. Основная волна (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 2 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 9 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 16 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 37 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 46 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 47 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 50 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 74 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 77 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 78 (Часть С).
- ЕГЭ по химии — 2016. Основная волна. Вариант 86 (Часть С).
- ЕГЭ 2016, Химия, Типовые тестовые задания, Медведев Ю.Н.
- ЕГЭ 2016, Химия, Эксперт в ЕГЭ, Медведев Ю.Н., Антошин А.Э., Лидин Р.А
- ЕГЭ, Химия, 50 тренировочных вариантов экзаменационных работ, Савинкина Е.В., Живейнова О.Г., 2016.
- ЕГЭ 2016, Тематический тренинг, Задания базового и повышенного уровней сложности, Доронькин В.Н., 2015.
- Химия, Новые задания ЕГЭ, Доронькин В.Н., 2016.
2015
Развернуть/свернуть
- ЕГЭ 2015, Демонстрационный вариант.
- ЕГЭ 2015, Досрочный экзамен.
- ЕГЭ-2015. Химия. Тематическая диагностическая работа 1. «Кислородсодержащие. Азотсодержащие.» 45-90 мин. Вар. 00101-00104. 09.10.2014г., критерии, спецификация
- ЕГЭ-2015. Химия. Тематическая диагностическая работа 2. «Строение веществ. Химические реакции.» 90 мин. Вар. 10303-10304. 14.11.2014г., критерии + Демо
- ЕГЭ-2015. Химия. Тренировочная работа 1. 180 мин. Вар. 10101-10102. 16.12.2014г., критерии
- ЕГЭ-2015. Химия. Тренировочная работа. Санкт-Петербург. Вар. 1-2. 06.02.2015г., с ответами
- ЕГЭ-2015. Химия. Репетиционная работа 1. 180 мин. Вар. 10401-10402. 11.02.2015г., критерии
- ЕГЭ-2015. Химия. Тренировочная работа 2. 180 мин. Вар. 10501-10504. 11.03.2015г., критерии (501-502)
- 11 класс. Химия. Краевая диагностическая работа. ( и 12кл. ВСОШ) Краснодар. Вар. 1-4. 12.03.2015г., с ответами
- ЕГЭ-2015. Химия. Тематическая диагностическая работа 3. «Металлы. Неметаллы.» 90 мин. Вар. 10603-10604. 03.04.2015г., критерии + Демо
- ЕГЭ-2015. Химия. Тренировочная работа 3. 180 мин. Вар. 10701-10702. 15.04.2015г., критерии
- ЕГЭ-2015. Химия. Репетиционная работа 2. 180 мин. Вар. 10801-10802. 12.05.2015г.
- СтатГрад: Тренировочная работа по химии 16.12.2014 Вариант ХИ10101.
- СтатГрад: Тренировочная работа по химии 16.12.2014 Вариант ХИ10102.
- СтатГрад: Репетиционная работа 11.02.2015 Вариант ХИ10401.
- СтатГрад: Репетиционная работа 11.02.2015 Вариант ХИ10402.
- СтатГрад: Тренировочная работа 11.03.2015 Вариант ХИ10501.
- СтатГрад: Тренировочная работа 11.03.2015 Вариант ХИ10502.
- Пробные варианты ЕГЭ 2015 по химии, апрель 2015
- Тренировочные варианты ЕГЭ 2015 по химии, апрель 2015
- Тренировочные варианты ЕГЭ 2015 по химии, март 2015
- Пробный ЕГЭ 2015 по химии 2 варианта, февраль 2015
- Пробный ЕГЭ 2015 по химии с ответами
- Тренировочные варианты ЕГЭ 2015 по химии (с ответами)
- ЕГЭ 2015, Химия, Сборник заданий, Оржековский П.А., Богданова Н.Н., Васюкова Е.Ю., Мещерякова Л.М., 2014.
- ЕГЭ 2015, Химия, Тематические тестовые задания, Медведев Ю.Н.
- ЕГЭ-2015, Химия, Самое полное издание типовых вариантов для подготовки к ЕГЭ, Савинкина Е.В., Живейнова О.Г.
2014
Развернуть/свернуть
- ЕГЭ 2014, Химия, Демонстрационный вариант.
- ЕГЭ 2014, Химия. Самое полное издание типовых вариантов заданий, Каверина А.А., Добротин Д.Ю., Снастина М.Г.
- ЕГЭ 2014, Химия, Досрочный этап, 3 варианта КИМ, с сайта ФЦТ.
- ЕГЭ 2014, Химия, Типовые тестовые задания, Медведев Ю.Н.
- ЕГЭ 2014, Химия, Тренировочная работа с ответами, Варианты 601-602, 21.03.2014.
- ЕГЭ 2014, Химия, Тренировочная работа с ответами, Варианты 501-502, 30.01.2014.
- ЕГЭ 2014, Химия, Тренировочная работа №1 с ответами, Варианты 101-104, 25.10.2013.
- ЕГЭ, Химия, 11 класс, Тренировочная работа, Варианты 10701-10702, 2014.
- Химия, Подготовка к ЕГЭ 2014, Диагностические работы, Богданова Н.Н., Смирнов С.С.
- Пробный ЕГЭ 2014 по химии с ответами и решениями, январь 2014
- Пробный ЕГЭ 2014 по химии с ответами и решениями, октябрь 2013
2013
Развернуть/свернуть
- ЕГЭ 2013, Химия, Демонстрационный вариант.
- ЕГЭ 2013, Химия, Основной этап, Дальний Восток.
- ЕГЭ 2013, Химия, Основной этап, Сибирь.
- ЕГЭ 2013, Химия, Основной этап, Урал.
- ЕГЭ 2013, Химия, Основной этап, Центр.
- ЕГЭ-2013. Химия. Экзамен. Основной этап. 20 вар. 11.06.2013г.
- ЕГЭ-2013. Химия. 14 вариантов КИМ (с сайта ФЦТ)
- ЕГЭ 2013, Химия, Диагностическая работа 1 (вариант №1-4)
- ЕГЭ 2013, Химия, Тренировочная работа 1 (вариант №1-4)
- ЕГЭ 2013, Химия, Тренировочная работа 2 (вариант №1-4)
- ЕГЭ 2013, Химия, Тренировочная работа 3 (вариант №1-4)
- ЕГЭ 2013, Химия, Диагностическая работа 2 (вариант №1-4) + краткая (2 варианта)
- ЕГЭ 2013, Химия, Тренировочная работа 4 (вариант №1-4)
- ЕГЭ 2013. Химия. Краевая диагностическая работа по химии за 2013 год
- ЕГЭ 2013, Химия, Самое полное издание типовых вариантов заданий, Каверина А.А., Добротин Д.Ю., Снастина М.Г.
- ЕГЭ 2013, Химия, Тематические тренировочные задания, Соколова И.А., 2012.
- ЕГЭ 2013, Химия, Типовые экзаменационные варианты, 30 вариантов, Каверина А.А., 2012.
2012
Развернуть/свернуть
- ЕГЭ 2012, Химия, Демонстрационный вариант.
- ЕГЭ 2012, Химия, Диагностическая работа
- ЕГЭ 2012, Химия, Диагностическая работа 1 (вариант №1-2)
- ЕГЭ 2012, Химия, Диагностическая работа 2 (вариант №3-4)
- ЕГЭ 2012, Химия, Тренировочная работа 1
- ЕГЭ 2012, Химия, Тренировочная работа 2
- ЕГЭ 2012, Химия, Тренировочная работа 3
- ЕГЭ 2012, Химия, Тренировочная работа 4
- ЕГЭ 2012, Химия, Краевая диагностическая работа
- ЕГЭ 2012, Химия, Типовые тестовые задания, Медведев Ю.Н., 2012.
- ЕГЭ 2012, Химия, Типовые экзаменационные варианты, 30 вариантов, Каверина А.А.
- ЕГЭ 2012. Химия. Самое полное издание типовых вариантов.
- Химия, Диагностические работы в формате ЕГЭ, Еремин В.В., Дроздов А.А., 2012.
2011
Развернуть/свернуть
- ЕГЭ 2011. Химия. Демонстрационный вариант 2011
- ЕГЭ 2011, Химия, Основной этап (8 вариантов)
- ЕГЭ 2011, Химия, Основной этап. Реальные фото с экзамена
- ЕГЭ 2011, Химия, Диагностическая работа 1 (вариант №1-2)
- ЕГЭ 2011, Химия, Диагностическая работа 2 (вариант №1-2)
- ЕГЭ 2011, Химия, Тренировочная работа 1 (вариант №1-2)
- ЕГЭ 2011, Химия, Тренировочная работа 2 (вариант №1-2)
- ЕГЭ 2011, Химия, Тренировочная работа 3 (вариант №1-2)
- ЕГЭ 2011, Химия, Тренировочная работа 4 (вариант №1-2)
- ЕГЭ 2011, Химия, Краевая тренировочная работа 1 (вариант №1-4)
- ЕГЭ 2011, Химия, Пробный вариант
- ЕГЭ 2011, Химия, Самое полное издание типовых вариантов заданий, Корощенко А.С., Каверина А.А., Добротин Д.Ю.
- ЕГЭ 2011. Химия. Типовые тестовые задания. Медведев Ю.Н. 2011
2010
Развернуть/свернуть
- ЕГЭ 2010. Химия. Демонстрационный вариант.
- ЕГЭ 2010, Химия, Реальный Вариант №1
- ЕГЭ 2010, Химия, Реальный Вариант №2
- ЕГЭ 2010, Химия, Реальный Вариант №3
- ЕГЭ 2010, Химия, Реальный Вариант №4
- ЕГЭ 2010, Химия, Реальный Вариант №5
- ЕГЭ 2010, Химия, Реальный Вариант №121
- ЕГЭ 2010, Химия, Реальный Вариант №128
- ЕГЭ 2010, Химия, Реальный Вариант №133
- ЕГЭ 2010, Химия, Досрочный Вариант №1
- ЕГЭ 2010, Химия, Досрочный Вариант №2
- ЕГЭ 2010, Химия, Досрочный Вариант №3
- ЕГЭ 2010, Химия, Диагностическая работа 1 (вариант № 1-2)
- ЕГЭ 2010, Химия, Диагностическая работа 2 (вариант № 1-2)
- ЕГЭ 2010, Химия, Краевая диагностическая работа 1 (вариант № 1-4)
- ЕГЭ 2010, Химия, Тренировочная работа 1
- ЕГЭ 2010, Химия, Тренировочная работа 2
- ЕГЭ 2010, Химия, Тренировочная работа 4
- ЕГЭ 2010, Химия, Тренировочная работа 5
- ЕГЭ 2010, Химия, Тренировочная работа 6
- ЕГЭ-2010 — Химия — самые новые реальные задания. Корощенко А.С., Снастина М.Г.
- Самое полное издание типовых вариантов реальных заданий ЕГЭ 2010 — Химия.
2009
Развернуть/свернуть
- ЕГЭ, Химия, Демонстрационный вариант, 2009
- ЕГЭ 2009, Химия, Реальный Вариант (37 вариантов)
- ЕГЭ 2009, Химия, Репетиционный экзамен
- ЕГЭ 2009, Химия, Тренировочная работа 1
- ЕГЭ 2009, Химия, Тренировочная работа 2
- ЕГЭ 2009, Химия, Тренировочная работа 3
- ЕГЭ 2009 — Химия — Сборник экзаменационных заданий. Каверина А.А., Медведев Ю.Н., Добротин Д.Ю.
- ЕГЭ-2009 — Химия — Самые новые реальные задания. Корощенко А.С., Снастина М.Г.
- Самое полное издание типовых вариантов реальных заданий — ЕГЭ 2009 — Химия. Корощенко А.С., Снастина М.Г.
2008
- ЕГЭ 2008, Химия, Демонстрационный вариант
- ЕГЭ 2008, Химия, Реальный Вариант (35 вариантов)ЕГЭ 2008. Химия. Самое полное издание реальных заданий. Корощенко А.С., Снастина М.Г.
2007
- ЕГЭ 2007, Химия, Демонстрационный вариант
2006
- ЕГЭ 2006, Химия, Демонстрационный вариант
- ЕГЭ 2006, Химия, Реальные варианты (29 вариантов)
2005
- ЕГЭ 2005, Химия, Демонстрационный вариант
- ЕГЭ 2005, Химия, Реальный вариант
2004
- ЕГЭ 2004, Химия, Демонстрационный вариант
2003
- ЕГЭ 2003, Химия. Реальный вариант
2002
- ЕГЭ 2002, Химия, Демонстрационный вариант
- ЕГЭ 2002, Химия. Реальный вариант
Часть материалов, которые представлены на этой странице, скачаны из интернтета. Все они находятся в свободном доступе и на каждом задании указаны ссылки на авторов. По сему мы не претендуем на авторство. Всё это сделано для удобства учащихся, которые готовятся к ЕГЭ.
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ по темам (номерам заданий) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку



 Азот на ЕГЭ
Азот на ЕГЭ