Задание №1 ЕГЭ по химии
Описание задания
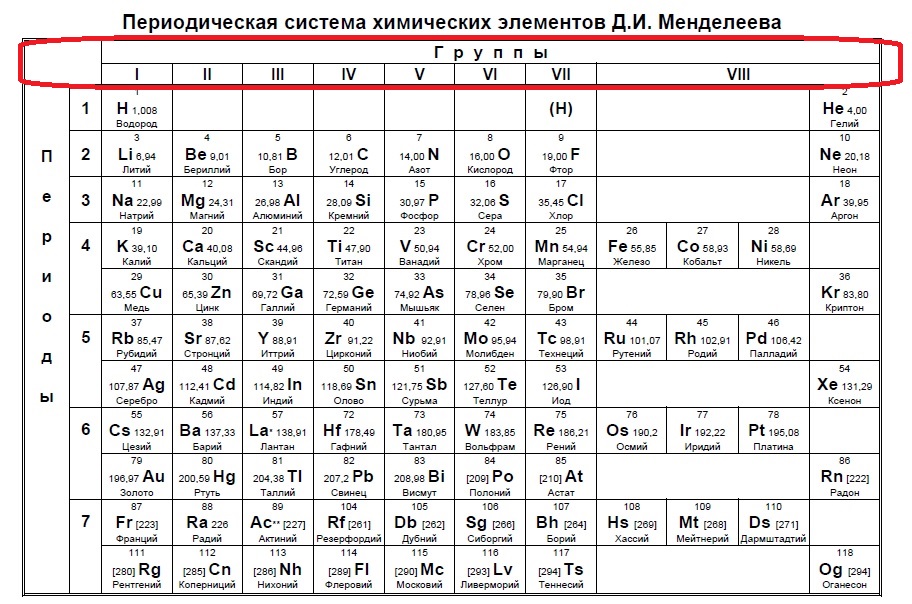
В Задании №1 нам необходимо уметь хорошо пользоваться таблицей Менделеева. Первое задание — это поиск атома или иона с заданной конфигурацией электронов, обычно это количество электронов на внешнем уровне (соответствует номеру группы).
Тематика заданий: электронная конфигурация атомов
Бал: 1
Сложность задания: ♦◊◊
Примерное время выполнения: 1 мин.
Разбор типовых вариантов заданий №1 ЕГЭ по химии
Вариант 1ЕХ1
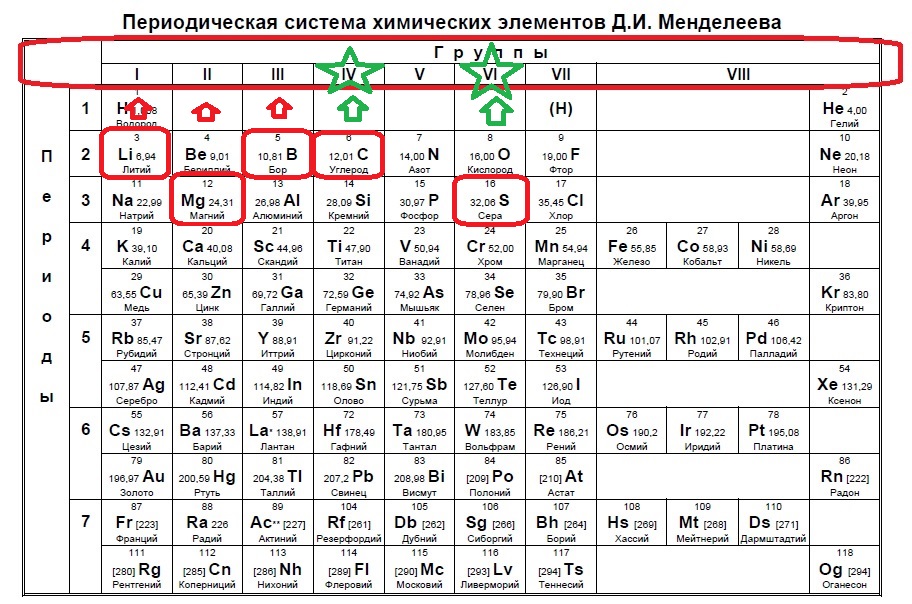
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне пять электронов.
P
N
S
Al
O
Данный пример — типичный вариант первого задания — необходимо определить количество электронов на внешнем уровне. Вспоминаем, что на количество электронов на внешнем уровне указывает номер ГРУППЫ:
Напомню, что нам важно обращать внимание на то, в главной или побочной группе находится элемент. К сожалению, в таблице, которая дана на ЕГЭ нет деления на главные или побочные группы (какие-то элементы пишут правее, какие-то левее, но это не деление на главные и побочные группы), данная таблица не удобна, однако, по правилам можно пользоваться только ей. Обсуждать недостатки данной таблицы мы не будем, скажем лишь, что в условиях задания представлены всегда элементы главных групп, поэтому данный вопрос отпадает сам собой на экзамене (но нет гарантий, что не могут дать определить количество внешних электронов у кобальта, например, по номеру группы в данной таблице это не определишь).
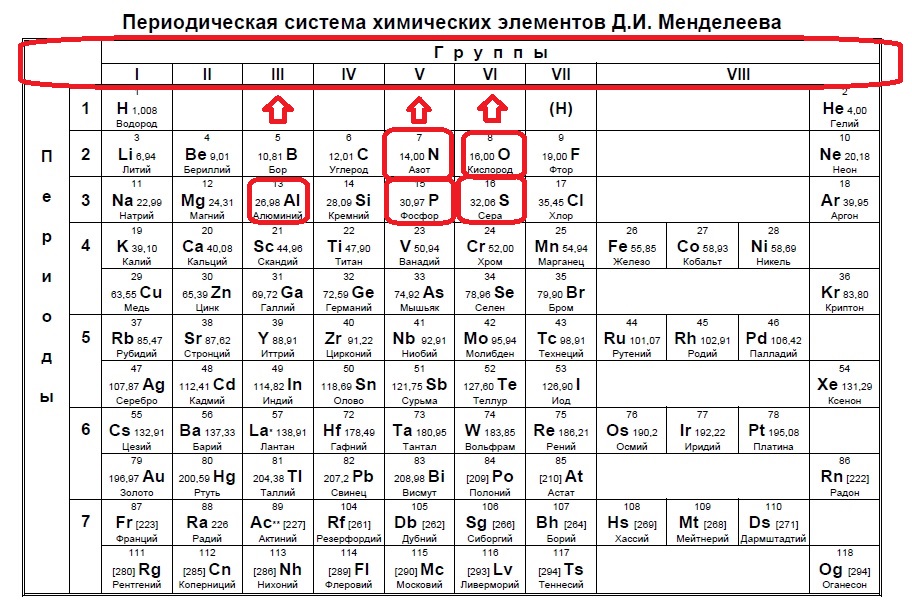
Итак, находим наши пять элементов из условия:
Определяем номер группы — у алюминия 3 группа, у азота и фосфора — пятая, у кислорода и серы — шестая.
В условии нас спрашивают про пять электронов — значит выбираем элементы из пятой группы — азот и фосфор!
Ответ: 12
Вариант 1ЕХ2
Определите, двум атомам каких из указанных элементов до завершения внешнего уровня не хватает шести электронов.
Ba
At
Bi
Mg
Cs
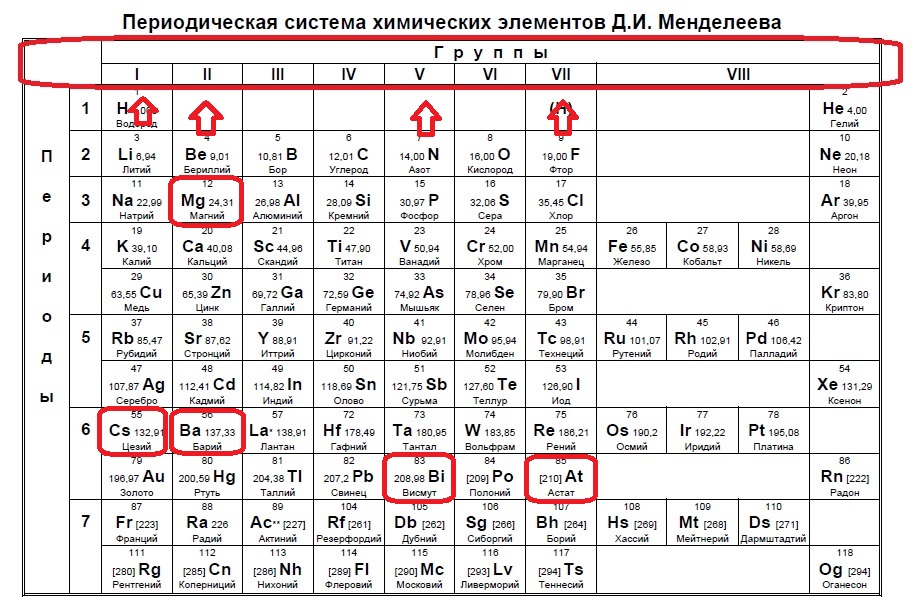
Данное задание немного другого типа, в нем необходимо определить элементы, которым не хватает какого-то количества электронов до завершения внешнего уровня. В этом случае наш алгоритм прост: мы знаем, что на внешнем уровне должно быть 8 электронов (2 и 3 период, или главные группы 4,5,6.. — в заданиях в основном фигурируют именно эти элементы), а значит вычитаем из 8 заданное число — в нашем случае 6: 8-6=2. Значит, в нашем элементе должно быть два электрона на внешнем уровне и, следовательно, расположен он во второй группе. Определяем группы элементов из условия:
В данном случае элементы второй группы — магний и барий.
Ответ: 14
Вариант 1ЕХ3
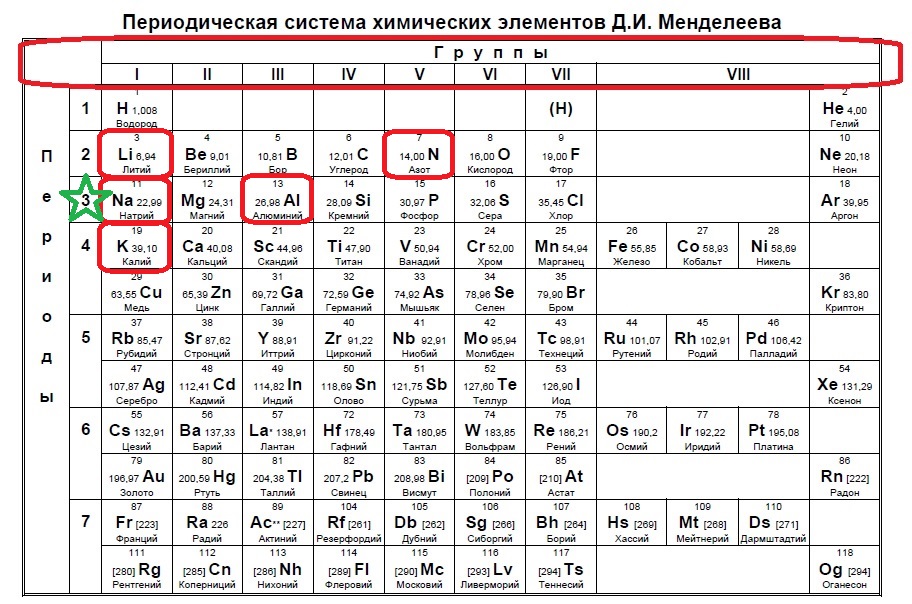
Определите, атомы каких двух из указанных в ряду элементов в основном состоянии содержат один неспаренный электрон.
S
Na
Al
Si
Mg
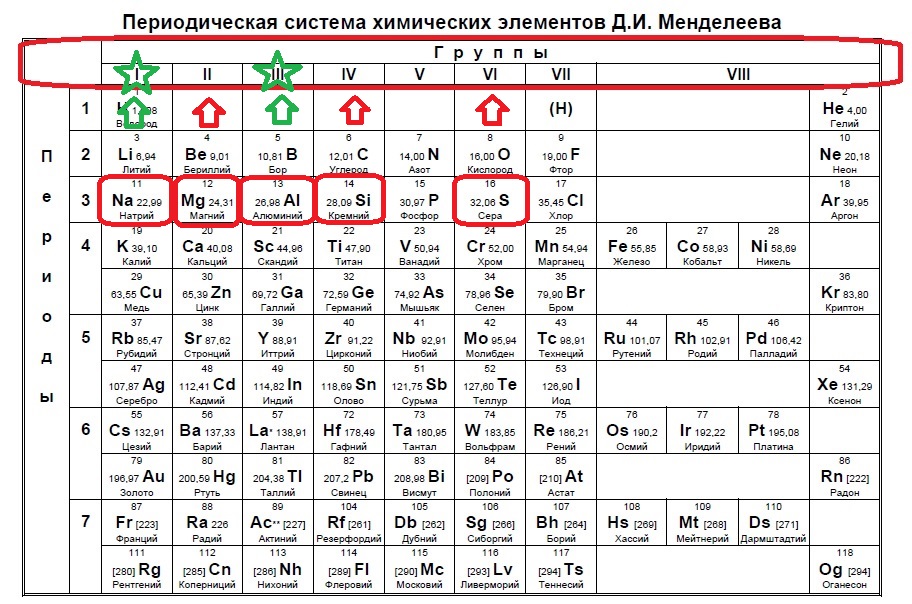
Следующий вид задания на поиск элементов с неспаренным электроном. Тут все достаточно просто. Так как электроны у нас в орбиталях всегда располагаются по парам (если помните, то есть квадратик, в котором мы рисуем стрелочку вверх и низ), то логично, что неспаренный электрон образуется, когда количество электронов на внешнем уровне нечетно, то есть в элемент должен быть расположен в нечетной группе, а именно 1,3,5,7. Определяем группы указанных нам элементов:
Итак, натрий в первой группе, магний во второй, алюминий в третьей, кремний в четвертой, а сера в шестой.
Выбираем элементы в нечетных группах — это натрий и алюминий!
Ответ: 23
Вариант 1ЕХ4
Определите, атомы каких двух из указанных в ряду элементов в основном состоянии содержат два неспаренных электрона.
S
Mg
C
B
Li
В данном задании нужно найти два неспаренных электрона. Данное распределение можно найти, начиная с p-подуровня, а именно два неспаренных электрона образуются в четвертой группе, так как на s -подуровне два электрона + 2 должно быть на p-подуровне, и в шестой группе, где 2s+2p(спаренные)+2p(неспаренные) (так как в p-подуровне три орбитали по два электрона на каждой). Таким образом нужно найти элементы четвертой группы или шестой:
В нашем случае это углерод и сера.
Ответ: 13
Вариант 1ЕХ5
Определите, какие два из указанных элементов образуют устойчивый положительный ион, содержащий 10 электронов.
Na
K
N
Li
Al
В данном варианте задания речь идет уже об ионе, причем положительном, который содержит 10 электронов. В такого вида заданиях необходимо определить, сколько заполнено уровней у иона в зависимости от количества электронов. В нашем случае 10 электронов — это полностью заполненные первый (2) и второй (8) уровни (или периоды в таблице). Так мы говорим о положительном ионе — значит элемент потерял электроны, но у него их было больше чем 10, а значит, он расположен в третьем периоде. Ищем такие элементы:
Нам подходят натрий и алюминий.
Ответ: 15
Вариант 1ЕХ6
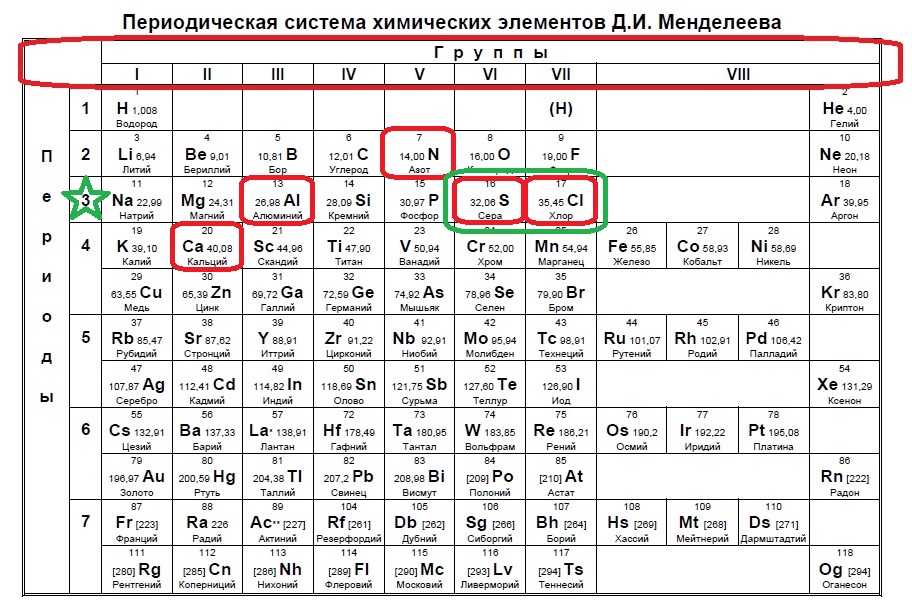
Определите, какие из указанных элементов образуют устойчивый отрицательный ион, содержащий 18 электронов.
N
Al
S
Cl
Ca
Отрицательный ион получается путем добавления электронов к атому. 18 электронов — это полностью заполненный третий уровень или период, значит, наши элементы расположены именно в нем (в отличии от предыдущего задания, где мы искали в следующем периоде, так как ион положительный). Смотрим на предоставленные в условии элементы:
В данном случае в третий период попали алюминий, сера и хлор. Алюминий не может принять электроны до 18, так как является металлом и отдает электроны. Наиболее типичные элементы-любители электронов расположены правее. Это сера и хлор для данного задания.
Ответ: 34
Вариант 1ЕХ7
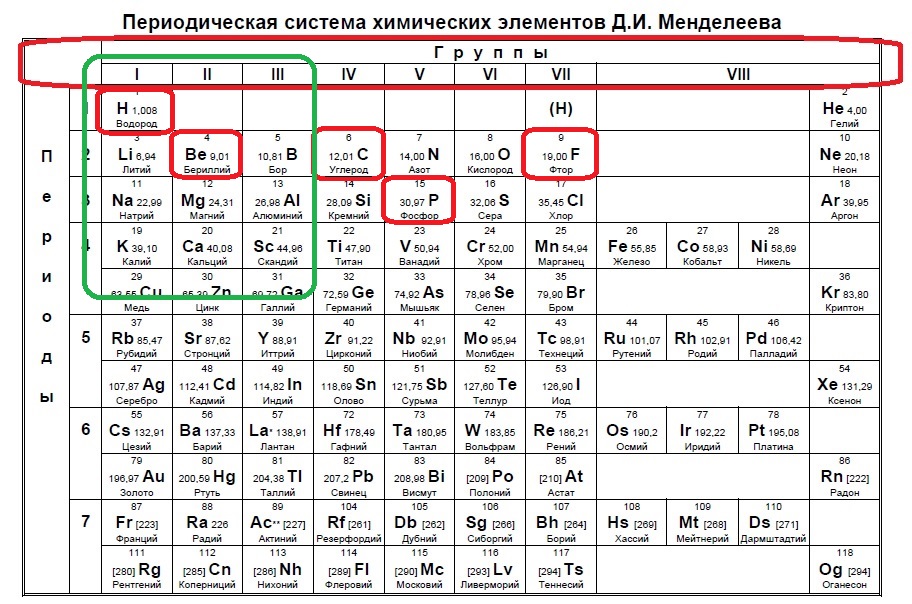
Определите, какие из указанных элементов на внешнем уровне содержат больше s-электронов, чем p-электронов (в основном состоянии).
H
C
F
Be
P
Такие виды заданий часто встречаются в тренировочных вариантах, нужно либо определить кого меньше, когда равно или кого больше. Разберем для наглядности данный пример. s-электронов всего два, значит p-электронов должно быть 1, чтобы было меньше. В сумме у элемента на внешнем уровне получается максимум 3 электрона (но может быть и ноль p-электронов и один или два s!), а значит он в третьей, второй или первой группе.
Нам подходит водород и бериллий.
Ответ: 14.
Остальные задания очень похожи на разобранные, поэтому вы их точно сможете решить, разобравшись с выше представленными решениями.
За это задание ты можешь получить 1 балл. На решение дается около 3 минут. Уровень сложности: базовый.
Средний процент выполнения: 79.2%
Ответом к заданию 1 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Задача 1
1) N 2) S 3) P 4) Se 5) As
Определите, атомы каких из указанных в ряду элементов имеют в возбуждённом состоянии электронную конфигурацию внешнего энергетического уровня ns1np3nd1. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация ns1np3nd1 в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 5 электронов, значит нужны элементы из пятой группы главной подгруппы, таких три: азот, фосфор и мышьяк. Однако атом азота не может переходить в возбужденное состояние, так как на втором энергетическом уровне нет d — подуровня, следовательно, ответ: фосфор и мышьяк.
Ответ: 35
Задача 2
1) Te 2) I 3) O 4) S 5) Sr
Определите, анионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 5s25p6. Запишите в поле ответа номера выбранных элементов.
Решение
Анионы образуются из нейтральных атомов неметаллов при присоединении электронов:
$Э^0 + nē = Э^{n–}$
Электронную конфигурацию внешнего энергетического уровня $5s^{2}5p^{6}$ имеет ксенон Xe, который находится в главной подгруппе VIII группы пятого периода, следовательно, анионы с такой электронной конфигурацией могут образовывать атомы неметаллов, находящихся в пятом периоде, т. е. теллур (ответ — 1) и йод (ответ — 2).
Вывод: правильные ответы — 1, 2.
Ответ: 12
Задача 3
1) Al 2) S 3) P 4) Cr 5) Si
Определите, атомы каких из указанных в ряду элементов в основном состоянии во внешнем слое содержат один неспаренный электрон. Запишите в поле ответа номера выбранных элементов.
Решение
Здесь лучше всего расписать конфигурации атомов, но можно и запомнить, что 1 неспаренный электрон на внешнем уровне имеют атомы элементов 1,3 и 7 групп или атомы элементы с провалом электрона. В 3 группе находится алюминий (3s2 3p1), а у хрома имеется провал электрона (3d5 4s1)
Ответ: 14
Задача 4
1) Mg 2) Bi 3) Ba 4) Sr 5) Al
Определите, катионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 3s0. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $3s^0$ описывает строение внешнего энергетического уровня, следовательно, элемент имеет три энергетических уровня, то есть находится в третьем периоде. Из предложенных элементов в третьем периоде находятся магний(Mg) и алюминий(Al). Обрати внимание, что речь идет про катионы!
Ответ: 15
Задача 5
1) I 2) N 3) Br 4) P 5) Cl
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np3. Запишите в поле ответа номера выбранных элементов.
Решение
Конфигурация внешнего энергетического уровня $ns^{2}np^{3}$ означает, что на внешнем энергетическом уровне атома находится 5 электронов, следовательно, это атом элемента, стоящего в главной подгруппе V группы таблицы Менделеева. Из предложенных элементов в главной подгруппе V группы находятся N и P.
Ответ: 24
Задача 6
1) Bi 2) N 3) Br 4) P 5) Cl
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np5. Запишите в поле ответа номера выбранных элементов.
Решение
Электронную конфигурацию $ns^{2}np^{5}$ имеют элементы, которые находятся в 7 группе главной подгруппы, такими элементами являются бром и хлор.
Ответ: 35
Задача 7
1) K 2) S 3) Na 4) Si 5) Se
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np4. Запишите в поле ответа номера выбранных элементов.
Решение
Конфигурация внешнего энергетического уровня $ns^{2}np^{4}$ означает, что на внешнем энергетическом уровне атома находится 6 электронов, а заполнение только s и p подуровней указывает на элементы главной подгруппы. Следовательно, это атомы элементов, стоящих в главной подгруппе VI группы таблицы Менделеева. Из предложенных элементов в главной подгруппе VI группы находятся S и Se.
Ответ: 25
Задача 8
1) S 2) Na 3) He 4) Cl 5) Se
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np4. Запишите в поле ответа номера выбранных элементов.
Решение
Электронную конфигурацию $ns^{2}np^{4}$ имеют элементы, которые находятся в 6 группе главной подгруппы, такими элементами являются сера и селен.
Ответ: 15
Задача 9
1) Mg 2) Al 3) Sb 4) N 5) Bi
Определите, катионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 3s0. Запишите в поле ответа номера выбранных элементов.
Решение
Конфигурация внешнего энергетического уровня КАТИОНА $3s^0$ означает, что данный элемент, образующий такой катион, имеет три энергетических уровня, следовательно, в таблице Менделеева находится в III периоде. Из представленных элементов в III периоде находятся Mg и Al.
Ответ: 12
Задача 10
1) Cu 2) Te 3) Se 4) Ag 5) O
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns1(n–1)d10. Запишите в поле ответа номера выбранных элементов.
Решение
Элементы с такой конфигурацией должны находиться в побочной подгруппе, поскольку заполняется d подуровень ( произошел перескок электрона в связи с устойчивостью полностью заполненного d подуровня), поскольку внешних электронов 1, то группа первая. Ищем элементы I группы побочной подгруппы.
Ответ: 14
Задача 11
1) Ti 2) Cl 3) Zr 4) I 5) F
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию энергетического уровня ns2(n–1)d2. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $ns^{2}(n–1)d^2$ указывает на то, что перед нами d-элемент, а значит, находится в побочной подгруппе. Галогены Cl, I и F находятся в главной подгруппе VII группы, а титан Ti и цирконий Zr — в побочной подгруппе IV группы, имеют 2 электрона на внешнем энергетическом слое.
Ответ: 13
Задача 12
1) S 2) K 3) O 4) Te 5) Na
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns1. Запишите в поле ответа номера выбранных элементов.
Решение
Электронную конфигурацию внешнего энергетического уровня $ns^1$ имеют элементы главной подгруппы I группы. Из представленных к ним относятся калий К и натрий Na.
Ответ: 25
Задача 13
1) N 2) S 3) P 4) Se 5) As
Определите, атомы каких из указанных в ряду элементов имеют в возбуждённом состоянии электронную конфигурацию внешнего энергетического уровня ns1np3nd1. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация внешнего энергетического уровня $ns^1np^3nd^1$ означает, что на нём находится 5 электронов (в возбуждённом состоянии количество электронов не отличается от основного состояния), следовательно, элемент находится в V группе Периодической таблицы. Из предложенных элементов в главной подгруппе V группы находятся N, P и As, но азот не имеет d- подуровня, поэтому не может иметь такую конфигурацию внешнего энергетического уровня.
Ответ: 35
Задача 14
1) Mg 2) Cl 3) S 4) Br 5) Ca
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np5. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация внешнего энергетического уровня $ns^{2}np^{5}$ свидетельствует о наличии на внешнем энергетическом слое 7 электронов, следовательно, искать нужно элементы VII группы, к ним относятся Cl и Br.
Ответ: 24
Задача 15
1) Te 2) Be 3) I 4) Ba 5) Sr
Определите, катионы каких из указанных в ряду элементов могут иметь электронную конфигурацию внешнего энергетического уровня 5s2. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $5s^2$ у катиона(!) показывает, что на внешнем слое было как минимум 3 электрона (часть от отдал, чтобы стать катионом), при этом внешний слой – пятый. Поэтому из всех элементов выбираем те, которые находятся в 5 периоде и в группах от третьей и дальше. Таких элементов два: теллур и иод, которые в степени окисления +4 и +5, соответственно, будут иметь конфигурацию $5s^2$.
Ответ: 13
Задача 16
1) Li 2) Se 3) K 4) S 5) Cs
Определите, атомы каких из указанных в ряду элементов в возбуждённом состоянии могут иметь электронную конфигурацию ns2np3nd1. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $ns^{2}np^{3}nd^{1}$ говорит о наличии шести электронов на последнем энергетическом слое атома. В возбуждённом состоянии электроны переходят на другой энергетический подуровень, но количество их не меняется, поэтому оно равно номеру группы, следовательно, подходят элементы шестой группы — селен и сера.
Ответ: 24
Задача 17
1) O 2) S 3) N 4) Te 5) P
Определите, анионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 3s23p6. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $3s^{2}3p^6$ описывает строение внешнего энергетического уровня, следовательно, элемент имеет 3 энергетических уровня, то есть находится в третьем периоде. Из предложенных элементов в третьем периоде находятся фосфор (P) и сера (S). Фосфор принимает 3 электрона, чтобы образовать анион P$^{3-}$, а сера принимает 2 электрона, чтобы образовать анион S$^{2-}$
Ответ: 25
Задача 18
1) Ga 2) S 3) B 4) In 5) Se
Определите, атомы каких из указанных в ряду элементов в возбуждённом состоянии имеют электронную конфигурацию внешнего энергетического уровня ns1np3nd2. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация $ns^1np^3nd^2$ в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 6 электронов, значит нужны элементы из шестой группы главной подгруппы, таких два: сера и селен.
Ответ: 25
Задача 19
1) As 2) Cr 3) Na 4) V 5) Sc
Определите, атомы каких из указанных в ряду элементов имеют 1 неспаренный электрон во внешнем слое в основном состоянии. Запишите в поле ответа номера выбранных элементов.
Решение
Для определения количества неспаренных электронов на внешнем слое нужно представить электронную конфигурацию атома. Атом натрия находится в 3 периоде, поэтому имеет 3 слоя. Всего он имеет 11 электронов, поэтому на последнем слое атом натрия имеет один неспаренный электрон. Атом хрома находится в 4 периоде, он имеет 4 слоя, 3d подуровень заполняется после 4s, но у хрома происходит провал электрона, один электрон с 4s падает на 3d, чтобы быть более энергетически устойчивым, так как в таком случае атом не будет иметь пустых орбиталей на 3d. У мышьяка 3 неспаренных электрона на внешнем слое. У скандия и ванадия их нет.
Ответ: 23
Вопрос №1 «Строение атома»
Подготовка к ЕГЭ, алгоритмы выполнения
1 тип заданий
Определите, атомы каких из указанных элементов в основном состоянии содержат одинаковое число электронов на внешнем уровне
Необходимая теория:
Основное состояние атома – это наиболее устойчивое состояние атома, в котором энергия его электронной оболочки минимальная (обычное состояние)
Электроны на внешнем уровне – определяем по номеру группы (для элементов главных подгрупп), равно 2 ( для элементов побочных подгрупп, кроме Cr, Cu,Mo,Ru,Rh,Pd) Cr, Cu,Mo,Ru,Rh,Pd (для них =1) — у атомов этих элементов происходит «провал» электронов внешнего уровня с 4 s на 3 d подуровень, что объясняется большей энергетической устойчивостью, образующейся конфигурации.
Определите , атомы каких из указанных элементов в основном состоянии содержат одинаковое число электронов на внешнем уровне 1) Na; 2)Cl; 3)Si; 4)Mn; 5)Cr
Ответ 1,5
Na – элемент 1 группы главной подгруппы; Cr – элемент побочной подгруппы с провалом электрона.
2 тип заданий
Определите, атомы каких из указанных элементов в основном состоянии во внешнем слое содержат один неспаренный электрон
Необходимая теория: можно составлять электронно-графические формулы и считать.
Можно запомнить и использовать информацию, что у элементов главных подгрупп 1,3,7групп – 1 неспаренный электрон; у элементов 4,6 групп – 2 неспаренных электрона; у элементов 5 группы – 3 неспаренных электрона; у элементов 2 и 8 групп неспаренных электронов нет.
У элементов побочных подгрупп : у всех 2 спаренных электрона, кроме Cr, Cu,Mo,Ru,Rh по причине «провала» электронов.
Определите, атомы каких из указанных элементов в основном состоянии во внешнем слое содержат один неспаренный электрон : 1) Li; 2)C; 3)Cu; 4) Mn; 5)O
Ответ: 1,3
Li – элемент 1 группы главной подгруппы; Cu – элемент побочной подгруппы с провалом электрона.
3 тип задания
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns 2
Необходимая теория : конфигурации основного состояния
ns 1
Элементы 1 группы
ns 2
Элементы 2 группы и He
ns 2 n p 1
ns 2 n p 2
Элементы 3 группы
Элементы 4 группы
ns 2 n p 3
Элементы 5 группы
ns 2 n p 4
Элементы 6 группы
ns 2 n p 5
Элементы 7 группы
ns 2 n p 6
Элементы 8 группы
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns 1 : 1 ) Cs; 2)He; 3) Li; 4) Ar; 5)Ne
Ответ: 1,3
Li и Cs – элементы первой группы
Второй вариант заданий данного типа
Определите, атомы каких из указанных в ряду элементов в возбужденном состоянии имеют электронную конфигурацию внешнего энергетического уровня ns 1 n p 3
1 ) Al; 2)B; 3) C; 4) N; 5)Si
Ответ: 3,5
Необходимая теория: возбужденное состояние могут приобретать атомы элементов, которые в своем строении имеют «вакантные» пустые электронные орбитали
4 тип заданий
Определите, атомы каких из указанных элементов в основном состоянии содержат одинаковое число валентных электронов
Необходимая теория: количество валентных электронов (максимальная валентность) равна номеру групп в таблице Менделеева.
Валентность определяется:
- Числом неспаренных электронов;
- Числом вакантных орбиталей на валентном слое атомов элемента.
Определите, атомы каких из указанных элементов в основном состоянии содержат одинаковое число валентных электронов 1) Na; 2) Cl; 3) Si; 4) Mn; 5)Cr
Ответ: 2,4 – это элементы 7 группы
5 тип заданий
либо s – электроны и т.д.
Необходимая теория:
S
У элементов 1 и 2 группы, а также у гелия
P
У элементов 3,4,5,6,7,8 групп, главных подгрупп
d
У элементов побочных подгрупп, предыдущего энергетического уровня, начиная с 3 энергетического уровня
f
У элементов побочных подгрупп, предпредыдущего энергетического уровня начиная с 4 энергетического уровня
Встречающиеся задания
- По изменениям в атоме
Необходимая теория и алгоритм выполнения
п1. Для подсчета количества электронов в частицах пользуемся таблицей Менделеева. Находим по порядковому номеру общее количество электронов в атоме и, если частица превращена в анион , к общему количеству электронов атома прибавляем число заряда с минусом ; если частица превращена в катион , от общего количества электронов атома отнимаем число заряда с плюсом.
п2.Если в задании дана конфигурация, тогда общее количество электронов считаем, складывая степенные значения в конфигурации, затем выполняем так же,
как в п. 1.
По строению атома, изотопам или ядра атома
Задание №1 ЕГЭ по химии
Описание задания
В Задании №1 нам необходимо уметь хорошо пользоваться таблицей Менделеева. Первое задание —
это поиск атома или иона с заданной конфигурацией электронов, обычно это количество электронов
на внешнем уровне (соответствует номеру группы).
Тематика заданий: электронная конфигурация атомов
Бал: 1
Сложность задания: ♦◊◊
Примерное время выполнения: 1 мин.
Разбор типовых вариантов заданий №1 ЕГЭ по химии
Вариант 1ЕХ1
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом
уровне пять электронов.
1. P
2. N
3. S
4. Al
5. O
Данный пример — типичный вариант первого задания — необходимо определить количество
электронов на внешнем уровне. Вспоминаем, что на количество электронов на внешнем уровне
указывает номер ГРУППЫ:
Напомню, что нам важно обращать внимание на то, в главной или побочной группе находится
элемент. К сожалению, в таблице, которая дана на ЕГЭ нет деления на главные или побочные группы
(какие—то элементы пишут правее, какие—то левее, но это не деление на главные и побочные группы),
данная таблица не удобна, однако, по правилам можно пользоваться только ей. Обсуждать
недостатки данной таблицы мы не будем, скажем лишь, что в условиях задания представлены всегда
элементы главных групп, поэтому данный вопрос отпадает сам собой на экзамене (но нет гарантий,
что не могут дать определить количество внешних электронов у кобальта, например, по номеру
группы в данной таблице это не определишь).
Итак, находим наши пять элементов из условия:
Определяем номер группы — у алюминия 3 группа, у азота и фосфора — пятая, у кислорода и серы
— шестая.
В условии нас спрашивают про пять электронов — значит выбираем элементы из пятой группы —
азот и фосфор!
Ответ: 12
Вариант 1ЕХ2
Определите, двум атомам каких из указанных элементов до завершения внешнего уровня не хватает
шести электронов.
1. Ba
2. At
3. Bi
4. Mg
5. Cs
Данное задание немного другого типа, в нем необходимо определить элементы, которым не хватает
какого—то количества электронов до завершения внешнего уровня. В этом случае наш алгоритм
прост: мы знаем, что на внешнем уровне должно быть 8 электронов (2 и 3 период, или главные группы
4,5,6.. — в заданиях в основном фигурируют именно эти элементы), а значит вычитаем из 8 заданное
число — в нашем случае 6: 8—6=2. Значит, в нашем элементе должно быть два электрона на внешнем
уровне и, следовательно, расположен он во второй группе. Определяем группы элементов из условия:
В данном случае элементы второй группы — магний и барий.
Ответ: 14
Вариант 1ЕХ3
Определите, атомы каких двух из указанных в ряду элементов в основном состоянии содержат один
неспаренный электрон.
1. S
2. Na
3. Al
4. Si
5. Mg
Следующий вид задания на поиск элементов с неспаренным электроном. Тут все достаточно просто.
Так как электроны у нас в орбиталях всегда располагаются по парам (если помните, то есть квадратик,
в котором мы рисуем стрелочку вверх и низ), то логично, что неспаренный электрон образуется,
когда количество электронов на внешнем уровне нечетно, то есть в элемент должен быть
расположен в нечетной группе, а именно 1,3,5,7. Определяем группы указанных нам элементов:
Итак, натрий в первой группе, магний во второй, алюминий в третьей, кремний в четвертой, а сера в
шестой.
Выбираем элементы в нечетных группах — это натрий и алюминий!
Ответ: 23
Вариант 1ЕХ4
Определите, атомы каких двух из указанных в ряду элементов в основном состоянии содержат два
неспаренных электрона.
1. S
2. Mg
3. C
4. B
5. Li
В данном задании нужно найти два неспаренных электрона. Данное распределение можно найти,
начиная с p-подуровня, а именно два неспаренных электрона образуются в четвертой группе, так как
на s —подуровне два электрона + 2 должно быть на p—подуровне, и в шестой группе, где
2s+2p(спаренные)+2p(неспаренные) (так как в p—подуровне три орбитали по два электрона на
каждой). Таким образом нужно найти элементы четвертой группы или шестой:
В нашем случае это углерод и сера.
Ответ: 13
Вариант 1ЕХ5
Определите, какие два из указанных элементов образуют устойчивый положительный ион,
содержащий 10 электронов.
1. Na
2. K
3. N
4. Li
5. Al
В данном варианте задания речь идет уже об ионе, причем положительном, который содержит 10
электронов. В такого вида заданиях необходимо определить, сколько заполнено уровней у иона в
зависимости от количества электронов. В нашем случае 10 электронов — это полностью заполненные
первый (2) и второй (8) уровни (или периоды в таблице). Так мы говорим о положительном ионе —
значит элемент потерял электроны, но у него их было больше чем 10, а значит, он расположен в
третьем периоде. Ищем такие элементы:
Нам подходят натрий и алюминий.
Ответ: 15
Вариант 1ЕХ6
Определите, какие из указанных элементов образуют устойчивый отрицательный ион, содержащий
18 электронов.
1. N
2. Al
3. S
4. Cl
5. Ca
Отрицательный ион получается путем добавления электронов к атому. 18 электронов — это
полностью заполненный третий уровень или период, значит, наши элементы расположены именно в
нем (в отличии от предыдущего задания, где мы искали в следующем периоде, так как ион
положительный). Смотрим на предоставленные в условии элементы:
В данном случае в третий период попали алюминий, сера и хлор. Алюминий не может принять
электроны до 18, так как является металлом и отдает электроны. Наиболее типичные элементы—
любители электронов расположены правее. Это сера и хлор для данного задания.
Ответ: 34
Вариант 1ЕХ7
Определите, какие из указанных элементов на внешнем уровне содержат больше s—электронов, чем
p-электронов (в основном состоянии).
1. H
2. C
3. F
4. Be
5. P
Такие виды заданий часто встречаются в тренировочных вариантах, нужно либо определить кого
меньше, когда равно или кого больше. Разберем для наглядности данный пример. s—электронов всего
два, значит p—электронов должно быть 1, чтобы было меньше. В сумме у элемента на внешнем уровне
получается максимум 3 электрона (но может быть и ноль p—электронов и один или два s!), а значит
он в третьей, второй или первой группе.
Нам подходит водород и бериллий.
Ответ: 14.
Остальные задания очень похожи на разобранные, поэтому вы их точно сможете решить,
разобравшись с выше представленными решениями.
Ниже приведен подробный разбор демоверсии ЕГЭ-2023 по химии, проектная версия. Задания разобраны от 1 до 34 подряд, приведена логика рассуждения по каждому из них. Если есть желание разобраться более детально, то переходите по ссылкам в тексте или записывайтесь к нам на курс.
Для выполнения первого задания всегда рекомендую расписать электронно-графические формулы элементов (с ячейками). В большинстве случаев достаточно изобразить внешний и предвнешний уровень. Напомню также, что для элементов дальше IV периода не нужно изображать формулу целиком, а можно воспользоваться аналогией строения валентных подуровней с соседом из подгруппы. По приведенным элементам:
- Цезий находится в первой группе, главной подгруппе, аналог натрия по строению внешнего уровня. Имеет 1 электрон на 6s-подуровне, он же является неспаренным.
- Углерод находится в четвертой группе, главной подгруппе. На внешнем уровне имеет 4 электрона, из них неспаренных два, которые находятся на 2р-подуровне.
- Кислород находится в шестой группе, главной подгруппе. На внешнем уровне имеет 6 электронов, из них неспаренных два, которые находятся на 2р-подуровне.
- Хром находится в шестой группе, побочной подгруппе. Необходимо вспомнить о проскоке электрона, за счет которого на внешнем уровне, 4s-подуровне, имеет 1 электрон, а не предвнешнем, 3d-подуровне, – пять. Итого 6 неспаренных.
- Азот находится в пятой группе, главной подгруппе. На внешнем уровне имеет 5 электронов, из них неспаренных три, которые находятся на 2р-подуровне.
Выбираем углерод и кислород, у обоих по два неспаренных электрона.
Ответ: 23
Необходимо вспомнить, что к р-элементам можно отнести элементы главных подгрупп шести последних групп в периоде. Представители первых двух относятся к s-элементам, а элементы побочных подгрупп относим к d-элементам. Исходя из приведенных соображений, выбираем пункты 2), 3), 5).
Атомный радиус уменьшается направо по периоду, поэтому располагаем выбранные ранее элементы в порядке 2), 5), 3).
Ответ: 253
Для выполнения такого рода заданий рекомендую выписать на лист бумаги высшую и низшую степени окисления для каждого из элементов.
- Цезий имеет высшую степень окисления +1, низшую – 0. Разность 1.
- Углерод имеет высшую степень окисления +4, низшую – -4. Разность 8.
- Кислород имеет высшую степень окисления +2, низшую – -2. Разность 4.
- Хром имеет высшую степень окисления +6, низшую – 0. Разность 6.
- Азот имеет высшую степень окисления +5, низшую – -3. Разность 8.
Таким образом, выбираем углерод и азот.
Ответ: 25
В задании, по сути, есть два фильтра: по типу строения и по характеру связи. Начнем с типа строения. Поскольку необходимо выбрать вещества молекулярного строения, то сразу можно исключить соли и иные соединения, имеющие ионные связи. Убираем из рассмотрения пункты 1) и 4). Среди оставшихся нужно найти вещества с ковалентной полярной связью. Вспомним, что такая связь может возникать между атомами разных неметаллов (или сильно различающихся фрагментов в органических молекулах). По такому принципу можно исключить пункт 5). Остаются вещества 2) и 3).
Ответ: 23
К двухосновным кислотам относятся те из них, которые содержат в молекуле 2 атома водорода, способных замещаться на катионы металлов. Подобным требованиям отвечает сернистая кислота, пункт 4).
К средним можно отнести соли, не содержащие способных к замещению атомов водорода, фрагментов ОН, комплексных ионов и подобного. Из приведенного списка можно взять аммиачную селитру, тривиальное название нитрата аммония.
К амфотерным гидроксидам можно отнести гидроксиды металлов в степенях окисления +3 и +4, также гидроксиды бериллия, цинка, свинца, олова. Подойдет пункт 2).
Ответ: 482
Попробуем найти в приведенном списке сильные кислоты. Пункт 1) подходит, поскольку в пункте 3) находится слабая кислота. Таким образом X уже установлен.
Среди оставшихся пунктов нужно найти вещество, которое при добавлении вызовет растворение гидроксида алюминия. Поскольку гидроксид является амфотерным, то сможет прореагировать с кислотой, кроме наиболее слабых, или щелочью. Среди приведенных соединений можно взять 4), поскольку гидроксид калия является щелочью.
Ответ: 14
Для выполнения подобных заданий советую следующий порядок действий:
- Берем вещество из левого столбика
- Классифицируем его, вспоминаем характерные типы реакций для такого класса соединений
- Оцениваем его с точки зрения кислотно-основных и окислительно-восстановительных свойств
- Подбираем вещества и правого столбика, противоположные по свойствам и способные реагировать с веществом из правого столбика
Пункт А):
Сера относится к простым веществам-неметаллам, средняя по активности. Способна вступать в реакцию со щелочами, сильными окислителями и активными восстановителями. С водой и кислотами, кроме кислот-окислителей, реакции нет.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 3) водород выступит против серы в качестве восстановителя, хлор и кислород – окислители. Подходит.
В пункте 4) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 5) нет реакции уже с первым веществом, дальше не продолжаем.
Пункт Б):
Оксид серы (VI) относится к кислотным оксидам, реагирует с водой, большинством веществ основной и амфотерной природы. Восстановительных свойств не проявляет, может быть окислителем.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) оксид бария – основный, КОН – щелочь, с водой реакция тоже есть. Подходит.
В пункте 3) хлор и кислород – окислители, не подходит.
В пункте 4) нет реакции с уксусной кислотой, не подходит.
В пункте 5) нет реакции уже со вторым веществом, дальше не продолжаем.
Пункт В):
Гидроксид цинка относится к амфотерным гидроксидам, может реагировать со щелочами, кислотами. Выраженных окислительных или восстановительных свойств не проявляет. В воде нерастворим, с солями не обменивается.
В пункте 1) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 2) нет реакции с водой, не подходит.
В пункте 3) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 4) реагирует с кислотами и щелочью. Подходит.
В пункте 5) нет реакции с хлоридом бария, не подходит.
Пункт Г):
Бромид цинка относится к солям, может вступать в реакции обмена со щелочами и солями. Может проявлять восстановительные свойства за счет бромид-иона.
В пункте 1) обмен имеет смысл с первым и вторым веществам, с третьим будет ОВР. Подходит.
В пункте 2) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 3) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 4) нет реакции уже с первым веществом, дальше не продолжаем.
В пункте 5) нет реакции уже с первым веществом, дальше не продолжаем.
Ответ: 3241
Для ответа на вопрос имеет смысл оценить свойства веществ в каждой паре, а при необходимости записать уравнение реакции между ними. Сделаем и то, и другое.
В пункте А) магний является сильным восстановителем, а концентрированная серная кислота – окислителем. Магний способен восстановить серу до низшей степени окисления:
4Mg + 5H2SO4 = 4MgSO4 + H2S + 4H2O
В пункте Б) встречаются основный оксид и кислота, произойдет обмен:
MgO + H2SO4 = MgSO4 + H2O
В пункте В) сера выступает в качестве восстановителя, а концентрированная серная кислота – окислитель. Произойдет ОВР:
S + 2H2SO4 = 3SO2 + 2H2O
В пункте Г) сероводород выступает в качестве восстановителя, а кислород – окислитель. Произойдет ОВР:
2H2S + 3O2 = 2SO2 + 2H2O
Ответ: 5144
Обратим внимание, что железо в одну стадию переходит в степень окисления +3. Для этого нам нужен сильный окислитель- хлор.
2Fe + 3Cl2 = 2FeCl3
Во второй реакции железо понижает степень окисления до +2, поэтому необходимо найти восстановитель. Им тут может быть только йодид калия.
2FeCl3 + 2KI = 2FeCl2 + I2 + 2KCl
Ответ: 43
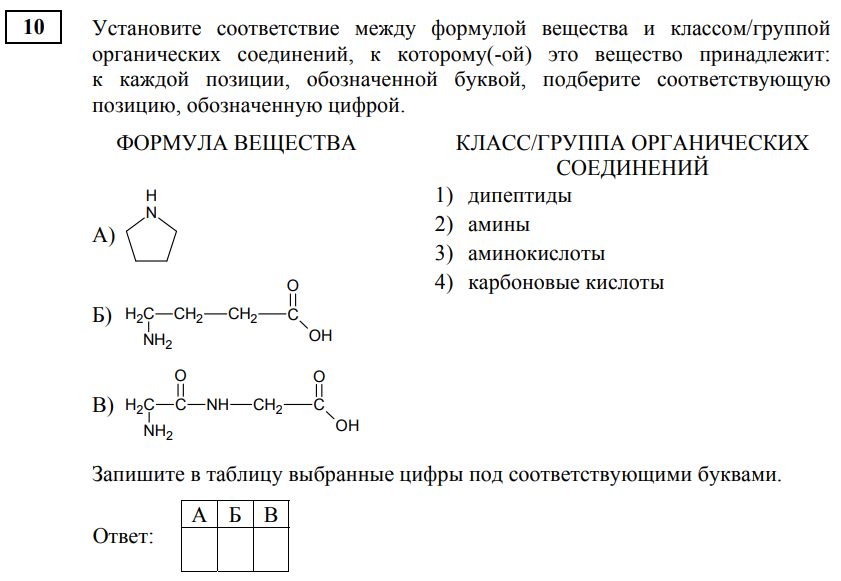
Для установления соответствия имеет смысл найти в структурах из левого столбика характерные функциональные группы и фрагменты.
В структуре А) видим фрагмент -NH-, который можно отнести ко вторичному амину. Циклическая структура молекулы в данном случае ничего не значит.
В структуре Б) есть аминогруппа и карбоксильная группа. Соответственно, вещество можно отнести к аминокислотам.
В структуре В) есть структурный фрагмент -С(О)NH- и просматриваются два остатка от аминокислот, что указывает на дипептид.
Ответ: 231
К решению подобных заданий может быть несколько подходов. Можно для начала определить молекулярную формулу бутена-1, а затем сравнить ее с молекулярными формулами предложенных вариантов. Изомеры по определению должны иметь одинаковые молекулярные формулы.
Бутен-1 – С4Н8
- С4Н10
- С4Н8
- С4Н6
- С4Н6
- С4Н8
Ответ: 25
Поскольку подкисленный раствор перманганата проявляет сильные окислительные свойства, следует поискать вещества, которые могут окисляться с образованием карбоновой кислоты. Прокомментируем все предложенные пункты:
- Окисляется с разрывом кратной связи, кислота будет
- Не окисляется
- Окисляется по боковой цепи, кислота будет
- Не окисляется
- Окисляется до кислоты
Ответ: 135
Метиламин относится к первичным алифатическим аминам, проявляет выраженные основные свойства, вступает в реакции алкилирования, реагирует с азотистой кислотой. Прокомментируем все предложенные пункты:
- Алкан, низкая активность, реакции нет
- Хлоралкан, реакция алкилирования, реагирует
- Водород, гидрировать нечего, не реагирует
- Основание, не реагирует
- Кислота, образование соли, реагирует
Ответ: 25
Для решения имеет смысл записать классы соединений из левого столбика, далее оценить происходящие изменения:
А) 1,2-дигалогеналкан – алкен
Б) моногалогеналкан – алкен
В) моногалогеналкан – алкан
Г) 1,2-дигалогеналкан – алкин
По изменениям назвать тип происходящей реакции и подобрать к ней подходящий реагент:
А) дегалогенирование, магний
Б) дегидрогалогенирование, спиртовой раствор щелочи
В) реакция Вюрца, натрий
Г) дегидрогалогенирование, спиртовой раствор щелочи
Ответ: 1252
Для надежности перед выбором ответа имеет смысл преобразовать названия веществ в формулы и прописать предложенные реакции. Попробуем это сделать:
А) 2CH3COOH + Na2S = 2CH3COONa + H2S
Б) HCOOH + NaOH = HCOONa + H2O
В) HCOH + 4Cu(OH)2 = 2Cu2O + CO2 + 5H2O
Г) 2CH3CH2OH + 2Na = 2CH3CH2ONa + H2
Ответ: 5462
При рассмотрении цепочек превращений бывает полезно посмотреть через одну стадию и оценить, как можно осуществить такое превращение. Также очень полезно сравнить число атомов углерода в исходной молекуле и продукте, может навести на мысль.
В первых двух реакциях цепочки число атомов углерода удваивается, что наводит на мысль о реакции Вюрца. Если рассуждение верное, то веществом Х должен быть галогеналкан. Действительно, его можно получить в одну стадию из спирта, а затем превратить в алкан.
Следующее превращение можно понять, если посмотреть на условия реакции. Нагревание линейного алкана в присутствии хлорида алюминия приводит к его изомеризации в разветвленный алкан.
Ответ: 54
Для решения можно переписать вещества в парах в виде формул, оценить их окислительно-восстановительные свойства и возможность реакции между ними:
- K2S – восстановитель, KMnO4 – окислитель, имеет смысл
- H2SO4 – окислитель, NaCl – очень слабый восстановитель, не ОВР
- NH4Cl – очень слабый восстановитель, NaNO2 – окислитель, специфический случай обмена, сопровождаемого ОВР
- SiO2 – выраженных окислительно-восстановительных свойств не проявляет, Na2CO3 — выраженных окислительно-восстановительных свойств не проявляет, не ОВР
- HI – восстановитель, Na2Cr2O7 – сильный окислитель, имеет смысл
Для надежности можно записать уравнения реакций между ними:
- 2KMnO4 + 3K2S + 4H2O = 2MnO2 + 3S + 8KOH
- NaCl + H2SO4 = NaHSO4 + HCl
- NaNO2 + NH4Cl = NaCl + N2 + 2H2O
- Na2CO3 + SiO2 = Na2SiO3 + CO2
- Na2Cr2O7 + 14HI = 2NaI + 2CrI3 + 3I2 + 7H2O
Ответ: 135
Изменение давления не будет влиять на скорость реакций, в которых нет газообразных реагентов. Среди приведенных пунктов это будут 2), 3), 5).
Ответ: 235
Для решения подобных заданий нужно расставить степени окисления на атомах азота до и после реакции.
Если степень не меняется, то азот не проявляет окислительно-восстановительных свойств. Так будет в пункте А) (переход -3 в -3).
Если степень увеличится, то азот проявляет восстановительные свойства. Так будет в пунктах Б) (переход -3 в 0) и В) (переход -3 в +2).
Ответ: 422
В первом случае для решения необходимо вспомнить зависимость продуктов электролиза от состава соли:
А) соль образована катионом активного металла и кислородсодержащим анионом, на электродах выделятся водород и кислород.
Б) соль образована катионом активного металла и галогенид-ионом, на электродах выделятся водород и галоген.
В) соль образована катионом малоактивного металла и галогенид-ионом, на электродах выделятся металл и галоген.
Ответ: 342
Во втором случае нужно помнить, что алюминий получают при электролизе раствора оксида в расплаве криолита. Калий и подобные наиболее активные металлы только из расплавов галогенидов. Кислород в данном случае можно получить при электролизе водного раствора фторида калия.
Ответ: 124
Для начала имеет смысл определить класс каждого из соединений:
- Средняя соль
- Средняя соль
- Средняя соль
- Сильная кислота
Исходя из этого уже можно сказать, что наиболее низкое значение рН (самая кислая среда) будет в пункте 4).
Как разобраться с солями? Нужно оценить их способность к гидролизу и потенциальное влияние на среду раствора:
- Соль сильной кислоты и сильного основания, не гидролизуется, среда нейтральная
- Соль слабого основания и сильной кислоты, гидролиз по катиону, среда кислая
- Соль сильного основания и слабой кислоты, гидролиз по аниону, среда щелочная
Ответ: 4213
В задании на равновесие следует учитывать разные факторы. Пройдем по каждому из пунктов:
А) кислота при диссоциации может дать дополнительное количество ионов Н+, которые участвуют в равновесии. При увеличении их концентрации равновесие сместится в сторону обратной реакции.
Б) давление в данном случае не окажет влияния, поскольку нет участников-газов
В) повышение температуры сместит равновесие в сторону эндотермической реакции. В данном случае – прямой.
Г) твердая щелочь может раствориться и прореагировать с Н+, уменьшая концентрацию таких ионов в системе. Равновесие сместится в сторону прямой реакции.
Ответ: 2311
Задания подобного типа удобнее всего решать с помощью таблицы. Данный подход к решению задания ЕГЭ-2023 на равновесие в реакторе можно посмотреть по ссылке ниже:
Способ, на мой взгляд, наиболее оптимальный и доступный каждому.
Ответ: 25
В первом случае нужно подобрать такое вещество из правого столбика, которое реагирует с одним или двумя веществами из пары в левом столбике. При этом очень важно, чтобы реакция сопровождалась видимыми признаками:
Пара А):
- Есть реакция с азотной кислотой, сопровождается выделением газа и растворением твердого вещества. Нитрат натрия не реагирует. Подходит.
- Есть реакция с азотной кислотой, но внешних признаков нет. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
Пара Б):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с гидроксидом калия, но внешних признаков нет. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с гидроксидом натрия, сопровождается образованием осадка. Хлорид калия не реагирует. Подходит.
Пара В):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Есть реакция с хлоридом бария, сопровождается образованием осадка. Хлорид натрия не реагирует. Подходит.
Пара Г):
- Нет реакции ни с одним веществом из пары. Не подходит.
- Специфический случай, поскольку один из изначально образовавшихся нерастворимых гидроксидов (Al(OH)3) может раствориться снова при избытке щелочи. Подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
- Нет реакции ни с одним веществом из пары. Не подходит.
В заданиях второго типа имеет смысл записать происходящие реакции и попытаться себе их представить. Как может выглядеть и что увидим:
- 2CH3CH2COOH + 2Li = 2CH3CH2COOLi + H2
- 2CH3CH(OH)CH3 + 2K = 2CH3CH(OK)CH3 + H2
- Zn(OH)2 + 2CH3COOH = Zn(CH3COO)2 + 2H2O
- C2H2 + 2Br2 = CHBr2-CHBr2
В первом и втором случаях наблюдаем выделение газообразного водорода. В третьем наблюдаем растворение осадка гидроксида цинка. В четвертом исчезнет окраска брома, наблюдается обесцвечивание.
Ответ: 4415
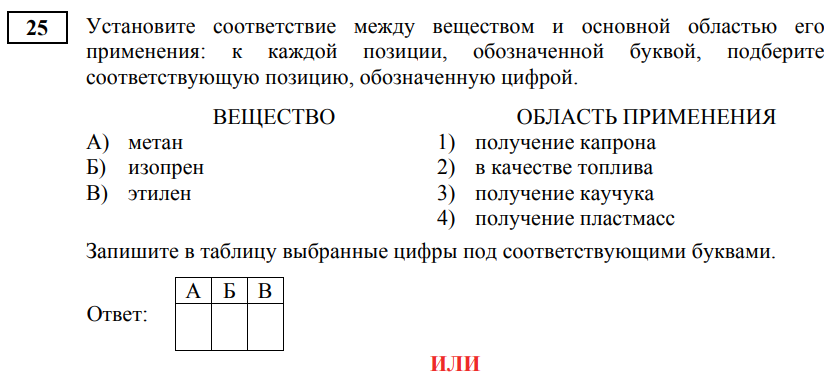
Задание 25 охватывает несколько совершенно разнородных тем, каждая из которых требует отдельного блока знаний. Приведу здесь ссылки на полезные материалы по заданию, поскольку многое здесь нужно просто выучить.
По первому блоку следует знать, что сопряженные алкадиены используются для производства каучуков, а алкены – пластмасс. Метан в составе природного газа используют в качестве топлива.
По второму блоку можно относительно легко соотнести мономер и полимер, если представить себе структуру молекулы мономера. В молекуле этена всего два атома углерода, поэтому элементарное звено формулы полимера тоже содержит два атома углерода. По той же логике здесь можно действовать и для пропена с дивинилом.
Третий блок нужно просто выучить. По переработке углеводородов можно заглянуть сюда. Хорошее описание технологических процессов можно посмотреть здесь.
Ответ: 234; 214; 312
Для решения подобных заданий на растворы рекомендую использовать метод таблиц, подробно описанный здесь.
В итоге решение задачи сводится к уравнению вида
(15+х)/(150+х) = 0,12
15+х = 18+0,12х
0,88х = 3
х = 3,4
Ответ: 3,4 г
Задания такого типа сводятся к решению пропорции. Для начала переведем известный объем аммиака в количество:
n(NH3) = V(NH3)/Vm = 0,56/22,4 = 0,025 (моль)
2 моль – 92 кДж
0,025 моль – х кДж
х = 1,15 кДж
Ответ: 1,15 кДж
Для решения первой задачи запишем уравнение протекающей реакции:
CaCO3 + 2HNO3 = Ca(NO3)2 + CO2 + H2O
Далее вычислим количество нитрата кальция:
n(Ca(NO3)2) = m(Ca(NO3)2)/M(Ca(NO3)2) = 196800/164 = 1200 (моль)
Вычислим массу чистого карбоната кальция, который содержался в известняке:
m(CaCO3) = n(Ca(NO3)2)·M(Ca(NO3)2) = 1200·100 = 120000 (г) = 120 (кг)
Вычислим массу примесей в известняке:
m(примеси) = m(известняка) – m(CaCO3) = 150 — 120 = 30 (кг)
Определим массовую долю примеси в известняке:
ω(примеси) = m(примеси)/m(известняка)·100% = 30/150·100% = 20%
Ответ: 20%
Для решения второй задачи запишем уравнение протекающей реакции:
3С2Н2 = С6Н6
Вычислим количества ацетилена и практически полученного бензола:
n(С2Н2) = V(С2Н2)/Vm = 26,88/22,4 = 1,2 (моль)
n(С6Н6 практ.) = m(С6Н6)/M(С6Н6) = 23,4/78 = 0,3 (моль)
Вычислим теоретически возможное количество бензола и сравним его с практическим:
n(С6Н6 теор.) = n(С2Н2)/3 = 1,2/3 = 0,4 (моль)
η(С6Н6) = n(С6Н6 практ.)/n(С6Н6 теор.)·100% = 0,3/0,4·100% = 75%
Ответ: 75%
При выполнении заданий 29 и 30 имеет смысл записать все представленные вещества в виде молекулярных формул:
KMnO4, NaHCO3, Na2SO3, BaSO4, KOH, H2O2
Далее следует внимательно прочитать описание реакции. Поскольку должно происходить изменение цвета раствора, нужно найти окрашенный реагент. Из предложенных это может быть только KMnO4. Это вещество проявляет сильные окислительные свойства, поэтому нужно подобрать восстановитель. Осадка в ходе реакции образоваться не должно, поэтому брать нейтральную среду нельзя. В противном случае выпадет осадок MnO2. Среда может быть кислой или щелочной. Кислоты в предложенном наборе нет, поэтому выберем гидроксид калия для создания среды. Восстановителей в предложенном наборе два: сульфит натрия и пероксид водорода. Пероксид брать нельзя, поскольку по описанию реакции газа образоваться не должно. Таким образом приходим к выводу, что нужно взять сульфит, перманганат и щелочь. Приведем соответствующую реакцию и электронный баланс:
2KMnO4 + Na2SO3 + 2KOH = 2K2MnO4 + Na2SO4 + H2O
2∙ | Mn+7 + 1ē → Mn+6
1∙ | S+4 – 2ē → S+6
марганец в степени окисления +7 (или перманганат калия) является окислителем.
сера в степени окисления +4 (или сульфит натрия) – восстановителем.
Есть хороший инструмент для отработки данного задания, рекомендую.
При выполнении заданий 29 и 30 имеет смысл записать все представленные вещества в виде молекулярных формул:
KMnO4, NaHCO3, Na2SO3, BaSO4, KOH, H2O2
Далее следует внимательно прочитать описание реакции. К кислым солям здесь относится только NaHCO3. В обмен с ней вступит только гидроксид калия, поскольку кислое и щелочь точно смогут прореагировать. Приведем молекулярное, полное и сокращенное ионные уравнения:
2NaHCO3 + 2KOH = Na2CO3 + K2CO3 + 2H2O
2Na+ + 2HCO3− + 2K+ + 2OH− = 2Na+ + CO32− + 2K+ + CO32− + 2H2O
HCO3− + OH− = CO32− + H2O
Решение 31 номера сводится к знанию неорганической химии, свойств и реакций отдельных веществ. Приведем уравнения протекающих процессов:
2Cu(NO3)2 + 2H2O = 2Cu + O2 + 4HNO3
Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O
SO2 + 2H2S = 3S + 2H2O
3S + 6KOH = K2SO3 + 2K2S + 3H2O
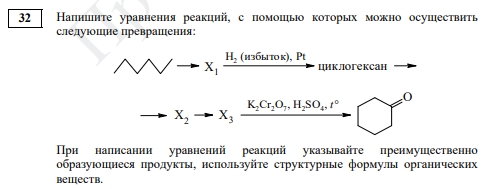
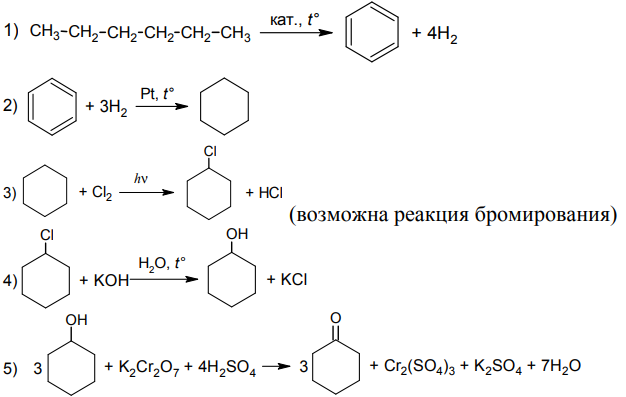
При рассмотрении цепочек превращений бывает полезно посмотреть через одну стадию и оценить, как можно осуществить такое превращение. Также очень полезно сравнить число атомов углерода в исходной молекуле и продукте, может навести на мысль.
Начнем с циклогексана. Получить его путем гидрирования можно, например, из бензола. Его, в свою очередь, можно получить из гексана по реакции дегидроциклизации. Х1 – бензол. Далее в цепочке много неизвестных веществ, заглянем в самый конец. Циклогексанон относится к кетонам, получить его можно из вторичного спирта. Условия последней реакции на это указывают, поскольку там дан сильный окислитель в кислой среде. Тогда Х3 – циклогексанол. Получить такой спирт в две стадии нужно из циклоалкана. Тогда можно предположить последовательно галогенирование и замещение полученного галогенпроизводного под действием водного раствора щелочи. Тогда Х2 – хлорциклогексан, можно бромциклогексан. Последовательность реакций получается следующей:
Решение задачи начинается с анализа и расчета молекулярной формулы. Поскольку продуктами сгорания являются только углекислый газ и вода, можно приписать веществу формулу CxHyOz. Вычислим количества углекислого газа и воды:
n(H2O) = m(H2O)/M(H2O) = 1,8/18 = 0,1 (моль)
n(СО2) = V(CO2)/Vm = 4,48/22,4 = 0,2 (моль)
Тогда можно определить количества и массы элементов, входивших в состав исходного вещества:
n(С) = n(СО2) = 0,2 моль
m(С) = n(С)·M(С) = 0,2·12 = 2,4 г
n(H) = 2n(H2O) = 0,2 моль
m(H) = n(H)·M(H) = 0,2·1 = 0,2 г
m(О) = m(CxHyOz) − m(С) − m(H) = 3,4 − 2,4 − 0,2 = 0,8 (г)
n(O) = m(O)/M(O) = 0,8/16 = 0,05 (моль)
Вычислим молекулярную формулу неизвестного вещества:
x : y : z = n(С) : n(H) : n(O) = 0,2 : 0,2 : 0,05 = 4 : 4 : 1
Поскольку по условию один из фрагментов молекулы должен содержать 7 атомов углерода, разумным будет удвоить простейшее соотношение и получить формулу C8H8O2.
С8Н8О2 – молекулярная формула
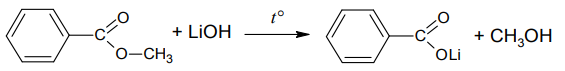
Вещество по условию реагирует со щелочью, процесс гидролиза с образованием соли и спирта. В остатке кислоты 7 атомов углерода и малое количество атомов водорода, что вполне соответствует бензоату. Тогда на спирт приходится всего один атом углерода, что соответствует метанолу. Тогда можно предложить структуру метилбензоата:
Запишем уравнение его реакции с гидроксидом лития:
К заданию 34 следует приступать только после ПОЛНОГО выполнения и проверки всех остальных заданий КИМа. Убедитесь также, что все прочие задания перенесены в бланк ответов, а не остались на черновике. Времени на это задание нужно больше всего, поэтому велик риск потерять остальное и не успеть что-то перенести в бланк.
Для решения следует внимательно прочитать условие и написать реакции, которые сразу же очевидны, без дополнительных расчетов. Здесь их можно записать две:
Ca + 2HCl = CaCl2 + H2
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
Поскольку напрямую ничего не известно про массу и количество кальция и карбоната кальция, можно сказать, что кальция было х моль, а его карбоната у моль. Тогда в ходе реакций выделилось х моль водорода и у моль углекислого газа. Выразим массы указанных веществ:
m(Ca) = n·M = 40х г
m(CaCO3) = n·M = 100у г
m(Н2) = n·M = 2х г
m(CO2) = n·M = 44у г
Выразим массу раствора после добавления исходной твердой смеси к соляной кислоте:
m(р-ра) = m(Ca) + m(CaCO3) + m(р-ра HCl) − m(Н2) − m(CO2)
m(р-ра) = 40х + 100у + 300 − 2х − 44у = 330 (г)
38х + 56у = 30
Первое уравнение системы готово. Второе составим по массовой доле кальция в исходной смеси:
m(смеси) = m(Ca) + m(CaCO3) = 40х + 100у (г)
m(Ca) = 40х + 40у (г)
ω(Са) = m(Ca)/m(смеси)·100% = (40х+40у)/(40х+100у)·100% = 50%
(40х+40у)/(40х+100у) = 0,5
Составим и решим систему уравнений:
38х + 56у = 30
(40х + 40у)/(40х + 100у) = 0,5
38х + 56у = 30
(2х + 2у)/(2х + 5у) = 0,5
38х + 56у = 30
2х + 2у = х + 2,5у
38х + 56у = 30
х = 0,5у
75у = 30
у = 0,4
х = 0,2
n(Ca) = 0,2 моль
n(CaСО3) = 0,4 моль
Далее вычислим количество и массу углекислого газа:
n(СО2) = n(CaСО3) = 0,4 моль
m(СО2) = n(СО2)·M(СО2) = 0,4·44 = 17,6 г
Вычислим массу и количество гидроксида натрия:
m(NaOH) = m(р-ра NaOH)·ω(NaOH)/100% = 400·4%/100% = 16 (г)
n(NaOH) = m(NaOH)/M(NaOH) = 16/40 = 0,4 (моль)
Далее нужно сравнить количества щелочи и углекислого газа, чтобы понять, какая будет реакция между ними:
n(СО2)/n(NaOH) = 0,4/0,4 = 1:1
Соотношение 1:1, поэтому образуется кислая соль:
NaOH + CO2 = NaHCO3
Вычислим массу образовавшейся соли и массу раствора:
n(NaHCO3) = n(СО2) = 0,4 моль
m(NaHCO3) = n·M = 0,4·84 = 33,6 г
m(р-ра конечн.) = m(р-ра NaOH) + m(CO2) = 400 + 17,6 = 417,6 (г)
Вычислим массовую долю гидрокарбоната натрия в полученном растворе:
ω(NaHCO3) = m(NaHCO3)/m(р-ра конечн.)·100% = 33,6/417,6·100% = 8,05%
Ответ: 8,05%
Задание №1 ЕГЭ химия. Теория и практика
Первое задание в ЕГЭ по химии посвящено электронной конфигурации атома. Для его выполнения дается ряд химических элементов, среди которых нужно выбрать два с одинаковым свойством:
— одинаковое число валентных электронов;
— одинаковое количество неспаренных электронов в основном или возбужденном состоянии;
— одна и та же общая электронная конфигурация валентного уровня.
Для правильного выполнения этого задания полезно помнить последовательность заполнения электронами атомных орбиталей, которую можно легко понять и усвоить благодаря данному рисунку:
Рис.1 Порядок заполнения электронами атомных орбиталей.
Атом — электро нейтральная частицей. Положительный заряд ядра уравновешивается числом отрицательно заряженных электронов, которые движутся в его поле. Заряд ядра атома химического элемента равен его порядковому номеру в периодической системе Д.И. Менделеева. При переходе от одного элемента к следующему заряд ядра увеличивается на единицу. И на единицу возрастает число электронов в атоме. Каждый следующий добавляемый электрон занимает низшую свободную атомную орбиталь.
Рассмотрим электронную конфигурацию на примере атома водорода. Заряд ядра атома водорода +1. Значит, в поле ядра движется 1 электрон, и он занимает самую первую по энергии атомную орбиталь — 1s. Электронная формула атома водорода записывается 1s1

У атома гелия (заряд ядра +2) следующий электрон займет ту же самую s-орбиталь, однако спин у него будет противоположный (стрелка, изображающая электрон, направлена в другую сторону):
Рис.2.Конфигурация атома гелия в основном состоянии.
На этом ёмкость 1 энергетического уровня становится полностью заполненной. Поэтому следующий электрон, который появляется у атома лития и бериллия, займёт s- орбиталь второго энергетического уровня (2s-орбиталь):
Рис. 3. Конфигурации атома лития и бериллия в основном состоянии.
Правило Хунда: электроны заполняют атомную орбиталь таким образом, чтобы её суммарный спин был максимальным.
Иными словами, при заполнении p, d, f-орбиталей электроны сначала будут занимать квантовые ячейки орбитали по одному, и только потом будут спариваться. По этому поводу можно привести хорошую аналогию: при размещении пассажиров в изначально пустом автобусе, если все люди незнакомы, сначала они будут занимать места по одному, и только когда мест станет не достаточно, незнакомые люди станут занимать места рядом с теми, кто зашел в автобус раньше. На этом основании запишем электронную конфигурацию атома серы и изобразим распределение электронов по квантовым ячейкам:
Рис. 4. Конфигурация атома серы в основном состоянии. Красным цветом показаны электроны валентного уровня.
В образовании химических связей участвуют только электроны внешнего (валентного) энергетического уровня. В атоме серы таким уровнем является третий. На нём расположено шесть электронов, два из которых не спарены.
Число валентных электронов в атоме равно номеру группы (исключения: атомы кобальта и никеля, у них число валентных электронов равно 9 и 10, соответственно).
Особой энергетической устойчивостью обладают наполовину и полностью заполненные орбитали.
Запишем электронную конфигурацию атома хрома. Найдем хром в таблице Менделеева. Его порядковый номер — 24. Это означает, что заряд ядра атома Cr +24, следовательно, в поле ядра движется 24 электрона.
Распределим 24 электрона по орбиталям, пользуясь уже известными нам правилами. Помним, что между 4s и 4p-орбиталями заполняется 3d-орбиталь:
Однако, на d-орбитали не хватает одного электрона до наполовину заполненного состояния. А наполовину заполненные орбитали отличаются пониженной энергией. Всё в мире стремится к минимуму энергии; и атом тоже. Поэтому один электрон с 4s-орбитали перескакивает на 3d-орбиталь, благодаря близости энергий этих орбиталей.
Символом в квадратных скобках (у нас это — [Ar]) принято сокращать электронную конфигурацию полностью заполненных невалентных нижних энергетических уровней. У всех благородных газов, которые находятся в 18 группе длиннопериодного варианта периодической системы или в 8 группе краткопериодного, орбитали заполнены полностью, и чтобы не переписывать каждый раз одно и то же пользуются таким способом сокращения записи.
Таким же исключением из правил является атом меди. Ему не хватает одного электрона для полного заполнения 3d-орбитали. И он, как и хром, берет этот электрон с 4-s -орбитали
Именно на тех же основаниях электронная конфигурация молибдена — [Kr] 4d55s1, серебра — [Kr] 4d105s1.
Пользуясь информацией, изложенной выше, можно легко вычислить число валентных, внешних и неспаренных электронов в атоме и безошибочно выполнить первое задание ЕГЭ, за которое можно получить 1 первичный балл.
Задание 1
1) N 2) S 3) P 4) Se 5) As
Определите, атомы каких из указанных в ряду элементов имеют в возбуждённом состоянии электронную конфигурацию внешнего энергетического уровня ns1np3nd1. Запишите в поле ответа номера выбранных элементов.
Задание 2
1) Te 2) I 3) O 4) S 5) Sr
Определите, анионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 5s25p6. Запишите в поле ответа номера выбранных элементов.
Задание 3
1) Al 2) S 3) P 4) Cr 5) Si
Определите, атомы каких из указанных в ряду элементов в основном состоянии во внешнем слое содержат один неспаренный электрон. Запишите в поле ответа номера выбранных элементов.
Задание 4
1) Mg 2) Bi 3) Ba 4) Sr 5) Al
Определите, катионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 3s0. Запишите в поле ответа номера выбранных элементов.
Задание 4
1) I 2) N 3) Br 4) P 5) Cl
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns2np3. Запишите в поле ответа номера выбранных элементов.