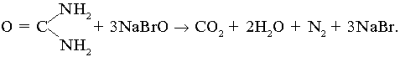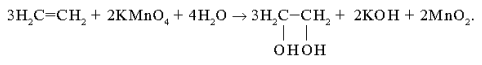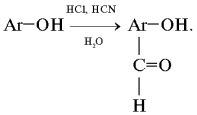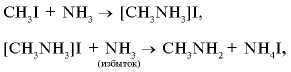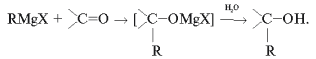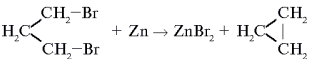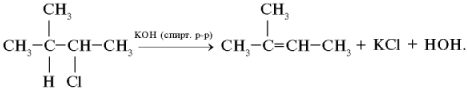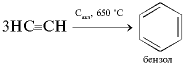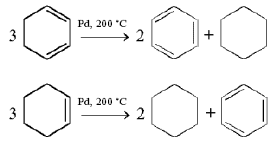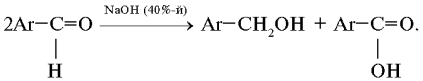10 января 2023
В закладки
Обсудить
Жалоба
Именные реакции в органической химии
Краткое описание 17 реакций.
im-r.docx
im-r.pdf
1. Реакция М.И. Коновалова
2. Реакция Ш.А. Вюрца (cинтез Вюрца)
3. Реакция Кольбе – Шмидта
4. Реакция Дюма
5. Реакция Г.Г. Густавсона
6. Правило В.В. Марковникова
7. Правило А.М. Зайцева
8. Реакция Е.Е. Вагнера
9. Реакция С.В. Лебедева
10. Реакция М.Г. Кучерова
11. Реакция Фриделя – Крафтса
12. Реакции Н.Д. Зелинского (получение бензола)
13. Реакция Вюрца – Фиттига
14. Реакция Сергеева – Удрисома – Кружалова
15. Реакция А.У. Уильямсон (синтез Вильямсона)
16. Реакция К.С. Кирхгофа
17. Реакция Н.Н. Зинина
Именные реакции в органической химии очень часто носят имя исследователя, который открыл или исследовал такую реакцию. Нередко реакции называются двойными именами учёных.
Такое случалось, когда автор первого издания впервые открыл и исследовал реакцию, а второй учёный одновременно опубликовал точно такие же материалы.
Ниже приведён список именных химических реакций, которые чаще всего встречаются на экзаменах.
Именные реакции в органической химии для подготовки к ЕГЭ
Абитуриенту, поступающему на химический факультет, необходимо знать ряд именных реакций. Далее рассмотрим таблицу всех необходимых реакций для подготовки к сдаче ЕГЭ.
Реакция Вюрца
Основана на методе, в котором проходит синтез симметричных насыщенных углеводородов, в которых воздействует металлический натрий на моногалогенопроизводные углеводородов (чаще всего разновидность бромидов или иодидов). В результате получаем удвоенный углеродный скелет.
Реакция считается подходящей для получения симметричных алканов:
2CH3 CH2 Br + 2Na = CH3
CH2 CH2 CH3 + 2NaBr.
Реакция Вюрца-Фиттига
Разновидностью предыдущей реакции считается реакция Вюрца-Фиттига, в результате которой образуются ароматические углеводороды:
Реакция Дюма
Нагревание смеси соли карбоновой кислоты и гидроксида Na, при котором происходит отщепление группы COONa от молекулы соли:
C2H5COONa (пропионат натрия, тв.) + NaOH(тв.) = CH4 (метан) + Na2CO3;
CH3COONa (ацетат натрия, тв.) + NaOH(тв.) = CH4 (метан) + Na2CO3.
Реакция Кольбе
Получение насыщенных углеводородов путём электролиза водных растворов калиевых или натриевых солей карбоновых кислот:
2CH3COONa (ацетат натрия) + 2H2O =[электролиз]=> 2СО2 + Н2 + CH3-CH3 (этан) + 2NaOH.
Синтез Густавсона
Результат отщепления двух атомов галогена от дигалогеналканов:
СlСН2-СН2-СН2-СН2Cl + Zn = C4H8 (циклобутан) + ZnCl2
Магний возможно заменять цинком.
Синтез Лебедева
Процесс получения бутадиена из этанола:
2C2Н5-OH = Н2 + 2Н2O + СН2 = CH-CH = СН2
Реакция Бутлерова
Процесс получения моносахаридов из формальдегида в слабощелочном водном растворе при наличии ионов металлов, к примеру кальция:
6НCНO = C6Н12O6
Реакция Коновалова
Механизм нитрования алифатического, алициклического и жирноароматического соединения разбавленного НNО3:
C2H6 + HNO3 = C2H5NO2 + Н2O.
Эффект Хараша
Процесс присоединения бромоводорода при наличии перекиси. Реакция проходит вопреки правилу Марковникова:
СН3-СН = СН2 + HBr = [Н2О2] => СН3-СН2-СН2Br.
Реакция Вагнера
Взаимодействие перманганата калия и холодного раствора воды – процесс мягкого окисления алкенов (образуется диол). Уравнение выглядит следующим образом:
3СН3-СН = СН2 + 2KMnO4 + 4H2O = 2MnO2 + 2KOH + 3СН3-СН(OH)-СН2(OH).
Реакция Кучерова
Механизм, при котором получаются карбонильные соединения из алкинов при наличии соли ртути (II) в кислой водной среде. В результате гидратации получается енол, изомеризующийся в разновидность альдегида или кетона.
C2H2 + H2O = CH3CHO.
Реакция Зелинского
Способ тримеризации ацетилена. Процесс проходит во время пропускания ацетилена над активированным углем. Получается раствор бензола:
3C2H2 = C6H6.
Реакция Зинина
Образование ароматического амина путем восстановления нитросоединений в растворах в щелочной и нейтральной среде:
R-NO2 + 3(NH4)2S = R-NH2 + 3S + 6NH3 +2H2O.
Реакция Фриделя-Крафтса
Процесс алкилирования или ацилирования ароматического соединения при наличии катализатора кислотного характера, минеральной кислоты, окислов, катионообменной смолы.
Агентами алкилирования являются алкилгалогенид, олефин, спирт, сложный эфир; ацилирования — карбоновая кислота, её галогенангидрид и ангидрид.
Общий вид процесса:
C₆H₆ + R-Hal = [AlCl₃] => C₆H₅-R + Hhal.
Реакция Зелинского–Казанского
Получение бензола из циклогексана при температуре 420-4800С:
C6H12
=> C6H6 + 3H2.
Реакция Прилежаева
Каталитическое окисление этилена с получением эпоксида. Автор реакции российский химик органик Н. А. Прилежаев.
Реакция происходит при температуре 2000С:
2CH2
= CH2 + O2 => эпоксид этилена.
Именные реакции в органической химии
1. Реакция Вюрца: действие металлического натрия на моногалогенопроизводные углеводородов. Происходит удвоение углеродного скелета. Реакция подходит для получения симметричных алканов.
2CH3–CH2Br + 2Na = CH3–CH2–CH2–CH3 +2NaBr
2. Синтез Лебедева: получение бутадиена из этанола.
2C2H5OH = Н2 + 2Н2O + CH2=CH-CH=CH2
3. Реакция Дюма: декарбоксилирование солей карбоновых кислот — сплавление со щелочами.
CH3COONa (тв.) + NaOH(тв.) = CH4 + Na2CO3
4. Синтез Густавсона: отщепление двух атомов галогена от дигалогеналканов:
СlCH2-CH2-CH2-CH2Cl + Zn = C4H8 (циклобутан) + ZnCl2
Вместо магния может использоваться цинк.
5. Реакция Кольбе: электролиз растворов солей карбоновых кислот:
CH3COONa + 2H2O =[эл.ток]=> 2СО2 + Н2 + С2Н6 + 2NaOH
6. Реакция Коновалова – нитрование алканов разбавленной (10%-ной) азотной кислотой:
C2H6 + HNO3 = C2H5NO2 + Н2O
Избирательность нитрования:
третичный атом > вторичный атом > первичный атом углерода.
7. Реакция Кучерова: гидратация алкинов. Присоединение воды происходит в присутствии солей ртути (II) и идет через образование неустойчивого енола, который изомеризуется в альдегид или кетон. Гидратация ацетилена дает альдегид, других алкинов – кетон.
C2H2 + H2O = CH3CHO
8. Эффект Хараша: присоединение бромоводорода в присутствии перекиси. Реакция протекает против правила Марковникова:
СН3-СН=СН2 + HBr =[Н2О2]=> СН3-СН2-СН2Br
9. Реакция Вагнера: реакция с холодным водным раствором перманганата калия – мягкое окисление алкенов (образуется диол)
3СН3-СН=СН2 + 2KMnO4 + 4H2O = 2MnO2 + 2KOH + 3СН3 -СН(OH)-СН2(OH)
10. Реакция Зинина: восстановление нитросоединений в растворе в щелочной и нейтральной среде:
R-NO2 + 3(NH4)2S = R-NH2 + 3S + 6NH3 +2H2O
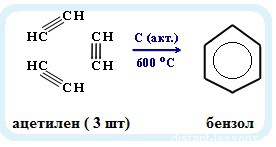
11. Реакция Зелинского: тримеризация ацетилена над активированным углем. Образуется бензол.
3C2H2 = C6H6
ИПолучение
1. Реакция Вюрца: действие металлического натрия на моногалогенопроизводные углеводородов. Происходит удвоение углеродного скелета. Реакция подходит для получения симметричных алканов.
2CH3–CH2Br + 2Na = CH3–CH2–CH2–CH3 +2NaBr
2. Реакция Дюма: декарбоксилирование солей карбоновых кислот — сплавление со щелочами.
CH3COONa (тв.) + NaOH(тв.) = CH4 + Na2CO3
3. Реакция Кольбе: электролиз растворов солей карбоновых кислот:
CH3COONa + 2H2O =[эл.ток]= 2СО2 + Н2 + С2Н6 + 2NaOH
4. Синтез Густавсона: отщепление двух атомов галогена от дигалогеналканов:
СlCH2-CH2-CH2-CH2Cl + Zn = C4H8 (циклобутан) + ZnCl2
Вместо магния может использоваться цинк.
5. Синтез Лебедева: получение бутадиена из этанола.
2C2H5OH = Н2 + 2Н2O + CH2=CH-CH=CH2
Химические свойства
1. Реакция Коновалова – нитрование алканов разбавленной (10%-ной) азотной кислотой:
C2H6 + HNO3 = C2H5NO2 + Н2O
Избирательность нитрования:
третичный атом вторичный атом первичный атом углерода.
2. Эффект Хараша: присоединение бромоводорода в присутствии перекиси. Реакция протекает против правила Марковникова:
СН3-СН=СН2 + HBr =[Н2О2]= СН3-СН2-СН2Br
3. Реакция Вагнера: реакция с холодным водным раствором перманганата калия – мягкое окисление алкенов (образуется диол)
3СН3-СН=СН2 + 2KMnO4 + 4H2O = 2MnO2 + 2KOH + 3СН3 -СН(OH)-СН2(OH)
4. Реакция Кучерова: гидратация алкинов. Присоединение воды происходит в присутствии солей ртути (II) и идет через образование неустойчивого енола, который изомеризуется в альдегид или кетон. Гидратация ацетилена дает альдегид, других алкинов – кетон.
C2H2 + H2O = CH3CHO
5. Реакция Зелинского: тримеризация ацетилена над активированным углем. Образуется бензол.
3C2H2 = C6H6
6. Реакция Зинина: восстановление нитросоединений в растворе в щелочной и нейтральной среде:
R-NO2 + 3(NH4)2S = R-NH2 + 3S + 6NH3 +2H2O
ТО, ЧТО НАС ОБЬЕДИНЯЕТ…
Реакция Арбузова (перегруппировка Арбузова, изомеризация Арбузова) Каталитическая изомеризация эфиров фосфористой кислоты в эфиры алкилфосфиновых кислот (1904).
Правило Бейльштейна Если оба заместителя в ароматическом кольце принадлежат к одному и тому же типу, то преобладающее направление замещения определяется тем из них, влияние которого сильнее (1866).
Проба Бейльштейна Открытие галогенов в органических соединениях путем прокаливания на окисленной медной проволоке (1872). Вещество в смеси с CuO наносят на медную (или платиновую) проволоку и вносят в пламя; образующиеся при этом летучие галогениды меди окрашивают пламя в зеленый или голубовато-зеленый цвет.
Реактив Бенедикта (проба Бенедикта) [Benedict’s reagent, Benedict’s test]. Обнаружение алифатических альдегидов действием на них водного раствора, содержащего сульфат меди(II) CuSO4, карбонат натрия Na2CO3 и цитрат натрия. При нагревании образуются красные, желтые, зеленые осадки.
Реакция Бородина Разложение карбамида:
Реакция Бутлерова-Лермонтовой-Эльтекова Получение углеводородов изостроения каталитическим алкилированием низших олефинов алкилгалогенидами (1878).
Реакция Вагнера (окисление по Вагнеру, перманганатная проба).Окисление органических соединений, содержащих двойную связь, действием 1-3%-го раствора перманганата калия (1887) в цис-a-гликоли в щелочной среде (считается положительной, если раствор перманганата быстро обесцвечивается в кислой среде или буреет в щелочной и нейтральной):
Реакция Вёлера Взаимодействие карбида кальция с водой (1862). Практическое значение реакция приобрела после того, как А.Муассан и Т.Вильсон разработали способ дешевого получения карбида кальция в электропечи в результате сплавления кокса и извести (1892).
Реакция Вильямсона (метод Вильямсона) [Williamson’s synthesis]. Получение простых эфиров из алкилгалогенида и алкоголята натрия (или калия):
Реакция Вюрца. [Wurtz reaction]. Синтез алканов действием металлического натрия в инертном растворителе на алкилгалогениды (1855):
в общем виде:
Реакция Вюрца-Фиттига. [Wurtz-Fittig reaction]. Получение алкилбензолов из смеси алифатических и ароматических галогенидов действием металлического натрия в инертном растворителе (1864):
Реакция Гарриеса. (1866-1923), профессор (Германия). Основные исследования посвящены химии каучука. Президент Немецкого химического общества (1920-1922). Образование озонидов.
Реакция Гаттермана. Получение ароматического альдегида при взаимодействии фенола с хлороводородом и циановодородом в присутствии катализаторов (кислот Льюиса) с последующим гидролизом продукта (1898):
Правила ориентации Голлемана Ориентанты (заместители) первого рода (CH3, C2H5, галогены, аминогруппа, гидроксил) повышают реакционную способность ароматического ядра и направляют реагенты в орто- и параположения.
2. Ориентанты (заместители) второго рода (нитро- и сульфогруппы, карбоксильная и карбонильная группы) уменьшают реакционную способность ароматического ядра и направляют реагенты в метаположение (1895). (В настоящее время эти эффекты объясняются на основе электронных представлений: мезомерные и индукционные эффекты, 1920 г.).
Реакция Гофмана. Получение алифатических аминов из алкилгалогенидов:
и так далее до образования третичного амина (CH3)3N.
Реактив Гриньяра. [Grignard reagent] Синтез органических веществ из алкилгалогенидов и магния в эфире. Реакция открыта П.Барбье в 1899 г. и подробно изучена В.Гриньяром в 1900 г.:
Реактив Гриньяра RMgX используется для присоединения по кратным связям
Реакция Густавсона. Получение циклоалканов из дигалогенпроизводных (1887).
Реакция Дильса-Альдера (диеновый синтез) Присоединение ненасыщенного соединения, кратная связь которого активирована соседней группой (такое соединение имеет название «диенофил«: акролеин, малоновый ангидрид, кротоновый альдегид), к ненасыщенному углеводороду (диену), имеющему сопряженные двойные связи (бутадиен, циклогексадиен, антрацен, фуран) (1928).
Правило Зайцева. Отщепление галогеноводородных кислот от алкилгалогенидов или воды от спиртов преимущественно происходит так, что с галогеном или гидроксилом уходит водород от наименее гидрогенизованного соседнего атома углерода (1875):
Реакция Зелинского-Казанского (метод Зелинского-Казанского). Тримеризация ацетилена (полимеризация ацетилена) на активированном угле при нагревании (1924):
Реакция Зелинского (необратимый катализ, катализ Зелинского)Каталитическое диспропорционирование циклогексадиена и циклогексена (1911):
Реакция Зинина. Восстановление ароматических нитросоединений (1842):
Реакция Канниццаро [Cannizzaro reaction]. Окислительно-восстановительное диспропорционирование двух молекул ароматического альдегида в щелочной среде, приводящее к образованию спирта и кислоты (1853):
Реакция Кирхгофа. Получение глюкозы гидролизом крахмала при его нагревании с катализатором — разбавленной серной кислотой (1811):
Реакция Клемменсена (восстановление по Клемменсену). Восстановление альдегидов и кетонов в гомологи бензола водородом в момент его выделения (восстановление карбонильной группы до метиленовой) (1913):
Реакция Кольбе-Шмитта. Получение ароматических оксикислот карбоксилированием фенолятов щелочных металлов (1860):
Реакция Кольбе (электрохимическая). Получение алканов с четным числом атомов углерода электролизом растворов солей щелочных металлов и карбоновых кислот с неразветвленной углеродной цепью (1849):
Реакция Коновалова. Получение нитроалканов (1888):
Реакция Кучерова (гидратация по Кучерову). Каталитическая гидратация ацетиленовых углеводородов с образованием карбонилсодержащих соединений (1881):
Реакция Лебедева. Получение бутадиена пиролизом этанола (1926):
Реакция Львова-Шешукова. Хлорирование олефинов в a-положение к двойной связи, сопровождающееся аллильным сдвигом двойной связи (1883):
Правило Марковникова. В случае присоединения водородсодержащих соединений (протонных кислот или воды) к несимметричному алкену атом водорода преимущественно присоединяется к наиболее гидрогенизованному атому углерода, стоящему при двойной связи (1869):
Реакция Настюкова (формалитовая реакция). Взаимодействие ароматических углеводородов с формальдегидом (определение ароматических углеводородов) в присутствии концентрированной серной кислоты (1904):
Образование красно-коричневой смолы подтверждает наличие бензола и его гомологов. Реакции мешает присутствие непредельных циклических соединений.
Правило Несмеянова-Борисова. Электрофильные и радикальные замещения у углеродного атома, связанного двойной углерод-углеродной связью, происходят с сохранением геометрической конфигурации молекулы вещества.
Реакция Раймера-Тимана. Получение ароматических о-оксиальдегидов взаимодействием фенола с хлороформом в растворе щелочи. Реакция приводит к введению альдегидной группы в бензольное кольцо (замещение обычно происходит в ортоположение):
Реакция Розенмунда. Получение ароматических альдегидов из хлорангидридов кислот в среде бензола, толуола и других ароматических углеводородов:
Реакция открыта М.М.Зайцевым в 1872 г. и подробно изучена К.В.Розенмундом в 1918 г.
Реакция Сабатье-Сандерана. Жидкофазное гидрирование этилена до этана в присутствии мелкораздробленного никеля как катализатора (1899):
Реакция Савича. Получение алкинов из дигалогенпроизводных алканов (1861):
Проба Селиванова. Качественное открытие фруктозы (1887) (кетозы при нагревании с резорцином и соляной кислотой дают вишнево-красное окрашивание; альдозы в этих же условиях взаимодействуют медленнее и дают бледно-розовую окраску):
(Можно использовать раствор, состоящий из 0,05 г резорцина в 50 мл воды и нескольких капель концентрированной соляной кислоты плотностью 1,19 г/мл.)
Реакция Тищенко. Диспропорционирование альдегида — получение сложного эфира из альдегида — в присутствии алкоголята алюминия (1906):
Проба Толленса (реакция «серебряного зеркала»). Взаимодействие формальдегида с аммиачным раствором оксида серебра (реактив Толленса):
Реакция Ульмана. Получение высших ароматических гомологов из арилгалогенидов действием порошкообразной меди:
Реакция Фаворского. Конденсация карбонильных соединений с алкинами с образованием ацетиленовых спиртов:
Синтез Фишера-Тропша. Получение алканов при каталитическом гидрировании (взаимодействие с водородом) монооксида углерода под давлением (1923).
Реакция Фокина. Гидрогенизация жиров (1902):
Реакция Фриделя-Крафтса. Алкилирование или ацилирование ароматических соединений соответственно алкил- или ацилгалогенидами (получение гомологов бензола) в присутствии безводного катализатора (AlCl3, BF3, ZnCl2 и др.) (1877):
Реакция Чугаева (ксантогеновая реакция). Превращение спиртов в алкены термическим разложением ксантогеновых эфиров, получаемых из этих спиртов (1902).
Крекинг по Шухову. Высокотемпературная переработка нефтяного сырья для получения продуктов меньшей молекулярной массы — расщепление углеводородов нефти (1891).
Правило Эльтекова (перегруппировка Эльтекова). Соединения, в которых гидроксильная группа находится при углеродном атоме, образующем углерод-углеродную кратную связь (енолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения — альдегиды или кетоны (1877):
Реакция Юрьева. Взаимные превращения 5-членных гетероциклических соединений, содержащих один гетероатом (1936).
Именные органические реакции
10-Дек-2012 | Нет комментариев | Лолита Окольнова
Именные органические реакции

В органической химии существует огромное число реакций, носящих имя исследователя, открывшего или исследовавшего данную реакцию.
Именные реакции можно найти во многих справочниках по органической химии, но я хочу разделить их по классам химических соединений. И, конечно, это далеко не все именные реакции, это те реакции, которые часто встречаются в школьном курсе органической химии.
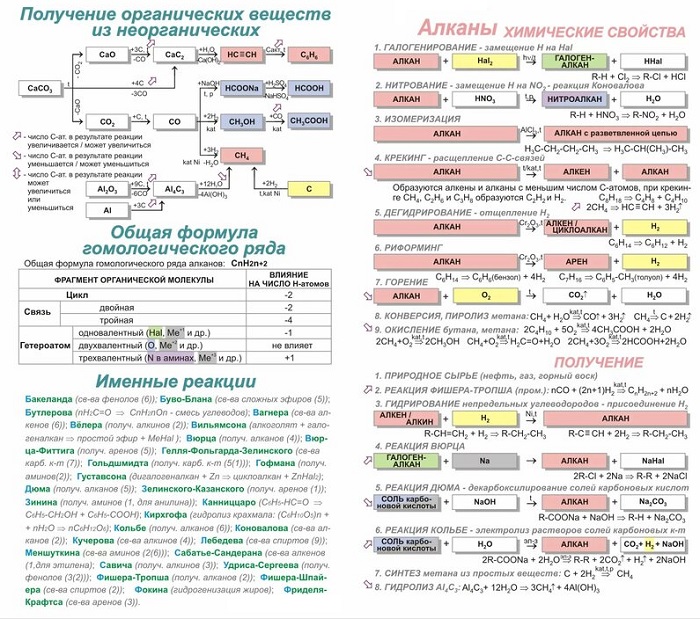
Именные реакции алканов:
- Реакция Вюрца — «именная» реакция удлинения цепи, а точнее, удвоение количества атомов углерода:
C2H5Cl + 2Na +ClC2H5 → C4H10 + 2NaCl (из этана получили бутан)
- Реакция Коновалова: c разбавленной азотной кислотой под давлением алканы нитруются:
С2H6 + HNO3 (HO-NO2) → С2H5NO2 + H2O (нитроэтан)
- Еще одна «именная» реакция: реакция Кольбе: электролиз солей карбоновых кислот:
2СH3COONa -(электролиз)-→ СH3-CH3 (этан) + 2СO2 +2Na
Именные реакции алкенов:
- Присоединение по правилу Марковникова:
водород присоединяется к наиболее гидрогенезированному (= к тому, у которого больше водородов) атому углерода при двойной связи:
СH2=CH-CH3 + HCl = CH3-CHCl-CH3
- Обратная реакция — дегидрирования — правило Зайцева — водород отнимается от самого ненасыщенного водородами (наименее гидрогенизированного) атома углерода.
Именные реакции алкинов:
- реакция Кучерова
CH3-C≡CH + H2O -> (катализатор — Hg2+) -> CH3-C(=O)-CH3
- реакция Зелинского
Именные реакции аренов:
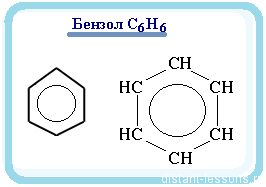
- Ту структурную формулу, которую мы сейчас используем — «скворечник», называют формулой Кекуле:
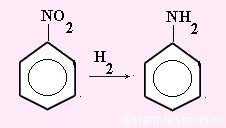
- Реакция Зинина — восстановление нитробензола и его нитрогомологов:
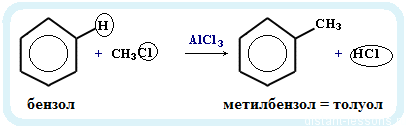
- Реакция Фриделя-Крафтца — алкилирование аренов:
Как это может быть применимо в ЕГЭ? Представьте себе, было как-то такое задание в части В:
Соотнесите именную реакцию или правило с той или иной реакцией или нужным правилом
1. Реакция Вюрца 1. 2CH3CH2OH → CH2=CH–CH=CH2 (+ H2; + 2H2O)
2. Реакция Кучерова 2. R–H + HNO3 → R–NO2 (+ H2O)
3. Реакция Зелинского 3. 2C2H5I + 2Na → н-C4H10 (+ 2NaI)
4. Реакция Коновалова 4. цикло-C6H12 → C6H6 (+ 3H2)
5. Реакция Зинина 5. C2H2 + H2O → CH3CHO
6. Реакция Бутлерова 6. C6H5NO2 + H2 (H+) → C6H5NH2
7. Правило Марковникова 7. CH3CH2CH(OH)CH3 → CH3CH=CHCH3 (+ H2O)
8. Правило Зайцева 8. CH3CH2CH=CH2 + HCl → CH3CH2–CHCl–CH3
Вообще, такие задания — именные реакции -редкость в ЕГЭ, но лучше знать, чем потом ломать голову над такой задачкой! Да и повторить еще раз основные органические реакции — не лишнее.
Обсуждение: «Именные органические реакции»
(Правила комментирования)
Именные
реакции в органической химии
Получение
1.
Реакция Вюрца:
действие металлического натрия на
моногалогенопроизводные углеводородов.
Происходит удвоение углеродного скелета.
Реакция подходит для получения
симметричных алканов.
2CH3–CH2Br
+ 2Na = CH3–CH2–CH2–CH3
+2NaBr
2.
Реакция Дюма:
декарбоксилирование солей карбоновых
кислот — сплавление со щелочами.
CH3COONa
(тв.) + NaOH(тв.) = CH4
+ Na2CO3
3.
Реакция Кольбе:
электролиз растворов солей карбоновых
кислот:
CH3COONa +
2H2O
=[эл.ток]=> 2СО2
+ Н2
+ С2Н6
+ 2NaOH
4.
Синтез Густавсона:
отщепление двух атомов галогена от
дигалогеналканов:
СlCH2-CH2-CH2-CH2Cl + Zn = C4H8
(циклобутан) + ZnCl2
Вместо
магния может использоваться цинк.
5.
Синтез Лебедева:
получение бутадиена из этанола.
2C2H5OH
= Н2
+ 2Н2O
+ CH2=CH-CH=CH2
Химические
свойства
1.
Реакция Коновалова
– нитрование алканов разбавленной
(10%-ной) азотной кислотой:
C2H6
+ HNO3
= C2H5NO2
+ Н2O
Избирательность
нитрования:
третичный
атом > вторичный атом > первичный
атом углерода.
2.
Эффект
Хараша:
присоединение бромоводорода в присутствии
перекиси. Реакция протекает против
правила Марковникова:
СН3-СН=СН2
+ HBr =[Н2О2]=>
СН3-СН2-СН2Br
3.
Реакция Вагнера:
реакция с холодным водным раствором
перманганата калия – мягкое окисление
алкенов (образуется диол)
3СН3-СН=СН2
+ 2KMnO4
+ 4H2O
= 2MnO2
+ 2KOH + 3СН3
-СН(OH)-СН2(OH)
4.
Реакция Кучерова:
гидратация алкинов. Присоединение воды
происходит в присутствии солей ртути (II)
и идет через образование неустойчивого
енола, который изомеризуется в альдегид
или кетон. Гидратация ацетилена дает
альдегид, других алкинов – кетон.
C2H2
+ H2O
= CH3CHO
5.
Реакция Зелинского:
тримеризация ацетилена над активированным
углем. Образуется бензол.
3C2H2
= C6H6
6.
Реакция Зинина:
восстановление нитросоединений в
растворе в щелочной и нейтральной
среде:
R-NO2
+ 3(NH4)2S
= R-NH2
+ 3S + 6NH3
+2H2O
7. Реакция
Фриделя-Крафтса: алкилирование и
ацилирование аренов и их производных
в присутствии безводного AlCl₃. Классический
пример — алкилирование бензола
алкилгалогенидами (HCl, HBr, HI). Общий вид
реакции: C₆H₆+ R-Hal =[AlCl₃]=> C₆H₅-R +
HHal
Реакция на примере хлора: C₆H₆+
CH₃Cl =[AlCl₃]=> C₆H₆-CH₃ + HCl
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- Реакция Вюрца (удлинение углеродной цепи алканов):
CH3–Br+2Na+Br–CH2–CH3⟶tCH3–CH2–CH3+2NaBr
- Реакция Дюма (декарбоксилирование солей карбоновых кислот — сплавление со щелочами):
CH3COONa(тв.)+NaOH(тв.)=CH4+Na2CO3
- Реакция Кольбе (электролиз растворов солей карбоновых кислот):
CH3COONa+2H2O−→−−эл.ток2CO2+H2+C2H6+2NaOH
- Реакция Вюрца–Фиттига (получение гомологов бензола из галогенбензола):
C6H5–Br+2Na+Br–CH3⟶C6H5–CH3+2NaBr
- Реакция Кучерова (гидратация алкинов):
CH≡CH+H2O−→−−−−−Hg2+,H+[CH2=CH–OH]−→−−−−−−изомеризацияH3C–C(=O)H
- Реакция Зелинского (тримеризация ацетилена):
CH≡CH−→−−−−−−−t>400∘C,CактC6H6
- Реакция Зелинского–Казанского (получение бензола из циклогексана):
C6H12−→−−−−−−−−−420–480∘C,Pd,PtC6H6+3H2
- Реакция Коновалова (нитрование алканов):
CH3–CH2–CH3+HNO2−→−−−−−110–140∘CCH3–CH(NO2)–CH3+H2O
- Реакция Зинина (восстановление нитробензола до анилина):
C6H5–NO2⟶[H]C6H5–NH2+2H2O
- Реакция Густавсона (получение циклоалкана из дигалогенопроизводных):
Br–CH2–CH2–CH2–Br+Zn−→−−−−−20∘C,спиртциклопропан
- Реакция Фриделя–Крафтса (алкилирование бензола):
C6H6+Cl–CH3⟶AlCl3C6H5–CH3+HCl
C6H6+H2C=CH–CH3⟶AlCl3 C6H5–CH(CH3)–CH3
- Реакция Прилежаева (каталитическое окисление этилена с получением эпоксида):
2CH2=CH2+O2−→−−−−−200∘C,Ag+эпоксид этилена
- Реакция Вагнера (мягкое окисление алкенов):
CH3–CH=CH2+H2O+[O]−→−−−−−−−20∘C,KMnO4H3C–CH(OH)–CH2–OH
- Реакция Лебедева (получение бутадиена-1,3):
2C2H5OH−→−−−−−−−−−−−−400–500∘C,Al2O3,ZnOCH2=CH–CH=CH2+2H2O+H2