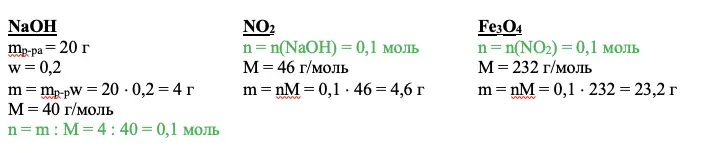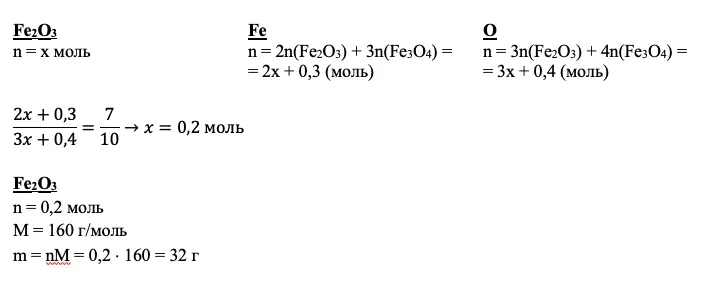5 апреля 2017
В закладки
Обсудить
Жалоба
Полезная информация по оформлению заданий с развернутым ответом и критерии оценивания. Памятка основана на демоверсии текущего года.
В задачах 33 и 34 единого правила оформления нет, но решение должно быть записано четко и логично, а все величины соотноситься с веществами.
Источник: vk.com/chem4you
himiya-30-34.pdf
Ни для кого не секрет, что задача 33 (она же бывшая задача 34) в ЕГЭ по химии — самое сложное задание, а судя по статистике (только 8,3% выпускников справляются с ним), она еще и практически невыполнимая. Поэтому значительное число выпускников даже не читают условие этой задачи. А зря. Если вы пришли на экзамен по химии, то уж точно сможете записать несколько уравнений, ведь так?
Задача 33 по химии: суть и критерии оценивания
Задание № 33 в ЕГЭ по химии — это расчетная задача высокого уровня сложности. Чтобы успешно решить ее, вам необходимо знать химические свойства веществ, уметь устанавливать логические связи между реакциями, применять расчетные формулы для нахождения количества вещества, массы и объема, массовой доли вещества в смеси.
Для получения максимально возможных 4 баллов за задачу 33 вам предстоит:
- записать все уравнения реакций, описанных в тексте (1 балл);
- рассчитать количества вещества всех известных и искомых веществ (1 балл);
- провести анализ и рассчитать искомые величины (1 балл);
- дать правильный ответ и безошибочно оформить решение (1 балл; снимается за отсутствие размерных величин — больше трех, также за математические ошибки)
Но слова в сторону, нам нужна успешная пошаговая стратегия: что делать, чтобы не получить за этот номер 0?
ЕГЭ по химии — в принципе достаточно сложный экзамен. Чтобы получить за него высокий балл, нужно хорошо постараться. Так, необходимо хорошо знать теорию и формулы, уметь выводить уравнения без ошибок, понимать, как правильно читать задания (в них могут быть ловушки!) и оформлять ответы по критериям. И все это — за ограниченный период времени.
Чтобы не стрессовать на экзамене и показать лучший результат, записывайтесь ко мне на курсы подготовки к ЕГЭ по химии. Мы изучим только то, что гарантированно пригодится вам на экзамене: ничего лишнего, только актуальные знания. А пробные экзамены, которые мы обязательно проводим, помогут понять, что ЕГЭ — совсем не такое страшное. Приходите к нам — за знаниями и спокойствием!
Пошаговый разбор реального задания 33
Уровень «Новичок»
Вы выбрали химию для поступления и готовилист к ЕГЭ минимум год. Вам абсолютно под силу записать уравнения реакций, описанных в тексте. Чаще всего здесь встречаются реакции обмена, замещения и разложения, ОВР, электролиз и совместный гидролиз. Правильно записанные реакции с расставленными коэффициентами дают 1 первичный балл за 33 задачу в ЕГЭ по химии.
ШАГ 1. Запишите все уравнения реакций, о которых идет речь в тексте
Если возможны вариации одной и той же реакции, рассмотрите их на черновике (например, получение средних/кислых солей, образование амфотерного гидроксида/ комплексной соли и т.п.). Какую реакцию оставить, вы поймете после получения первых результатов расчета.
Совет: повторите перед экзаменом тривиальные названия. Например, если вы не знаете, что такое «железная окалина», то ни записать реакцию, ни решить данную задачу не удастся 🙃
Смесь железной окалины и оксида железа III растворяют в азотной концентрированной кислоте. Запишем их по очереди. Железная окалина содержит железо в степени окисления +2, отсюда и протекание окислительно-восстановительной реакции: железо повышает степень окисления до +3, а азот изменяет свою степень окисления с +5 до +4. Вторая реакция представляет собой классическую реакцию обмена:
Fe3O4 + 10HNO3 = 3Fe(NO3)3 + NO2 + 5H2O
Fe2O3 + 6HNO3 = 2Fe(NO3)3 + 3H2O
Образовавший газ (это NO2, полученный в первой реакции) взаимодействует с гидроксидом натрия:
2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
ИТОГО: +1 балл
С одним пунктом вы справились. Далее запишите «дано». Баллов за эту запись вам не добавят, но при этом вы сможете увидеть все известные величины и помнить, что необходимо найти.
Дано:
N(Fe) : N(O) = 7 : 10
mp-p(HNO3) = 500 г
mp-p(NaOH) = 20 г
w(NaOH) = 20%
Найти:
w(Fe(NO3)3) — ?
Уровень «Мастер»
Вы готовы сделать больше, чем записать уравнения реакции. Вы помните основные расчетные формулы и можете найти количество вещества по заданной массе и объему.
ШАГ 2. Используйте известные числовые значения, чтобы рассчитать количества вещества всех необходимых участников реакций
Переходим к действию. Нужно найти вещество, о котором мы все знаем. В приведенном примере это гидроксид натрия. Необходимо рассчитать количество вещества. Используем для этого основные расчетные формулы:
NaOH
mp-pa = 20 г
w = 0,2
m = mp-pw = 20 × 0,2 = 4 г
М = 40 г/моль
n = m : M = 4 : 40 = 0,1 моль
Задаем себе вопрос: что нам дает это значение? Каждый ответ должен вести к следующему действию. Так, мы можем рассчитать количество оксида азота IV – NO2, а благодаря ему получим количество вещества Fe3O4.
Совет: в задаче 33 по химии рассчитывайте сразу и количество вещества, и массу любого соединения, с которым работаете. Эти массы пригодятся при нахождении итогового раствора. А если не пригодятся, не переписывайте их в чистовик.
ИТОГО: +1 балл
Уровень «Гуру»
Вас не пугает уравнение с иксом в химии. Более того, вы можете его и составить, и решить.
ШАГ 3. Продумайте, как от найденных количеств вещества дойти по цепочке до искомого соединения
Что нужно найти дополнительно, чтобы получить ответ в задаче 33 по химии? Здесь может пригодиться работа с переменными, пропорции, соотношения и даже составление системы уравнений с двумя неизвестными.
Работаем!
Мы получили количества вещества нескольких соединений. Но так и не добрались до второй реакции и Fe2O3. Кроме того, мы не использовали соотношение атомов. Если вам ничего не дано для вещества по условию, а также вам не удалось подойти к нему через промежуточные расчеты, дело за уравнением. За х всегда принимайте количество неизвестного вещества.
Для нашего примера получим:
Совет: не пытайтесь принять за х все, что не получается рассчитать. Чаще всего задача 33 по химии решается без каких-либо переменных.
ИТОГО: +1 балл
Уровень «Профессионал»
Самое сложное уже позади. Теперь вам остается грамотно довести до конца. Обычно в завершении задачи требуется рассчитать массу полученного раствора и массовую долю вещества в нем. Чтобы не допустить ошибку на последнем этапе, помним, что в раствор входят все вещества, описанные в условии задачи, за исключением веществ, участвующих в реакциях сплавления, разложения и горения. Также обязательно нужно вычесть из этой массы потери. Потерями считаем осадки, газы, выпаренную воду, непрореагировавшие металлы и их оксиды.
ШАГ 4. Внимательно прочитайте вопрос задачи и рассчитайте искомую величину
Чаще всего необходимо вычислять массовую долю вещества в растворе. Предварительно вычислите массу полученного раствора с учетом всех потерь — осадков, газов и т.п.
В приведенном примере в раствор входит смесь железной окалины и оксида железа (III) и раствор азотной кислоты. Потеря — газообразное вещество NO2 (он же бурый газ).
mp-pa = m(Fe3O4) + m(Fe2O3) + mp-p(HNO3) – m(NO2) = 23,2 + 32 + 500 – 4,6 = 550,7 г
Зная количества вещества оксидов, вычислим количество вещества и массу искомой соли, а также ее массовую долю:
ИТОГО: +1 балл
Вот вы и решили 33 задачу в ЕГЭ по химии. Сложная ли она? Безусловно. Но можно ли с ней побороться? Да! Помните, что это задание, как и любое другое из второй части, оценивают согласно критериям. Не оставляйте его совсем без решения. Вы сможете остановиться на любом этапе и при этом принести в свою копилку больше, чем 0 баллов. А в пересчете на 100-балльную шкалу это будет уже весомо!
А если хотите научиться пошагово решать и другие задания из ЕГЭ по химии, записывайтесь ко мне на курсы подготовки к экзамену. Мы разберемся во всей теории, будем тренироваться в практических заданиях и научимся оформлять ответы в полном соответствии с критериями. Не теряйте возможность получить 80+ за ЕГЭ по химии — записывайтесь.
Александр Есманский,
преподаватель Олимпиадных школ МФТИ по химии, репетитор ЕГЭ и ОГЭ,
автор и составитель методических разработок
Задание № 30
Что требуется
Из предложенного перечня веществ необходимо выбрать те, между которыми возможно протекание окислительно-восстановительной реакции (ОВР), записать уравнение этой реакции и подобрать в ней коэффициенты методом электронного баланса, а также указать окислитель и восстановитель.
Особенности
Это одно из самых сложных заданий ЕГЭ по предмету, поскольку оно проверяет знание всей химии элементов, а также умение определять степени окисления элементов. По этим данным нужно определить вещества, которые могут быть только окислителями (элементы в составе этих веществ могут только понижать степень окисления), только восстановителями (элементы в составе этих веществ могут только повышать степень окисления) или же проявлять окислительно-восстановительную двойственность (элементы в составе этих веществ могут и понижать, и повышать степень окисления).
Также в задании необходимо уметь самостоятельно (без каких-либо указаний или подсказок) записывать продукты широкого круга окислительно-восстановительных реакций. Кроме того, нужно уметь грамотно оформить электронный баланс, после чего перенести полученные в балансе коэффициенты в уравнение реакции и дополнить его коэффициентами перед веществами, в которых элементы не изменяли степеней окисления.
Советы
Окислительно-восстановительные реакции основаны на принципе взаимодействия веществ противоположной окислительно-восстановительной природы. Согласно этому принципу любой восстановитель может взаимодействовать практически с любым окислителем. В задаче № 30 окислители и восстановители часто подобраны таким образом, что между ними точно будет протекать реакция.
Для нахождения пары окислитель/восстановитель нужно, прежде всего, обращать внимание на вещества, содержащие элементы в минимальной и максимальной степени окисления. Тогда вещество с минимальной степенью окисления будет являться типичным восстановителем, а вещество с максимальной степенью окисления с большой долей вероятности окажется сильным окислителем.
Если в списке только одно вещество (вещество 1) содержит элемент в максимальной или минимальной степени окисления, нужно найти ему в пару вещество, в котором элемент находится в промежуточной степени окисления и может проявлять свойства и окислителя, и восстановителя (вещество 2). Тогда вещество 1 определит окислительно-восстановительную активность вещества 2.
Когда пара окислитель/восстановитель определена, нужно обязательно проверить, в какой среде (кислой, нейтральной или щелочной) может протекать эта реакция. Если нет особенных правил, связанных со средой протекания выбранной реакции, то в качестве среды следует выбрать водный раствор того вещества (кислоты или щелочи), которое есть в предложенном списке реагентов.
Чтобы верно записать продукты окислительно-восстановительной реакции, нужно знать теоретические сведения о химии того или иного вещества и специфику его свойств. Однако запоминать все реакции наизусть — дело утомительное, да и не очень полезное. Для того чтобы упростить задачу, можно выявить некоторые общие закономерности в протекании ОВР и научиться предсказывать продукты реакций. Для этого нужно следовать трем простым правилам:
- Процессы окисления и восстановления — это две стороны единого процесса: процесса передачи электрона. Если какой-либо элемент (восстановитель) отдает электроны, то в этой же реакции обязательно должен быть какой-то элемент (окислитель), который принимает эти электроны.
- Если в реакции участвует простое вещество, эта реакция — всегда окислительно-восстановительная.
- При взаимодействии сильных окислителей с различными восстановителями обычно образуется один и тот же основной продукт окисления. Многие окислители при взаимодействии с различными восстановителями также часто восстанавливаются до какого-то одного продукта, соответствующего их наиболее устойчивой степени окисления.
Задание № 31
Что требуется
Из предложенного перечня веществ (того же, что и в задании № 30) необходимо выбрать такие вещества, между которыми возможна реакция ионного обмена. Необходимо записать уравнение реакции в молекулярной форме и привести сокращенную ионную форму.
Особенности
Это задание значительно легче предыдущего, поскольку круг возможных реакций ограничен и определен условиями протекания реакций ионного обмена, которые школьники изучают еще в 8-9 классах.
Советы
Нужно помнить, что любая реакция ионного обмена — это обязательно реакция, протекающая в растворе. Все реакции ионного обмена являются неокислительно-восстановительными!
В реакциях ионного обмена могут участвовать:
- солеобразующие оксиды;
- основания и амфотерные гидроксиды;
- кислоты;
- соли (средние, кислые, основные). Теоретически можно составить реакцию ионного обмена с участием смешанных, двойных или комплексных солей, но это для задания № 31 — экзотика.
Чаще всего в этой задаче встречаются реакции ионного обмена с участием оснований, амфотерных гидроксидов, кислот и средних солей. Однако обмен ионами может осуществляться далеко не с любыми парами веществ. Для того чтобы протекала реакция ионного обмена, необходимо выполнение некоторых ограничительных условий, которые связаны с реагентами и продуктами реакции.
Для написания ионных форм уравнений нужно следовать правилам, согласно которым одни вещества представляются в диссоциированной форме (в виде ионов), а другие — в недиссоциированной (в виде молекул).
Расписываем на ионы в реакциях ионного обмена:
- растворимые сильные электролиты;
- малорастворимые сильные электролиты, если они являются реагентами.
Не расписываем на ионы в реакциях ионного обмена:
- неэлектролиты;
- нерастворимые в воде вещества;
- слабые электролиты;
- малорастворимые сильные электролиты, если они являются продуктами реакции.
Когда уже сокращенная форма реакции ионного обмена записана, будет нелишним проверить для нее выполнение материального и электрического баланса. Другими словами, верно ли расставлены в сокращенной форме коэффициенты и сохраняется ли общий электрический заряд в левой и правой частях уравнения. Это позволит избежать потерянных коэффициентов или зарядов ионов на пути от молекулярной формы через полную ионную — к сокращенной.
Задание № 32
Что требуется
По приведенному текстовому описанию необходимо записать уравнения четырех реакций.
Особенности
Это задание так же, как и задание № 30, проверяет знание всей химии элементов, которая содержится в спецификации ЕГЭ. Однако часто составление четырех уравнений, описанных в задании № 32, является более простой задачей, чем составление одного уравнения в вопросе № 30. Во-первых, здесь не нужно самостоятельно выбирать реагенты, поскольку они уже даны в условии, а продукты часто можно угадать, используя данные условия, которые, по сути, являются подсказками. Во-вторых, из четырех описанных в задании уравнений, как правило, два можно записать, используя знания 8-9 классов. Например, это могут быть реакции ионного обмена. Два других уравнения — посложнее, подобные тем, которые предлагаются в задании № 30.
Советы
Конечно, можно просто выучить всю химию элементов наизусть и с ходу записать все уравнения. Это самый верный способ. Если же возникают трудности с определением продуктов, то нужно по максимуму использовать подсказки, приведенные в условии. Чаще всего в задании указываются наблюдаемые химические явления: выпадение или растворение осадков, выделение газов, изменение цвета твердых веществ или растворов. А если еще и указан конкретный цвет осадка, газа или раствора, можно с высокой точностью определить, о каком веществе идет речь. Для этого необходимо всего лишь знать цвета наиболее часто использующихся в задачах школьной программы осадков и газов, а также цвета растворов солей. Это сильно облегчит написание проблемного уравнения реакции, и задание № 32 покажется очень даже простым.
Задание № 33
Что требуется
Необходимо записать уравнение пяти реакций с участием органических веществ по приведенной схеме (цепочке превращений).
Особенности
В этом задании предлагается классическая цепочка превращений, какие школьники учатся решать с первого года изучения химии, только здесь в каждом уравнении участвует хотя бы одно органическое вещество. Задача на каждой стадии цепочки может быть сформулирована в двух вариантах. В первом варианте даются один из реагентов и продукт реакции. В этом случае необходимо подобрать второй реагент, а также указать все условия осуществления реакций (наличие катализаторов, нагревание, соотношение реагентов). Во втором варианте известны все реагенты, а часто и условия реакции. Необходимо только записать продукты.
Советы
Лучший способ успешно выполнить цепочку по органике — это знать наизусть все типы реакций каждого класса соединений и специфические свойства органических веществ, содержащиеся в школьном курсе органической химии.
Главное правило задания № 33 — использование графических (структурных) формул органических веществ в уравнениях реакций. Это указание обязательно прописано в каждом варианте тренировочных работ и пробных вариантов ЕГЭ по химии, поэтому известно всем выпускникам. Однако некоторые школьники все равно иногда пренебрегают этим правилом и часть органических веществ записывают в молекулярном виде. Будьте внимательны! Уравнения реакций с молекулярными формулами органических веществ в этом задании не засчитываются.
В задачах № 32 и № 33 уравнение считается написанным верно, если в нем расставлены все коэффициенты и при необходимости указаны условия протекания реакции. Уравнения реакций, в которых хотя бы один коэффициент неверен или не указаны важные условия, не засчитываются.
Задание № 34
Что требуется
Решить расчетную задачу, тематика которой меняется от года к году и от варианта к варианту.
Особенности
В спецификации ЕГЭ под номером 34 заявлены задачи с использованием понятия доли (массовой, объемной, мольной) вещества в смеси. Частным случаем таких задач являются задачи «на массовую долю вещества в растворе», задачи «на примеси», то есть с использованием понятия доли чистого вещества в составе технического. Сюда же относятся расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного, а также расчеты по уравнению реакции, если один из реагентов дан в избытке.
Предсказать, какие задачи будут отобраны для ЕГЭ именно в этом году, практически невозможно. Единственное, что можно ожидать по опыту прошлых лет, — это то, что задача не окажется сложной и будет полностью соответствовать профильной школьной программе (не олимпиадной). Это значит, что такая задача по зубам любому школьнику, освоившему курс химии на профильном школьном уровне и обладающему обыкновенной математической и химической логикой.
Советы
Для того чтобы решить эту задачу, прежде всего, нужно знать базовые формулы и определения основных физических величин. Необходимо осознать понятие «математической доли» как отношения части к целому. И тогда все типы долей в химии принимают одинаковый внешний вид.
| Массовая доля вещества в смеси | ({omega_{1}} = {{m_{в-ва}} over m_{смеси}}) |
| Массовая доля вещества растворе | ({omega_{1}} = {{m_{в-ва}} over m_{р-ра}}) |
| Мольная доля вещества в смеси (растворе) | ({chi} = {{nu_{в-ва}} over nu_{смеси}}) |
| Объемная доля вещества в смеси (растворе) | ({varphi} = {{V_{в-ва}} over V_{смеси}}) |
| Доля чистого вещества в составе технического (степень чистоты) | ({omega_{чист}} = {{m_{чист}} over m_{техн}}) |
| Доля выхода продукта от теоретически возможного (выход продукта) |
({eta} = {{upsilon_{практ}} over upsilon_{теор}} = {{m_{практ}} over m_{теор}} )
(m_{практ}) — масса продукта, которая получилась в результате химической реакции (m_{теор}) — масса продукта, которая могла образоваться в соответствии с теоретическим расчетом по уравнению реакции |
| Количество вещества |
({v} = {m over M} )
([{v}] = моль ) ({nu} = {{V} over V_{m}}) Молярный объем, т.е. объем одного моля газа, одинаков для всех газов при одинаковых условиях |
| Молярная концентрация (молярность) вещества в растворе |
({C} = {{v_{в-ва}} over V_{р-ра}} )
([{C}] = {моль over л} = М) |
| Плотность раствора |
({rho} = {{m_{р-ра}} over V_{р-ра}} )
([{rho}] = {г over мл} = {г over см^3} ) |
Задание № 35
Что требуется
Решить расчетную задачу на установление молекулярной и структурной формулы вещества, записать предложенное уравнение реакции с данным веществом.
Особенности
Идеологическая часть задач на вывод формулы изучается школьниками еще в 8-9 классах, поэтому это наиболее простая задача части 2 ЕГЭ. Хотя в спецификации не указано, формулу какого вещества необходимо установить. Опыт показывает, что из года в год здесь традиционно участвуют органические вещества.
Советы
Все задачи на вывод формулы, встречающиеся в ЕГЭ, можно условно разделить на три типа. Первый тип — это установление формулы по массовым долям элементов в веществе. Здесь работает формула для массовой доли элемента в сложном веществе:
({omega} = {n times {A_{r}(элемента)} over {M_{r}(вещества)}} times 100 %)
где n — число атомов элемента в молекуле, то есть индекс элемента.
Иногда в этом типе задач нужно знать еще и общую формулу класса, к которому относится неизвестное органическое вещество. Затем следует выразить относительную молекулярную массу вещества через n и подставить в уравнение для массовой доли. Решением уравнения будет искомое значение n, а следовательно, и молекулярная формула вещества. Дополнительные сведений о веществе, указанные в условии задачи, позволяют установить структурную формулу вещества, с которой далее требуется записать уравнение реакции.
Второй тип задач — это установление формулы через расчеты по уравнению химической реакции. Здесь нужно обязательно знать еще общую формулу класса, к которому относится неизвестное органическое вещество, и записать с ним уравнение реакции. Иногда приходится расставлять коэффициенты в общем виде через n. Тем не менее это наиболее понятный тип задач на вывод формулы, поскольку он чаще всего сводится к одному уравнению с одним неизвестным n, решение которого дает нам искомую молекулярную формулу. Дополнительные сведения о веществе, указанные в условии задачи, позволяют установить структурную формулу вещества, с которой далее требуется записать уравнение реакции.
И, наконец, третий тип задач — это установление формулы по продуктам сгорания вещества. Этот вариант наиболее часто встречается на ЕГЭ в этом задании. Выглядит он чуть более громоздко, чем два предыдущих, однако решается также очень просто. План решения заключается в нахождении простейшей формулы вещества и переходе к истинной (то есть молекулярной) формуле через известную молярную массу вещества. Простейшая формула находится из закона, согласно которому индексы элементов относятся так же, как их количества вещества в молях. Если молярная масса вещества не дана в условии, то можно попробовать доказать единственность решения через соответствие формулы правилам валентности. Но такой подход часто бывает трудоемок, и его можно легко обойти, если использовать дополнительные сведения об искомом веществе, указанные в условии задачи. Это может быть класс соединения, наличие или отсутствие каких-либо типов изомерии и, наконец, химическая реакция, в которую это вещество способно вступать или с помощью которой оно может быть получено. Помимо молекулярной формулы, эти же дополнительные сведения позволяют однозначно определить и структурную формулу вещества, с которой далее требуется записать уравнение реакции.