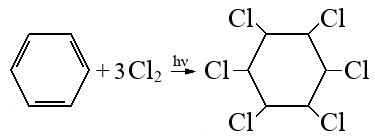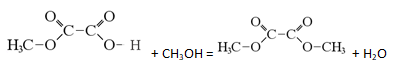Чтобы поделиться, нажимайте
Задание 34 из ЕГЭ по химии 2022
Предлагаем вашему вниманию задачи с подробными видео-объяснениями и (или) решениями, которые могут быть использованы при проведении ЕГЭ по химии 2022
Составитель — репетитор по химии в Skype или Zoom — Александр Владимирович Коньков (подробнее здесь)
ЕГЭ по химии 2022. Задание 34. Вариант 1
При нагревании с водным раствором гидроксида натрия некоторое органическое вещество подвергается гидролизу с образованием двух продуктов в соотношении 2 : 1. О первом продукте известно, что в нём массовая доля углерода равна 29,27%, водорода 3,66%, кислорода 39,02%, а остальное приходится на натрий. При сжигании образца второго продукта гидролиза массой 46,4 г можно получить 53,76 л (н.у.) углекислого газа и 43,2 г воды. Также о втором продукте известно, что оно относится к насыщенным алициклическим соединениям, в котором все атомы углерода входят в состав цикла, функциональные группы находятся рядом, а относительная плотность паров этого вещества по водороду равна 58.
На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества, которое подвергли гидролизу; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции гидролиза исходного вещества в растворе гидроксида натрия.
ЕГЭ по химии 2022. Задание 34. Вариант 2
При взаимодействии 41,4 г предельной одноосновной карбоновой кислоты с избытком раствора гидрокарбоната натрия выделилось 20,16 л (н.у.) газа. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнение реакции окисления этого вещества сернокислым раствором перманганата калия.
ЕГЭ по химии 2022. Задание 34. Вариант 3
При полном сгорании органического вещества массой 29,6 г образовалось 26,88 л (н.у.) углекислого газа и 21,6 г воды. Относительная плотность паров этого вещества по водороду равна 37. Установлено, что оно не реагирует с гидрокарбонатом натрия, не даёт реакции «серебряного зеркала», но взаимодействует со щелочами. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте возможные структурные формулы этого вещества, которые однозначно отражают порядок связи атомов в молекуле; 4) напишите уравнение реакции этого вещества с гидроксидом натрия.
ЕГЭ по химии 2022. Задание 34. Вариант 4
При дегидрировании 52,8 г предельного спирта над медным катализатором образовалось 51,6 г кетона. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы исходного спирта; 2) запишите молекулярные формулы спирта и кетона; 3) составьте возможные структурные формулы спирта и кетона, которые однозначно отражают порядок связи атомов в молекуле; 4) напишите уравнение реакции спирта с натрием в молекулярном виде.
ЕГЭ по химии 2022. Задание 34. Вариант 5
При обработке первичного предельного одноатомного спирта натрием выделилось 6,72 л газа (н.у.). При полной дегидратации такого же количества спирта образуется этиленовый углеводород массой 33,6 г. На основании данных условия задания: 1) произведите вычисления, необходимые для установления молекулярной формулы исходного органического вещества; 2) запишите молекулярную формулу исходного органического вещества; 3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 4) напишите уравнения описанных в условии задания реакций.
ЕГЭ по химии 2022. Задание 34. Вариант 6
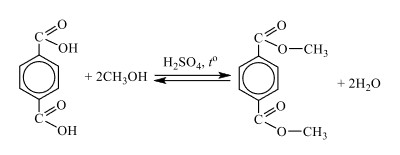
Органическое вещество А содержит 3,61% водорода и 38,55% кислорода по массе и образуется при взаимодействии органического вещества Б с раствором перманганата калия в присутствии серной кислоты. Известно, что вещество Б относится к ароматическим соединениям и содержит по одному радикалу в пара-положениях. Также известно, что вещество А имеет молярную массу 166 г/моль. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества А. 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле. 3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 7
Органическое вещество А содержит 40% углерода, 6,7% водорода и 53,3% кислорода по массе. Относительная плотность паров этого вещества по водороду равна 30. Вещество А образуется при взаимодействии органического вещества Б с аммиачным раствором оксида серебра (I). На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества А. 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле. 3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 8
Органическое вещество А содержит 9,68% водорода и 51,61% кислорода по массе и образуется при взаимодействии органического вещества Б с водным раствором перманганата калия. Относительная плотность паров вещества А по гелию равна 15,5. Известно, что вещество Б является углеводородом. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества А. 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле. 3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 9
Органическое вещество А содержит 6,67% водорода и 13,33% кислорода по массе и образуется при взаимодействии органического вещества Б с хлорангидридом уксусной кислоты в присутствии хлорида алюминия. Известно, что вещество А относится к ароматическим кетонам. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества А. 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле. 3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 10
Органическое вещество А содержит 8,11% водорода и 43,24% кислорода по массе и образуется при взаимодействии с органическим веществом Б. Известно, что вещество Б содержит один атом углерода и является ядом. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества. 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле. 3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 11
При сгорании 26,2 г органического вещества получили 26,88 л углекислого газа (н.у.), 2,24 л азота (н.у.) и 23,4 г воды. При нагревании с бромоводородной кислотой данное вещество подвергается гидролизу, продуктами которого являются соединение состава C2H6NO2Br и третичный спирт.
На основании данных условия задания:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение гидролиза вещества в присутствии бромоводородной кислоты (используйте структурные формулы органических веществ).
ЕГЭ по химии 2022. Задание 34. Вариант 12
При сгорании органического вещества А массой 43,65 г получили 20,16 л (н.у.) углекислого газа и 20,16 л (н.у.) хлороводорода.
Вещество А образуется при взаимодействии вещества Б с хлором под действием ультрафиолетового освещения. Известно, что в молекуле вещества Б все атомы углерода находятся в sp2-гибридизации, а в молекуле вещества Б — в sp3-гибридизации. На основании данных задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А при хлорировании вещества Б (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1. n = m/M, n = V/Vm
m = n ∙ M,
n (CO2) = 20,16 л / 22,4 л/моль = 0,9 моль
n (С) = n (СО2) = 0,9 моль
m (C) = 0,9 моль ∙ 12 г/моль = 10,8 г
n (HCl) = 20,16 л / 22,4 л/моль = 0,9 моль
n (H) = n (HCl) = 0,9 моль
m (H) = 0,9 моль ∙ 1 г/моль = 0,9 г
m (Cl) = 0,9 моль ∙ 35,5 г/моль = 31,95 г
m (C) + m (H) + m (Cl) = 10,8 г + 0,9 г + 31,95 г = 43,65 г
m (O) = 43,65 г – 43,65 г = 0
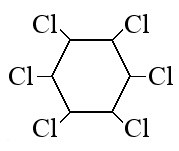
n (C) : n (H) : n (Cl) = 0,9 : 0,9 : 0,9 = 1 : 1 : 1 = 6 : 6 : 6
Следовательно молекулярная формула C6H6Cl6
- Структурная формула
- Уравнение реакции
ЕГЭ по химии 2022. Задание 34. Вариант 13
Неизвестное органическое вещество А содержит 34,62% углерода, а также водород и кислород, причём массовая доля кислорода в 15,982 раза больше массовой доли водорода. Известно, что 1 моль вещества А может вступить в реакцию с 2 моль гидроксида натрия, или 1 моль гидрокарбоната калия, или 1 моль метанола.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с избытком метанола (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1. Общая формула вещества CxHyOz
ω (O + H) = 100% — 34,62% = 65,38%
Пусть ω (Н) = х %, тогда ω (О) = 15,982х %, следовательно получаем математическое уравнение:
х + 15,982х = 65,38
16,982х = 65,38
х = 3,85% (ω (Н)), ω (О) = 15,982∙3,67 = 61,53%
x : y : z = 34,62/12 : 3,85/1 : 61,53/16 = 2,885 : 3,85 : 3,85 = 3 : 4 : 4
Следовательно, молекулярная формула C3H4O4.
- По описанным данным, можно предположить, что раз это вещество реагирует только с 1 моль гидрокарбоната или 1 моль спирта, то значить в этом веществе находится одна карбоксильная группа, но так как это же вещество может реагировать с 2 моль щелочи, то значит есть эфирная связь, которая будет подвергаться щелочному гидролизу. Поэтому это монометиловый эфир щавелевой кислоты.
Структурная формула:
- Уравнение реакции:
ЕГЭ по химии 2022. Задание 34. Вариант 14
При сгораниии 9,9 г органического вещества А получили 12,096 л углекислого газа, 0,672 л азота (н.у.) и 5,94 г воды.
Известно, что вещество А подвергается и щелочному и кислотному гидролизу, при этом образуется первичный насыщенный одноатомный спирт (молекула которого содержит 2 атома углерода) и органическая соль (соль образуется при любом типе гидролиза). Также известно, что вещество А можно получить каталитическим гидрированием вещества Б, в котором заместители максимально удалены друг от друга.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А путём каталитического гидрирования вещества Б (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1) исходное органическое вещество точно содержит в своём составе атомы элементов углерод, азот и водород, так как при сгорании этого вещества образуются углекислый газ, газ азот и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода, азота и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода, азота и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, n = V/Vm
m = n ∙ M,
n (CO2) = 12,096 л / 22,4 л/моль = 0,54 моль
n (С) = n (СО2) = 0,54 моль
m (C) = 0,54 моль ∙ 12 г/моль = 6,48 г
М(Н2О) = 18 г/моль
n (H2O) = 5,94 г / 18 г/моль = 0,33 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,33 моль = 0,66 моль
m (H) = 0,66 моль ∙ 1 г/моль = 0,66 г
n (N2) = 0,672 л / 22,4 л/моль = 0,03 моль
n (N) = 2 ∙ n (N2) = 2 ∙ 0,03 моль = 0,06 моль
m (N) = 0,06 моль ∙ 14 г/моль = 0,84 г
m (C) + m (H) + m (N) = 6,48 г + 0,66 г + 0,84 г = 7,98 г, что НЕ равно массе исходного вещества, а значит атомы кислорода присутствуют в веществе.
m (O) = 9,9 г – 7,48 г = 1,92 г
n (O) = 1,92 г / 16 г/моль = 0,12 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (N) : n (O) = 0,54 : 0,66 : 0,06 : 0,12 = 9 : 11 : 1 : 2
Следовательно молекулярная формула вещества: C9H11NO2.
2) Анализируя информацию о веществе А, можно предположить, что гидролизу подвергаются такие классы органических веществ, как эфиры (включая жиры), углеводы, пептиды, ангидриды кислот и некоторые другие. Но с образованием спирта гидролизуются только эфиры. Причём если молекула спирта содержит только два атома углерода, то делаем вывод, что вещество А – это сложный эфир некой кислоты и спирта этанола. Необходимо заметить, что в независимости от тиипа гидролиза образуется соль, а такое возможно для аминокислот. Следовательно мы имеем сложный эфир, состоящий из остатков спирта этанола и некой аминокислоты, причем ароматической, так как молекулярная формула содержит малое количество атомов водорода. Используя информацию о получении вещества А гидрированием вещества Б, делаем вывод, что вещество Б –нитросоединение, содержащее NO2-группу, потому что при гидрировании нитро-группа переходит в амино-группу (NH2-). А также понимаем, что эта нитро-группа находится в пара-положении, так как только это положение подходит под описание, когда заместители максимально удалены друг от друга, там же будет и NH2-группа.
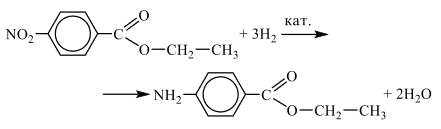
Следовательно, структурная формула —
3) Уравнение получения вещества А путём гидрирования вещества Б:
ЕГЭ по химии 2022. Задание 34. Вариант 15
При сгорании 13,28 г органического вещества А получили 3,8528∙1023 молекул углекислого газа и 4,32 мл воды.
Известно, что вещество А содержит атомы углерода только в sp2-гибридизации, заместители максимально удалены друг от друга, а также может вступать в реакцию с метанолом (в присутствии серной кислоты) в соотношении либо 1:1 либо 1:2.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции взаимодействия вещества А с метанолом (в присутствии серной кислоты) в соотношении 1:2 соответственно (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1) исходное органическое вещество точно содержит в своём составе атомы элементов углерод и водород, так как при сгорании этого вещества образуются углекислый газ и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = N/NA, n = m/M
m = n ∙ M,
n (CO2) = 3,8528 молекул / 6,02∙1023 моль-1 = 0,64 моль
n (С) = n (СО2) = 0,64 моль
m (C) = 0,64 моль ∙ 12 г/моль = 7,68 г
т.к. плотность воды 1 г/мл, то m (H2O) = 4,32 мл ∙ 1 г/мл = 4,32 г
М(Н2О) = 18 г/моль
n (H2O) = 4,32 г / 18 г/моль = 0,24 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,24 моль = 0,48 моль
m (H) = 0,48 моль ∙ 1 г/моль = 0,48 г
m (C) + m (H) = 7,68 г + 0,48 г = 8,16 г, что НЕ равно массе исходного вещества, а значит атомы кислорода присутствуют в веществе.
m (O) = 13,28 г – 8,16 г = 5,12 г
n (O) = 5,12 г / 16 г/моль = 0,32 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (O) = 0,64 : 0,48 : 0,32 = 2 : 1,5 : 1 = 4 : 3 : 2. Но составить структурную формулу с таким соотношением атомов не представляется возможным, поэтому данные индексы надо ещё раз удвоить.
Следовательно молекулярная формула вещества: C8H6O4.
2) Анализируя информацию о веществе А, можно предположить, что данное вещество является ароматическим, так как молекула содержит небольшое число атомов водорода. И так как реагирует со спиртами, то это может быть карбоновая кислота, но с учётом разного соотношения – дикарбоновая кислота, причем вторая карбоксильная группа находится в пара-полложении, так как сказано, что заместители максимально удалены друг от друга.
Следовательно, структурная формула — 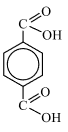
ЕГЭ по химии 2022. Задание 34. Вариант 16
При сгораниии 13,7 г органического вещества А получили 15,68 л углекислого газа, 1,12 л азота (н.у.) и 6,3 г воды.
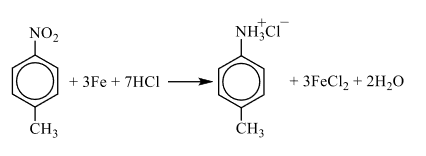
Известно, что вещество А содержит в составе одной молекулы 5 вторичных атомов углерода , один третичный и один первичный атом, а функциональная группа находится в пара-положении. Вещество А при реакции с парами хлороводорода в присутствии железа при нагревании переходит в органическое вещество Б немолекулярного строения.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества;
2) составьте структурную формулу вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А парами хлороводорода в присутствии железа при нагревании (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1) исходное органическое вещество точно содержит в своём составе атомы элементов углерод, азот и водород, так как при сгорании этого вещества образуются углекислый газ, газ азот и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода, азота и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода, азота и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, n = V/Vm
m = n ∙ M,
n (CO2) = 15,68 л / 22,4 л/моль = 0,7 моль
n (С) = n (СО2) = 0,7 моль
m (C) = 0,7 моль ∙ 12 г/моль = 8,4 г
М(Н2О) = 18 г/моль
n (H2O) = 6,3 г / 18 г/моль = 0,35 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,35 моль = 0,7 моль
m (H) = 0,7 моль ∙ 1 г/моль = 0,7 г
n (N2) = 1,12 л / 22,4 л/моль = 0,05 моль
n (N) = 2 ∙ n (N2) = 2 ∙ 0,05 моль = 0,1 моль
m (N) = 0,1 моль ∙ 14 г/моль = 1,4 г
m (C) + m (H) + m (N) = 8,4 г + 0,7 г + 1,4 г = 10,5 г, что НЕ равно массе исходного вещества, а значит атомы кислорода присутствуют в веществе.
m (O) = 13,7 г – 10,5 г = 3,2 г
n (O) = 3,2 г / 16 г/моль = 0,2 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (N) : n (O) = 0,7 : 0,7 : 0,1 : 0,2 = 7 : 7 : 1 : 2
Следовательно молекулярная формула вещества: C7H7NO2.
2) Анализируя информацию о веществе А, можно предположить, что это вещество является ароматическим (по указанию первичных, вторичных и третичных атомов углерода). Также для определения класса/группы перебираем известные в школе кислородсодержащие соединения и делаем вывод, что под получившуюся молекулярную формулу подходят либо нитросоединение либо аминокислота. Но так как вещество реагирует с железом и хлороводородом, то узнаём реакцию Зинина, по которой нитрогруппа переходит в аминогруппу с последующей реакцией с кислотой и с образованием органической соли, которая и является веществом Б немолекулярного строения. Вариант с аминокислотой исключаем, так как для реакции аминокислоты с HCl железо не нужно.
2) следовательно, структурная формула: 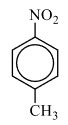
ЕГЭ по химии 2022. Задание 34. Вариант 17
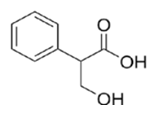
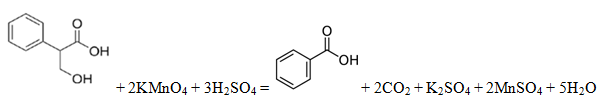
Вещество А содержит 65,06% углерода, 6,02% водорода, 28,92% кислорода по массе. Известно, что вещество А окисляется до бензойной кислоты. Также известно, что вещество А при взаимодействии с бромоводородом даёт бромопроизводное Б. При воздействии на это бромопроизводное Б спиртового раствора щёлочи происходит дегидрогалогенирование и образуется соль ненасыщенной кислоты.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции окисления вещества А перманганатом калия в присутствии серной кислоты (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1. Общая формула вещества А – CxHyOz
x : y : z = 65,06/12 : 6,02/1 : 28,92/16 = 5,422 : 6,02 : 1,808 = 3 : 3,33 : 1 = 9 : 10 : 3. Следовательно, молекулярная формула С9Н10О3.
2. Соединение С9Н10О3 окисляется до бензойной кислоты, значит его основу составляет бензолное кольцо. Отсюда следует, что заместитель имеет три атома углерода. Так как в конце всех превращений (описанных в задаче) образуется соль ненасыщенной кислоты, то вещество А содержит карбоксильную группу. Из трёх атомов кислорода в веществе А два входят в состав карбоксила, а третий принадлежит спиртовому гидроксилу, так как вещество А при взаимодействии с бромоводородом образует бромпроизводное Б, что невозможно в случае наличия фенольного гидроксила. При взаимодействии на это бромпроизводное спиртового раствора щёлочи происходит дегидрогалогенирование и образуется соль ненасыщенной карбоновой кислоты, следовательно, спиртовой гидроксил находится в β-положении по отношению к карбоксильной группе, так как именно β-гидроксикислоты при нагревании отщепляют воду и образуют ненасыщенные соединения.
Структурная формула:
3. Уравнение реакции:
ЕГЭ по химии 2022. Задание 34. Вариант 18
При сгорании органического вещества Н массой 7 г получено 8,96 л (н.у.) углекислого газа и 5,4 г воды. Известно, что вещество Н подвергается полному гидрированию при нагревании, повышенном давлении и в присутствии катализатора, в результате чего образуется предельный одноатомный первичный спирт В. Про исходное вещество Н также известно, что один из его концевых атомов углерода в молекуле находится в состоянии sp3-гибридизации.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества Н;
2) составьте структурную формулу вещества Н, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции полного гидрирования вещества Н при нагревании, повышенном давлении и в присутствии катализатора (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1. Исходное органическое вещество Н точно содержит в своём составе атомы элементов углерод, водород, так как при сгорании этого вещества образуются углекислый газ и вода. А кислород как может входить в состав это вещества, так может и не входить. Но так как в условии задачи сказано, что при гидрировании вещества Н (а это реакция с водородом) образуется спирт (в котором есть атомы кислорода), то делаем вывод, что исходное вещество Н точно содержит атомы кислорода. Разница между массой вещества за вычетом масс атомов элементов углерода и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, n = V/Vm
m = n ∙ M,
n (CO2) = 8,96 л / 22,4 л/моль = 0,4 моль
n (С) = n (СО2) = 0,4 моль
m (C) = 0,4 моль ∙ 12 г/моль = 4,8 г
М(Н2О) = 18 г/моль
n (H2O) = 54 г / 18 г/моль = 0,3 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,3 моль = 0,6 моль
m (H) = 0,6 моль ∙ 1 г/моль = 0,6 г
m (C) + m (H) = 4,8 г + 0,6 г = 5,4 г
m (O) = 7 г – 5,4 г = 1,6 г
n (O) = 1,6 г / 16 г/моль = 0,1 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (O) = 0,4 : 0,6 : 0,1 = 4 : 6 : 1
Следовательно молекулярная формула вещества: C4H6O.
- Как правило, спирты образуются при гидрировании либо альдегидов, либо кетонов. Но первичные спирты образуются из альдегидов, поэтому делаем вывод, что СНО-группа находится на конце. Составляя структурную формулу, замечаем, что не хватает атомов водорода, чтобы получить насыщенный альдегид. Поэтому понимаем, что альдегид ненасыщенный, т.е. содержит двойную связь (именно двойная связь подходит по числу атомов водорода в молекуле). Но так как сказано, что один из концевых атомов углерода в молекуле находится в состоянии sp3-гибридизации, делаем вывод, что двойная связь НЕ может быть на конце (так как атом углерода при двойной связи находится в состоянии sp2-гибридизации). Отсюда получаем, что кратная (двойная) связь отходит от второго атома углерода (между вторым и третьим).
Структурная формула:
3. Уравнение реакции:
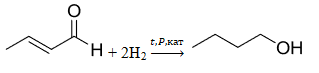
ЕГЭ по химии 2022. Задание 34. Вариант 19
Вещество А содержит 48% углерода, 4% водорода и 48% кислорода по массе. Известно, что вещество А относится к гетероциклическим соединениям и получается дегидратацией при нагревании вещества Б, которое не содержит третичных и четвертичных атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А путём дегидратации вещества Б при нагревании (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
- Общая формула вещества А – CxHyOz
x : y : z = 48/12 : 4/1 : 48/16 = 4 : 4 : 3. Следовательно, молекулярная формула С4Н4О3.
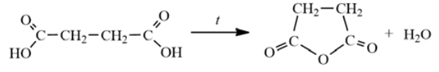
- Соединение С4Н4О3 является гетероциклическим, а значит в состав цикла входят не только атому углерода, но и атомы кислорода. Учитывая, что это вещество образуется путём дегидратации, то можно предположить, что вещество А получается из карбоновой кислоты, так как при дегидратации спиртов образуются алкены, а альдегиды и простейшие эфиры не подвергаются дегидратации . Но так как образуется цикл, то в веществе Б должно быть две карбоксильные группы. И так как по условию задачи сказано, что вещество Б не содержит третичные и четвертичные атомы углерода, то значит его цепочка прямая и неразветвлённая, а значит карбоксильные группы расположены по концам. Как следствие, будет образовываться пятичленный цикл вещества А.
Структурная формула вещества А:
- 3. Уравнение реакции:
ЕГЭ по химии 2022. Задание 34. Вариант 20
Неизвестное ациклическое органическое вещество содержит 73,17% углерода, 7,32% водорода и 19,51% кислорода по массе. Это вещество можно получить в реакции избытка спиртового раствора щёлочи с дихлорпроизводным, содержащим такое же число атомов углерода в молекуле как и неизвестное органическое вещество, причём атомы хлора располагаются по разным концам молекулы.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу неизвестного органического вещества;
2) составьте структурную формулу неизвестного органического вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения неизвестного органического вещества путём взаимодействия дихлорпроизводного с избытком спиртового раствора щёлочи (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
- Общая формула вещества А – CxHyOz
x : y : z = 73,17/12 : 7,32/1 : 19,51/16 = 6,098 : 7,32 : 1,219 = 5 : 6 : 1. Следовательно, молекулярная формула С5Н6О.
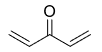
- Анализируя условие задачи, можно предположить, что неизвестное органическое вещество будет либо спиртом, либо альдегидом, либо кетоном, либо карбоновой кислотой, либо эфиром. Но так как сказано, что вещество является ациклическим и получается из дихлопроизводного, в котором атомы хлора располагаются по противоположным концам молекулы, то значит при щелочном гидролизе отщепляются две молекулы хлороводорода и по концам образуются двойные связи, и, значит, кислород находится по центру у третьего атома углерода, а значит это ненасыщенный кетон.
Структурная формула неизвестного вещества:

ЕГЭ по химии 2022. Задание 34. Вариант 21
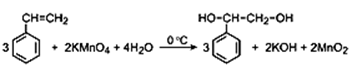
Устойчивое органическое соединение количеством 0,25 моль окислили водным раствором перманганата натрия. В результате образовались только карбонат натрия массой 8,798 г, гидрокарбонат натрия массой 14,028 г, оксид марганца (IV) массой 28,971 г и вода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу неизвестного органического вещества;
2) составьте структурную формулу неизвестного органического вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции описанное в условии задачи (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
Видео-объяснение смотрите на Ютуб по ссылке или ниже
ЕГЭ по химии 2022. Задание 34. Вариант 22
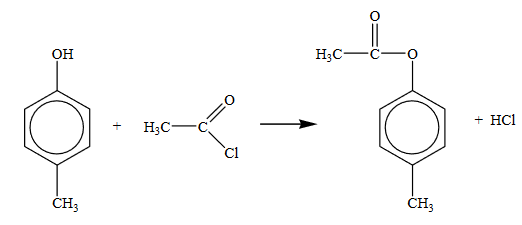
Вещество А содержит 72% углерода, 6,67% водорода и 21,33% кислорода по массе. Известно, что вещество А содержит два заместителя, которые максимально удалены друг от друга. Также известно, что вещество А получается при нагревании ацетилхлорида (хлорангидрид уксусной кислоты) с веществом Б, которое не вступает в реакции этерификации.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А путём взаимодействия ацетилхлорида с веществом Б при нагревании (используйте структурные формулы органических веществ).
Решение:
Развернуть/свернуть
1. Общая формула вещества А – CxHyOz
x : y : z = 72/12 : 6,67/1 : 21,33/16 = 6 : 6,67 : 1,333 = 4,5 : 5 : 1 = 9 : 10 : 2. Следовательно, молекулярная формула С9Н10О2.
- Соединение С9Н10О2 является ароматическим, так как содержит небольшое число атомов водорода. Также по условию известно, что имеется два заместителя, которые максимально удплены друг от друга, а значит, что один из заместителей находится в пара-положении. Учитывая, что вещество А образуется путём взаимодействия с ацетилхлоридом, то можно предположить, что в первом заместителе содержится два атома углерода, а во втором – один. Учитывая, что исходное вещество Б не вступает в реакции этерефикации, но содержит один атом кислорода (так как один из атомов кислорода находится в ацетилхлориде), то оно относится к классу фенолов, в частности это пара-крезол. Отсюда получаем структурную формулу вещества А:
- Уравнение реакции:
ЕГЭ по химии 2022. Задание 34. Вариант 23
Неизвестное органическое вещество содержит 17,98% углерода, 2,25% водорода и 79,77% хлора по массе. Известно, что в этом веществе все атомы хлора находятся у одного атома углерода и это вещество подвергается щелочному гидролизу. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение щелочного гидролиза вещества в присутствии избытка гидроксида калия (используйте структурные формулы органических веществ).
Развернуть/свернуть
Найдем соотношение количества вещества углерода, водорода и хлора.
Примем массу соединения за 100 грамм, тогда количество вещества элементов следующее:
n(С) = 17,98/12 = 1,5
n(Сl) = 79,77/35,5 = 2,25
n(H) = 2,25/1 = 2,25
Соотношение углерода к хлору и водороду 1,5 : 2,25 : 2,25 = 1 : 1,5 : 1,5 = 2 : 3 : 3
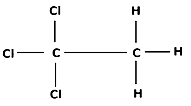
Молекулярная формула вещества C2H3Cl3
Структурная формула
Уравнение щелочного гидролиза в избытке гидроксида калия:
CH3-CCl3 + 4KOH = CH3COOK + 3KCl + 2H2O.
ЕГЭ по химии 2022. Задание 34. Вариант 24
При сгорании 40,5 г неизвестного органического вещества получили 40,32 л углекислого газа (н.у.) и 40,5 г воды. Из навески этого вещества массой 20,25 г вся сера была переведена в сульфат-ион, который дал осадок BaSO4 массой 52,425 г. Неизвестное органическое вещесто относится к классу тиоэфиров, которые по строению схожи с простыми эфирами, только вместо атомов кислорода содержат атомы серы. Известно, что это вещество имеет симметричное строение и может быть получено по реакции моногалогеналкана с сульфидом натрия при нагревании. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение получения этого органического вещества из моногалогеналкана и сульфида натрия (используйте структурные формулы органических веществ).
Развернуть/свернуть
Исходное органическое вещество точно содержит в своём составе углерод, водород и серу, так как при сгорании этого вещества образуются углекислый газ и вода, и серу выделяют через осадок сульфида бария. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода, водорода и серы, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода,водорода и серы и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, m = n ∙ M, n = V/Vm.
n (CO2) = 40,32 л/22,4 л/моль = 1,8 моль
n (С) = n (СО2) = 1,8 моль
m (C) = 1,8 моль ∙ 12 г/моль = 21,6 г
n (H2O) = 40,5 г / 18 г/моль = 2,25 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 2,25 моль = 4,5 моль
m (H) = 4,5 моль ∙ 1 г/моль = 4,5 г
Надо заметить, что при сжигании, масса вещества была 40,5 г, а при выделении серы – 20,25 г. Поэтому надо привести эти массы к одному значению. Эти массы отличаются в 2 раза, значит при из 40,5 г вещества можно выделить в 2 раза больше осадка сульфата бария: 2 ∙ 52,425 = 104,85 г.
n (BaSO4) = 104,85 г/233 г/моль = 0,45 моль
n (S) = n (BsSО4) = 0,45 моль
m (S) = 0,45 моль ∙ 32 г/моль = 14,4 г
m (C) + m (H) + m (S) = 21,6 г + 4,5 г + 14,4 г = 40,5 г, что равно массе исходного вещества, а значит там НЕТ кислорода.
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (S) = 1,8 : 4,5 : 0,45 = 4 : 10 : 1
Следовательно молекулярная формула вещества: C4H10S.
Так как вещество имеет симметричное строение, то структурная формула:
CH3 – CH2 – S – CH2 – CH3
Уравнение получения по реакции моногалогеналкана с сульфидом натрия при нагревании:
2CH3 – CH2 – Cl + Na2S → CH3 – CH2 – S – CH2 – CH3 + 2NaCl
ЕГЭ по химии 2022. Задание 34. Вариант 25
К смеси газообразного углеводорода с аммиаком общим объёмом 300 л прибавили избыток кислорода и смесь подожгли. После полного сгорания объём смеси стал равен 1250 л, после конденсации паров воды уменьшился до 550 л, а после обработки щёлочью уменьшился до 250 л, из которых 100 л приходится на азот. Объёмы газов измерены в одинаковых условиях. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение нитрования этого вещества по Коновалову (используйте структурные формулы органических веществ).
Развернуть/свернуть
Запишем уравнения полного сгорания углеводорода и аммиака:
2CxHy + (2x + 0,5y)O2 = 2xCO2 + yH2O (уравнение 1)
4NH3 + 3O2 = 2N2 + 6H2O (уравнение 2)
Для вывода формулы, надо знать количество углерода, которое перешло из углеводорода в углекислый газ и количество водорода, перешедшего в воду по уравнению 1.
Вода при условиях опыта – газ. Поэтому по данным условия находим объём газообразной воды с учётом того, что вода выделяется в обоих уравнениях:
Vобщ (H2O) = 1250 л – 550 л = 700 л
Так как нам по условию задачи известен объём азота, то по уравнению 2 мы можем найти воду, которая образовалась в этом уравнении и потом найти объём газообразной воды, образовавшейся по уравнению 1.
V2 (H2O) = 3V (N2) = 3 ∙ 100 л = 300 л (по уравнению 2)
V1 (H2O) = Vобщ (H2O) – V2 (H2O) = 700 л – 300 л = 400 л
Находим химическое количество водорода в воде, образовавшейся по уравнению 1:
n1 (H2O) 400 л/22,4 л/моль = 17,86 моль
n (H) = 2n1 (H2O) = 2 ∙ 17,86 моль = 35,72 моль
Теперь найдём химическое количество углерода через углекислый газ, который поглотился щёлочью:
CO2 + NaOH = NaHCO3 или CO2 + 2NaOH = Na2CO3 + H2O
Анализируя уравнения, делаем вывод, что объём смеси уменьшился за счёт поглощённого углекислого газа, значит V (CO2) = 550 л – 250 л = 300 л
n (CO2) = 300 л/22,4 л/моль = 13,39 моль
n (C) = n (CO2) = 13,39 моль
Теперь выводим формулу углеводорода. Для этого необходимо сделать перерасчёт на 1 моль вещества. Значит, необходимо узнать, сколько углеводорода было в смеси.
V (NH3) = 2V (N2) = 200 л (по уравнению 2)
V (CxHy) = V (исходной смеси) – V (NH3) = 300 л -200 л = 100 л
n (CxHy) = 100 л/22,4 л/моль = 4,46 моль
4,46 моль углеводорода содержит 13,39 моль углерода и 35,72 моль водорода
1 моль углеводорода содержит x моль углерода и y моль водорода.
По пропорции:
x = 3
y = 8
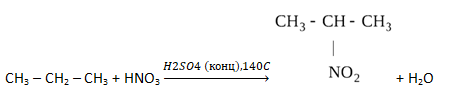
Следовательно, молекулярная формула углеводорода C3H8
Структурная формула CH3 – CH2 – CH3
Уравнение нитрования по Коновалову:
ЕГЭ по химии 2022. Задание 34. Вариант 26
При сгорании 69 г органического вещества получили 89,6 л углекислого газа (н.у.) и 45 г воды. Это вещество можно получить мягким окислением ароматического углеводорода водным раствором перманганата калия на холоду. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение получения этого вещества окислением ароматического углеводорода водным раствором перманганата калия (используйте структурные формулы органических веществ).
Развернуть/свернуть
Исходное органическое вещество точно содержит в своём составе углерод и водород, так как при сгорании этого вещества образуются углекислый газ и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, m = n ∙ M, n = V/Vm.
n (CO2) = 89,6 л/22,4 л/моль = 4 моль
n (С) = n (СО2) = 4 моль
m (C) = 4 моль ∙ 12 г/моль = 48 г
n (H2O) = 45 г / 18 г/моль = 2,5 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 2,5 моль = 5 моль
m (H) = 5 моль ∙ 1 г/моль = 5 г
m (C) + m (H) = 48 г + 5 г = 53 г, что НЕ равно массе исходного вещества, а значит там есть кислород.
m (O) = m (в-ва) – m (C+H) = 69 г – 53 г = 16 г
n (O) = 16 г / 16 г/моль = 1 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (O) = 4 : 5 : 1
Следовательно простейшая формула вещества: C4H5O.
Но так как в условии сказано, что исходное вещество получается мягким окислением ароматического УВ водным раствором перманганата калия, то значит исходное вещество должно содержать бензольное кольцо (так как при мягком окислении не наблюдается разрыва цикла). Следовательно, простейшую формулу необходимо удвоить.
Молекулярная формула C8H10O2.
При мягком окислении кратных связей между атомами углерода образуются многоатомные спирты.
Структурная формула
ЕГЭ по химии 2022. Задание 34. Вариант 27
Неизвестное органическое вещество содержит 60% углерода, 5% водорода и 35% азота по массе. Относительная плотность паров этого вещества по водороду равна 40. Это вещество можно отнести к производным циановодородной кислоты и алкана. А получить его можно нагреванием дибромалкана с цианидом калия. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение получения исходного органического соединения нагреванием дибромалкана с цианидом калия (используйте структурные формулы органических веществ).
Развернуть/свернуть
Найдем соотношение количества вещества углерода, водорода и азота.
Примем массу соединения за 100 грамм, тогда количество вещества элементов следующее:
n(С) = 60 г/12 г/моль = 5 моль
n(N) = 35 г/14 г/моль = 2,5 моль
n(H) = 5 г/1 г/моль = 5 моль
Соотношение углерода к азоту и водороду 5 : 2,5 : 5 = 2 : 1 : 2
Простейшая формула C2H2N, М (C2H2N) = 40 г/моль
А по относительной плотности по водороду находим, что М (исходного вещества) = 2 г/моль ∙ 40 = 80 г/моль
Значит, простейшую формулу необходимо удвоить.
Молекулярная формула вещества C4H4N2
Так как исходное вещество является производным циановодородной кислоты, то там должна сохраняться структура кислотного остатка С≡N
Структурная формула N≡C – CH2 – CH2 – C≡N
Уравнение получения:
Br – CH2 – CH2 – Br + 2KCN = N≡C – CH2 – CH2 – C≡N + 2KBr.
ЕГЭ по химии 2022. Задание 34. Вариант 28
При сгорании 33,2 г органического вещества получили 35,84 л углекислого газа (н.у.) и 10,8 г воды. При нагревании данное вещество подвергается внутримолекулярной дегидратации. Также известно, что исходное вещество содержит две одинаковые функциональные группы и находятся они у соседних атомов углерода. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение гидролиза вещества в присутствии бромоводородной кислоты (используйте структурные формулы органических веществ).
Развернуть/свернуть
Исходное органическое вещество точно содержит в своём составе углерод и водород, так как при сгорании этого вещества образуются углекислый газ и вода. А кислород как может входить в состав это вещества, так может и не входить. Проверить это можно сложив массы атомов элементов углерода и водорода, если эта сумма будет равна массе исходного органического вещества, то кислорода нет, а если масса окажется меньше – то кислород есть, и разница между массой вещества за вычетом масс атомов элементов углерода и водорода и есть масса атомов элемента кислорода.
Найдём эти массы:
n = m/M, m = n ∙ M, n = V/Vm.
n (CO2) = 35,84 л/22,4 л/моль = 1,6 моль
n (С) = n (СО2) = 1,6 моль
m (C) = 1,6 моль ∙ 12 г/моль = 19,2 г
n (H2O) = 10,8 г / 18 г/моль = 0,6 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 0,6 моль = 1,2 моль
m (H) = 1,2 моль ∙ 1 г/моль = 1,2 г
m (C) + m (H) = 19,2 г + 1,2 г = 20,4 г, что НЕ равно массе исходного вещества, а значит там есть кислород.
m (O) = m (в-ва) – m (C+H) = 33,2 г – 20,4 г = 12,8 г
n (O) = 12,8 г / 16 г/моль = 0,8 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (O) = 1,6 : 1,2 : 0,8 = 4 : 3 : 2
Следовательно простейшая формула вещества: C4H3O2.
Попытки составить структурную формулу, удовлетворяющие условию задания с полученной простейшей формулой, не увенчаются успехом. Либо вещества будут неустойчивыми. Поэтому надо удвоить простейшую формулу.
Молекулярная формула C8H6O2.
Структурная формула
ЕГЭ по химии 2022. Задание 34. Вариант 29
В состав органического вещество входит 6,78% водорода, 20,34% кислорода и 11,86% азота по массе. Это вещество подвергается гидролизу с образованием двух веществ, одно из которых является производным первого, в котором один атом водорода замещён фенильной группой. Известно, что одно из веществ, образующихся при гидролизе имеет очень важную биологическую функцию и является незаменимым для организма человека. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение гидролиза вещества в присутствии кислоты (используйте структурные формулы органических веществ).
Развернуть/свернуть
Найдём массовую долю углерода, так как в состав всех органических соединений входит углерод.
w (C) = 100% — 6,78% — 20,34% — 11,86% = 61,02%
Найдем соотношение количества вещества углерода, водорода, кислорода и азота.
Примем массу соединения за 100 грамм, тогда количество вещества элементов следующее:
n (С) = 61,02 г/12 г/моль = 5,085 моль
n (H) = 6,78 г/1 г/моль = 6,78 моль
n (O) = 20,34 г/16 г/моль = 1,271 моль
n (N) = 11,86 г/14 г/моль = 0,847 моль
Соотношение углерода к водороду, кислороду и азоту 5,085 : 6,78 : 1,271 : 0,847 = 6 : 8 : 1,5 : 1= 12 : 16 : 3 : 2
Молекулярная формула вещества C12H16O3N2
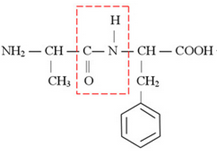
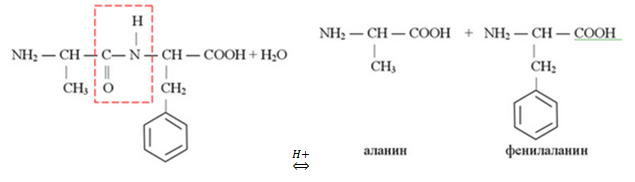
Анализируя рописание вещества, делаем вывод, что исходное вещество – дипептид аланина и незаменимой аминокислоты фенилаланина, которое и является производным аланина.
Структурная формула
Уравнение кислотного гидролиза:
ЕГЭ по химии 2022. Задание 34. Вариант 30
В состав вещества входят атомы углерода, водорода и азота, причём массовая доля атомов углерода в нём 53,33%. Масса азота, полученного из 0,546 г вещества, равна 0,170 г. Относительная плотность этого вещества по озону равна 0,9375. Известно, что данное вещество реагирует раствором нитрита калия в присутствиии соляной кислоты с образованием органического вещества, относящегося к другому классу, и выделением газа, входящего в состав атмосферы. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение реакции этого вещества с раствором нитрита калия в присутствии соляной кислоты (используйте структурные формулы органических веществ).
Развернуть/свернуть
M (CxHyNz) = M (O3) ∙ DO3 (CxHyNz) = 48 г/моль ∙ 09375 = 45 г/моль
n (CxHyNz) = 0546 г/45 г/моль = 0,012 моль
n (N2) = 0,170 г/28 г/моль = 0,006 моль
n (N) = 2 ∙ n (N2) = 2 ∙ 0,006 моль = 0,012 моль
0,012 моль вещества содержат 0,012 моль N, следовательно 1 моль вещества содержит 1 моль N, т.е. в формуле 1 атом азота.
m (C) = Mr (CxHyNz) ∙ w (CxHyNz) = 45 ∙ 0,5333 = 24 (г)
n (С) = 24 г/12 г/моль = 2 моль.
Следовательно 1 моль вещества содержит 2 моль углерода, т.е. в формуле 2 атома углерода.
N (H) = (M (CxHyNz) – M (C2N)) /1 г/моль = (45 г/моль – 38 г/моль) /1 г/моль = 7
Следовательно, молекулярная формула C2H7N
Азотсодержащим веществом может быть либо амин либо нитросоединения. Предполагаем, что исходное вещество амин. Так как вещество реагирует с азотистой кислотой (нитрит калия + соляная кислота), то оно относится к первичным аминам, потому что вторичные амины в эту реакцию не вступают, равно как и нитросоединения.
Структурная формула CH3 – CH2 – NH2
Уравнение реакции:
CH3 – CH2 – NH2 + KNO2 + HCl → CH3 – CH2 – OH + N2 + KCl + H2O
ЕГЭ по химии 2022. Задание 34. Вариант 31
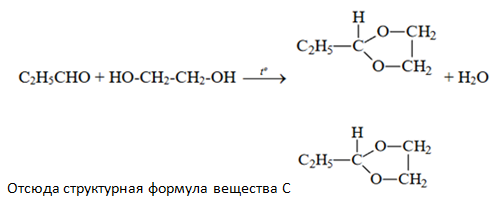
Органическое ещество А при нагревании реагирует с двухатомным спиртом Б с образованием воды и органического вещества С, которое является гетероциклическим и содержит радикал этил. В состав вещества А входит 62,07% углерода, 10,34% водорода и 27,59% кислорода, функциональная группа находится у первого атома углерода. А при сжигании двухатомного спирта Б массой 62 г образуется 54 г воды и 88 г углекислого газа.
На основании данных условия задания:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества С;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение получения вещества С из веществ А и Б (используйте структурные формулы органических веществ).
Развернуть/свернуть
Найдём формулу вещества А.
Примем массу соединения А за 100 грамм, тогда количество вещества элементов следующее:
n (С) = 62,07 г/12 г/моль = 5,173 моль
n (H) = 10,34 г/1 г/моль = 10,34 моль
n (O) = 27,59 г/16 г/моль = 1,724 моль
Соотношение углерода к водороду, кислороду и азоту 5,173 : 10,34 : 1,724 = 3 : 6 : 1
Молекулярная формула вещества А C3H6O – это пропаналь.
Найдём формулу вещества Б.
n (CO2) = 88 г/44 г/моль = 2 моль
n (С) = n (СО2) = 2 моль
m (C) = 2 моль ∙ 12 г/моль = 24 г
n (H2O) = 54 г / 18 г/моль = 3 моль
n (H) = 2 ∙ n (H2O) = 2 ∙ 3 моль = 6 моль
m (H) = 6 моль ∙ 1 г/моль = 6 г
m (O) = 62 г – 24 г – 6 г = 32 г
n (O) = 32 г / 16 г/моль = 2 моль
Для нахождения молекулярной формулы необходимо найти соотношение химических количеств атомов элементов входящих в состав исходного органического вещества.
n (C) : n (H) : n (O) = 2 : 6 : 2
Следовательно молекулярная формула вещества Б: C2H6O2 – это этиленгликоль.
Чтобы вывести структурную формулу вещества С, лучше сначало написать уравнение взаимодействия пропаналя с этиленгликолем, с учётом образования воды и того, что вещество С является гетероциклическим (т.е. в состав цикла входят НЕ только атомы углерода) и содержит радикал этил:
В случае, если вы нашли ошибку или опечатку, просьба сообщать об этом автору проекта в контакте https://vk.com/id30891697 или на электронную почту yoursystemeducation@gmail.com
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув:
- Посмотреть видео-объяснения решений всех типов задач вы можете здесь, нажав на эту строку
- Просмотреть задания ЕГЭ всех лет (реальные, пробные и тренировочные задания) вы можете здесь, нажав на эту строку
- Посмотреть все видео-уроки вы можете здесь, нажав на эту строку
- Прочитать всю теорию для подготовки к ЕГЭ и ЦТ вы можете здесь, нажав на эту строку
- Все видео-объяснения вы можете найти на YouTube канале, нажав на эту строку
Муниципальное автономное общеобразовательное учреждение
гимназия №4 г. Канска
Методическое пособие для обучающихся 11 классов
профильного направления «Химия»
Алгоритмы решения 34 задания ЕГЭ по химии
Подготовил:
ученик 11Б класса
МАОУ гимназии №4
Ходасевич Егор
Канск, 2022 г.
Оглавление
|
Спецификация:………………………………… |
3 |
|
Оценивание 34 задания………………………. |
4 |
|
Типы задач…………………………………….. |
5 |
|
Что нужно знать для выполнения?……………. |
7 |
|
Химические свойства………………………… |
8 |
|
• Оксиды …………………………………… |
8 |
|
• Основания………………………………… |
9 |
|
• Соли……………………………………….. |
10 |
|
• Кислоты…………………………………… |
11 |
|
Алгоритм решения……………………………. |
12 |
|
Примеры решения задач по алгоритму……… |
13 |
|
Задача на электролиз………………………….. |
13 |
|
Задача на кристаллогидрат…………………… |
18 |
|
Задача на пластинку …………………………… |
21 |
|
Задача на выход реакции……………………… |
24 |
|
Задача на растворимость……………………… |
26 |
34 задание ЕГЭ по химии является расчётной задачей высокого уровня сложности. При решении данного типа задач задействуются все алгоритмы, механизмы и знания по неорганической химии за школьный курс.
Спецификация:
- Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе».
- Расчёты массы (объёма, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси).
- Расчёты массы (объёма, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определённой массовой долей растворённого вещества.
- Расчёты массовой доли (массы) химического соединения в смеси
Так как задание повышенного уровня сложности, решает его маленький процент сдающих экзамен.
Правильный ответ должен включать в себя:
- Правильно записанные уравнения всех реакций
- Правильно выполненные вычисления
- Логическую взаимосвязь физических величин, на основании которой проводятся расчёты
- Правильно определённая искомая величина
Оценивание 34 задания
|
Ответ правильный и полный, содержит следующие элементы: • правильно записаны уравнения реакций, соответствующих условию задания; • правильно произведены вычисления, в которых используются необходимые физические величины, заданные в условии задания; • продемонстрирована логически обоснованная взаимосвязь физических величин, на основании которой проводятся расчёты; • в соответствии с условием задания определена искомая физическая величина |
4 |
|
Правильно записаны три элемента ответа |
3 |
|
Правильно записаны два элемента ответа |
2 |
|
Правильно записаны один элемента ответа |
1 |
|
Все элементы ответа записаны неверно |
0 |
|
Максимальный балл |
4 |
Типы задач
Существует несколько типов 34 задания
- На атомы
Смесь малахита ((CuOH)2CO3) и карбоната цинка, в которой
соотношение числа атомов углерода к числу атомов кислорода равно 5 : 19, растворили в 580,1 г разбавленного раствора серной кислоты. При этом все исходные вещества прореагировали полностью, и выделилось 11,2 л газа (н.у.). К полученному раствору добавили 52 г цинка. После того как массовая доля сульфата меди(II) уменьшилась до 2,5%, всю смесь цинка и меди отделили. Вычислите массовую долю сульфата цинка в конечном растворе.
- На растворимость
Растворимость карбоната аммония составляет 96 г на 100 г воды. Приготовили насыщенный раствор с 250 мл воды, разделили его на две колбы. В первую колбу добавили избыток твёрдого гидроксида натрия и нагрели, а во вторую — 250 г соляной кислоты (тоже в избытке). При этом из второй колбы выделилось в три раза меньше газа (при одинаковых условиях), чем из первой. Определите массовую долю соли во второй пробирке.
- На электролиз
Для проведения электролиза взяли раствор нитрата серебра. После того
как объём газа, выделившийся на аноде, оказался в 1,2 раза меньше
объёма газа, выделившегося на катоде, процесс остановили. (Объёмы
газов измерены при одинаковых условиях). Масса образовавшегося в
процессе электролиза раствора оказалась на 51,8% меньше массы
исходного раствора. К полученному раствору добавили равный ему по
массе 20%-ный раствор гидроксида натрия. Определите среду конечного
раствора и массовую долю соли в нём.
- На неполное разложение
При нагревании образца нитрата алюминия часть вещества разложилась.
При этом образовался твёрдый остаток массой 37,98 г. В этом остатке
число атомов алюминия в 5 раз меньше числа атомов кислорода.
Остаток полностью растворили в необходимом для реакции
минимальном объёме 24%-ного раствора гидроксида натрия. При этом
образовался тетрагидроксоалюминат натрия. Определите массовую
долю нитрата натрия в полученном растворе.
- На пластинку
Магниевую пластинку поместили в 483 г 20%-ного раствора сульфата цинка. После того как масса раствора уменьшилась на 20,5 г, пластинку вынули. К оставшемуся раствору добавили 224 г 40%-ного раствора гидроксида калия. Определите массовую долю гидроксида калия в образовавшемся растворе. (Процессами гидролиза пренебречь.)
- Определение типа соли
Раствор гидрокарбоната кальция содержит 88,8% кислорода по массе.
Этот раствор массой 540 г по каплям добавили к 120 г 0,4%-ного
раствора гидроксида натрия. Выпавший осадок отделили, а оставшийся
раствор нагрели до прекращения выделения газа. Вычислите массу
конечного раствора и массу соли в нём.
- Выход реакции
При обжиге 65,79 г известняка, содержащего 5% примесей, был получен углекислый газ с выходом 80%, который пропустили через 328 мл 20%-ого раствора гидроксида натрия (p=1,22 г/мл). Определите состав и массовые доли веществ в полученном растворе.
- На смесь
Смесь, состоящую из порошков алюминия и угля, прокалили без доступа воздуха. После завершения реакции масса твёрдого остатка составила 12,24 г. К этому остатку добавили 300 г раствора гидроксида калия, взятого в избытке. При этом выделилось 10,752 л (н.у.) смеси газов. Вычислите массовую долю тетрагидроксоалюмината калия в конечном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
- На кристаллогидрат
Оксид меди (II) массой 16 г обработали 40 мл 5,0%-ного раствора серной кислоты (р = 1,03 г/см3). Полученный раствор отфильтровали, фильтрат упарили. Определите массу полученного кристаллогидрата.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Что нужно знать для выполнения?
- Формулы
- Химические свойства веществ, чтобы записать уравнения реакций
- Примерный алгоритм решения
Начнём с формул. На самом деле формулы для решения задач запомнить не так трудно, потому что их небольшое количество. Большую часть формул можно вывести из других.
Пример: m = n ∙ M
n = m/М
Для решения расчетных задач по химии понадобятся следующие физические величины и формулы для их вычисления.
|
Формула |
|
|
Количество вещества n (моль) |
n=m/Mr n=V/22.4 (л/моль) |
|
Масса вещества m (г) |
m=n•Mr |
|
Объем вещества V (л) |
V=n • 22.4 (л/моль) V=m/ρ |
|
Массовая доля W (%) |
А)элемента W=Ar*n/Mr*100% Б)веществаW=m(ч.в.)/m(р-ра)*100% |
|
Плотность ρ (г/мл) |
ρ=m(р-ра)/V(р-ра) |
|
Выход продукта реакции (%) |
η=m(пр.)/m(теор.) |
|
Относительная плотность газа А по газу В |
Dв(A)=M(A)/M(B) |
Химические свойства
Для составления уравнений реакций в решении задачи, следует знать все химические свойства всех веществ. Ведь это обязательное условие для решения задачи.
-
Оксиды
это сложные вещества, состоящие из двух химических элементов (т. е. бинарные соединения), один из которых — кислород в степени окисления −2.
Оксиды делятся на две группы солеобразующие (ВеО, ZnO, CaO) и несолеобразующие (NO, N2O, CO).
В свою очередь солеобразующие делятся ещё на три группы: основные (степень окисления метала +1,+2), амфотерные (степень окисления метала +3,+4,+5), кислотные (степень окисления метала +6,+7; степень окисления не метала +3 и больше)
Основные
1.Взаимодействие оксидов щелочных и щелочноземельных металлов с водой
CaO + H2O → Ca(OH)2
2.Взаимодействие с кислотами
MgO+ 2HNO3 → Mg(NO3)2+ 2H2O
3.Взаимодействие с кислотными оксидами
BaO + SO3 → BaSO4
4. Взаимодействие с амфотерными оксидами
Na2O + Al2O33 → NaAlO2
Кислотные
1.Взаимодействие с водой (образование кислоты)
SO3 + H2O → H2SO4
2. Взаимодействие с основными оксидами
SO3 + CuO → CuSO4
3. Взаимодействие с амфотерными оксидами
SO3 + Al2O3 → Al2 (SO4) 3
4. Взаимодействие с основаниями
N2O5 + 2NaOH → 2NaNO3 + H2O
Амфотерные
1. С кислотами (образование соли этой кислоты и воды)
Al2O3 + 6HCl → 2AlCl3 + 3H2O
2. Взаимодействие с кислотными оксидами
Al2O3 + N2O5 → 2Al(NO3) 3
3.Взаимодействие с основными оксидами
Al2O3 + Na2O → 2NaAlO2
4. Взаимодействие с щелочами (раствор)
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH) 4]
5. Взаимодействие с щелочами (расплав)
ZnO + 2KOH → K2ZnO2 + H2O
-
Основания
это сложные вещества, которые состоят из катиона металла и гидроксильной группы (OH).
1.Взаимодействие с кислотными оксидами
N2O5 + 2NaOH → 2NaNO3 + H2O
2. Взаимодействие с кислотами
Ba(OH) 2 + 2HNO3 → Ba(NO3) 2 + 2H2O
3. Взаимодействие с солями
KOH + MgSO4 → Mg(OH) 2↓ + K2SO4
4. Термическое разложение (только нерастворимые основания)
Cu(OH) 2 → CuO +H2O
5. Взаимодействие амфотерных гидроксидов со щелочами
Al(OH) 3(тв.) + KOH(тв.) → KAlO2 + 2H2O
Al(OH) 3(р-р) + KOH(р-р) → K[Al(OH) 4]
-
Соли
это сложные вещества, в состав которых входят катионы металла и анионы кислотного остатка. Иногда в состав солей входят водород или гидроксид-ион.
Соли делятся на 4 группы: средние (метал + кислотный остаток), кислые (метал + Н + кислотный остаток), основные (метал + ОН + кислотный остаток), комплексные(K[Al(OH)4])
Средние
1.Диссоциация
NaCl → Na+ + Cl—
2. Термическое разложение
CaCO3 → CaO + CO2
3. Взаимодействие солей с металлами
Fe + CuSO4 → FeSO4 + Cu
4. Гидролиз
Na2 CO3 + H2 O → NaOH + NaHCO3
5.Взаимодействие с кислотами
K2 CO3 + 2HCl → 2KCl + CO2 +H2 O
6. Взаимодействие с основаниями
Fe(NO3)3 + 3NaOH → Fe(OH)3 + 3NaNO3
7.Взаимодействие с солями
AgCl + 2Na2 S2 O3 → Nа3 [Ag(S2 O3)2] + NaCl
Кислые
1.Диссоциация.
NaHCO3 → Na + +HCO3 — HCO3− → H + + CO3 2-
2. Термическое разложение
Ca(HCO3)2 → CaCO3 + CO2 + H2 O
3. Взаимодействие солей со щелочью.
Ba(HCO3)2 + Ba(OH)2 → 2BaCO3 + 2H2 O
Основные
1.Термическое разложение
[Cu(OH)]2 CO3 → 2CuO + CO2 + H2 O
2.Взаимодействие с кислотами
Sn(OH)Cl + HCl → SnCl2 + H2 O
3. Диссоциация
Mg(OH)Cl → Mg(OH)+ + Cl— Mg(OH)+ → Mg2+ + OH—
Комплексные
1.Взаимодействие с кислотами
Na[Al(OH)4] + 4HCl(изб.) → NaCl + AlCl3 + 4H2 O
Na[Al(OH)4] + HCl(нед.) → NaCl + Al(OH)3 + H2 O
2.Диссоциация
K[Al(OH)4] → K++ [Al(OH)4] —
3. Взаимодействие с сероводородом
K[Al(OH)4]+ H2 S → KHS+Al(OH)3 ↓ +H2 O
4. Взаимодействие с кислотными оксидами
K[Al(OH)4]+CO2 → KHCO3+Al(OH)3 ↓
5.Термическое разложение
K[Al(OH)4] → KAlO2 +2H2 O
-
Кислоты
это сложные вещества, состоящие из атомов водорода (которые могут замещаться на атомы металлов) и кислотных остатков.
1. Диссоциация
HNO3 → H + + NO -3
2. Разложение
H2CO3 → H2O + CO2 ↑
3. Взаимодействие с металлами (до Н)
Mg + 2HCl → MgCl2 + H2 ↑
4. Взаимодействие с основаниями
H3 PO4+3NaOH →Na 3 PO4+3H2O
5. Взаимодействие с солями
BaCl2 + H2SO4 → BaSO4↓ + 2HCl↑
6. Взаимодействие с основными оксидами
K2O + 2HNO3 → 2KNO3 + H2O
7. Взаимодействие с амфотерными оксидами
2HNO 3 +ZnO → Zn(NO3) 2+H2O
Алгоритм решения
На самом деле все задачи уникальны и сложны по-своему. Очень трудно составить один алгоритм для решения всех задач. Можно только выявить некоторые базовые модули, определяющие общую стратегию и основные этапы решения задачи. А уже из них выстраивать ход решения, наполняя пустой алгоритм содержанием.
Поэтому я разработал алгоритм, которым можно пользоваться при решении этих задач
А) Определяем тип задачи
Б) Структурируем все данные (пишем дано)
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
Г) Устанавливаем логические связи (формулируем главный вопрос задачи, т.е. находим вещество, количество которого необходимо рассчитать, и логическую цепочку, связывающую количество этого вещества с веществами, количество которых мы знаем или можем вычислить).
Д)Решаем задачу
Примеры решения задач по алгоритму
Задача на электролиз
Электролиз 640 г 15%-го раствора сульфата меди(II) прекратили, когда масса раствора уменьшилась на 32,0 г. К образовавшемуся раствору добавили 400 г 20%-го раствора гидроксида натрия. Определите массовую долю щёлочи в полученном растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
А) Определяем тип задачи
Данная задача относится к типу задач на электролиз. Нужно вспомнить что мы знаем про электролиз.
Электролиз (греч. elektron — янтарь + lysis — разложение) — химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
- NaCl + H2O → H2 + Cl2 + NaOH
- CuSO4 + H2O → Cu + O2 + H2SO4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
- В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl3 → Al + Cl2
LiBr → Li + Br2
Если в условии задачи электролиз прекратили, то в дальнейшем взаимодействует не только продукт реакции, но и то вещество, которое подверглось электролизу.
Пример: При проведении электролиза 500 г 16%-го раствора сульфата меди(II) процесс прекратили, когда на аноде выделилось 1,12 л газа (н. у.). К образовавшемуся раствору прибавили 53,0 г 10%-го раствора карбоната натрия. Определите массовую долю сульфата меди(II) в полученном растворе.
В данном случае будет составлено 3 уравнения реакций:
- Электролиз сульфата меди (II).
- Реакция остатка сульфата меди (II) с карбонатом натрия
- Реакция серной кислоты с карбонатом натрия
Б) Структурируем все данные (пишем дано)
m (р-ра)(CuSO4)=640г
w (CuSO4)=15%
m (р-ра)(NaOH)=400г
w (NaOH)=20%
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
1) 2 CuSO4 + 2 H2O → O2 + 2 H2SO4 + 2 Cu
(электролиз 640 г 15%-го раствора сульфата меди(II) прекратили)
2) H2SO4 + 2 NaOH → 2 H2O+ Na2SO4
(К образовавшемуся раствору добавили 400 г 20%-го раствора гидроксида натрия)
3) CuSO4 + 2 NaOH → Na2SO4 + Cu(OH)2
(так как электролиз прекратили, в нём осталась какая-то доля сульфата меди(II), которая тоже будет реагировать с гидроксидом натрия)
Вывод: у нас получилось 3 уравнения реакций по которым мы будем вести вычисления
Г) Устанавливаем логические связи
Требуется найти массовую долю гидроксида натрия в полученном растворе.
1.Чтобы найти массовую долю гидроксида натрия в полученном растворе нужно знать массу раствора и массу самого гидроксида в этом растворе
W=m(ч.в.)/m(р-ра)*100%
2. Сульфат меди количественно связан с гидроксидом натрия- гидроксида натрия в 2 раза больше (3 реакция)
3. Гидроксид натрия связан с серной кислотой- гидроксида натрия в 2 раза больше (2 реакция)
4. Сульфат меди связан с серной кислотой – равны (1 реакция)
5.Сульфат меди связан с гидроксидом меди- равны (3 реакция)
Д)Решаем задачу
1.m(ч-в)(CuSO4)= 640г*15%/100% = 96г
2.n(CuSO4)= m/Mr = 96г/160 = 0,6 моль
3.m(ч-в)(NaOH)= 400г*20%/100% = 80г
4.n(NaOH)= m/Mr = 80г/40 = 2 моль
Пусть количество вещества образовавшегося кислорода n(O2) = х моль. Тогда количество вещества образовавшейся меди n(Сu) = 2xмоль. m(O2) = 32x(г), а m(Сu) = 64∙2x = 128x(г). По условию задачи: m(O2) + m(Сu) = 32.
32x + 128x = 32
х = 0,2(моль)
5.n(O2)=0,2 моль, а n(Cu)=0,4 моль, тогда n( изр)(CuSO4)=0,4 моль
6. n(ост)(CuSO4)(3ур.)=0,2 моль, а n(NaOH) в 2 раза больше (по 3 уравнению).
n(NaOH)=0,4 моль (в 3 реакции)
7.m(NaOH)=0,4 моль*40г/моль=16г
8.n( изр)(CuSO4)(1ур)=n(H2SO4)=0,4 моль
9.m(1ур)(H2SO4)=0,4 моль*98г/моль=39,2г
10.n(2ур.)(NaOH) в 2 раза больше n(H2SO4) (по 2 реакции)
n (2ур.) (NaOH)=0,8 моль
11.n(изр)(NaOH)=0,8+0,4=1,2 моль
12.n(ост)(NaOH)=2 моль-1,2 моль=0,8моль
13.m(ост)(NaOH)=0,8*40=32г
14.n(Cu(OH2)=n(CuSO4)=0,2 моль (по 3 реакции)
15.m(Cu(OH2)=0,2 моль *98г/моль=19,6 г
16.m(кон.раств.)=m(CuSO4)+ m(NaOH)-32г- m(Cu(OH2)=640+400-32- 19,6=988,4г
17.w(NaOH)= m(NaOH)/ m(кон.раств.)=32г*100%/988,4г=3,24%
Ответ: w(NaOH)= 3,24%
Задача на кристаллогидрат
Смесь цинка и цинкового купороса (ZnSO4 · 7H2O) полностью растворилась в 160 г раствора гидроксида натрия, при этом выделилось 2,24 л газа (н.у.) и образовался раствор массой 172,04 г. Вычислите массовые доли солей в полученном растворе
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
А) Определяем тип задачи
Кристаллогидраты — это сложные вещества, которые содержат в кристаллической решетке молекулы воды.
Многие соединения (чаще всего соли) выкристаллизовываются из водных растворов в виде кристаллогидратов.
При расчёте молярной массы нельзя забывать про воду.
Пример: ZnSO4 · 7H2O
Его молярная масса будет не 161г/моль, а 287г/моль (161 — ZnSO4 ,126 — 7H2O)
Часто встречающиеся кристаллогидраты в ЕГЭ
|
Кристаллогидрат |
Тривиальное название/ название по систематической номенклатуре |
|
Na2CO3 · 10H2O |
Кристаллическая сода, декагидрат карбоната натрия |
|
CaSO4 · 2H2O |
Гипс, дигидрат сульфата кальция |
|
CuSO4 · 5H2O |
Медный купорос, пентагидрат сульфата меди(II) |
|
Na2SO4 · 10H2O |
Кристаллическая сода, декагидрат карбоната натрия |
|
FeSO4 · 7H2O |
Железный купорос, гептагидрат сульфата железа(II) |
|
ZnSO4 · 7H2O |
Цинковый купорос, гептагидрат сульфата цинка(II) |
Б) Пишем «дано» исходя из условия задачи
m(NaOH)=160г
V(H2)=2,24л
m(кон.раств.)=172,04г
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
1) ZnSO4 + 4NaOH → Na2 [Zn(OH)4] + Na2SO4
(Смесь цинка и цинкового купороса (ZnSO4 ·7H2O) полностью растворилась в 160 г раствора гидроксида натрия)
2) Zn + 2NaOH + 2H2O → Na2 [Zn(OH)4] + H2
(Смесь цинка и цинкового купороса (ZnSO4 · 7H2O) полностью растворилась в 160 г раствора гидроксида натрия)
Г) Устанавливаем логические связи
Требуется найти массовые доли солей в полученном растворе
1.Чтобы найти массовые доли солей в полученном растворе нужно знать массу раствора и массу самих солей в этом растворе
W=m(ч.в.)/m(р-ра)*100%
2. Цинк связан с водородом –равны (2 реакция)
3. Сульфат натрия связан с сульфатом цинка- равны(1 реакция)
Д)Решаем задачу
1.n(H2)=2,24л/22,4л/моль=0,1 моль
2.m(H2)=0,1 моль*2 г/моль=0,2 г
3. n(Zn)= n(H2)=0,1 моль
4. m(Zn)= 0,1 моль* 65г/моль=6,5г
5. m(кон.раств.)= m(исх)+m(Zn)+m(ZnSO4 · 7H2O)-m(H2)
m(ZnSO4 · 7H2O)=m(кон.раств.)-m(исх)— m(Zn)-m(H2)=172,04г-160г-6,5г+0,2г=5,74г
6.n (ZnSO4 · 7H2O)=n(ZnSO4)=5,74г/287г/моль=0,02 моль
7.n(Na2SO4)=n(ZnSO4)= 0,02 моль
8.n(Na2 [Zn(OH)4])=n(Zn)+ n(ZnSO4)=0,1 моль+0,02 моль=0,12 моль
9. m(Na2SO4)=0,02 моль*142г/моль=2,84г
10. m(Na2 [Zn(OH)4])=0,12 моль*179г/моль=21,48г
11.w(Na2SO4)=2,84г/172,04г*100%=1,65%
12. w(Na2 [Zn(OH)4])=21,48г/172,04г*100%=12,49%
Ответ: w(Na2SO4)= 1,65%; w(Na2 [Zn(OH)4])=12,49%
Задача на пластинку
Навеску оксида меди(II) массой 12,0 г растворили в 200 г 9,8 %-й серной кислоты. В полученный раствор опустили железную пластинку, выдержали до прекращения реакции и удалили из раствора. Найдите массовую долю соли в полученном растворе. Примите Ar(Cu)=64. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите необходимые вычисления (указывайте единицы измерения искомых физических величин).
А) Определяем тип задачи
Данная задача относится к типу задач на пластинку. Решая задачи, важно понимать, что реакции металлов с солями являются окислительно-восстановительными и протекают на поверхности металла, погруженного в раствор соли а выделившийся в результате реакции металл осаждается на данной поверхности.
Б) Пишем «дано» исходя из условия задачи
m(CuO)=12,0г
m(H2SO4)=200г
w(H2SO4)=9,8%
Ar(Cu)=64
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
1) CuO+ H2SO4→ CuSO4+ H2O
(Навеску оксида меди(II) массой 12,0 г растворили в 200 г 9,8 %-й серной кислоты)
2) CuSO4+Fe→FeSO4+Cu
(В полученный раствор опустили железную пластинку, выдержали до прекращения реакции и удалили из раствора)
3) H2SO4+ Fe→ FeSO4+ H2
( В полученный раствор опустили железную пластинку, выдержали до прекращения реакции и удалили из раствора)
Г) Устанавливаем логические связи
Требуется найти массовую долю соли в полученном растворе
1.Чтобы найти массовую долю соли в полученном растворе нужно знать массу раствора и массу самой соли в этом растворе
W=m(ч.в.)/m(р-ра)*100%
2.Сульфид меди связан с оксидом меди — равны (1 реакция)
3.Сульфид железа связан с сульфидом меди – равны (2 реакция)
4.Серная кислота связана с оксидом меди – равны
5.Сульфид железа связан с серной кислотой – равны (3 реакция)
Д)Решаем задачу
1)n(CuO)=12/80=0,15 моль
2) m(H2SO4)=200*9,8%/100%=19,6г
3) n(H2SO4)=200*0,098/98=0,2 моль
4) n(CuSO4)= n(CuO)=0,15 моль (1 реакция)
5) n(FeSO4)= n(CuSO4)= )=0,15 моль (2 реакция)
6) n(H2SO4)= n(CuO)=0,15 моль
7) n(H2SO4)=0,2 моль-0,15 моль=0,05 моль (3 реакция)

9)m(FeSO4)=(0,15+0,05)*152=30,4г
10)m(H2O в FeSO4)= m(H2O в H2SO4)+ m(H2O) = (200 -19,6)+0,15*18= 183,1г
11)mраств(FeSO4)=m(FeSO4)+m(H2O)=30,4+183,1= 213,5
12) w(FeSO4)=30,4*100/213,5=14,2%
Ответ: w(FeSO4)= 14,2%
Задача на выход реакции
При взаимодействии в сернокислой среде 17,4 г диоксида марганца с 58 г бромида калия при 77%-ном выходе выделился бром. Какой объём (н. у.) пропена может провзаимодействовать с полученным количеством брома?
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
А) Определяем тип задачи
Данная задача относится к типу задач на выход реакции. Выход продукта реакции (выход реакции) — это коэффициент, определяющий полноту протекания химической реакции. Он численно равен отношению количества (массы, объема) реально полученного продукта к его количеству (массе, объему), которое может быть получено по стехиометрическим расчетам (по уравнению реакции).
Б) Пишем «дано» исходя из условия задачи
m (MnO2)=17,4г
m (KBr)=58г
η=77%=0,77
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
1)MnO2+2KBr+2 H2SO4 →MnSO4+Br2+K2SO4+2 H2O
(При взаимодействии в сернокислой среде 17,4 г диоксида марганца с 58 г бромида калия при 77%-ном выходе выделился бром)
2)C3H6+Br2→C3H6Br2
(Какой объём (н. у.) пропена может провзаимодействовать с полученным количеством брома)
Г) Устанавливаем логические связи
1)Требуется найти объём пропена. Что бы найти объём нужно знать его количество
V=n • 22.4 (л/моль)
2)Бром связан с диоксидом марганца – равны (1 реакция)
3)Пропен связан с бромом – равны (2 реакция)
Д)Решаем задачу
1) n(MnO2)=17,4/81=0,2 моль
2) n(KBr)=58/119=0,49
KBr – избыток
3) n(Br2)= n(MnO2)=0,2 моль (1 реакция)
4) n(Br2)=0,2 моль*0,77=0,154 моль (с учётом выхода реакции)
5) n(C3H6)= n(Br2)=0,154 моль (2 реакция)
6)V(C3H6)=0,154 моль *22,4 л/моль=3,450 л
Ответ: V(C3H6)= 3,450 л
Задача на расстворимость
Растворимость карбоната аммония составляет 96 г на 100 г воды. Приготовили насыщенный раствор с 250 мл воды, разделили его на две колбы. В первую колбу добавили избыток твёрдого гидроксида натрия и нагрели, а во вторую — 250 г соляной кислоты (тоже в избытке). При этом из второй колбы выделилось в три раза меньше газа (при одинаковых условиях), чем из первой. Определите массовую долю соли во второй пробирке. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
А) Определяем тип задачи
Данная задача относится к типу задач на растворимость.
Б) Пишем «дано» исходя из условия задачи
m(H2O)=250г
m(HCl)=250г
В) Проводим анализ условия (составляем уравнения химических реакций, о которых упоминается в условии задачи)
1) (NH4)2CO3+2NaOH→Na2CO3+NH3+2H2O
(В первую колбу добавили избыток твёрдого гидроксида натрия и нагрели)
2) (NH4)2CO3+2HCl→2NH4Cl+H2O+CO2
(а во вторую — 250 г соляной кислоты (тоже в избытке))
Г) Устанавливаем логические связи
Требуется найти массовую долю соли во 2 пробирке
1.Чтобы найти массовую долю соли во 2 пробирке нужно знать массу раствора и массу самой соли в этом растворе
W=m(ч.в.)/m(р-ра)*100%
2)Углекислый газ связан с карбонатом амония – равны (2 реакция)
3)Хлорид амония связан с карбонатом амония – в 2 раза меньше (2 реакция)
Д)Решаем задачу
1) m((NH4)2CO3)= 96г – m(H2O)=100г
m((NH4)2CO3)=x г — m(H2O)=250г
m((NH4)2CO3)=96г*250г/100г=240г
2)n((NH4)2CO3)=240г/96г/моль=2,5 моль
3) Пусть n((NH4)2CO3) во 2 колбе = х моль, тогда n((NH4)2CO3) в 1 колбе =1,5х моль
х+1,5х=2,5
х=1 моль n((NH4)2CO3)=1 моль (2 реакция)
4)m((NH4)2CO3)=1 моль*96г/моль= 96г (2 реакция)
5) m раств((NH4)2CO3)=196г
6) n(CO2)= n((NH4)2CO3)=1 моль (2 реакция)
7) m(CO2)=1 моль *44г/ моль =44г

9) m(NH4Cl)= 2 моль * 53,5 г/моль= 107 г
10)w(NH4Cl)= m(NH4Cl)/ (m раств((NH4)2CO3)+ m(HCl) — m(CO2))*100%=107г/(196+250-44)*100%=107г/402г*100%=26,6%
Ответ: w(NH4Cl)= 26,6%
Задания 34 (2022). Расчет массовой доли химического соединения в смеси.
Задание №1
Смесь меди и оксида меди(II), в которой масса протонов в ядрах всех атомов составляет 46% от общей массы смеси, разделили на две равные части. К первой части добавили избыток разбавленного раствора серной кислоты. При этом образовалось 528 г раствора с массовой долей соли 10%. Ко второй части добавили 700 г разбавленного раствора азотной кислоты, взятого в избытке. Вычислите массовую долю нитрата меди(II) в образовавшемся растворе.
Решение
Ответ: ꞷ(Cu(NO3)2)=12,31 %
Пояснение:
CuO + H2SO4 ⟶ CuSO4 + H2O (I)
3Cu + 8HNO3 ⟶ 3Cu(NO3)2 + 2NO + 4H2O (II)
CuO + 2HNO3 ⟶ Cu(NO3)2 + H2O (III)
1) Исходя из условия, можем сразу найти количество вещества сульфата меди(II):
m(CuSO4) = = 52,8 г
n(CuSO4) = 52,8/160 = 0,33 моль
2) Найдем количество протонов в смеси меди и оксида меди (II), при этом примем количество обоих веществ за 1 моль.
N(p+) в Cu = 29 частиц;
N(p+) в CuO = 29 + 8 = 37 частиц;
3) По условию массовая доля протонов составляет 46% от общей массы. Это значит, что масса протонов составляет 46% (или 0,46) от суммы масс двух веществ. Составим уравнение, зная, что молярная масса одного протона составляет 1 г/моль.
ꞷ(p+) = mp+ / m(Cu) + m(CuO)
4) Пусть n(Cu) = x моль, тогда m(Cu) = 64x г;
m общ.(CuO) = nобщ.(CuO) · M
nобщ.(CuO) = 0,33 · 2 = 0,66 моль – так как смесь разделили на 2 равные части
m общ.(CuO) = 0,66 · 80 = 52,8 г
m(p+) = mCu(p+) + mCuO(p+)
Если в 1 моль меди содержится 29 протонов, то в n(Cu) = x моль, содержится 29x протонов, а значит: m(p+) = (29x моль) · (1 г/моль) = 29x г
Если в 1 моль оксида меди(II) содержится 37 моль протонов, то в n(CuO) = 0,33 моль содержится 0,66 ∙ 37 = 24,42 моль протонов, а значит: m(p+) = 24,42 ∙ 1 = 24,42 г.
5) Подставим под уравнение:
0,46 = (29x + 24,42) / (64x + 52,8)
29,44x + 24,29 = 29x + 24,42
0,44x = 0,13
x = 0,13/0,44 = 0,3 моль – общее количество меди.
0,3/2 = 0,15 моль – количество меди в одной части смеси.
6) По уравнениям реакций найдем m(Cu(NO3)2):
n2(Cu(NO3)2) = n2(Cu) = 0,15 моль
n3(Cu(NO3)2) = n3(CuO) = 0,33 моль
nобщ.(Cu(NO3)2) = 0,15 + 0,33 = 0,48 моль.
mобщ.(Cu(NO3)2) = M·n = 0,48 · 188 = 90,24 г
7) Найдем ꞷ(Cu(NO3)2):
mр—ра(Cu(NO3)2) = m(Cu) + m(CuO) + mр—ра(HNO3) – m(NO)
m(Cu) = M·n = 0,15 · 64 = 9,6 г
m(CuO) = M·n = 0,33 · 80 = 26,4 г
m(NO) = 2/3 · n·M = 2/3 · 0,15 · 30 = 3 г
mр—ра(Cu(NO3)2) = 9,6 + 26,4 + 700 – 3 = 733 г
ꞷ(Cu(NO3)2) = (90,24/733) · 100% = 12,31 %
Задание №2
К 60 г раствора дигидрофосфата натрия, в котором 55% от общей массы раствора составляет масса протонов в ядрах всех атомов, добавили 40 г 15%-ного раствора гидроксида натрия. Затем к образовавшемуся раствору добавили 51 г нитрата серебра. Определите массовую долю нитрата серебра в конечном растворе.
Решение
Ответ: ꞷ(AgNO3) = 13,68 %
Пояснение:
1) Так как при взаимодействии дигидрофосфата натрия со щелочью может образовываться два типа солей: фосфат натрия либо гидрофосфат натрия – необходимо вычислить соотношение реагентов.
m(NaOH) = 0,15 · 40 = 6 г
n(NaOH) = 6/40 = 0,15 моль
2) Известно, что в растворе NaH2PO4 протоны в ядрах всех атомов составляют 55 % от общей массы раствора. Понимая, что раствор состоит из массы самого растворенного вещества и массы воды, примем, что m(NaH2PO4) = x г, а m(H2O) = y г.
Посчитаем массу протонов в каждом из веществ, примем их количество за 1 моль, а молярную массу одного протона за 1 г/моль:
а) mp+(NaH2PO4) = mp+(Na) + 2mp+(H) + mp+(P) + 4mp+(O) = 11+2+15+32 = 60 г
mp+(NaH2PO4) : m(NaH2PO4) = 60 : 120 = 1 : 2
Следовательно, в x г NaH2PO4 содержится 0,5x г протонов.
б) mp+(H2O)=2mp+(H) + mp+(O) = 2+8=10 г — протонов содержится в 1 моль воды (18г).
Следовательно, в y г H2O содержится 10y/18 г протонов.
Найдем общую массу протонов в растворе:
mp+(р-раNaH2PO4) = mр-ра(NaH2PO4) · ꞷp+ = 60 · 0,55 = 33 г
0,5x + 10/18y = 33 (г)
Составим систему уравнений:
Решая которую находим, что:
y = 54
x = 60 – 54 = 6
m(H2O) = 54 г
m(NaH2PO4) = 6 г
3) n(NaH2PO4)= 6/120 = 0,05 моль
Таким образом, мы можем записать, что количества веществ дигидрофосфата натрия и гидроксида натрия относятся друг к другу как:
n(NaH2PO4) : n(NaOH) = 0,05 : 0,15 = 1:3,
следовательно, щелочь в избытке и протекать будут следующие реакции:
NaH2PO4 + 2NaOH ⟶ Na3PO4 + 2H2O (I)
Na3PO4 + 3AgNO3 ⟶ Ag3PO4 + 3NaNO3 (II)
2NaOH + 2AgNO3 ⟶ Ag2O + H2O + 2NaNO3 (III)
Найдем ꞷ(AgNO3) в конечном растворе:
а) nост.(NaOH) = nисх.(NaOH) — n1(NaOH)
n1(NaOH) = 2n(NaH2PO4) = 2 · 0,05 = 0,1 моль
nост.(NaOH) = 0,15 – 0,1 = 0,05 моль
n(Ag3PO4) = n(Na3PO4) = n(NaH2PO4) = 0,05 моль
m(Ag3PO4) = 0,05 · 419 = 20,95 г
n(AgNO3) = 51/170 = 0,3 моль
nост.(NaOH) : n(AgNO3) = 0,05 : 0,3 =1:6 – следовательно, n(AgNO3) в избытке
n(Ag2O) = 0,5nост.(NaOH) = 0,025 моль
m(Ag2O) = 0,025 · 232 = 5,8 г
б) Найдем массу конечного раствора. Помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки.
mр-ра кон.(AgNO3) = mр-ра(NaH2PO4) + mр-ра(NaOH) + m(AgNO3) – m(Ag3PO4) – m(Ag2O)
mр-ра кон.(AgNO3) = 60 + 40 + 51 – 20,95 – 5,8 = 124,25 г
в) nост.(AgNO3) = 0,3 – n2(AgNO3) – n3(AgNO3) = 0,3 – 3n2(Na3PO4) – n(NaOH) = 0,3 – 0,15 – 0,05 = 0,1 моль
mост. (AgNO3) = 0,1 · 170 = 17 (г)
ꞷ(AgNO3) = 17/124,25 · 100% = 13,68%
Ответ: ꞷ(AgNO3) = 13,68%
Задание №3
Олеум массой 114 г, в котором общее число электронов в 58 раз больше числа Авогадро, растворили в 26 г воды, затем добавили 23,2 г железной окалины и нагрели. Вычислите массовую долю соли в конечном растворе. Возможным образованием кислых солей пренебречь.
Решение
Ответ: ꞷ(Fe2(SO4)3) = 37,5%
Пояснение:
Для решения подобных задач удобнее считать, что олеум – это раствор SO3 в безводной H2SO4, т.е. воды в нем нет.
1) Для начала определим соотношение веществ в олеуме:
а) Пусть n(SO3) = x моль, а n(H2SO4) = y моль, тогда m(SO3) = 80x г, а m(H2SO4) = 98y г. По условию масса олеума составляет 114 г, следовательно: 80x + 98y = 114 г.
б) Найдем количество электронов в обоих веществах. При этом помним, что количество электронов = количеству протонов = порядковому номеру элемента.
n(e) в x моль SO3 равно: 16x + 3·8x = 40x моль;
n(e) в y моль H2SO4 равно: 2·1y + 16y + 4·8y = 50y моль;
По условию известно, что N(e) в 58 раз больше числа Авогадро (NA), вспоминаем формулу:
n(e) = N/NA , где N = 58NA , то есть: n(e) = 58NA/NA = 58 моль ⇒ 40x + 50y = 58 моль
в) Составим систему уравнений:
решая которую, получаем, что:
y = 1, x = 0,2,
n(H2SO4) = 1 моль, n(SO3) = 0,2 моль, следовательно, n(SO3) в недостатке.
Для того чтобы понять какое уравнение следует записать для второй реакции нам следует понять какой концентрации раствор серной кислоты мы получим в результате добавления олеума к воде. Если раствор серной кислоты получится разбавленным — железная окалина растворится в растворе серной кислоты с образованием двух солей (железа (II) и железа (III). Если же раствор серной кислоты окажется концентрированным, реакция железной окалины с серной кислотой приведет к образованию диоксида серы, сульфата железа(III) и воды.
При добавлении олеума к воде протекает следующая реакция:
SO3 + H2O ⟶ H2SO4 (I)
а) nI(H2SO4) = n(SO3) = 0,2 моль;
mI(H2SO4) = 98 + 0,2 = 19,6 г;
б) mр—ра(H2SO4) = m(олеума) + m(H2O);
mр—ра(H2SO4) = 114 + 26 = 140 г;
в) m(H2SO4) = mисх.(H2SO4) + mI(H2SO4);
m(H2SO4) = 98 + 19,6 = 117,6 г;
ꞷ(H2SO4) = 117,6/140 · 100% = 84% — следовательно, образовавшийся раствор кислоты можно считать концентрированным, а значит протекает следующая реакция:
2Fe3O4 + 10H2SO4 = 3Fe2(SO4)3 + SO2 + 10H2O (II)
Определим массовую долю соли в конечном растворе:
а) n(Fe3O4) = 23,2/232 = 0,1 моль;
б) n(Fe2(SO4)3) = 3/2n(Fe3O4) = 3/2 · 0,1 = 0,15 моль;
m(Fe2(SO4)3) = 0,15 · 400 = 60 г;
в) n(SO2) = 1/2n(Fe3O4) = 0,5 · 0,1 = 0,05 моль;
m(SO2) = 0,05 · 64 = 3,2 г;
г) mр—ра(Fe2(SO4)3) = mр—ра(H2SO4) + m(Fe3O4) – m(SO2);
mр—ра(Fe2(SO4)3) = 140 + 23,2 – 3,2 = 160 г;
д) ꞷ(Fe2(SO4)3) = 60/160 · 100% = 37,5%.
Задание №4
Смесь фосфида цинка и нитрида магния общей массой 65,7 г, в которой общее число электронов в 32 раза больше числа Авогадро, растворили в 730 г 30%-ной соляной кислоты. Вычислите массовую долю кислоты в конечном растворе.
Решение
Ответ: ꞷост.(HCl) = 10,18%
Пояснение:
Сразу запишем уравнения реакций:
Zn3P2 + 6HCl = 3ZnCl2 + 2PH3 (I)
Mg3N2 + 8HCl = 3MgCl2 + 2NH4Cl (II)
Для начала можем сразу определить n(HCl), исходя из условия:
а) m(HCl) = 730 · 0,3 = 219 г
n(HCl) = 219/36,5 = 6 моль
2) По условию масса смеси (Zn3P2 и Mg3N2) равна 65,7 г. Составим первое уравнение системы:
Пусть n(Zn3P2) = x моль, тогда m(Zn3P2) = 257x г
Пусть n(Mg3N2) = y моль, тогда m(Mg3N2) = 100y г
Следовательно: 257x + 100y = 65,7 г
3) Далее перейдем к количеству электронов. По условию: общее число электронов в смеси в 32 раза больше числа Авогадро – это можно записать так:
n(e) = N/NA , где N = 32NA , то есть: n(e) = 32NA/NA = 32 моль
Далее найдем количества электронов в веществах смеси отдельно. При этом помним, что количество электронов = количеству протонов = порядковому номеру элемента.
а) Ne(Zn3P2) = 30 ·3 + 15 · 2 = 120 электронов.
Если в 1 моль Zn3P2 содержится 120 · 1 = 120 моль электронов, то в x моль (Zn3P2) содержится 120x моль.
б) Ne(Mg3N2) = 12 · 3 + 7 · 2 = 50 электронов.
Если в 1 моль Mg3N2 содержится 50 · 1 = 50 моль электронов, то в y моль (Zn3P2) содержится 50y моль.
в) Составим второе уравнения системы: 120x + 50y = 32
Решим систему уравнений, найдем x и y:
x = 0,1 (моль) – n(Zn3P2);
y = 0,4 (моль) – n(Mg3N2);
Найдем массу оставшейся в растворе соляной кислоты (логично, что если она осталась, значит была в избытке):
а) n1(HCl) = 6n(Zn3P2) = 0,1 · 6 = 0,6 моль
n2(HCl) = 8n(Mg3N2) = 0,4 · 8 = 3,2 моль
nост.(HCl) = 6 — 3,2 — 0,6 = 2,2 моль
б) mост.(HCl) = 2,2 · 36,5 = 80,3 г
Найдем массу конечного раствора. Помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки. Из газов у нас только PH3 (никакого NH3 там нет! Он прореагировал с соляной кислотой и перешел в NH4Cl! баллы не теряем).
а) mконечн. р-ра(HCl) = mсмеси + mисх. р-ра (HCl) – m(PH3)
б) n(PH3) = 2n(Zn3P2) = 0,2 моль
m(PH3) = 0,2 · 34 = 6,8 г
в) mконечн. р-ра(HCl) = 65,7 + 730 – 6,8 = 788,9 г
Найдем ꞷост.(HCl):
ꞷост.(HCl) = (80,3/788,9) · 100% = 10,18%
Ответ: ꞷост.(HCl) = 10,18% .
Задание №5
К 125 г раствора аммиака, в котором 56% от общей массы раствора составляет масса протонов в ядрах всех атомов, добавили 40,05 г хлорида алюминия. Через образовавшийся раствор пропустили сернистый газ, при этом прореагировало 2,24 л (н.у.) газа. Вычислите массовые доли солей в конечном растворе. Растворимостью газов в воде пренебречь.
Решение
Ответ: ꞷ(NH4Cl) = 32,5%; ꞷ(NH4HSO3) = 6,69%
Пояснение:
1) Для начала можем сразу записать следующую реакцию:
AlCl3 + 3NH3 + 3H2O = Al(OH)3 + 3NH4Cl (I)
2) Найдем количества веществ, данных в условии:
а) n(AlCl3) = 40,05/133,5 = 0,3 моль;
б) n(SO2) = 2,24/22,4 = 0,1 моль;
3) Далее мы не можем сразу сделать вывод о том какая реакция протекает:
SO2 + NH3 + H2O = NH4HSO3 либо SO2 + 2NH3 + H2O = (NH4)2SO3
Также возможен случай когда образуются сразу две соли одновременно.
Обратим внимание на соотношение реагентов (SO2 и NH3) в двух реакциях: 1:1 и 1:2 соответственно. Чтобы сделать вывод, какая из двух реакций протекает, необходимо провести дальнейшие расчеты.
4) В условии сказано, что масса раствора аммиака составляет 125 г. Раствор состоит из воды и аммиака.
Пусть n(NH3) = x моль, а n(H2O) = y моль. Тогда m(NH3) = 17x г, а m(H2O) = 18y г.
Составим первое уравнение системы: 17x + 18y = 125 г
5) Также известно, что массовая доля протонов в ядрах всех атомов составляет 56% от массы раствора. Найдем количество и массу протонов. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
а) Np+(NH3) = 7 + 1 · 3 = 10 протонов;
Если в 1 моль NH3 содержится 10 · 1 = 10 моль протонов, то в x моль NH3 содержится 10x моль.
m p+(NH3) = 10x · 1 = 10x г;
б) Np+(H2O) = 1 · 2 + 8 = 10 протонов;
Если в 1 моль H2O содержится 10 · 1 = 10 моль протонов, то в y моль H2O содержится 10y моль.
mp+( H2O) = 10y · 1 = 10y г;
в) Составим второе уравнение системы:
0,56 = (10x + 10y)/125 ⇒ 10x + 10y = 70
Составим систему уравнений:
Решая которую находим, что:
y = 6
x = 1
Следовательно:
n(H2O) = y моль = 6 моль,
n(NH3) = x моль = 1 моль
7) Вернемся к действию 3) и сравним количества веществ, но для этого нам сначала необходимо найти количество оставшегося аммиака, так как его часть ушла на первую реакцию.
а) n1(NH3) = 3n(AlCl3) = 3 · 0,3 = 0,9 моль
nост.(NH3) = 1 – 0,9 = 0,1 моль;
б) n(SO2) : n(NH3) = 0,1 : 0,1 = 1 : 1 – следовательно, реакция протекает до образования кислой соли.
SO2 + NH3 + H2O = NH4HSO3 (II)

а) n(NH4Cl) = 3n(AlCl3) = 3 · 0,3 = 0,9 моль
m(NH4Cl) = 0,9 · 53,5 = 48,15 г;
б) n(NH4HSO3) = n(SO2) = 0,1 моль,
m(NH4HSO3) = 0,1 · 99 = 9,9 г;
9) Напишем уравнение массы конечного раствора. Помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки.
mконечн. р-ра = mр-ра(NH3) + m(AlCl3) – m(Al(OH)3) + m(SO2)
Вычислим недостающие данные:
а) n(Al(OH)3) = n(AlCl3) = 0,3 моль
m(Al(OH)3) = 0,3 · 78 = 23,4 г;
б) m(SO2) = 0,1 · 64 = 6,4 г;
в) Найдем массу конечного раствора:
mконечн. р-ра = 125 + 40,05 – 23,4 + 6,4 = 148,05 г
Найдем массовую долей солей в образовавшемся растворе:
ꞷ(NH4Cl) = (48,15/148,05) · 100% = 32,5% ;
ꞷ(NH4HSO3) = (9,9/148,05) · 100% = 6,69%
Ответ: ꞷ(NH4Cl) = 32,5%; ꞷ(NH4HSO3) = 6,69% .
Задание №6
Пластинку, сделанную из сплава цинка со свинцом, в которой общее число электронов в атомах металлов в 56 раз больше числа Авогадро, поместили в 100 г раствора хлорида олова(II). После того как хлорид олова(II) прореагировал полностью, пластинку с выделившимся на ней металлом извлекли из раствора. В результате общее число электронов в атомах трёх металлов пластинки увеличилось на 12,5% по сравнению с числом электронов в атомах металлов исходной пластинки. К оставшемуся раствору добавили 480 г 20%-ного раствора гидроксида натрия. Вычислите массовую долю щёлочи в конечном растворе. Процессом гидролиза солей пренебречь.
Решение
Ответ: ꞷост.(NaOH) = 7,13%
Пояснение:
1) Для начала можно записать уравнение первой реакции (понятно, что реагировать из двух металлов пластинки будет цинк, так как он активнее):
Zn + SnCl2 = ZnCl2 + Sn (I)
Уравнение второй реакции сразу записать нельзя, так как она может протекать по двум направлениям:
ZnCl2 + 4NaOH = Na2[Zn(OH)4] + 2NaCl либо ZnCl2 + 2NaOH = Zn(OH)2 + 2NaCl
Обратим внимание на соотношение реагентов: 1:4 и 1:2 — и на основании дальнейших расчетов сделаем вывод о том, какая реакция протекает.
По условию, общее число электронов пластинки в 56 раз больше числа Авогадро. Записать это можно следующим образом:
n(e) = N/NA , где N = 56NA , то есть: n(e) = 56NA/NA = 56 моль, то есть общее количество электронов в Zn-Pb пластинке равно 56 моль.
Пусть n(Zn) = x моль, а n(Pb) = y моль. Помним, что количество электронов в атоме химического элемента точно такое же, как и количество протонов и численно равно порядковому номеру элемента.
В таком случае, количество вещества электронов в металлическом цинке будет равно:
ne(Zn) = N(e—)·n(Zn) = 30x моль,
а количество вещества электронов в металлическом свинце будет равно:
ne(Pb) = 82y моль
Тогда, суммарное количество вещества электронов пластинки из цинка и свинца будет равно:
ne(Zn/Pb пластинки) = (30x + 82y) моль,
в то же время мы знаем, что ne(Zn/Pb пластинки) = 56 моль, отсюда следует первое уравнение системы:
30x + 82y = 56
Известно, что общее число электронов в пластинке из трёх металлов на 12,5% по сравнению больше по сравнению с числом электронов в атомах металлов исходной пластинки из двух металлов.
Тогда, изменение количества вещества электронов пластинки после реакции будет равно:
Δne(пластинки) =56 · 0,125 = 7,
а общее количество электронов в пластинке из трех металлов (после реакции):
ne(пластинки Zn-Pb-Sn) = 56 + 7 = 63 – общее количество электронов пластинки после реакции.
Изменение количества электронов пластинки произошло из-за того, что часть цинка с пластинки ушла в раствор, а часть олова из раствора соли выделилась на пластинке.
Количество электронов в исходной пластинке:
Ne исходной пл. = Ne(Pb) + Ne исх.(Zn),
а количество вещества электронов в исходной пластинке:
ne исходной пл. = ne(Pb) + ne исх.(Zn),
Количество электронов в конечной пластинке:
Ne конечной пл. = Ne(Pb) + Ne исх.(Zn) – Ne прореаг.(Zn) + Ne(Sn),
а количество вещества электронов в конечной пластинке:
ne конечной пл. = ne(Pb) + ne исх.(Zn) – ne прореаг.(Zn) + Ne(Sn),
Тогда, разница количества вещества электронов может быть записано как:
Δne(пластинки) = ne конечной пл. — ne исходной пл. = (ne(Pb) + ne исх.(Zn) – ne прореаг.(Zn) + Ne(Sn)) — (ne(Pb) + ne исх.(Zn)) = ne(Pb) + ne исх.(Zn) – ne прореаг.(Zn) + Ne(Sn) — ne(Pb) — ne исх.(Zn) = — ne прореаг.(Zn) + ne(Sn) = ne(Sn) — ne прореаг.(Zn)
т.е. Δne(пластинки) = ne(Sn) — ne прореаг.(Zn)
Из уравнения реакции I можно сделать вывод, что количество вещества осевшего Sn равно количеству прореагировавшего Zn. Пусть n(Sn) = nпрореаг.(Zn) = z моль.
Тогда количество вещества электронов в образовавшемся олове будет равно:
ne(Sn) = 50z моль,
а количество вещества электронов в прореагировавшем цинке будет равно:
ne прореаг.(Zn) = 30z моль.
Таким образом,
Δne(пластинки) = ne(Sn) — ne прореаг.(Zn) = 50z — 30z = 20z моль,
в то же время:
Δne(пластинки) = 7 моль,
следовательно:
7 = 20z
z = 0,35,
а n(Sn) = nпрореаг.(Zn) = n1(ZnCl2) = 0,35 моль,
Перейдем теперь к расчету соотношения щелочи и хлорида цинка.
а) mисх.(NaOH) = 480 · 0,2 = 96 г
nисх.(NaOH) = 96/40 = 2,4 моль;
б) nисх.(NaOH)/n(ZnCl2)= 2,4/0,35 = 6,9
Следовательно, можно сделать вывод, что NaOH находится в избытке, поэтому реакция будет протекать по пути комплексообразования:
ZnCl2 + 4NaOH = Na2[Zn(OH)4] + 2NaCl (II)
Рассчитаем количество вещества и массу непрореагировавшего гидроксида натрия:
а) nпрореаг.(NaOH) = 4n(ZnCl2) = 0,35 · 4 = 1,4 моль
nост.(NaOH) = 2,4 – 1,4 = 1 моль;
б) mост.(NaOH) = 1 · 40 = 40 г
Напишем выражение массы конечного раствора:
mконечн. р-ра = mр-ра(SnCl2) + mушедш.(Zn) – mосевш.(Sn) + mр-ра(NaOH)
mконечн. р-ра = 100 + (65 · 0,35) – (119 · 0,35) + 480 = 561,1 г
Рассчитаем массовую долю щелочи в конечном растворе:
ꞷост.(NaOH)= (40/561,1) · 100% = 7,13%
Ответ: ꞷост.(NaOH) = 7,13%
Задание №7
Смесь фосфида и нитрида лития, в которой масса протонов в ядрах всех атомов составляет 46% от общей массы смеси, растворили в 200 г 36,5%-ной соляной кислоты. При этом выделилось 5,6 л (н.у.) газа. Вычислите массовую долю кислоты в конечном растворе.
Решение
Ответ: ꞷост.(HCl) = 7,766%
Можем сразу записать уравнения реакций:
Li3P + 3HCl = 3LiCl + PH3 (I)
Li3N + 4HCl = 3LiCl + NH4Cl (II)
Найдем количество вещества и массу фосфина:
n(PH3) = 5,6/22,4 = 0,25 моль
m(PH3) = 0,25 · 34 = 8,5 г
По условию, масса протонов в ядрах всех атомов составляет 46%. Напишем уравнение:
ꞷp+ = (mp+(Li3N + Li3P)/ m(Li3N + Li3P)
Найдем недостающие данные.
а) n(Li3P) = n(PH3) = 0,25 моль
m(Li3P) = 0,25 · 52 = 13 г;
б) Пусть n(Li3N) = x моль, тогда m(Li3N) = 35x г
в) Найдем количество и массу протонов в смеси. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
np+ = Np+ · n(в-ва)
Np+(Li3P) = 3 · 3 + 15 = 24
Np+(Li3N) = 3 · 3 + 7 = 16
np+(Li3P) = 24 · 0,25 = 6 моль, mp+(Li3P) = 6 г;
np+(Li3N) = 16x моль, mp+(Li3N) = 16x г;
Решим уравнение:
0,46 = (6 + 16x)/(35x + 13) ⇒ 16x + 6 = 16,1x + 5,98 ⇒ 0,02 = 0,1x ⇒ x = 0,2 моль — n(Li3N).
Найдем сразу массу нитрида лития: m(Li3N) = 35 · 0,2 = 7 г
Найдем массу и количество оставшейся соляной кислоты:
а) m(HCl) = 200 · 0,365 = 73 г
n(HCl) = 73/36,5 = 2 моль;
б) n1(HCl) = 3n(Li3P) = 3 · 0,25 = 0,75 моль
n2(HCl) = 4n(Li3N) = 4 · 0,2 = 0,8 моль
nобщ.(HCl) = 0,75 + 0,8 = 1,55 моль;
в) nост.(HCl) = 2 – 1,55 = 0,45 моль
mост.(HCl) = 0,45 · 36,5 = 16,425 г
Найдем массу раствора. Помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки:
mконечн. р-ра = m(Li3N) + m(Li3P) + mр-ра(HCl) – m(PH3)
mконечн. р-ра = 13 + 7 + 200 – 8,5 = 211,5 г
Найдем ꞷост.(HCl):
ꞷост.(HCl) = (16,425/211,5) · 100% = 7,766%
Ответ: ꞷост.(HCl) = 7,766%
Задание №8
В 800 г раствора нитрата серебра, в котором общее число атомов в 110 раз больше числа Авогадро, внесли 16 г порошка меди. К образовавшемуся раствору добавили 200 г 30%-ного раствора гидроксида натрия. Определите массовую долю щёлочи в конечном растворе.
Решение
Ответ: ꞷост.(NaOH) = 2,27%
Пояснение:
Напишем уравнения реакции:
2AgNO3 + Cu = Cu(NO3)2 + 2Ag (I)
Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3 (II)
Найдем количества веществ, данных в условии:
а) n(Cu) = 16/64 = 0,25 моль
б) m(NaOH) = 200 · 0,3 = 60 г
n(NaOH) = 60/40 = 1,5 моль
По условию, общее число атомов в 110 раз больше числа Авогадро, это можно записать так:
n(атомов) = N/NA , где N = 110NA , то есть: n(ат.) = 110NA/NA = 110 моль, то есть общее количество атомов равно 110 моль.
Понимаем, что в задаче говорится именно о количестве атомов – это значит, что 1 молекула H2O содержит в сумме 3 атома: 2 атома водорода и 1 атом кислорода.
n(ат.) = n(в-ва) · N
а) Обозначим n(H2O) как x моль, тогда m(H2O) = 18x г.
Если в 1 моль H2O mатомов = (2 ·1 +1) · 1 = 3г, то в x моль H2O mатомов = (2 · 1 + 1) · x = 3x г;
б) Обозначим n(AgNO3) как y моль, тогда m(AgNO3) = 170y г
Если в 1 моль AgNO3 mатомов = (1 + 1 + 3) · 1 = 5г, то в y моль AgNO3 mатомов = (1 + 1 + 3) · y = 5y г.
Составим систему уравнений:
y = 1 моль — n(AgNO3)
x = (110 – 5)/3 = 35 моль – n(H2O)
По реакции I, n(AgNO3) – в избытке, так как n1(AgNO3) = 2n(Cu) = 0,25 · 2 = 0,5 моль
nост.(AgNO3) = 1 – 0,5 = 0,5 моль
Следовательно, будет протекать следующая реакция:
2AgNO3 + 2NaOH = Ag2O + 2NaNO3 + H2O (III)
Найдем количество вещества и массу оставшегося NaOH:
а) n2(NaOH) = 2n(Cu(NO3)2) = 2n1(Cu) = 0,5 моль
n3(NaOH) = n(AgNO3) = 0,5 моль
nост.(NaOH) = 1,5 – 0,5 – 0,5 = 0,5 моль;
б) mост.(NaOH) = 0,5 · 40 = 20 г;
Составим уравнение массы конечного раствора. Помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки:
mконеч. р-ра = mр-ра(AgNO3) + m(Cu) – m(Ag) + mр-ра(NaOH) – m(Cu(OH)2) – m(Ag2O)
Найдем недостающие данные:
а) n(Ag) = 2n(Cu) = 0,5 моль
m(Ag) = 108 · 0,5 = 54 г;
б) n2(Cu(OH)2) = n(Cu(NO3)2) = 0,25 моль
m(Cu(OH)2) = 0,25 · 98 = 24,5 г;
в) n(Ag2O) = 0,5n3(AgNO3) = 0,5 · 0,5 = 0,25моль
m(Ag2O) = 0,25 · 232 = 58 г;
г) mконеч. р-ра = 800 + 16 – 54 + 200 – 24,5 – 58 = 879,5 г
Найдем ꞷост.(NaOH):
ꞷост.(NaOH) = (20/879,5) · 100% = 2,27%
Ответ: ꞷост.(NaOH) = 2,27%
Задание №9
Смесь нитрата железа(II) и нитрата железа(III), в которой масса протонов в ядрах всех атомов составляет 49,07% от общей массы смеси, прокалили до постоянной массы. Твёрдый остаток растворили в избытке соляной кислоты. При этом образовалось 299 г раствора с массовой долей соли 25%. Вычислите массу исходной смеси нитратов.
Решение
Ответ: mсмеси = 98,92 г
Пояснение:
Запишем уравнения реакций:
4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2 (I)
4Fe(NO3)3 = 2Fe2O3 + 12NO2 + 3O2 (II)
Fe2O3 + 6HCl = 2FeCl3 + 3H2O (III)
Найдем массу и количество FeCl3. Так как смесь прокалили до постоянной массы, разложение полное и твердый остаток составляет только хлорид железа (III).
m(FeCl3) = 299 · 0,25 = 74,75 г
n(FeCl3) = 74,75/162,5 = 0,46 моль
По условию масса протонов составляет 0,4907 от общей массы смеси, по сути, та же массовая доля протонов. Составим для нее уравнение:
0,4907 = (mp+(Fe(NO3)2 + Fe(NO3)3))/m(Fe(NO3)2 + Fe(NO3)3)
а) Помним, что молярная масса одного протона составляет 1г/моль. Найдем массу протонов в ядрах смеси.
а) Обозначим n(Fe(NO3)3) за x моль, тогда m(Fe(NO3)3) = 242x г. А n(Fe(NO3)2) за y моль, тогда m(Fe(NO3)2) = 180y г.
б) np+ = Np+ · n(в-ва)
Np+(Fe(NO3)3) = 26 + 21 + 72 = 119; Np+(Fe(NO3)2) = 26 + 14 + 48 = 88;
mp+(Fe(NO3)3) = 119x г; mp+(Fe(NO3)2) = 88y г;
в) Составим 1ое уравнение системы:
0,4907 = (119x + 88y)/(242x + 180y) ⇒ 0,4907(242x + 180y) = 119x + 88y
Обратим внимание, что FeCl3 образуется из Fe2O3, который образуется после разложения двух нитратов.
n(Fe2O3) = 2/4n(Fe(NO3)3) + 2/4n(Fe(NO3)2) = 0,5(n(Fe(NO3)3) + n(Fe(NO3)2)) = 0,5(x + y) – моль;
n(FeCl3) = 2n(Fe2O3) = 2 · 0,5(x + y) = x + y = 0,46 моль – 2о-е уравнение системы.
Решим систему уравнений:
y = 0,2, т.е. n(Fe(NO3)2) = 0,2 моль,
x = 0,26, т.е. n(Fe(NO3)3) = 0,26 моль
Найдем массу смеси:
m(Fe(NO3)3) + m(Fe(NO3)2) = 242 · 0,26 + 180 · 0,2 = 62,92 + 36 = 98,92 г
Ответ: mсмеси = 98,92 г
Задание №10
Смесь нитрата натрия и нитрата серебра общей массой 42,5 г, в которой масса протонов в ядрах всех атомов составляет 48% от массы смеси, прокалили до постоянной массы. Выделившуюся смесь газов пропустили через 10 мл воды. Вычислите массовую долю растворённого вещества в образовавшемся растворе.
Решение
Ответ: ꞷ(HNO3) = 40,9%
Пояснение:
2NaNO3 = 2NaNO2 + O2 (I)
2AgNO3 = 2Ag + 2NO2 + O2 (II)
4NO2 + O2 + 2H2O = 4HNO3 (III)
1) По условию, масса смеси составляет 42,5 г, составим 1ое уравнение системы:
Пусть n(NaNO3) = x моль, тогда m(NaNO3) = 85x г;
Пусть n(AgNO3) = y моль, тогда m(AgNO3) = 170y г;
Составим первое уравнение системы: 85x + 170y = 42,5 г
2) Найдем количество и массу протонов в ядрах смеси. При этом помним, что для атома химического элемента количество протонов совпадает с порядковым номером элемента, а молярная масса одного протона составляет 1г/моль.
а) np+ = Np+ · n(в-ва)
Np+(NaNO3) = 11 + 7 + 24 = 42
np+(NaNO3) = 42x моль; mp+(NaNO3) = 42x · 1 = 42x г
Np+(AgNO3) = 47 + 7 + 24 = 78
np+(AgNO3) = 78y моль; mp+(AgNO3) = 78y · 1 = 78y г
б) Составим второе уравнение системы:
0,48 = (mp+(NaNO3 + AgNO3))/m(NaNO3 + AgNO3)
0,48 = (42x + 78y)/(85x + 170y) ⇒ 3y = x
3) Составим и решим систему уравнений:
y = 0,1, т.е. n(AgNO3) = 0,1 моль,
x = 0,3, т.е. n(NaNO3) = 0,3 моль
4) Сравним количества NO2 и O2 в реакции (III):
а) nобщ.(O2) = 0,5n(NaNO3) + 0,5 n(AgNO3) = 0,15 + 0,05 = 0,2 моль
n(NO2) = n(AgNO3) = 0,1 моль;
б) n(NO2)/4 < n(O2)/1 , так как 0,025 < 0,2 – следовательно n(NO2) в недостатке, расчет будем вести по нему.
5) Найдем n(O2), которое израсходовалось в реакции.
n(O2) = 1/4n(NO2) = 1/4 ·0,1 = 0,025 моль
m(O2) = 0,025 · 32 = 0,8 г;
6) Найдем количество и массу HNO3:
n(HNO3) = n(NO2) = 0,1 моль
m(HNO3) = 0,1 · 63 = 6,3 г;
7) Найдем массу раствора:
mконеч. р-ра = m(NO2) + mистр.(O2) + m(H2O)
а) Найдем недостающие данные:
m(NO2) = 0,1 · 46 = 4,6 г
m(H2O) = V(H2O) · ρ(H2O) = 10 · 1 = 10г;
б) mконеч. р-ра = 4,6 + 0,8 + 10 = 15,4 г;

ꞷ(HNO3) = (6,3/15,4) · 100% = 40,9%
Ответ: ꞷ(HNO3) = 40,9%
Задание №11
Смесь нитрата магния и нитрата серебра, в которой масса протонов в ядрах всех атомов составляет 48,32% от общей массы смеси, прокалили до постоянной массы. Выделившуюся смесь газов пропустили через 800 мл воды. При этом объём непоглотившегося газа составил 13,44 л (н.у.). Вычислите массовую долю растворённого вещества в образовавшемся растворе.
Решение
Ответ: ꞷ(HNO3) = 48,1 %
Пояснение:
2Mg(NO3)2 = 2MgO + 4NO2 + O2
2AgNO3 = 2Ag + 2NO2 + O2
4NO2 + O2 + 2H2O = 4HNO3
1) По условию, масса протонов в ядрах всех атомов составляет 46%. Напишем уравнение:
ꞷp+ = (mp+(Mg(NO3)2 + AgNO3)/m(Mg(NO3)2 + AgNO3)
Найдем недостающие данные.
Пусть n(Mg(NO3)2) = x моль, тогда m(Mg(NO3)2) = 148x г
Пусть n(AgNO3) = y моль, тогда m(AgNO3) = 170y г;
2) Найдем количество и массу протонов в смеси. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
а) np+ = Np+ · n(в-ва)
np+(Mg(NO3)2) = (12 + 14 + 48)x = 74x моль
np+(AgNO3) = (47 + 7 + 24)y = 78y моль
б) mp+ = np+ · 1г/моль
mp+(Mg(NO3)2) = 74x г;
mp+(AgNO3) = 78y г
3) Решим уравнение:
0,4832 = (74x + 78y)/(148x + 170y) ⇒ 2,49x = 4,14y ⇒ x = 1,66y
4) Найдем и сравним количества веществ в 3 реакции, при этом примем x = 1,66y:
а) nобщ.(NO2) = 2n(Mg(NO3)2) + n(AgNO3) = 2x + y = 4,32y моль
nобщ.(O2) = 0,5n(Mg(NO3)2) + 0,5n(AgNO3) = 0,5(x+y) = 1,33y моль
б)n(NO2)/4 < n(O2)/1, так как 1,08y < 1,32y – следовательно, n(NO2) в недостатке, расчет будем вести по нему.
P.S. А вообще можно было бы избежать этих всех расчетов и просто оценить избыток/недостаток по соотношению коэффициентов в реакции. Обратим внимание, что в 3й реакции соотношение
n(NO2) : n(O2) = 4 : 1
В 1о-й реакции соотношение n(NO2) : n(O2) такое же (4 : 1) – это значит, что вещества истратились полностью.
Во 2о-й реакции соотношение n(NO2) : n(O2) = 2 : 1 (или 4 : 2) – это значит, что NO2 истратился полностью, а часть O2 нет, соответственно n(O2) – в избытке.
nост.(O2) = 13,44/22,4 = 0,6 моль
Составим уравнение для nобщ.(O2):
nобщ.(O2) = nреаг.(О2) + nост.(О2)
nреаг.(О2) = 1/4n(NO2) = (2x + y)/4 моль
0,5x + 0,5y = (2x + y)/4 + 0,6 ⇒ y = 2,4 моль – n(AgNO3).
x = 1,66 · 2,4 = 3,98 = 4 моль – n(Mg(NO3)2);
Найдем количество и массу HNO3:
n(HNO3) = n(NO2) = 2 · 4 + 2,4 = 10,4 моль
m(HNO3) = 10,4 · 63 = 655,2 г;
Найдем массу раствора:
mконеч. р-ра = m(NO2) + mистр.(O2) + m(H2O)
а) Найдем недостающие данные:
m(NO2) = 10,4 · 46 = 478,4 г
m(H2O) = V(H2O) · ρ(H2O) = 800 · 1 = 800г;
nреаг.(О2) = 1/4n(NO2) = 2,6 моль
mреаг.(О2) = 2,6 · 32 = 83,2 г
б) mконеч. р-ра = 478,4 + 83,2 + 800 = 1361,6 г;

ꞷ(HNO3) = (655,2/1361,6) · 100% = 48,1%
Ответ: ꞷ(HNO3) = 48,1 %
Задание №12
К 112 г 30%-ного раствора гидроксида калия добавили 13 г цинка. После окончания реакции к образовавшемуся раствору прилили 245 г 20%-ного раствора серной кислоты. Известно, что в условиях, при которых была проведена реакция, растворимость сульфата цинка составляет 57,7 г на 100 г воды, растворимость сульфата калия – 12,0 г на 100 г воды. Вычислите массу выпавшего осадка.
Решение
Ответ: m(K2SO4) = 18 г
Пояснение:
Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2 (I)
1) Найдем количества веществ, данных в условии.
а) m(KOH) = 112 · 0,3 = 33,6 г
n(KOH) = 33,6 / 56 = 0,6 моль
б) n(Zn) = 13 / 65 = 0,2 моль
2) Сравним количества реагентов:
n(Zn)/1 < n(KOH)/2, следовательно n(KOH) – в избытке.
nост.(KOH) = 0,6 – n1(KOH) = 0,6 – 2n(Zn) = 0,6 – 0,4 = 0,2 моль
Дальше к полученному раствору добавляют серную кислоту. Обратим внимание, что протекать у нас могут 2 реакции (так как в растворе осталась и комплексная соль, и щелочь). Однако в первую очередь будет протекать реакция нейтрализации, так как ее скорость выше.
2KOH + H2SO4 = K2SO4 + 2H2O (II)
3) Найдем n(H2SO4):
m(H2SO4) = 245 · 0,2 = 49 г
n(H2SO4) = 49 / 98 = 0,5 моль
4) Сравним количества веществ в реакции 2:
n(KOH)/2 < n(H2SO4)/1 , следовательно n(H2SO4) – в избытке. Найдем nост.(H2SO4):
nост.(H2SO4) = 0,5 – n2(H2SO4) = 0,5 – 1/2n2(KOH) = 0,5 – 0,1 = 0,4 моль
5) Сравним соотношение n(K2[Zn(OH)4]) и n(H2SO4):
n1(K2[Zn(OH)4]) = n(Zn) = 0,2 моль
n(H2SO4)/ n(K2[Zn(OH)4]) = 0,4/0,2 = 2/1– следовательно, n(K2[Zn(OH)4]) : n(H2SO4) = 1 : 2
Значит будет протекать следующая реакция:
K2[Zn(OH)4] + 2H2SO4 = K2SO4 + ZnSO4 + 4H2O (III)
6) В условии просят найти массу выпавшего осадка. Так как в «привычный» осадок в уравнениях реакций ничего не выпадает, а в условии дана растворимость двух солей, приходим к выводу, что в осадок будет выпадать одна или две соли (нужно проверить). Здесь необходимо вспомнить понятие о насыщенном растворе. После того, как содержание соли в растворе превышает значение её растворимости при данной температуре, часть соли кристаллизуется и выпадает в осадок.
7) Найдем количества и массу двух солей:
а) n(K2SO4) = n2(K2SO4) + n3(K2SO4) = 1/2n2(KOH) + n(K2[Zn(OH)4]) = 0,1 + 0,2 = 0,3 моль
m(K2SO4) = 0,3 · 174 = 52,2 г
б) n(ZnSO4) = n(K2[Zn(OH)4]) = 0,2 моль
m(ZnSO4) = 0,2 · 161 = 32,2 г

m(H2O) = mконеч. р—ра – m(K2SO4) –m(ZnSO4)
а) mконеч. р—ра = mр—ра(KOH) + m(Zn) – m(H2) + mр—ра(H2SO4)
Найдем недостающие данные:
n(H2) = n(Zn) = 0,2 моль
m(H2) = 0,2 · 2 = 0,4 г
mконеч. р-ра = 112 + 13 – 0,4 + 245 = 369,6 г
б) m(H2O) = 369,6 – 52,2 – 32,2 = 285,2 г
9) Проанализируем растворимость для двух солей. Составим пропорции:
а) для K2SO4: если в 100 г воды растворяется 12 г соли, то в 285,2 г воды растворяется x г соли:
x = (285,2 · 12)/100 = 34,2 г соли способно раствориться. По расчетам в задаче образовалось 52,2 г соли.
52,2 – 34,2 = 18 г – K2SO4 выпадет в осадок.
б) для ZnSO4: если в 100 г воды растворяется 57,7 г соли, то в 285,2 г воды растворяется y г соли:
y = (285,2 · 57,7)/100 = 164,56 г соли способно раствориться. По расчетам в задаче образовалось 32,2г соли. Масса образовавшейся соли не превышает растворимость, поэтому ZnSO4 в осадок не выпадает.
Ответ: m(K2SO4) = 18 г
Задание №13
Алюминий массой 8,1 г сплавили с 9,6 г серы. Полученную смесь растворили в 96 г насыщенного раствора гидроксида натрия. Вычислите массу выпавшего осадка. Растворимость гидроксида натрия составляет 100 г на 100 г воды, растворимость сульфида натрия в условиях реакции – 20,6 г на 100 г воды.
Решение
Ответ: m(Na2S) = 14,62 г
Пояснение:
1) Для начала сравним количества веществ в 1ой реакции и определим, какое из них находится в избытке.
а) n(Al) = 8,1 / 27 = 0,3 моль
n(S) = 9,6 / 32 = 0,3 моль
б)n(S)/3 < n(Al)/2 , так как 0, 1 < 0,15 – следовательно, n(Al) – избыток, n(S) – недостаток.
Сразу определим nост.(Al) и nобр.(Al2S3)
nост.(Al) = 0,3 – 2/3n(S) = 0,3 – 0,2 = 0,1 моль;
nобр.(Al2S3) = 1/3n(S) = 1/3 · 0,3 = 0,1 моль;
2) Полученную смесь веществ составляют 0,1 моль Al и 0,1 моль Al2S3. Запишем реакции:
Al2S3 + 8NaOH = 2Na[Al(OH)4] + 3Na2S (II)
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 (III)
3) Найдем количество NaOH. В условии дана его растворимость, а также сказано о том, что раствор насыщенный. По растворимости найдем массу NaOH.
ρ(NaOH) = 100 г на 100 г воды, можно записать это в расчете на массу раствора, то есть 100 г (NaOH) на 200 г раствора NaOH. Составим пропорцию:
Если в 200 г насыщенного раствора растворяется 100 г NaOH, то в 96 г насыщенного раствора растворяется x г NaOH.
x = (100 · 96) / 200 = 48 г – m(NaOH)
n(NaOH) = 48 / 40 = 1,2 моль
4) Найдем nост.(NaOH):
nост.(NaOH) = 1,2 – n2(NaOH) – n3(NaOH) = 1,2 – 8n(Al2S3) – n3(Al) = 1,2 – 0,8 – 0,1 = 0,3 моль
mост.(NaOH) = 40 · 0,3 = 12 г
5) В условии просят найти массу выпавшего осадка. Так как в «привычный» осадок в уравнениях реакций ничего не выпадает, а в условии дана растворимость NaOH и Na2S, приходим к выводу, что в осадок будут выпадать оба вещества или одно из них. Также необходимо вспомнить понятие о насыщенном растворе. После того, как содержание соли в растворе превышает значение её растворимости при данной температуре, часть соли кристаллизуется и выпадает в осадок.
6) Найдем m(Na2S):
n(Na2S) = 3n(Al2S3) = 0,1 · 3 = 0,3 моль
m(Na2S) = 0,3 · 78 = 23,4 г
7) Так как в условии растворимость дается на 100 г воды, необходимо найти массу воды в конечном растворе.
m(H2O) = mконеч. р-ра – m(Na2S) – m(Na[Al(OH)4]) – mост.(NaOH)
а) mконеч. р-ра = m(Al) + m(S) – m(H2) + mр-ра(NaOH)
Найдем недостающие данные:
n(H2) = 3/2n3(Al) = 3/2 · 0,1 = 0,15 моль
m(H2) = 0,15 · 2 = 0,3 г
n(Na[Al(OH)4]) = 2n(Al2S3) + n(A
mконеч. р-ра = 8,1 + 9,6 – 0,3 + 96 = 113,4 г
б) m(H2O) = 113, 4 – 23,4 – 35,4 – 12 = 42,6 г

а) для Na2S: если в 100 г воды растворяется 20,6 г соли, то в 42,6 г воды растворяется x г соли:
x = (20,6 · 42,6)/100 = 8,78 г соли способно раствориться. По расчетам в задаче образовалось 23,4 г соли.
23,4 – 8,78 = 14,62 г – K2SO4 выпадет в осадок.
б) для NaOH: если в 100 г воды растворяется 100 г гидроксида , то в 42,6 г воды растворяется y г NaOH:
y = (42,6 ·100 )/100 = 42,6 г соли способно раствориться. По расчетам в задаче образовалось 12 г NaOH. Масса образовавшегося NaOH не превышает растворимость, поэтому NaOH в осадок не выпадает.
Ответ: m(Na2S) = 14,62 г
Задание №14
Кристаллогидрат нитрата железа(II), в котором массовая доля протонов в ядрах всех атомов составляет 52,05%, прокалили до постоянной массы. Твёрдый остаток растворили в 300 г йодоводородной кислоты, взятой в избытке. Через образовавшуюся смесь пропустили сернистый газ, при этом прореагировало 2,24 л (н.у.) газа. Вычислите массовую долю соли йодоводородной кислоты в конечном растворе и массу исходного кристаллогидрата.
Решение
Ответ: m(Fe(NO3)2 ∙ 9H2O) = 68,4 г; ꞷ(FeI2) = 19,23%
Пояснение:
Записать разложение кристаллогидрата сразу мы не можем, так как нам неизвестно соотношение безводной соли и воды в кристаллогидрате, но мы можем записать его в общем виде для начала. Важно(!) в конце всех расчетов не забыть записать правильное уравнение:
4Fe(NO3)2 ∙ nH2O = 2Fe2O3 + 8NO2 + O2 + 4nH2O (I)
Дальше можем записать остальные уравнения:
Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O (II)
SO2 + I2 + 2H2O = H2SO4 + 2HI (III)
Можем сразу найти n(SO2):
n(SO2) = 2,24 / 22,4 = 0,1 моль
Далее найдем n(I2), n(Fe2O3), так как они взаимосвязаны:
n(I2) = n(SO2) = 0,1 моль
n(Fe2O3) = n(I2) = 0,1 моль
По количеству оксида железа (III) найдем количество безводной соли в кристаллогидрате и заодно ее массу:
n(Fe(NO3)2) = 4/2n(Fe2O3) = 2 · 0,1 = 0,2 моль
m(Fe(NO3)2) = 0,2 · 180 = 36 г
Известно, что массовая доля протонов в ядрах всех атомов кристаллогидрата составляет 52,05%. Составим уравнение для неё:
ꞷp+ = mp+(Fe(NO3)2) · mp+(H2O) / m(Fe(NO3)2 ∙ nH2O)
Пусть n(H2O) = x моль, тогда m(H2O) = 18x г
Найдем количество и массу протонов в ядрах кристаллогидрата. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
а) np+ = Np+ ∙ n(в-ва)
np+(Fe(NO3)2) = (26 + 14 + 48) · 0,2 = 17,6 моль
np+(H2O) = (2 + 8)x = 10x моль
б) mp+ = np+ · 1г/моль
mp+( Fe(NO3)2) = 17,6 г;
mp+(H2O) = 10x г
Решим уравнение:
0, 5205 = (17,6 + 10x) / (36 + 18x)
18,738 + 9,369x = 17,6 + 10x
1,138 = 0,631x
x = 1,8 моль – n(H2O) в кристаллогидрате, m(H2O) = 1,8 · 18 = 32,4 г
Найдем общую массу кристаллогидрата, а затем его молярную массу, так как зная молярную массу можно вывести его формулу. При этом помним, что количество кристаллогидрата равно количеству его безводной соли, так как в 1 формульной единице кристаллогидрата содержится 1 формульная единица безводной соли.
m(Fe(NO3)2∙nH2O) = m(Fe(NO3)2) + m(H2O) = 36 + 32,4 = 68,4 г
M(Fe(NO3)2∙nH2O) = m/n
M(Fe(NO3)2∙nH2O) = 68,4/0,2 = 342 (г/моль).
Учитывая, что M(Fe(NO3)2∙nH2O) = M(Fe(NO3)2) + M(H2O) – найдем молярную массу воды, а из нее и количество молекул воды в кристаллогидрате.
M(H2O) = 342 – 180 = 162 (г/моль), N(H2O) = 162/18 = 9 молекул воды содержит 1 формульная единица кристаллогидрата.
Формула кристаллогидрата: Fe(NO3)2∙9H2O. Не забываем уравнять 1-ую реакцию(!)
4Fe(NO3)2∙9H2O = 2Fe2O3 + 8NO2 + O2 + 36H2O
Найдем количество и массу соли йодоводородной кислоты – FeI2:
n(FeI2) = 2n(Fe2O3) = 2 · 0,1 = 0,2 моль
m(FeI2) = 0,2 · 310 = 62 г
Найдем массу конечного раствора. При этом помним, что для расчета массы раствора необходимо сложить массы всех добавленных субстанций и вычесть из этого массу всех газов и осадков. Обратим внимание, что выпавший йод в реакции (II), израсходовался в реакции (III). Фактически это означает, что массу йода надо сначала вычесть затем прибавить при расчете массы раствора. То есть при расчете массы раствора массу йода можно не использовать.
mконеч. р-ра = m(Fe2O3) + mр-ра(HI) + m(SO2)
Найдем недостающие данные:
m(SO2) = 0,1 · 64 = 6,4 г
m(Fe2O3) = 0,1 · 160 = 16 г
mконеч. р-ра = 16 + 300 + 6,4 = 322,4 г
Найдем массовую долю FeI2:
ꞷ(FeI2) = (62/322,4) · 100% = 19,23% .
Ответ: m(Fe(NO3)2 ∙ 9H2O) = 68,4 г; ꞷ(FeI2) = 19,23%
Задание №15
Через 440 г раствора нитрата меди(II), в котором 52,5% от общей массы раствора составляет масса протонов в ядрах всех атомов, пропускали электрический ток, используя инертные электроды. После того как на аноде выделилось 6,72 л (н.у.) газа электрический ток отключили, а электроды оставили в растворе. Определите массовую долю всех протонов в растворе после окончания всех реакций.
Решение
Ответ: ꞷp+ = 52,78%
Пояснение:
Запишем уравнение реакции электролиза:
2Cu(NO3)2 + 2H2O = 2Cu + O2 + 4HNO3 (I)
1) По условию, масса протонов в ядрах всех атомов составляет 52,5% от общей массы раствора. Найдем массу протонов:
(440/100) · 52,5 = 231 г
Пусть n(Cu(NO3)2) = x моль, m(Cu(NO3)2) = 188x г.
Пусть n(H2O) = y моль, m(H2O) = 18y г.
Составим первое уравнение системы: 188x + 18y = 440
Найдем количество протонов в ядрах всех атомов. При этом помним, что количество протонов численно равно порядковому номеру элемента в периодической системе, а молярная масса протона составляет 1г/моль.
а) np+ = Np+ ∙ n(в-ва)
np+(Cu(NO3)2) = (29 + 14 + 48) · x = 91x моль
np+(H2O) = (2 + 8)y = 10y моль
б) mp+ = np+ · 1г/моль
mp+(Cu(NO3)2) = 91x г;
mp+(H2O) = 10y г
Составим второе уравнение системы: 91x + 10y = 231
2) Решим систему уравнений:
24,2x = 24,2
x = 1 моль – n(Cu(NO3)2)
y = 14 моль – n(H2O)
3) Дальше необходимо проверить, идет ли далее электролиз воды. Для этого нам необходимо рассчитать количество выделившегося на аноде газа и сравнить его с тем количеством, которое бы выделилось, если бы электролиз соли прошел полностью.
n(газа) = 6,72/22,4 = 0,3 моль
n1(O2) = 0,5n(Cu(NO3)2) = 0,5 · 1 = 0,5 моль
0,3 < 0,5 – из чего делаем вывод, что электролиза воды не было, но электролиз соли прошел не полностью, и часть её осталась в растворе.
4) В условии сказано, что электроды после окончания электролиза оставили в растворе, поэтому кислота из анодного пространства стала растворять медь, образовавшуюся на катоде.
5) Чтобы записать следующую реакцию, необходимо знать концентрацию азотной кислоты, так как реакция может протекать с образованием NO либо NO2.
Обратим внимание, что количество веществ в 1ой реакции дальше нужно считать по количеству выделившегося кислорода, так как он в недостатке.
n(HNO3) = 4n(O2) = 0,3 · 4 = 1,2 моль
m(HNO3) = 1,2 · 63 = 75,6 г
Найдем массу раствора после1ой реакции:
mр—ра 1 = mр—ра(Cu(NO3)2) – m(Cu) – m(O2)
mр-ра 1 = 440 – (2n(O2) ·64) – (0,3 · 32) = 440 – 38,4 – 9,6 = 392 г
Найдем концентрацию HNO3:
ꞷ(HNO3) = (75,6/392) · 100% = 19,28% — следовательно, кислота разбавленная, поэтому растворение меди протекает с образованием NO.
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O (II)
6) Сравним количества меди и азотной кислоты и определим избыток/недостаток.
n(HNO3)/8 < n(Cu)/3 = 1,2/8 < 0,6/3 = 0,15 < 0,2 – следовательно, HNO3 в недостатке.
Найдем количество и массу прореагировавшей меди:
n2(Cu) = 3/8n(HNO3) = 0,45 моль
m2(Cu) = 0,45 · 64 = 28,8 г
7) В задаче просят найти массовую долю протонов в растворе после окончания всех реакций. Для начала нам необходимо определиться с тем, какие вещества остались в растворе. Это: нитрат меди (II) и вода.
а) Найдем общее количество и массу нитрата меди(II):
nобщ.(Cu(NO3)2) = n1 ост.(Cu(NO3)2) + n2 обр.(Cu(NO3)2)
nобщ.(Cu(NO3)2) = (1 – 2n1(O2)) + 3/8n(HNO3) = 1 – 0,6 + 0,45 = 0,85 моль
mобщ.(Cu(NO3)2) = 0,85 · 188 = 159,8 г
б) Найдем общее количество воды:
m(H2O) = mконечн. р-ра – m(Cu(NO3)2)
mконечн. р-ра = mр-ра 1 + mпрореаг.(Cu) – m(NO)
mконечн. р-ра = 392 + 28,8 – (2/8n(HNO3) · 30) = 392 + 28,8 – 9 = 411,8 г
m(H2O) = 411, 8 – 159,8 = 252 г
n(H2O) = 252/18 = 14 моль

а) np+ = Np+ ∙ n(в-ва)
np+(Cu(NO3)2) = (29 + 14 + 48) · 0,85 = 77,35 моль
np+(H2O) = (2 + 
б) mp+ = np+ · 1г/моль
mp+(Cu(NO3)2) = 77,35 г;
mp+(H2O) = 140 г
9) Найдем ꞷp+:
ꞷp+ = (77,35 + 140)/411,8 · 100% = 52,78% .
Ответ: ꞷp+ = 52,78%
Задание №16
Через 526,5 г раствора хлорида натрия, в котором массовая доля протонов в ядрах всех атомов составляет 54,7%, пропускали электрический ток до тех пор, пока на аноде не выделилось 22,4 л (н.у.) газа. К образовавшемуся в результате электролиза раствору добавили 13 г цинка. Определите массовую долю всех протонов в конечном растворе.
Решение
Ответ: ꞷp+ = 54,8%
Пояснение:
2NaCl + 2H2O = H2 + Cl2 + 2NaOH (I)
1) По условию, масса протонов в ядрах всех атомов составляет 54,7% от общей массы раствора. Найдем массу протонов:
(526,5/100) · 54,7 = 288 г
Пусть n(NaCl) = x моль, тогда m(NaCl) = 58,5x г
Пусть n(H2O) = y моль, тогда m(H2O) = 18y г
Составим 1-е уравнение системы: 58,5x + 18y = 526,5
2) Найдем количество протонов в ядрах всех атомов. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
а) np+ = Np+ ∙ n(в-ва)
np+(NaCl) = (11 + 17) · x = 28x моль
np+(H2O) = (2 + 8)y = 10y моль
б) mp+ = np+ · 1г/моль
mp+(NaCl) = 28x г;
mp+(H2O) = 10y г
Составим второе уравнение системы: 28x + 10y = 288
3) Решим систему уравнений:
8,1x = 8,1
x = 1, т.е. n(NaCl) = 1 моль
y = 26, т.е. n(H2O) = 26 моль
4) Дальше необходимо проверить, идет ли электролиз воды. Для этого нам необходимо рассчитать количество выделившегося на аноде газа и сравнить его с тем количеством, которое бы выделилось, если бы электролиз соли прошел полностью.
n(газа) = 22,4/22,4 = 1 моль
n1(Cl2) = 0,5n(NaCl) = 0,5 · 1 = 0,5 моль
m1(Cl2) = 0,5 · 71 = 35,5 г – выделилось при электролизе соли.
0,5 < 1 – из чего делаем вывод, что помимо электролиза соли также шел и электролиз воды.
Запишем вторую и третью реакцию.
2H2O = 2H2 + O2 (II)
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2 (III)
Найдем сразу количество цинка: n(Zn) = 13/65 = 0,2 моль
5) Из прошлого пункта мы понимаем, что n(газа) = n(Cl2) + n(O2). Можем найти количество и массу кислорода во второй реакции:
n(O2) = 1 – 0,5 = 0,5 моль;
m(O2) = 0,5 · 32 = 16 г
6) В задаче просят найти массовую долю протонов в растворе после окончания всех реакций. Для начала нам необходимо определиться с тем, какие вещества остались в растворе. Это: NaOH, H2O, Na2[Zn(OH)4].
а) Найдем общее количество и массу NaOH:
nост.(NaOH) = nобр.(NaOH) – nистр.(NaOH)
nост.(NaOH) = 2n1(Cl) – 2n(Zn) = 1 – 0,4 = 0,6 моль
mост.(NaOH) = 0,6 · 40 = 24 г
б) Найдем общее количество и массу Na2[Zn(OH)4]:
n(Na2[Zn(OH)4]) = n(Zn) = 0,2 моль
m(Na2[Zn(OH)4]) = 0,2 · 179 = 35,8 г
в) Сразу найти количество и массу H2O нельзя, так как:
m(H2O) = mконечн. р-ра – m(NaOH) – m(Na2[Zn(OH)4])
Поэтому сначала найдем массу конечного раствора. При этом помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки.
mконечн. р-ра = mр-ра(NaCl) – m1(H2) – m1(Cl2) – m2(H2) – m2(O2) + m(Zn) – m3(H2)
Найдем недостающие данные:
n1(H2) = n1(Cl2) = 0,5 моль; m1(H2) = 0,5 · 2 = 1 г
n2(H2) = 2n2(O2) = 1 моль; m1(H2) = 1 · 2 = 2 г
n3(H2) = n(Zn) = 0,2 моль; m1(H2) = 0,2 · 2 = 0,4 г
Найдем массу конечного раствора:
mконечн. р-ра = 526,5 – 1 – 35,5 – 2 – 16 + 13 – 0,4 = 484,6 г
Теперь мы можем найти количество и массу воды:
m(H2O) = 484,6 – 24 – 35,8 = 424,8 г; n(H2O) = 424,8/18 = 23,6 моль
7) Найдем количество и массу протонов в конечном растворе. При этом помним, что количество протонов = порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль.
а) np+ = Np+ ∙ n(в-ва)
np+(NaOH) = (11 + 8 + 1) · 0,6 = 12 моль
np+(H2O) = (2 + 
np+(Na2[Zn(OH)4]) = (11 · 2 + 30 + 8 ·4 + 4 · 1) · 0,2 = 17,6 моль
б) mp+ = np+ · 1г/моль
mp+(NaOH) = 12 г;
mp+(H2O) = 236 г
mp+( Na2[Zn(OH)4]) = 17,6 г

ꞷp+ = (12 + 236 + 17,6)/484,6 · 100% = 54,8%
Ответ: ꞷp+ = 54,8%
Задание №17
Через 500 г раствора хлорида бария, в котором 53% от общей массы раствора составляет масса протонов в ядрах всех атомов, пропускали электрический ток до тех пор, пока на аноде не выделилось 8,96 л (н.у.) газа. К образовавшемуся в результате электролиза раствору добавили 63,6 г карбоната натрия. Определите массовую долю карбоната натрия в конечном растворе.
Решение
Ответ: ꞷост.(Na2CO3) = 2,43 %
Пояснение:
BaCl2 + 2H2O = H2 + Cl2 + Ba(OH)2 (I)
По условию, масса протонов в ядрах всех атомов составляет 54,7% от общей массы раствора. Найдем массу протонов:
(500/100) · 53 = 265 г
Пусть n(BaCl2) = x моль, тогда m(BaCl2) = 208x г
Пусть n(H2O) = y моль, тогда m(H2O) = 18y г
Составим первое уравнение системы: 208x + 18y = 500
Найдем количество протонов в ядрах всех атомов. При этом помним, что количество протонов равно порядковому номеру элемента, а молярная масса одного протона составляет 1г/моль. Если забыли об этом вспоминаем состав атома водорода — 1 протон и 1 электрон, масса электрона пренебрежимо мала, поэтому можно считать, что масса протона равна массе одного атома водорода.
а) np+ = Np+ ∙ n(в-ва)
np+(BaCl2) = (56 + 17 · 2) · x = 90x моль
np+(H2O) = (2 + 8)y = 10y моль
б) mp+ = np+ · 1г/моль
mp+(BaCl2) = 90x г;
mp+(H2O) = 10y г
Составим 2-е уравнение системы: 90x + 10y = 265 г
Решим систему уравнений:
46x = 23
x = 0,5, т.е. n(BaCl2) = 0,5 моль,
y = 22, т.е. n(H2O) = 22 моль.
Дальше необходимо проверить, идет ли электролиз воды. Для этого нам необходимо рассчитать количество выделившегося на аноде газа и сравнить его с тем количеством, которое бы выделилось, если бы электролиз соли прошел полностью.
n(газа) = 8,96/22,4 = 0,4 моль,
n1(Cl2) = n(BaCl2) = 0,5 моль
0,4 < 0,5 – из чего делаем вывод, что электролиза воды не было и электролиз соли прошел не полностью, и часть её осталась в растворе.
Обратим внимание, что количество веществ в 1ой реакции дальше нужно считать по количеству выделившегося хлора, так как он в недостатке.
Найдем nост.(BaCl2) = 0,5 – n1(BaCl2) = 0,5 – n(Cl2) = 0,5 – 0,4 = 0,1 моль
Запишем следующие реакции:
Ba(OH)2 + Na2CO3 = BaCO3 + 2NaOH (II)
BaCl2 + Na2CO3 = BaCO3 + 2NaCl (III)
Найдем количество добавленного карбоната натрия:
n(Na2CO3) = 63,6 / 106 = 0,6 моль
Далее найдем количество и массу оставшегося карбоната натрия, так как в задаче просят найти его массовую долю:
nост.(Na2CO3) = 0,6 – n2(Na2CO3) – n3(Na2CO3)
n2(Na2CO3) = n(Ba(OH)2) = n(Cl2) = 0,4 моль;
n3(Na2CO3) = nост.(BaCl2) = 0,1 моль;
nост.(Na2CO3) = 0,6 – 0,4 – 0,1 = 0,1 моль
mост.(Na2CO3) = 0,1 · 106 = 10,6 г
Найдем массу конечного раствора. При этом помним, что масса раствора – это всё, что смешали, минус образовавшиеся газы и осадки.
mконечн. р-ра = mр-ра(BaCl2) – m(H2) – m(Cl2) + m(Na2CO3) – mобщ.(BaCO3)
Найдем недостающие данные:
n(H2) = n(Cl2) = 0,4 моль; m(H2) = 0,4 · 2 = 0,8 г
m(Cl2) = 0,4 · 71 = 28,4 г
nобщ.(BaCO3) = n(Ba(OH)2) + nост.(BaCl2) = 0,4 + 0,1 = 0,5 моль;
mобщ.(BaCO3) = 0,5 · 197 = 98,5 г
Теперь мы можем найти массу раствора:
mконечн. р-ра = 500 – 0,8 – 28,4 + 63,6 – 98,5 = 435,9 г
Найдем ꞷост.(Na2CO3):
ꞷост.(Na2CO3) = (10,6/435,9) · 100% = 2,43 %
Ответ: ꞷост.(Na2CO3) = 2,43 %.
За это задание ты можешь получить 4 балла. На решение дается около 15 минут. Уровень сложности: высокий.
Средний процент выполнения: 23.8%
Ответом к заданию 34 по химии может быть развернутый ответ (полная запись решения с обоснованием выполненных действий).
Разбор сложных заданий в тг-канале
Задачи для практики
Задача 1
Коэффициент растворимости хлорида меди(II) при 100 °С — 110 г / 100 г $Н_2О$, при 20 °С — 72,7 г. 420 г насыщенного при 100 °С раствора соли охладили до 20 °С и выделившийся осадок кристаллогидрата $CuCl_2 ∙ 2H_2O$ отделили. К оставшемуся раствору добавили 200 г 10%-ного раствора гидроксида натрия. Определите массовую долю веществ в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$CuCl_2 + 2H_2O = CuCl_2 ∙ 2H_2O$ (1)
$CuCl_2 + 2NaOH = Cu(OH)_2↓ + 2KCl$ (2)
2) Находим количество вещества и массу хлорида меди(II) и воды в исходном растворе (при 100 °С).
Пусть $m(CuCl_2)$ = x моль, тогда справедливо соотношение
${m(CuCl_2)}/{m_{p-pa}(CuCl_2)} = {110}/{110 + 100} = {x}/{420}$
x = 220 г $CuCl_2$; $m(H_2O)$ = 420 – 220 = 200 г
$M(CuCl_2)$ = 135 г/моль; $n(CuCl_2)_{100}$ = 220 / 135 ≈ 1.63 моль
3) Находим количество вещества хлорида меди(II) после кристаллизации кристаллогидрата (при 20 °С).
Пусть выделилось x моль $CuCl_2$. тогда справедливо соотношение
$m(CuCl_2)_{выделился}$ = 135x г; $m(H_2O)$ = 2 ∙ 18x = 36x г
${m(CuCl_2)_{20}}/{m_{p-pa}(CuCl_2)} = {72.7}/{72.7 + 100} = {220 – 135х}/{420 – 135х – 36х}$
x ≈ 0.69 моль $CuCl_2$
$m(CuCl_2)_{выделился}$ = 0.69 ∙ 135 = 93.15 г
$m(H_2O)$ = 0.69 ∙ 36 = 24.84 г
$n(CuCl_2)_{20 (осталось)}$ = 1.63 – 0.69 = 0.94 моль
4) По уравнению (2):
а) $m(NaOH)_{чист.}$ = 0.1 ∙ 200 = 20 г
M(NaOH) = 40 г/моль; n(NaOH) = 20 / 40 = 0.5 моль
б) имеется $CuCl_2$ — 0.94 моль
прореагирует $CuCl_2$ — 0.25 моль
останется $CuCl_2$ — (0.94 – 0.25) = 0.69 моль
$m(CuCl_2)_{остался}$ = 0.69 ∙ 135 = 93.15 г
в) $n(Cu(OH)_2)$ = 0.5n(NaOH) = 0.5 ∙ 0.5 = 0.25 моль
$M(Cu(OH)_2)$ = 98 г/моль; $m(Cu(OH)_2)$ = 0.25 ∙ 98 = 24.5 г
г) n(NaCl) = n(NaOH) = 0.5 моль
M(NaCl) = 58.5 г/моль; m(NaCl) = 0.5 ∙ 58.5 = 29.25 г
5) $m_{р-ра}$ = 420 – 93.15 – 24.84 + 200 – 24.5 = 477.51 г
$ω(CuCl_2)$ = 93.15 / 477.51 ≈ 0.1951. или 19.51 %
ω(NaCl) = 29.25 / 477.51 ≈ 0.0613. или 6.13 %
$ω(H_2O)$ = 100 – 19.51 – 6.13 = 74.36 %
Ответ:
Задача 2
Растворимость безводного сульфида натрия при определённой температуре 18,8 г на 100 г воды. При этой температуре приготовили 29,6 г насыщенного раствора сульфида натрия. Раствор разделили на две части. К первой части прилили избыток раствора сульфата алюминия. Ко второй части раствора добавили 36,5 г соляной кислоты (избыток), причём объём выделившегося газа в первой порции в два раз меньше, чем во второй. Вычислите массовую долю хлорида натрия во второй колбе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$3Na_2S_{(1)} +Al_2(SO_4)_3 + 6H_2O = 3Na_2SO_4 + 3H_2S_{(1)}↑ + 2Al(OH)_3↓$ (1)
$Na_2S_{(2)} + 2HCl = 2NaCl + H_2S_{(2)}$↑
2) Находим количество $Na_2S$ в исходном растворе.
Составляем пропорцию:
18.8 / (18.8 + 100) = x / 29.6
x = 18.8 ∙ 29.6 / 118.8 ≈ 4.68 г
M($Na_2S$) = 78 г/моль, $n(Na_2S)_{(1 + 2)}$ = 4.68 / 78 = 0.06 моль
3) Находим количество $Na_2S$, прореагировавшего по уравнению (2).
Пусть по уравнению (1) прореагировало x моль $Na_2S$, по уравнению (2) – y моль $Na_2S$, тогда:
а) x + y = 0.06
б) $n(H_2S)_{(1)} = n(Na_2S)_{(1)}$ = x моль
$n(H_2S)_{(2)} = n(Na_2S)_{(2)}$ = y моль
y = 2x
${tablex + y = 0.6; y = 2x;$ ${tablex = 0.02 моль H_2S_{(1)}; y = 0.04 моль H_2S_{(2)};$
4) По уравнению (2):
а) $n(NaCl)_{(2)} = 2n(H_2S)_{(2)}$ = 2 ∙ 0.04 / 1 = 0.08 моль
M(NaCl) = 58.5 г/моль, $m(NaCl)_{(2)}$ = 0.08 ∙ 58.5 = 4.68 г
б) $n(Na_2S)_{(2)} = n(H_2S)_{(2)}$ = 0.04 моль
в) $M(H_2S)$ = 34 г/моль, $m(H_2S)$ = 0.04 ∙ 34 = 1.36 г
г) находим массу второй части раствора $Na_2S$.
Так как концентрация вещества в растворе и в любой его части одинакова, то
0.06 / 29.6 = 0.04 / x
x = 0.04 ∙ 29.6 / 0.06 ≈ 19.73 г
5) $ω_2(NaCl)$ = 4.68 / (19.73 + 36.5 – 1.36) = 4.68 / 54.87 ≈ 0.0853, или 8.53 %
Ответ:
Задача 3
При электролизе 9,4 %-ного раствора нитрата меди(II) на катоде выделилось в 1,5 раза больше газа по объёму, чем на аноде. Рассчитайте массовые доли веществ в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$2Cu(NO_3)_2 + 2H_2O = 2Cu↓ + O_2↑ + 4HNO_3$ (1)
$2H_2O = 2H_2 + O_2$ (2)
Уравнение (1) описывает электролиз раствора $Cu(NO_3)_2$. После полного осаждения меди будет происходить электролиз воды (раствора $HNO_3$) (уравнение 2).
2) Пусть в реакции (1) выделился 1 моль $O_2$. тогда рассчитываем по уравнению (1):
а) $М(O_2)$ = 32 г/моль; $m(O_2)_{(1)}$ = 1 · 32 = 32 г
б) $n(Cu(NO_3)_2$ = 2n$(O_2)$ = 2 моль
$M(Cu(NO_3)_2)$ = 188 г/моль; $m(Cu(NO_3)_2)$ = 2 · 188 = 376 г
$m_{р-ра}(Cu(NO_3)_2)$ = 376 / 0,094 = 4000 г
в) n(Cu) = 2n($O_2$) = 2 моль
M(Cu) = 64 г/моль; m(Cu) = 2 · 64 = 128 г
г) $n(HNO_3) = 4n(O_2)$ = 4 моль
$M(HNO_3)$ = 63 г/моль; $m(HNO_3)$ = 4 · 63 = 252 г
3) Пусть по реакции (2) выделилось x моль $O_2$. тогда:
а) $n(H_2) = 2n(O_2)$ = 2x моль
$V(H_2)$ = 2x · 22.4 л
б) общий объём выделившегося кислорода:
$V(O_2)$ = (1 + x) · 22.4 л
в) так как объём водорода в 1.5 раза больше суммарного объёма выделившегося кислорода, то:
2x / (1 + x) = 1.5
x = 3
$n(H_2)_{(2)}$ = 6 моль; $n(O_2)_{(2)}$ = 3 моль
г) рассчитываем массу выделившихся газов:
$M(H_2)$ = 2 г/моль; $m(H_2)$ = 6 · 2 = 12 г
$m(O_2)_{(2)}$ = 3 · 32 = 96 г
4) $ω(HNO_3) = m(HNO_3)$ / $m_{р-ра}(HNO_3)$
$m_{р-ра}(HNO_3)$ = 4000 – (128 + 32 + 12 + 96) = 3732 г
$ω(HNO_3)$ = 252 / 3732 ≈ 0.0675, или 6.75 %
$ω(H_2O)$ = 100 – 6.75 = 93.25 %
Ответ:
Задача 4
При обжиге образца сульфида меди(II) часть вещества прореагировала и образовался остаток массой 16,8 г. После добавления этого остатка в 182,5 г 10%-ного раствора соляной кислоты в растворе осталось 40 % хлороводорода. Рассчитайте первоначальную массу сульфида и массовую долю соли в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$2CuS + 3O_2 = 2CuO + 2SO_2↑$ (1)
$CuO + 2HCl = CuCl_2 + H_2O$ (2)
$CuS + HCl ≠$ (3)
2) Находим количество вещества HCl, вступившего в реакцию с CuO:
$m_1(HCl)_{чист.}$ = 0.10 ∙ 182.5 = 18.25 г
M(HCl) = 36.5 г/моль, $n(HCl)_{начальн.}$ = 18.25 / 36.5 = 0.5 моль
$n(HCl)_{прорегировало}$ = 0.5 ∙ 0.6 = 0.3 моль
3) По уравнению (2):
n(CuO) = 0.5n(HCl) = 0.5 ∙ 0.3 = 0.15 моль
M(CuO) = 80 г/моль, m(CuO) = 0.15 ∙ 80 = 12 г
4) Находим количество CuS, вступившего в реакцию окисления.
По уравнению (1):
$n(CuS)_{(1)}$ = n(CuO) = 0.15 моль
M(CuS) = 96 г/моль, $m(CuS)_{прореаг.}$ = 0.15 ∙ 96 = 14.4 г
5) Находим массу исходной смеси:
$m(CuS)_{осталось}$ = 16.8 – 12 = 4.8 г
$m(CuS)_{исходное}$ = 4.8 + 14.4 = 19.2 г
6) По уравнению (2):
$n(CuCl_2)$ = 0.5n(HCl) = 0.5 ∙ 0.3 = 0.15 моль
$M(CuCl_2)$ = 135 г/моль, $m(CuCl_2)$ = 0.15 ∙ 135 = 20.25 г
7) $ω(CuCl_2)$ = 20.25 / (182.5 + 12) = 0.1041, или 10.41 %
Ответ:
Задача 5
Определите массовую долю карбоната калия в растворе, полученном кипячением 150 г 15 %-ного раствора гидрокарбоната калия. Какой объём 15,6 %-ного раствора хлорида бария (плотностью 1,11 г/мл) прореагирует с полученным карбонатом калия? Испарением воды можно пренебречь. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Не знаешь, с чего начать решение? Посмотри подсказку тут:
Решение
1) Уравнения реакций:
$2KHCO_3 = K_2CO_3 + H_2O + CO_2↑$ (1)
$K_2CO_3 + BaCl_2 = BaCO_3↓ + 2KCl$ (2)
2) Количество вещества гидрокарбоната калия $KHCO_3$:
$m(KHCO_3)_{чист.}$ = 0.15 · 150 = 22.5 г
$M(KHCO_3)$ = 100 г/моль; $n(KHCO_3)$ = 22.5 / 100 = 0.225 моль
3) По уравнению (1):
$n(K_2CO_3) = 0.5n(KHCO_3)$ = 0.225 / 2 = 0.1125 моль
$M(K_2CO_3)$ = 138 г/моль; $m(K_2CO_3)$ = 0.1125 · 138 = 15.525 г
4) По уравнению (1):
$n(CO_2) = 0.5n(KHCO_3)$ = 0.1125 моль
$M(CO_2)$ = 44 г/моль; $m(CO_2)$ = 0.1125 · 44 = 4.95 г
5) Массовая доля $K_2CO_3$:
$m_{р-ра}(K_2CO_3) = m_{р-ра}(KHCO_3) – m(CO_2)$ = 150 – 4.95 = 145.05 г
$ω(K_2CO_3)$ = 15.525 / 145.05 ≈ 0.107, или 10.7 %
6) По уравнению (2):
$n(BaCl_2) = n(K_2CO_3)$ = 0.1125 моль
$M(BaCl_2)$ = 208 г/моль; $m(BaCl_2)_{чист.}$ = 0.1125 · 208 = 23.4 г
$m_{р-ра}(BaCl_2)$ = 23.4 / 0.156 ≈ 150 г
$V_{р-ра}(BaCl_2)$ = 150 / 1.11 ≈ 135.14 мл
Ответ:
Задача 6
Железный купорос ($FeSO_4 · 7H_2O$) массой 55,6 г растворили в воде и получили раствор с массовой долей соли 10 %. К этому раствору добавили 39 г цинка. После завершения реакции добавили 250 г 29,2 %-ного раствора соляной кислоты. Определите массовые доли веществ в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$FeSO_4 · 7H_2O = FeSO_4 + 7H_2O$ (1)
$FeSO_4 + Zn = Fe↓ + ZnSO_4$ (2)
$Fe + 2HCl = FeCl_2 + H_2↑$ (3)
$Zn + 2HCl = ZnCl_2 + H_2↑$ (4)
2) Находим количество вещества $FeSO_4$ и массу раствора:
а) $M(FeSO_4 · 7H_2O)$ = 278 г/моль, $n(FeSO_4 · 7H_2O)$ = 55.6 / 278 = 0.2 моль
б) По уравнению (1):
$n(FeSO_4) = n(FeSO_4 · 7H_2O)$ = 0.2 моль
$M(FeSO_4)$ = 152 г/моль, $m(FeSO_4)$ = 0.2 · 152 = 30.4 г
$m_{р-ра}(FeSO_4) = m_{в-ва} / ω$; $m_{р-ра}$ = 30.4 / 0.1 = 304 г
3) По уравнению (2):
а) M(Zn) = 65 г/моль; n(Zn) = 39 / 65 = 0.6 моль
б) имеется — 0.6 моль Zn
прореагирует — 0.2 моль Zn
останется — (0.6 – 0.2) = 0.4 моль Zn (избыток)
в) n(Fe) = $n(FeSO_4)$ = 0.2 моль
г) $n(ZnSO_4)$ = n(Fe) = 0.2 моль
$M(ZnSO_4)$ = 161 г/моль, $m(ZnSO_4)$ = 0.2 · 161 = 32.2 г
4) По уравнению (3):
а) $m(HCl)_{чист.}$ = 0.292 · 250 = 73 г
M(HCl) = 36.5 г/моль; n(HCl) = 73 / 36.5 = 2 моль (избыток)
б) $n(FeCl_2)$ = n(Fe) = 0.2 моль
$M(FeCl_2)$ = 127 г/моль, $m(FeCl_2)$ = 0.2 · 127 = 25.4 г
в) $n(H_2)_{(3)}$ = n(Fe) = 0.2 моль
$M(H_2)$ = 2 г/моль; $m(H_2)_{(3)}$ = 0.2 · 2 = 0.4 г
г) $n(HCl)_{(3)}$ = 2n(Fe) = 0.4 моль
5) По уравнению (4):
а) $n(ZnCl_2)$ = n(Zn) = 0.4 моль
$M(ZnCl_2)$ = 136 г/моль, $m(ZnCl_2)$ = 0.4 · 136 = 54.4 г
б) $n(H_2)_{(4)}$ = n(Zn) = 0.4 моль
$m(H_2)_{(4)}$ = 0.4 · 2 = 0.8 г
в) $n(HCl)_{(4)}$ = 2n(Zn) = 0.8 моль
6) Рассчитываем массовые доли веществ в растворе:
а) $m_{р-ра} = m_{р-ра}(FeSO_4) + m(Zn) + m_{р-ра}(HCl) — m(H2)_{(3) + (4)}$ = 304 + 39 + 250 – 0.4 – 0.8 = 591.8 г
б) $ω(ZnSO_4) = m(ZnSO_4)$ / $m_{р-ра}$ = 32.2 / 591.8 ≈ 0.0544. или 5.44 %
в) $ω(FeCl_2) = m(FeCl_2)$ / $m_{р-ра}$ = 25.4 / 591.8 ≈ 0.0429. или 4.29 %
г) $ω(ZnCl_2) = m(ZnCl_2)$ / $m_{р-ра}$ = 54.4 / 591.8 ≈ 0.0919. или 9.19 %
д) $n(HCl)_{изб.}$ = 2 – 0.4 – 0.8 = 0.8 моль
$m(HCl)_{изб.}$ = 0.8 · 36.5 = 29.2 г
ω(HCl) = m(HCl) / $m_{р-ра}$ = 29.2 / 591.8 ≈ 0.0493. или 4.93 %
е) $ω(H_2O)$ = 100 – 5.44 – 4.29 – 9.19 – 4.93 = 76.15 %
Ответ:
Задача 7
Через 120 г 10%-ного раствора едкого натра пропустили электрический ток, в результате выделилось 134,4 л (н. у.) газов. Часть полученного раствора, 12,8 г, использовали для полного осаждения меди из 32 г раствора сульфата меди(II). Вычислите массовую долю сульфата меди(II) в растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$2H_2O = 2H_2 + O_2$ (1)
$CuSO_4 + 2NaOH = Cu(OH)↓ + Na_2SO_4$ (2)
2) Количество вещества реагентов:
$m(NaOH)_{чист.}$ = 0.1 ‧ 120 = 12 г
M(NaOH) = 40 г/моль; n(NaOH) = 12 / 40 = 0.3 моль
3) По уравнению (1).
Пусть выделилось x моль $O_2$. тогда:
а) $V(O_2)$ = 22.4x л
б) $n(H_2)$ = 2x моль, $V(H_2)$ = 2x ‧ 22.4 л
в) 2x ‧ 22.4 + 22.4x = 134.4
x = 2
г) $M(H_2)$ = 2 г/моль, $n(H_2)$ = 2 ∙ 2 = 4 моль, $m(H_2)$ = 4 ‧ 2 = 8 г
$M(O_2)$ = 32 г/моль, $n(O_2)$ = 2 моль, $m(O_2)$ = 2 ‧ 32 = 64 г
4) Находим количество NaOH в отобранной порции раствора:
а) масса раствора после электролиза
$m_{р-ра}(NaOH)_{после электролиза}$ = 120 – 8 – 64 = 48 г
б) так как концентрация вещества в растворе и в любой его части одинакова, то
0.3 / 48 = x / 12.8
x = 0.3 ∙ 12.8 / 48 = 0.08 моль NaOH
5) Находим массовую долю $CuSO_4$ в растворе:
а) по уравнению (2):
$n(CuSO_4)$ = 0.5n(NaOH) = 1 ∙ 0.08 / 2 = 0.04 моль
$M(CuSO_4)$ = 160 г/моль, $m(CuSO_4)$ = 0.04 ∙ 160 = 6.4 г
б) $ω(CuSO_4)$ = 6.4 / 32 = 0.2. или 20 %
Ответ:
Задача 8
Цинковую пластинку массой 50 г поместили в 120 г раствора, содержащего 6% сульфата магния и нитрат серебра. После завершения реакции пластинку вынули, промыли водой, высушили и взвесили. К оставшемуся раствору добавили 135, 14 мл 11,2%-ного раствора гидроксида калия (плотность 1,11 г/мл). Осадок отделили и взвесили; масса осадка 10,41 г. Вычислите массу пластинки после реакции. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций.
$Zn + MgSO_4 ≠$ (1)
$Zn + 2AgNO_3 = Zn(NO_3)_2 + 2Ag↓$ (2)
$MgSO_4 + 2KOH = Mg(OH)_2↓ + K_2SO_4$ (3)
$Zn(NO_3)_2 + 2KOH = Zn(OH)_2↓ + 2KNO_3$ (4)
$Zn(NO_3)_2 + 4KOH_{(изб.)} = K_2[Zn(OH)_4] + 2KNO_3$ (5)
2) Находим количество реагирующих веществ:
а) $m(MgSO_4)_{чист.}$ = 0.06 ∙ 120 = 7.2 г
$M(MgSO_4)$ = 120 г/моль, $n(MgSO_4)$ = 7.2 / 120 = 0.06 моль
б) $m_{р-ра}(KOH)$ = 1.11 ∙ 135.14 ≈ 150.0054 г
$m(KOH)_{чист.}$ = 0.112 ∙ 150 = 16.8 г
M(KOH) = 56 г/моль, n(KOH) = 16.8 / 56 = 0.3 моль
3) По уравнению (3):
а) $n(Mg(OH)_2) = n(MgSO_4)$ = 0.06 моль
$M(Mg(OH)_2)$ = 58 г/моль, $m(Mg(OH)_2)$ = 0.06 ∙ 58 = 3.48 г
б) $n(КOH)_{(2)} = 2n(MgSO_4)$ = 2 ∙ 0.06 = 0.12 моль
4) По уравнению (4):
а) $m(Zn(OH)_2)$ = 10.41 – 3.48 = 6.93 г
$M(Zn(OH)_2)$ = 99 г/моль, $n(Zn(OH)_2)_{(4)}$ = 6.93 / 99 = 0.07 моль
б) $n(КOH)_{(4)} = 2n(Zn(OH)_2)_4$ = 2 ∙ 0.07 = 0.14 моль
в) $n(Zn)_{(4)} = n(Zn(NO_3)_2)_{(4)} = n(Zn(OH)_2)_{(4)}$ = 0.07 моль
5) По уравнению (5):
а) $n(KOH)_{(5)}$ = 0.3 – (0.12 + 0.14) = 0.04 моль
б) $n(Zn) = n(Zn(NO_3)_2)_{(5)} = 0.25n(KOH)_{(5)}$ = 0.25 ∙ 0.04 = 0.01 моль
6) Находим массу пластинки после реакции:
а) $n(Zn)_{(4) + (5)}$ = 0.07 + 0.01 = 0.08 моль
M(Zn) = 65 г/моль, $m(Zn)_{(4) + (5)}$ = 0.08 ∙ 65 = 5.2 г
б) по уравнению (2):
$n(Ag) = 2n(Zn)_{(4) + (5)}$ = 2 ∙ 0.08 = 0.16 моль
M(Ag) = 108 г/моль, $m(Ag)_{(2)}$ = 0.16 ∙ 108 = 17.28 г
m(пластинки после реакции) = 50 – 5.2 + 17.28 = 62.08 г
Ответ:
Задача 9
Газ, полученный при сжигании 6,4 г серы, без остатка прореагировал с 138 мл 8%-ного раствора NaOH (плотностью 1,087 г/мл). Рассчитайте массовые доли веществ в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Не знаешь, с чего начать решение? Посмотри подсказку тут:
Решение
1) Уравнения реакций:
$S + O_2 = SO_2$ (1)
$2NaOH_{(изб.)} + SO_2 = Na_2SO_3 + H_2O$ (2)
и если $SO_2$ в избытке, то
$SO_2 + H_2O + Na_2SO_3 = 2NaHSO_3$ (3)
2) Количество вещества S и NaOH:
а) M(S) = 32 г/моль; n(S) = 6.4 / 32 = 0.2 моль
б) $m_{р-ра}$(NaOH) = 138 · 1.087 = 150 г
$m_{в-ва}$(NaOH) = 0.08 · 150 = 12 г
M(NaOH) = 40 г/моль; n(NaOH) = 12 / 40 = 0.3 моль
3) По уравнению (1):
n($SO_2$) = n(S) = 0.2 моль
M($SO_2$) = 64 г/моль; m($SO_2$) = 0.2 · 64 = 12.8 г
4) По уравнению (2):
а) имеется $SO_2$ — 0.2 моль
прореагирует $SO_2$ — 0.15 моль
избыток $SO_2$ — (0.2 – 0.15) = 0.05 моль
б) $n(Na_2SO_3)$ = 0.5n(NaOH) = 0.5 · 0.3 = 0.15 моль
5) По уравнению (3):
а) имеется $Na_2SO_3$ — 0.15 моль
прореагирует $Na_2SO_3$ — 0.05 моль
избыток $Na_2SO_3$ = (0.15 – 0.05) = 0.1 моль
M($Na_2SO_3$) = 126 г/моль; $m(Na_2SO_3)_{изб.}$ = 0.1 · 126 = 12.6 г
б) n($NaHSO_3$) = 2n($SO_2$) = 2 · 0.05 = 0.1 моль
M($NaHSO_3$) = 104 г/моль; m($NaHSO_3$) = 0.1 · 104 = 10.4 г
6) Массовые доли веществ в растворе:
а) $m_{р-ра} = m_{р-ра}(NaOH) + m(SO_2)$ = 150 + 12.8 = 162.8 г
б) ω($Na_2SO_3$) = 12.6 / 162.8 ≈ 0.0774. или 7.74 %
в) ω($NaHSO_3$) = 10.4 / 162.8 ≈ 0.0639, или 6.39 %
г) ω($H_2O$) = 100 – (7.74 + 6.39) = 85.87 %
Ответ:
Задача 10
При растворении 69,5 г железного купороса ($FeSO_4 ‧ 7H_2O$) в воде был получен раствор с массовой долей соли 9,5 %. В этот раствор добавили смесь калия и оксида калия, содержащую 92,34 % оксида. Смесь растворилась, при этом выделилось 560 мл (н. у.) газа. Найдите массовые доли веществ в конечном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$FeSO_4 ‧ 7H_2O = FeSO_4 + 7H_2O$ (1)
$2K + 2H_2O = 2KOH + H_2↑$ (2)
$K_2O + H_2O = 2KOH$ (3)
$FeSO_4 + 2KOH = Fe(OH)_2↓ + K_2SO_4$ (4)
2) Количество реагирующих веществ:
а) $M(FeSO_4 ‧ 7H_2O)$ = 278 г/моль; $n(FeSO_4 ‧ 7H_2O)$ = 69.5 / 278 = 0.25 моль
б) n($H_2$) = 0.56 / 22.4 = 0.025 моль; m($H_2$) = 0.025 ‧ 2 = 0.05 г
3) По уравнению (1):
$n(FeSO_4) = n(FeSO_4 ‧ 7H_2O)$ = 0.25 моль
$M(FeSO_4)$ = 152 г/моль; $m(FeSO_4)$ = 0.25 ‧ 152 = 38 г
$m_{р-ра}(FeSO_4)$ = 38 / 0.095 = 400 г
4) По уравнению (2):
а) n(K) = 2n($H_2$) = 2 ‧ 0.025 = 0.05 моль
M(K) = 39 г/моль; n(K) = 0.05 моль; m(K) = 1.95 г
ω = $m_{в-ва}$ / $m_{смеси}$; $m_{смеси} = m_{в-ва}$ / ω
$m_{смеси}(K + K_2O)$ = 1.95 / (1 – 0.9234) = 1.95 / 0.0766 ≈ 25.46 г
б) $m(K_2O)$ = 25.46 – 1.95 = 23.51 г
$M(K_2O)$ = 94 г/моль; $n(K_2O)$ = 23.51 / 94 ≈ 0.25 моль
в) n(KOH)(2) = n(K) = 0.05 моль
5) По уравнению (3):
а) $n(KOH)_{(3)} = 2n(K_2O)$ = 2 ‧ 0.25 = 0.5 моль
б) $n(KOH)_{общее}$ = 0.05 + 0.5 = 0.55 моль
6) По уравнению (4):
а) имеется KOH — 0.55 моль
прореагирует KOH — 0.5 моль
останется KOH — (0.55 – 0.5) = 0.05 моль
M(KOH) = 56 г/моль; $m(KOH)_{останется}$ = 0.05 ‧ 56 = 2.8 г
б) $n(Fe(OH)_2) = n(FeSO_4)$ = 0.25 моль
$M(Fe(OH)_2)$ = 90 г/моль; $m(Fe(OH)_2)$ = 0.25 ‧ 90 = 22.5 г
в) $n(K_2SO_4) = n(FeSO_4)$ = 0.25 моль
$M(K_2SO_4)$ = 174 г/моль; $m(K_2SO_4)$ = 0.25 ‧ 174 = 43.5 г
7) а) $m_{р-ра}$ = 400 + 25.46 – 0.05 – 22.5 = 402.91 г
б) ω(KOH) = 2.8 / 402.91 ≈ 0.0069, или 0.69 %
в) $ω(K_2SO_4)$ = 43.5 / 402.91 ≈ 0.1080. или 10.8 %
г) $ω(H_2O)$ = 100 – (0.69 + 10.8) = 88.51 %
Ответ:
Задача 11
Насыщенный раствор хлорида алюминия (растворимость 46 г в 100 г воды при 20 °С) массой 50,85 г разлили в две колбы: в первую добавили избыток раствора $Na_2CO_3$, во вторую 20,4 г 25%-ного раствора аммиака. Во второй колбе осадок в 2 раза тяжелее, чем в первой. Найдите концентрацию аммиака во второй колбе после окончания реакции. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций.
$2AlCl_{3(1-я часть)} + 3Na_2CO_3 + 3H_2O = 2Al(OH)_3↓ + 3CO_2↑ + 6NaCl$ (1)
$AlCl_{3(2-я часть)} + 3NH_3 + 3H_2O = Al(OH)_3↓ + 3NH_4Cl$ (1)
2) Находим количество $AlCl_3$ в исходном растворе.
Составляем пропорцию:
46 / (46 + 100) = x / 50.85
x = 46 ∙ 50.85 / 146 ≈ 16.02 г
M($AlCl_3$) = 133.5 г/моль, $n(AlCl_3)_{(1 + 2)}$ = 16.02 / 133.5 = 0.12 моль
3) Находим количество $AlCl_3$, прореагировавшего по уравнению (2).
Пусть по уравнению (1) прореагировало x моль $AlCl_3$,
по уравнению (2) — y моль $AlCl_3$, тогда:
а) x + y = 0.12
б) $n(Al(OH)_3)_{(1)} = n(AlCl_3)_{(1)}$ = x моль
$n(Al(OH)_3)_{(2)} = n(AlCl_3)_{(2)}$ = y моль
y = 2x
в) ${table x + y = 0.12; y = 2x;$ ${table x = 0.04 моль AlCl_3(1); y = 0.08 моль AlCl_3 (2);$
4) По уравнению (2):
а) $m(NH_3)_{чист.}$ = 0.25 ∙ 20.4 = 5.1 г
$M(NH_3)$ = 17 г/моль, $n(NH_3)$ = 5.1 / 17 = 0.3 моль
б) имеется 0.3 моль $NH_3$
прореагирует (0.08 ∙ 3/1) = 0.24 моль $NH_3$
останется (0.3 – 0.24) = 0.06 моль $NH_3$ (избыток)
$m(NH_3)_{изб.}$ = 0.06 ∙ 17 = 1.02 г
в) $n(Al(OH)_3)_{(2)} = n(AlCl_3)_{(2)}$ = 0.08 моль
$M(Al(OH)_3)$ = 78 г/моль, $m(Al(OH)_3)_{(2)}$ = 0.08 ∙ 78 = 6.24 г
г) находим массу 2-й части раствора $AlCl_3$.
Концентрация вещества в растворе и в любой его части одинакова, следовательно
0.12 / 50.85 = 0.08 / x
x = 0.08 ∙ 50.85 / 0.12 = 33.9 г
5) $ω_2(NH_3)$ = 1.02 / (33.9 + 20.4 – 6.24) = 1.02 / 48.06 ≈ 0.0212, или 2.12 %
Ответ:
Задача 12
В 250 мл воды растворили 13,8 г натрия, затем добавили 10%-ный раствор сульфата меди(II), полученный растворением в воде 62,5 г медного купороса. Определите массовую долю соли в полученном растворе и укажите характер среды. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
1) Уравнения реакций:
$2Na + 2H_2O = 2NaOH + H_2↑$ (1)
$CuSO_4 ∙ 5H_2O = CuSO_4 + 5H_2O$ (2)
$2NaOH + CuSO_4 = Na_2SO_4 + Cu(OH)_2↓$ (3)
2) Рассчитываем количество реагирующих веществ:
а) M(Na) = 23 г/моль, n(Na) = 13.8 / 23 = 0.6 моль
б) $M(H_2O)$ = 18 г/моль, $n(H_2O)$ = 1 · 250 / 18 ≈ 13.9 моль
3) По уравнению (1):
n(Na) = $n(H_2O)$, следовательно,
$H_2O$ — в избытке в количестве (13.9 – 0.6) = 13.3 моль
n(NaOH) = n(Na) = 0.6 моль
n($H_2$) = 0.5n(Na) = 0.5 · 0.6 = 0.3 моль
M($H_2$) = 2 г/моль, m($H_2$) = 0.3 · 2 = 0.6 г
4) По уравнению (2):
а) $M(CuSO_4 ∙ 5H_2O)$ = 250 г/моль, $n(CuSO_4 ∙ 5H_2O)$ = 62.5 / 250 = 0.25 моль
б) $n(CuSO_4) = n(CuSO_4 ∙ 5H_2O)$ = 0.25 моль
$M(CuSO_4)$ = 160 г/моль, $m(CuSO_4)$ = 0.25 ∙ 160 = 40 г
в) $m_{р-ра}(CuSO_4)$ = 40 / 0.1 = 400 г
5) По уравнению (3):
а) имеется NaOH — 0.6 моль
прореагирует NaOH — 0.5 моль
избыток NaOH = (0.6 – 0.5) = 0.1 моль, щелочная среда
б) $n(Na_2SO_4) = n(CuSO_4)$ = 0.25 моль
$M(Na_2SO_4)$ = 142 г/моль, $m(Na_2SO_4)$ = 0.25 · 142 = 35.5 г
в) $n(Cu(OH)_2) = n(CuSO_4)$ = 0.25 моль
$M(Cu(OH)_2)$ = 98 г/моль, $m(Cu(OH)_2)$ = 0.25 · 98 = 24.5 г
6) Рассчитываем массовую долю соли в растворе:
$ω(Na_2SO_4) = m(Na_2SO_4) / m_{(р-ра)}$
$m_{(р-ра)} = m(H_2O) + m(Na) – m(H_2) + m_{р-ра}(CuSO_4) – m(Cu(OH)_2)$ = 250 · 1 + 13.8 – 0.6 + 400 – 24.5 = 638.7 г
$ω(Na_2SO_4)$ = 35.5 / 638.7 ≈ 0.0556, или 5.56 %
Ответ:
Задача 13
При прокаливании нитрата алюминия часть вещества разложилась и выделилось 6,72 л газа (н. у.). Твёрдый остаток массой 25,38 г растворили в минимально возможном количестве 20%-ного раствора гидроксида калия. Рассчитайте массовую долю нитрата калия в полученном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Не знаешь, с чего начать решение? Посмотри подсказку тут:
Решение
Вариант ответа:
Составлены уравнения реакций:
$4Al(NO_3)_3 = 2Al_2O_3 + 12NO_2↑ + 3O_2↑$ (1)
$Al_2O_3 + 2KOH + 3H_2O = 2K[Al(OH)_4]$ (2)
$Al(NO_3)_3 + 4KOH = K[Al(OH)_4] + 3KNO_3$ (3)
Рассчитан количественный состав твёрдого остатка, образовавшегося при прокаливании $Al(NO_3)_3$:
а) по уравнению (1):
V($O_2$) = 3 · 6.72 / 15 = 1.344 л
n($O_2$) = 1.344 / 22.4 = 0.06 моль
V($NO_2$) = 12 · 6.72 / 15 = 5.376 л
n($NO_2$) = 5.376 / 22.4 = 0.24 моль
б) по уравнению (1):
n($Al_2O_3$) = 2 / 3n($O_2$) = 2 · 0.06 / 3 = 0.04 моль
M($Al_2O_3$) = 102 г/моль; m($Al_2O_3$) = 0.04 · 102 = 4.08 г
в) m($Al(NO_3)_3$)осталось = 25.38 – 4.08 = 21.3 г
M($Al(NO_3))3$) = 213 г/моль
n($Al(NO_3)_3$) = 21.3 / 213 = 0.1 моль
Рассчитана масса раствора KOH, израсходованного на растворение остатка:
а) по уравнению (2):
n(KOH) = 2n($Al_2O_3$) = 2 · 0.04 = 0.08 моль
б) по уравнению (3):
n(KOH) = 4n($Al(NO_3)_3$)осталось = 4 · 0.1 = 0.4 моль
в) n(KOH)по ур-ям 2 и 3 = 0.08 + 0.4 = 0.48 моль
M(KOH) = 56 г/моль; m(KOH) = 0.48 · 56 = 26.88 г
$m_{р-ра}$(KOH) = 26.88 / 0.2 = 134.4 г
Рассчитана массовая доля $KNO_3$:
а) по уравнению (3):
n($KNO_3$) = 3n($Al(NO_3)_3$)осталось = 3 · 0.1 = 0.3 моль
M($KNO_3$) = 101 г/моль; m($KNO_3$) = 0.3 · 101 = 30.3 г
б) $m_{р-ра}(KNO_3) = m_{(твёрдого остатка)} + m_{р-ра}(KOH)$ = 25.38 + 134.4 = 159.78 г
в) $ω(KNO_3)$ = 30.3 / 159.78 ≈ 0.1896, или 18.96 %
Ответ:
Задача 14
Растворимость безводного карбоната калия при некоторой температуре составляет 117,7 г в 100 г воды. Приготовленный насыщенный раствор карбоната калия массой 306,3 г разделили на две части. К первой части прилили избыток раствора хлорида бария. При этом образовалось 157,6 г осадка. Вторую часть раствора использовали для нейтрализации 9,8%-ного раствора серной кислоты. Определите массовую долю соли в образовавшемся растворе.
В ответе приведите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
Решение
Вариант ответа:
Составлены уравнения реакций:
$K_2CO_{3(1-я часть)} + BaCl_2 = 2KCl + BaCO_3↓$ (1)
$K_2CO_{3(2-я часть)} + H_2SO_4 = K_2SO_4 + CO_2↑ + H_2O$ (2)
Рассчитано количество $K_2CO_3$ в исходном растворе.
Составляем пропорцию:
117.7/(117.7 + 100) = x/306.3
x = 117.7 ∙ 306.3/217.7 ≈ 165.6 г
M($K_2CO_3$) = 138 г/моль, n($K_2CO_3$)(1 + 2) = 165.6/138 = 1.2 моль
Рассчитано количество $K_2CO_3$, вступившего в реакцию с $BaCl_2$:
а) M($BaCO_3$) = 197 г/моль, n($BaCO_3$) = 157.6/197 = 0.8 моль
б) n($K_2CO_3)_{(1-я часть)}$ = n($BaCO_3$) = 0.8 моль
Рассчитана масса образовавшегося $K_2SO_4$:
а) n($K_2CO_3)_{(2-я часть)}$ = n($K_2CO_3)_{(1 + 2)} – n(K_2CO_3)_{(1-я часть)}$ = 1.2 – 0.8 = 0.4 моль
б) n($K_2SO4$) = n($K_2CO_3)_{(2-я часть)}$ = 0.4 моль
M($K_2SO_4$) = 174 г/моль, m($K_2SO_4$) = 0.4 ∙ 174 = 69.6 г
Рассчитана массовая доля $K_2SO_4$:
а) n($H_2SO_4$) = n($K_2CO_3)_{(2-я часть)}$ = 0.4 моль
M($H_2SO_4$) = 98 г/моль, m($H_2SO_4$) = 0.4 ∙ 98 = 39.2 г
$m_{р-ра}(H_2SO_4$) = 39.2/0.098 = 400 г
б) n($CO_2$) = n($K_2CO_3)_{(2-я часть)}$ = 0.4 моль
M($CO_2$) = 44 г/моль, m($CO_2$) = 0.4 ∙ 44 = 17.6 г
в) находим массу 2-й части раствора $K_2CO_3$.
Концентрация вещества в растворе и в любой его части одинакова, следовательно
1.2/306.3= 0.4/x
x = 0.4 ∙ 306.3/1.2 = 102.1 г
г) $ω_2(K_2SO4)$ = 69.6/(102.1 + 400 – 17.6) = 69.6/484.5 ≈ 0.1436, или 14.36 %
Ответ:
Рекомендуемые курсы подготовки
22 июня 2022
В закладки
Обсудить
Жалоба
Подборка задач 33 и 34 с прошедшего ЕГЭ 2022 по химии.
→ 33 с ответами и уравнениями описанных реакций: 33.pdf
→ 34 c ответами: 34.pdf
Источник: vk.com/examtop