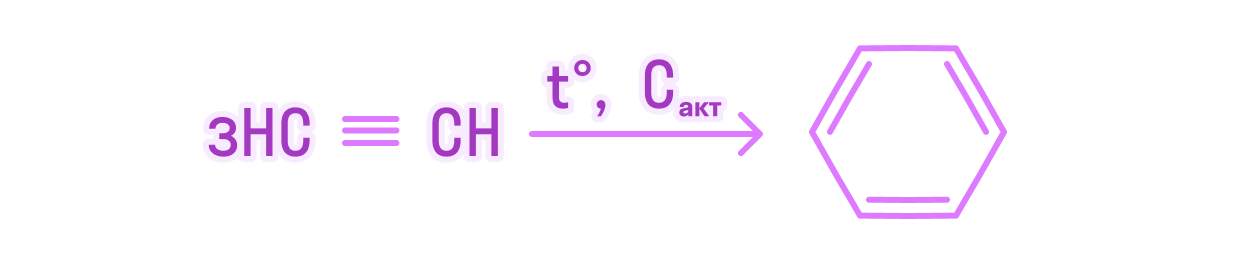Подготовка к ЕГЭ по химии
Как проходит ЕГЭ по химии в 2023 году
На ЕГЭ по химии, как и в случае с большинством других предметов, ученик 11 класса должен будет справиться с 2 частями экзамена:
-
1-я часть: 28 заданий с кратким ответом;
-
2-я часть: 6 заданий с развернутым ответом.
Чтобы решить все 34 задания единого государственного экзамена, у ученика будет 210 минут. За это время нужно будет успеть ответить на вопросы обеих частей, подготовить полное решение для задач 2-й части и перенести ответы в бланк.
Кстати, в отличие от ОГЭ, на ЕГЭ по химии не будет задания-эксперимента. Только обычные химические задания разной сложности. В таблице ниже можно посмотреть, сколько будет легких, средних и сложных вопросов.
| Уровень сложности заданий на ЕГЭ по химии | |
|---|---|
| Базовая | 17 |
| Повышенная | 11 |
| Высокая | 6 |
Если вы хотите больше узнать об особенностях экзамена и подготовки к нему, советуем заглянуть в раздел «Демоверсии, спецификации, кодификаторы» сайта ФИПИ. Там вы найдете всю актуальную информацию о ЕГЭ по химии и методические рекомендации. Все это поможет распланировать подготовку к экзамену так, чтобы сдать его на 100 баллов.
Изменения в ЕГЭ по химии
По сравнению с 2022 годом экзамен по химии немного изменится. Вот список нововведений:
-
Немного поменялось условие задания 23, в котором нужно рассчитать концентрацию веществ. Теперь данные в нем будут записаны текстом, а не в таблице.
-
Задания 33 и 34 поменялись местами.
-
Задания 9, 12 и 16 теперь станут повышенной сложности.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Полезные подарки для родителей
В колесе фортуны — гарантированные призы, которые помогут наладить учебный процесс и выстроить отношения с ребёнком!
Как хорошо сдать ЕГЭ по химии: разбор сложных задач
Как мы узнали из таблицы в предыдущем разделе, экзамен по химии — один из самых сложных. На 34 задания в нем приходится целых 11 повышенной сложности и 6 — высокой. Но если вы хотите поступить в вуз мечты, советуем научиться их решать так, чтобы не упустить ни одного балла. А потому предлагаем начать подготовку прямо сейчас и вместе разобрать несколько таких задач.
Задание 7
Это задание проверяет буквально все ваши знания в области неорганической химии. Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Установите соответствие между веществом и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Вещество | Реагенты |
|---|---|
| А) S | 1) AgNO3, K3PO4, Cl2 |
| Б) SO3 | 2) BaO, NaOH, H2O |
| В) Zn(OH)2 | 3) H2, Cl2, O2 |
| Г) ZnBr2 | 4) HBr, LiOH, CH3COOH (p-p) |
| 5) H3PO4 (p-p), BaCl2, CuO |
Решение:
-
Вариант под буквой А — простое вещество, сера. Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
-
Вещество под буквой Б — кислотный оксид. Кислотные оксиды не реагируют с кислотами, поэтому смело вычеркиваем варианты, где присутствует хоть одна кислота. Остаются варианты № 1–3. Реагенты под цифрой 3 тоже можем вычеркнуть, так как кислотный оксид уже в своей максимальной степени окисления и дальше взаимодействовать с кислородом не может. Остаются варианты № 1 и № 2. Оксид серы (VI) может реагировать с основным оксидом с образованием соли, со щелочью с образованием соли и воды, и с водой, при этом образуя кислоту. Выбираем № 2.
-
Амфотерный нерастворимый в воде гидроксид цинка может взаимодействовать только с теми, что способны его растворить. Единственно верный вариант под № 4, где указаны кислоты и щелочь.
-
При взаимодействии соли с другими сложными веществами надо помнить про три признака протекания химической реакции: выпадения осадка, выделение газа и образование малодиссоциирующего вещества — воды. Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Ответ: 3241.
Задание 15
Это задание Единого государственного экзамена проверит ваши знания химических свойств органических соединений. Чтобы справиться с ним, нужно по записанным словами реагирующим веществам составить уравнение реакции и выбрать из перечня один из получившихся продуктов. Давайте рассмотрим на примере, как решать такую задачу.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Реагирующие вещества | Продукт взаимодействия |
|---|---|
| А) уксусная кислота и сульфид калия | пропионат калия |
| Б) муравьиная кислота и гидроксид калия | этилат калия |
| В) муравьиный альдегид и гидроксид меди (II) при нагревании | формиат меди (II) |
| Г) этанол и калий | формиат калия |
| ацетат калия | |
| углекислый газ |
Решение:
-
Органические кислоты могут реагировать с солями, если те имеют летучий анион. В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
-
Муравьиная кислота проявляет свойства неорганической кислоты и может взаимодействовать с щелочами с образованием соли и воды. Соль муравьиной кислоты — формиат. Правильный ответ № 4.
-
Под буквой В описана качественная реакция на альдегиды с образованием соответствующей кислоты, оксида меди (I) и воды. Исключение — муравьиный альдегид. Он окисляется до углекислого газа, а остальные продукты реакции те же. Соответственно, правильный ответ № 6.
-
Калий как активный металл может замещать протон водорода в гидроксогруппе у спиртов с образованием алкоголята. Правильный ответ: № 2.
Ответ: 5462.
Задание 16
Это задание всё так же проверяет ваши знания по химическим свойствам и, как следствие, умение записывать превращения в рамках органической химии. Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами х и у:
-
2-бромбутан;
-
этаналь;
-
этен;
-
метилпропан;
-
хлорэтан.
Решение:
Посмотрим, что случилось с известными нам веществами.
-
У спирта исчезла ОН-группа, затем что-то произошло, и углеродная цепочка увеличилась вдвое. Мы помним, что когда цепочка увеличивается вдвое, то, скорее всего, это реакция Вюрца. А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
-
Бутан подвергают нагреванию с использованием катализатора. Нужно помнить, что в таких условиях проводится изомеризация алканов. Из бутана получается метилпропан. Ответ: № 4.
Ответ: 54.
Задание 26
Теперь разберем задачи, которые заканчивают тестовую часть ЕГЭ по химии. Рассмотрим условие одной из них на нахождение массы соли, которую необходимо добавить для получения раствора с новой заданной массовой долей.
Вычислите массу нитрата калия (в граммах), которую следует растворить в 160 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. Ответ округлите до десятых.
Чтобы решить эту задачу, вспомним основную формулу нахождения массовой доли:
-
Найдем массу изначально растворенного нитрата калия в растворе, выразив из формулы выше:
подставим значения:
-
Чтобы увеличить массовую долю соли в растворе, необходимо ее добавить еще. Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
-
Далее в дело вступает чистая математика. Разделим обе части уравнения на 100%:
-
По пропорции перемножим крест-накрест:
0,12 * (160 + X) = 16 + X.
-
Раскроем скобки:
19,2 + 0,12Х = 16 + Х.
-
Приведем подобные: с Х в одну сторону, без Х — в другую:
3,2 = 0,88Х.
-
Найдем Х:
Масса нитрата калия, которую необходимо добавить для увеличения массовой доли раствора до 12%, равна 3,6 граммам.
Ответ: 3,6.
Задание 28
Эта задача может встретиться на экзамене в нескольких вариантах. Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
В результате реакции тримеризации ацетилена объемом 26,88 л (н.у) получили 24,96 г бензола. Вычислите массовую долю выхода продукта реакции от теоретически возможного.
Решение:
-
Для начала напишем формулу, по которой считается доля выхода продукта:
Как определить, какая масса практическая, а какая — теоретическая? Значения, которые даются после слова «получили», — это практическая масса. Та, которая получилась в результате проведения химической реакции в реальных условиях. Масса теоретическая — та, которую рассчитывают из уравнения реакции, зная массу исходных реагентов.
-
Напишем уравнение химической реакции тримеризации ацетилена:
-
Найдем количество вещества ацетилена:
подставим значения:
-
Перейдем на количество вещества бензола, получаемого из ацетилена:
-
Зная количество вещества бензола, найдем его массу:
подставим значения:
m = 0,4 * 78 = 31,2 грамма.
-
Масса, рассчитываемая по уравнению реакции, является теоретической. Масса практическая дана нам по условию. Подставим полученные данные по массам в формулу для нахождения доли выхода продукта реакции:
Доля выхода бензола из данного объема ацетилена составляет 80%.
Ответ: 80.
Как оценивают готовые работы на ЕГЭ по химии
1-я часть
В 1-й части Единого государственного экзамена по химии задания 1–5, 9–13, 16–21, 25–28 оценивают 1 баллом, если вы запишете верный ответ по эталону. При этом в заданиях 1, 3, 4, 11, 12, 13, 17 и 18 ответ — это ряд цифр. То, в каком порядке вы их запишете, не влияет на оценку. Например, если в задании верны варианты под номерами 1 и 4, их можно записать как 14 или как 41. И в обоих случаях ответ засчитают как верный.
За правильные ответы в заданиях 6, 7, 8, 14, 15, 22, 23 и 24 можно получить по 2 балла. Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
2-я часть
В этой части нужно записать не только ответ, но и решение. А значит, и оценивать такие задания будут сразу по нескольким критериям. Зато за верный ответ в некоторых вопросах можно получить больше баллов, чем за любое задание 1-й части. Максимум — 5 баллов. А теперь давайте разберемся, как именно их будут оценивать.
| Задание № 29 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества и записал уравнение химической реакции, составил электронный баланс, указал окислитель и восстановитель | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 30 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества, записал все нужные уравнения реакции | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 31 | Баллы |
|---|---|
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 4 |
| Задание № 32 | Баллы |
|---|---|
| Правильно записаны 5 уравнений реакции | 5 |
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 5 |
| Задание № 33 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 3 элемента | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 3 |
| Задание № 34 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 4 элемента | 4 |
| Правильно записаны только 3 элемента ответа | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 4 |
Как сдать ЕГЭ по химии на 3, 4 и 5
Мы уже познакомились с критериями, по которым будут оценивать работы на ЕГЭ. А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
Будьте внимательны: баллы из таблиц выше — первичные, а требования к абитуриентам на поступление выражены в тестовых. Чтобы понять, сколько заданий точно нужно решить, чтобы поступить, надо перевести баллы из одной системы в другую. Это можно сделать по таблице ниже.
| Первичные баллы | Тестовые баллы | Оценка |
|---|---|---|
| <11 | <36 | 2 |
| 11–25 | 36–55 | 3 |
| 26–38 | 56–72 | 4 |
| 39–56 | 73–100 | 5 |
6 рекомендаций, как подготовиться к ЕГЭ по химии
Единый государственный экзамен — это ответственная задача, от результатов подготовки к которой иногда многое зависит. Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
-
Узнайте все о структуре ЕГЭ и научитесь работать с КИМами.
-
Начинайте готовиться заранее. Но если получилось так, что осталось мало времени, составьте новый экспресс-план с помощью вашего преподавателя.
-
Ведите календарь подготовки к экзамену. Отмечайте на нем запланированные темы, разные методики, занятия у репетитора, пробные ЕГЭ и самоподготовку.
-
Распределяйте время на темы, исходя из ваших знаний. Больше учите то, что «западает», остальное — повторяйте.
-
Советуйтесь с учителем. Это может быть ваш преподаватель по химии или репетитор. Круто, если он сможет поделиться с вами опытом подготовки к ЕГЭ.
-
Заботьтесь о своем здоровье, не забывайте отдыхать, не лишайте себя живого общения. Все это может сказаться на вашем самочувствии, а значит, и баллах тоже.
Если вы хотите сдать ЕГЭ по химии на 100 баллов, советуем тщательно продумать, как вы будете готовиться к нему. Лучший из них — совмещать самостоятельную работу и дополнительные занятия.
На курсах подготовки к ЕГЭ по химии в Skysmart школьники отрабатывают все типы задач и разбирают критерии оценок. Для каждого из них мы составляем индивидуальный план, который приведет к нужным баллам. Он учитывает уровень знаний ученика и время до экзамена, что позволяет «выжать» максимум из подготовки. А еще мы рассказываем о ЕГЭ без «страшилок» и прикрас, чтобы школьник точно знал, что его ждет на экзамене. Ждем на первом бесплатном занятии!
Елена Батаева,
преподаватель химии в школе «Интеллектуал»,
доцент химфака МГУ
В чем, по-вашему, самая большая сложность ЕГЭ по химии? Есть ли в этом году какие-то существенные изменения в структуре экзамена?
В этом году структура экзамена изменилась, в варианте 2017 года не осталось вопросов, которые предполагают выбор только одного ответа. Теперь все задания будут с выбором минимум двух ответов. Принципиально они не сложнее, но так как надо выбирать два раза, вероятность ошибки возрастает. Таким образом, получается, что экзамен стал чуть труднее.
Заданий теперь меньше — осталось 34 задания: пять — в части 2, которая раньше называлась «часть С»: решения этих заданий пишутся от руки, и их проверяет эксперт. И 29 заданий в части 1, той, которую проверяет компьютер. Стоит отметить, что именно в этой части дети делают больше всего ошибок. Почему это происходит, сложно сказать: мы не имеем возможности анализировать часть, которую проверяет машина, и апелляций по части 1 нет.
Скорее всего, существенная доля этих ошибок не зависит от конкретного предмета и связана с невнимательностью или волнением на экзамене. Экзамен по химии очень сложным назвать нельзя, те, кто нормально занимался на профильном уровне, должен, по идее, справиться. Но я смотрела статистику, несколько лет назад были такие цифры — 10-12% сдают предмет неудовлетворительно, то есть не набирают минимум, (а это всего 14 баллов из 60 первичных). Вторичный средний балл тоже очень невысокий — около 50 баллов из 100. Я не очень понимаю, как так получается, и меня это вопрос гложет. Что-то здесь не так.
Какие темы, по вашим наблюдениям, хуже всего даются школьникам? Какие вопросы традиционно считаются самыми сложными?
По моим ощущениям, хуже всего у школьников получается решать задания на проверку эмпирических знаний — свойств конкретных элементов и их соединений, то есть «Химия элементов». Есть задания, для решения которых надо предъявить довольно простое знание, — например, задания № 6 (выбрать вещество, которое реагирует с предложенным в задании), № 8 и № 9 (выбрать формулы веществ, участвующих в цепочке превращений из двух шагов). Есть задание № 11, в котором нужно соотнести вещество и несколько веществ, с которыми оно будет реагировать, — традиционно это задание оказывается одним из самых сложных.
Тяжело даются некоторые задания по органической химии, особенно задания № 18 и № 19, где требуется соотнести реагенты и продукты реакции. Дело в том, что в большинстве случаев продукт однозначен, но иногда бывает, что процесс описан неоднозначно. Ученик выбирает не тот вариант ответа, на который рассчитывал составитель. При этом, вполне возможно, что ход рассуждений был верным, и, если бы это задание проверял эксперт, то он понял бы, что мысль идет в правильном направлении, но при механической проверке просто фиксируется ошибка.
Сейчас таких «кривых» заданий становится меньше, ЕГЭ в этом смысле совершенствуется — по крайней мере, судя по тренировочным ЕГЭ, которые мы имеем возможность видеть.
Есть задания № 27, № 28 и № 29, которые, по сути, очень простые, но в них легко ошибиться. Это расчетные задачи, решение которых состоит из нескольких простых шагов. На любом этапе можно сделать ошибку и «протащить» ее дальше. Да еще и в ответе, где указано «запишите число с точностью до …», можно неудачно округлить.
Но самое неприятное для школьника задание, на мой взгляд, — это задание № 26, в которое входят вопросы по производству и области применения. Эти вопросы в школьной программе обсуждаются в разных темах, и не всегда в конце курса удается обобщить и повторить их. Ответ на вопрос этого задания требует не только воспроизвести информацию из различных разделов химии, но и применить общую эрудицию, которой у школьника может не быть. Это вопрос сразу про все: про жизнь, про производство, про применение. Редкий ребенок сможет ответить, для производства какого полимера используется терефталевая кислота, даже если в 10 классе он это знал.
Какие вопросы дают больше всего баллов? На что стоит обратить внимание?
Вся часть 2, которая пишется от руки и проверяется экспертом, в сумме дает 20 баллов. Каждое задание здесь «весит» больше одного балла: за задание № 30 можно получить до 3 баллов, за задание № 31 — максимум 4 балла, за задание № 32 — 5 баллов, а задания № 33 и № 34 дают до 4 баллов.
В задании № 31 в текстовой форме описано проведение эксперимента, и надо описать его в форме уравнений реакций. Это достаточно сложное задание, потому что если школьник не делал или не видел эксперимента, справиться тяжело.
Задание № 32 — органическая цепочка, одно из самых сложных, поскольку школьники тут могут что-то упустить: написать схему вместо уравнения, не написать все продукты и так далее.
Все задания части 2 достаточно сложные, но нужно попытаться их сделать. Даже если не все понятно — решить хотя бы часть задач, «отгрызть» хотя бы часть баллов, потому что там оценка суммируется: написал уравнение — получил 1 балл, посчитал — еще 1 балл, и так далее.
Как лучше готовиться к экзамену по химии?
В апреле к ЕГЭ начинать готовиться, конечно, поздновато. Правильной стратегией было бы все время учить химию, не задумываясь об экзамене, — химия, которую дают в школе на профильном уровне, несколько выше, чем требует ЕГЭ. Если школьник нормально учил этот предмет на профильном уровне, ему достаточно в апреле-мае взять с сайта ФИПИ вопросы, купить книжку с вариантами и по ним потренироваться с этой формой. Если что-то не получается, есть возможность подойти к преподавателю и поинтересоваться, мол, а что я делаю не так.
Любой школьный учебник по химии для профильного уровня подойдет для подготовки. Их несколько, и все профильные учебники приличные. «Профильный» или «углубленный» здесь ключевые слова, поскольку учебники для базового уровня не подходят для подготовки к ЕГЭ, они просто предназначены для другой аудитории.
Не все, конечно, зависит от самого ученика. Дело в том, что химия — это наука о веществе, и, по-хорошему, ее надо начинать со знакомства с веществом, с чувства вещества, чтобы она не стала набором странных и непонятных формул. В некоторых учебниках химия начинается с абстракции, со строения атома. Тогда она и становится набором формул, и это очень тяжело — у ребенка даже в 8 классе, как правило, не сформировано абстрактное мышление, психологически ребенок не готов к оперированию большим числом абстрактных понятий.
Химия — это вообще «про реальное», это экспериментальная наука, без опытов здесь никак, заучивать бесполезно. Официальная программа по химии начинается в 8 классе, но во многих школах за год до этого вводится пропедевтический курс: в течение года дети проводят реакции и опыты, а потом уже узнают про формулы.
Что может сделать школьник, если ему не повезло, и подобного курса не было? Сейчас в интернете выкладывается очень много видеозаписей опытов. Можно хотя бы смотреть, раз не можешь сделать сам. Когда есть привязка к чему-то реальному, все становится гораздо проще. Записи экспериментов имеются на портале «Российское образование», но на этом сайте очень сложно что-либо найти. Есть ресурс «Дети и наука», где в разделе «Химия» опубликованы по некоторым темам конспекты, описан конкретный, реальный эксперимент, и к нему снято видео. В крайнем случае можно все найти на YouTube.
Химия – предмет, не относящийся к обязательным для сдачи ЕГЭ, и выбирают его выпускники, которые хорошо в нем разбираются. Но и у них даже, казалось бы, самые легкие задания могут вызвать затруднения. На каких моментах часто спотыкаются участники экзамена и как можно избежать ошибок, рассказывает Наталия Покровская, эксперт Московского центра качества образования, ответственный секретарь предметной комиссии ЕГЭ по химии.
Вариант контрольно-измерительных материалов единого государственного экзамена по химии состоит из 35 заданий: 29 в первой части – с выбором ответа или кратким ответом, и 6 во второй – высокого уровня сложности с развернутым ответом.
Задания 1–3
– Первые три задания не относятся к разряду трудных, но и в них выпускники могут допустить ошибки: иногда ребят сбивает с толку простое изменение формулировки вопроса, – рассказывает Наталия Покровская. – Например, если в задании 3 написано «Выберите элементы, проявляющие высшую степень окисления +5», всем ясно, о чем идет речь. А нестандартная формулировка вроде «Выберите элементы, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления» вызывает непонимание, хотя суть задания не изменилась! Таким образом, старшеклассники должны быть готовы к тому, что вопрос может звучать по-разному.
Задание 7
Это задание также нельзя назвать трудным. Главное при его выполнении быть внимательными. Например, в условии может быть сказано: «Добавили раствор вещества Х». Значит, выбирая из предложенного списка вещество Х, сразу нужно исключить все нерастворимые вещества. Поскольку задание чаще всего направлено на проверку знаний о реакциях, протекающих в растворах, следует вспомнить, в каких случаях выделяются газы: разложение получившихся непрочных кислот (сернистой, угольной) или гидрата аммиака, появление в продуктах сероводорода, совместный полный гидролиз, вытеснение водорода из кислоты металлом. Всю информацию, касающуюся осадков, можно найти в таблице растворимости. Написание схемы реакции поможет визуализировать условие задания и не допустить ошибок.
Задания 8, 30, 31 и 32
Задания 8, 30, 31 и 32 направлены на проверку знаний свойств неорганических веществ. Изменившийся формат заданий 30 и 31 ограничивает экзаменуемых в выборе веществ, между которыми идет реакция. Теперь уравнение должно соответствовать указанным в условии признакам: меняется ли цвет раствора, образуется или не образуется осадок либо газ. Поэтому не любое правильно написанное уравнение будет считаться верным: оценивается уравнение только той реакции, которая полностью соответствует условию. Для выполнения задания 30 нужно хорошо знать, какие конкретно вещества являются окислителями и восстановителями, а для задания 31 – вспомнить формулы малодиссоциирующих веществ (их нельзя записывать в виде ионов).
Важно помнить: если в исходных веществах есть кислота, то в продуктах не может получиться основание или основная соль, и наоборот. Следует проверять, чтобы получившиеся продукты реакции не реагировали между собой и с реагентами. Если есть возможность дальнейшего протекания реакции, значит, уравнение неверно. Больше информации о выполнении этих заданий можно найти на сайте Московского образовательного телеканала в видеоролике «Учимся вместе. Я сдам ЕГЭ!».
Задания 8 и 32 различаются тем, что первое предполагает только выбор возможных реакций, а во втором требуется написание уравнений (при этом даются подсказки в виде признаков протекания реакций). Приступая к выполнению задания 8, нужно рассмотреть предложенные формулы веществ с двух позиций: их кислотно-основных и окислительно-восстановительных свойств. Это позволит сразу понять, от какого списка реагентов можно отказаться: например, кислота не реагирует с кислотой, а восстановитель – с восстановителем. Для выполнения задания 32 особенно важно знать цвета осадков и растворов – это может быть хорошей подсказкой для определения продуктов реакции. Выучить палитру довольно просто, если раскрасить таблицу растворимости, отмечая все известные цветовые признаки соединений. Дополнительную информацию о задании 32 можно посмотреть по ссылке.
Задание 13
Очень много ошибок выпускники делают в задании 13 (свойства углеводородов), особенно если вопрос заключается в определении механизма реакции. Рекомендую обратить внимание на то, что ионный механизм всегда связан с присутствием ионов, то есть разноименно заряженных частиц. Но есть вещества, которые при разных условиях могут образовывать и частицы-ионы, и частицы-радикалы. Например, молекула хлора при облучении распадается на радикалы, а вот катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи, и получаются ионы.
Гораздо легче запомнить свойства углеводородов, если учитывать возможность веществ с определенным типом связи вступать в соответствующие реакции: кратная связь – реакции присоединения, одинарная связь – реакции замещения. Но не следует забывать также, что при изменении условий могут быть исключения даже в основных законах: с перекисью водорода в качестве катализатора реакция присоединения идет вопреки правилу Марковникова, а если хлорирование алкена проводить при температуре 600 0С, то вместо реакции присоединения пойдет замещение у атома углерода в sp3-гибридизации.
Задания 15 и 17
Не менее сложны задания 15 (азотсодержащие органические вещества и углеводы) и 17 (кислородсодержащие органические вещества). При изучении свойств этих соединений нужно обратить внимание, что реакции могут идти как по функциональной группе, так и по радикалу. Чтобы выучить как можно больше свойств органических соединений, можно составить конспект, выписать побольше уравнений для каждого класса. И конечно же, нужно выполнять цепочки на взаимосвязь органических веществ. Рекомендую посмотреть видеоролики по этим заданиям на Московском образовательном телеканале – «Химия, ЕГЭ. Задание № 15» и «Химия, ЕГЭ. Задание № 17», а также видео «Химия, 10 класс. Взаимосвязь классов органических веществ».
Затруднения вызывают и вопросы по окислительно-восстановительным реакциям в органической химии, особенно если нужно расставить коэффициенты. Справиться с такими заданиями поможет консультация эксперта: «Химия, 11 класс. Окислительно-восстановительные реакции в органической химии».
Задания 34 и 35
Самыми трудными для выполнения являются задания 34 и 35 – это расчетные задачи с химическим содержанием.
Ошибки в задании 35 чаще всего случаются из-за неправильного определения структурной формулы. Обычно это связано с недостаточным знанием химических свойств органических веществ. Поэтому здесь только один совет: стараться каждый день выполнять хотя бы одну цепочку превращений, писать уравнения реакций.
Задание 34 сложно тем, что для него нет единого алгоритма решения. Есть задачи на электролиз, смеси, атомистику, а бывает, что в условии переплетается несколько типов задач. Я бы советовала сначала отработать какой-то один тип задач, разобраться в его логике. Потом подключить задачи другого типа и понять, в чем отличие, определить последовательность действий.
При решении этих задач требуется повышенное внимание: лучше прочитать условие несколько раз, возвращаться к нему по мере выполнения задания, отмечать массы веществ, которые уходят из раствора, чтобы исключить их при нахождении массы конечного раствора. Формулы, применяемые для решения задачи 34, простые и хорошо известные, например: массовая доля равна массе растворенного вещества, деленной на массу раствора. Сложности – в деталях: при вычислении массы раствора нужно не забыть сложить все массы добавляемых веществ, вычесть массы осадков и выделившихся газов. Важно помнить, что амфотерные гидроксиды в избытке щелочи растворяются, и если в начале задачи трудно определить избыток или недостаток щелочи, можно написать два возможных уравнения – образования гидроксида и образования комплексной соли.
Полезные ссылки
Для успешной сдачи экзамена по химии нужно готовиться, повторять теорию и выполнять упражнения. Найти их можно в открытом банке заданий на сайте Федерального института педагогических измерений.
Также я рекомендую посмотреть видеоролики Московского образовательного телеканала, где в рубриках «Субботы московского выпускника» (совместный проект с Московским центром качества образования), «Спроси эксперта», «Учимся вместе. Я сдам ЕГЭ!» ведущие эксперты предметных комиссий разбирают задания ЕГЭ и дают рекомендации, как лучше подготовиться. А все новости, касающиеся ЕГЭ, можно найти на сайте Московского центра качества образования.
Источник: Activityedu.ru
В каких заданиях ЕГЭ по химии 2022 легко ошибиться?
В прошлом году 20,31% абитуриентов не преодолели минимальный порог ЕГЭ по химии. Как видишь, экзамен не был лёгким. Судя по демоверсии от ФИПИ, сложные задания останутся и в ЕГЭ 2022. Давай разберём их в статье ниже.
Строение атома и вещества. Химическая связь
Задание 1
Здесь просят указать элементы, атомы которых в основном состоянии имеют одинаковое количество неспаренных электронов. В прошлом году 12% абитуриентов запутались в модели структуры атомов, поэтому допустили ошибку. Также, выбирая ответ, внимательно смотри на расположение химических элементов в группе.
Задание 3
В третьем примере из числа указанных в ряду элементов нужно выбрать два, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления. С правильным ответом тебе поможет таблица Менделеева и простые навыки вычисления. Естественно, умение определять степень окисления химического элемента — главное для третьего задания.
Неорганическая химия
Задание 8
Вопрос проверяет твоё умение соотнести исходное вещество, вступающее в реакцию, вместе с продуктами взаимодействия. Распространённой ошибкой на ЕГЭ является решение таких заданий «в уме». То есть ты должен прогнозировать возможности протекания реакций, анализируя столбец реагенты по вертикали. То есть сначала определи вероятность взаимодействия вещества А с первым веществом каждого ряда и так далее.
Органическая химия
Задание 11
В прошлом году в задании 11 ошиблись 13% абитуриентов. Согласно условиям, из предложенного перечня тебе надо выбрать два вещества, которые являются изомерами бутена-1. Без знания органики ты вряд ли тщательно проанализируешь строение каждого из веществ. Помни об этом, чтобы дать правильный ответ на экзамене.
Расчёты по химическим формулам и уравнениям реакций
Задание 18
Для успешного выполнения 18 вопроса тебе нужно разбираться в свойствах давления и скорости реакций, а также уменьшении концентрации исходных веществ. Важно вспомнить все факторы, влияющие на протекание реакции, которая указана в условии задания.
Задание 23
Выполняя задание 23, выпускники чаще всего спотыкались о незнание принципов протекания представленной необратимой реакции и забывали о необходимости работать с таблицей. На самом деле, решить это задание можно за считанные минуты. Главное — не запутаться в подсчётах и не забыть учесть коэффициенты.
Расчёты по химическим формулам и уравнениям реакций
Задание 34
В задании 34 выпускников ожидает задача высокого уровня сложности. Помимо знаний по химии необходимо неплохое владение математикой, ведь значительная часть ошибок в этом пункте допускалась из-за неверных подсчётов. Поэтому советуем тебе не спешить и ещё раз проверить свои подсчёты перед внесением ответа в бланк.
Как видишь, эти задания вполне реально решить, если внимательно прочитать условия и не забыть дополнительно проверить правильность вычислений. А чтобы тебе не пришлось переживать, что на ЕГЭ попадутся вопросы, на которые не будешь знать ответ, приходи на курсы подготовки к ЕГЭ!
Спасибо, что дочитал до конца. Мы рады, что были полезны. Чтобы получить больше информации, посмотри ещё:
Каталог учебных заведений Адукар
5 заблуждений об учёбе в университете, которые родились из фильмов про студентов
Не пропускай важные новости и подписывайся на наш YouTube, ВК, Instagram, Telegram.
***
Если хотите разместить этот текст на своём сайте или в социальной сети, свяжись с нами по адресу info@adukar.by. Перепечатка материалов возможна только с письменного согласия редакции.
Хочешь быть в курсе новостей ЦТ?
Подписывайся на Адукар в соцсетях!
Начни подготовку к ЦТ и ЦЭ прямо сейчас!

Адукар обещает крутых преподавателей и много полезной практики.
итоговые занятия перед ЦТ? Такие занятия мы проводим уже четвёртый год, и преподаватели нашего учебного центра
научились достаточно точно предсказывать, какие вопросы будут на ЦТ. На этом занятии мы прорешаем их вместе с тобой!
Регистрируйся,
если еще не сделал этого — и увеличь свои шансы на поступление!