Тривиальные названия неорганических веществ (тривиальная номенклатура) — это названия неорганических веществ, которые присвоили тем или иным веществам, и которые не относятся ни к какой системе названия веществ (систематической номенклатуре и др.).
Тривиальные названия органических веществ (тривиальная номенклатура)
| Тривиальное название | Формула | Название |
| Аммиак | NH3 | |
| Бертолетова соль | KClO3 | Хлорат калия |
| Боксит, глинозем | Al2O3 | Оксид алюминия |
| Бурый газ, лисий хвост | NO2 | Оксид азота (IV) |
| Веселящий газ, закись азота | N2O | Оксид азота (I) |
| Гашеная известь | Ca(OH)2 | Гидроксид кальция |
| Гипс | CaSO4⋅2H2O | Дигидрат сульфата кальция |
| Глауберова соль | Na2SO4⋅10Н2О | Декагидрат сульфата натрия |
| Доломит | CaCO3⋅MgCO3 | Карбонат кальция-магния |
| Едкий натр, каустик, каустическая сода | NaOH | Гидроксид натрия |
| Едкое кали | КОН |
Гидроксид калия |
| Железная окалина | Fe3O4 | Оксид железа (II, III) |
| Железный купорос | FeSO4⋅7H2O |
Гептагидрат сульфата железа (II) |
| Желтая кровяная соль | K4[Fe(CN)6] |
Гексацианоферрат (II) калия |
| Известковая вода | Са(ОН)2 |
Раствор гидроксида кальция |
| Известняк, мел, мрамор | СаСО3 |
Карбонат кальция |
| Каменная соль, галит | NaCl |
Хлорид натрия |
| Карбамид (мочевина) | СО(NH2)2 |
Амид угольной кислоты |
| Карборунд | SiC |
Карбид кремния |
| Красная кровяная соль | K3[Fe(CN)6] |
Гексацианоферрат (III) калия |
| Кремнезем, кварц, песок | SiO2 |
Оксид кремния |
| Криолит | Na3AlF6 |
Гексафтороалюминат натрия |
| Малахит | (CuOH)2CO3 |
Гидроксокарбонат меди |
| Медный купорос | CuSO4⋅5H2O |
Пентагидрат сульфата меди |
| Нашатырный спирт | NH3⋅H2O | Раствор NH3 в воде |
| Нашатырь | NH4Cl | Хлорид аммония |
| Негашеная известь | СаО |
Оксид кальция |
| Олеум | SO3 в H2SO4 конц. | Раствор SO3 в H2SO4 конц. |
| Плавиковая кислота | HF |
Фтороводородная кислота |
| Пирит, железный колчедан, серный колчедан | FeS2 |
Персульфид железа (II) |
| Пиролюзит | MnO2 |
Оксид марганца (IV) |
| Поташ | K2CO3 |
Карбонат калия |
| Селитра аммиачная | NH4NO3 |
Нитрат аммония |
| Селитра калийная (индийская) | КNO3 |
Нитрат калия |
| Селитра кальциевая (норвежская) | Сa(NO3)2 |
Нитрат кальция |
| Селитра натриевая (чилийская) | NaNO3 |
Нитрат натрия |
| Сернистый газ | SO2 |
Оксид серы (IV) |
| Силан | SiH4 | |
| Сода кальцинированная | Na2CO3 |
Карбонат натрия |
| Сода кристаллическая | Na2CO3⋅10Н2О |
Декагидрат карбоната натрия |
| Сода питьевая (пищевая) | NaHCO3 |
Гидрокарбонат натрия |
| Суперфосфат двойной | Ca(H2PO4)2 |
Дигидрофосфат кальция |
| Угарный газ | СО |
Оксид углерода (II) |
| Углекислый газ | CO2 | Оксид углерода (IV) |
| Фосфорит | Ca3(PO4)2 |
горная порода, фосфат кальция |
| Фосфин | PH3 | |
| Хлорная известь | СаОСl2 |
Хлорид-гипохлорит кальция |
| Царская водка | смесь HNO3 конц. и НСl конц. в объемном отношении 1:3 |
Тривиальные названия неорганических и органических веществ, углеводородных радикалов.
Тривиальные названия неорганических веществ
| Na3[AlF6] | криолит |
| SiO2 | кварц, кремнезем |
| FeS2 | пирит, железный колчедан |
| CaSO4∙2H2O | гипс |
| CaC2 | карбид кальция |
| Al4C3 | карбид алюминия |
| KOH | едкое кали |
| NaOH | едкий натр, каустическая сода |
| H2O2 | перекись водорода |
| CuSO4∙5H2O | медный купорос |
| NH4Cl | нашатырь |
| CaCO3 | мел, мрамор, известняк |
| N2O | веселящий газ |
| NO2 | бурый газ |
| NaHCO3 | пищевая (питьевая) сода |
| Fe3O4 | железная окалина |
| NH3∙H2O (NH4OH) | нашатырный спирт |
| CO | угарный газ |
| CO2 | углекислый газ |
| SiC | карборунд (карбид кремния) |
| PH3 | фосфин |
| NH3 | аммиак |
| KClO3 | бертолетова соль (хлорат калия) |
| (CuOH)2CO3 | малахит |
| CaO | негашеная известь |
| Ca(OH)2 | гашеная известь |
| прозрачный водный раствор Ca(OH)2 | известковая вода |
| взвесь твердого Ca(OH)2 в его водном растворе | известковое молоко |
| K2CO3 | поташ |
| Na2CO3 | кальцинированная сода |
| Na2CO3∙10H2O | кристаллическая сода |
| MgO | жженая магнезия |
Тривиальные названия органических веществ и углеводородных радикалов
Углеводороды и галогенпроизводные углеводородов
Углеводородные радикалы
Спирты
Фенолы
Альдегиды и кетоны
Тривиальные названия карбоновых кислот и образуемых ими солей и сложных эфиров
Углеводы
| Название | Формула | Класс углевода |
| глюкоза | C6H12O6 | многоатомный альдегидоспирт |
| фруктоза | C6H12O6 | многоатомный кетоспирт |
| сахароза | C12H22O11 | дисахарид |
| крахмал | (C6H10O5)n | полисахарид |
| целлюлоза | (C6H10O5)n | полисахарид |
| гликоген | (C6H10O5)n | полисахарид |
Амины и аминокислоты
Тривиальные названия ЕГЭ
Материал по химии
- Тривиальные названия неорганических веществ ЕГЭ
- Какие кристаллогидраты нужно знать на ЕГЭ?
- Какие тривиальные названия неорганических веществ нужно знать на ОГЭ по химии?
- Что означает римская цифра в химии?
- Флеш-карточки и тренировочные задания ЕГЭ по химии
Тривиальные названия неорганических веществ ЕГЭ
Таблица. Тривиальные названия неорганических веществ
|
Na |
Сильвинит |
mNaCl·nKCl |
|
Галит, поваренная или каменная соль |
NaCl |
|
|
Мирабилит, глауберова соль |
Na2SO4·10H2O |
|
|
Едкий натр, каустическая сода |
NaOH |
|
|
Кальцинированная сода |
Na2CO3 |
|
|
Кристаллическая сода |
Na2CO3·10H2O |
|
|
Питьевая/пищевая сода |
NaHCO3 |
|
|
Чилийская или натронная селитра |
NaNO3 |
|
|
Криолит |
Na3[AlF6] |
|
|
Антихлор, тиосульфат натрия |
Na2S2O3 |
|
|
K |
Карналлит |
KCl·MgCl2·6H2O |
|
Едкое кали |
KOH |
|
|
Поташ, зола |
K2CO3 |
|
|
Калийная или калиевая, или индийская селитра |
KNO3 |
|
|
Марганцовка |
KMnO4 |
|
|
Берлинская лазурь |
KFe[Fe(CN)6] |
|
|
Желтая кровяная соль |
K4[Fe(CN)6] |
|
|
Красная кровяная соль |
K3[Fe(CN)6] |
|
|
Бертолетова соль |
KClO3 |
|
|
Хромпик |
K2Cr2O7 |
|
|
Ag |
Ляпис |
AgNO3 |
|
Cu |
Малахит, основной карбонат меди |
(CuOH)2CO3 |
|
Медный блеск, халькозин |
Cu2S |
|
|
Be |
Аквамарин/изумруд |
3BeO·Al2O3·6SiO2 |
|
Mg |
Английская соль, горькая соль |
MgSO4·7H2O |
|
Асбест |
3MgO·2SiO2·2H2O |
|
|
Оливин |
2MgO·SiO2 |
|
|
Жженая магнезия |
MgO |
|
|
Шпинель |
MgO·Al2O3 |
|
|
Тальк |
3MgO·4SiO2·H2O |
|
|
Магнезит |
MgCO3 |
|
|
Ca |
Фосфорит, апатит |
Ca3(PO4)2 |
|
Доломит |
CaCO3·MgCO3 |
|
|
Гипс |
CaSO4·2H2O |
|
|
Негашеная известь, кипелка |
CaO |
|
|
Гашеная известь, пушонка, известковая вода, известковое молоко |
Ca(OH)2 |
|
|
Известняк, мрамор, мел, мергель, кальцит, исландский шпат |
CaCO3 |
|
|
Флюорит |
CaF2 |
|
|
Хлорная известь, белильная известь, хлорка |
CaCl2+Ca(ClO)2+Ca(OH)2 |
|
|
Ba |
Баритовая вода, едкий барит |
Ba(OH)2 |
|
Zn |
Цинковые белила |
ZnO |
|
Цинковая обманка, сфалерит |
ZnS |
|
|
Hg |
Киноварь |
HgS |
|
Сулема |
HgCl2 |
|
|
Al |
Глинозем |
Al2O3 |
|
C |
Болотный или рудничный газ, метан |
CH4 |
|
Сухой лёд (твердый), углекислый газ (газообразный) |
CO2 |
|
|
Угарный газ |
СО |
|
|
Фосген |
COCl2 |
|
|
Хлороформ |
CHCl3 |
|
|
Si |
Карборунд |
SiC |
|
Кремнезем |
SiO2 |
|
|
Силан |
SiH4 |
|
|
Pb |
Свинцовые белила (основный карбонат свинца) |
2PbCO3.Pb(OH)2 |
|
Свинцовый сахар |
Pb(CH3COO)2.3H2O |
|
|
Свинцовый сурик |
Pb3O4 – двойной оксид (2PbO·PbO2) |
|
|
Ti |
Титановые белила |
TiO2 |
|
N |
Веселящий газ, закись азота |
N2O |
|
Аммиак |
NH3 |
|
|
Нашатырный спирт, аммиачная вода |
NH3·H2O или NH4OH |
|
|
Нашатырь |
NH4Cl |
|
|
Аммиачная селитра |
NH4NO3 |
|
|
P |
Фосфин |
PH3 |
|
As |
Арсин |
AsH3 |
|
S |
Сернистый газ |
SO2 |
|
Серный ангидрид |
SO3 |
|
|
Серный цвет |
S |
|
|
H |
Плавиковая кислота |
HF |
|
Синильная кислота |
HCN |
|
|
Соляная кислота |
HCl |
|
|
Mn |
Пиролюзит |
MnO2 |
|
Fe |
Железная окалина, закись-окись железа |
Fe3O4 – двойной оксид (FeO·Fe2O3) |
|
Гематит, окись железа |
Fe2O3 |
|
|
Закись железа |
FeO |
|
|
Хлористое железо |
FeCl2 |
|
|
Хлорное железо |
FeCl3 |
|
|
Пирит, железный или серный колчедан |
FeS2 |
Какие кристаллогидраты нужно знать на ЕГЭ?
Многие соли при выпаривании из них воды, способны образовывать кристаллогидраты, но, к нашему счастью, для успешной сдачи ЕГЭ по химии необходимо знать ограниченный список таких веществ. В первую очередь популярным кристаллогидратам относятся купоросы. Купоросы – кристаллогидраты сульфатов переходных металлов во второй валентности.
|
Формула соли |
Количество воды |
Название тривиальное |
Название систематическое |
|
FeSO4 |
7H2O |
Железный купорос |
Гептагидрат сульфата железа II |
|
ZnSO4 |
7H2O |
Цинковый купорос |
Гептагидрат сульфата цинка |
|
CuSO4 |
5H2O |
Медный купорос |
Пентагидрат сульфата меди II |
Железный купорос – FeSO4·7H2O – кристаллы бледно-зеленого или голубовато-зеленого цвета. ZnSO4·7H2O – цинковый купорос – белые кристаллы, CuSO4·5H2O – медный купорос – имеет голубой цвет кристаллов. Другие купоросы (никелевый, свинцовый, кобальтовый) на ЕГЭ не встречаются.
Помимо купоросов на экзамене может встретиться Na2SO4·10H2O (декагидрат сульфата натрия) – глауберова соль, Na2CO3·10H2O (декагидрат карбоната натрия) – кристаллическая сода, CaSO4·2H2O (дигидрат сульфата кальция) – гипс.
Какие тривиальные названия неорганических веществ нужно знать на ОГЭ по химии?
|
Формула |
Систематическое название |
Тривиальное название |
|
NaCl |
Хлорид натрия |
Поваренная или каменная соль |
|
Na2CO3 |
Карбонат натрия |
Кальцинированная сода |
|
NaHCO3 |
Гидрокарбонат натрия |
Питьевая или пищевая сода |
|
CaO |
Оксид кальция |
Негашеная известь |
|
Ca(OH)2 |
Гидроксид кальция |
Гашеная известь, известковая вода |
|
CaCO3 |
Карбонат кальция |
Известняк, мрамор, мел |
|
CH4 |
Метан |
Болотный газ |
|
CO |
Оксид углерода II, монооксид углерода |
Угарный газ |
|
CO2 |
Оксид углерода IV, диоксид углерода |
Углекислый газ |
|
SiO2 |
Оксид кремния IV, диоксид кремния |
Кремнезем |
|
N2O |
Оксид азота I |
Веселящий газ |
|
NH3 |
Не используют |
Аммиак |
|
SO2 |
Оксид серы IV, диоксид серы |
Сернистый газ |
|
HF |
Фтороводородная кислота |
Плавиковая кислота |
|
HCl |
Хлороводородная кислота |
Соляная кислота |
Что означает римская цифра в химии?
Римские цифры после названия вещества обозначают валентность образующего вещество элемента, например в веществе Оксид серы IV сера имеет валентность «4».
Флеш-карточки и тренировочные задания ЕГЭ по химии
Флеш-карточки являются популярным и удобным методом запоминания информации. Мы создали для Вас несколько подборок карточек, в которых перекликаются вещества из разных групп, таким образом, чтобы вы возвращались к веществам не один раз. Если Вы хотите перемешать карточки – просто обновите страницу.
Подборка флэш-карточек с тривиальными названиями простых оксидов и двойных оксидов.
-
CO2
углекислый газ, сухой лёд
-
N2O
Веселящий газ, закись азота
-
Fe2O3
Гематит, окись железа
-
Fe3O4
Железная окалина, закись-окись железа
Задание в формате ЕГЭ с ответом:
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- железная окалина
- негашеная известь
- глинозем
- Fe2O3
- CaO
- Al2O3
- CO2
- Fe3O4
Пример задания из КИМ ЕГЭ:
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- закись азота
- окись железа
- закись железа
- NO
- FeO
- Fe3O4
- N2O
- Fe2O3
Подборка флэш-карточек с тривиальными названиями хлоридов и хлорсодержащих веществ.
-
NaCl
каменная или поваренная соль, галит
Задание по образцу ФИПИ:
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- хлорное железо
- бертолетова соль
- сулема
- FeCl2
- FeCl3
- KCl
- KClO3
- HgCl2
Попробуйте решить задание ЕГЭ:
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- хлористое железо
- хлороформ
- фосген
- FeCl2
- COCl2
- CCl4
- FeCl3
- CHCl3
Подборка флэш-карточек с тривиальными названиями сульфатов и серосодержащих веществ.
-
MgSO4·7H2O
горькая, английская соль
-
FeS2
Пирит, железный или серный колчедан
-
Na2S2O3
антихлор, тиосульфат натрия
-
Na2SO4·10H2 O
глауберова соль, мирабилит
-
Cu2S
медный блеск, халькозин
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- глауберова соль
- горькая соль
- железный купорос
- Mg2SO4·7H2O
- Zn2SO4·7H2O
- Na2CO3·10H2O
- Fe2SO4·7H2O
- Na2SO4·10H2O
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- сернистый газ
- серный цвет
- пирит
- S
- SO2
- SO3
- PbS
- FeS2
Подборка флэш-карточек с тривиальными названиями железосодержащих веществ.
-
K4[Fe(CN)6]
желтая кровяная соль
-
Fe2O3
Гематит, окись железа
-
FeS2
Пирит, железный или серный колчедан
-
Желтая кровяная соль
K4[Fe(CN)6]
-
Берлинская лазурь
KFe[Fe(CN)6]
-
Красная кровяная соль
K3[Fe(CN)6]
-
Fe3O4
Железная окалина, закись-окись железа
-
K3[Fe(CN)6]
красная кровяная соль
-
KFe[Fe(CN)6]
берлинская лазурь
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- железная окалина
- желтая кровяная соль
- хлористое железо
- K4[Fe(CN)6
- Fe3O4
- K3[Fe(CN)6
- FeCl2
- FeO
Подборка флэш-карточек с тривиальными названиями карбонатов.
-
Кальцинированная сода
Na2CO3
-
Кристаллическая сода
Na2CO3·10H2O
-
(CuOH)2CO3
малахит, основной карбонат меди
-
Na2CO3·10H2O
кристаллическая сода
-
Na2CO3
кальцинированная сода
-
CaCO3
мел, мрамор, известняк
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- каустическая сода
- кальцинированная сода
- питьевая сода
- Na2CO3
- NaHCO3
- NaOH
- Ca(HCO3)2
- CaCO3
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- кристаллическая сода
- поташ
- малахит
- Na2CO3·10H2O
- (CuOH)2CO3
- CaCO3
- K2CO3
- NaHCO3
Установите соответствие между тривиальным названием вещества и формулой этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
- магнезит
- доломит
- известняк
- FeCO3
- MgCO3
- MgCO3·CaCO3
- CaCO3
- Na2CO3
5 января 2022
В закладки
Обсудить
Жалоба
Тривиальные названия неорганических веществ
→ triv.pdf
→ Другая подборка.
H2O – вода
CO – угарный газ
CO2 – углекислый газ
NO2 – бурый газ
Al2O3 – глинозем
SiO2 – кремнезем, кварц, песок
SO2 – сернистый газ
CaO – негашеная известь
MnO2 – пиролюзит
Fe3O4 – железная окалина
N2O – веселящий газ
NaOH – едкий натр
KOH – едкое кали
Ca(OH)2 – гашеная известь
Прозрачный раствор Ca(OH)2 – известковая вода
Суспензия Ca(OH)2 – известковое молоко
NaCl – поваренная соль
Na3[AlF6] – криолит
CaCO3 – мел, мрамор, известняк
NaHCO3 – пищевая сода, питьевая сода
KNO3 – калийная селитра
KClO3 – бертолетова соль
Cu2(OH)2CO3 – малахит
H2O2 – перекись водорода
FeS2 – пирит, серный колчедан, железный колчедан
SiC – карборунд
SiH4 – силан
NH3 – аммиак
PH3 – фосфин
NH3∙H2O – аммиачная вода, нашатырный спирт
Смесь CO и H2 – синтез-газ
Раствор SO3 в безводной H2SO4 – олеум
Классификация неорганических веществ с примерами соединений
Теперь проанализируем представленную выше классификационную схему более детально.
Как мы видим, прежде всего все неорганические вещества делятся на простые и сложные:
Простыми веществами называют такие вещества, которые образованы атомами только одного химического элемента. Например, простыми веществами являются водород H2, кислород O2, железо Fe, углерод С и т.д.
Среди простых веществ различают металлы, неметаллы и благородные газы:
Металлы образованы химическими элементами, расположенными ниже диагонали бор-астат, а также всеми элементами, находящимися в побочных группах.
Благородные газы образованы химическими элементами VIIIA группы.
Неметаллы образованы соответственно химическими элементами, расположенными выше диагонали бор-астат, за исключением всех элементов побочных подгрупп и благородных газов, расположенных в VIIIA группе:
Названия простых веществ чаще всего совпадают с названиями химических элементов, атомами которых они образованы. Однако для многих химических элементов широко распространено такое явление, как аллотропия. Аллотропией называют явление, когда один химический элемент способен образовывать несколько простых веществ. Например, в случае химического элемента кислорода возможно существование молекулярных соединений с формулами O2 и O3. Первое вещество принято называть кислородом так же, как и химический элемент, атомами которого оно образовано, а второе вещество (O3) принято называть озоном. Под простым веществом углеродом может подразумеваться любая из его аллотропных модификаций, например, алмаз, графит или фуллерены. Под простым веществом фосфором могут пониматься такие его аллотропные модификации, как белый фосфор, красный фосфор, черный фосфор.
Сложные вещества
Сложными веществами называют вещества, образованные атомами двух или более химических элементов.
Так, например, сложными веществами являются аммиак NH3, серная кислота H2SO4, гашеная известь Ca(OH)2 и бесчисленное множество других.
Среди сложных неорганических веществ выделяют 5 основных классов, а именно оксиды, основания, амфотерные гидроксиды, кислоты и соли:
Оксиды — сложные вещества, образованные двумя химическими элементами, один из которых кислород в степени окисления -2.
Общая формула оксидов может быть записана как ЭxOy, где Э — символ какого-либо химического элемента.
Номенклатура оксидов
Название оксида химического элемента строится по принципу:
Например:
Fe2O3 — оксид железа (III); CuO — оксид меди (II); N2O5 — оксид азота (V)
Нередко можно встретить информацию о том, что в скобках указывается валентность элемента, однако же это не так. Так, например, степень окисления азота N2O5 равна +5, а валентность, как это ни странно, равна четырем.
В случае, если химический элемент имеет единственную положительную степень окисления в соединениях, в таком случае степень окисления не указывается. Например:
Na2O — оксид натрия; H2O — оксид водорода; ZnO — оксид цинка.
Классификация оксидов
Оксиды по их способности образовывать соли при взаимодействии с кислотами или основаниями подразделяют соответственно на солеобразующие и несолеобразующие.
Несолеобразующих оксидов немного, все они образованы неметаллами в степени окисления +1 и +2. Список несолеобразующих оксидов следует запомнить: CO, SiO, N2O, NO.
Солеобразующие оксиды в свою очередь подразделяются на основные, кислотные и амфотерные.
Основными оксидами называют такие оксиды, которые при взаимодействии с кислотами (или кислотными оксидами) образуют соли. К основным оксидам относят оксиды металлов в степени окисления +1 и +2, за исключением оксидов BeO, ZnO, SnO, PbO.
Кислотными оксидами называют такие оксиды, которые при взаимодействии с основаниями (или основными оксидами) образуют соли. Кислотными оксидами являются практически все оксиды неметаллов за исключением несолеобразующих CO, NO, N2O, SiO, а также все оксиды металлов в высоких степенях окисления (+5, +6 и +7).
Амфотерными оксидами называют оксиды, которые могут реагировать как с кислотами, так и основаниями, и в результате этих реакций образуют соли. Такие оксиды проявляют двойственную кислотно-основную природу, то есть могут проявлять свойства как кислотных, так и основных оксидов. К амфотерным оксидам относятся оксиды металлов в степенях окисления +3, +4, а также в качестве исключений оксиды BeO, ZnO, SnO, PbO.
Некоторые металлы могут образовывать все три вида солеобразующих оксидов. Например, хром образует основный оксид CrO, амфотерный оксид Cr2O3 и кислотный оксид CrO3.
Как можно видеть, кислотно-основные свойства оксидов металлов напрямую зависят от степени окисления металла в оксиде: чем больше степень окисления, тем сильнее выражены кислотные свойства.
Основания
Основания — соединения с формулой вида Me(OH)x, где x чаще всего равен 1 или 2.
Исключения: Be(OH)2, Zn(OH)2, Sn(OH)2 и Pb(OH)2 не относятся к основаниям, несмотря на степень окисления металла +2. Данные соединения являются амфотерными гидроксидами, которые еще будут рассмотрены в этой главе более подробно.
Классификация оснований
Основания классифицируют по количеству гидроксогрупп в одной структурной единице.
Основания с одной гидроксогруппой, т.е. вида MeOH, называют однокислотными основаниями, с двумя гидроксогруппами, т.е. вида Me(OH)2, соответственно, двухкислотными и т.д.
Также основания подразделяют на растворимые (щелочи) и нерастворимые.
К щелочам относятся исключительно гидроксиды щелочных и щелочно-земельных металлов, а также гидроксид таллия TlOH.
Номенклатура оснований
Название основания строится по нижеследующему принципу:
Например:
Fe(OH)2 — гидроксид железа (II),
Cu(OH)2 — гидроксид меди (II).
В тех случаях, когда металл в сложных веществах имеет постоянную степень окисления, указывать её не требуется. Например:
NaOH — гидроксид натрия,
Ca(OH)2 — гидроксид кальция и т.д.
Кислоты
Кислоты — сложные вещества, молекулы которых содержат атомы водорода, способные замещаться на металл.
Общая формула кислот может быть записана как HxA, где H — атомы водорода, способные замещаться на металл, а A — кислотный остаток.
Например, к кислотам относятся такие соединения, как H2SO4, HCl, HNO3, HNO2 и т.д.
Классификация кислот
По количеству атомов водорода, способных замещаться на металл, кислоты делятся на:
— одноосновные кислоты: HF, HCl, HBr, HI, HNO3;
— двухосновные кислоты: H2SO4, H2SO3, H2CO3;
— трехосновные кислоты: H3PO4, H3BO3.
Следует отметить, что количество атомов водорода в случае органических кислот чаще всего не отражает их основность. Например, уксусная кислота с формулой CH3COOH, несмотря на наличие 4-х атомов водорода в молекуле, является не четырех-, а одноосновной. Основность органических кислот определяется количеством карбоксильных групп (-COOH) в молекуле.
Также по наличию кислорода в молекулах кислоты подразделяют на бескислородные (HF, HCl, HBr и т.д.) и кислородсодержащие (H2SO4, HNO3, H3PO4 и т.д.). Кислородсодержащие кислоты называют также оксокислотами.
Более детально про классификацию кислот можно почитать здесь.
Номенклатура кислот и кислотных остатков
Нижеследующий список названий и формул кислот и кислотных остатков обязательно следует выучить.
В некоторых случаях облегчить запоминание может ряд следующих правил.
Как можно видеть из таблицы выше, построение систематических названий бескислородных кислот выглядит следующим образом:
Например:
HF — фтороводородная кислота;
HCl — хлороводородная кислота;
H2S — сероводородная кислота.
Названия кислотных остатков бескислородных кислот строятся по принципу:
Например, Cl— — хлорид, Br— — бромид.
Названия кислородсодержащих кислот получают добавлением к названию кислотообразующего элемента различных суффиксов и окончаний. Например, если кислотообразующий элемент в кислородсодержащей кислоте имеет высшую степень окисления, то название такой кислоты строится следующим образом:
Например, серная кислота H2S+6O4, хромовая кислота H2Cr+6O4.
Все кислородсодержащие кислоты могут быть также классифицированы как кислотные гидроксиды, поскольку в их молекулах обнаруживаются гидроксогруппы (OH). Например, это видно из нижеследующих графических формул некоторых кислородсодержащих кислот:
Таким образом, серная кислота иначе может быть названа как гидроксид серы (VI), азотная кислота — гидроксид азота (V), фосфорная кислота — гидроксид фосфора (V) и т.д. При этом число в скобках характеризует степень окисления кислотообразующего элемента. Такой вариант названий кислородсодержащих кислот многим может показаться крайне непривычным, однако же изредка такие названия можно встретить в реальных КИМах ЕГЭ по химии в заданиях на классификацию неорганических веществ.
Амфотерные гидроксиды
Амфотерные гидроксиды — гидроксиды металлов, проявляющие двойственную природу, т.е. способные проявлять как свойства кислот, так и свойства оснований.
Амфотерными являются гидроксиды металлов в степенях окисления +3 и +4 (как и оксиды).
Также в качестве исключений к амфотерным гидроксидам относят соединения Be(OH)2, Zn(OH)2, Sn(OH)2 и Pb(OH)2, несмотря на степень окисления металла в них +2.
Для амфотерных гидроксидов трех- и четырехвалентных металлов возможно существование орто- и мета-форм, отличающихся друг от друга на одну молекулу воды. Например, гидроксид алюминия (III) может существовать в орто-форме Al(OH)3 или мета-форме AlO(OH) (метагидроксид).
Поскольку, как уже было сказано, амфотерные гидроксиды проявляют как свойства кислот, так и свойства оснований, их формула и название также могут быть записаны по-разному: либо как у основания, либо как у кислоты. Например:
| Амфотерный гидроксид в форме основания | Амфотерный гидроксид в форме кислоты | «Кислотный» остаток |
| Zn(OH)2 гидроксид цинка |
H2ZnO2 цинковая кислота |
ZnO22- цинкат |
| Al(OH)3 (орто)гидроксид алюминия |
H3AlO3 ортоалюминиевая кислота |
AlO33- ортоалюминат |
| AlO(OH) метагидроксид алюминия |
HAlO2 метаалюминиевая кислота |
AlO2— метаалюминат |
Соли
Соли — это сложные вещества, в состав которых входят катионы металлов и анионы кислотных остатков.
Так, например, к солям относятся такие соединения как KCl, Ca(NO3)2, NaHCO3 и т.д.
Представленное выше определение описывает состав большинства солей, однако же существуют соли, не попадающие под него. Например, вместо катионов металлов в состав соли могут входить катионы аммония или его органические производные. Т.е. к солям относятся такие соединения, как, например, (NH4)2SO4 (сульфат аммония), [CH3NH3]+Cl— (хлорид метиламмония) и т.д.
Также противоречат определению солей выше класс так называемых комплексных солей, которые будут рассмотрены в конце данной темы.
Классификация солей
С другой стороны, соли можно рассматривать как продукты замещения катионов водорода H+ в кислоте на другие катионы или же как продукты замещения гидроксид-ионов в основаниях (или амфотерных гидроксидах) на другие анионы.
При полном замещении образуются так называемые средние или нормальные соли. Например, при полном замещении катионов водорода в серной кислоте на катионы натрия образуется средняя (нормальная) соль Na2SO4, а при полном замещении гидроксид-ионов в основании Ca(OH)2 на кислотные остатки нитрат-ионы образуется средняя (нормальная) соль Ca(NO3)2.
Соли, получаемые неполным замещением катионов водорода в двухосновной (или более) кислоте на катионы металла, называют кислыми. Так, при неполном замещении катионов водорода в серной кислоте на катионы натрия образуется кислая соль NaHSO4.
Соли, которые образуются при неполном замещении гидроксид-ионов в двухкислотных (или более) основаниях, называют основными солями. Например, при неполном замещении гидроксид-ионов в основании Ca(OH)2 на нитрат-ионы образуется основная соль Ca(OH)NO3.
Соли, состоящие из катионов двух разных металлов и анионов кислотных остатков только одной кислоты, называют двойными солями. Так, например, двойными солями являются KNaCO3, KMgCl3 и т.д.
Если соль образована одним типом катионов и двумя типами кислотных остатков, такие соли называют смешанными. Например, смешанными солями являются соединения Ca(OCl)Cl, CuBrCl и т.д.
Существуют соли, которые не попадают под определение солей как продуктов замещения катионов водорода в кислотах на катионы металлов или продуктов замещения гидроксид-ионов в основаниях на анионы кислотных остатков. Это — комплексные соли. Так, например, комплексными солями являются тетрагидроксоцинкат- и тетрагидроксоалюминат натрия с формулами Na2[Zn(OH)4] и Na[Al(OH)4] соответственно. Распознать комплексные соли среди прочих чаще всего можно по наличию квадратных скобок в формуле. Однако нужно понимать, что, чтобы вещество можно было отнести к классу солей, в его состав должны входить какие-либо катионы, кроме (или вместо) H+, а из анионов должны быть какие-либо анионы помимо (или вместо) OH—. Так, например, соединение H2[SiF6] не относится к классу комплексных солей, поскольку при его диссоциации из катионов в растворе присутствуют только катионы водорода H+. По типу диссоциации данное вещество следует скорее классифицировать как бескислородную комплексную кислоту. Аналогично, к солям не относится соединение [Ag(NH3)2]OH, т.к. данное соединение состоит из катионов [Ag(NH3)2]+ и гидроксид-ионов OH—, т.е. его следует считать комплексным основанием.
Номенклатура солей
Номенклатура средних и кислых солей
Название средних и кислых солей строится по принципу:
Если степень окисления металла в сложных веществах постоянная, то ее не указывают.
Названия кислотных остатков были даны выше при рассмотрении номенклатуры кислот.
Например,
Na2SO4 — сульфат натрия;
NaHSO4 — гидросульфат натрия;
CaCO3 — карбонат кальция;
Ca(HCO3)2 — гидрокарбонат кальция и т.д.
Номенклатура основных солей
Названия основных солей строятся по принципу:
Например:
(CuOH)2CO3 — гидроксокарбонат меди (II);
Fe(OH)2NO3 — дигидроксонитрат железа (III).
Номенклатура комплексных солей
Номенклатура комплексных соединений значительно сложнее, и для сдачи ЕГЭ многого знать из номенклатуры комплексных солей не нужно.
Следует уметь называть комплексные соли, получаемые взаимодействием растворов щелочей с амфотерными гидроксидами. Например:
*Одинаковыми цветами в формуле и названии обозначены соответствующие друг другу элементы формулы и названия.
Тривиальные названия неорганических веществ
Под тривиальными названиями понимают названия веществ не связанные, либо слабо связанные с их составом и строением. Тривиальные названия обусловлены, как правило, либо историческими причинами либо физическими или химическими свойствами данных соединений.
Список тривиальных названий неорганических веществ, которые необходимо знать:
| Na3[AlF6] | криолит |
| SiO2 | кварц, кремнезем |
| FeS2 | пирит, железный колчедан |
| CaSO4∙2H2O | гипс |
| CaC2 | карбид кальция |
| Al4C3 | карбид алюминия |
| KOH | едкое кали |
| NaOH | едкий натр, каустическая сода |
| H2O2 | перекись водорода |
| CuSO4∙5H2O | медный купорос |
| NH4Cl | нашатырь |
| CaCO3 | мел, мрамор, известняк |
| N2O | веселящий газ |
| NO2 | бурый газ |
| NaHCO3 | пищевая (питьевая) сода |
| Fe3O4 | железная окалина |
| NH3∙H2O (NH4OH) | нашатырный спирт |
| CO | угарный газ |
| CO2 | углекислый газ |
| SiC | карборунд (карбид кремния) |
| PH3 | фосфин |
| NH3 | аммиак |
| KClO3 | бертолетова соль (хлорат калия) |
| (CuOH)2CO3 | малахит |
| CaO | негашеная известь |
| Ca(OH)2 | гашеная известь |
| прозрачный водный раствор Ca(OH)2 | известковая вода |
| взвесь твердого Ca(OH)2 в его водном растворе | известковое молоко |
| K2CO3 | поташ |
| Na2CO3 | кальцинированная сода |
| Na2CO3∙10H2O | кристаллическая сода |
| MgO | жженая магнезия |
Автор: С.И. Широкопояс https://scienceforyou.ru/
Skip to content
Чтобы поделиться, нажимайте
Тривиальные названия неорганических веществ:






Тривиальные названия органических веществ:
|
Тривиальное название |
Структурная формула |
Систематическое название |
|
Ацетилен |
CH ≡ CH |
Этин |
|
Анилин |
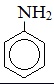 |
Фениламин |
|
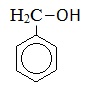
Бензиловый спирт |
|
|
|
Винилацетилен |
CH2 = CH — C ≡ CH |
Бутен-1-ин-3 |
|
Дивинил |
H2C = CH — CH = CH2 |
Бутадиен-1,3 |
|
Изобутан |
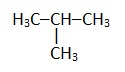 |
2-метилпропан |
|
Изопрен |
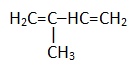 |
2-метилбутадиен-1,3 |
|
Крезол |
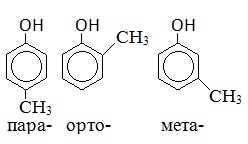 |
Метилфенол |
|
Ксилол |
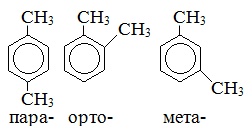 |
Диметилбензол |
|
Кумол |
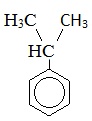 |
Изопропилбензол |
|
Пирогаллол |
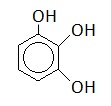 |
1,2,3-тригидроксибензол |
|
Пирокатехин |
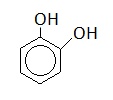 |
1,2-дигидроксибензол |
|
Пропилен |
CH2 = CH- CH3 |
Пропен |
|
Стирол |
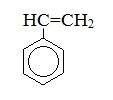 |
Винилбензол |
|
Толуол |
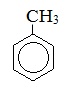 |
Метилбензол |
|
Хлоропрен |
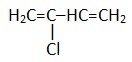 |
2-хлорбутадиен-1,3 |
|
Этилен |
СH2 = CH2 |
Этен |
|
Глицерин |
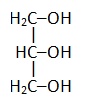 |
Пропантриол-1,2,3 |
|
Глицерат меди |
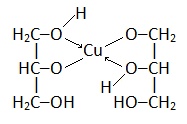 |
|
|
Нитроглицерин |
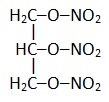 |
|
|
Этиленгликоль |
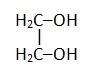 |
Этандиол |
|
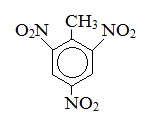
Тротил* |
|
2,4,6 – тринитротолуол |
|
Название кислоты |
Структурная формула |
Систематическое название |
Названия солей и эфиров |
|
Муравьиная кислота |
HCOOH |
Метановая кислота |
Формиат |
|
Уксусная кислота |
CH3COOH |
Этановая кислота |
Ацетат |
|
Пропионовая кислота |
C2H5-COOH |
Пропановая кислота |
Пропионат |
|
Масляная кислота |
C3H7-COOH |
Бутановая кислота |
Бутират |
|
Валериановая кислота |
C4H9-COOH |
Пентановая кислота |
Валерат |
|
Капроновая кислота |
C5H11-COOH |
Гексановая кислота |
|
|
Щавелевая кислота |
HOOC-COOH |
Этандиовая кислота |
Оксалат |
|
Бензойная кислота |
C6H5-COOH | Бензойная кислота |
Бензоат |
|
Акриловая кислота |
H2C = CH-COOH |
Пропеновая кислота |
Акрилат |
|
Линолевая кислота |
C17H31COOH |
Линолеат |
|
|
Олеиновая кислота |
C17H33COOH |
Олеат |
|
|
Пальмитиновая кислота |
C15H31COOH |
Пальмитат |
|
|
Пикриновая кислота |
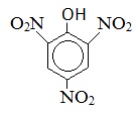 |
2,4,6-тринитрофенол |
Пикрат |
|
Стеариновая кислота |
C17H35COOH |
Стеарат |
|
|
Фталевая кислота |
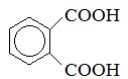 |
Фталат |
|
|
Молочная кислота |
 |
2-гидроксипропановая |
Лактат |
|
Глицин |
H2N-CH2-COOH |
Аминоуксусная кислота |
Аминоацетат |
|
Аланин |
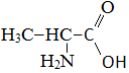 |
2-аминопропионовая кислота |
Аминопропионат |
|
Название альдегида |
Структурная формула |
Систематическое название |
|
Формальдегид |
HCOH |
Метаналь |
|
Ацетальдегид |
CH3COH |
Этаналь |
| Название радикала | Структурная форма радикала |
| Изопропил | 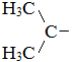 |
| Бензил |  |
| Винил | H2C = CH — |
А также вы можете получить доступ ко всем видео-урокам, заданиям реального ЕГЭ, ЦТ и РТ с подробными видео-объяснениями, задачам и всем материалам сайта кликнув здесь «Получить все материалы сайта»
Александр Коньков, автор и основатель первого в СНГ проекта по видео-подготовке к ЦТ и ЕГЭ по химии «Your System Education»
Home
Expert solutions
Тривиальные названия неорганических веществ
5.0 (8 reviews)
Term
KClO3
Click the card to flip 👆
Created by
mayer_him
Тривиальные названия для ЕГЭ и олимпиад(!)
Terms in this set (120)
KClO3
бертолетова соль
K4[Fe(CN)6]
гексацианоферрат(II) калия, жёлтая кровяная соль, ферроцианид
FeS2
пирит, железный колчедан, серный колчедан
K3[Fe(CN)6]
гексацианоферрат(III) калия, красная кровяная соль, феррицианид
Fe(CNS)3
тиоционат железа(III)
SiH4
силан
NH3
аммиак
PH3
фосфин
H2S
сероводород
COCl2
фосген
Students also viewed
Науки в Биологии
51 terms
zhanna_kazanskayaTeacher
Видоизменения в ботанике
47 terms
zhanna_kazanskayaTeacher
Ботаника Представители (названия) мг 04.09
32 terms
zhanna_kazanskayaTeacher
Ботаника Представители водорослей
18 terms
zhanna_kazanskayaTeacher
Recent flashcard sets
Photosynthesis
8 terms
Purple-HeartDaDragon
Globalization
6 terms
auser1234566
Accessory Proteins
7 terms
Danaals6
chapter 3
31 terms
tropical432
Sets found in the same folder
Кислоты, кислотные остатки и с.о.
56 terms
mayer_him
Кристаллические решётки
48 terms
mayer_him
Химические связи
32 terms
mayer_him
Агрегатные состояния неорганических веществ
155 terms
mayer_him
Other sets by this creator
Механизмы реакций в органической химии
8 termsImages
mayer_him
Галогенирование органических веществ
10 termsImages
mayer_him
Окисление кислородсодержащих органических вещ…
11 termsImages
mayer_him
Специфические свойства кислородсодержащих орг…
19 termsImages
mayer_him
Other Quizlet sets
Chapter 9
34 terms
Mikey_Disbennett
PLSC Midterm 2
72 terms
chasevecc
DH 229 Exam 1 (Introduction to Oral Pathology…
50 termsImages
Kittystar22
Python 3220 Chapter 5
20 termsImages
skylernunn8
1
/
5