Всего: 148 1–20 | 21–40 | 41–60 | 61–80 …
Добавить в вариант
При взаимодействии 1,74 г алкана с бромом образовалось 4,11 г монобромпроизводного. Определите молекулярную формулу алкана.
При взаимодействии одного и того же количества алкена с различными галогеноводородами образуется соответственно 7,85 г хлорпроизводного или 12,3 г бромпроизводного. Определите молекулярную формулу алкена.
Неизвестный алкен массой 5,04 г полностью обесцвечивает 100 г 9,6%-го раствора брома в тетрахлорметане. Найдите молекулярную формулу алкена.
При окислении 5,6 л (н. у.) алкена холодным водным раствором перманганата калия образовалось 22,5 г двухатомного спирта. Реакция окисления идёт со 100%-м выходом. Установите молекулярную формулу алкена.
Установите молекулярную формулу алкена, если известно, что 0,5 г его способны присоединить 200 мл (н. у.) водорода.
Установите молекулярную формулу алкена, если известно, что 1,5 г его способны присоединить 600 мл (н. у.) хлороводорода.
Определите молекулярную формулу алкена, если известно, что одно и то же количество его, взаимодействуя с различными галогеноводородами, образует, соответственно, или 5,23 г хлорпроизводного, или 8,2 г бромпроизводного.
При взаимодействии алкана с хлором при освещении образовалось 22,6 г дихлорпроизводного и 14,6 г хлороводорода. Найдите молекулярную формулу алкана.
Неизвестный алкен массой 1,96 г способен вступить в химическую реакцию с 2,56 г хлороводорода. Определите молекулярную формулу неизвестного алкена.
Неизвестный алкен массой 16,8 г способен присоединить 64 г брома. Определите молекулярную формулу неизвестного алкена.
Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1) алканы
2) алкены
3) алкадиены
4) циклоалканы
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите молекулярную формулу алкена, образовавшегося в результате взаимодействия спиртового раствора щёлочи с соответствующим монобромалканом, относительная плотность которого по воздуху равна 4,24.
Какие алкены реагируют с водой в соответствии с правилом Марковникова?
1) пропен
2) этен
3) бутен-2
4) бутен-1
5) 2,3-диметилбутен-2
6) 2-метилбутен-2
Источник: ЕГЭ по химии 10.06.2013. Основная волна. Сибирь. Вариант 2
Установите соответствие между общей формулой гомологического ряда и классом (группой) органических соединений, соответствующим этой формуле: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
1) альдегиды
2) алкены
3) одноатомные фенолы
4) карбоновые кислоты
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) многоатомные спирты
Б) одноатомные спирты
В) карбоновые кислоты
Г) алкены
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО
ОПРЕДЕЛЕНИЯ
1) аммиачный раствор оксида серебра
2) карбонат натрия
3) оксид меди (II)
4) бромная вода
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) алкадиены
Б) одноатомные спирты
В) карбоновые кислоты
Г) алкены
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО
ОПРЕДЕЛЕНИЯ
1) аммиачный раствор оксида серебра
2) гидрокарбонат натрия
3) оксид меди (II)
4) бромная вода
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите все вещества, способные окислять алкены.
Запишите номера выбранных ответов в порядке возрастания.
Установите соответствие между структурной формулой вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СТРУКТУРНАЯ ФОРМУЛА
КЛАСС/ГРУППА
1) алканы
2) алкены
3) циклоалканы
4) арены
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между формулой вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
СТРУКТУРНАЯ ФОРМУЛА ВЕЩЕСТВА
КЛАСС/ГРУППА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1) алканы
2) алкены
3) циклоалкены
4) алкадиены
Запишите в таблицу выбранные цифры под соответствующими буквами.
Установите соответствие между формулой вещества и его принадлежностью к определённому(-ой) классу (группе) органических соединений.
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
1) алкины
2) амины
3) простые эфиры
4) арены
5) алканы
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Всего: 148 1–20 | 21–40 | 41–60 | 61–80 …
Алкены. Тематические задания для подготовки к ЕГЭ.
Алкены. Тестовые задания с выбором двух вариантов ответа.
Задание №1
Выберите два утверждения, справедливые для алкенов:
1) встречаются в природе
2) вступают в реакции присоединения
3) способны обесцвечивать бромную воду
4) все алкены при нормальных условиях является жидкостями
5) при гидролизе карбида кальция образуется алкен
Решение
Ответ: 23
Задание №2
Выберите два утверждения, которые справедливы и для этана, и для этилена:
1) при нормальных условиях являются газами
2) взаимодействуют с бромом
3) входят с состав природного газа
4) обесцвечивают водный раствор перманганата калия
5) реагируют с натрием
Решение
Ответ: 12
Задание №3
Выберите два утверждения, которые справедливы и для этана и для этилена:
1) имеют структурные изомеры
2) все атомы углерода в молекулах находятся в состоянии sp2— гибридизации
3) могут быть получены друг из друга в одну стадию
4) плохо растворимы в воде
5) вступают в реакцию с бромной водой
Решение
Ответ: 34
Задание №4
Выберите два утверждения, которые справедливы и для этена, и для пентена:
1) при нормальных условиях являются жидкостями
2) все атомы углерода в молекулах находятся в состоянии sp2— гибридизации
3) имеют общую формулу CnH2n
4) существуют в виде цис- и транс-изомеров
5) при взаимодействии с водным раствором перманганата калия образуют гликоли
Решение
Ответ: 35
Задание №5
Выберите два утверждения, которые справедливы и для этилена, и для бутена-1:
1) в молекулах есть атомы углерода в состоянии sp2-гибридизации
2) имеют межклассовые изомеры
3) являются гомологами
4) молекулы имеют плоское строение
5) при нормальных условиях представляют собой жидкости
Решение
Ответ: 13
Задание №6
Выберите два утверждения, которые справедливы и для пропена, и для бутена-2:
1) в молекулах есть фрагменты тетраэдрической формы
2) имеют межклассовые изомеры
3) хорошо растворимы в воде
4) в молекулах есть атомы углерода в состоянии sp-гибридизации
5) входят в состав природного газа
Решение
Ответ: 12
Задание №7
Выберите два утверждения, которые справедливы и для пропена, и для бутена-2:
1) реагируют со спиртовым раствором гидроксида натрия
2) имеют межклассовые изомеры среди алкинов
3) имеют структурные изомеры
4) могут существовать в виде цис— и транс -изомеров
5) при гидрировании образуют алканы
Решение
Ответ: 35
Задание №8
Из предложенного перечня реакций, выберите две таких, в которые может вступать этилен:
1) гидролиз
2) дегидрирование
3) гидрирование
4) дегидратация
5) изомеризация
Решение
Ответ: 23
Задание №9
Из предложенного перечня, выберите два таких типа реакций, в которые могут вступать все алкены:
1) окисления
2) обмена
3) дегидратации
4) присоединения
5) изомеризации
Решение
Ответ: 14
Задание №10
Из предложенного перечня, выберите два таких типа реакций, которые не характерны для алкенов:
1) окисления
2) обмена
3) гидратации
4) дегидрогалогенирования
5) полимеризации
Решение
Ответ: 24
[adsp-pro-3]
Задание №11
Выберите два утверждения, которые справедливы для этилена:
1) при нормальных условиях является газом с резким запахом
2) продуктом его полимеризации является каучук
3) образуется при дегидрировании ацетилена
4) продукт его окисления используют в качестве антифриза
5) присоединяет хлороводород
Решение
Ответ: 45
Задание №12
Выберите два утверждения, которые справедливы и для этилена, и для бутена-1:
1) вступают в реакцию как с бромом, так и с бромной водой
2) при гидрировании образуют алкины
3) вступают в реакции гидратации
4) не обесцвечивают раствор перманганата калия
5) имеют общую формулу CnH2n-2
Решение
Ответ: 13
Задание №13
Из предложенного перечня выберите два вещества, которые могут существовать в виде цис- и транс-изомеров
1) этилен
2) 3-метилпентен-2
3) 3-метилпентен-1
4) 2-хлорбутен-2
5) бутен-1
Решение
Ответ: 24
Задание №14
Из предложенного перечня выберите два вещества , которые являются структурными изомерами пентена-2
1) гексен-2
2) метилциклопентан
3) этилциклопропан
4) бутен-2
5) 2-метилбутен-1
Решение
Ответ: 35
Задание №15
Из предложенного перечня выберите два вещества , которые являются структурными изомерами пентена-1
1) пентен-2
2) циклопентен
3) 2,3-диметилбутен-2
4) пентан
5) 1,2-диметилциклопропан
Решение
Ответ: 15
Задание №16
Из предложенного перечня выберите два вещества, которые являются структурными изомерами для бутена-2
1) пентен-2
2) метилциклобутан
3) метилциклопропан
4) метилпропен
5) бутин-2
Решение
Ответ: 34
Задание №17
Из предложенного перечня выберите два геометрических изомера, в форме которых может существовать гексен-2:
1) транс-гексен-2
2) гексен-3
3) циклопентан
4) цис-гексен-2
5) гексин-2
Решение
Ответ: 14
Задание №18
Из предложенного перечня выберите два вещества, которые являются гомологами пентена-2
1) бутин-2
2) пентин-1
3) гексен-2
4) бутен-2
5) гептин-2
Решение
Ответ: 34
Задание №19
Из предложенного перечня выберите два вещества, которые являются гомологами бутена-1
1) циклобутан
2) этилен
3) 2-метилпропен
4) пентен-2
5) пропилен
Решение
Ответ: 25
Задание №20
Выберите два утверждения, которые справедливы и для этилена, и для бутена-1:
1) вступают в реакцию с галогеноводородами по правилу Марковникова
2) являются гомологами пропена
3) не способны образовывать пространственных изомеров
4) вступают в реакцию с аммиачным раствором оксида серебра
5) все атомы углерода в молекулах находятся в состоянии sp2— гибридизации
Решение
Ответ: 23
[adsp-pro-3]
Задание №21
Среди представленных формул выберите две, которые могут соответствовать алкенам:
- 1. С2Н2
- 2. С3Н4
- 3. С3Н6
- 4. С2Н4
- 5. С2Н6
Решение
Ответ: 34
Задание №22
Из предложенного перечня выберите два вещества, которые относятся к классу алкенов.
1) СН3-СН=СН-СН=СН2
2) СН3-С≡СН
3) СН3-СН=СН2
4) СН3-СН2-СН3
5) СН2=СН2
Решение
Ответ: 35
Задание №23
Из предложенного перечня реакций, выберите две таких, в которые может вступать этилен:
1) взаимодействие с бромоводородом
2) взаимодействие c водным раствором гидроксида натрия
3) взаимодействие с раствором хлорида натрия
4) взаимодействие с аммиачным раствором хлорида меди (I)
5) каталитическое окисление
Решение
Ответ: 15
Задание №24
Из предложенного перечня реагентов выберите два таких, с каждым из которых реагирует этен:
1) металлический натрий
2) раствор бромной воды
3) этан
4) серная кислота
5) водород
Решение
Ответ: 25
Задание №25
Среди перечисленных, выберите два вещества, которые не относятся к классу алкенов
1) СН3-СН=СН-СН=СН2
2) СН3-СН2-СН2-СН=СН2
3) СН3-СН=СН2
4) СН3-С≡СН
5) СН2=СН2
Решение
Ответ: 14
Задание №26
Из предложенного перечня веществ выберите два, которые не могут образоваться при окислении этилена:
1) пропиленгликоль
2) этаналь
3) этан
4) этиленгликоль
5) карбонат калия
Решение
Ответ: 13
Задание №27
Из предложенного перечня веществ выберите два, которые могут образоваться в реакциях окисления этилена:
1) диметиловый эфир
2) метаналь
3) карбонат натрия
4) этанол
5) углекислый газ
Решение
Ответ: 35
Задание №28
Из предложенного перечня веществ выберите два, которые могут образоваться в реакциях окисления этилена:
1) этаналь
2) метанол
3) этандиол-1,2
4) карбид кальция
5) ацетат калия
Решение
Ответ: 13
Задание №29
Из предложенного перечня веществ выберите два, которые могут образоваться при окислении пропена:
1) этанол
2) этаналь
3) этановая кислота
4) этиленгликоль
5) пропиленгликоль
Решение
Ответ: 35
Задание №30
Из предложенного перечня веществ выберите два, которые могут образоваться при окислении пропена:
1) этанол
2) этановая кислота
3) этаналь
4) этиленгликоль
5) ацетат калия
Решение
Ответ: 25
[adsp-pro-3]
Задание №31
Из предложенного перечня продуктов, которые могут образоваться при окислении пропена:
1) пропандиол-1,2
2) этаналь
3) этиленгликоль
4) ацетат и карбонат калия
5) этанол
Решение
Ответ: 14
Задание №32
Из предложенного перечня выберите два вещества, которые существуют в виде цис-, транс-изомеров
1) пентен-2
2) пентен-1
3) пентин-2
4) 2,3-диметилбутен-2
5) бутен-2
Решение
Ответ: 15
Задание №33
Из предложенного перечня веществ выберите две реакции, которые являются качественными на двойную связь:
1) взаимодействие с металлическим натрием
2) взаимодействие с аммиачным раствором хлорида меди (I)
3) обесцвечивание бромной воды
4) обесцвечивание раствора перманганата калия
5) взаимодействие с аммиачным раствором оксида серебра
Решение
Ответ: 34
Задание №34
Как метан, так и этилен могут вступать в реакции
1) гидрирования
2) галогенирования
3) горения
4) гидратации
5) полимеризации
Решение
Ответ: 23
Задание №35
Из предложенного перечня реакций, выберите две таких, в которые может вступать пропен:
1) гидролиз
2) дегидроциклизация
3) гидрирование
4) гидратация
5) изомеризация
Решение
Ответ: 34
Задание №36
Из предложенного перечня выберите две пары реагентов, среди которых есть вещество не реагирующее с этиленом:
- 1. Cl2, H2
- 2. Cu(OH)2, Br2
- 3. Cl2, O2
- 4. O2, KMnO4
- 5. HCl, [Ag(NH3)2]OH
Решение
Ответ: 25
Задание №37
Из предложенного перечня реакций, выберите две таких, в которые может вступать как пропен, так и бутан:
1) окисление раствором перманганата калия
2) дегидрирование
3) изомеризация в присутствии AlCl3
4) полимеризация
5) каталитическое окисление
Решение
Ответ: 25
Задание №38
Из предложенного перечня выберите два реагента, с каждым из которых не реагирует пропан, но реагирует этилен:
- 1. HCl
- 2. Cl2
- 3. Н2О
- 4. O2
- 5. N2
Решение
Ответ: 13
Задание №39
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получен пропен:
1) взаимодействие хлорэтана с натрием
2) взаимодействие 1-хлорпропана с водным раствором щелочи
3) гидрирование пропана
4) внутримолекулярная дегидратация пропанола -1
5) взаимодействие 2-хлорпропана со спиртовым раствором щелочи
Решение
Ответ: 45
Задание №40
Из предложенного перечня реакций выберите две таких, которые приводят к образованию бутена-1:
1) взаимодействие бутанола-2 с концентрированной серной кислотой при температуре более 140oС
2) реакция 1,2-дихлорбутана с водным раствором щелочи
3) гидрирование изопрена
4) взаимодействие 1-хлорбутана со спиртовым раствором гидроксида калия при нагревании
5) взаимодействие 1,2-дибромбутана с цинком при нагревании
Решение
Ответ: 45
[adsp-pro-3]
Задание №41
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получен этилен:
1) взаимодействие хлорэтана с натрием
2) взаимодействие хлорэтана с водным раствором щелочи
3) внутримолекулярная дегидратация этанола
4) взаимодействие 1,2-дихлорэтана со спиртовым раствором щелочи
5) взаимодействие хлорэтана со спиртовым раствором щелочи
Решение
Ответ: 35
Задание №42
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получен этилен:
1) дегидрирование этана
2) взаимодействие бромэтана с водным раствором щелочи
3) межмолекулярная дегидратация этанола
4) взаимодействие 1,2-дибромэтана с цинком
5) взаимодействие 1,1-дихлорэтана со спиртовым раствором щелочи
Решение
Ответ: 14
Задание №43
Из предложенного перечня выберите два вещества, с которыми реагируют алкены:
- 1. Br2 (р-р)
- 2. Na
- 3. Н2О (Н+)
- 4. [Cu(NH3)2]OH
- 5. С3Н8
Решение
Ответ: 13
Задание №44
Из предложенного перечня выберите два вещества, с которыми может вступать в реакцию пропен:
- 1. NaOH
- 2. С2Н6
- 3. СН2=СН-СН3
- 4. HBr
- 5. АlCl3
Решение
Ответ: 34
Задание №45
Из предложенного перечня реакций, выберите две таких, которые протекают в соответствии с правилом В.В. Марковникова:
1) пентана с бромом
2) пропена с водородом
3) бромной воды с этеном
4) бромоводорода с пропеном
5) бутена-1 с водой
Решение
Ответ: 45
Задание №46
Взаимодействие пропена и хлороводорода протекает
1) с преимущественным образованием 1-хлорпропана
2) по цепному радикальному механизму
3) с промежуточным образованием частицы СН3-СН+-СН3
4) с разрывом π-связи в молекуле пропена
5) с образованием 1,2-дихлорпропана
Решение
Ответ: 34
Задание №47
Из предложенного перечня выберите два утверждения, которые справедливы в отношении взаимодействия бутена-1 с бромоводородом:
1) в ходе реакции преимущественно образуется 1,2-дибромбутан
2) реакция протекает по правилу В.В. Марковникова
3) реакция протекает по правилу A.M. Зайцева
4) в ходе реакции преимущественно образуется 2-бромбутан
5) реакция идёт по радикальному механизму
Решение
Ответ: 24
Задание №48
Среди перечисленных реакций выберите две, в ходе которых происходит промежуточное образование карбокатиона СН3-СН+-СН3
1) образуется при реакции пропена с кислородом воздуха
2) образуется при присоединении бромоводорода к молекуле пропена
3) образуется при хлорировании пропана
4) образуется при присоединении воды к молекуле пропена
5) образуется при присоединении водорода к молекуле пропана
Решение
Ответ: 24
Задание №49
Среди перечисленных, выберите две реакции, протекающие по ионному механизму
1) этана и кислорода
2) пропена и бромоводорода
3) пропена и хлора при нагревании 500°С
4) этилена с раствором бромной воды
5) метана и азотной кислоты
Решение
Ответ: 24
Задание №50
Среди перечисленных реакций выберите две, которые протекают против правила Марковникова:
1) хлороводорода с 6,6,6-трифторгексеном-1
2) акриловой кислоты с хлороводородом
3) бромоводорода с 3,3,3-трихлорпропеном
4) бромоводорода с пропеном
5) бутена-1 с водой
Решение
Ответ: 23
[adsp-pro-3]
Задание №51
Среди перечисленных реакций выберите две, которые протекают против правила Марковникова:
1) 3,3,3-трихлорпропена и хлороводорода
2) пропена с водой
3) этилена с бромоводородом
4) бромоводорода с пропеном в присутствии перекиси водорода
5) бутена-1 с водой
Решение
Ответ: 14
Задание №52
Среди перечисленных реакций выберите две, которые протекают против правила Марковникова
1) CH3-CH=CH2 + HCl →
2) CH2=CH-CCl3 + HCl →
3) CH2=CH-C(O)H + HCl →
4) CH3-CH=CH-CH2-CH3 + H2O →
5) CH3-CH=CH2 + H2O →
Решение
Ответ: 23
Задание №53
Из предложенного перечня утверждений выберете два таких, которые справедливы для характеристики взаимодействия бутена-1 с бромоводородом:
1) реакция протекает по правилу В.В. Марковникова
2) реакция протекает по правилу A.M. Зайцева
3) с разрывом σ-связи в молекуле пропена
4) в ходе реакции преимущественно образуется 1-бромбутан
5) реакция идёт по ионному механизму
Решение
Ответ: 15
Алкены. Задания на установление соответствия.
Задание №1
Установите соответствие между названием алкена и основным продуктом его взаимодействия с хлороводородом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| АЛКЕН | ПРОДУКТ ГИДРОХЛОРИРОВАНИЯ |
|
А) пропен В) 2-метилпропен Г) 2,3-диметилбутен-1 Д) 2,3-диметилбутен-2 |
1) 2-метил-2-хлорбутан 2) 1-хлорпропан 3) 2,3-диметил-2-хлорбутан 4) 2-хлорпропан 5) 2,3-диметил-2,3-дихлорбутан 6) 2-метил-2-хлорпропан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 4633
Задание №2
Установите соответствие между названием соединения с двойной связью в молекуле и основным продуктом его взаимодействия с хлороводородом: к каждой позиции, обозначенной буквой, подберите соответ ствующую позицию, обозначенную цифрой.
| СОЕДИНЕНИЕ | ПРОДУКТ ГИДРОХЛОРИРОВАНИЯ |
|
А) 3,3,3-трихлорпропен Б) 2-метилпропен В) бутен-1 Г) 1,4-дихлорбутен-2 |
1) 1,1,1,3-тетрахлорпропан 2) 1-хлор-2-метилпропан 3) 2-хлор-2-метилпропан 4) 1,2,4-трихлорбутан 5) 1-хлобутан 6) 2-хлорбутан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 1364
Задание №3
Установите соответствие между названием алкена и основным продуктом его взаимодействия с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| АЛКЕН | ПРОДУКТ ГИДРАТАЦИИ |
|
А) этен Б) пропен В) бутен-1 Г) бутен-2 |
1) пропанол-1 2) этаналь 3) этанол 4) пропанол-2 5) бутанол-1 6) бутанол-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 3466
Задание №4
Установите соответствие между названием алкена и основным продуктом его взаимодействия с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| АЛКЕН | ПРОДУКТ ГИДРАТАЦИИ |
|
А) 2,3-диметилбутен-1 Б) 2,3-диметилбутен-2 В) 2-метилбутен-1 Г) 3,3-диметилбутен-1 |
1) 2,3-диметилбутанол-2 2) 2,2-диметилбутанол-2 3) 2-метилбутанол-1 4) 2,2-диметилбутанол-3 5) 2-метилбутанол-2 6) 3,3-диметилбутанол-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 1156
Задание №5
Установите соответствие между названием алкена и основным продуктом его взаимодействия с водой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| АЛКЕН | ПРОДУКТ ГИДРАТАЦИИ |
|
А) 3-метилпентен-1 Б) 2-метилбутен-1 В) пентен-1 Г) 3,3-диметилбутен-1 |
1) 3-метилпентанол-2 2) 2-метилбутанол-2 3) пентанол-1 4) пентанол-2 5) 2,2-диметилбутанол-3 6) 3,3-диметилбутанол-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 1246
[adsp-pro-3]
Задание №6
Установите соответствие между названием спирта и продуктом его внутримолекулярной дегидратации: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СПИРТ | ПРОДУКТ ДЕГИДРАТАЦИИ |
|
А) пропанол-2 Б) пропанол-1 В) бутанол-1 Г) этанол |
1) бутен-1 2) пропен 3) этилен 4) этан 5) бутен-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 2213
Задание №7
Установите соответствие между названием спирта и продуктом его внутримолекулярной дегидратации: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СПИРТ | ПРОДУКТ ДЕГИДРАТАЦИИ |
|
А) пропанол-2 Б) пропанол-1 В) бутанол-1 Г) бутанол-2 |
1) бутен-2 2) пропан 3) бутен-1 4) пропен 5) бутан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 4431
Задание №8
Установите соответствие между названием спирта и продуктом его внутримолекулярной дегидратации: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СПИРТ | ПРОДУКТ ДЕГИДРАТАЦИИ |
|
А) 2-метилпропанол-2 Б) 2,4-диметилпентанол-3 В) 3-метилбутанол-2 Г) 2-метилбутанол-2 |
1) 2,4-диметилпентен-3 2) 3-метилбутен-2 3) 2-метилпропен 4) 2,4-диметилпентен-2 5) 2-метилбутен-2 6) 2,4-диметилпентен-1 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 3455
Задание №9
Установите соответствие между моногалогеналканом и продуктом его взаимодействия со спиртовым раствором щелочи при нагревании:к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| МОНОГАЛОГЕНАЛКАН | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) хлорэтан Б) 2-хлорпропан В) 2-хлор-2-метилпропан Г) 2-бромбутан |
1) пропилен 2) этилен 3) бутен-1 4) 2-метилпропен 5) бутен-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 2145
Задание №10
Установите соответствие между моногалогеналканом и продуктом его взаимодействия со спиртовым раствором щелочи: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТЫ | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
А) 1-бром-3,3-диметилбутан Б) 2-хлор-2,3-диметилбутан В) 1-хлор-2-метилпропан Г) 1-бром-3-метилбутан |
1) 2,3-диметилбутен-1 2) 2-бромбутен-3 3) 2-метилпропен 4) 2,3-диметилбутен-2 5) 3,3-диметилбутен-1 6) 3-метилбутен-1 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 5436
[adsp-pro-3]
Задание №11
Установите соответствие между схемой реакции и органическим веществом образующимися при их взаимодействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТЫ | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
|
1) 2,2-диметилбутен-3 2) пропин 3) 3,3-диметилбутен-1 4) пропен 5) 2-метилбутен-1 6) 2-метилбутен-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 4463
Задание №12
Установите соответствие между названием алкена и продуктом, который образуется при его окислении подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТ | ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
А) пропилен Б) бутен-1 В) бутен-2 Г) пентен-2 |
1) пропаналь 2) пропионовая и уксусная кислоты 3) пропановая кислота и оксид углерода (IV) 4) уксусная кислота и углекислый газ 5) уксусная кислота 6) пропановая кислота |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 4352
Задание №13
Установите соответствие между названием алкена и продуктом, который образуется при его окислении подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТ | ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
А) 2-метилпропен Б) этен В) бутен-2 Г) 2-метилбутен-2 |
1) пропанон и оксид углерода (IV) 2) пропанон и уксусная кислота 3) пропановая кислота и оксид углерода (IV) 4) уксусная кислота и углекислый газ 5) уксусная кислота 6) оксид углерода (IV) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 1652
Задание №14
Установите соответствие между формулой алкена и продуктом(ами) , который образуется при окислении: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТ | ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
|
1) уксусная кислота и углекислый газ 2) оксид углерода (IV) 3) пропандиол-1,2 4) ацетат калия и карбонат калия 5) уксусная кислота 6) этиленгликоль |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 4642
[adsp-pro-3]
Цепочки на алкены.
Задание №1
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
CH3-CH2-Cl X1
X2
X3
X4
X5
X6
Решение
Задание №2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
Решение
Задание №3
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
бутен-1 2-хлорбутан
бутен-2
бутанол-2
бутен-2
бутандиол-2,3
Решение
Задание №4
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
метан бромметан
этан
хлорэтан
этилен
этанол
дивинил
Решение
Задание №5
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
этан X1
C4H10
X2
CH3-CH=CH-CH3
C2H4O2
Решение
[adsp-pro-3]
Задание №6
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
Решение
Задание №7
Напишите уравнения реакций, в соответствии с которыми можно осуществить следующие превращения:
циклобутан X1
X2
X3
X4
X5
X6
Решение
Задание №8
При сжигании навески неизвестного углеводорода образовалось 11,2 л углекислого газа (н.у.) и 9 г паров воды. Плотность паров вещества по этилену равна 3. Определите молекулярную формулу углеводорода и его структуру, если известно, что оно обесцвечивает бромную воду и содержит четвертичный атом углерода.
Решение
Вычислим количество вещества углекислого газа, воды и углерода и водорода соответственно:
n(CO2) = n(C) = V/Vm = 11,2 л/22,4 л/моль = 0,5 моль;
n(H2O) = m/M = 9 г/18 г/моль = 0,5 моль, n(H) = 2n(H2O) = 0,5 моль ⋅ 2 = 1 моль.
Мольное соотношение углерода и водорода запишем в виде x : y = 0,5 : 1 = 1 : 2.
Простейшая формула данного углеводорода CH2, где M(CH2) = 14 г/моль.
Обозначим формулу углеводорода как CxHy и вычислим ее молекулярную массу:
M(CxHy) = DCH2=CH2 ⋅ M(C2H4) = 3 ⋅ 28 г/моль = 84 г/моль.
M(CxHy) : M(CH2) = 6, следовательно, молекулярная формула углеводорода — это C6H12.
Структурная формула данного соединения (3,3-диметилбутен-1):
Задание №9
При сжигании навески неизвестного углеводорода образовалось 5,6 л углекислого газа (н.у.) и 4,5 г паров воды. Плотность паров вещества равна 2,5 г/л. Определите молекулярную формулу углеводорода и его структуру, если известно, что его молекула реагирует с бромоводородом с образованием третичного галогенпроизводного.
Решение
Вычислим количество вещества углекислого газа, воды и углерода и водорода соответственно:
n(CO2) = n(C) = V/Vm = 5,6 л/22,4 л/моль = 0,25 моль;
n(H2O) = m/M = 4,5 г/18 г/моль = 0,25 моль, n(H) = 2n(H2O) = 0,25 моль ⋅ 2 = 0,5 моль.
Мольное соотношение углерода и водорода запишем в виде x : y = 0,25 : 0,5 = 1 : 2.
Простейшая формула данного углеводорода CH2, где M(CH2) = 14 г/моль.
Обозначим формулу углеводорода как CxHy и вычислим ее молекулярную массу:
M(CxHy) = p(CxHy) ⋅ Vm = 2,5 г/л ⋅ 22,4 л/моль = 56 г/моль.
M(CxHy) : M(CH2) = 4, следовательно, молекулярная формула углеводорода — это C4H8.
Поскольку молекула углеводорода реагирует с бромоводородом с образованием третичного галогенпроизводного, то исходным углеводородом является
Задание №10
При сжигании навески неизвестного углеводорода образовалось 33 г углекислого газа и 16,8 л паров воды (н.у.). Плотность вещества по аммиаку равна 3,29. Определите молекулярную формулу углеводорода и его структуру, если известно, что его молекула может существовать в виде двух геометрических изомеров.
Решение
Вычислим количество вещества углекислого газа, воды и углерода и водорода соответственно:
n(CO2) = n(C) = m/M = 33 г/44 г/моль = 0,75 моль;
n(H2O) = V/Vm = 16,8 л/22,4 л/моль = 0,75 моль, n(H) = 2n(H2O) = 0,75 моль ⋅ 2 = 1,5 моль.
Мольное соотношение углерода и водорода запишем в виде x : y = 0,75 : 1,5 = 1 : 2.
Простейшая формула данного углеводорода CH2, где M(CH2) = 14 г/моль.
Обозначим формулу углеводорода как CxHy и вычислим ее молекулярную массу:
M(CxHy) = DNH3 ⋅ M(NH3) = 3,29 ⋅ 17 г/моль ≈ 56 г/моль.
M(CxHy) : M(CH2) = 4, следовательно, молекулярная формула углеводорода — это C4H8.
Поскольку молекула вещества может существовать в виде двух геометрических изомеров, данным веществом является бутен-2 (бутен-2 может существовать в виде цис— и транс-изомеров):
[adsp-pro-3]
Задание №11
При сжигании навески неизвестного углеводорода образовалось 3,36 л углекислого газа (н.у.) и 2,025 г паров воды. Плотность вещества по гелию равна 13,5. Определите молекулярную формулу углеводорода и его структуру, если известно, что оно не реагирует с аммиачным раствором оксида серебра и способно к 1,4-присоединению.
Решение
Вычислим количество вещества углекислого газа, воды и углерода и водорода соответственно:
n(CO2) = n(C) = V/Vm = 3,36 л/22,4 л/моль = 0,15 моль;
n(H2O) = m/M = 2,025 г/18 г/моль = 0,1125 моль; n(H) = 2n(H2O) = 0,1125 моль ⋅ 2 = 0,225 моль.
Мольное соотношение углерода и водорода запишем в виде x : y = 0,15 : 0,225 = 2 : 3.
Простейшая формула данного углеводорода C2H3, где M(C2H3) = 27 г/моль.
Обозначим формулу углеводорода как CxHy и вычислим ее молекулярную массу:
M(CxHy) = DHe ⋅ M(He) = 13,5 ⋅ 4 г/моль ≈ 54 г/моль.
M(CxHy) : M(C2H3) = 2, следовательно, молекулярная формула углеводорода — это C4H6.
Поскольку вещество не реагирует с аммиачным раствором оксида серебра и способно к 1,4-присоединению, данным веществом является 1,3-бутадиен.
Задание №12
При сжигании навески неизвестного углеводорода массой 1,7 г образовалось 5,5 г углекислого газа. Плотность паров вещества равна 3,036 г/л. Определите молекулярную формулу углеводорода и его структуру, если известно, что оно не реагирует с аммиачным раствором оксида серебра, способно к 1,4-присоединению и является изомером изопрена.
Решение
Вычислим массу и количество вещества углекислого газа и углерода соответственно:
n(CO2) = n(C) = m/M = 5,5 г/44 г/моль = 0,125 моль; m(C) = M ⋅ n = 12 г/моль ⋅ 0,125 моль = 1,5 г;
m(H) = m(орг. в-ва) — m(C) = 1,7 г — 1,5 г = 0,2 г; n(H) = m/M = 0,2 г/1 г/моль = 0,2 моль.
Мольное соотношение углерода и водорода запишем в виде x : y = 0,125 : 0,2 = 5 : 8.
Простейшая формула данного углеводорода C5H8, где M(C5H8) = 68 г/моль.
Обозначим формулу углеводорода как CxHy и вычислим ее молекулярную массу:
M(CxHy) = p ⋅ Vm = 3,036 г/л ⋅ 22,4 л/моль = 68 г/моль.
M(CxHy) : M(C5H8) = 1, следовательно, молекулярная формула углеводорода — это C5H8.
не реагирует с аммиачным раствором оксида серебра, способно к 1,4-присоединению и является изомером изопрена, данным веществом является пентадиен-1,3.
Задание №13
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
CH3-CH2-CH3 X1
X2
X3
X2
X4
Решение
Задание №14
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этилен 1,2-дибромэтан
этилен
этанол
этилен
этиленгликоль
Решение
[adsp-pro-10]
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 1.
А1. Общая формула алкенов:
1) CnH2n 2) CnH2n+2 3) CnH2n-2 4) CnH2n-6.
А2. Молекулярная формула пентина:
1) С5Н12 2) С4Н8 3) С5Н8 4) С6Н6.
А3. Число атомов водорода в молекуле гексадиена:
1) 8 2) 10 3) 12 4) 14.
А4. Число -связей в молекуле пропена:
1) 1 2) 3 3) 6 4) 8.
А5. Реакции, присоединения галогеноводородов к непредельным углеводородам, называются реакциями:
1) галогенирования 2) гидрогалогенирования
3) гидрирования 4) гидратации.
А6. Нагревание натурального каучука с серой и различными наполнителями называют:
1) эластичностью 2) полимеризацией
3) гидратацией 4) вулканизацией.
А7. При взаимодействии бутена-1 с хлороводородом образуется:
1) 1-хлорбутан 2) 2-хлорбутан
3) 1,2-дихлорбутан 4) бутан.
А8. В промышленности ацетилен получают:
- дегидрогалогенированием дигалогеноалканов
- дегидродимеризация (пиролиз) метана
- реакцией Вюрца
- разложением карбида алюминия.
Б1. Валентный угол между sp2-гибридными орбиталями равен … .
Б2. Написать структурные формулы: гексен-3, 3-хлорпентадиен-1,4, 3-метилбутин-1.
Б3. Осуществить превращения, назвать органические вещества, указать условия реакций:
С2Н2 — С2Н4 — С2Н5Br — С4Н10
С1. Построить изомеры гексадиену-1,2, используя разные виды изомерии, дать им названия.
С2. Выведите формулу газообразного соединения, массовая доля азота в котором 82,36%, а водорода – 17,64%. Относительная плотность по водороду 8,5.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 2.
А1. Общая формула алкадиенов:
1) CnH2n 2) CnH2n+2 3) CnH2n-2 4) CnH2n-6.
А2. Молекулярная формула гептена:
1) С6Н14 2) С7Н14 3) С6Н12 4) С7Н16.
А3. Число атомов углерода в молекуле ацетилена:
1) 2 3) 4 3) 6 4) 8.
А4. Число — связей в молекуле пентадиен-1,3:
1) 2 3) 4 3) 6 4) 8.
А5. Присоединение водорода к молекулам непредельных углеводородов, называют реакциями:
1) галогенирования 2) гидрогалогенирования
3) гидрирования 4) гидратации.
А6. Качественной реакцией на непредельные углеводороды является взаимодействие с:
1) бромной водой 2) хлороводородом
3) металлическим натрием 4) нет правильного ответа.
А7. При взаимодействии бутина-2 с одной молекулой брома образуется:
1) 2-бромбутен-2 2) 1,2-дибромбутан
3) 2,3-дибромбутан 4) 2,3-дибромбутен-2.
А8. Этилен в лаборатории получают:
- карбидным способом
- термический крекинг алканов
- дегидрирование алканов
- дегидратация спиртов.
Б1. Вид гибридизации атомов углерода при тройной связи … .
Б2. Построить структурные формулы: 2-бромпентен-1, гептадиен-1,4, 5-метилгексен-1.
Б3. Осуществить превращения, указать условия реакций:
карбид кальция — ацетилен — этан — нитроэтан.
С1. Построить изомеры, используя разные виды изомерии, дать им названия для пентена-1.
С2. При сжигании углеводорода массой 29 г образовалось 88 г оксида углерода (IV) и 45 г воды. Относительная плотность углеводорода по воздуху равна 2. Найдите молекулярную формулу этого углеводорода.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 3.
А1. Общая формула алкинов:
1) CnH2n 2) CnH2n+2 3) CnH2n-2 4) CnH2n-6.
А2. Молекулярная формула гексадиена:
1) С6Н12 2) С6Н14 3) С6Н10 4) С7Н12.
А3. Число атомов водорода в молекуле бутена:
1) 8 2) 10 3) 12 4) 14.
А4. Число химических связей между атомами углерода в пентине-2:
1) 4 2) 5 3) 6 4) 7.
А5. Присоединение галогенов к молекулам непредельных углеводородов называют:
1) галогенированием 2) гидрогалогенированием
3) гидрированием 4) гидратацией.
А6. Способность растягиваться и сжиматься под действием внешней нагрузки, а затем восстанавливать прежнюю форму после снятия последней, называется:
1) деформацией 2) эластичностью
3) гибкостью 4) вулканизацией.
А7. При взаимодействии бутадиена-1,3 с одной молекулой хлора образуется:
1) 1,2-дихлорбутен-3 2) 3,4-дихлорбутен-1
3) 1,4-дихлорбутен-2 4) 1,2,3,4-тетрахлорбутан.
А8. Ацетилен в лаборатории получают:
1) крекингом алканов 2) карбидным способом
3) реакцией Вюрца 4) вулканизацией каучука.
Б1. Расстояние между атомами углерода при двойной связи равно … .
Б2. Написать структурные формулы: пропен, 1,4-дибромбутадиен-1,2, 4-метилпентин-1.
Б3. Осуществить превращения, указать условия реакций:
этилен — 2-бромэтан — бутан — бутен-1.
С1. Построить изомеры, используя разные виды изомерии, дать им названия для гексина-1.
С2. Выведите формулу газообразного соединения, массовая доля кремния в котором 87,5%, а водорода – 12,5%. Относительная плотность его по кислороду 1.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 4.
А1. Общая формула этиленовых углеводородов:
1) СnH2n+2 2) CnH2n-6 3) CnH2n-2 4) CnH2n.
А2. Молекулярная формула пентадиена:
1) С5Н12 2) С5Н10 3) С5Н8 4) С4Н6.
А3. Число атомов углерода в молекуле гептина:
1) 6 2) 8 3) 7 4) 5.
А4. Число химических связей между атомами углерода и водорода в молекуле бутен-1:
1) 8 2) 3 3) 11 4) 12.
А5. Присоединение воды к молекулам непредельных углеводородов называется:
1) галогенированием 2) гидрогалогенированием
3) гидрированием 4) гидратацией.
А6. Процесс вулканизации натурального каучука приводит к образованию:
1) полимеров 2) резины
3) эбонита 4) нет правильного ответа.
А7. Полное гидрирование пентина-1 приводит к образованию:
1) пентана 2) пентена-1
3) пентанола-2 4) пентанола-2.
А8. В промышленности этилен получают:
- из нефти и природного газа
- дегидрогалогенирование галогенопроизводных алканов
- по реакции Вюрца
- термическим крекингом алканов.
Б1. Валентный угол между sp-гибридными орбиталями равен … .
Б2. Построить структурные формулы: 3-метилгексен-2, пропадиен, 4-хлоргептин-1.
Б3. Осуществить превращения, указать условия реакций:
пропан — пропен — 2-бромпропан — гексан.
С1. Построить изомеры, используя разные виды изомерии, дать названия изомерам для пентадиена-1,2.
С2. Найдите молекулярную формулу углеводорода, если при сжигании 2 г его образовалось 2,12 г воды и 6,48 г оксида углерода (IV). Относительная плотность паров этого вещества по водороду равна 34.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 5.
А1. Общая формула диеновых углеводородов:
1) CnH2n+2 2) CnH2n-6 3) CnH2n-2 4) CnH2n.
А2. Молекулярная формула ацетилена:
1) СН4 2) С2Н2 3) С2Н4 4) С2Н6.
А3. Число атомов водорода в молекуле октена:
1) 8 2) 14 3) 16 4) 18.
А4. Число химических связей в молекуле бутадиена-1,2:
1) 11 2) 6 3) 5 4) 13.
А5. Процесс последовательного соединения одинаковых молекул друг с другом, протекающий за счёт разрыва кратных связей называется:
1) вулканизацией 2) полимеризацией
3) поликонденсацией 4) эластичностью.
А6. При проведении вулканизации натурального каучука с большим количеством серы, чем её требуется для образования резины, получается:
1) полиэтилен 2) синтетический каучук
3) эбонит 4) ацетилен.
А7. При полном окислении этилена получается:
1) этиленгликоль 2) углекислый газ и вода
3) этанол 4) полиэтилен.
А8. Натуральный каучук получают :
1) из нефти и природного газа
2) из млечного сока некоторых растений
3) полимеризацией бутадиена-1,3
4) полимеризацией ацетилена.
Б1. Вид гибридизации атома углерода при двойной связи … .
Б2. Построить структурные формулы: октен-3, 4-хлорпентадиен-1,2, 5-метилгексин-2.
Б3. Осуществить превращения, назвать органические вещества, указать условия реакций:
CaC2 — C2H2 — C2H4 — C2H5OH.
С1. Построить изомеры, используя разные виды изомерии, назвать изомеры для гексена-1.
С2. Выведите формулу газообразного соединения, массовая доля вольфрама в котором 61,745%, а фтора – 38,255%. Относительная плотность его по водороду 149.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 6.
А1. Общая формула ацетиленовых углеводородов:
1) CnH2n+2 2) CnH2n-6 3) CnH2n-2 4) CnH2n.
А2. Молекулярная формула пентена:
1) С5Н12 2) С5Н10 3) С5Н8 4) С6Н12.
А3. Число атомов углерода в молекуле бутадиена-1,3:
1) 3 2) 5 3) 4 4) 6.
А4. Количество — связей в молекуле гексина-3:
1) 3 2) 1 3) 2 4) 7.
А5. Присоединение водорода к атому углерода при двойной связи протекает согласно:
1) правила Марковникова 2) метода Лебедева
3) правила Зайцева 4) реакции Вюрца.
А6. Вулканизация натурального каучука – это нагревание его:
- со спиртовым раствором щёлочи
- с концентрированной серной кислотой
- с металлическим натрием
- с серой и другими наполнителями.
А7. В результате гидратации пентена-1 получается:
1) пентан 2) пентанол-1
3) пентанол-2 4) пентин-1.
А8. Синтетические каучуки получаю:
1) гидратацией 2) полимеризацией
3) вулканизацией 4) гидрированием.
Б1. Расстояние между атомами углерода при тройной связи … .
Б2. Построить структурные формулы: 2,3-диметилпентен-1, гексадиен-1,2, 4-бромбутин-1.
Б3. Осуществить превращения, указать условия реакции, назвать органические вещества:
СН3Br — С2Н6 — С2Н4 — ( -СН2 – СН2 -)n
С1. Построить изомеры, используя разные виды изомерии, дать им названия для гептина-1.
С2. При сжигании углеводорода массой 5,2 г выделилось 8,96 л оксида углерода (IV) ( н.у.) и 3,6 г воды. Относительная плотность вещества пол водороду равна 13. Найдите молекулярную формулу этого углеводорода.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 7.
А1. Общая формула алкенов:
1) CnH2n-2 2) CnH2n 3) CnH2n-6 4) CnH2n+2.
А2. Молекулярная формула гексадиена:
1) С6Н10 2) С5Н8 3) С6Н12 4) С6Н14.
А3. Число атомов водорода в бутине-2:
1) 12 2) 10 3) 8 4) 6.
А4. Число -связей в молекуле пентадиена-1,2:
1) 6 2) 12 3) 8 4) 10.
А5. Гидрирование – это присоединение к молекулам непредельных углеводородов по месту разрыва кратных связей:
1) воды 2) водорода
3) галогенов 4) галогеноводородов.
А6. Способность растягиваться и сжиматься под действием внешней нагрузки, а затем восстанавливать прежнюю форму после снятия последней, называется:
1) гибридизацией 2) вулканизацией
3) эластичностью 4) полимеризацией.
А7. Полимеризацией называется:
- соединение одинаковых молекул
- нагревание натурального каучука с серой и другими наполнителями
- взаимодействие ацетилена с водой
- взаимодействие непредельных углеводородов с кислородом.
А8. Впервые дивинил получил:
1) Марковников 2) Зайцев
3) Вюрц 4) Лебедев.
Б1. Валентный угол между sp2-гибридными орбиталями … .
Б2. Построить структурные формулы: этилен, 2-хлоргептадиен-1,5, 3-метилпентин-1.
Б3. Осуществить превращения, указать условия реакций:
бутан — бутадиен-1,3 — бутен-2 — 2,3-дихлорбутан.
С1. Построить изомеры, используя разные виды изомерии, дать им названия для гексадиена-1,3.
С2. Выведите формулу газообразного соединения, массовая доля азота в котором 30,43%, а кислорода – 69,57%. Относительная плотность его по кислороду 1,44.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 8.
А1. Общая формула алкадиенов:
1) CnH2n-2 2) CnH2n 3) CnH2n-6 4) CnH2n+2.
А2.Общая формула гексина:
1) С7Н12 2) С6Н10 3) С7Н14 4) С6Н12.
А3. Число атомов углерода в октене-3:
1) 9 2) 8 3) 7 4) 10.
А4. Число химических связей в пентадиене-1,4:
1) 4 2) 5 3) 6 4) 7.
А5. Отщепление водорода у атома углерода при двойной связи происходит:
- по правилу Марковникова
- по правилу Зайцева
- по методу Лебедева
- по реакции Вюрца.
А6. Качественной реакцией для распознавания непредельных углеводородов является взаимодействие с:
1) водородом 2) раствором перманганата калия
3) бромоводородом 4) водой.
А7. При бромировании 3-метилпентена-2 получается:
1) 2-бром-3-метилпентен-2 2) 1-бром-3-метил-пентен-2
3) 2,3-дибром-3-метилпентан 4) 3,4-дибром-3-метилпропан.
А8. Ацетилен в лаборатории получают:
1) по реакции Вюрца 2) дегидрированием этана
3) дегидратацией этанола 4) крекингом алканов.
Б1. Вид гибридизации атомов углерода при тройной связи … .
Б2. Построить структурные формулы: 3-бромгексен-2, бутадиен-1,2, 4-метилоктин-1.
Б3. Осуществить превращения, указать условия реакций:
бромэтан — бутан — 2-хлорбутан — бутен-2.
С1. Построить изомеры, используя разные виды изомерии, дать им названия для октена-1.
С2. При сжигании углеводорода массой 11, 2 г получили 35,2 г оксида углерода (IV) и 14,4 г воды. Относительная плотность углеводорода по воздуху равна 1,93. Найдите молекулярную формулу этого углеводорода.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 9.
А1. Общая формула алкинов:
1) CnH2n-2 2) CnH2n 3) CnH2n-6 4) CnH2n+2.
А2. Молекулярная формула дивинила:
1) С2Н4 2) С4Н6 3) С6Н10 4) С4Н8.
А3. Число атомов водорода в молекуле ацетилена:
1) 6 2) 2 3) 4 4) 8.
А4. Число -связей между атомами углерода в молекуле гексена-3:
1) 8 2) 7 3) 6 4) 5.
А5. Впервые бутадиеновый синтетический каучук был получен:
1) Марковниковым 2) Зайцевым
3) Вюрцем 4) Лебедевым.
А6. При бромировании пентина-2 получается на первой стадии:
1) 2,3-дибромпентен-2 2) 2,2,3,3-тетрабромпентан
3) 2,3-дибромпентан 4) 1,2-дибромпентан.
А7. Взаимодействие непредельных углеводородов с бромной водой является:
- способом получения непредельных углеводородов
- качественной реакцией для распознавания непредельных углеводородов
- физическим свойством непредельных углеводородов
- все ответы верны.
А8. Этилен в промышленности получают:
- дегидратацией спиртов
- дегидрированием алканов
- дегидрогалогенированием галогенопроизводных алканов
- из нефти и природного газа.
Б1. Расстояние между атомами углерода при двойной связи … .
Б2. Построить структурные формулы: этилен, 2-метилпентадиен-1,3, 3-хлорбутин-1.
Б3. Осуществить превращения, назвать органические вещества, указать условия реакций:
СаС2 — С2Н2 — С2Н4 — СО2.
С1. Построить изомеры, используя разные виды изомерии, дать им названия: пентин-1.
С2. Выведите молекулярную формулу углеводорода, массовая доля водорода в котором составляет 25%. Относительная плотность углеводорода по кислороду 0,5.
11 КЛАСС
ТЕСТ 2
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ВАРИАНТ 10.
А1. Общая формула этиленовых углеводородов:
1) CnH2n+2 2) CnH2n 3) CnH2n-2 4) CnH2n-6.
А2. Молекулярная формула изопрена:
1) С5Н8 2) С4Н6 3) С6Н10 4) С5Н10.
А3. Число атомов углерода в этилене:
1) 4 2) 3 3) 2 4) 1.
А4. Число -связей в молекуле гексадиена-1,3:
1) 2 2) 5 3) 7 4) 10.
А5. Присоединение воды к молекулам непредельных углеводородов называют:
1) гидрирование 2) гидрогалогенированием
3) гидратацией 4) полимеризацией.
А6. Резина получается в результате:
1) крекинга алканов 2) вулканизации каучука
3) гидратации спиртов 4) переработки нефти.
А7. При взаимодействии пентена-1 с хлороводородом получается:
1) 2-хлорпентан 2) 4-хлорпентан
3) 1-хлорпентан 4) хлорпентан.
А8. Этилен в лаборатории получают:
- крекингом алканов
- дегидрированием алканов
- из нефти и природного газа
- дегалогенированием дигалогенопроизводных алканов.
Б1. Валентный угол между sp-гибридными орбиталями равен … .
Б2. Построить структурные формулы: 3-этилпентен-1, дивинил, 4-бромгептин-2.
Б3. Осуществить превращения, указать условия реакций:
2-хлорпентан — пентен-2 — пентан — оксид углерода (IV).
С1. Построить изомеры, используя разные виды изомерии, дать им названия для гептадиена-1,2.
С2. При сжигании алкена массой 11,2 г получили 35, 2 г оксида углерода (IV) и 14,4 г воды. Относительная плотность алкена по воздуху 1,93. найдите молекулярную формулу алкена.
Алкены — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит
одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда — этилену — CH2=CH2.
Общая формула их гомологического ряда — CnH2n.
Номенклатура и изомерия алкенов
Названия алкенов формируются путем добавления суффикса «ен» к названию алкана с соответствующим числом:
этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию
атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого
начинается двойная связь.
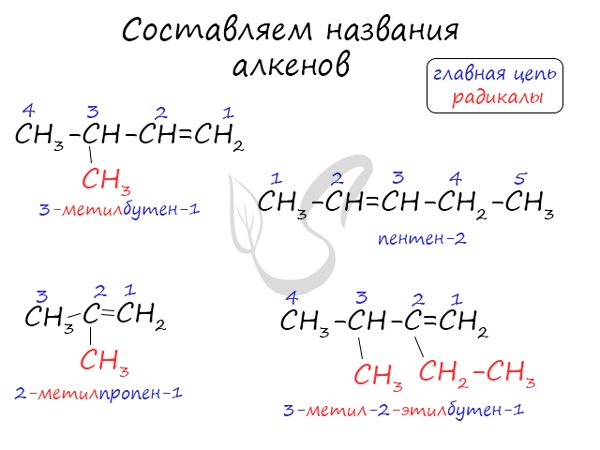
Атомы углерода, прилежащие к двойной связи находятся в sp2 гибридизации.
Для алкенов характерна изомерия углеродного скелета, положения двойной связи, межклассовая изомерия с циклоалканами и пространственная геометрическая
изомерия в виде существования цис- и транс-изомеров.
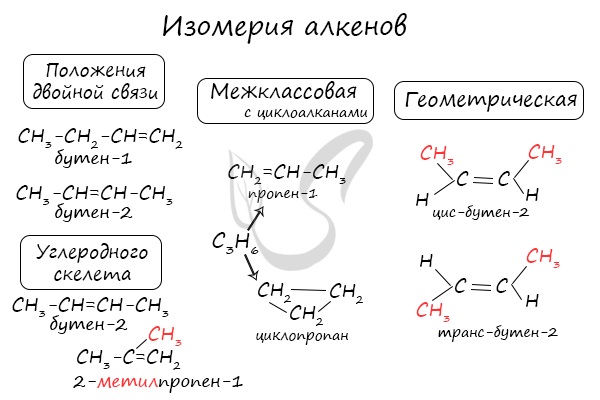
Некоторые данные, касающиеся алкены, надо выучить:
- Длина связи между атомами углерода составляет 0,134 нм
- Тип гибридизации атомов углерода (прилежащих к двойной связи) — sp2
- Валентный угол (между химическими связями) составляет 120°
Получение алкенов
Алкены получают несколькими способами:
- Крекинг нефти
- Дегидрирование алканов
- Дегидрогалогенирование галогеналканов
- Дегалогенирование дигалогеналканов
- Внутримолекулярная дегидратация спиртов
В результате крекинга нефти образуется один алкан и один алкен.
C12H26 → C6H12 + C6H14
При наличии катализатора и повышенной температуры от молекул алканов отщепляется водород. Наиболее легко
водород отдает третичный атом, чуть труднее — вторичный и заметно труднее — первичный.
CH3-CH3 → (t, кат) CH2=CH2 + H2

В реакции галогеналкана со спиртовым(!) раствором щелочи образуется алкен. По правилу Зайцева, водород
отщепляется от соседнего наименее гидрированного атома углерода.

В подобных реакциях применяется цинк (цинковая пыль) — двухвалентный металл, который связывает расположенные
рядом атомы галогенов. Между атомами углерода, которым принадлежали галогены, завязывается двойная связь.

При нагревании спиртов c серной кислотой — H2SO4, обладающей выраженными водоотнимающими
свойствами, происходит отщепление воды от спирта по правилу Зайцева. В результате образуется алкен.
Внутримолекулярная дегидратация спиртов происходит при t > 140 °C.

Химические свойства алкенов
Алкены — ненасыщенные углеводороды, охотно вступающие в реакции присоединения. Реакции замещения для них не характерны.
- Гидрирование
- Галогенирование
- Гидрогалогенирование
- Гидратация
- Окисление
- Полимеризация
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).

Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная
вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
Реакция с хлором на свету протекает по свободнорадикальному механизму, так как на свету молекулы хлора расщепляются, образуя свободные радикалы.
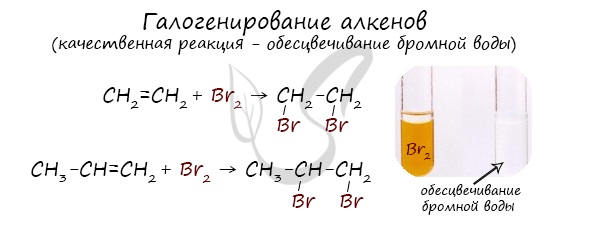
Алкены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а
атом галогена — к наименее гидрированному атому углерода.

Присоединение воды, гидратация, происходит по правилу Марковникова. Водород присоединяется к наиболее гидрированному атому углерода,
гидроксогруппа — к наименее гидрированному.

При горении алкены, как и все органические соединения, сгорают с образованием углекислого газа и воды — полное окисление. При неполном
окислении образуются окиси.

Окисление алкенов перманганатом калия (марганцовкой) в нейтральной среде является качественной реакцией на алкены в частности, и непредельные
углеводороды в целом. В результате реакции фиолетовый раствор марганцовки обесцвечивается и выпадает осадок бурого цвета — MnO2.
В более жестких условиях — при подкислении раствора серной кислотой, реакция идет с полным разрывом в самом слабом месте молекулы — двойной
связи.
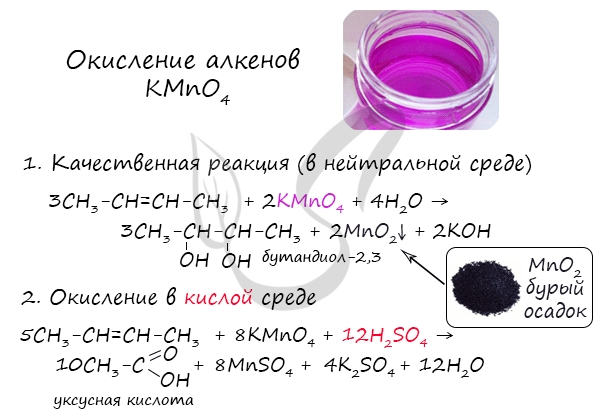
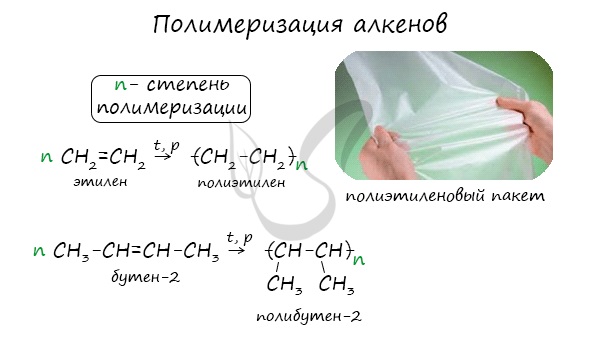
Полимеризация — цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения
молекул мономеров.
Индекс «n», степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Определение формулы вещества
(углеводороды)-решение –задание 35
1. В
результате сплавления натриевой соли карбоновой кислоты с гидроксидом
натрия массой 14 г получили карбонат натрия и газообразное
органическое вещество массой 15,4 г. Определите молекулярную формулу
полученного газообразного соединения.
Пояснение.
Составим
уравнение реакции:
Определим
количество моль гидроксида натрия и углеводорода:
Установим
формулу углеводорода:
Молекулярная
формула пропана —
2. Для
полного гидрирования 4,6 г гомолога бензола потребовалось 3,36 л
(н. у.) водорода. Запишите уравнение реакции в общем виде. Определите
молекулярную формулу циклоалкана, образовавшегося при гидрировании.
Пояснение.
Элементы
ответа:
1) Составлено
уравнение реакции в общем виде:
2) Рассчитано
количество вещества водорода и гомолога бензола:
3) Определено
число атомов углерода в составе гомолога бензола, и установлена молекулярная
формула циклоалкана:
Молекулярная
формула циклоалкана —
3. При
сгорании 17,5 г органического вещества получили 28 л (н. у.)
углекислого газа и 22,5 мл воды. Плотность паров этого вещества
(н. у.) составляет 3,125 г/л. Известно также, что это вещество было
получено в результате дегидратации третичного спирта. На основании
данных условия задачи:
1) произведите
вычисления, необходимые для установления молекулярной формулы органического
вещества;
2) запишите
молекулярную формулу органического вещества;
3) составьте
структурную формулу исходного вещества, которая однозначно отражает
порядок связи атомов в его молекуле;
4) напишите
уравнение реакции получения данного вещества дегидратацией соответствующего
третичного спирта.
Пояснение.
1)
Найдено количество вещества продуктов сгорания:
Значит
никаких других элементов в состав вещества не входит, так как его масса равна
сумме масс водорода и углерода.
2)
Установлена молекулярная формула вещества: простейшая
формула —
это алкен или циклоалкан.
Так как
вещество может быть получено при дегидратации спирта, то это алкен.
Для
определения его молекулярной формулы напишем реакцию горения в общем виде
Вспомним,
что плотность паров этого вещества (н.у.) составляет 3,125 г/л.
Значит .
По
уравнению реакции
получаем, что
Молекулярная
формула соединения
3)
Учитывая, что вещество может быть получено из третичного спирта, получаем
структурную формулу вещества:
4)
Составлено уравнение реакции дегидратации:
4. Жидкий
при обычных условиях ацетиленовый углеводород массой 4,51 г может
полностью прореагировать с 440 г бромной воды с массовой долей брома
4 %. Углеводород взаимодействует с аммиачным раствором оксида
серебра, и в его составе есть четвертичный атом углерода. Установите молекулярную
формулу углеводорода, изобразите его структурную формулу и напишите
уравнение реакции с водой.
Пояснение.
1) Напишем
уравнение реакции в общем виде и вычислим количество вещества брома:
2) Установим
молекулярную формулу углеводорода:
Молекулярная
формула углеводорода —
3) Изобразим
структурную формулу.
Углеводород
взаимодействует с аммиачным раствором оксида серебра, следовательно
тройная связь находится на краю цепи. Структурная формула с четвертичным
атомом углерода:
4) Напишем
уравнение реакции с водой:
5. Смесь
цис- и транс-изомеров этиленового углеводорода общим объёмом 1,568 л (н.
у.) пропустили через избыток водного раствора перманганата калия, в результате
образовался двухатомный спирт массой 6,30 г. Установите молекулярную формулу
углеводорода, изобразите структурную формулу транс-изомера и напишите
уравнение его реакции с подкисленным раствором перманганата калия.
Пояснение.
1) Напишем
уравнение реакции в общем виде и вычислим:
общее количество вещества этиленового
углеводорода:
или
2) Установим
молекулярную формулу углеводорода:
Молекулярная
формула углеводорода —
3) Изобразим
структурную формулу.
Цис-транс-изомеры
есть только у бутена-2. Структура транс-изомера:
4) Напишем
уравнение окисления бутена-2 до уксусной кислоты:
6. При
полном сгорании 17,1 г жидкого углеводорода образовалось 26,88 л (н. у.)
углекислого газа. Известно, что при радикальном хлорировании углеводорода
образуется только одно монохлорпроизводное. Установите молекулярную формулу
углеводорода, изобразите его структурную формулу и напишите уравнение
реакции с хлором на свету.
Пояснение.
1) Напишем
уравнение реакции в общем виде:
2) Установим
молекулярную формулу углеводорода:
Молекулярная
формула углеводорода —
3) Изобразим
структурную формулу.
Все атомы
водорода в молекуле эквивалентны. Среди всех изомеров таким
свойством обладает только 2,2,3,3-тетраметилбутан:
4) Напишем
уравнение реакции с хлором на свету:
7. При
бромировании 28,8 г гомолога бензола в присутствии железа получено
35,82 г монобромпроизводного. Выход продукта составил 75 %. Известно, что
при бромировании этого углеводорода на свету образуется единственное
монобромпроизводное. Установите молекулярную формулу углеводорода,
изобразите его структурную формулу и напишите уравнение реакции с
бромом на свету.
Пояснение.
1) Напишем
уравнение реакции в общем виде:
2) Установим
молекулярную формулу углеводорода:
mтеор
Молекулярная
формула —
3) Изображена
структурная формула.
Так как
на свету образуется только одно монобромпроизводное, все атомы водорода
в боковых цепях эквивалентны. Это означает, что в боковых цепях есть только
метильные группы. Среди трёх триметилбензолов наиболее
симметричным является 1,3,5-триметилбензол:
4) Написано
уравнение реакции с бромом на свету:
8. При полной
гидратации 20,5 г ацетиленового углеводорода образовалось органическое
вещество массой 25,0 г. Определите молекулярную формулу углеводорода
и установите его структуру, если известно, что он реагирует с аммиачным
раствором оксида серебра, а в состав молекулы входят три метильные
группы. Напишите уравнение реакции этого углеводорода с избытком
хлороводорода.
Пояснение.
1) Напишем
уравнение с водой в общем виде.
CnH2n−2+H2O
→ CnH2nO
2) Составим
математическое выражение и определим молекулярную формулу углеводорода.
Молекулярная
формула —
3) Изобразим
структурную формулу.
Углеводород
реагирует с аммиачным раствором оксида серебра, следовательно, тройная
связь находится на краю цепи. Три метильные группы есть в молекуле
3,3-диметилбутина-1:
4) Напишем
уравнение реакции с избытком хлороводорода:
9. При действии
избытка водного раствора перманганата калия на 10,5 г этиленового
углеводорода образовалось органическое вещество массой 15,6 г. Определите
молекулярную формулу углеводорода и установите его структуру,
если известно, что в результате реакции с горячим подкисленным раствором
перманганата калия образуются кетон и углекислый газ. Напишите
уравнение гидратации этого углеводорода.
Пояснение.
1) Напишем
уравнение окисления в общем виде:
Допускается
также схема в виде
2) Составим
математическое выражение и определим молекулярную формулу
углеводорода.
Молекулярная
формула —
3) Изобразим
структурную формулу.
При окислении
углеводорода образуются кетон и углекислый газ, следовательно, двойная
связь находится при разветвлении цепи, с одной стороны, и с края цепи, с
другой стороны. Углеводород – 2-метилбутен-1.
4) Напишем
уравнение реакции с водой:
10. При
сгорании 4,48 л (н. у.) газообразного органического вещества получили 35,2
г углекислого газа и 10,8 г воды. Плотность этого вещества составляет 2,41 г/л
(н. у.). Известно также, что это вещество не реагирует с аммиачным
раствором оксида серебра, а при реакции его с избытком бромной воды происходит
присоединение атомов брома только ко вторичным атомам углерода.
На
основании данных условия задачи:
1)
произведите вычисления, необходимые для установления молекулярной формулы
органического вещества;
2)
запишите молекулярную формулу органического вещества;
3)
составьте структурную формулу исходного вещества, которая однозначно отражает
порядок связи атомов в его молекуле;
4) напишите
уравнение реакции этого вещества с избытком бромной воды.
Пояснение.
Общая
формула вещества —
1)
Найдены количество вещества углекислого газа, воды и органического вещества:
= 35,2
/ 44 = 0,8 моль
= 10,8
/ 18 = 0,6 моль
=
2,41 · 22, 4 = 54 г/моль
= 4,48
/ 22,4 = 0,2 моль
2)
Определена молекулярная формула вещества:
=
= 0,8
моль
=
= 1,2
моль
=
/
=
0,8 / 0,2 = 4
=
/
= 1,2
/ 0,2 = 6
4 · 12 +
6 + z · 16 = 54
= 0
Молекулярная
формула —
3)
Составлена структурная формула вещества:
4)
Составлено уравнение реакции этого вещества с избытком бромной воды:
11. При
сгорании 16,2 г органического вещества нециклического строения получили 26,88 л
(н. у.) углекислого газа и 16,2 г воды. Известно, что 1 моль этого
органического вещества в присутствии катализатора присоединяет только 1 моль
воды и данное вещество не реагирует с аммиачным раствором оксида серебра.
На
основании данных условия задачи:
1)
произведите вычисления, необходимые для установления молекулярной формулы
органического вещества;
2)
запишите молекулярную формулу органического вещества;
3)
составьте структурную формулу органического вещества, которая однозначно
отражает порядок связи атомов в его молекуле;
4)
напишите уравнение реакции гидратации органического вещества.
Пояснение.
Искомое
вещество — углеводород
Простейшая
формула
Возможные
молекулярные формулы:,
,
и
т.д. Условию, что 1 моль этого органического вещества в присутствии
катализатора присоединяет только 1 моль воды, соответствует только
формула ,
при условии, что это алкин, а не алкадиен (остальные могут присоединять большее
количество воды)
Молекулярная
формула: —
бутин
Вещество
не реагирует с аммиачным раствором оксида серебра, значит, тройная связь находится
не у крайнего атома углерода − бутин-2
Структурная
формула:
12. При нитровании 26,5 г гомолога бензола получено 30,2 г
мононитропроизводного. Выход продукта составил 80 %, других нитропроизводных
не образовалось. Установите молекулярную формулу углеводорода, изобразите
его структурную формулу и напишите уравнение реакции с хлором на
свету.
Пояснение.
1) Напишем уравнение реакции в общем виде:
2) Установим молекулярную формулу углеводорода:
mтеор
Молекулярная формула —
3) Изобразим структурную формулу.
Так как образуется только одно мононитропроизводное, все
атомы водорода в бензольном кольце эквивалентны. Среди всех изомеров таким
свойством обладает только 1,4-диметилбензол (пара-ксилол):
4) Напишем уравнение реакции с хлором на свету:
13. При сгорании 10,5 г органического вещества получили
16,8 л углекислого газа (н. у.) и 13,5 г воды. Плотность паров этого
вещества (н. у.) составляет 1,875 г/л.
Известно, что в результате присоединения хлороводорода
к этому веществу образуется только одно монохлорпроизводное.
На основании данных условия задания:
1) произведите вычисления, необходимые для установления
молекулярной формулы органического вещества;
2) запишите молекулярную формулу исходного органического
вещества;
3) составьте структурную формулу этого вещества, которая
однозначно отражает порядок связи атомов в его молекуле;
4) напишите уравнение реакции этого вещества с
хлороводородом.
Пояснение.
1) Найдем количество вещества продуктов сгорания:
кислород отсутствует; вещество — углеводород
2) Установим молекулярную формулу вещества:
простейшая
формула
Значит, молекулярная формула вещества — .
3) Приведем структурную формулу вещества:
—
циклопропан или пропен. Циклопропан образует только одно хлоропроизводное в
реакции с хлороводородом:
4) Составим уравнение реакции вещества с хлороводородом:
14. При сжигании паров углеводорода было получено 20,16 л (н. у.)
углекислого газа и 7,2 г воды. При окислении углеводорода горячим подкисленным
раствором перманганата калия образуется терефталевая (бензол-1,4-дикарбоновая)
кислота. Определите молекулярную формулу углеводорода и установите его
структуру. Напишите уравнение описанной реакции с перманганатом калия.
Пояснение.
Вариант ответа:
1) Найдены количества углекислого газа и воды:
2) Определена молекулярная формула углеводорода.
Из условия следует, что углеводород – ароматический и содержит
одно бензольное кольцо, следовательно простейшая формула совпадает
с молекулярной формулой.
3) Изображена структурная формула.
До терефталевой кислоты окисляется ароматический углеводород,
имеющий две боковые цепи в пара-положении относительно друг друга. Подсчет
атомов водорода приводит к выводу о том, что в одной из цепей – тройная связь.
4) Написано уравнение реакции с перманганатом калия:
15. При гидратации 31,50 г этиленового углеводорода образовалось 23,76
г органического вещества. Выход продукта составил 60 %. Определите молекулярную
формулу углеводорода и установите его структуру, если известно, что при его
жёстком окислении перманганатом калия образуются кетон и кислота. Напишите
уравнение реакции углеводорода с водой, в уравнении изобразите структурные
формулы органических веществ.
Пояснение.
1) Написано уравнение реакции гидратации в общем виде:
2) Определена молекулярная формула углеводорода:
Молекулярная формула углеводорода —
(Возможен и другой способ вывода молекулярной формулы по массам
реагента и продукта)
3) Изображена структурная формула.
При окислении образуются кетон и кислота, следовательно углеродный
скелет разветвлённый, а двойная связь находится в середине цепи:
4) Написано уравнение реакции с водой:
Углеводороды
Классификация органических веществ
А 1. Общая форула алкенов:
1) C
n
H
2n+2
2) C
n
H
2n
3) C
n
H
2n-2
4) C
n
H
2n-6
А 2. Вещества с общей формулой C
n
H
2n
могут относиться к классам
1) алкинов и алкенов 2) алкинов и алкодиенов
3) алкенов и алкодиенов 4) алкенов и циклопарафинов
А 3. Ароматическим углеводородам соответствует общая формула
1) С
ņ
Н
2ņ-2
3) С
ņ
Н
2ņ+2
2) С
ņ
Н
2ņ-6
4) С
ņ
Н
2ņ
Гомологи
А 4. Гомологом этилена не является
1) СН
2
=СН—СН
2
—СН
3
2) СН
2
=СН—СН
2
—СН
2
—СН
3
3) СН
2
=СН—СН
3
4) СН
3
—СН
2
—СН
3
А 5. Гомолог вещества, формула которого СН
2
=СН—СН—СН
2
—СН
3
ﺍ
СН
3
1) 2 – метилгексан 2) гептан
3) гекан 4) 3 — метилгекен
А 6. Гомологами являются
1) пентин—1 и пентин-2 2) бутин—1 и бутен-1
3) 2-метилгексен—2 и 3—метилгексан 4)2,3-диметилпентин—1 и 2,3—диметилгексин-1
А 7. Гомологом ацетилена не является
1) СН
≡ С – СН
2
– СН
3
2) СН
3
– С ≡ СН
3) СН
2
= СН – СН
3
4) СН ≡ С – СН
2
– СН
2
– СН
3
Изомеры и их названия
А 8. Изомером вещества, формула которого СН
2
=СН—СН
2
—СН
3
, является:
1) 2-метилбутен-2 2) бутен-2
3) бутан 4) пентин-1
А 9. Число нециклических изомеров углеводорода С
4
Н
8
равно
1) 1 2) 3
3) 2 4) 4
А 10. Структурным изомером пентена – 1 является
1) циклопентан 2) пентен – 2
3) 2 – метилбутен 4) 2 – метилпентен 1
А 11. Как называется углеводород:
СН
3
– СН –СН — С ≡ С – СН – СН
3
│ │ │
СН
3
СН
3
С
2
Н
5
1) 2 – этил— 5,6 –диметилгептин – 3 2) 2,4 – диметил— 6 – этилгептин – 4
3) 1,4,5 – триметил – 1 – этилгексин – 2 4) 2,3,6 – триметилоктин – 4
Строение
А 12. Число σ связей в молекуле этилена равно
1) 1 2) 3
3) 5 4) 4
А 13. Номера атом, находящихся в состоянии sp
2
— гибридизации в молекуле бутена – 2
1) 1 и 2 2) 2 и 3
3) 3 и 4 4) 1 и 4
А 14. Вещество, являющееся исходным в реакции полимеризации, называется:
1) мономер 2) полимер
3) димер 4) тример
А 15. Только σ — связи имеются в молекуле
1) бутена 2) пропилена
3) этилена 4) пентана
А 16. Число σ связей в молекуле ацетилена равно
1) 1 2) 3
3) 5 4) 4
А 17. Число π—связей в молекуле пропина равно
1) 1 2) 3
3) 2 4) 4
Химические свойства
А 18. Вещество, для которого характерна реакция гидрирования:
1) пропан 2) пропен
3) этан 4) 2- метилпропан
А 19. Для получения углеводорода с более длинной углеродной цепью применяют
реакцию:
1) Вюрца 2) Зайцева
3) Кучерова 4) Марковникова
А 20. Условия проведения реакции Кучерова – это:
1) H
2
,(Ni) 2) Сl
2
,(h )
3) Pt, 5атм 4) р—р HgSO
4
А 21. Катализатором тримеризации ацетилена в бензол служит:
1) СuСl 2) С (актив)
3) АlСl
3
4) Рt.
А 22. Формулы веществ, вступающих в реакцию друг с другом:
1) С
2
Н
4
и СН
4
2) С
3
Н
8
и Н
2
3) С
6
Н
14
и Н
2
О 4) С
2
Н
4
и Н
2
А 23. В результате реакции Вюрца из 2 – иодбутана получается:
1) н — октан 2) н — гексан
2) 2,5 – диметилгексан 4) 3,4 – диметилгексан
А 24. Отличить 2—метилпентен-2 от 2—метилпентана можно с помощью:
1) бромоводорода 2) бромной воды
3) раствора серной кислоты 4) лакмуса
А 25. Какая из реакций бензола относится к реакциям замещения?
1) нитрование 2) горение
3) гидрирование 4) взаимодействие с хлором при действии УФ —
облучения.
А 26. Органическим веществом, при пропускании которого через бромную воду раствор
обесцвечивается, является:
1) метан 2) пропилен
3) хлорметан 4) этан
А 27. Бензол не взаимодействует с
1) азотной кислотой 2) бромоводородом
3) бромом 4) хлором
А 28. При взаимодействии бутена—1 c хлороводородом атом хлора присоединяется к атому
углерода:
1) первому 2) второму
3) третьему 4) четвертому
А 29. С водородом при определенных условиях реагируют оба вещества пары:
1) бутан и бутен 2) пропен и циклопропан
3) этилен и этан 4) гексан и изобутан
А 30. И бутан и бутилен реагируют с
1) бромной водой 2) раствором KMnO
4
3) водородом 4) хлором
А 31. Продуктом реакции бутена-1 с хлором является
1) 2-хлрбутен-1 2) 1,2-дихлорбутан
3) 1,1-дихлорбутан 4) 1,2-дихлорбутен-1
А 32. При полимеризации какого углеводорода образуется полимер, структурная формула
которого
1) пропана 2) 2- метилпропана
3) 2 – метилпрпена 4) пропена
А 33. Какой тип реакции характерен для ацетилена
1) разложения 2) замещения
3) присоединения 4) обмена
А 34. Гексахлорциклогексан образуется в результате взаимодействия
1) бензола и хлора при облучении 2) бензола и хлорметана в присутствии AlCl
3
3) бензола и хлора в присутствии FeCl
3
4)бензола и хлороводорода
Получение
А 35. Формула вещества Х в цепочке превращений
t
0
+ H
2
, Ni
СН
4
→ Х → С
2
Н
4
1) СО
2
2) С
2
Н
2
3)С
3
Н
8
4) С
2
Н
6
А 36. Тип реакции С
2
Н
5
ОН → С
2
Н
4
+ Н
2
О
1) замещение 2) присоединение
3) гидрирование 4) разложение
А 37. Бензол и его гомологи выделяют из:
1) мазута 2) попутного нефтяного газа;
3) кокса 4) каменноугольной смолы
Часть В
В 1. К способам получения алкенов относят:
А) дегидрирование алканов
Б) гидрирование бензола
В) дегидратацию спиртов
Г) отщепление галогенводородов от галогеналканов
Д) ароматизацию предельных углеводородов
Е) гидратацию алкинов
Ответ: _____________________
В 2. И для метана, и для пропена характерны:
А) реакции бромирования
Б) жидкое агрегатное состояние при н.у.
В) наличие π—связи в молекулах
Г) реакции гидрирования
Д) горение на воздухе
Е) малая растворимость в воде
Ответ: _____________________
В 3. К способам получения ацетилена относят:
А) дегидратацией этилового спирта
Б) гидратацией этилена
В) дегидрирование этилена
Г) сжиганием этана
Д) гидратацией карбида кальция
Е) термическим разложением метана
Ответ: _____________________
В 4. С каким из перечисленных веществ, при соответствующих условиях реагирует
пропин:
А) водород
Б) бром
В) этен
Г) метан
Д) углекислый газ
Е) хлороводород
Ответ: _____________________
В 5. С каким из перечисленных веществ, при соответствующих условиях реагирует
бензол:
А) хлор
Б) вода
В) азотная кислота
Г) бром
Д) р—р KMnO
4
Е) хлороводород
Ответ: _____________________
В 6. Выберите признаки, характерные для этана:
А) газообразное вещество
Б) горит бледным синеватым пламенем
В) имеет резкий запах
Г) в 1,5 раз тяжелее водорода
Д) растворим в воде
Е) вступает в реакции присоединения
Ответ: _____________________
В 7. Какие углеводороды можно получить реакцией дегидрирования
А) этан
Б) бутадиен
В) пропен
Г) ацетилен
Д) бутан
Е) пентан
Ответ: _____________________
В 8. Этилен не взаимодействует с веществами:
А) HNO
3
Б) О
2
В) C
2
H
2
Г) Н
2
Д) Cl
2
Е) CH
4
Ответ: _____________________
В 9. С каким из перечисленных веществ бензол не взаимодействует:
А) H
2
Б) C
2
H
2
В) НNO
3
Г) CH
4
Д) Н
2
О
Е) Cl
2
Ответ: _____________________
В 10. Какие пары углеводородов вступают в реакции гидрирования
А) пропан и пропилен
Б) бутадиен и бензол
В) пропен и этин
Г) метан и этан
Д) пентан и пентен
Е) бензол и ацетилен
Ответ: _____________________
В 11. Для этилена характерно
А) наличие в молекулах двойной связи
Б) хорошая растворимость в воде
В) обесцвечивание бромной воды
Г) наличие в молекулах только одинарных связей
Д) реакция полимеризации
Е) наличие тройной связи
Ответ: _____________________
В 12. С раствором бромной воды реагирует
А) метан
Б) циклогексан
В) этилен
Г) ацетилен
Д) бензол
Е) пентен-2
Ответ: _____________________
В 13. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) бутан А) алкены
2) бензол Б) алкины
3) бутен В) алканы
4) метан Г) арены
Д) циклоалканы
Е) алкадиены
В 14. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) бутадиен А) алканы
2) этан Б) алкины
3) пропен В) алкены
4) ацетилен Г) алкадиены
Д) циклоалканы
Е) арены
В 15. Установите соответствие между формулой вещества и степенью окисления углерода
в нем:
1) СН
4
А) +2
2) СН
3
Сl
Б) -3
3) ССl
4
В) -4
4) Al
4
С
3
Г) +1
Д) +4
Е) -2
В 16. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
3
Н
8
+ О
2
→
СО
2
+ Н
2
О
1) С
3
Н
8
А) 3
2) О
2
Б) 2
3) СО
2
В) 8
4) Н
2
О Г) 4
Д) 1
Е) 5
В 17. Установите соответствие между названием органического соединения и числом σ— и
π— связей.
Название органического соединения Число — σ— и π —связей
1) пропен А) 12 и 2
2) этин Б) 11 и 1
3) метан В) 3 и 2
4) бутадиен-1,3 Г) 8 и 1
Д) 10 и 3
Е) 4 и 0
В 18. Установите соответствие между названием органического соединения и числом σ— и
π— связей.
Название органического соединения Число σ— и π— связей
1) этан А) 3 и 2
2) этилен Б) 6 и 2
3) бутен-1 В) 11 и 1
4) ацетилен Г) 7 и 0
Е) 5 и 1
В 19. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
6
Н
6
+ О
2
→
СО
2
+ Н
2
О
1) С
6
Н
6
А) 6
2) О
2
Б) 2
3) СО
2
В) 3
4) Н
2
О Г) 12
Д) 15
Е) 1
В 20. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
5
Н
12
+ О
2
→
СО
2
+ Н
2
О
1) С
5
Н
12
А) 8
2) О
2
Б) 6
3) СО
2
В) 2
4) Н
2
О Г) 4
Д) 1
Е) 5
В 21. Установите соответствие между формулой вещества и коэффициентом, стоящим
перед ним в уравнении реакции:
С
4
Н
8
+ О
2
→
СО
2
+ Н
2
О
1) С
4
Н
8
а) 1
2) О
2
б) 2
3) СО
2
в) 4
4) Н
2
О г) 5
д) 6
е) 8
В 22. Установите соответствие между названием органического соединения и структурной
формулой
Название вещества Структурная формула
1) транс-5-метилгептен—2 А) СН
3
– СН
2
– С = СН – СН
2
– СН
3
|
2) 2,5-диметилгексен—1 СН
2
– СН
3
3) 2-метил-3,6-диэтилоктен-4 СН
3
Н
4) 3-этилгексен—3 Б) С=С
Н СН
2
– СН – СН
2
– СН
3
|
СН
3
В) СН
2
= С – СН
2
– СН
2
– СН – СН
2
– СН
3
| |
СН
3
СН
3
Н Н
Г) С=С
СН
3
СН
2
– СН – СН
2
– СН
3
|
СН
3
СН
3
|
Д) СН
3
– СН – СН – СН = СН – СН – СН
2
– СН
3
| |
СН
2
– СН
3
СН
2
– СН
3
В 23. Установите соответствие между структурной формулой органического соединения и
его названием
Структурная формула вещества Название вещества
1) А) 1,3,5-триметилбензол
Б) пара—метилэтилбензол
2)
В) 1-пропил-5-метил-2-этилбензол
3) Г) 1-метил-4-этилбензол
Д) пропилбензол
4)
Е) 1-метил-3-этил-4-пропилбензол
В 24. Установите соответствие между структурной формулой вещества и названием
гомологического ряда, к которому оно принадлежит
1) С
6
Н
5
— СН
2
—СН
3
2) СН
3
—С(СН
3
)
2
—СН
2
—СН
3
3) СН
2
=С=СН—СН
3
4) СН
3
—С≡С—СН
3
А) алкодиены
Б) алканы
В) арены
Г) алкены
Д) алкины
В 25. Установите соответствие между названием соединения и классом, к которому оно
принадлежит
Название вещества Класс соединений
1) гексен А) алкены
2) этан Б) алкины
3) циклобутан В) алканы
4) этилен Г) спирты
Д) циклоалканы
Е) алкадиены
В 26. Установите соответствие между структурной формулой вещества и названием
гомологического ряда, к которому оно принадлежит
1) С
6
Н
5
—СН
3
2) СН
3
—СН
2
—СН
2
— СН = СН—СН
3
3) СН
2
=СН—СН
2
—СН
3
4) СН
3
—С≡С—СН
2
—СН
3
А) алкодиены
Б) алканы
В) алкины
Г) алкены
Д) арены
В 27. Установите соответствие между исходными веществами и продуктами реакции
Вещества, вступившие в реакцию Основной продукт реакции
H
2
SO
4
(конц.)
1) + HNO
3
А) Б)
hν
2) + С1
2
В) Г)
3) AlCl
3
+ С
2
Н
5
С1
FeCl
3
4) + Cl
2
Д) Е)
В 28. Установите соответствие между названием вещества и формулой его
изомера
Название вещества Формула изомера
1) 2-метилбутен—2 А) СН
2
= СН – СН
2
– СН
2
– СН
3
2) цис-3-метилпентен-1 Н СН
3
3) бутен-1 Б) С=С
4) 2,3-диметилбутен-1 СН
3
СН
2
– СН
3
СН
3
|
В) СН
3
– С = С – СН
3
|
СН
3
СН
3
СН
3
Г) С=С
Н СН
2
– СН
3
Д) СН
3
– СН = СН – СН
3
Е) СН
3
– СН = С – СН
2
– СН
3
|
СН
2
– СН
3
В 29. Установите соответствие между исходными веществами и продуктами реакции
Вещества вступившие в реакцию Продукты реакции
1) СН
3
– С ≡ С – СН
3
+ Н
2
А) СН
3
СН
2
ОН
Б) СН
3
– СВr = СН
2
2) СН
3
– С ≡ СН + НВr В) СН
3
– СН = СН – СН
3
Г) СН
3
– СН = СНВr
3) СН ≡ СН + НОН Д) СН
3
– СНВr= СНВr- СН
3
4) СН
3
– С ≡ С – СН
3
+ Вr
2
Е) СН
3
СОН
В 30. Установите соответствие между исходными веществами и продуктами реакции
Вещества вступившие в реакцию Продукты реакции
1) СН
3
– С ≡ СН + Н
2
А) СН
2
=СН
2
Б) СН
3
– СН= СН
2
2) СН
3
– СН = СН
2
+ НВr В) СН
3
– СНВr-СН
3
Г) СН
3
– СН
2
—СНВr
3) СН ≡ СН + 2Н
2
Д) СН
3
– СНВr= СНВr- СН
3
4) СН
3
– С ≡ С – СН
3
+ Вr
2
Е) СН
3
—СН
3
Часть С
С 1. Определите формулу алкена, если известно, что 4,2 г этого алкена присоединяет 8,0 г
брома.
С 2. Осуществите следующие превращения. Запишите уравнения реакций.
+ Cl
2
+Na + Br
2
+ NaOH(спирт.) + Н
2
О
СН
3
– СН
3
→ Х
1
→ Х
2
→
Х
3
→ Х
4
→ Х
5
С 3. Осуществите следующие превращения. Запишите уравнения реакций.
С 4. Осуществите следующие превращения. Запишите уравнения реакций.
+Н
2
О, HgSO
4
С → СН
4
→ С
2
Н
2
→ Х
3
С 5. Напишите уравнения реакций, при помощи которых можно осуществить следующие
превращения, указав вещество X , и условия проведения реакций
+НNO
3
C
2
H
6
→ C
2
H
4
→ C
2
H
2
→ C
6
H
6
→
X
С 6. Осуществите следующие превращения. Запишите уравнения реакций.
+H
2
O +1мольCl
2
+Nа,t
Al
4
C
3
→X
1
→ X
2
→ X
3
С 7. Осуществите следующие превращения. Запишите уравнения реакций.
300
0
+ Cl
2
(FeCl
3
)
Гексен Гексан Х
1
Х
2
С 8. Напишите уравнения реакций, при помощи которых можно осуществить следующие
превращения, указав условия проведения реакций:
CH
4
→ C
2
H
2
→ C
2
H
4
→ C
2
H
2
→ C
6
H
6
С 9. Согласно термохимическому уравнению реакции
CH
4
+ 2O
2
→ CO
2
+ 2H
2
O + 900 кДж вычислите количество теплоты, которое
выделиться при сжигании 3,2 г метана.
С 10. Согласно термохимическому уравнению реакции
CH
4
+ 2O
2
→ CO
2
+ 2H
2
O + 900 кДж вычислите количество теплоты, которое
выделиться при сжигании 8 г метана.
С 11. Определите формулу углеводорода, массовая доля углерода в котором 85,7%, а
плотность паров по водороду 28.
С 12. Из 92 г этанола получили 33,6 л (н.у.) этилена. Вычислите выход продукта в
процентах от теоретически возможного.
С 13. Определите формулу углеводорода, массовая доля водорода в котором равна 20%.
Относительная плотность углеводорода по водороду равна 15.
С 14. Определите формулу углеводорода, при сжигании которого образовалось 1, 792л
(н.у) оксида углерода (IV ) и 1,44г воды. Относительная плотность вещества по водороду
равна 28.
С 15. Определите формулу углеводорода, при сжигании которого образовалось 4,48л
оксида углерода (IV) (н.у) и 1,8г воды. Масса 10л этого газа составляет 12,5г.
С 16. Найдите простейшую формулу углеводорода, содержащего 92,31% углерода по
массе.
С 17. Вычислите массовую долю углерода и водорода в молекуле пропана.
С 18. При нагревании иодметана массой 2,84 с избытком металлического
натрия получили 179,2 мл этана (н.у). Определите выход продукта реакции.
С 19. Определите алкан, 1 л которого при н.у. весит 2,59 г. Составьте его структурную
формулу.
С 20. Определите простейшую формулу углеводорода, при сжигании которого
образовалось 2,24л оксида углерода (IV) (н.у) и 3,6г воды.
С 21. Вычислите массу бромбензола, которую можно получить при бромировании
117 г бензола бромом массой 316 г.
С 22. Углеводород, плотность паров которого по водороду равна 15, содержит 80 %
углерода. Найдите его молекулярную формулу.
С 23. Из 7,8 г бензола получено 8,61 г нитробензола. Определите выход продукта реакции.
С 24. Технический карбид кальция массой 20 г обработали избытком воды. Какой объем
ацетилена получили, если массовая доля примесей техническом карбиде составляла 20 %.
С 25. Какая масса бромбензола образуется при взаимодействии 7,8 г бензола с избытком
брома в присутствии FeBr
3
, выход продукта реакции равен 90%?
С 26. При сжигании 29 г углеводорода образовалось 88 г оксида углерода (IV) и 45 г воды.
Выведите молекулярную формулу углеводорода.
С 27. Из 44,8 л метана получили 40 л хлорметана. Определите сколько это составляет в %
от теоретически возможного выхода.
С 28. Вычислите объем углекислого газа, выделившегося при сгорании 56 л метана в 48 л
кислорода
С 29. Из 92 г этанола получили 33,6 л (н.у.) этилена. Определите выход продукта в
процентах от теоретически возможного.
С. 30. Найдите объем этилена, необходимый для обесцвечивания 50 г 2%—ного раствора
бромной воды.
24 июля 2022
В закладки
Обсудить
Жалоба
Тест по теме «Непредельные (ненасыщенные) углеводороды»
2 варианта по 25 вопросов. Ответы прилагаются.
Алкены — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь). Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда — этилену — CH2=CH2. Общая формула их гомологического ряда — CnH2n.
npred-u.docx
npred-u.pdf
Автор: Иващенко Л.В.





















