12 января 2022
В закладки
Обсудить
Жалоба
Таблица «Общие формулы классов органических веществ»
Таблица поможет обучающимся систематизировать знания по органической химии.
→ tab.docx
→ Примеры соединений с формулами и тривиальными названиями.
| Класс органических веществ | Общая молекулярная формула |
| Алканы | CnH2n+2 |
| Алкены | CnH2n |
| Циклоалканы | CnH2n |
| Алкины | CnH2n−2 |
| Алкадиены | CnH2n−2 |
| Арены | CnH2n−6 |
| Предельные одноатомные спирты | CnH2n+2O |
| Простые эфиры | CnH2n+2O |
| Предельные двухатомные спирты | CnH2n+2O2 |
| Предельные трехатомные спирты | CnH2n+2O3 |
| Многоатомные спирты | CnH2n+2Ox |
| Ароматические спирты | CnH2n−6O |
| Фенолы | CnH2n−6O |
| Предельные альдегиды | CnH2nO |
| Кетоны | CnH2nO |
| Предельные карбоновые кислоты | CnH2nO2 |
| Сложные эфиры | CnH2nO2 |
| Амины предельные | CnH2n+3N |
| Амины ароматические | CnH2n-5N |
| Аминокислоты (предельные одноосновные) | CnH2n+1NН2 |
Автор: Давыдова Лариса Ивановна.

Подготовка к ЕГЭ начинается с
психологического настроя на успех, обязательную сдачу ЕГЭ.
Поэтому не
лишними будут помощь психолога, советы родителей и учителей.
Теория к ЕГЭ. Методика самостоятельной подготовки к ЕГЭ
ТЕОРИЯ ДЛЯ СДАЮЩИХ ЕГЭ
Дopoнькин ЕГЭ. Химия. Большой справочник
Adobe Acrobat Document
7.6 MB
РАСПЕЧАТАТЬ И ИСПОЛЬЗОВАТЬ
Методические рекомендации по подготовке
Adobe Acrobat Document
375.5 KB
ПРОРАБОТАТЬ И ПРИНЯТЬ К СВЕДЕНИЮ
анализ типичных ошибок ЕГЭ-2019 г.pdf
Adobe Acrobat Document
771.7 KB
ПРОГРАММА ПОДГОТОВКИ К ЕГЭ ПО ХИМИИ.doc
Microsoft Word Document
129.5 KB
ВНИМАНИЕ
Тривиальные названия органических вещест
Adobe Acrobat Document
340.1 KB
Теория и тест для самостоятельной проработки.
Основные способы получения металлов.pptx
Microsoft Power Point Presentation
920.7 KB
Все свойства органических веществ.
Реакции к основным темам курса 10 класса
Microsoft Word Document
158.0 KB
Общие формулы. УЧИТЬ!!!
Общие формулы классов органических вещес
Adobe Acrobat Document
188.4 KB
Металлы. Соединения металлов. УЧИТЬ!!!
Свойства металлов и их соединений.docx
Microsoft Word Document
2.5 MB
Цепочки превращений.
Задание С3. Цепочки превращений..docx
Microsoft Word Document
674.8 KB
Теория по основным классам неорганических соединений.
Основные классы и их свойства.doc
Microsoft Word Document
880.0 KB
Нужно разобраться и выучить.
Ряд активности металлов.pdf
Adobe Acrobat Document
315.0 KB

Документация и подготовка к ЕГЭ
таблица ПСХЭ.doc
Microsoft Word Document
396.5 KB
Таблица растворимости некоторых веществ
Microsoft Word Document
578.5 KB

Дополнительная информация, теория к ЕГЭ
Адреса сайтов подготовки.
Материалы для подготовки к ОГЭ и ЕГЭ.doc
Microsoft Word Document
15.2 KB
Таблица. Качественные признаки веществ.d
Microsoft Word Document
44.8 KB
Ряд ЭО. Названия кислот и остатков. Степ
Microsoft Word Document
518.7 KB
Таблица ПСХЭ . С обозначением классов со
Microsoft Word Document
498.4 KB
цвета оксидов.doc
Microsoft Word Document
24.0 KB
Номенклатура неорганических веществ.doc
Microsoft Word Document
135.5 KB
Определение ионов. Качественные реакции.
Microsoft Word Document
51.0 KB
Часть представленных здесь материалов взята с
сайта учителя химии Сикорской О.Э.
3.3. Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная).
Классификация органических веществ
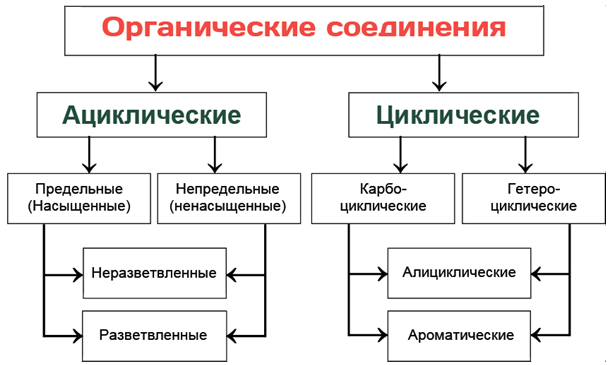
В зависимости от типа строения углеродной цепи органические вещества подразделяют на:
- ациклические и циклические.
- предельные (насыщенные) и непредельные (ненасыщенные).
- карбоциклические и гетероциклические.
- алициклические и ароматические.
Ациклические соединения — органические соединения, в молекулах которых отсутствуют циклы и все атомы углерода соединены друг с другом в прямые или разветвленные открытые цепи.
В свою очередь среди ациклических соединений выделяют предельные (или насыщенные), которые содержат в углеродном скелете только одинарные углерод-углеродные (С-С) связи и непредельные (или ненасыщенные), содержащие кратные — двойные (С=С) или тройные (С≡С) связи.
Циклические соединения — химические соединения, в которых присутствует три или более связанных атомов, образующие кольцо.
В зависимости от того, какими атомами образованы циклы различают карбоциклические соединения и гетероциклические соединения.
Карбоциклические соединения (или изоциклические) содержат в своих циклах только атомы углерода. Эти соединения в свою очередь делятся на алициклические соединения (алифатические циклические) и ароматические соединения.
Гетероциклические соединения содержат в составе углеводородного цикла один или несколько гетероатомов, чаще всего которыми являются атомы кислорода, азота или серы.
Простейшим классом органических веществ являются углеводороды – соединения, которые образованы исключительно атомами углерода и водорода, т.е. формально не имеют функциональных групп.
Поскольку углеводороды, не имеют функциональных групп для них возможна только классификация по типу углеродного скелета. Углеводороды в зависимости от типа их углеродного скелета делят на подклассы:
1) Предельные ациклические углеводороды носят название алканы. Общая молекулярная формула алканов записывается как CnH2n+2, где n — количество атомов углерода в молекуле углеводорода. Данные соединения не имеют межклассовых изомеров.
2) Ациклические непредельные углеводороды делятся на:
а) алкены — в них присутствует только одна кратная, а именно одна двойная C=C связь, общая формула алкенов CnH2n,
б) алкины – в молекулах алкинов также присутствует только одна кратная, а именно тройная С≡С связь. Общая молекулярная формула алкинов CnH2n-2
в) алкадиены – в молекулах алкадиенов присутствуют две двойные С=С связи. Общая молекулярная формула алкадиенов CnH2n-2
3) Циклические предельные углеводороды называются циклоалканы и имеют общую молекулярную формулу CnH2n.
Остальные органические вещества в органической химии рассматривают как производные углеводородов, образуемые при введении в молекулы углеводородов так называемых функциональных групп, которые содержат другие химические элементы.
Таким образом, формулу соединений с одной функциональной группой можно записать как R-X, где R – углеводородный радикал, а Х – функциональная группа. Углеводородным радикалом называют фрагмент молекулы какого-либо углеводорода без одного или нескольких атомов водорода.
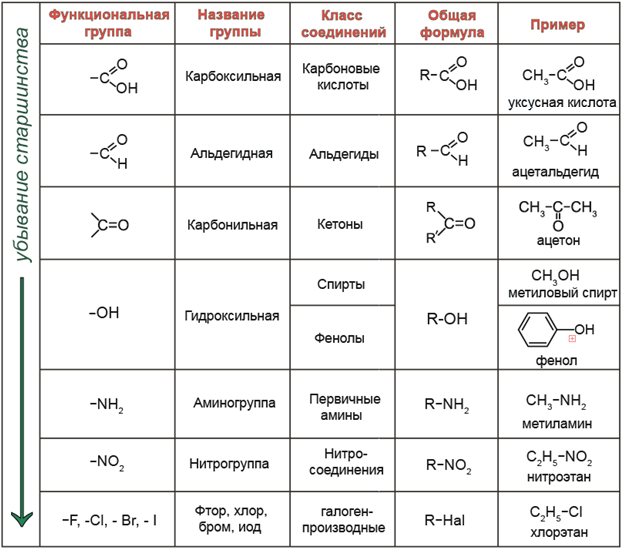
По наличию тех или иных функциональных групп соединения подразделяют на классы. Основные функциональные группы и классы соединений, в состав которых они входят, представлены в таблице:
Таким образом, различные комбинации типов углеродных скелетов с разными функциональными группами дают большое разнообразие вариантов органических соединений.
Галогенпроизводные углеводородов
Галогенпроизводными углеводородов называют соединения, получаемые при замене одного или нескольких атомов водорода в молекуле какого-либо исходного углеводорода на один или несколько атомов какого-либо галогена соответственно.
Пусть некоторый углеводород имеет формулу CnHm, тогда при замене в его молекуле X атомов водорода на X атомов галогена формула галогенпроизводного будет иметь вид CnHm-XHalX. Таким образом, монохлорпроизводные алканов имеют формулу CnH2n+1Cl, дихлорпроизводные CnH2nCl2 и т.д.
Спирты и фенолы
Спирты – производные углеводородов, один или несколько атомов водорода в которых заменены на гидроксильную группу -OH. Спирты с одной гидроксильной группой называют одноатомными, с двумя – двухатомными, с тремя трехатомными и т.д. Например:
Спирты с двумя и более гидроксильными группами называют также многоатомными спиртами. Общая формула предельных одноатомных спиртов CnH2n+1OH или CnH2n+2O. Общая формула предельных многоатомных спиртов CnH2n+2Ox , где x – атомность спирта.
Спирты могут быть и ароматическими. Например:
Общая формула таких одноатомных ароматических спиртов CnH2n-6O.
Однако, следует четко понимать, что производные ароматических углеводородов, в которых на гидроксильные группы заменены один или несколько атомов водорода при ароматическом ядре не относятся к спиртам. Их относят к классу фенолы. Например, это данное соединение является спиртом:
А это представляет собой фенол:
Причина, по которой фенолы не относят к спиртам, кроется в их специфических химических свойствах, сильно отличающих их от спиртов. Как легко заметить, однотомные фенолы изомерны одноатомным ароматическим спиртам, т.е. тоже имеют общую молекулярную формулу CnH2n-6O.
Амины
Аминами называют производные аммиака, в которых один, два или все три атома водорода замещены на углеводородный радикал.
Амины, в которых только один атом водорода замещен на углеводородный радикал, т.е. имеющие общую формулу R-NH2, называют первичными аминами.
Амины, в которых два атома водорода замещены на углеводородные радикалы, называют вторичными аминами. Формулу вторичного амина можно записать как R-NH-R’. При этом радикалы R и R’ могут быть как одинаковые, так и разные. Например:
| СH3-NH-CH3 | СH3-NH-CH2-CH3 |
| диметиламин | метилэтиламин |
Если в аминах отсутствуют атомы водорода при атоме азота, т.е. все три атома водорода молекулы аммиака замещены на углеводородный радикал, то такие амины называют третичными аминами. В общем виде формулу третичного амина можно записать как:
При этом радикалы R, R’, R’’ могут быть как полностью одинаковыми, так и все три разные.
Общая молекулярная формула первичных, вторичных и третичных предельных аминов имеет вид CnH2n+3N.
Ароматические амины с только одним непредельным заместителем имеют общую формулу CnH2n-5N
Альдегиды и кетоны
Альдегидами называют производные углеводородов, у которых при первичном атоме углерода два атома водорода заменены на один атом кислорода, т.е. производные углеводородов в структуре которых имеется альдегидная группа –СН=О. Общую формулу альдегидов можно записать как R-CH=O. Например:
Кетонами называют производные углеводородов, у которых при вторичном атоме углерода два атома водорода заменены на атом кислорода, т.е. соединения, в структуре которых есть карбонильная группа –C(O)-.
Общая формула кетонов может быть записана как R-C(O)-R’. При этом радикалы R, R’ могут быть как одинаковыми, так и разными.
Например:
Как можно заметить, альдегиды и кетоны весьма схожи по строению, однако их все-таки их различают как классы, поскольку они имеют существенные различия в химических свойствах.
Общая молекулярная формула предельных кетонов и альдегидов одинакова и имеет вид CnH2nO
Карбоновые кислоты
Карбоновыми кислотами называют производные углеводородов, в которых есть карбоксильная группа –COOH.
Если кислота имеет две карбоксильные группы, такую кислоту называют дикарбоновой кислотой.
Предельные монокарбоновые кислоты (с одной группой -COOH) имеют общую молекулярную формулу вида CnH2nO2
Ароматические монокарбоновые кислоты имеют общую формулу CnH2n-8O2
Простые эфиры
Простые эфиры – органические соединения, в которых два углеводородных радикала опосредованно соединены через атом кислорода, т.е. имеют формулу вида R-O-R’. При этом радикалы R и R’ могут быть как одинаковыми, так и разными.
Например:
| CH3-O-CH3 | CH3-O-C2H5 |
| диметиловый эфир | метилэтиловый эфир |
Общая формула предельных простых эфиров такая же, как у предельных одноатомных спиртов, т.е. CnH2n+1OH или CnH2n+2О.
Сложные эфиры
Сложные эфиры – класс соединений на основе органических карбоновых кислот, у которых атом водорода в гидроксильной группе замещен на углеводородный радикал R. Фомулу сложных эфиров в общем виде можно записать как:
Например:
Нитросоединения
Нитросоединения – производные углеводородов, у которых один или несколько атомов водорода заменены на нитрогруппу –NO2.
Предельные нитросоединения с одной нитрогруппой имеют общую молекулярную формулу CnH2n+1NO2
Аминокислоты
Соединения, имеющие в своей структуре одновременно две функциональные группы – амино NH2 и карбоксильную – COOH. Например,
NH2-CH2-COOH
Предельные аминокислоты с одной карбоксильной и одной аминогруппой изомерны соответствующим предельными нитросоединениям т.е. как и они имеют общую молекулярную формулу CnH2n+1NO2
В заданиях ЕГЭ на классификацию органических веществ важно уметь записывать общие молекулярные формулы гомологических рядов разных типов соединений, зная особенности строения углеродного скелета и наличия тех или иных функциональных групп. Для того, чтобы научиться определять общие молекулярные формулы органических соединений разных классов, будет полезен материал по этой теме.
Номенклатура органических соединений
Особенности строения и химических свойств соединений находят отражение в номенклатуре. Основными типами номенклатуры считаются систематическая и тривиальная.
Систематическая номенклатура фактически прописывает алгоритмы, в соответствии с которыми то или иное название составляется в строгом соответствии с особенностями строения молекулы органического вещества или, грубо говоря, его структурной формулы.
Рассмотрим правила составления названий органических соединений по систематической номенклатуре.
При составлении названий органических веществ по систематической номенклатуре наиболее важным является правильно определить число атомов углерода в наиболее длинной углеродной цепи или посчитать число атомов углерода в цикле.
В зависимости от количества атомов углерода в основной углеродной цепи, соединения, будут иметь в своем названии различный корень:
|
Количество атомов С в главной углеродной цепи |
Корень названия |
|
1 |
мет- |
|
2 |
эт- |
|
3 |
проп- |
|
4 |
бут- |
|
5 |
пент- |
|
6 |
гекс- |
|
7 |
гепт- |
|
8 |
окт- |
|
9 |
нон- |
|
10 |
дек(ц)- |
Вторая важная составляющая, учитываемая при составлении названий, — наличие/отсутствие кратных связей или функциональной группы, которые перечислены в таблице выше.
Попробуем дать название веществу, имеющему структурную формулу:
1. В главной (и единственной) углеродной цепи данной молекулы содержится 4 атома углерода, поэтому название будет содержать корень бут-;
2. В углеродном скелете отсутствуют кратные связи, следовательно, суффикс, который нужно использовать после корня слова будет -ан, как и у соответствующих предельных ациклических углеводородов (алканов);
3. Наличие функциональной группы –OH при условии, что нет более старших функциональных групп добавляет после корня и суффикса из п.2. еще один суффикс – «ол»;
4. В молекулах содержащих кратные связи или функциональные группы, нумерация атомов углерода главной цепи начинается с той стороны молекулы, к которой они ближе.
Рассмотрим еще один пример:
Наличие в главной углеродной цепи четырех атомов углерода говорит нам о том, что основой названия является корень «бут-», а отсутствие кратных связей говорит о суффиксе «-ан», который будет следовать сразу после корня. Старшая группа в данном соединении – карбоксильная, она и определяет принадлежность этого вещества к классу карбоновых кислот. Следовательно, окончание у названия будет «-овая кислота». При втором атоме углерода находится аминогруппа NH2—, поэтому данное вещество относится к аминокислотам. Также при третьем атоме углерода мы видим углеводородный радикал метил (CH3—). Поэтому по систематической номенклатуре данное соединение называется 2-амино-3-метилбутановая кислота.
Тривиальная номенклатура, в отличие от систематической, как правило, не имеет связи со строением вещества, а обусловлена по большей части его происхождением, а также химическими или физическими свойствами.
| Формула | Название по систематической номенклатуре | Тривиальное название |
| Углеводороды | ||
| CH4 | метан | болотный газ |
| CH2=CH2 | этен | этилен |
| CH2=CH-CH3 | пропен | пропилен |
| CH≡CH | этин | ацетилен |
| CH2=CH-CH= CH2 | бутадиен-1,3 | дивинил |
| 2-метилбутадиен-1,3 | изопрен | |
| метилбензол | толуол | |
| 1,2-диметилбензол | орто-ксилол (о-ксилол) |
|
| 1,3-диметилбензол | мета-ксилол (м-ксилол) |
|
| 1,4-диметилбензол | пара-ксилол (п-ксилол) |
|
| винилбензол | стирол | |
| Спирты | ||
| CH3OH | метанол | метиловый спирт, древесный спирт |
| CH3CH2OH | этанол | этиловый спирт |
| CH2=CH-CH2-OH | пропен-2-ол-1 | аллиловый спирт |
| этандиол-1,2 | этиленгликоль | |
| пропантриол-1,2,3 | глицерин | |
| фенол (гидроксибензол) |
карболовая кислота | |
| 1-гидрокси-2-метилбензол | орто-крезол (о-крезол) |
|
| 1-гидрокси-3-метилбензол | мета-крезол (м-крезол) |
|
| 1-гидрокси-4-метилбензол | пара-крезол (п-крезол) |
|
| фенилметанол | бензиловый спирт | |
| Альдегиды и кетоны | ||
| метаналь | формальдегид | |
| этаналь | уксусный альдегид, ацетальдегид | |
| пропеналь | акриловый альдегид, акролеин | |
| бензальдегид | бензойный альдегид | |
| пропанон | ацетон | |
| Карбоновые кислоты | ||
| метановая кислота | муравьиная кислота (соли и сложные эфиры — формиаты) |
|
| этановая кислота | уксусная кислота
(соли и сложные эфиры — ацетаты) |
|
| пропановая кислота | пропионовая кислота (соли и сложные эфиры — пропионаты) |
|
| C15H31COOH | гексадекановая кислота | пальмитиновая кислота (соли и сложные эфиры — пальмитаты) |
| C17H35COOH | октадекановая кислота | стеариновая кислота (соли и сложные эфиры — стеараты) |
| пропеновая кислота | акриловая кислота (соли и сложные эфиры — акрилаты) |
|
| HOOC-COOH | этандиовая кислота | щавелевая кислота (соли и сложные эфиры — оксалаты) |
| 1,4-бензолдикарбоновая кислота | терефталевая кислота | |
| Сложные эфиры | ||
| HCOOCH3 | метилметаноат | метилформиат, метиловый эфир мурвьиной кислоты |
| CH3COOCH3 | метилэтаноат | метилацетат, метиловый эфир уксусной кислоты |
| CH3COOC2H5 | этилэтаноат | этилацетат, этиловый эфир уксусной кислоты |
| CH2=CH-COOCH3 | метилпропеноат | метилакрилат, метиловый эфир акриловый кислоты |
| Азотсодержащие соединения | ||
| аминобензол, фениламин |
анилин | |
| NH2-CH2-COOH | аминоэтановая кислота | глицин, аминоуксусная кислота |
| 2-аминопропионовая кислота | аланин |
Качественные реакции органической химии.
1. Качественная реакция на алканы. Определить, что какое-то вещество в смеси или в чистом виде алкан, несложно. Для этого газ либо поджигают — горение алканов сопровождается синим пламенем, либо пропускают через раствор перманганата калия. Алканы не окисляются перманганатом калия на холоду, вследствие этого раствор не будет изменять окраску.
2. Качественная реакция на алкены. Чтобы убедиться в наличии алкена, нужно пропустить его в раствор перманганата калия (реакция Вагнера). В ходе реакции раствор обесцветится, выпадает бурый диоксид марганца MnO2 (реакция на примере этилена):
3C2H4 + 2KMnO4 + 4H2O ——> 3CH2OH-CH2OH + 2KOH + 2MnO2↓
Так же, алкены обесцвечивают бромную воду:
C2H4 + Br2 ——> C2H4Br2
Бромная вода обесцвечивается, образуется дибромпроизводное.
3. Качественная реакция на алкины. Алкины можно выявить и по реакции Вагнера или с помощью бромной воды:
3C2H2 + 8KMnO4 ——> 3KOOC-COOK + 8MnO2↓ + 2KOH + 2H2O
C2H2 + 2Br2 —-> C2H2Br4
Алкины с тройной связью у крайнего атома углерода реагируют с аммиачным раствором оксида серебра (гидроксид диаминсеребра (I)) (реактив Толленса):
C2H2 + 2[Ag(NH3)2]OH ——-> Ag2C2↓ + 4NH3↑ + 2H2O
Получившийся ацетиленид серебра (I) выпадает в осадок.
Алкины, у которых тройная связь в середине (R-C-=C-R) в эту реакцию невступают.
Такая способность алкинов — замещать протон на атом металла, подобно кислотам — обусловлено тем, что атом углерода находится в состоянии sp-гибридизации и электроотрицательность атома углерода в таком состоянии такая же, как у азота. Вследствие этого, атом углерода сильнее обогощается электронной плотностью и протон становится подвижным.
4. Качественная реакция на альдегиды. Одна из самых интересных качественных реакций в органической химии — на альдегиды, предназначена исключительно для выявления соединений, содержащих альдегидную группу. К альдегиду приливают аммиачный раствор оксида серебра, реакция идет при нагревании:
CH3-CHO + 2[Ag(NH3)2]OH —t—> CH3-COOH + 2Ag↓ + 4NH3↑ + H2O
Если опыт проведен грамотно, то выделяющееся серебро покрывает колбу ровным слоем, создавая эффект зеркала. Именно поэтому реакция называется реакцией серебряного зеркала.
Примечание: реакцией серебряного зеркала также можно выявить метановую (муравьиную) кислоту HCOOH. При чем тут кислота, если мы говорим про альдегиды? Все просто: муравьиная кислота — единственная из карбоновых кислот, содержащая одновременно альдегидную и карбоксильную группы:
В ходе реакции метановая кислота окисляется до угольной, которая разлагается на углекислый газ и воду:
HCOOH + 2[Ag(NH3)2]OH —t—> CO2↑ + 2H2O + 4NH3↑ + 2Ag↓
Помимо реакции серебряного зеркала существует также реакция с гидроксидом меди (II) Cu(OH)2. Для этого к свежеприготовленному гидроксиду меди (II) добавляют альдегид и нагревают смесь:
CuSO4 + 2NaOH ——> Na2SO4 + Cu(OH)2↓
CH3-CHO + 2Cu(OH)2 —t—> CH3-COOH + Cu2O↓ + 2H2O
Выпадает оксид меди (I) Cu2O — осадок красного цвета.
Еще один метод определения альдегидов — реакция с щелочным раствором тетраиодомеркурата (II) калия, известный нам из предыдущей статьи как реактив Несслера:
CH3-CHO + K2[HgI4] + 3KOH ——> CH3-COOK + Hg↓ + 4KI + 2H2O
При добавлении альдегида к раствору фуксинсернистой кислоты раствор окрашивается в светло-фиолетовый цвет.
5. Качественные реакции на спирты. Спирты по количеству гидроксильных групп бывают одно-, двух-, многоатомными. Для одно- и многоатомных реакции различны.
Качественные реакции на одноатомные спирты:
Простейшая качественная реакция на спирты — окисление спирта оксидом меди. Для этого пары спирта пропускают над раскаленным оксидом меди. Затем полученный альдегид улавливают фуксинсернистой кислотой, раствор становится фиолетовым:
CH3-CH2-OH + CuO —t—> CH3-CHO + Cu + H2O
Спирты идентифицируются пробой Лукаса — конц. раствор соляной кислоты и хлорида цинка. При пропускании вторичного или третичного спирта в такой раствор образуется маслянистый осадок соответствующего алкилхлорида:
CH3-CHOH-CH3 + HCl —ZnCl2—> CH3-CHCl-CH3↓ + H2O
Первичные спирты в реакцию не вступают.
Еще одним известным методом является иодоформная проба:
CH3-CH2-OH + 4I2 + 6NaOH ——> CHI3↓ + 5NaI + HCOONa + 5H2O
Качественные реакции на многоатомные спирты.
Наиболее известная качественная реакция на многоатомные спирты — взаимодействие их с гидроксидом меди (II). Гидроксид растворяется, образуется хелатный комплекс темно-синего цвета. Обратите внимание на то, что в отличии от альдегидов многоатомные спирты реагируют с гидроксидом меди (II) без нагревания. К примеру, при приливании глицерина образуется глицерат меди (II):
6. Качественные реакции на карбоновые кислоты. На карбоновые кислоты обычно подчеркивают образование цветных осадков с тяжелыми металлами. Но наиболее осуществимая качественная реакция на метановую кислоту HCOOH. При добавлении концентрированной серной кислоты H2SO4 к раствору муравьиной кислоты образуется угарный газ и вода:
HCOOH —H2SO4—> CO↑ + H2O
Угарный газ можно поджечь. Горит синем пламенем:
2CO + O2 —t—> 2CO2
Из многоосновных кислот рассмотрим качественную реакцию на щавелевую H2C2O4(HOOC-COOH). При добавлении к раствору щавелевой кислоты раствор соли меди (II) выпадет осадок оксалата меди (II):
Cu2+ + C2O42- ——> CuC2O4↓
Щавелевая кислота также, как и муравьиная, разлагается концентрированной серной кислотой:
H2C2O4 —-H2SO4—> CO↑ + CO2↑ + H2O
7. Качественные реакции на амины. На амины качественных реакций нет (за исключением анилина). Можно доказать наличие амина окрашиванием лакмуса в синий цвет. Если же амины нельзя выявить, то можно различить первичный амин от вторичного путем взаимодействия с азотистой кислотой HNO2. Для начала нужно ее приготовить, а затем добавить амин:
NaNO2 + HCl ——> NaCl + HNO2
Первичные дают азот N2:
CH3-NH2 + HNO2 ——> CH3-OH + N2↑ + H2O
Вторичные — алкилнитрозоамины — вещества с резким запахом (на примере диметилнитрозоамина):
CH3-NH-CH3 + HNO2 ——> CH3-N(NO)-CH3 + H2O
Третичные амины в мягких условиях с HNO2 не реагируют.
Анилин образует осадок при добавлении бромной воды:
C6H5NH2 + 3Br2 ——> C6H2NH2(Br)3↓ + 3HBr
Анилин также можно обнаружить по сиреневой окраске при добавлении хлорной извести.
8. Качественные реакции на фенол. Фенол лучше всего обнаруживает хлорид железа (III) — образуется фиолетовое окрашивание раствора. Это лучший метод обнаружения фенола, т.к. реакция очень чувствительна.
Также фенол наряду с анилином дает осадок желтоватого цвета при пропускании в водный раствор брома — 2,4,6 — трибромфенол:
C6H5OH + 3Br2 ——> C6H2OH(Br)3↓ + 3HBr
Фенолы дают фенол-альдегидные смолы при реакции с альдегидом в кислой среде. При этом образуются мягкие пористые массы фенол-альдегидных смол (реакция поликонденсации).
9. Качественная реакция на алкилхлориды. Вещества, содержащие хлор, могут окрашивать пламя в зеленый цвет. Для этого нужно обмакнуть медную проволоку в алкилхлориде и поднести к пламени (проба Бельштейна).
10. Качественная реакция на углеводы. Большинство углеводов имеют альдегидные и гидроксильные группы, поэтому для них характерны все реакции альдегидов и многоатомных спиртов.
Существует способ, который помогает различить глюкозу от фруктозы — проба Селиванова. Для того, чтобы различить эти углеводы, к ним приливают смесь резорцина и соляной кислоты. Реагирует со смесью фруктоза, при этом раствор окрашивается в малиновый цвет.
Крахмал в присутствии иода окрашивается в темно-синий цвет. При нагревании окраска исчезает, при охлаждении появляется вновь.
11. Качественная реакция на белки. Белки выявляются в основном на реакциях, основанных на окрасках.
Ксантопротеиновая реакция. Данная реакция обнаруживает ароматические аминокислоты, входящие в белки (на примере тирозина):
(OH)C6H4CH(NH2)COOH + HNO3 —-H2SO4——> (OH)C6H3(NO2)CH(NH2)COOH↓ + H2O — выпадает осадок желтого цвета.
(OH)C6H3(NO2)CH(NH2)COOH + 2NaOH ——-> (ONa)C6H3(NO2)CH(NH2)COONa + H2O — раствор становится оранжевым.
Обнаружение серосодержащих аминокислот:
Белок + (CH3COO)2Pb —NaOH—> PbS↓ (осадок черного цвета).
Биуретовая реакция для обнаружения пептидной связи (CO-NH):
Белок + CuSO4 + NaOH ——> красно-фиолетовое окрашивание.
Спецефический запах при горении:
Белок —-обжиг—-> запах паленой шерсти.


СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой

Была в сети 15.10.2022 09:22
Давыдова Лариса Ивановна
Учитель химии
66 лет
23 011
682
Таблица «Общие формулы классов органических веществ»
07.01.2022 22:38
Таблица поможет обучающимся систематизировать знания по органической химии
Просмотр содержимого документа
«Таблица «Общие формулы классов органических веществ»»
|
Класс органических веществ |
Общая молекулярная формула |
|
Алканы |
CnH2n+2 |
|
Алкены |
CnH2n |
|
Циклоалканы |
CnH2n |
|
Алкины |
CnH2n−2 |
|
Алкадиены |
CnH2n−2 |
|
Арены |
CnH2n−6 |
|
Предельные одноатомные спирты |
CnH2n+2O |
|
Простые эфиры |
CnH2n+2O |
|
Предельные двухатомные спирты |
CnH2n+2O2 |
|
Предельные трехатомные спирты |
CnH2n+2O3 |
|
Многоатомные спирты |
CnH2n+2Ox |
|
Ароматические спирты |
CnH2n−6O |
|
Фенолы |
CnH2n−6O |
|
Предельные альдегиды |
CnH2nO |
|
Кетоны |
CnH2nO |
|
Предельные карбоновые кислоты |
CnH2nO2 |
|
Сложные эфиры |
CnH2nO2 |
|
Амины предельные |
CnH2n+3N |
|
Амины ароматические |
CnH2n-5N |
|
Аминокислоты (предельные одноосновные) |
CnH2n+1NН2 |
Рекомендуем курсы ПК и ППК для учителей
Похожие файлы
В этой статье мы разберем, как составлять молекулярные формулы основных классов органических соединений из информации об особенностях строения (наличие кратных связей, циклов, функциональных групп), и наоборот — как определять общую формулу гомологического ряда веществ с определенными функциональными группами, кратными связями или циклами.
Углеводороды
За основу берем формулу алканов — предельных нециклических углеводородов с одинарными связями между атомами углерода.
В молекуле линейных алканов на каждый атом углерода приходится по два атома водорода плюс по одному дополнительному атому водорода на концах углеродной цепи:
Таким образом, общая формула предельных нециклических углеводородов (алканов) — CnH2n+2.
В алкенах присутствует одна двойная связь. Двойная связь «отщипывает» от молекулы два атома водорода:
Таким образом, общая формула нециклических углеводородов, в молекулах которых есть одна двойная связь (алкенов) CnH2n+2-2 — CnH2n.
Формулы алкенов отличаются от формул алканов с таким же количеством атомов углерода на 2 атома водорода:
C3H8 — C3H6 = 2H
Каждая пара атомов водорода определяет степень ненасыщенности молекулы. Степень ненасыщенности алкенов равна одному.
В алкинах присутствует одна тройная связь. Тройная связь «отщипывает» от молекулы уже четыре атома водорода:
| Ацетилен, этин | H-C≡C-H |
| Пропин | H-C≡C-СH3 |
| Бутин-1 | H-C≡C-СH2-СH3 |
Таким образом, общая формула нециклических углеводородов, в молекулах которых есть одна тройная связь (алкинов): CnH2n+2-4 — CnH2n-2.
Формулы алкинов отличаются от формул алканов с таким же количеством атомов углерода на 4 водорода:
C3H8 — C3H4 = 4H
Степень ненасыщенности алкинов равна двум.
В алкадиенах присутствуют две двойные связи. Две двойные связи «отщипывают» от молекулы уже четыре атома водорода:
Таким образом, общая формула нециклических углеводородов, в молекулах которых есть две двойные связи (алкадиенов): CnH2n+2-4 — CnH2n-2.
Степень ненасыщенности алкадиенов также равна двум.
В циклоалканах присутствуют только одинарные связи и атомы углерода образуют замкнутый цикл. Наличие цикла также уменьшает количество атомов водорода на два:
Таким образом, общая формула циклических углеводородов, в молекулах которых есть только одинарные связи (циклоалканов): CnH2n+2-2 — CnH2n.
В циклоалкенах присутствует одна одинарная связь и атомы углерода образуют замкнутый цикл. Наличие цикла и двойной связи уменьшает количество атомов водорода на четыре:
| Циклобутен |  |
Таким образом, общая формула циклических углеводородов, в молекулах которых есть одна двойная связь (циклоалкенов): CnH2n+2-4 — CnH2n-2.
Этот ряд можно продолжить и дальше:
Алкатриены — содержат три двойные связи, общая формула: CnH2n+2-6 = CnH2n-4
Алкенины — содержат одну двойную и одну тройную связь, общая формула:
CnH2n+2-6 = CnH2n-4
и так далее.
| Класс/группа | Тип связей и наличие цикла | Степень ненасыщенности | Общая формула |
| Алканы |
одинарные связи |
0 | CnH2n+2 |
| Алкены | двойная связь | 1 | CnH2n |
| Алкины | тройная связь | 2 | CnH2n-2 |
| Алкадиены | две двойные связи | 2 | CnH2n-2 |
| Циклоалканы | одинарные связи, цикл | 2 | CnH2n |
| Циклоалкены | двойная связь, цикл | 2 | CnH2n-2 |
| Циклоалкины | тройная связь, цикл | 6 | CnH2n-4 |
| Циклоалкадиены | две двойные связи, цикл | 6 | CnH2n-4 |
Определите молекулярную формулу и степень ненасыщенности гомологического ряда следующих классов органических веществ:
а) алкадиенины
б) циклоалкины
в) циклоалкатриены
г) алкендиины
а) CnH2n-6, степень ненасыщенности 4, не хватает 8 атомов Н до алкана
б) CnH2n-4, степень ненасыщенности 3, не хватает 6 атомов Н до алкана
в)CnH2n-6, степень ненасыщенности 4, не хватает 8 атомов Н до алкана
г) CnH2n-8, степень ненасыщенности 5, не хватает 10 атомов Н до алкана
Эта система работает и наоборот: знание молекулярной формулы можно определить возможный состав вещества.
Например, проанализируем формулу С3Н6.
До формулы алкана не хватает С3Н8 — С3Н6 = 2Н два атома водорода.
Степень непредельности равна одному. То есть в молекуле органического вещества есть либо цикл, либо двойная связь.
Определите возможную структуру (наличие кратных связей, циклов) молекул, которым соответствуют следующие формулы:
а) CnH2n-2
б) CnH2n-4
в) CnH2n-6
г) CnH2n-8
а) CnH2n-2, степень ненасыщенности 4, в молекуле либо две двойные связи, либо цикл и двойная связь, либо тройная связь
б) CnH2n-4, степень ненасыщенности 6, в молекуле либо три двойные связи; цикл и тройная связь; тройная связь и двойная связь и др.
в) CnH2n-6, степень ненасыщенности 8:
4 двойные связи; цикл и 3 двойные связи; две тройные связи; тройная связь и две двойные связи и др.
г) CnH2n-8, степень ненасыщенности 10:
5 двойных связей; цикл и 4 двойные связи и др.