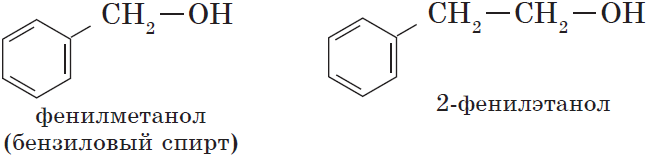
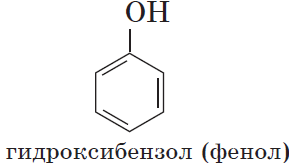
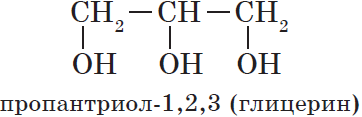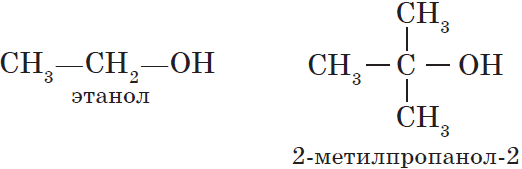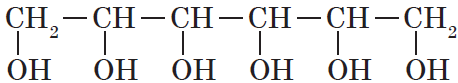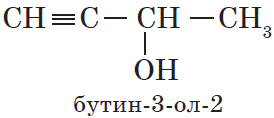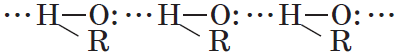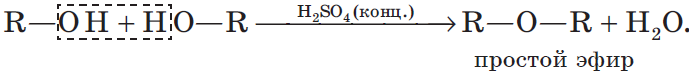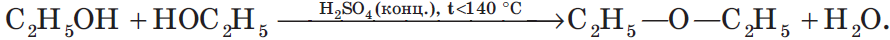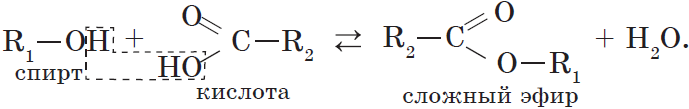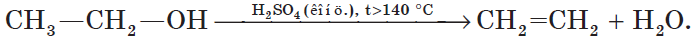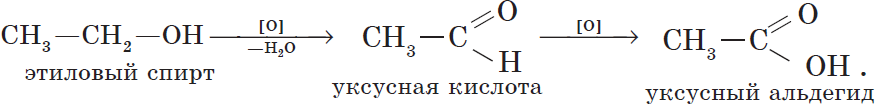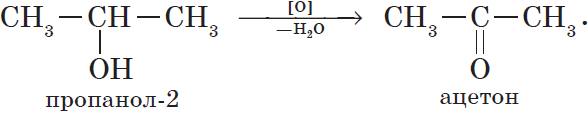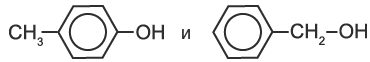Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
Строение, изомерия и гомологический ряд спиртов
Химические свойства спиртов
Способы получения спиртов
Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам.
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Химические свойства спиртов
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н+ соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
- слабые кислотные свойства, замещение водорода на металл;
- замещение группы ОН
- отрыв воды (элиминирование) – дегидратация
- окисление
- образование сложных эфиров — этерификация
1. Кислотные свойства
Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды.
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция практически не идет.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Спирты взаимодействуют с активными металлами. При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
Например, этанол взаимодействует с калием с образованием этилата калия и водорода.
Видеоопыт взаимодействия спиртов (метанола, этанола и бутанола) с натрием можно посмотреть здесь.
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Например, этилат калия разлагается водой:
CH3OH > первичные спирты > вторичные спирты > третичные спирты
Многоатомные спирты также реагируют с активными металлами:
Видеоопыт взаимодействия глицерина с натрием можно посмотреть здесь.
1.3. Взаимодействие с гидроксидом меди (II)
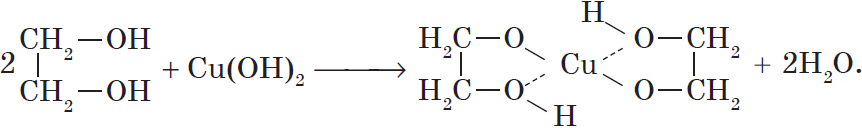
Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
Например, при взаимодействии этиленгликоля со свежеосажденным гидроксидом меди (II) образуется ярко-синий раствор гликолята меди:
Видеоопыт взаимодействия этиленгликоля с гидроксидом меди (II) можно посмотреть здесь.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
Например, этанол реагирует с бромоводородом.
Видеоопыт взаимодействия этилового спирта с бромоводородом можно посмотреть здесь.
третичные > вторичные > первичные > CH3OH.
Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами.
Например, этиленгликоль реагирует с бромоводородом:
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
Например, при взаимодействии этанола с аммиаком образуется этиламин.
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
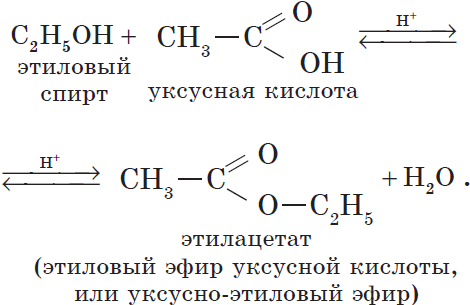
Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты):
Многоатомные спирты вступают в реакции этерификации с органическими и неорганическими кислотами.
Например, этиленгликоль реагирует с уксусной кислотой с образованием ацетата этиленгликоля:
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат:
Например, глицерин под действием азотной кислоты образует тринитрат глицерина (тринитроглицерин):
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен:
В качестве катализатора этой реакции также используют оксид алюминия.
Отщепление воды от несимметричных спиртов проходит в соответствии с правилом Зайцева: водород отщепляется от менее гидрогенизированного атома углерода.
Например, в присутствии концентрированной серной кислоты при нагревании выше 140оС из бутанола-2 в основном образуется бутен-2:
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
Например, при дегидратации этанола при температуре до 140оС образуется диэтиловый эфир:
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
Первичный спирт → альдегид → карбоновая кислота
Метанол → формальдегид → углекислый газ
Вторичные спирты окисляются в кетоны: вторичные спирты → кетоны
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол < первичные спирты < вторичные спирты < третичные спирты
Продукты окисления многоатомных спиртов зависят от их строения. При окислении оксидом меди многоатомные спирты образуют карбонильные соединения.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, этанол окисляется оксидом меди до уксусного альдегида
Видеоопыт окисления этанола оксидом меди (II) можно посмотреть здесь.
Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона
Третичные спирты окисляются только в жестких условиях.
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, при окислении пропанола-1 образуется пропаналь
Видеоопыт каталитического окисления этанола кислородом можно посмотреть здесь.
Например, пропанол-2 окисляется кислородом при нагревании в присутствии меди до ацетона
Третичные спирты окисляются только в жестких условиях.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот, вторичные спирты окисляются до кетонов, метанол окисляется до углекислого газа.
При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси.
Третичные спирты окисляются только в жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов. При этом происходит разрыв углеродной цепи и могут образоваться углекислый газ, карбоновая кислота или кетон, в зависимости от строения спирта.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Первичный спирт R-СН2-ОН | R-COOH/ R-CHO | R-COOK/ R-CHO |
| Вторичный спирт R1-СНОН-R2 | R1-СО-R2 | R1-СО-R2 |
Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ
Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота
Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2n+1ОН + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
Например, уравнение сгорания метанола:
2CH3OH + 3O2 = 2CO2 + 4H2O
5. Дегидрирование спиртов
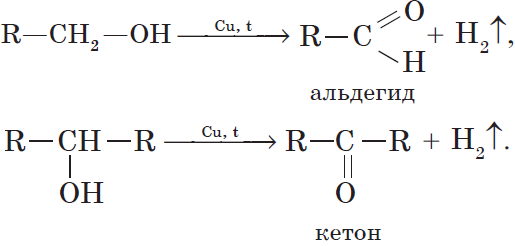
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола и первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
Например, при дегидрировании этанола образуется этаналь
Например, при дегидрировании этиленгликоля образуется диальдегид (глиоксаль)
Спирты — кислородсодержащие органические соединения, функциональной группой которых является гидроксогруппа (OH) у
насыщенного атома углерода.
Спирты также называют алкоголи. Первый член гомологического ряда — метанол — CH3OH.
Общая формула их гомологического ряда — CnH2n+1OH.
Классификация спиртов
По числу OH групп спирты бывают одноатомными (1 группа OH), двухатомными (2 группы OH — гликоли), трехатомными (3 группы
OH — глицерины) и т.д.

Одноатомные спирты также подразделяются в зависимости от положения OH-группы: первичные (OH-группа у первичного атома углерода),
вторичные (OH-группа у вторичного атома углерода) и третичные (OH-группа у третичного атома углерода).

Номенклатура и изомерия спиртов
Названия спиртов формируются путем добавления суффикса «ол» к названию алкана с соответствующим числом атомов углерода: метанол,
этанол, пропанол, бутанол, пентанол и т.д.

Для спиртов характерна изомерия углеродного скелета (начиная с бутанола), положения функциональной группы и межклассовая изомерия с
простыми эфирами, которых мы также коснемся в данной статье.

Получение спиртов
- Гидролиз галогеналканов водным раствором щелочи
- Гидратация алкенов
- Восстановление карбонильных соединений
- Получение метанола из синтез-газа
- Получение этанола брожением глюкозы
- Окисление алкенов KMnO4 в нейтральной (водной) среде
Помните, что в реакциях галогеналканов со сПИртовым раствором щелочи получаются Пи-связи (π-связи) — алкены, а в реакциях с водным раствором
щелочи образуются спирты.

Присоединения молекулы воды (HOH) протекает по правилу Марковникова. Атом водорода направляется к наиболее гидрированному атому углерода,
а гидроксогруппа идет к соседнему, наименее гидрированному, атому углерода.

В результате восстановления альдегидов и кетонов получаются соответственно первичные и вторичные спирты.

Синтез газом в промышленности называют смесь угарного газа и водорода, которая используется для синтеза различных
химических соединений, в том числе и метанола.
CO + 2H2 → (t,p,кат.) CH3-OH
В ходе брожения глюкозы выделяется углекислый газ и образуется этанол.

В результате такой реакции у атомов углерода, прилежащих к двойной связи, формируются гидроксогруппы — образуется двухатомный спирт (гликоль).

Химические свойства спиртов
Предельные спирты (не содержащие двойных и тройных связей) не вступают в реакции присоединения, это насыщенные кислородсодержащие соединения.
У спиртов проявляются новые свойства, которых мы раньше не касались в органической химии — кислотные.
- Кислотные свойства
- Реакция с галогеноводородами
- Реакции с кислотами
- Дегидратация спиртов
- Диметиловый эфир — CH3-O-CH3
- Метилэтиловый эфир — CH3-O-C2H5
- Диэтиловый эфир — C2H5-O-C2H5
- Окисление спиртов
- Качественная реакция на многоатомные спирты
- Кислотные свойства многоатомных спиртов
Щелочные металлы (Li, Na, K) способны вытеснять водород из спиртов с образованием солей: метилатов, этилатов, пропилатов и т.д.

Необходимо особо заметить, что реакция с щелочами (NaOH, KOH, LiOH) для предельных одноатомных спиртов невозможна, так как образующиеся
алкоголяты (соли спиртов) сразу же подвергаются гидролизу.
Реакция с галогеноводородами протекают как реакции обмена: атом галогена замещает гидроксогруппу, образуется молекула воды.

В результате реакций спиртов с кислотами образуются различные эфиры.

Дегидратация спиртов (отщепление воды) идет при повышенной температуре в присутствии серной кислоты (водоотнимающего) компонента.
Возможен межмолекулярный механизм дегидратации (при t < 140°С), в результате которого образуются простые эфиры. При более
высокой температуре (t > 140°С) механизм дегидратации становится внутримолекулярный — образуются алкены.
Названия простых эфиров формируются проще простого — по названию радикалов, входящих в состав эфира. Например:

Качественной реакцией на спирты является взаимодействие с оксидом меди II. В ходе такой реакции раствор приобретает характерное фиолетовое
окрашивание.
Замечу, что в обычных условиях третичные спирты окислению не подвергаются. Для них необходимы очень жесткие условия, при
которых углеродный скелет подвергается деструкции.

Вторичные и третичные спирты определяются другой качественной реакцией с хлоридом цинка II и соляной кислотой. В результате такой
реакции выпадает маслянистый осадок.

Первичные спирты окисляются до альдегидов, а вторичные — до кетонов. Альдегиды могут быть окислены далее — до карбоновых кислот, в отличие
от кетонов, которые являются «тупиковой ветвью развития» и могут только снова стать вторичными спиртами.

Такой реакцией является взаимодействие многоатомного спирта со свежеприготовленным гидроксидом меди II. В результате реакции раствор
окрашивается в характерный синий цвет.

Важным отличием многоатомных спиртов от одноатомных является их способность реагировать со щелочами (что невозможно для одноатомных спиртов).
Это говорит об их более выраженных кислотных свойствах.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
СВОЙСТВА ОДНОАТОМНЫХ СПИРТОВ
ОДНОАТОМНЫЕ СПИРТЫ содержат в углеводородной цепи одну гидроксильную группу ОН.
Общая формула CnH2n+1–OH или CnH2n+2O.
СТРОЕНИЕ ГИДРОКСИЛЬНОЙ ГРУППЫ.
Связи О–Н и С–О – полярные ковалентные.
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Атому кислорода в спиртах свойственна sp3-гибридизация, валентный угол C–О–H близок к тетраэдрическому.
ФИЗИЧЕСКИЕ СВОЙСТВА СПИРТОВ
Следствием полярности связи О–Н является способность гидроксисоединений к образованию водородных связей:
Поэтому даже низшие спирты — жидкости с относительно высокой температурой кипения (t кип. метанола +64,5оС).
При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.
Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
Спирты, содержащие до 15 атомов углерода – жидкости, 15 и более – твердые вещества.
Растворимость в воде зависит от молекулярной массы, чем она выше, тем спирт хуже растворяется воде. Так, низшие спирты (до пропанола) смешиваются с водой в любых пропорциях, а высшие практически не растворимы в ней.
Температура кипения также возрастает с увеличением атомной массы. Чем выше температура кипения, тем ниже летучесть, т.е. вещество плохо испаряется, что объясняется возникновением межмолекулярной водородной связи между отдельными молекулами самого соединения или спирта и воды
ХИМИЧЕСКИЕ СВОЙСТВА
В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
С–ОН с замещением или отщеплением ОН-группы
О–Н с замещением водорода.
ЗАМЕЩЕНИЕ В ГИДРОКСИЛЬНОЙ ГРУППЕ
ОН – поляризована (некоторая кислотность)
1.С активными металлами (Na, K, Mg), образуя соли — алкоголяты (алкоксиды):
Реакционная способность одноатомных спиртов в реакциях по связи О–Н:
CH3OH > первичные > вторичные > третичные.
Алкоголяты нестойкие и под действием воды полностью гидролизуются с выделением спирта и гидроксида металла:
Со щелочами одноатомные спирты НЕ реагируют.
2. Образование сложных эфиров.
Спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры (этерификация).
ЗАМЕЩЕНИЕ ГИДРОКСИЛЬНОЙ ГРУППЫ -ОН
1. Реакции замещения ОН на галоген:
происходит в реакции с галогеноводородами или другими галогенсодержащими веществами в присутствии сильной кислоты (конц. H2SO4).
Реакционная
способность:
третичные
> вторичные > первичные > CH3OH
1. Внутримолекулярная дегидратация: образуются алкены.
Идет в присутствии концентрированной серной кислоты или водоотнимающих оксидов при повышенной температуре:
Дегидратация спиртов с длинной углеродной цепью идет по правилу Зайцева – водород отщепляется от менее гидрогенизированного атома углерода.
Основной
продукт – бутен-2.
2. Межмолекулярная дегидратация: образуются простые эфиры.
При межмолекулярной дегидратации спиртов также происходит нуклеофильное замещение: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы.
3. Реакция Лебедева –
это получение бутадиена каталитическим пиролизом этилового спирта
ОКИСЛЕНИЕ
1.Горение —> углекислый газ и вода
2. Окисление спиртов ( CuO (to), O2 (кат.Cu, to), KMnO₄, K₂Cr₂O₇),
а также дегидрирование при нагревании над медной сеткой.
(первичные окисляются до альдегидов, вторичные до кетонов, третичные более устойчивые – разрыв цепи):
3)Окисление подкисленным раствором перманганата калия приводит к образованию карбоновых кислот:
ИСКЛЮЧЕНИЕ: Окисление метанола ведет к образованию углекислого газа!!!
4) Окисление подкисленным раствором дихромата калия приводит к образованию карбоновых кислот:
Качественная реакция одноатомных спиртов– цвет из оранжевого переходит в зеленый (определение содержания алкоголя)
СВОЙСТВА МНОГОАТОМНЫХ СПИРТОВ
Многоатомные (две и более групп -ОН). Общая формула CnH2n+2Om.
Современное название многоатомных спиртов — полиолы (диолы, триолы и т.д).
Этиленгликоль и глицерин вязкие, сладкие на вкус жидкости, сорбит — белый порошок, все вещества хорошо растворимые в воде.
ХИМИЧЕСКИЕ СВОЙСТВА.
1.Замещение Н –атома (кислотные свойства).
Этиленгликоль, глицерин вследствие взаимного влияния атомов (-I-эффект ОН-групп) являются более сильными кислотами, чем одноатомные спирты.
Образуют соли не только в реакциях с активными металлами, но и под действием щелочей (частично и обратимо):
2.Взаимодействие с раствором гидроксида меди (II) в присутствии щелочи
с образованием комплексных соединений (качественная реакция на многоатомные спирты ). Голубой осадок гидроксида меди растворяется с образованием синего комплексного соединения многоатомного спирта.
3.Образование сложных эфиров
Реакция с азотной кислотой.
4. Образование жиров.
Жиры — это сложные эфиры, продукты взаимодействия глицерина с высшими карбоновыми кислотами.
5. Взаимодействие с галогеноводородами
Замещение -ОН на галоген:
Реагируют также, как и одноатомные спирты.
6. Окисление.
Так же, как и одноатомные спирты – оксидом меди или над медной сеткой (каталитическое дегидрирование) многоатомные спирты окисляются в карбонильные соединения.
Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром.
Общая формула – СnH2n-7OH n>6 (для фенолов с одной ОН-группой)
ФИЗИЧЕСКИЕ СВОЙСТВА ФЕНОЛА
Это твёрдое бесцветное вещество с резким запахом.
При температуре больше 70 °C растворяется в воде в любых отношениях. Фенол ядовит.
Неподеленная электронная пара атома кислорода взаимодействует (вступает в сопряжение с ароматической π-системой, в результате:
Увеличивается электронная плотность на ароматической системе, происходит ее перераспределение, и на атомах 2,4,6 появляется избыточный отрицательный заряд;
Электронная пара связи О-Н смещается к атому кислорода, и связь становится менее прочной (по сравнению со спиртами)
ХИМИЧЕСКИЕ СВОЙСТВА ФЕНОЛА
Проявляет свойства слабой кислоты. Реакции замещения группы ОН и образование эфиров нехарактерны: эфиры получают с помощью фенолятов.
Фенол легко вступает в реакции электрофильного замещения в ароматическом кольце.
Качественные реакции:
1. Образование осадка 2,4,6 трибромфенола с бромной водой;
2. Появление фиолетовой окраски с хлоридом железа (FeCl₃)
РЕАКЦИИ С УЧАСТИЕМ ГИДРОКСИЛЬНОЙ ГРУППЫ (КИСЛОТНЫЕ СВОЙСТВА ФЕНОЛОВ)
1. Как и спирты, реагируют с активными металлами.
2. Реагируют с гидроксидами щелочных и щелочноземельных металлов (отличие от спиртов), образуя соли – феноляты.
Кислотные свойства очень слабые, кислота не окрашивает
индикаторы и вытесняется из солей даже угольной кислотой, т.е. феноляты легко гидролизируются.
Из фенолятов получают простые и сложные эфиры
1. Образование простых эфиров
2. Образование сложных эфиров
РЕАКЦИИ ФЕНОЛА ПО БЕНЗОЛЬНОМУ КОЛЬЦУ
1. Галогенирование.
Фенол легко при комнатной температуре взаимодействует с бромной водой (раствор желтый) с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол №1).
2. Нитрование.
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота).
3. Сульфирование фенолов
Образуются сульфофенолы
4. Поликонденсация
– образование полимера и низкомолекулярного побочного продукта (H₂O). С формальдегидом фенол образует фенолоформальдегидные смолы.
ОКИСЛЕНИЕ
Фенолы легко окисляются даже под действием кислорода воздуха.
Полное окисление (горение)
При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона образуется хинон:
Гидрирование (восстановление)— образуются циклические спирты
Качественная реакция на фенол №2: с хлоридом железа (III).
Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа.
14(Б) Тесты ЕГЭ ФИПИ 2015 Одноатомные спирты
14(Б) Тесты ЕГЭ ФИПИ 2015 Многоатомные спирты
14(Б) Тесты ЕГЭ ФИПИ 2015 Фенолы
Предельные одноатомные и многоатомные спирты
Спиртами (или алканолами) называются органические вещества, молекулы которых содержат одну или несколько гидроксильных групп (групп $—ОН$), соединенных с углеводородным радикалом.
По числу гидроксильных групп (атомности) спирты делятся на:
— одноатомные, например:
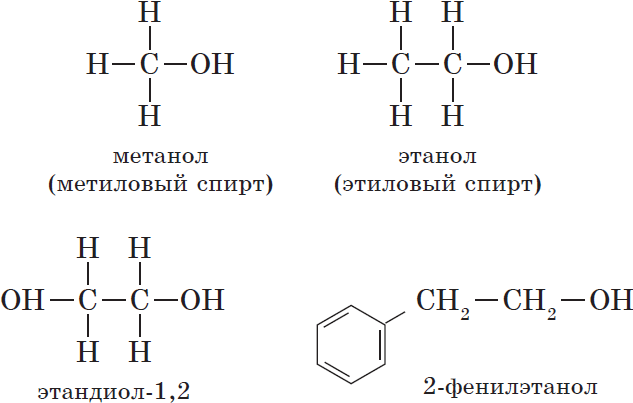
${CH_3-OH}↙{метанол(метиловый спирт)}$ ${CH_3-CH_2-OH}↙{этанол(этиловый спирт)}$
— двухатомные (гликоли), например:
${OH-CH_2-CH_2-OH}↙{этандиол-1,2(этиленгликоль)}$
${HO-CH_2-CH_2-CH_2-OH}↙{пропандиол-1,3}$
— трехатомные, например:
По характеру углеводородного радикала выделяют следующие спирты:
— предельные, содержащие в молекуле лишь предельные углеводородные радикалы, например:
— непредельные, содержащие в молекуле кратные (двойные и тройные) связи между атомами углерода, например:
${CH_2=CH-CH_2-OH}↙{пропен-2-ол-1 (аллиловый спирт)}$
— ароматические, т.е. спирты, содержащие в молекуле бензольное кольцо и гидроксильную группу, связанные друг с другом не непосредственно, а через атомы углерода, например:
Органические вещества, содержащие в молекуле гидроксильные группы, связанные непосредственно с атомом углерода бензольного кольца, существенно отличаются по химическим свойствам от спиртов и поэтому выделяются в самостоятельный класс органических соединений — фенолы. Например:
Существуют и полиатомные (многоатомные) спирты, содержащие более трех гидроксильных групп в молекуле. Например, простейший шестиатомный спирт гексаол (сорбит):
Номенклатура и изомерия
При образовании названий спиртов к названию углеводорода, соответствующего спирту, добавляют родовой суффикс -ол. Цифрами после суффикса указывают положение гидроксильной группы в главной цепи, а префиксами ди-, три-, тетра- и т. д. — их число:
В нумерации атомов углерода в главной цепи положение гидроксильной группы приоритетно перед положением кратных связей:
Начиная с третьего члена гомологического ряда, у спиртов появляется изомерия положения функциональной группы (пропанол-1 и пропанол-2), а с четвертого — изомерия углеродного скелета (бутанол-1, 2-метилпропанол-1). Для них характерна и межклассовая изомерия — спирты изомерны простым эфирам:
${CH_3-CH_2-OH}↙{этанол}$ ${CH_3-O-CH_3}↙{диметиловый эфир}$
Физические и химические свойства спиртов
Физические свойства.
Спирты могут образовывать водородные связи как между молекулами спирта, так и между молекулами спирта и воды.
Водородные связи возникают при взаимодействии частично положительно заряженного атома водорода одной молекулы спирта и частично отрицательно заряженного атома кислорода другой молекулы. Именно благодаря водородным связям между молекулами спирты имеют аномально высокие для своей молекулярной массы температуры кипения. Так, пропан с относительной молекулярной массой $44$ при обычных условиях является газом, а простейший из спиртов — метанол, имея относительную молекулярную массу $32$, в обычных условиях — жидкость.
Низшие и средние члены ряда предельных одноатомных спиртов, содержащие от $1$ до $11$ атомов углерода, — жидкости. Высшие спирты (начиная с $С_{12}Н_{25}ОН$) при комнатной температуре — твердые вещества. Низшие спирты имеют характерный алкогольный запах и жгучий вкус, они хорошо растворимы в воде. По мере увеличения углеводородного радикала растворимость спиртов в воде понижается, а октанол уже не смешивается с водой.
Химические свойства.
Свойства органических веществ определяются их составом и строением. Спирты подтверждают общее правило. Их молекулы включают в себя углеводородные и гидроксильные радикалы, поэтому химические свойства спиртов определяются взаимодействием и влиянием друг на друга этих групп. Характерные для данного класса соединений свойства обусловлены наличием гидроксильной группы.
1. Взаимодействие спиртов со щелочными и щелочноземельными металлами. Для выявления влияния углеводородного радикала на гидроксильную группу необходимо сравнить свойства вещества, содержащего гидроксильную группу и углеводородный радикал, с одной стороны, и вещества, содержащего гидроксильную группу и не содержащего углеводородный радикал, — с другой. Такими веществами могут быть, например, этанол (или другой спирт) и вода. Водород гидроксильной группы молекул спиртов и молекул воды способен восстанавливаться щелочными и щелочноземельными металлами (замещаться на них):
$2Na+2H_2O=2NaOH+H_2↑$,
$2Na+2C_2H_5OH=2C_2H_5ONa+H_2↑$,
$2Na+2ROH=2RONa+H_2↑$.
2. Взаимодействие спиртов с галогеноводородами. Замещение гидроксильной группы на галоген приводит к образованию галогеналканов. Например:
$C_2H_5OH+HBr⇄C_2H_5Br+H_2O$.
Данная реакция обратима.
3. Межмолекулярная дегидратация спиртов — отщепление молекулы воды от двух молекул спирта при нагревании в присутствии водоотнимающих средств:
В результате межмолекулярной дегидратации спиртов образуются простые эфиры. Так, при нагревании этилового спирта с серной кислотой до температуры от $100$ до $140°С$ образуется диэтиловый (серный) эфир:
4. Взаимодействие спиртов с органическими и неорганическими кислотами с образованием сложных эфиров (реакция этерификации):
Реакция этерификации катализируется сильными неорганическими кислотами.
Например, при взаимодействии этилового спирта и уксусной кислоты образуется уксусноэтиловый эфир — этилацетат:
5. Внутримолекулярная дегидратация спиртов происходит при нагревании спиртов в присутствии водоотнимающих средств до более высокой температуры, чем температура межмолекулярной дегидратации. В результате образуются алкены. Эта реакция обусловлена наличием атома водорода и гидроксильной группы при соседних атомах углерода. В качестве примера можно привести реакцию получения этена (этилена) при нагревании этанола выше $140°С$ в присутствии концентрированной серной кислоты:
6. Окисление спиртов обычно проводят сильными окислителями, например, дихроматом калия или перманганатом калия в кислой среде. При этом действие окислителя направляется на тот атом углерода, который уже связан с гидроксильной группой. В зависимости от природы спирта и условий проведения реакции могут образовываться различные продукты. Так, первичные спирты окисляются сначала в альдегиды, а затем в карбоновые кислоты:
При окислении вторичных спиртов образуются кетоны:
Третичные спирты достаточно устойчивы к окислению. Однако в жестких условиях (сильный окислитель, высокая температура) возможно окисление третичных спиртов, которое происходит с разрывом углерод-углеродных связей, ближайших к гидроксильной группе.
7. Дегидрирование спиртов. При пропускании паров спирта при $200–300°С$ над металлическим катализатором, например медью, серебром или платиной, первичные спирты превращаются в альдегиды, а вторичные — в кетоны:
Присутствием в молекуле спирта одновременно нескольких гидроксильных групп обусловлены специфические свойства многоатомных спиртов, которые способны образовывать растворимые в воде ярко-синие комплексные соединения при взаимодействии со свежеполученным осадком гидроксида меди (II). Для этиленгликоля можно записать:
Одноатомные спирты не способны вступать в эту реакцию. Поэтому она является качественной реакцией на многоатомные спирты.
СПИРТЫ- это соединения, содержащие помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Классификация спиртов.
1.По числу гидроксильных групп:
- одноатомные (одна группа -ОН).
Общая формула CnH2n+1–OH или CnH2n+2O.
- многоатомные (две и более групп -ОН).
Общая формула CnH2n+2Om.
Современное название многоатомных спиртов — полиолы (диолы, триолы и т.д).
Двухатомный спирт – этиленгликоль (этандиол) СH2–CH2
│ │
ОН ОН
Трехатомный спирт – глицерин (пропантриол-1,2,3) СH2–СН–CH2
│ │ │
ОН ОН ОН
2. В зависимости от того, с каким атомом углерода (первичным, вторичным или третичным) связана гидроксигруппа:
3. По строению радикалов, связанных с атомом кислорода:
- предельные, или алканолы (например, СH3CH2–OH)
- непредельные, или алкенолы (CH2=CH–CH2–OH)
- ароматические (C6H5CH2–OH).
- Фенолы (C6H5–OH).
СТРОЕНИЕ ГИДРОКСИЛЬНОЙ ГРУППЫ.
Связи О–Н и С–О – полярные ковалентные. Это следует из различий в электроотрицательности кислорода (ЭО = 3,5), водорода (ЭО = 2,1) и углерода (ЭО = 2,4).
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Разрыв таких связей происходит преимущественно по ионному механизму.
Атому кислорода в спиртах свойственна sp3-гибридизация. В образовании его связей с атомами C и H участвуют две sp3-гибридные орбитали, валентный угол C–О–H близок к тетраэдрическому.
В фенолах одна из электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца:
ВОДОРОДНЫЕ СВЯЗИ И ФИЗИЧЕСКИЕ СВОЙСТВА СПИРТОВ
Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей:
Ассоциация молекул ROH
Это объясняет, почему даже низшие спирты — жидкости с относительно высокой температурой кипения (t кип. метанола +64,5оС). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.
Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
Гидратация молекул ROH
Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена. C увеличением молярной массы растворимость спиртов в воде уменьшается.
Предельные одноатомные спирты
Общая формула – СnH2n+1OH или СnH2n+2O n>1
НОМЕНКЛАТУРА
В названии появляется суффикс: -«ОЛ» и номер атома углерода, к которому он присоединен. Нумерация ведется от ближайшего к ОН-группе конца цепи.
Приведенные выше соединения называют: метиловый спирт, этиловый спирт, н—пропило-вый спирт, изопропиловый спирт.
Метиловый спирт (метанол) CH3-OH
Этиловый спирт (этанол) CH3CH2-OH
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:
ИЗОМЕРИЯ СПИРТОВ.
Для спиртов характерна структурная изомерия:
*изомерия положения ОН-группы (начиная с С3);
*углеродного скелета (начиная с С4);
например, формуле C4H9OH соответствует 4 структурных изомера:
*межклассовая изомерия с простыми эфирами
(например, этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3).
Получение.
|
1. Щелочной гидролиз галогенпроизводных алканов. |
CH3–Br + NaOH(водн.) 🡪CH3–OH +NaBr |
|
2. Гидратация алкенов: присоединение воды к несимметричным алкенам идет по правилу Марковникова с образованием вторичных и третичных спиртов. |
CH2=CH2 + H2O –(H+)🡪CH3CH2OH CH3–CH=CH2 + H2O–(H+)🡪CH3CHCH3 ОН ОН / CH3–C=CH2 + H2O –(H+)->CH3 –C–СH3 ⎮ ⎮ СН3 СН3 |
|
3.Восстановление карбонильных соединений. |
При гидрировании альдегидов получаются первичные спирты: СН3-С=О + Н2 -(t,kat)🡪 CH3-CH2-OH ⎮ этанол Н При гидрировании кетонов образуются вторичные спирты: СН3-С=О + Н2 -(t,kat)🡪 CH3-CH-OH ⎮ ⎮ СН3 СН3 пропанол-2 |
|
4. Гидролиз сложных эфиров. |
CH3-C=O + H2O –(H2SO4,t)🡪 │ OC2H5 🡪 CH3-COOH + C2H5OH этанол |
|
5. Получение метанола из синтез-газа. |
1. Конверсия природного газа в синтез-газ: СН4 +Н2О = СО + 3Н2 2. Каталитический синтез метанола из монооксида углерода и водорода при температуре 300-400°С и давления 300—500 атм в присутствии катализатора — смеси оксидов цинка, хрома и др. Сырьем для синтеза метанола служит синтез-газ (CO + H2), обогащенный водородом: CO + 2 H2 ⇄ CH3OH Газ на выходе из реактора содержит 3-5% CH3OH, затем газ охлаждают и конденсируют полученный метанол, а оставшийся газ смешивают с исходным газом и направляют снова в реактор. |
|
6. Получение этанола спиртовым брожением. |
Спиртовое брожение глюкозы. С6Н12О6 –(фермент)-> 2С2Н5ОН + 2СО2 |
ХИМИЧЕСКИЕ СВОЙСТВА.
В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
- С–ОН с замещением или отщеплением ОН-группы
- О–Н с замещением водорода.
|
1.Одноатомные спирты реагируют с активными металлами (Na, K, Mg), образуя соли — алкоголяты (алкоксиды): |
Реакционная способность одноатомных спиртов в реакциях по связи О–Н: CH3OH > первичные > вторичные > третичные. 2R–OH + 2Na 🡪 2 R-ONa + H2 этилат калия (алкоголят) Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла: C2H5OК + H2O 🡪C2H5OH + КOH Со щелочами одноатомные спирты НЕ реагируют. |
|
2.Окисление одноатомных спиртов. |
1) Горение: 2CH3OH + 3O2 🡪2CO2 + 4H2O 2) Окисление первичных спиртов до альдегидов: Реагенты – CuO (to), O2 (Cu, to), а также дегидрирование при нагревании над медной сеткой. СН3-СН2-ОН +СuO –(to)🡪 CH3-C=O + Cu + H2O этанол ⎮ этаналь H 2) Дегидрирование: СН3-СН2-СН2-ОН –(Сu, to)🡪 CH3-CH2-C=O + H2 пропанол ⎮ пропаналь H 3) Окисление подкисленным раствором перманганата калия приводит к образованию карбоновых кислот: СН3-СН2-ОН + KMnO4 + H2SO4 -> CH3-COOH + MnSO4 + K2SO4 +H2O уксусная кислота При окислении метанола образуется углекислый газ!!! 5СН3ОН +6KMnO4 + 9H2SO4 -> 5CО2 + 6MnSO4 + 3K2SO4 +19H2O 4) При окислении вторичных спиртов любым окислителем образуются кетоны. |
|
3. Реакции замещения ОН на галоген: происходит в реакции с галогеноводородами в присутствии сильной кислоты (конц. H2SO4). |
Реакционная способность одноатомных спиртов в реакциях по связи С–О: третичные > вторичные > первичные > CH3OH |
|
4. Образование сложных эфиров. |
Спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры. |
|
5. Реакции дегидратации спиртов. |
|
|
Внутримолекулярная дегидратация: образуются алкены. |
Внутримолекулярная дегидратация спиртов с образованием алкенов идет в присутствии концентрированной серной кислоты при повышенной температуре: Основной продукт – бутен-2. Правило Зайцева – водород отщепляется от менее гидрогенизированного атома углерода. |
|
Межмолекулярная дегидратация: образуются простые эфиры. |
При межмолекулярной дегидратации спиртов также происходит нуклеофильное замещение: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. |
МНОГОАТОМНЫЕ СПИРТЫ.
ПОЛУЧЕНИЕ.
|
1.Окисление алкенов холодным водным раствором KMnO4: |
R-CH=CH2 + KMnO4 + H2O🡪 R- CH-CH2 +MnO2 + KOH алкен │ │ диол OH OH |
|
2. Замещение галогенов на гидроксогруппу: |
СН2— СН — СН2 + 3KOH 🡪 СН2— СН — СН2 + 3KCl │ │ │ (вод.р-р) │ │ │ Cl Сl Cl OH OH OH |
|
3.Восстановление поликарбонильных соединений: |
O=CH – CH =O + H2 –(t,kat)🡪 CH2-CH2 диальдегид │ │ OH OH |
ХИМИЧЕСКИЕ СВОЙСТВА.
|
1.Кислотные свойства. Этиленгликоль, глицерин вследствие взаимного влияния атомов (-I-эффект ОН-групп) являются более сильными кислотами, чем одноатомные спирты. |
Образуют соли не только в реакциях с активными металлами, но и под действием щелочей (частично и обратимо): HO–CH2-CH2–OH + 2Na 🡪 CH2-CH2 +H2 │ │ ONa ONa HO–CH2-CH2–OH +2NaOH ⇄ CH2-CH2 +2H2O │ │ ONa ONa |
|
2.Взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соединения (качественная реакция на многоатомные спирты ): |
— ярко-синий раствор гликолята меди. |
|
3.Образование сложных эфиров азотной кислоты: реакция с азотной кислотой. |
|
|
4. Замещение ОН на галоген: также, как и одноатомные спирты, реагируют с галогеноводородами. |
HO–CH2-CH2–OH + 2HBr 🡪 CH2-CH2 + 2H2O │ │ Br Br Можно заместить 1 или 2 группы ОН. |
|
5. Окисление. Так же, как и одноатомные спирты – оксидом меди или над медной сеткой многоатомные спирты окисляются в карбонильные соединения. |
CH2-CH2 –(t,Сu)🡪 O=CH–CH=O + H2 │ │ диальдегид — глиоксаль OH OH |
ФЕНОЛЫ
Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром.
Общая формула – СnH2n-7OH n>6 (для фенолов с одной ОН-группой)
В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:
Изомерия
1. Фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
2. Фенолы изомерны ароматическим спиртам
C6H4(СН3)OН – крезол и C6H5-СН2-OН бензиловый спирт
ПОЛУЧЕНИЕ.
|
1. Из хлорбензола. |
+ Cl2 –(AlCl3)🡪 C6H5Cl + HCl Хлорбензол обрабатывают избытком щелочи, получая водный раствор фенолята натрия: C6H5Cl + 2NaOH –(t,p)🡪C6H5ONa + NaCl хлорбензол фенолят натрия Затем фенол выделяют, пропуская углекислый газ. С6H5ONa + CO2 +H2O 🡪 C6H5OH + Na2CO3 |
|
2. Из кумола. |
1) Алкилирование бензола пропеном: + CH3-CH=CH2 –(H3PO4)🡪 2) Окисление кумола кислородом на катализаторе: |
СВОЙСТВА ФЕНОЛОВ.
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
Сходство и отличие фенола и спиртов.
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличие:
-фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
-фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
-фенол не вступает в реакции дегидратации.
|
Кислотные свойства фенолов. |
|
|
1. Как и спирты, реагируют с активными металлами. |
2C6H5OH + 2Na ->2C6H5ONa + H2 Феноляты легко гидролизуются: C6H5ONa + HСl 🡪 C6H5OH + NaCl C6H5ONa +H2О +СО2 🡪 C6H5OH + NaНСО3 |
|
2. Реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты. |
C6H5OH + NaOH 🡪C6H5ONa + H2O |
|
Реакции фенола по бензольному кольцу. |
|
|
3. Галогенирование. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол №1). |
|
|
4. Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов. При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота). |
|
|
5. Конденсация с альдегидами. С формальдегидом фенол образует фенолоформальдегидные смолы. |
|
|
5. Окисление. Фенолы легко окисляются даже под действием кислорода воздуха. |
При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона образуется хинон: |
|
6. Гидрирование (восстановление) |
C6H5OН +3Н2 –(Ni)🡪 C6H11OH циклогексанол |
|
7. Качественная реакция на фенол №2: с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа. |
3.5. Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола.
В зависимости от типа углеводородного радикала, а также в некоторых случаях особенностей прикрепления группы -ОН к этому углеводородному радикалу соединения с гидроксильной функциональной группой разделяют на спирты и фенолы.
Спиртами называют соединения, в которых гидроксильная группа соединена с углеводородным радикалом, но не присоединена непосредственно к ароматическому ядру, если таковой имеется в структуре радикала.
Примеры спиртов:
Если в структуре углеводородного радикала содержится ароматическое ядро и гидроксильная группа, при том соединена непосредственно с ароматическим ядром, такие соединения называют фенолами.
Примеры фенолов:
Почему же фенолы выделяют в отдельный от спиртов класс? Ведь, например, формулы
очень похожи и создают впечатление веществ одного класса органических соединений.
Однако непосредственное соединение гидроксильной группы с ароматическим ядром существенно влияет на свойства соединения, поскольку сопряженная система π-связей ароматического ядра сопряжена также и с одной из неподеленных электронных пар атома кислорода. Из-за этого в фенолах связь О-Н более полярна по сравнению со спиртами, что существенно повышает подвижность атома водорода в гидроксильной группе. Другими словами, у фенолов значительно ярче, чем у спиртов выражены кислотные свойства.
Химические свойства спиртов
Одноатомные спирты
Реакции замещения
Замещение атома водорода в гидроксильной группе
1) Спирты реагируют со щелочными, щелочноземельными металлами и алюминием (очищенным от защитной пленки Al2O3), при этом образуются алкоголяты металлов и выделяется водород:
Образование алкоголятов возможно только при использовании спиртов, не содержащих растворенной в них воды, так как в присутствии воды алкоголяты легко гидролизуются:
CH3OK + Н2О = СН3ОН + KOH
2) Реакция этерификации
Реакцией этерификации называют взаимодействие спиртов с органическими и кислородсодержащими неорганическими кислотами, приводящее к образованию сложных эфиров.
Такого типа реакции являются обратимыми, поэтому для смещения равновесия в сторону образования сложного эфира, реакцию желательно проводить при нагревании, а также в присутствии концентрированной серной кислоты как водоотнимающего агента:
Замещение гидроксильной группы
1) При действии на спирты галогеноводородных кислот происходит замещение гидроксильной группы на атом галогена. В результате такой реакции образуются галогеналканы и вода:
2) При пропускании смеси паров спирта с аммиаком через нагретые оксиды некоторых металлов (чаще всего Al2O3) могут быть получены первичные, вторичные или третичные амины:
Тип амина (первичный, вторичный, третичный) будет в некоторой степени зависеть от соотношения исходного спирта и аммиака.
Реакции элиминирования (отщепления)
Дегидратация
Дегидратация, фактически подразумевающая отщепление молекул воды, в случае спиртов различается на межмолекулярную дегидратацию и внутримолекулярную дегидратацию.
При межмолекулярной дегидратации спиртов одна молекула воды образуется в результате отщепления атома водорода от одной молекулы спирта и гидроксильной группы — от другой молекулы.
В результате этой реакции образуются соединения, относящиеся к классу простых эфиров (R-O-R):
Внутримолекулярная дегидратация спиртов протекает таким образом, что одна молекула воды отщепляется от одной молекулы спирта. Данный тип дегидратации требует несколько более жестких условий проведения, заключающихся в необходимости использования заметно более сильного нагревания по сравнению с межмолекулярной дегидратацией. При этом из одной молекулы спирта образуется одна молекула алкена и одна молекула воды:
Поскольку молекула метанола содержит только один атом углерода, для него невозможна внутримолекулярная дегидратация. При дегидратации метанола возможно образование только простого эфира (CH3-O-CH3).
Нужно четко усвоить тот факт, что в случае дегидратации несимметричных спиртов внутримолекулярное отщепление воды будет протекать в соответствии с правилом Зайцева, т.е. водород будет отщепляться от наименее гидрированного атома углерода:
Дегидрирование спиртов
а) Дегидрирование первичных спиртов при нагревании в присутствии металлической меди приводит к образованию альдегидов:
б) В случае вторичных спиртов аналогичные условия приведут у образованию кетонов:
в) Третичные спирты в аналогичную реакцию не вступают, т.е. дегидрированию не подвергаются.
Реакции окисления
Горение
Спирты легко вступают в реакцию горения. При этом образуется большое количество тепла:
2СН3-ОН + 3O2 = 2CO2 + 4H2O + Q
Неполное окисление
Неполное окисление первичных спиртов может приводить к образованию альдегидов и карбоновых кислот.
В случае неполного окисления вторичных спиртов возможно образование только кетонов.
Неполное окисление спиртов возможно при действии на них различных окислителей, например, таких, как кислород воздуха в присутствии катализаторов (металлическая медь), перманганат калия, дихромат калия и т.д.
При этом из первичных спиртов могут быть получены альдегиды. Как можно заметить, окисление спиртов до альдегидов, по сути, приводит к тем же органическим продуктам, что и дегидрирование:
Следует отметить, что при использовании таких окислителей, как перманганат калия и дихромат калия в кислой среде возможно более глубокое окисление спиртов, а именно до карбоновых кислот. В частности, это проявляется при использовании избытка окислителя при нагревании. Вторичные спирты могут в этих условиях окислиться только до кетонов.
ПРЕДЕЛЬНЫЕ МНОГОАТОМНЫЕ СПИРТЫ
Замещение атомов водорода гидроксильных групп
Многоатомные спирты так же, как и одноатомные реагируют со щелочными, щелочноземельными металлами и алюминием (очищенным от пленки Al2O3); при этом может заместиться разное число атомов водорода гидроксильных групп в молекуле спирта:
2. Поскольку в молекулах многоатомных спиртов содержится несколько гидроксильных групп, они оказывают влияние друг на друга за счет отрицательного индуктивного эффекта. В частности, это приводит к ослаблению связи О-Н и повышению кислотных свойств гидроксильных групп.
Большая кислотность многоатомных спиртов проявляется в том, что многоатомные спирты, в отличие от одноатомных, реагируют с некоторым гидроксидами тяжелых металлов. Например, нужно запомнить тот факт, что свежеосажденный гидроксид меди реагирует с многоатомными спиртами с образованием ярко-синего раствора комплексного соединения.
Так, взаимодействие глицерина со свежеосажденными гидроксидом меди приводит к образованию ярко-синего раствора глицерата меди:
Данная реакция является качественной на многоатомные спирты. Для сдачи ЕГЭ достаточно знать признаки этой реакции, а само уравнение взаимодействия уметь записывать необязательно.
3. Так же, как и одноатомные спирты, многоатомные могут вступать в реакцию этерификации, т.е. реагируют с органическими и кислородсодержащими неорганическими кислотами с образованием сложных эфиров. Данная реакция катализируется сильными неорганическими кислотами и является обратимой. В связи с этим при осуществлении реакции этерификации образующийся сложный эфир отгоняют из реакционной смеси, чтобы сместить равновесие вправо по принципу Ле Шателье:
Если в реакцию с глицерином вступают карбоновые кислоты с большим числом атомов углерода в углеводородном радикале, получающиеся в результате такой реакции, сложные эфиры называют жирами.
В случае этерификации спиртов азотной кислотой используют так называемую нитрующую смесь, представляющую собой смесь концентрированных азотной и серной кислот. Реакцию проводят при постоянном охлаждении:
Сложный эфир глицерина и азотной кислоты, называемый тринитроглицерином, является взрывчатым веществом. Кроме того, 1%-ный раствор данного вещества в спирте обладает мощным сосудорасширяющим действием, что используется при медицинских показаниях для предотвращения приступа инсульта или инфаркта.
Замещение гидроксильных групп
Реакции данного типа протекают по механизму нуклеофильного замещения. К взаимодействиям такого рода относится реакция гликолей с галогеноводородами.
Так, например, реакция этиленгликоля с бромоводородом протекает с последовательным замещением гидроксильных групп на атомы галогена:
Химические свойства фенолов
Как уже было сказано в самом начале данной главы, химические свойства фенолов заметно отличаются от химических свойств спиртов. Связано это с тем, что одна из неподеленных электронных пар атома кислорода в гидроксильной группе сопряжена с π-системой сопряженных связей ароматического кольца.
Реакции с участием гидроксильной группы
Кислотные свойства
Фенолы являются более сильными кислотами, чем спирты, и в водном растворе в очень небольшой степени диссоциированы:
Большая кислотность фенолов по сравнению со спиртами в плане химических свойств выражается в том, что фенолы, в отличие от спиртов, способны реагировать со щелочами:
Однако, кислотные свойства фенола выражены слабее, чем даже у одной из самых слабых неорганических кислот – угольной. Так, в частности, углекислый газ, при пропускании его через водный раствор фенолятов щелочных металлов, вытесняет из последних свободный фенол как еще более слабую, чем угольная, кислоту:
Очевидно, что любой другой более сильной кислотой фенол также будет вытесняться из фенолятов:
3) Фенолы являются более сильными кислотами, чем спирты, а спирты при этом реагируют с щелочными и щелочноземельными металлами. В связи с этим очевидно, что и фенолы будут реагировать с указанными металлами. Единственное, что в отличие от спиртов, реакция фенолов с активными металлами требует нагревания, так как и фенолы, и металлы являются твердыми веществами:
Реакции замещения в ароматическом ядре
Гидроксильная группа является заместителем первого рода, и это значит, что она облегчает протекание реакций замещения в орто- и пара-положениях по отношению к себе. Реакции с фенолом протекают в намного более мягких условиях по сравнению с бензолом.
Галогенирование
Реакция с бромом не требует каких-либо особых условий. При смешении бромной воды с раствором фенола мгновенно образуется белый осадок 2,4,6-трибромфенола:
Нитрование
При действии на фенол смеси концентрированных азотной и серной кислот (нитрующей смеси) образуется 2,4,6-тринитрофенол – кристаллическое взрывчатое вещество желтого цвета:
Реакции присоединения
Поскольку фенолы являются ненасыщенными соединениями, возможно их гидрирование в присутствии катализаторов до соответствующих спиртов:


















![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)