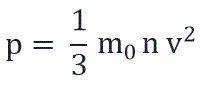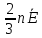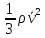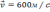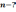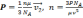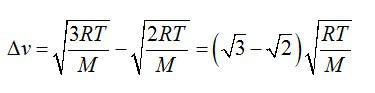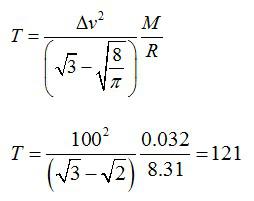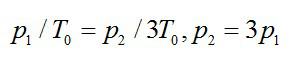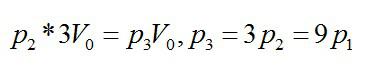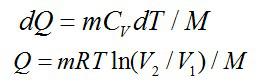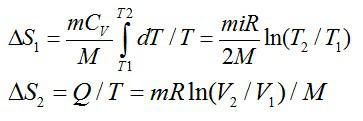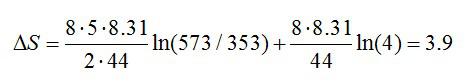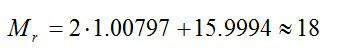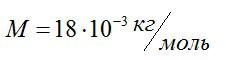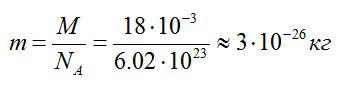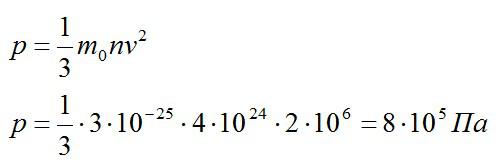Пройти тестирование по 10 заданиям
Пройти тестирование по всем заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Среднюю кинетическую энергию теплового движения молекул разреженного газа уменьшили в 2 раза и концентрацию молекул газа уменьшили в 2 раза. Чему равно отношение конечного давления к начальному?
2
Концентрацию молекул одноатомного идеального газа уменьшили в 5 раз. Одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. Чему равно отношение конечного давления к начальному?
3
Во сколько раз изменится давление идеального газа, если среднюю кинетическую энергию теплового движения молекул газа увеличить в 2 раза и концентрацию молекул газа увеличить в 2 раза?
4
При неизменной концентрации молекул идеального газа средняя квадратичная скорость теплового движения его молекул увеличилась в 4 раза. Во сколько раз изменилось давление газа?
5
При неизменной концентрации молекул идеального газа средняя квадратичная скорость теплового движения его молекул уменьшилась в 2 раза. Чему равно отношение конечного давления к начальному?
Пройти тестирование по этим заданиям
Основное уравнение МКТ. Задачи
1. При неизменной концентрации молекул гелия средняя кинетическая энергия теплового движения его молекул уменьшилась в 4 раза. При этом давление газа:
1) уменьшилось в 16 раз
2) уменьшилось в 2 раза
3) уменьшилось в 4 раза
4) не изменилось
Согласно основному уравнению МКТ, давление p прямо пропорционально средней кинетической энергии поступательного движения молекул: 
2. Давление газа зависит от:
А) концентрации молекул
Б) средней кинетической энергии молекул
Выберите верный вариант:
1) только от А 2) только от Б 3) и от А, и от Б 4)ни от А, ни от Б
Правильный ответ — 3, согласно основному уравнению МКТ, см. предыдущую задачу.
3. В результате остывания газа средняя кинетическая энергия теплового движения его молекул уменьшилась в три раза. При этом абсолютная температура газа:
1) уменьшилась в 3 раза
2) уменьшилась в 9 раз
3) уменьшилось в 
4) не изменилась
Из основного уравнения МКТ: 


Ответ: 1.
4. В результате нагревания идеального газа его давление при постоянной концентрации молекул увеличилось в два раза. При этом абсолютная температура газа:
1) увеличилась в 4 раза
2) увеличилась в 2 раза
3) уменьшилось в 2 раза
4) не изменилась
Согласно зависимости давления газа от абсолютной температуры Т и концентрации его молекул: 
Ответ: 2.
5. При понижении температуры газа в запаянном сосуде давление газа уменьшается. Это уменьшение давления объясняется тем, что
1) уменьшается объём сосуда за счет остывания его стенок
2) уменьшается энергия теплового движения молекул газа
3) уменьшаются размеры молекул газа при его охлаждении
4) уменьшается энергия взаимодействия молекул газа друг с другом
Объем сосуда может измениться вследствие уменьшения давления газа при понижении температуры — так стенки канистры, если в ней был бензин и остались его пары, втягиваются внутрь при похолодании. Но за счет остывания стенок мы это вряд ли заметим невооруженным глазом.
Размеры молекул — величина постоянная и не меняется ни с температурой, ни по другим причинам.
Энергия взаимодействия молекул газа друг с другом определяется их средней кинетической энергией, которая-то и зависит от температуры: 

Ответ: 2.
6. На графике показана зависимость давления от концентрации для двух идеальных газов при фиксированных температурах. Отношение температур 
1) 1
2) 2
3) 0,5
4)
Согласно уравнению идеального газа 
Для первого газа:
Для второго газа:
Отношение температур тогда: 


Ответ: 2.
7. На графиках представлены зависимости концентрации n и температуры T идеального газа от времени. Из этих зависимостей следует, что давление газа с течением времени

2) уменьшалось
3) не изменялось
4) сначала увеличивалось, а потом не изменялось
Согласно уравнению идеального газа 
Ответ: 1.
8. В результате охлаждения одноатомного идеального газа его давление уменьшилось в 4 раза, а концентрация молекул газа не изменилась. При этом средняя кинетическая энергия теплового движения молекул газа
1) уменьшилась в 16 раз
2) уменьшилась в 2 раза
3) уменьшилась в 4 раза
4) не изменилась
Давление газа зависит от средней кинетической энергии теплового движения молекул так: 
2 комментария
оля
✉️
04.06.2017 10:34:12
здравствуйте. у меня вопрос. почему в 7 задании в ответе написано, что Т и n увеличиваются? ветви параболы повёрнуты в разные стороны, значит T уменьшается
Анна Валерьевна
✨
05.06.2017 10:18:09
Это не параболы. Время растет, следовательно, двигаемся по графику слева направо, при этом график лезет все выше и выше: температура растет.
Основное уравнение мкт задачи егэ
Среднюю кинетическую энергию теплового движения молекул разреженного газа уменьшили в 2 раза и концентрацию молекул газа уменьшили в 2 раза. Чему равно отношение конечного давления к начальному?
Давление разреженного газа пропорционально произведению концентрации молекул газа и средней кинетической энергии теплового движения, например, для одноатомного газа:
При одновременном уменьшении средней кинетической энергии теплового движения в два раза и концентрации молекул в два раза давление разреженного газа уменьшится в 4 раза.
Концентрацию молекул одноатомного идеального газа уменьшили в 5 раз. Одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. Чему равно отношение конечного давления к начальному?
Давление одноатомного идеального газа пропорционально произведению концентрации молекул газа и средней энергии хаотического движения:
При увеличении средней энергии теплового движения в два раза и уменьшении концентрации молекул в пять раз конечное давление одноатомного идеального газа составит от начального.
Практическая работа по теме: Решение задач на применение основного уравнения МКТ
Цель: Научиться применять основное уравнение МКТ при решении задач.
Просмотр содержимого документа
«Практическая работа по теме: Решение задач на применение основного уравнения МКТ»
Практическая работа № 5
Решение задач на применение основного уравнения МКТ
Цель: Научиться применять основное уравнение МКТ при решении задач.
Физический смысл основного уравнения МКТ заключается в том, что давление идеального газа — это совокупность всех ударов молекул о стенки сосуда. Это уравнение можно выразить через концентрацию частиц, их среднюю скорость и массу одной частицы:
P =
P =
p – давление молекул газа на границы емкости,
m0 – масса одной молекулы,
n — концентрация молекул, число частиц N в единице объема V;
v 2 — средне квадратичная скорость молекул.
Как известно из законов динамики, кинетическая энергия любого тела или частицы. Заменив произведение массы каждой из частичек и квадрата их скорости в записанном нами уравнении, мы можем представить его в виде:
Также кинетическая энергия газовых молекул выражается формулой, что нередко используется в задачах. Здесь k – это постоянная Больцмана, устанавливающая связь между температурой и энергией. k=1,38•10 -23 Дж/К.
Основное уравнение МКТ лежит в основе термодинамики.
Средняя квадратичная скорость молекул азота 600 м/с. Если его давление 0,28 МПа, то концентрация молекул равна….
P = 0,28 МПа = 28*10 4 Па
Основное уравнение молекулярно-кинетической теории:
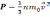
Зная число Авогадро, массу одной молекулы m0 выразим как:
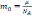
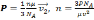
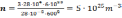
Ответ: 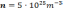
Задания для аудиторной работы
1.Найти температуру газа при давлении 100 кПа и концентрации молекул
2. Каково давление газа, если в каждом см³ его содержится 10 6 молекул, а температура 87°С?
3. В сосуде находится газ. Какое давление он производит на стенки сосуда, если масса газа 5 г, его объем 1 л, средняя квадратичная скорость молекул 500 м/с?
4. Определите давление водорода, если средняя квадратичная скорость его молекул 800 м/с, а его плотность 2.4 кг/м³.
5. Какова скорость теплового движения молекул, если при давлении 250 кПа газ массой 8 кг занимает объем 15 м³.
6. Определить число молекул водорода в 1 м³, если давление равно 200 мм РТ. Столба, а средняя квадратичная скорость его молекул равна 24000 м/с.
7. Определите среднюю квадратичную скорость молекул газа, плотность которого при давлении р = 50 кПа составляет ρ = 4.1·10‾² кг/м³.
8. Чему равны средняя квадратичная скорость и средняя энергия поступательного движения молекул азота, если 2.5 кг его, занимая объем 3.2 м³, производит давление 2.5·10 5 Па?
1. Определите температуру газа, если средняя кинетическая энергия поступательного движения его молекул равна 1.6·10‾ 19 Дж.
2. Сколько молекул газа находится в сосуде вместимостью 480 см³ при температуре 20°С и давлении 2.5·10 4 Па?
3. Определите давление азота в ампуле, если в 1м³ находится 3.5·10 14 молекул, средняя скорость теплового движения которых равна 490 м/с.
4. Определите концентрацию молекул водорода при давлении 100 кПа, если среднее значение скорости теплового движения молекул равно 450 м/с.
5. Средняя энергия молекулы идеального газа равна 6.4·10‾²¹ Дж. Давление газа 4 мПа. Найти число молекул газа в единице объема.
6. Чему равны средняя квадратичная скорость и средняя энергия поступательного движения молекул азота, если 2.5 кг его, занимая объем 3.2 м³, производит давление 2.5·10 5 Па?
7. Определить среднюю кинетическую энергию Ек поступательного движения молекул газа, находящегося под давлением 0.2 Па. Концентрация молекул газа равна 10 14 см‾³.
8. Определите среднюю квадратичную скорость молекул газа, плотность которого при давлении р = 50 кПа составляет ρ = 4.1·10‾² кг/м³.
Основное уравнение мкт задачи егэ
Основное уравнение МКТ .
(p) — Давление газа
(m_0) — масса молекулы газа
(n) -концентрация молекул газа
(bar ) — усредненный квадрат скорости молекул
Это уравнение связывает макроскопический параметр давление с микроскопическими параметрами: массой молекулы и среднеквадратичной скоростью молекул
макроскопические параметры это то что мы можем увидеть глазами или измерить прибором
Мы живем в макромире
Молекулы мы не можем пощупать, увидеть или измерить их скороть, они находятся в микромире
Попробуем преобразовать наше уравнение, используя формулу кинетической энергии:
(p=dfrac<1> <3>m_0 n bar=dfrac<1> <3>n m_0 bar=dfrac<1> <3>n cdot 2bar< E_к>= dfrac<2> <3>n bar < E_к>)
это тоже основное уравнение МКТ
Другие формулы этой темы:
(k) — постоянная Больцмана
Эта формула связывает среднюю кинетическую энергию молекулы с температурой в градусах Кельвина
Задача 1.(Основное уравнение МКТ) .формула (p= dfrac<2> <3>n bar < E_к>)
Найти давление газа в баллоне, если концентрация молекул газа (n=10^ <26>м^ <-1>), а средняя кинетическая энергия молекул газа (bar< E_к>=3 cdot 10^ <-21>Дж )
Показать ответ Показать решение Видеорешение
Ответ: ( p= 200000Па )
Запишем основное уравнение МКТ в преобразованном виде:
(p= dfrac<2> <3>cdot 10^ <26>м^ <-1>3 cdot 10^ <-21>Дж=2 cdot 10^ <5>Па=200000Па)
источники:
http://multiurok.ru/files/praktichieskaia-rabota-po-tiemie-rieshieniie-zad-1.html
http://kornev-school.ru/f10_basic_equation_of_molecular_kinetic_theory.html
Любишь теорию – люби и задачи решать. Во всяком случае, лучше полюбить, ведь заниматься этим все равно придется. Сегодня занимаемся решением задач по молекулярно-кинетической теории и радуемся.
Присоединяйтесь к нам в телеграм и будьте в курсе самых актуальных студенческих новостей.
А прежде чем приступать к решению задач, вспомните памятку по решению задач по физике и держите наготове основные формулы.
Задачи по молекулярно-кинетической теории
Задача №1. Средняя квадратичная скорость молекул и температура
Условие
При какой температуре средняя квадратичная скорость молекул кислорода больше их наиболее вероятной скорости на 100 м/с.
Решение
Находим разницу скоростей, используя формулы для средней квадратичной и наиболее вероятной скорости молекул:
Отсюда выражаем температуру:
Ответ: 121 К.
Задача №2. Изопроцессы
Условие
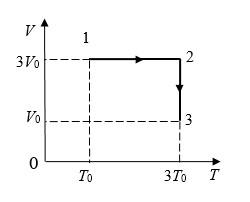
На диаграмме V – T изображены процессы перехода идеального газа постоянного количества из состояния 1 в состояние 3. Каким соотношением связаны конечное давление Р3 и начальное давление Р1?
Решение
При изохорном процессе:
Далее при изотермическом:
Ответ: Р3=9Р1
Задача №3. Приращение энтропии
Условие
Найти приращение энтропии при переходе массы m=8 г углекислого газа от объема V1=10 л при температуре t1=80° С к объему V2=40 л при температуре t2=300° С.
Решение
Рассмотрим процесс перехода между состояниями вначале по
изохоре, а затем по изотерме:
Соответствующие изменения при каждом процессе:
В сумме получаем общее изменение энтропии:
Ответ: 3,9 Дж/К.
Задача №4. Молярная масса
Условие
Каковы масса и молярная масса одной молекулы воды.
Решение
Молекула воды состоит из двух атомов водорода и одного атома кислорода. Их относительные атомные массы берем в таблице Менделеева, а затем вычисляем относительную молярную массу молекулы:
Молярная масса воды:
Чтобы найти массу одной молекулы, разделим массу моля воды на количество молекул, содержащихся в нем (число Авогадро):
Ответ: 3*10^-26 кг.
Задача №5. Основное уравнение молекулярно-кинетической теории
Условие
Каково давление газа на стенки сосуда, если известны средний квадрат скорости его молекул (2*10^6 м2/с2), концентрация молекул (4*10^24 1/м^3) и масса одной молекулы (3*10^-25 кг).
Решение
Используем основное уравнение МКТ:
Ответ: 800 кПа.
Вопросы по молекулярно кинетической теории
Вопрос 1. Что такое основное уравнение МКТ?
Ответ. Основное уравнение МКТ – это уравнение, которое связывает макроскопические параметры системы (давление, объем, температура) с микроскопическими (масса молекул, скорость движения молекул)
Вопрос 2. Сформулируйте основные положения МКТ.
Ответ. Основные положения молекулярно-кинетической теории:
- Все вещества могут быть в жидком, твердом и газообразном состоянии. Вещество состоит из частиц (молекулы, атомы, ионы). Элементарные молекулы могут иметь сложное строение, то есть иметь в своем составе несколько атомов. Молекулы и атомы – электрически нейтральные частицы, которые в определенных условиях приобретают дополнительный электрический заряд и переходят в положительные или отрицательные ионы.
- Частицы вещества постоянно находятся в хаотическом движении.
- Силы, с которыми частицы взаимодействуют между собой, имеют электрическую природу. Гравитационным взаимодействием между частицами можно пренебречь.
Вопрос 3. Что такое 1 моль вещества?
Ответ. Это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0,012 кг углерода.
Вопрос 4. Каково экспериментальные подтверждение хаотического движения молекул?
Ответ. Броуновское движение – наиболее очевидное подтверждение второго положения МКТ.
Броуновское движение – это тепловое хаотическое движение микроскопических частиц, взвешенных в жидкости или газе.
Было открыто ботаником Робертом Броуном в 1827 году на примере пыльцы, но первые сведения об описании подобных явлений относятся к Древнему Риму.
Вопрос 5. Что происходит с кинетической энергией теплового движения молекул при спаде температуры.
Ответ. С ростом температуры кинетическая энергия теплового движения увеличивается, а при спаде температуры – наоборот, уменьшается.
В 19 веке существовала гипотеза тепловой смерти Вселенной, согласно которой в определенный момент, при достижении абсолютного нуля температуры, все процессы остановятся, и Вселенная придет в состояние термодинамического равновесия. В настоящее время эта теория опровергнута.
Нужна помощь в решении задач и других заданий по учебе? Профессиональный студенческий сервис и его лучшие специалисты всегда к вашим услугам и справятся с любой темой.
Задачи по молекулярной физике с решениями
Элементы молекулярной физики. Основное уравнение молекулярно-кинетической теории (МКТ)
4.1.1 В баллоне находится 20 моль газа. Сколько молекул газа находится
4.1.2 Определить массу молекулы кислорода
4.1.3 Сколько молекул содержится в 5 кг кислорода?
4.1.4 При температуре 320 К средняя квадратичная скорость молекулы кислорода 500 м/с
4.1.5 Определить давление водорода, если средняя квадратичная скорость его молекул
4.1.6 Какова средняя кинетическая энергия поступательного движения молекул газа
4.1.7 Определить давление, при котором 1 м3 газа, имеющий температуру 60 C, содержит
4.1.8 Сколько молекул содержится в 1 л воды?
4.1.9 Какое значение температуры по шкале Кельвина соответствует температуре 100 C?
4.1.10 Какой объем при нормальных условиях занимают 5 г углекислого газа?
4.1.11 Чему равна температура газа, если при концентрации 2,65×10^25 м^(-3) он создает
4.1.12 Определить число молекул, содержащихся в 1 г воды
4.1.13 Определить количество вещества, содержащегося в медной отливке массой 96 кг
4.1.14 В комнате размером 4x5x2,7 м^3 испарился кристаллик йода массой 20 мг. Сколько
4.1.15 В лабораторных условиях создан высокий вакуум, то есть очень малое давление
4.1.16 Определить молярную массу газа, если его плотность при нормальных условиях
4.1.17 Найти число молекул в 2 кг углекислого газа
4.1.18 Во сколько раз масса молекулы углекислого газа CO2 больше массы молекулы аммиака NH3
4.1.19 За 20 суток из стакана полностью испарилась 0,2 кг воды. Сколько в среднем молекул
4.1.20 Считая, что диаметр молекул водорода составляет около 0,23 нм, подсчитать, какой длины
4.1.21 В сосуде находится газ под давлением 150 кПа при температуре 23 C. Найти
4.1.22 Определить среднюю квадратичную скорость молекул водорода
4.1.23 Под каким давлением находится кислород в баллоне, если при температуре 27 C
4.1.24 При какой температуре средняя квадратичная скорость молекул кислорода
4.1.25 Какова плотность сжатого воздуха при 0 C в камере шины автомобиля “Волга”? Давление
4.1.26 Определить среднюю квадратичную скорость молекул азота при температуре
4.1.27 Определить плотность воздуха при нормальных условиях. Молярную массу принять
4.1.28 Каково давление азота, если его плотность равна 1,35 кг/м^3, а средняя квадратичная
4.1.29 Сколько молекул кислорода находится в сосуде объемом 1 л, если температура
4.1.30 Определить плотность воздуха при 27 C и давлении 0,1 МПа
4.1.31 Какое давление на стенки сосуда производят молекулы газа, если масса газа 3 г, объем
4.1.32 Какое давление производит углекислый газ при температуре 330 К, если его плотность
4.1.33 Вычислить среднюю квадратичную скорость молекул углекислого газа
4.1.34 Определить среднеквадратичную скорость молекул газа при давлении 100 кПа и плотности
4.1.35 В баллоне емкостью 40 л находится 10 кг кислорода под давлением 20 МПа. Найти
4.1.36 Энергия поступательного движения, которой обладают все молекулы газа, находящегося
4.1.37 Найти концентрацию молекул газа, у которого средняя квадратичная скорость молекул
4.1.38 В первом сосуде находится азот, во втором – водород. Чему равно отношение давления
4.1.39 В сосуде вместимостью 2 м3 находится 2,4 кг газа. Под каким давлением находится газ
4.1.40 Плотность газа в баллоне электрической лампы 0,9 кг/м3, давление при горении 110 кПа
4.1.41 При какой температуре находится одноатомный газ, если средняя кинетическая энергия
4.1.42 Под каким давлением находится кислород в баллоне, если при температуре 27 C
4.1.43 Найдите отношение средних скоростей молекул O2 и H2 при одинаковой температуре
4.1.44 Найти среднюю квадратичную скорость молекул газа, имеющего плотность 1,8 кг/м3
4.1.45 В баллоне находится кислород при давлении 4 МПа и температуре 42 C. Определить
4.1.46 В баллоне объемом 0,01 м3 находится газ, кинетическая энергия поступательного движения
4.1.47 Во сколько раз плотность метана (CH4) отличается от плотности кислорода (O2)
4.1.48 Определить давление азота в ампуле, если при 0 C в ней концентрация молекул
4.1.49 Во сколько раз средняя квадратичная скорость молекул воздуха при температуре 303 К
4.1.50 При некоторой температуре средняя скорость молекул азота равна 600 м/с. Какова
4.1.51 До какой температуры при нормальном атмосферном давлении надо нагреть кислород
4.1.52 Во сколько раз плотность воздуха зимой при температуре минус 23 C больше плотности
4.1.53 Во сколько раз изменится средняя квадратичная скорость теплового движения молекул
4.1.54 Во сколько раз изменится средняя квадратичная скорость молекул идеального газа
4.1.55 Гелий находится при температуре 580 К. При какой температуре должен находиться
4.1.56 Во сколько раз изменится плотность молекул газа, если при увеличении температуры
4.1.57 Каким давлением нужно сжать воздух, чтобы при температуре 100 C его плотность стала
4.1.58 Среднеквадратичная скорость молекул газа равна 500 м/с. Какой объем займет газ массой
4.1.59 Оценить минимальное расстояние между центрами соседних атомов железа, считая его
4.1.60 Какое время понадобится для того, чтобы на поверхность стекла нанести слой серебра
4.1.61 Концентрация молекул кислорода (M=32 г/моль) в сосуде вместимостью 5 л равна
4.1.62 Если m0 – масса одной молекулы газа, N – общее число молекул газа, а NА – число Авогадро
4.1.63 Если m – масса газа, M – молярная масса газа, а NА – число Авогадро, то по какой формуле
4.1.64 Какое количество вещества содержится в алюминиевой ложке массы 27 г? Относительная
4.1.65 Чему равно среднее расстояние между молекулами насыщенного водяного пара при
4.1.66 Молекула двухатомного газа содержит 16 протонов и 16 нейтронов. Чем равна плотность
4.1.67 В сосуде вместимостью 4 м3 находится 4,8 кг идеального газа. Средняя квадратичная
4.1.68 В сосуде под давлением 10^5 Па плотность идеального газа составляет 1,2 кг/м3. Чему
4.1.69 Если температура идеального газа уменьшится в 4 раза, то во сколько раз изменится
4.1.70 По какой формуле можно рассчитать давление газа через его температуру T
4.1.71 Если M – молярная масса, m0 – масса молекулы, а v^2 – средний квадрат скорости молекул
4.1.72 В 1 см3 объема при давлении 20 кПа находятся 5×10^19 атомов гелия (молярная масса гелия
4.1.73 Если температура идеального газа возрастает в 2 раза, то как изменяется среднеквадратичная
4.1.74 Каким выражением определяется суммарная кинетическая энергия поступательного
4.1.75 В 1 дм3 объема при давлении 10^5 Па находятся 3×10^21 молекул кислорода (молярная
Уравнение Клапейрона-Менделеева
4.2.1 Какой объем занимает 1 кг кислорода при 0 C и давлении 800 кПа?
4.2.2 Найти массу углекислого газа в баллоне вместимостью 40 л при температуре 288 К и
4.2.3 В баллоне емкостью 25,6 л находится 1,04 кг азота при давлении 3,55 МПа. Определите
4.2.4 Баллон содержит 28 кг кислорода при давлении 770 кПа. Какова масса гелия, занимающего
4.2.5 В изотермическом процессе объем газа уменьшился вдвое. Во сколько раз
4.2.6 Некоторая масса газа при давлении 126 кПа и температуре 295 К занимает объем 500 л
4.2.7 Сколько молекул хлора содержится при нормальных условиях в колбе емкостью 0,5 л?
4.2.8 До какой температуры нужно нагреть запаянный шар, содержащий 9 г воды, чтобы шар
4.2.9 Сколько молекул воздуха содержится в комнате объемом 60 м3 при нормальных
4.2.10 Сколько весит воздух, занимающий объем 150 л при температуре 15 C и давлении
4.2.11 В баллоне емкостью 4 л создано давление 0,1 мкПа. Сколько молекул газа содержится
4.2.12 Баллон емкостью 40 л содержит 2,6 кг кислорода. При какой температуре возникает
4.2.13 Найти концентрацию молекул газа, если в баллоне емкостью 4 л создано давление
4.2.14 Сколько молекул ртути содержится в 1 м3 воздуха в помещении, зараженном ртутью
4.2.15 В баллоне емкостью 40 л содержится 1,98 кг углекислого газа при 0 С. При повышении
4.2.16 Баллон содержит 50 л кислорода, температура 27 C, давление 2 МПа. Найти массу
4.2.17 Сколько молекул газа заключено в объеме 0,5 м3, если он при температуре 300 К
4.2.18 В баллоне для сжиженных газов находится 4,2 кг метана (CH4) при давлении 1 МПа
4.2.19 В 1 м3 газа при давлении 120 кПа содержится 2×10^25 молекул, средняя квадратичная
4.2.20 Найти массу водорода, находящегося в баллоне объемом 20 л под давлением 830 кПа
4.2.21 Газ массой 16 г при давлении 1 МПа и температуре 112 C занимает объем 1600 см3
4.2.22 Найти число молекул воздуха в комнате, имеющей объем 8x5x4 м3, при температуре 10 C
4.2.23 Вычислить молярную массу бутана, 2 л которого при температуре 15 C и давлении 87 кПа
4.2.24 Какая часть газа осталась в баллоне, давление в котором было 12,2 МПа, а температура
4.2.25 Идеальный газ при давлении 1,33 кПа и температуре 15 C занимает объем 2 л. Каким
4.2.26 Из баллона емкостью 5 л из-за неисправности вентиля произошла утечка газа, в результате
4.2.27 Газ, объем которого 0,8 м3 при температуре 300 К производит давление 280 кПа. На сколько
4.2.28 В баллоне объемом 200 л при температуре 20 C и давлении 10 МПа находится кислород
4.2.29 Некоторый газ массой 7 г, находящийся в баллоне при температуре 27 C, создает давление
4.2.30 Сколько молекул воздуха выходит из комнаты объемом 80 м3 при повышении температуры
4.2.31 В цилиндре дизеля воздух сжимается от 80 до 3000 кПа, а объем уменьшается от 7,5 до 0,5 л
4.2.32 В открытом сосуде газ нагрели так, что его температура увеличилась в 3 раза. Сколько
4.2.33 Температура воздуха в комнате была 10 C. После того как печь протопили, температура
4.2.34 Газ массой 1,2 г занимает объем 400 см3 при температуре 280 К. После нагревания газа
4.2.35 Из баллона со сжатым водородом объемом 0,01 м3 вытекает газ, при температуре 280 К
4.2.36 Откачанная лампа накаливания объемом 10 см3 имеет трещину, в которую проникает
4.2.37 Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%
4.2.38 При температуре 727 C газ занимает объем 8 л и производит давление 200 кПа на стенки
4.2.39 Воздух в открытом сосуде нагревают от 10 до 600 C и затем, герметически закрыв сосуд
4.2.40 До какой температуры нагрели колбу, содержащую воздух, если давление воздуха в ней
4.2.41 Баллон, содержащий 1 кг азота, при испытании взорвался при температуре 630 К. Какое
4.2.42 При какой температуре давление 240 л водорода равно 126,6 кПа, если при нормальных
4.2.43 В баллоне находилось 5 кг газа при давлении 1 МПа. Какое количество газа взяли из баллона
4.2.44 Во сколько раз изменится объем кислорода массой 0,32 кг, если его давление увеличится
4.2.45 Баллон содержит газ при температуре 7 C и давлении 91,2 МПа. Каким будет давление
4.2.46 В баллоне находится газ при температуре 15 C. Во сколько раз изменится его давление
4.2.47 Сколько электронов заключается в 1 л кислорода при давлении 1 МПа и температуре
4.2.48 Плотность пара некоторого соединения углерода с водородом равна 3 г/л при 43 C
4.2.49 В комнате объемом в 30 м3 температура с 15 C поднялась до 25 C. На сколько при этом
4.2.50 Баллон содержит сжатый газ при 27 C и давлении 3 МПа. Каково будет давление, если
4.2.51 На сколько уменьшится масса воздуха в открытом сосуде, если его нагреть от 0 до 100 C?
4.2.52 Баллон содержит сжатый газ при 27 C и давлении 2000 кПа. Каково будет давление, если
4.2.53 Перед проведением газосварочных работ манометр баллона с кислородом показывал
4.2.54 Газ при давлении 126,6 кПа и температуре 300 К занимает объем 0,6 м3. Найти объем
4.2.55 Газ при давлении 0,2 МПа и температуре 15 C имеет объем 5 л. Чему равен объем
4.2.56 Сосуд вместимостью 0,6 м3, содержащий гелий массой 2 кг, разорвался при температуре
4.2.57 В сосуде объемом 10 литров находится 2 г водорода при температуре 2000 К. Определить
4.2.58 Какова минимальная разница в массе воздуха зимой и летом при нормальном атмосферном
4.2.59 Воздух в сосуде объемом 5 л находится при температуре 27 C под давлением 2 МПа
4.2.60 Некоторая масса водорода находится при температуре 200 К и давлении 0,4 кПа. Газ
4.2.61 Перед проведением газосварочных работ манометр баллона с кислородом показывал
4.2.62 В сосуде находится 1 литр воды при температуре 27 C. Чему стало бы равным давление
4.2.63 В двух сосудах находится одинаковое количество одного и того же газа. В первом сосуде
4.2.64 Резиновая камера содержит воздух при температуре 27 C и нормальном атмосферном
4.2.65 В баллоне объемом 10 л находится кислород, масса которого 12,8 г. Давление в баллоне
4.2.66 Баллон содержит 0,3 кг гелия. Абсолютная температура в баллоне уменьшилась на 10%
4.2.67 В откачанной ампуле объемом 3 см3 содержится радий массой 5 г в течение одного года
4.2.68 Два сосуда, содержащих одинаковую массу одного и того же газа, соединены трубкой
4.2.69 Сколько молей газа следует добавить к одному молю данного газа, чтобы его давление
4.2.70 В открытом цилиндре находится 90 г газа. Температуру газа увеличили от 300 до 450 К
4.2.71 Из баллона объемом 200 дм3, содержащего гелий при давлении 2 МПа и температуре 273 К
4.2.72 На рисунке показан график процесса, происходящего с идеальным газом. Укажите точки
4.2.73 На PT-диаграмме изображен замкнутый процесс, который совершает кислород некоторой
4.2.74 Если нагреть 1 моль идеального газа на 1 К при постоянном объеме, то давление возрастет
4.2.75 Имеется два сосуда с одним и тем же газом при одинаковой температуре. Плотность газа
4.2.76 При увеличении температуры газа на 60 К его объем возрос на 1 л. На сколько литров
4.2.77 Насос захватывает при каждом качании 1 л воздуха при нормальных условиях и нагнетает
4.2.78 Воздушный шар имеет легкорастяжимую теплоизолированную оболочку массой 130 кг
4.2.79 В некотором процессе давление и объем идеального газа связаны соотношением
4.2.80 Какой радиус должен иметь наполненный гелием воздушный шар, чтобы он мог подняться
4.2.81 Надувной шарик, заполненный гелием, удерживают на нити. Найдите натяжение нити
4.2.82 Два баллона с объемами 20 и 10 л соединены длинной тонкой трубкой и содержат 6 моль
4.2.83 Воздушный шар объемом 20 м3, наполненный гелием, поднялся на высоту 180 м за 0,5 минуты
4.2.84 Внутри замкнутого цилиндра, наполненного воздухом, находится шарик радиусом 3 см
4.2.85 На дне цилиндра, наполненного воздухом, плотность которого 1,29 кг/м3, лежит полый
4.2.86 В замкнутом сосуде к верхней стенке на пружине жесткостью 4 Н/м подвешена сфера
4.2.87 Во сколько раз изменится температура идеального газа, если уменьшить его объем
4.2.88 Внутри закрытого с обоих концов горизонтального цилиндра есть поршень
4.2.89 Тонкий резиновый шар радиусом 2 см наполнен воздухом при температуре 20 C
4.2.90 Цилиндрический сосуд делится невесомым поршнем на две части. В одну часть сосуда
4.2.91 Два одинаковых шара соединены тонкой трубкой, в которой находится капелька ртути
4.2.92 Внутри закрытого с обоих концов горизонтального цилиндра имеется тонкий поршень
4.2.93 Два одинаковых сосуда, содержащих газ при 300 К, соединили горизонтальной трубкой
4.2.94 Горизонтально расположенный цилиндр разделен скользящей без трения перегородкой
4.2.95 Объем пузырька, всплывающего на поверхность со дна озера, увеличился в два раза
4.2.96 Состояние одного киломоля идеального газа менялось по графику 1-2-3. Определить
4.2.97 Сосуд объемом 5 л разделен перегородкой на две части, заполненные одним газом
4.2.98 При некотором процессе идеального газа связь между давлением и объемом газа pV^3=const
4.2.99 Воздушный шар объемом 1000 м3 наполнен гелием при температуре окружающего воздуха
4.2.100 В цилиндре с площадью основания 100 см2 находится воздух. Поршень расположен на высоте
4.2.101 В сосуд, на дне которого лежит твердый шар, нагнетают воздух при температуре 27 C
4.2.102 В закрытом с обоих концов цилиндре длиной 2 м поршень соединён с днищами пружинами
4.2.103 Тонкостенный резиновый шар собственным весом 0,6 Н наполнен неоном и погружен в озеро
4.2.104 Давление воздуха в сосуде равно 102,4 кПа. Вместимость цилиндра разрежающего насоса
4.2.105 Компрессор всасывает в 1 мин 3 м3 сухого воздуха при температуре 290 К и давлении 100 кПа
4.2.106 Давление воздуха в сосуде 97 кПа. После трёх ходов откачивающего поршневого насоса
4.2.107 В цилиндре длиной 2L=2 м тонкий поршень соединён с днищами пружинами одинаковой
4.2.108 Газ, занимающий при температуре 127 C и давлении 100 кПа объем 2 л, изотермически
4.2.109 В цилиндре под поршнем находится газ при нормальных условиях. Сначала объем газа
4.2.110 При увеличении абсолютной температуры идеального газа в 2 раза его давление
4.2.111 Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%
Изопроцессы
4.3.1 Определить начальную температуру газа, если при изохорном нагревании
4.3.2 В закрытом баллоне находится газ при температуре 295 К
4.3.3 Давление в откачанной рентгеновской трубке при 15 градусах Цельсия
4.3.4 На сколько Кельвин надо нагреть воздух при постоянном давлении
4.3.5 Газ изотермически сжимают от объема 0,15 м3 до объема 0,1 м3
4.3.6 Газ нагрели на 1 К при постоянном объеме. Давление газа при этом
4.3.7 Газ нагрели на 100 К при постоянном объеме. Давление газа
4.3.8 В закрытом сосуде находится идеальный газ. Во сколько раз
4.3.9 Во сколько раз изменяется плотность идеального газа
4.3.10 В процессе изобарного нагревания газа его объем увеличился в 2 раза
4.3.11 Сосуд объемом 12 м3, содержащий газ под давлением 400 кПа
4.3.12 Сосуд, содержащий 10 л воздуха при давлении 1 МПа, соединяют с пустым
4.3.13 Резиновая камера содержит воздух под давлением 104 кПа. Камеру
4.3.14 До какой температуры нужно нагреть воздух, взятый при 20 градусах
4.3.15 Объем некоторой массы газа при изобарном нагревании на 10 К
4.3.16 Даны две изохоры для одной и той же массы идеального газа
4.3.17 Газ сжат изотермически от 8 до 6 л. Давление при этом возросло
4.3.18 В сосуде объемом 1 л при температуре 183 градуса Цельсия находится
4.3.19 В цилиндре под поршнем изотермически сжимают 9 г водяного
4.3.20 Во сколько раз изменится плотность идеального газа при температуре
4.3.21 При 27 градусах Цельсия газ занимает объем 10 л. До какой
4.3.22 Продукты сгорания газа охлаждаются в газоходе с 1000 до 300 градусов
4.3.23 Газ занимает объем 8 л при температуре 300 К. Определите массу газа
4.3.24 Давление азота в электрической лампочке объемом 0,15 л равно 68 кПа
4.3.25 Бутылка с газом закрыта пробкой, площадь сечения которой 2,5 см2
4.3.26 В цилиндре под поршнем находится газ. Масса поршня 0,6 кг
4.3.27 Два сосуда объемом 2 и 4 л, заполненные одинаковым газом, соединены
4.3.28 В цилиндре под поршнем находится воздух. Вес поршня 60 Н
4.3.29 В цилиндре под поршнем находится вода массой 35 мг и пар массой 25 мг
4.3.30 Баллон, наполненный воздухом при температуре 273 К и атмосферном
4.3.31 В цилиндре под поршнем находится воздух при давлении 0,2 МПа
4.3.32 Один конец цилиндрической трубки, длина которой 25 см и радиус 1 см
4.3.33 Расположенная горизонтально, запаянная с обоих концов стеклянная трубка
4.3.34 В вертикальном закрытом цилиндре находится подвижный поршень
4.3.35 Открытую стеклянную трубку длиной 1 м наполовину погружают в ртуть
4.3.36 В стеклянной трубке находится столбик ртути длиной 10 см. Когда
4.3.37 Посередине откачанной и запаянной с обоих сторон горизонтально
4.3.38 Открытую с обеих сторон стеклянную трубку длиной 60 см
4.3.39 В трубке длиной 1,73 м, заполненной газом, находится столбик ртути
4.3.40 В каком из изображенных на рисунке процессов, проведенных
4.3.41 Горизонтально расположенный закрытый цилиндрический сосуд
4.3.42 На рисунке изображены гиперболы для трех идеальных газов с одинаковыми массами
4.3.43 На рисунке изображены гиперболы для трех идеальных газов с разными массами
4.3.44 Постоянную массу идеального газа переводят из состояния 1
4.3.45 Горизонтально расположенный закрытый цилиндрический сосуд длины
4.3.46 Температура воздуха в комнате повысилась от 17 до 27 градусов Цельсия
4.3.47 Газ при 27 градусах Цельсия занимает объем V. До какой температуры
4.3.48 Баллон, содержащий 12 л кислорода при давлении 1 МПа, соединяют
Влажность
4.4.1 Определите относительную влажность воздуха при температуре 18 C, если точка росы
4.4.2 Определите давление водяных паров в воздухе при температуре 20 С и относительной
4.4.3 5 м3 воздуха при температуре 25 С содержат 86,5 г водяного пара. Определить абсолютную
4.4.4 Определить абсолютную влажность воздуха при температуре 37 C, если давление
4.4.5 В 6 м3 воздуха с температурой 19 С содержится 51,3 г водяного пара. Определите
4.4.6 В 10 м3 воздуха с температурой 19 С содержится 71,3 г водяного пара. Определите
4.4.7 В комнате объемом 120 м3 при температуре 15 C относительная влажность составляет 60%
4.4.8 Найти массу водяного пара, содержащегося в спортивном зале объемом 1100 м3
4.4.9 В комнате объемом 200 м3 относительная влажность воздуха при 20 С равна 70%
4.4.10 При температуре 22 C относительная влажность воздуха равна 60%. Найти относительную
4.4.11 В комнате размером 10x5x3 м3 поддерживается температура 293 К, а точка росы 283 К
4.4.12 В цистерне объемом 10 м3 находится воздух с относительной влажностью 70%
4.4.13 Воздух в помещении имеет температуру 24 C и относительную влажность 50%. Определите
4.4.14 Найти массу водяных паров в 1 м3 воздуха при нормальном атмосферном давлении
4.4.15 Давление водяного пара в воздухе на 40% ниже давления насыщенных паров при этой же
4.4.16 В сосуде объемом 100 л при 27 C находится воздух с относительной влажностью 30%
4.4.17 Влажность в комнате объемом 520 м3 при температуре 25 C равна 90%. Какое количество
4.4.18 Сколько надо испарить воды в 1000 м3 воздуха, относительная влажность которого 40%
4.4.19 В комнате объемом 60 м3 при температуре 18 C относительная влажность воздуха 50%
( 63 оценки, среднее 4.44 из 5 )