Вариант
1.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Ядро атома алюминия (27Al)
образовано
1) 14 протонами и
13электронами 3) 13 протонами и 14 нейтронами
2) 14 протонами и
13 нейтронами 4) 13 нейтронами и 14 электрона
2. Массовая
доля серы в сернистой кислоте равна
1)
18,0% 2) 24,5% 3)
39,0% 4) 65,2%
3. Высшую степень окисления хлор имеет в
соединении
1) KClO3 2)
CaCl2 3)
NH4Cl
4) KClO4
4.
Гидроксид
бария реагирует с каждым из двух веществ:
1) HCl и KNO3
3) Na2SO4 и FeCl3
2)
CO2 иCa(OH)2
4) SiO2 и CuO
5. Порядковый
номер элемента соответствует
1)
высшей валентности атома 3) числу нейтронов в ядре
2)
числу электронов в атоме 4) числу электронных уровней в атоме
6. Ковалентная
неполярная связь в молекуле:
1)
PH3
2) P4
3) NaBr 4) H2O
7. В каком ряду химических элементов
усиливаются неметаллические свойства соответствующих им простых веществ?
1) барий→магний→кальций
3) литий→натрий→калий
2)
германий→кремний→углерод 4) кислород→азот→углерод
8. Признаком
протекания химической реакции между карбонатом магния и соляной кислотой
является
1) образование осадка 3)
изменение цвета
2) выделение газа 4)
появление запаха
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите соответствие между формулой
вещества и классом веществ, к которому оно относится.
|
ФОРМУЛА |
КЛАСС |
|
А) K2O Б) Fe(OH)2 В) Na2SO4 Г) |
1) 2) 3) 4) 5) нерастворимое |
10. Установите
соответствие между исходными веществами и продуктами реакции
|
ИСХОДНЫЕ |
ПРОДУКТЫ |
|
А) CaO + H2O Б) K2CO3 В) SO2 Г) KOH + H2SO4 |
1) CaCO3 2) K2SO3 3) Ca(OH)2 4) K2SO4 5) Ca(OH)2 |
Часть 2
11. С какими
из указанных веществ реагирует гидроксид натрия: оксид калия, оксид углерода(IV),
гидроксид бария, серная кислота, хлорид меди (II). Составьте
уравнения возможных реакций. Для реакций ионного обмена напишите уравнения в
полном и сокращенном виде.
12. Какую
массу соли нужно растворить в 270 г воды для получения 10 % раствора.
Вариант
2.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Ядро атома фосфора (31Р)
образовано
1) 15 протонами и
16 электронами 3) 15 протонами и 16 нейтронами
2) 16 протонами и
15 нейтронами 4) 15 нейтронами и 16 электронами
2. Массовая
доля кислорода в фосфорной кислоте равна
1)
3,1% 2) 31,6% 3)
16,3% 4) 65,3%
3. Степень окисления — 4 углерод
проявляет в соединении
1) K2CO3
2) CCl4 3)
Al4C3 4)
CO2
4. Раствор
хлороводородной кислоты реагирует с каждым из двух веществ:
1)
CuO и KNO3
3) H2SO4 и Fe2O3
2)
AgNO3 и Ca(OH)2
4) SiO2 и MgO
5. Номер
периода периодической системы определяет
1)
высшую валентность атома 3) число протонов в ядре
2)
число электронов в атоме 4) число электронных уровней в
атоме
6.
Ионная
связь в молекуле:
1) SO2 2) N2
3)K2O
4)H2SO4
7. У какого из указанных химических элементов
наибольший атомный радиус
1) кислород 2)
сера 3) фтор 4) хлор
8. Признаком
протекания химической реакции между гидроксидом железа (II) и соляной кислотой
является
1) образование осадка 3)
растворение осадка
2) выделение газа 4)
появление запаха
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите соответствие между формулой
вещества и классом веществ, к которому оно относится.
|
ФОРМУЛА |
КЛАСС |
|
А) Na2S В) Na2O Г) |
1) 2) 3) 4) 5) |
10. Установите
соответствие между исходными веществами и продуктами реакции
|
ИСХОДНЫЕ |
ПРОДУКТЫ |
|
А) Na2O Б) Na2SO4 В) H2SO4 Г) Na + H2O |
1) BaO + NaCl 2) NaOH + H2 3) BaSO4 4) BaSO4 5) NaOH |
Часть 2
11. С какими
из указанных веществ реагирует раствор серной кислоты: оксид кальция, оксид
углерода(IV),
гидроксид бария, медь, магний. Составьте уравнения возможных реакций. Для
реакций ионного обмена напишите уравнения в полном и сокращенном виде.
12. Какую
массу соли нужно растворить в 160 г воды, для получения 20% раствора.
Вариант
3.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1.
Электронная формула внешнего энергетического уровня 2s2 2p1 соответствует
химическому элементу
1)
B; 2)
Al; 3)
Na; 4)
K.
2. Какова массовая доля фосфора в фосфате
кальция?
1) 41,3% 2)
38,7% 3) 12,9% 4)20%
3. Формула
вещества, в котором степень окисления марганца равна +6:
1)
MnO2 2) К2MnO4 3)
КMnO4 4)
Mn(OH)2
4. Оксид
натрия взаимодействует с оксидом фосфора (V) с образованием
1)
фосфида натрия 2) фосфата натрия 3) фосфина 4)
фторида натрия
5. Число
электронов на внешнем слое атома с зарядом +15 равно
1)
5 2) 2 3)
3 4) 4
6. Ковалентная
полярная связь образуется между химическими элементами:
1)
серой и хлором 3) калием и хлором
2)
фтором и натрием 4) кислородом и кислородом.
7.
Кто
проявляет более неметаллические свойства
1) фосфор 3) сера
2) мышьяк 4) азот
8. Реакция
между цинком и соляной кислотой относится к реакциям:
1)
разложения; 2) соединения; 3) замещения; 4)
обмена.
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9.Установите
соответствие между формулой вещества и его названием
ИСХОДНЫЕ
ВЕЩЕСТВА НАЗВАНИЕ ВЕЩЕСТВА
А)
Na2SO4
1. Оксид серы (VI)
Б)
H2SO4
2.
Сульфит натрия
В)
SO3 3.
Сероводородная кислота
Г)
H2S 4.
Серная кислота
5.
Сульфат натрия
10. Установите соответствие
|
ТИП ХИМИЧЕСКОЙ |
СХЕМА ХИМИЧЕСКОЙ |
|
А) реакция Б) реакция В)Реакция Г)Реакция |
1. MgCO3 = 2. CuO + Al = Cu + Al2O3 3. NO + O2 = 4. BaCl2 +Na2SO4 |
Часть 2
11. Используя метод электронного баланса,
составьте уравнение реакции, соответствующее схеме превращений
HCl + HNO3 → NO + Cl2+ H2O
Определите
окислитель и восстановитель.
12.К
200г 10%-ного раствора нитрата натрия добавили 50г воды. Определите массовую
долю вещества в полученном растворе.
Вариант
4.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Восьмиэлектронную внешнюю оболочку имеет ион
1) Р3+
2) S2-
3) С4+ 4) Fe2+
2.
Массовая доля кальция наибольшая в
1) CaF2
2) CaI2
3) CaCl2
4) CaBr2
3.
Минимальную и максимальную степень окисления атомы азота проявляют в веществах:
1) NH3, N2О5 2) N2О, N2О3 3)NО2,NО 4)
NH3, NО
4. Оксид
калия взаимодействует с оксидом серы (VI) с образованием
1)
сульфида калия 2) сульфата калия
3)
сульфита калия 4) гидроксида калия
5. Число
электронов на внешнем слое атома, ядро которого содержит 11 протонов, равно
1)
1 2) 6 3)
3 4) 8
6. С
каким веществом вступает во взаимодействие гидроксид цинка?
1)
хлорид натрия 2) оксид серы (VI)
3)
вода 4) сульфат
бария
7. Ковалентная
полярная связь характерна для вещества, формула которого:
1) O2
2) NaH3 3)
KCl 4) Na
8. Какая из предложенных реакций представляет собой
реакцию замещения?
1) FeO + H2SO4 = FeSO4
+ H2O
2) Fe + H2SO4= FeSO4
+ H2
3) 3Fe + 2O2 = Fe3O4
4) FeCO3 = FeO + CO2
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите
соответствие между формулой вещества и его названием
|
ИСХОДНЫЕ |
НАЗВАНИЕ |
|
А) HNO3 Б) N2O5 В) KNO3 Г) Cu(NO3)2 |
1. Оксид 2. 3. 4. 5. |
10. Установите
соответствие:
|
ХИМИЧЕСКИЕ |
ПРИЗНАКИ |
|
|
А) Ржавление Б) Скисание В) Гниение мяса Г) Горение дров |
1) выпадение 2) изменение 3) выделение 4) изменение 5) выделение |
|
Часть 2
11. Используя метод электронного баланса,
составьте уравнение реакции, соответствующее схеме превращений
S + HNO3 → NO2 + H2SO4 + H2O
Определите
окислитель и восстановитель.
12. Смешали 200 г 40% и 100 г 30% раствора
азотной кислоты. Определите массовую долю кислоты в полученном растворе.
Вариант
5.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Химический
элемент расположен в 3 периоде, 4 группе, главной подгруппе. Это
1)
Ga 2)
Si 3)
Ti 4)
C
2. Массовая
доля кислорода в карбонате кальция равна:
1)0,16
2) 0,48 3) 0,3 4) 0,25
3. Степень
окисления фосфора равна +3 в соединении:
1)
Mg3P4 2)
P2O5 3)
H3PO4 4)
P2O3
4. Химическая
реакция возможна между растворами веществ:
1) NaOH и Ba(NO3)2
3) FeCl2 и MgCl2
3) HCl и KNO3
4) Na2SO4 и Ba(OH)2
5. На внешнем
энергетическом уровне у атома Na находится:
1)
3e 2)
8e 3)
5e 4)
1e
6. Выберите
вещество, с которым вступает в реакцию гидроксид меди (II):
1)
нитрат натрия
2)
гидроксид хрома (III)
3)
азотная кислота
4)
сульфат бария
7. Какая
группа веществ относится к сложным:
1)
NaCl, O3, Cl2, H2О
3) H2SO4, NH3, SiО2, ZnO
2)
CaCO3, O2, Cu, HNO2 4)
KCl, P4, Br2 , Fe
8. К
физическим явлениям относится :
1)
горение магния 3) замерзание воды
2)
ржавление железа 4) горение угля
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите
соответствие между формулой вещества и его названием
|
ИСХОДНЫЕ |
НАЗВАНИЕ |
|
А) Cr(OH)3 Б) CrO В) Cr(NO2)3 Г) |
1) оксид 2) нитрит 3) нитрат 4) |
10. Установи соответствие между реагирующими веществами
и продуктами их взаимодействия.
|
ИСХОДНЫЕ |
ПРОДУКТЫ |
|
А) N2+H2 |
1) NO2 2) NH3 3) NH3+NaCI+H2O 4) NH4CI |
Часть 2
11. Осуществите превращения. Запишите
необходимые уравнения реакций в молекулярном виде, а уравнения № 3 и № 4 в
полном и сокращенном ионном виде.
12.
Смешали
150 г 25% раствора селитры и 200 г 45% раствора селитры. Определите массовую
долю селитры в полученном растворе.
Вариант
6.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Химический
элемент расположен в 5 периоде ,1 группе, побочной подгруппе. Это
1)
Cu 2)Rb 3)
Ag 4)
Sr
2. Массовая
доля (%) натрия в сульфате натрия равна:
1)32,4%
2) 15,6% 3) 23,6% 4) 30,3%
3. Степень
окисления азота равна +1 в соединении:
1)
N2 2)
NH3 3)
HNO3 4)
N2O
4. В каком
случае вещества не взаимодействуют между собой?
1)
H,SO4 и К2СO3
2)
НCl и
AgNO3
3)
HNO3 и ZnCl2
4)
HNO3 и NaOH
5. На внешнем
энергетическом уровне у атома фосфора находится:
1)
3e 2)
15e 3)
5e
4) 8e
6. Ковалентная
полярная связь в молекуле:
1)
О3 2) ZnCl2 3)
H2O 4)
H2
7. Какая
группа веществ относится к простым:
1)
Н2, НCl, Cl2, О2
3) NaCl, Cl2, Na, О3
2)
Fe, O3, P4, N2 4)
FeO, Fe, Mg, HNO3
8. К
химическим явлением относится :
1)
горение серы 3) плавление серы
2)
испарение воды 4) замерзание воды
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите
соответствие:
|
ФОРМУЛА СОЕДИНЕНИЯ |
НАЗВАНИЕ |
|
А. ZnO Б. Ca (NO3)2 В. H2SiO3 Г. Mn(OH)2 |
1) 2) Оксид 3) 4) 5) 6) |
10.Установи соответствие между реагирующими веществами
и продуктами их взаимодействия.
|
ФОРМУЛА |
НАЗВАНИЕ |
|
А. ZnO +HCl Б. Ca(NO3)2+NaOH В. H2SiO3+ Г. Mn(OH)2 |
1) K2SiO3+H2O 2) ZnCl2+H2O 3) MnSO4+H2O 4) Ca(OH)2+NaNO3 |
Часть 2
11. Какие ниже перечисленные
вещества будут взаимодействовать с гидроксидом калия: SO3,
CuO, P2O5,
SiO2, Fe2O3.
Составьте молекулярные и ионные уравнения возможных реакций.
12.
К
80 г 15% раствора прибавлено 20 г воды. Какова массовая доля полученного
раствора?
Вариант
7.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Определите
элемент, если в его атоме 40 электронов:
1)
Алюминий 2) Цирконий
3)
Германий 4) Галлий
2.
Массовая
доля азота наибольшая в…….
1) Ba3N2 2) Ca3N2
3)
Be3N2
4)
Mg3N2
3. Как
называется элемент X, если
формула его соединения SX3, а
массовая доля серы 40%
1) кислород 2) фтор 3) селен 4) бром
4. Выберите
вещество, с которым взаимодействует сероводород:
1)
хлорид натрия 2) хлорид меди (II)
3)
соляная кислота 4) сульфат бария
5. Чему равно
число электронов на внешнем энергетическом уровне атома:
1)
Порядковому номеру
2)
Номеру периода
3)
Номеру группы
4)
Числу нейтронов в ядре
6.
Вещества
только с ионной связью – в наборе:
1)
HCl, KCl 2) NH4Cl, SiCl4
3)
NaF, CsCl 4) NaI, P2O5
7. В каком
ряду расположены сложные вещества?
1) S,
Al, N2 2) CO2,
Fe, H2O
3) HNO3,
CaO, PH3 4) Si, P4, Fe2O3
8. В каком
ряду последовательно расположены формулы основания, кислоты, основного оксида,
кислой соли
1) KOH,
HCl, CuO, Na(HSO4)
2) Ca(OH)2,
SO2, CaO, KHS
3) (CuOH)2CO3,
CO2, HNO3, MgO, Ca(HCO3)2
4) NaOH,
HCN, BaO, K2S
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите
соответствие:
|
НАЗВАНИЕ |
ФОРМУЛА |
|
А. Б. Кремниевая В. Азотная Г. Соляная |
1) HCl 2) HNO3 3) H2SO4 4) HNO3 5) H2S 6) H2SiO3 |
10. Установи соответствие между исходными веществами и
продуктами реакции
|
ИСХОДНЫЕ |
ПРОДУКТЫ |
|
А. Mg + H2SO4 Б. SO3 В. BaCl2 Г. Ba + HCl |
1) BaCl2 2) K2SO4 3) MgSO4 4) BaSO4 |
Часть 2
11.
С какими из перечисленных ниже веществ будет взаимодействовать хлорид
меди (II):
цинк, нитрат натрия, гидроксид калия, серебро, вода, гидроксид алюминия, нитрат
серебра? Составьте молекулярные и ионные уравнения возможных реакций.
12.
К
100 г 30% раствора соли добавили 10 г сахара. Какова массовая доля соли в
полученном растворе?
Вариант
8.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Определите
элемент, если в его атоме 25 электронов:
1)
Титан 2) Хром
3)
Марганец 4) Бром
2.
Массовая
доля калия наибольшая в……..
1) KBr 2) KCl
3) KF
4) KI
3. Степень окисления азота в соединениях N2O5, NH3 соответственно
равна
1) +2 и -3
2) +5 и -3 3) +5 и +3
4) -5 и +3
4. Укажите
вещества, при взаимодействии которых выделяется газ:
1)
гидроксид алюминия и хлорид натрия
2)
нитрат серебра и хлорид натрия
3)
карбонат кальция и уксусная кислота
4)
хлорид калия и нитрат натрия
5. В ряду
элементов O — S – Se –Te радиусы
атома
1) уменьшаются 2) увеличиваются
3) не изменяются 4) не знаю
6.
В
каком веществе связь полярнее
1) H2S 2) H2O 3) HCl 4) KH
7. В каком
ряду расположены простые вещества?
1) S,
Al, N2 2) CO2,
Fe, H2O
3) HNO3,
CaO, PH3 4) Si, P4, Fe2O3
8. В каком
ряду последовательно расположены формулы кислоты, кислотного оксида, основной
соли и основания
1) HCl, SO2, (CuOH)2CO3
, KOH ,
2) Ca(OH)2,
CaO, KHS, CO2
3) CuO, Na(HSO4),
HNO3, MgO, Ca(HCO3)2
4) NaOH, HCN, BaO,
K2S
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установите соответствие между формулой
вещества и его названием
|
ФОРМУЛА |
НАЗВАНИЕ |
|
А. MgO Б. Ca (NO3)2 В.H2SO3 Г.КOH |
1) 2) Оксид 3) 4) 5) 6) |
10. Установите
соответствие:
|
ТИП |
СХЕМА |
|
А. Б. реакция В. реакция Г. реакция |
1) СaCO3 = 2) ZnO + H2 3) NO + O2 4) BaCI2 |
Часть 2
11.
С какими из предложенных веществ может взаимодействовать раствор
нитрата меди (II): соляная кислота, гидроксид калия, цинк, фосфат кальция, сульфид
калия, серебро, вода, гидроксид магния? Уравнения реакций, протекающих в растворах,
составьте в ионном виде.
12.
Какова
массовая доля сахара в растворе, полученном при упаривании 100 г 20% раствора
до 80 г?
Вариант
9.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Суммарное число электронов в катионе Mg2+ и анионе F— равно
1) 9 2)
10 3) 20 4) 21
2.
Массовая
доля хлора будет наименьшей в
1) FeCl3 2) CrCl3 3)AlCl3 4)
TiCl3
3.
Как
называется неметалл Э, если формула его соединения ЭО3, а массовая
доля кислорода 60% (Ответ: 4)
1) азот 2) селен 3) фосфор 4)
сера
4. Какая пара
оксидов не может вступать в реакцию?
1)
СаО и SiO2
2)
SO2 и CrO3
3)СО
и MgO 4) Al2O3 и Na2O
5.
В
ряду элементов P – Si – Al – Mg радиусы
атома
1) уменьшаются 2) увеличиваются
3) не изменяются 4) не знаю
6. Тип химической связи в молекуле азота
1) ковалентная неполярная
2) ионная
3) ковалентная полярная 4)
металлическая
7.
При
взаимодействии с водой образует щелочь
1) Li2O 2) SO3
3)
CO2
4)
FeO
8.
Сумма
коэффициентов в уравнении реакции между CO2 и Ca(OH)2 равна
1) 1 2) 2 3)
3 4) 4
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установи соответствие между исходными веществами и
продуктами реакции
|
10.
Установите
соответствие между формулой вещества и его названием
|
ФОРМУЛА |
НАЗВАНИЕ |
|
А.CO2 Б.MgSO4 В.Ca(OH)2 Г.Li2O |
1) 2) 3) соль 4) 5) |
Часть 2
11. Используя метод электронного баланса,
составьте уравнение реакции, соответствующее схеме превращений
KClO3 + S → KCl + SO2
Определите
окислитель и восстановитель.
12. Смешали 20 г 45% и 10 г 35% раствора
азотной кислоты. Определите массовую долю кислоты в полученном растворе.
Вариант
10.
Часть 1
При выполнении заданий 1–8 выберите один правильный
ответ
1. Электронная формула Э2- (He)3s23p6 отвечает
элементу
1) аргон 2)
хлор 3) сера 4) фосфор
2.
Относительная
молекулярная масса будет наибольшей для
1) Na3PO4 2) Tl3PO4 3) Rb3PO4
4)
Li3PO4
3. Как называется металл М, если формула его
соединения МО, а массовая доля кислорода 40%
1) кальций 2) медь 3) магний 4)
титан
4. С каким
веществом вступает во взаимодействие оксид кремния (IV)?
1)
оксид йода (V) 2) оксид серы (VI)
3)
вода 4) оксид кальция
5.
Неметаллические
свойства в ряду элементов Al – Si – C – N
1) увеличиваются 2) уменьшаются
3) не изменяются 4) не знаю
6.
В
хлориде натрия химическая связь
1) ионная 2)
ковалентная полярная
3) ковалентная неполярная 4) водородная
7.
Гидроксид
натрия взаимодействует с
1) SO3 2)
Na2O
3) Mg(OH)2
4)N2O
8.
Реакция
между магнием и соляной кислотой относиться к реакциям
1) обмена 2) замещения
3) разложения 4) соединения
При
выполнении заданий 9, 10 к каждому элементу первого столбца подберите
соответствующий
элемент из второго столбца.
9. Установи соответствие между исходными веществами и
продуктами реакции
|
ИСХОДНЫЕ |
ПРОДУКТЫ |
|
А. Zn + H2SO4 Б. ZnSO4 В. ZnO + SO3 Г. ZnO + H2SO4 |
1) ZnSO4 2) ZnSO4 3) ZnSO4 4) Zn(OH)2 |
10. Установите соответствие между формулой
вещества и его названием
|
ФОРМУЛА |
НАЗВАНИЕ |
|
А. K2SiO3 Б. Mn(OH)2 В. SO2 Г. KOH |
1) кислотный 2) 3) соль 4) 5) |
Часть 2
11.
Даны
следующие вещества: гидроксид натрия, соляная кислота, фторид аммония, нитрат
серебра. Напишите уравнения всех возможных реакций, протекающих попарно между
предложенными веществами в водном растворе.
12. К 10 г 3%
раствора соли добавили 5 г сахара. Какова массовая доля соли в полученном
растворе?
Пояснительная
записка
Экзаменационная
работа по химии для учащихся 8 классов составлена на основе программы курса
химии для 8-11 классов общеобразовательных учреждений/ О.С. Габриелян. М.:
Дрофа, 2011 и на основе программы по учебным предметам. Химия 8-9 классы:
проект.- М.: Просвещение, 2010. – (стандарты второго поколения), соответствующих
требованиям государственного стандарта образования, и предназначена для
учащихся 8 классов, изучающих химию на базовом уровне.
Время проведения
экзаменационной работы – 40 минут.
Экзаменационная
работа составлена в 10 вариантах, в форме ОГЭ.
Задания 1-8 с
выбором одного правильного ответа;
задание 9, 10 на
установление соответствия;
задания 11, 12
требуют выполнение с развёрнутым ответом.
Оценивание работы
Задания 1-8 оцениваются одним баллом.
Задания 9, 10 считаются
выполненными верно, если правильно установлены четыре соответствия, при этом
задание оценивается двумя баллами. Если установлены три соответствия, ответ
оценивается 1 баллом.
Задания 11 — 5 баллов
Задания 12 — 5 баллов
Максимальное количество баллов – 22 балла
Шкала перевода первичных баллов в школьную отметку
|
Баллы |
0-6 |
7-13 |
14-18 |
19-22 |
|
Отметка |
2 |
3 |
4 |
5 |
ОТВЕТЫ К ЭКЗАМЕНАЦИОННОЙ РАБОТЕ ПО ХИМИИ ДЛЯ 8 КЛАССА
Часть 1
|
№ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
1 |
3 |
3 |
1 |
2 |
2 |
3 |
2 |
3 |
3 |
3 |
|
2 |
3 |
4 |
4 |
1 |
2 |
1 |
3 |
3 |
3 |
2 |
|
3 |
4 |
3 |
2 |
1 |
4 |
4 |
1 |
4 |
4 |
3 |
|
4 |
3 |
2 |
2 |
2 |
4 |
3 |
2 |
3 |
3 |
4 |
|
5 |
2 |
4 |
1 |
1 |
4 |
3 |
3 |
2 |
2 |
1 |
|
6 |
2 |
3 |
1 |
2 |
3 |
3 |
3 |
4 |
1 |
1 |
|
7 |
2 |
2 |
3 |
2 |
3 |
2 |
3 |
1 |
1 |
1 |
|
8 |
2 |
1 |
3 |
2 |
3 |
1 |
1 |
1 |
4 |
2 |
|
9 |
3541 |
4235 |
5413 |
4153 |
5123 |
2564 |
3621 |
2531 |
2311 |
3412 |
|
10 |
3124 |
5342 |
1423 |
2135 |
2143 |
2413 |
3241 |
4132 |
1325 |
3412 |
Часть 2
Вариант 1.
|
Утверждаю Директор ___________Л.С.Жуковская – Латышева «_____» _____________ 2016 г. |
Материалы письменного экзамена по химии
8Б, Р класса МБОУ гимназии № 44
в 2015 – 2016 учебном году
Прохорова В.В., учитель химии высшей категории.
|
Рассмотрено и согласовано на ШМО «Природа» учителей протокол № ___ от ___ ______2016 г. Руководитель ШМО __________ Т. А. Степанова |
Экзаменационная
работа по химии
ученика
8 __ класса
(Фамилия, Имя)
Часть 1.
(задание 1-8)
|
№ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
Ответ |
Баллы: ________
(задание 9,10)
|
№ |
9 |
10 |
|
Ответ |
_ _ _ _ |
_ _ _ _ |
Баллы: ________
Часть 2.
Баллы: ________
Всего баллов:
________
Оценка: ________
Председатель
аттестационной комиссии: _____________ / /
Учитель:
_____________ / /
Член
аттестационной комиссии: _____________
/ /
Задания переводного экзамена по химии в 8 классе
Вариант 2
1. Знак Cl имеет химический элемент:
|
А) хром |
В) медь |
|
Б) хлор |
Г) кальций |
2. Число протонов в ядре фосфора:
3. Неметаллом является:
|
А) бром |
В) барий |
|
Б) калий |
Г) железо |
4. Немолекулярное строение у вещества:
|
А) водород |
В) кислород |
|
Б) вода |
Г) медь |
5. Раствором является:
|
А) вода с глиной |
В) вода с речным песком |
|
Б) морская вода |
Г) дистиллированная вода |
6. К химическим явлениям относится:
|
А) плавление льда |
В) ковка металлов |
|
Б) испарение воды |
Г) сгорание угля |
7. К сложным веществам относится:
|
А) кислород |
В) хлороводород |
|
Б) сера |
Г) алмаз |
8. Условная запись состава вещества — это
|
А) химический символ |
В) химическое уравнение |
|
Б) химическая формула |
Г) химический знак |
9. Вокруг ядра атома движутся
|
А) протоны |
В) электроны |
|
Б) нейтроны |
Г) протоны и электроны |
10. В состав сульфидов обязательно входит химический элемент
|
А) кислород |
В) хлор |
|
Б) водород |
Г) сера |
11. Переменную валентность, равную IV, имеет
|
А) углерод |
В) фосфор |
|
Б) кислород |
Г) водород |
12. Для разделения воды и поваренной соли надо использовать
|
А) выпаривание |
В) фильтрование |
|
Б) отстаивание |
Г) кристаллизацию |
13. Метану соответствует химическая формула
14. В химической реакции 2H2O 2H2 + O2 происходит
|
А) соединение |
В) обмен |
|
Б) замещение |
Г) разложение |
15. Обозначение Ar имеет
|
А) объем вещества |
В) относительная атомная масса |
|
Б) масса вещества |
Г) относительная молекулярная масса |
16. Молярный объем газа имеет значение
|
А) 22,4 г/моль |
В) 18 л/моль |
|
Б) 22,4 л/моль |
Г) 6,02 *1023 моль-1 |
17. Относительная атомная масса хлора равна
18. Относительная молекулярная масса воды равна
19. К химическим приборам относится
|
А) пробирка |
В) химический стакан |
|
Б) колба |
Г) пробирконагреватель |
20. В химической лаборатории разрешается
|
А) употреблять пищу |
В) сливать растворы в раковину |
|
Б) хранить ядовитые вещества |
Г) использовать битую посуду |
21. Указать название химического вещества:
MgCl2 _________________________
22. Провести соответствие между химическими формулами и классами веществами:
|
А) гидроксид натрия |
1) оксиды |
|
Б) карбонат алюминия |
2) основания |
|
В) оксид цинка |
3) кислоты |
|
Г) азотная кислота |
4) соли |
23. Провести соответствие между химическими уравнениями и типами реакций:
|
А) Сu(OH)2 СuO + H2О |
1) обмен |
|
Б) H2 + Cl2 2HCl |
2) замещение |
|
В) Fe + CuSO4 FeSO4 + Cu |
3) разложение |
|
Г) KOH + HCl KCl + H2O |
4) соединение |
24. Закончить схемы химических реакций:
|
А) Al + О2 |
|
Б) К + Cl2 |
25. Решить задачу:
Вычислить объем водорода, вступающего в реакцию с 6 г углерода.
Дано: Решение.
С + 2H2 СН4
Ответ:
Экзаменационную работу по химии за 20__-20__ учебный год
выполнил__ учени___ 8 класса
______________________________________________
Количество набранных баллов: ___________
Оценка: ____________
Экзаменующий учитель: ______________
Ассистент: ________________
Вариант 1
1. Во 2-м периоде VIA группе Периодической системы находится химический элемент, схема строения атома которого
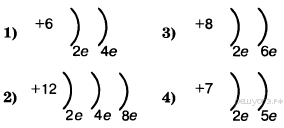
2. В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) алюминий → фосфор → хлор
2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
3. В соединении натрия с кислородом химическая связь
1) ионная
2) ковалентная полярная
3) ковалентная неполярная
4) металлическая
4. В каком соединении степень окисления фосфора равна +3?
1)
2)
3)
4)
5. Сложным является каждое из двух веществ:
1) кислород и озон
2) белый фосфор и азотная кислота
3) серная кислота и вода
4) вода и барий
6. К какому типу реакций относится уравнение реакции между гидроксидом алюминия и серной кислотой
1) соединение
2) замещение
3) обмен
4) разложение
7. Наибольшее количество положительных ионов образуется при диссоциации 1 моль
1) фосфата натрия
2) серной кислоты
3) нитрата железа(III)
4) сульфида калия
8. При взаимодействии хлорида железа(III) и гидроксида калия образуется
1) вода
2) газ
3) осадок
4) реакция не идет
9. Оксид меди(II) взаимодействует с водным раствором
1) хлорида калия
2) хлороводорода
3) карбоната натрия
4) сульфата магния
10. Определите формулу неизвестного вещества в схеме реакции:
1)
2)
3)
4)
11. Практически осуществимой является реакция между
1) и
2) и
3) и
4) и
12. К окислительно-восстановительным относят реакцию, уравнение которой
1)
2)
3)
4)
13. На какой диаграмме распределение массовых долей элементов соответствует ?
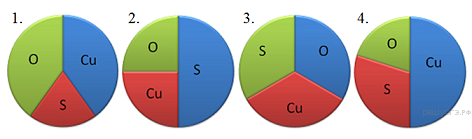
14. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
Среди химических элементов
1) наибольший радиус имеют атомы серы
2) наибольшую электроотрицательность имеет магний
3) степень окисления −4 и +4 характерны только для кремния
4) только сера образует высший оксид с кислотными свойствами
5) простое вещество-металл образует только магний
15. Используя метод электронного баланса, составьте уравнение реакции.
Mg + HCl =
Определите окислитель и восстановитель.
16. К 106 г раствора карбоната натрия c массовой долей 10% добавляли соляную кислоту до прекращения выделения газа. Найти массу необходимой кислоты.
Вариант 2
1. Элемент имеет два электрона на 3-м энергетическом уровне. Порядковый номер элемента
1) 2
2) 3
3) 12
4) 16
2. Кислотные свойства высших оксидов ослабевают в ряду:
1)
2)
3)
4)
3. Какой вид химической связи характерен для меди?
1) ионная
2) металлическая
3) ковалентная полярная
4) ковалентная неполярная
4. Степень окисления -2 атом серы проявляет в каждом из соединений:
1) и
2) и
3) и
4) и
5. Простым является каждое из двух веществ:
1) кислород и метан
2) аммиак и ртуть
3) алмаз и хлор
4) медь и вода
6. Какое уравнение соответствует реакции обмена?
1)
2)
3)
4)
7. К сильным электролитам относится каждое из двух веществ:
1) и
2) и
3) и
4) и
8. Вода образуется при действии азотной кислоты на
1)
2)
3)
4)
9. Оксид калия реагирует
1) только с оснóвными оксидами
2) только с кислотными оксидами
3) как с кислотными, так и с оснóвными оксидами
4) как с кислотными, так и с амфотерными оксидами
10. Соляная кислота вступает в окислительно-восстановительную реакцию с
1)
2)
3)
4)
11. Раствор хлорида цинка реагирует с каждым из двух веществ:
1) и
2) и
3) и
4) и
12. Элемент азот является окислителем в реакции
1)
2)
3)
4)
13. На какой диаграмме распределение массовых долей элементов соответствует количественному составу фосфата кальция?
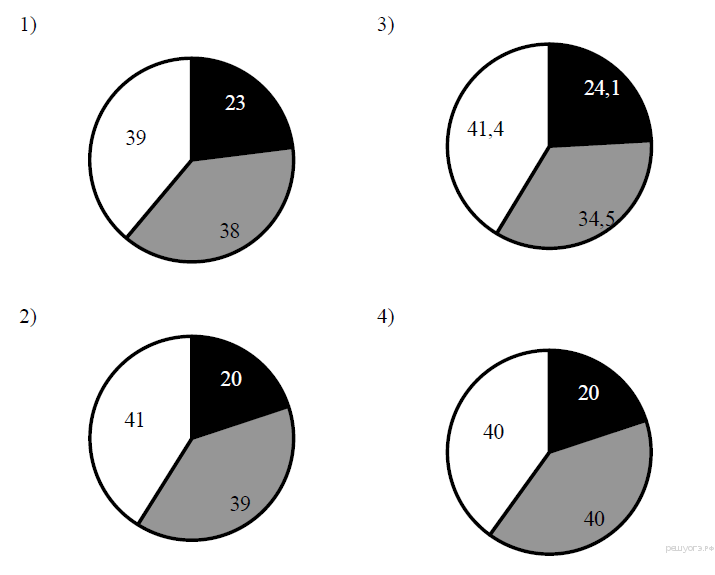
14. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
Значения высших степеней окисления элементов увеличиваются в рядах:
1)
2)
3)
4)
5)
15 . Используя метод электронного баланса, составьте уравнение реакции.
Al + O2=
Определите окислитель и восстановитель.
16. Через 80 г раствора гидроксида натрия с массовой долей растворённого вещества 10% пропустили углекислый газ до образования карбоната натрия. Вычислите объём (н.у.), затраченного на реакцию газа.
Вариант 3
1. В атоме химического элемента содержится 15 электронов. Сколько из них находятся на внешнем энергетическом уровне?
1) 1
2) 3
3) 5
4) 7
2. В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) алюминий → фосфор → хлор
2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
3. Ковалентная полярная связь имеется в молекуле
1) серной кислоты
2) пластической серы
3) хлора
4) сульфида рубидия
4. В каком из соединений степень окисления азота равна −3?
1) N2O3
2) KNO2
3) NH4Cl
4) HNO3
5. Формулам и
соответствуют названия
1) оксид азота(I) и гидроксид меди(I)
2) оксид азота(II) и гидроксид меди(I)
3) оксид азота(II) и гидроксид меди(II)
4) оксид aзотa(IV) и гидроксид меди(II)
6. Какое уравнение соответствует реакции замещения?
1)
2)
3)
4)
7. Хорошо растворимым в воде сильным электролитом является каждое из двух веществ:
1) и
2) и
3) и
4) и
8. В реакцию и с гидроксидом кальция, и с нитратом серебра вступает
1) карбонат магния
2) хлорид аммония
3) нитрат натрия
4) сульфат бария
9. Оксид серы(IV) может реагировать с каждым веществом пары
1)
2)
3)
4)
10. Гидроксид кальция реагирует с
1) углекислым газом
2) кислородом
3) водородом
4) поваренной солью
11. С раствором сульфата меди (II) реагирует
1)
2)
3)
4)
12. Установите соответствие между схемой химической реакции и элементом-восстановителем в этой реакции.
|
СХЕМА РЕАКЦИИ |
ВОССТАНОВИТЕЛЬ |
|
A) |
1) |
|
Б) |
2) |
|
B) |
3) |
|
4) |
|
|
5) |
|
13. На какой диаграмме распределение массовых долей элементов соответствует ?

14. Сходство бора, углерода и азота проявляется в том, что
1) в ядрах их атомов одинаковое число протонов
2) в их атомах одинаковое число электронных слоёв
3) простые вещества проявляют неметаллические свойства
4) в соединениях проявляют только положительные степени окисления
5) образуемые ими высшие оксиды относятся к основным оксидам
15. Используя метод электронного баланса, составьте уравнение реакции по схеме:
Са + HCl =
Определите окислитель и восстановитель
16. К раствору карбоната калия массой 110,4 г и массовой долей 5% прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.
Вариант 4
1. Число электронов во внешнем электронном слое атома, ядро которого содержит 10 протонов, равно
1) 8
2) 2
3) 6
4) 4
2. Валентность элемента в водородном соединении уменьшается в ряду
1)
2)
3)
4)
3. Такой же вид химической связи, как и в молекуле H2S, характерен для
1) K2O
2) S8
3) Na2S
4) СО2
4. В каком соединении хлор проявляет высшую возможную степень окисления?
1)
2)
3)
4)
5. Кислоте соответствует оксид
1)
2)
3)
4)
6. Какое уравнение соответствует реакции обмена?
1)
2)
3)
4)
7. Сульфат-анион при диссоциации в водном растворе образует каждое из двух веществ:
1) и
2) и
3) и
4) и
8. При взаимодействии карбоната кальция и соляной кислоты происходит образование
1) воды
2) газа
3) осадка
4) реакция не идет
9. Оксид натрия реагирует с каждым из двух веществ:
1) и
2) и
3) и
4) и
10. Соль и вода образуются в результате взаимодействия гидроксида меди(II) c
1) серой
2) водородом
3) соляной кислотой
4) сульфидом натрия
11. Среди веществ: ,
,
в реакцию с раствором
вступает(-ют)
1) только
2) и
3) и
4) и
12. Установите соответствие между схемой химической реакции и элементом-окислителем в этой реакции.
|
СХЕМА РЕАКЦИИ |
ОКИСЛИТЕЛЬ |
|
A) |
1) |
|
Б) |
2) |
|
B) |
3) |
|
4) |
|
|
5) |
13. На какой диаграмме распределение массовых долей элементов соответствует количественному составу фосфата бария?
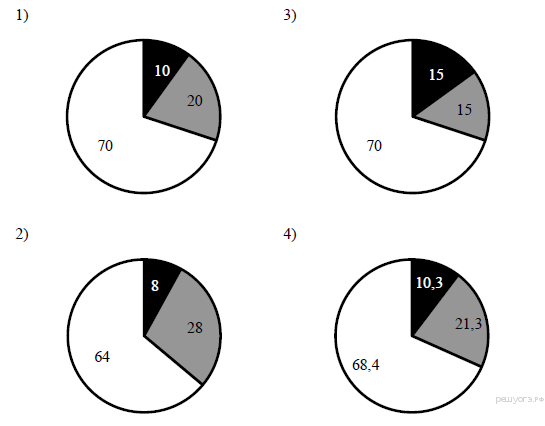
14. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
В ряду химических элементов уменьшается
1) заряд ядра атома
2) радиус атома
3) электроотрицательность элемента
4) валентность в летучем водородном соединении
5) число заполненных электронами энергетических уровней
15. Используя метод электронного баланса, составьте уравнение реакции по схеме:
Li + O2 =
Определите окислитель и восстановитель.
16. К 106 г раствора карбоната натрия c массовой долей 10% добавляли раствор хлорида кальция до прекращения выделения осадка. Вычислите массу осадка.
Ответы к экзаменационному материалу по химии в 8 классе.
Вариант 1
1) 3
2) 1
3) 1
4) 2
5) 3
6) 3
7) 1

9) 2
10) 2
11) 3
12) 2
13) 1
14) 35
15)
Mg0 + 2H+Cl— = Mg+2Cl—2 + Н20
Mg0 – 2е = Mg+2 восстановитель
2H+ +2е = Н20 окислитель
16)
1. Рассчитаем массу вещества карбоната натрия
m(Na2CO3)=106*0,1=10,6 г
2. Составим уравнение реакции:
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
3. Найдем молярные массы веществ и составим пропорцию
10,6/106=х/2*71
х= 14,2 г
Ответ: m(HCl)= 14,2 г
Вариант 2
1) 3
2) 1
3) 2
4) 4
5) 3
6) 1
7) 2

9) 4
10) 4
11) 2
12) 1
13) 2
14) 14
15) 4Al0 + 3O20 = 2Al2+3O3-2
Al0 -3e = Al+3 восстановитель
O20 +4e = 2O-2 окислитель
16) 1. Рассчитаем массу вещества гидроксида натрия
m(NaOH)=80*0,1=8 г
2. Составим уравнение реакции:
2NaOH + CO2 = Na2CO3 + H2O
3. Найдем молярные массы веществ и составим пропорцию
8/2*40=х/22,4
х= 2,24 л
Ответ: m(CO2)= 2,24 л
Вариант 3
1) 3
2) 1
3) 1
4) 3
5) 4
6) 1
7) 2

9) 1
10)1
11) 2
12) 235
13) 1
14) 23
15. Са0 + 2H+Cl— = Са+2Cl—2 + Н20
Са0 – 2е = Са+2 восстановитель
2H+ +2е = Н20 окислитель
16) 1. Рассчитаем массу вещества карбоната калия
m(K2CO3)=110,4*0,05=5,52 г
2. Составим уравнение реакции:
K2CO3 + Ca(NO3)2 = 2KNO3 + CaCO3
3. Найдем молярные массы веществ и составим пропорцию
5,52/138=х/100
х= 4
Ответ: m(CaCO3)= 4 г
Вариант 4
1) 1
2) 4
3) 4
4) 2
5) 3
6) 3
7) 2

9) 3
10) 3
11) 1
12) 143
13) 4
14) 24
15) 2Li0 + O20 = 2Li2+ O-2
Li0 -1e = Li+ восстановитель
O20+ 4е = 2O-2 окислитель
16) 1. Рассчитаем массу вещества карбоната натрия
m(Na2CO3)=106*0,1=10,6 г
2. Составим уравнение реакции:
3. Найдем молярные массы веществ и составим пропорцию
10,6/106=х/100
х= 1
Ответ: m(CaCO3)= 1 г
Вариант 5
1. Число электронов во внешнем электронном слое атома, ядро которого содержит 10 протонов, равно
1) 8
2) 2
3) 6
4) 4
2. Среди перечисленных элементов наименьшей электроотрицательностью обладает
1) сера
2) кислород
3) углерод
4) кремний
3. Вещество, образованное посредством ионных связей:
1) оксид серы(IV)
2) оксид бария
3) сероводород
4) аммиак
4. Степень окисления азота уменьшается в ряду:
1)
2)
3)
4)
5. Кислоте соответствует оксид
1)
2)
3)
4)
6. Горение сероводорода
является реакцией
1) соединения
2) окислительно-восстановительной
3) замещения
4) обмена
7. При диссоциации 1 моль соли в растворе образовалось 4 моль положительных и отрицательных ионов. Формула соли —
1)
2)
3)
4)
8. Практически полностью в водном растворе взаимодействуют вещества:
1) нитрат серебра и хлороводород
2) нитрат кальция и хлорид калия
3) хлороводород и нитрат натрия
4) хлороводород и нитрат калия
9. Оксид серы(IV) может реагировать с каждым веществом пары
1)
2)
3)
4)
10. Гидроксид магния реагирует с
1) оксидом углерода (II)
2) сульфатом натрия
3) алюминием
4) азотной кислотой
11. Среди веществ: — в реакцию с соляной кислотой вступает(-ют)
1) и
2) и
3) только
4) и
12. Фосфор является окислителем в реакции
1)
2)
3)
4)
13. На какой диаграмме распределение массовых долей элементов соответствует количественному составу фосфата кальция?

14. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
В ряду химических элементов происходит уменьшение (ослабление)
1) числа протонов в ядрах атомов
2) числа электронных слоев в атомах
3) радиуса атомов
4) металлических свойств
5) кислотного характера свойств высших оксидов
15. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
Zn + HNO3 =
Определите окислитель и восстановитель.
16. К 89 г раствора хлорида алюминия с массовой долей 15% добавили избыток раствора нитрата свинца. Определите массу выпавшего осадка.
Примерный план экзаменационной работы для учащихся 8 класса по химии
Проверяемые элементы содержания
Атомы химических элементов.
Закономерности Периодической системы
Типы химических связей. Степень окисления
Соединения химических элементов
Типы химических реакций. Изменения
происходящие с веществами
Растворение. Растворы. Свойства растворов
электролитов
Химические свойства классов
неорганических соединений
Количественные отношения в химии
Закономерности периодической системы
Химические свойства классов химических
соединений
Окислительно—восстановительные реакции
Химические свойства классов
неорганических соединений
Химические свойства веществ
Количественные отношения в химии (задачи)
Обозначения типов задания:
ВО— с выбором ответа
КО— с кратким ответом
РО— с развернутым ответом
Оценивание заданий и работы в целом
Верное выполнение каждого задания части 1 работы оценивается одним
баллом. Задания с выбором ответа считается выполненным, если учащимся
указан код правильного ответа. Во всех остальных случаях (выбран другой
ответ; выбрано два или более ответа, среди которых может быть и
правильный; ответ на вопрос отсутствует) задание считается невыполненным.
Учащийся получает 0 баллов.
Задание с кратким ответом на установление соответствия или на
множественный выбор считается выполненным верно, если из шести
предлагаемых ответов учащийся выбирает 3 правильных. В других случаях
(выбран один правильный ответ; среди двух выбранных ответов один
неправильный; выбрано более двух ответов, вреди которых один правильный)
выполнение задания оценивается 1 баллом. Если же среди выбранных ответов
нет ни одного правильного, задание считается невыполненным. Учащийся
получает 0 баллов.
Каждое из двух заданий с развернутым ответом предусматривает
проверку усвоения трех элементов содержания (устанавливать взаимосвязи
между понятиями и фактами, самостоятельно и осознанно использовать знания
при ответе, использовать дополнительные знания при ответе). Следовательно,
выполнение задания с развернутым ответом оценивается 3,2,1 и 0 баллами.
Экзаменационная оценка ученика по пятибалльной шкале определяется
на основе суммарного числа баллов, полученных за выполнения задания:
«5» 25-30 баллов
«4» 19-24 баллов
«3» 10-18 баллов
«2» 1-9 баллов
Организация и проведение промежуточной аттестации
Время выполнения работы: Примерное время, отводимое на выполнение
отдельных заданий, составляется для каждого задания:
Части 1— 1-2 минуты
Части 2— 2-3 минуты
Части 3— до 5 минут
Общая продолжительность работы 60—70 минут
Экзаменационная работа по химии 8 класс
Демонстрационная версия
Инструкция:
Работа состоит из 3 частей
1 часть— тестовая (с выбором одного правильного ответа), состоящая из
16 вопросов. Правильный ответ оценивается 1 баллом
2 часть— задания на соответствие, состоящая из 4 вопросов. Полностью
правильный ответ оценивается 2 баллами, 2 из 4—ых соответствий
оцениваются 1 баллом.
3 часть— задание со свободным ответом, состоящая из 2 вопросов.
Полностью правильный ответ оценивается 3 баллами
ЧАСТЬ 1
Внимательно прочитай вопрос и предложенные к нему варианты
ответов и выбери только один правильный.
Внимательно прочитай задание выбери один правильный ответ и
перенеси в бланк ответов, обметив его «крестиком»
соответствующим правильному ответу
А 1. Число нейтронов в ядре атома марганца равно
1) 45 2) 55 3) 30 4) 25
А 2. Основные свойства оксидов в ряду: Al
2
O
3
→ MgO → Na
2
O
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
А 3. В хлориде натрия химическая связь
1) ковалентная полярная 2) ковалентная неполярная
3) ионная 4) металлическая
А 4. Степень окисления —3 азот имеет в соединении
1) N
2
O
3
2) KNO
3
3) NaNO
2
4) NH
4
NO
3
А 5. К основному оксиду относится
1) CO
2
2) Р
2
О
5
3) SiО
2
4) Na
2
O
А 6. Признаком реакции между сульфатом меди (II) и гидроксидом
калия является
1) выделение газа 2) изменение цвета раствора
3) выпадение осадка 4) появление запаха.
А 7. Серная кислота вступает в реакцию замещения с
1) серебром
2) гидроксидом натрия
3) хлороводородной кислотой
4) магнием
А 8. Реакция ионного обмена возможна между:
1) гидроксидом натрия и хлоридом железа (III)
2) железом и соляной кислотой
3) кальцием и водой
4) оксидом магния и водой
А 9. Электролитом является
1) оксид цинка
2) сахар
3) этиловый спирт
4) хлороводородная кислота
А 10. Наибольшее число ионов образуется при полной диссоциации
1) FeCl
2
2) FeCl
3
3) Fe (NO
3
)
2
4) Fe
2
(SO
4
)
3
А 11. Соляная кислота не способна взаимодействовать:
1) гидроксидом калия
2) оксидом цинка
3) оксидом углерода (IV)
4) силикат натрия
А 12. Са(ОН)
2
может про взаимодействовать с каждым из двух
веществ:
1) НСl и СuО
2) Н
2
SО
4
и СО
2
3) НNО
3
и Н
2
О
4) O
2
и Nа
2
О
А 13. Какие из пар оксидов могут про взаимодействовать:
1) СuО и СаО 2) SiО
2
, и Н
2
О 3) СаО и Н
2
О 4) SО
2
и СО
2
А 14. Какие из всех солей ряда относятся к кислым:
1) К
2
SO
4
, СаНSO
4
, СаОНСl
2) КНSО
3
, СаНSO
4
, ВаНРО
4
3) KNO
3
, ВаНРО
4
, К
3
РО
4
4) NaCl, КНSО
3
, FеСl
3
.
А 15. Смесь воды и бензина можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) делительной воронки
А16. Массовая доля серы в сульфите натрия равна
1) 25,4% 2) 36,5% 3) 50,0% 4) 28,6%
ЧАСТЬ 2
Внимательно прочитай вопрос и варианты ответов и выбери только
правильные 2 ответа
В1. В ряду химических элементов Rb → K → Na → Li
1) увеличивается число электронов во внешнем слое
2) ослабевают металлические свойства
3) увеличивается радиус атомов
4) уменьшается число протонов в ядре
5) увеличиваются заряды ядер атомов
В2. Натрий вступает в реакцию с
1) водой
2) раствором соляной кислоты
3) алюминием
4) хлором
5) оксидом кальция
В3. Выберите уравнения реакций, которые относятся к
окислительно—восстановительным:
1) 2NO + 4CuO = N
2
+ 2Cu
2
O
2) NаОН + НСl = NаСl + Н
2
О
3) СuСl
2
+ 2LiОН = 2LiСl + Сu(ОН)
2
4) N
2
+ 3Ca = Ca
3
N
2
5) NH
4
Сl + КОН = NН
3
+ Н
2
O + КСl
В задании В4 на установление соответствия запишите в таблицу
цифры выбранных вами ответов. Получившуюся
последовательность цифр запишите в строку ответа.
В4. Установите соответствие между исходными веществами и
продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) CаО + H
2
SО
4
→ 1) → Са(NО
3
)
2
+ АgСl
Б) Са + H
2
SО
4
→ 2) → СаSО
4
+Н
2
В) СаСl
2
+ АgNО
3
3) → СаSО
4
4) → СаSО
4
+Н
2
О
Ответ: _________________ .
ЧАСТЬ 3
С1. Напишите уравнения реакций, с помощью которых можно
осуществить следующие превращения:
Ва → ВаО → ВаСl
2
→ ВаSО
4
С2. К 100 г 48% — ного раствора сульфата меди (II) прилили избыток
раствора фосфата натрия. Определите массу выпавшего осадка.
Экзаменационная работа по химии 8 класс
Вариант 1
Инструкция:
Работа состоит из 3 частей
1 часть— тестовая (с выбором одного правильного ответа), состоящая из
16 вопросов. Правильный ответ оценивается 1 баллом
2 часть— задания на соответствие, состоящая из 4 вопросов. Полностью
правильный ответ оценивается 2 баллами, 2 из 4—ых соответствий
оцениваются 1 баллом.
3 часть— задание со свободным ответом, состоящая из 2 вопросов.
Полностью правильный ответ оценивается 3 баллами
ЧАСТЬ 1
Внимательно прочитай вопрос и предложенные к нему варианты
ответов и выбери только один правильный.
Внимательно прочитай задание выбери один правильный ответ и
перенеси в бланк ответов, обметив его «крестиком»
соответствующим правильному ответу
А 1. Число протонов в ядре атома ванадия равно
1) 51 2) 50 3) 23 4) 28
А 2. Основные свойства оксидов в ряду: Na
2
O→ MgO → Al
2
O
3
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
А 3. В оксиде кремния химическая связь
1) ковалентная полярная 2) ковалентная неполярная
3) ионная 4) металлическая
А 4. Степень окисления +5 азот имеет в соединении
1) N
2
O
3
2) KNO
3
3) NaNO
2
4) NH
4
NO
2
А 5. К кислотному оксиду относится
1) CаO 2) Р
2
О
5
3) К
2
О 4) Na
2
O
А 6. Признаком реакции между силикатом натрия и соляной
кислотой является
1) выделение газа 2) изменение цвета раствора
3) выпадение осадка 4) появление запаха.
А 7. Соляная кислота вступает в реакцию замещения с
1) железом
2) серебром
3) хлороводородной кислотой
4) гидроксидом натрия
А 8. Реакция ионного обмена возможна между:
1) кальцием и водой
2) железом и соляной кислотой
3) карбонатом натрия и серной кислотой
4) оксидом магния и водой
А 9. Электролитом является
1) оксид железа (III)
2) натрий
3) этиловый спирт
4) фосфорная кислота
А 10. Наибольшее число ионов образуется при полной диссоциации
1) FeCl
2
2) FeCl
3
3) Fe (NO
3
)
2
4) Fe
2
(SO
4
)
3
А 11. Фосфорная кислота не способна взаимодействовать:
1) оксидом цинка
2) гидроксидом натрия
3) оксидом серы (IV)
4) хлоридом бария
А 12. Ва(ОН)
2
может про взаимодействовать с каждым из двух
веществ:
1) НСl и СuО
2) O
2
и Nа
2
О
3) НNО
3
и Н
2
О
4) Н
2
SО
4
и СО
2
А 13. Какие из пар оксидов могут провзаимодействовать при
обычных условиях:
1) ВаО и СаО 2) SО
2
, и Н
2
О 3) МgО и Н
2
О 4) SiО
2
и СО
2
А 14. Какие из всех солей ряда относятся к основным:
1) КНSО
3
, СаНSO
4
, ВаНРО
4
2) KNO
3
, ВаНРО
4
, К
3
РО
4
3) NaCl, КНSО
3
, FеСl
3
.
4) (ВаОН)
2
SO
4
, (МgОН)NО
3
, СаОНСl
А 15. Смесь воды и песка можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) делительной воронки
А16. Массовая доля азота в нитрате натрия равна
1) 25,4% 2) 36,5% 3) 16,5% 4) 28,6%
ЧАСТЬ 2
Внимательно прочитай вопрос и варианты ответов и выбери только
правильные 2 ответа
В1. В ряду химических элементов Li → Na → K → Rb
1) увеличивается число электронов во внешнем слое
2) ослабевают металлические свойства
3) увеличивается радиус атомов
4) уменьшается число протонов в ядре
5) увеличиваются заряды ядер атомов
В2. Оксид серы (VI) вступает в реакцию с
1) водой
2) раствором соляной кислоты
3) алюминием
4) хлором
5) оксидом кальция
В3. Выберите уравнения реакций, которые относятся к
окислительно—восстановительным:
1) NаОН + НСl = NаСl + Н
2
О
2) NH
4
Сl + КОН = NН
3
+ Н
2
O + КСl
3) 2N
2
O + C = 2N
2
+ CO
2
4) СuСl
2
+ 2LiОН = 2LiСl + Сu(ОН)
2
5) 4NH
3
+ 5O
2
= 4NO + 6H
2
O
В задании В4 на установление соответствия запишите в таблицу
цифры выбранных вами ответов. Получившуюся
последовательность цифр запишите в строку ответа.
В4. Установите соответствие между исходными веществами и
продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) CаО + H
2
SО
4
→ 1) → Са(NО
3
)
2
+ АgСl
Б) Са + H
2
SО
4
→ 2) → СаSО
4
+Н
2
В) СаСl
2
+ АgNО
3
3) → СаSО
4
4) → СаSО
4
+Н
2
О
ЧАСТЬ 3
С1. Напишите уравнения реакций, с помощью которых можно
осуществить следующие превращения:
Р → Р
2
О
5
→ Н
3
РО
4
→ Са
3
(РО
4
)
2
С2. К 100 г 50% — ного раствора гидроксида бария прилили избыток
раствора серной кислоты. Определите массу выпавшего осадка.
Экзаменационная работа по химии 8 класс
Вариант 2
Инструкция:
Работа состоит из 3 частей
1 часть— тестовая (с выбором одного правильного ответа), состоящая из
16 вопросов. Правильный ответ оценивается 1 баллом
2 часть— задания на соответствие, состоящая из 4 вопросов. Полностью
правильный ответ оценивается 2 баллами, 2 из 4—ых соответствий
оцениваются 1 баллом.
3 часть— задание со свободным ответом, состоящая из 2 вопросов.
Полностью правильный ответ оценивается 3 баллами
ЧАСТЬ 1
Внимательно прочитай вопрос и предложенные к нему варианты
ответов и выбери только один правильный.
Внимательно прочитай задание выбери один правильный ответ и
перенеси в бланк ответов, обметив его «крестиком»
соответствующим правильному ответу
А 1. Число электронов в ядре атома железа равно
1) 26 2) 55 3) 56 4) 30
А 2. Кислотные свойства оксидов в ряду: SiO
2
→ Р
2
O
5
→ SO
3
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
А 3. В оксиде алюминия химическая связь
1) ковалентная полярная 2) ковалентная неполярная
3) ионная 4) металлическая
А 4. Степень окисления +3 азот имеет в соединении
1) N
2
O
3
2) KNO
3
3) NaNO
3
4) NH
4
NO
3
А 5. К основному оксиду относится
1) CO
2
2) Р
2
О
5
3) SiО
2
4) Na
2
O
А 6. Признаком реакции между карбонатом натрия и соляной
кислотой является
1) выделение газа 2) изменение цвета раствора
3) выпадение осадка 4) появление запаха.
А 7. Серная кислота вступает в реакцию замещения с
1) серебром
2) гидроксидом натрия
3) хлороводородной кислотой
4) магнием
А 8. Реакция ионного обмена возможна между:
1) гидроксидом натрия и хлоридом железа (III)
2) железом и соляной кислотой
3) кальцием и водой
4) оксидом магния и водой
А9. Электролитом не является
1) серная кислота
2) сахар
3) гидроксид натрия
4) хлороводородная кислота
А 10. Наименьшее число ионов образуется при полной диссоциации
1) FeCl
2
2) FeCl
3
3) Fe (NO
3
)
3
4) Fe
2
(SO
4
)
3
А 11. Соляная кислота способна взаимодействовать:
1) гидроксидом калия
2) оксидом серы (IV)
3) оксидом углерода (IV)
4) серной кислотой
А 12. Са(ОН)
2
может про взаимодействовать с каждым из двух
веществ:
1) НСl и СuО
2) Н
2
SО
4
и СО
2
3) НNО
3
и Н
2
О
4) O
2
и Nа
2
О
А 13. Какие из пар оксидов могут про взаимодействовать:
1) СuО и СаО 2) SiО
2
, и Н
2
О 3) СаО и Н
2
О 4) SО
2
и СО
2
А 14. Какие из всех солей ряда относятся к средним:
1) К
2
SO
4
, СаНSO
4
, СаОНСl
2) КНSО
3
, СаНSO
4
, ВаНРО
4
3) KNO
3
, ВаНРО
4
, К
3
РО
4
4) NaCl, К
2
SО
3
, FеСl
3
.
А 15. Смесь железа и песка можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) действия магнита
А16. Массовая доля кислорода в оксиде алюминия равна
1) 25,4% 2) 36,5% 3) 50,0% 4) 47,0%
ЧАСТЬ 2
Внимательно прочитай вопрос и варианты ответов и выбери только
правильные 2 ответа
В1. В ряду химических элементов Сl → Вr → I → Аt
1) увеличивается число электронов во внешнем слое
2) ослабевают неметаллические свойства
3) увеличивается радиус атомов
4) уменьшается число протонов в ядре
5) уменьшаются заряды ядер атомов
В2. Оксид калия вступает в реакцию с
1) водой
2) соляной кислотой
3) алюминием
4) хлором
5) оксидом кальция
В3. Выберите уравнения реакций, которые относятся к
окислительно—восстановительным:
1) 2NO + 4CuO = N
2
+ 2Cu
2
O
2) NаОН + НСl = NаСl + Н
2
О
3) СuСl
2
+ 2LiОН = 2LiСl + Сu(ОН)
2
4) N
2
+ 3Ca = Ca
3
N
2
5) NH
4
Сl + КОН = NН
3
+ Н
2
O + КСl
В задании В4 на установление соответствия запишите в таблицу
цифры выбранных вами ответов. Получившуюся
последовательность цифр запишите в строку ответа.
В4. Установите соответствие между исходными веществами и
продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) ВаО + SО
3
→ 1) → Ва(NО
3
)
2
+ АgСl
Б) Ва(ОН)
2
+ H
2
SО
4
→ 2) → ВаSО
4
+Н
2
В) ВаСl
2
+ АgNО
3
3) → ВаSО
4
4) → ВаSО
4
+Н
2
О
ЧАСТЬ 3
С1. Напишите уравнения реакций, с помощью которых можно
осуществить следующие превращения:
Сu → СuО → СuСl
2
→ Сu(ОН)
2
С2. К 50 г 20% — ного раствора гидроксида натрия прилили избыток
раствора сульфата меди (II). Определите массу выпавшего осадка.
Экзаменационная работа по химии 8 класс
Вариант 3
Инструкция:
Работа состоит из 3 частей
1 часть— тестовая (с выбором одного правильного ответа), состоящая из
16 вопросов. Правильный ответ оценивается 1 баллом
2 часть— задания на соответствие, состоящая из 4 вопросов. Полностью
правильный ответ оценивается 2 баллами, 2 из 4—ых соответствий
оцениваются 1 баллом.
3 часть— задание со свободным ответом, состоящая из 2 вопросов.
Полностью правильный ответ оценивается 3 баллами
ЧАСТЬ 1
Внимательно прочитай вопрос и предложенные к нему варианты
ответов и выбери только один правильный.
Внимательно прочитай задание выбери один правильный ответ и
перенеси в бланк ответов, обметив его «крестиком»
соответствующим правильному ответу
А 1. Число протонов в ядре атома алюминия равно
1) 13 2) 14 3) 27 4) 26
А 2. Кислотные свойства оксидов в ряду: СO
2
→ SiO
2
→ GeO
2
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
А 3. В молекуле хлора химическая связь
1) ковалентная полярная 2) ковалентная неполярная
3) ионная 4) металлическая
А 4. Степень окисления +7 хлор имеет в соединении
1) НСlO 2) НСlO
2
3) НСlO
3
4) НСlO
4
А 5. К кислотному оксиду относится
1) CO 2) СО
2
3) Nа
2
O 4) N
2
O
А 6. Признаком реакции между сульфидом натрия и соляной
кислотой является
1) выделение газа 2) изменение цвета раствора
3) выпадение осадка 4) появление запаха.
А 7. Азотная кислота вступает в реакцию нейтрализации с
1) серебром
2) гидроксидом натрия
3) хлороводородной кислотой
4) магнием
А 8. Реакция ионного обмена возможна между:
1) цинком и серной кислотой
2) натрий и водой
3) гидроксидом калия и хлоридом меди (II)
4) оксидом магния и водой
А 9. Электролитом является
1) оксид железа (III)
2) кальций
3) этиловый спирт
4) серная кислота
А 10. Наименьшее число ионов образуется при полной диссоциации
1) Na
2
SO
4
2) NaNO
3
3) Na
3
PO
4
4) Na
2
SiO
3
А 11. Гидроксид натрия не способен взаимодействовать:
1) оксидом серы
2) оксидом углерода (IV)
3) гидроксидом калия
4) сульфат меди (II)
А 12. НСl может про взаимодействовать с каждым из двух веществ:
1) НNO
3
и СuО
2) Н
2
SО
4
и СО
2
3) AgNО
3
и NaOH
4) O
2
и Nа
2
О
А 13. Какие из пар оксидов могут про взаимодействовать:
1) СuО и СаО 2) SiО
2
, и Н
2
О 3) SiО
2
и СО 4) K
2
О и Н
2
О
А 14. Какие из всех солей ряда относятся к основным:
1) NaCl, КНSО
3
, FеСl
3
.
2) (МgОН)
2
SО
3
, (СаОН)
2
SO
4
, (ВаОН)
3
РО
4
3) KNO
3
, ВаНРО
4
, К
3
РО
4
4) К
2
SO
4
, СаНSO
4
, СаОНСl
А 15. Смесь воды и масла можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) делительной воронки
А16. Массовая доля кислорода в фосфате натрия равна
1) 49% 2) 39% 3) 59% 4) 29%
ЧАСТЬ 2
Внимательно прочитай вопрос и варианты ответов и выбери только
правильные 2 ответа
В1. В ряду химических элементов F → Cl → Br → I
1) увеличивается число электронов во внешнем слое
2) ослабевают металлические свойства
3) увеличивается радиус атомов
4) уменьшается число протонов в ядре
5) увеличиваются заряды ядер атомов
В2. Оксид натрия вступает в реакцию с
1) оксидом кальция
2) раствором соляной кислоты
3) алюминием
4) хлором
5) водой
В3. Выберите уравнения реакций, которые относятся к
окислительно—восстановительным:
1) N
2
+ 3Ca = Ca
3
N
2
2) NH
4
Сl + КОН = NН
3
+ Н
2
O + КСl
3) NаОН + НСl = NаСl + Н
2
О
4) 2NO + 4CuO = N
2
+ 2Cu
2
O
5) СuСl
2
+ 2LiОН = 2LiСl + Сu(ОН)
2
В задании В4 на установление соответствия запишите в таблицу
цифры выбранных вами ответов. Получившуюся
последовательность цифр запишите в строку ответа.
В4. Установите соответствие между исходными веществами и
продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) SO
3
+ NaOH
→ 1) → H
2
SO
4
+ H
2
O
Б) S + О
2
→ 2) → Na
2
SO
4
+Н
2
В) SO
3
+ H
2
O →
3) → Nа
2
SО
4
+ H
2
O
4) → SO
2
5) → H
2
SO
4
ЧАСТЬ 3
С1. Напишите уравнения реакций, с помощью которых можно
осуществить следующие превращения:
Li → Li
2
O → LiOH → Li
3
PO
4
С2. К раствору карбоната калия массой 110,4 г и массовой долей 5%
прилили избыток раствора нитрата кальция. Вычислите массу образо—
вавшегося осадка
.
Экзаменационная работа по химии 8 класс
Вариант 4
Инструкция:
Работа состоит из 3 частей
1 часть— тестовая (с выбором одного правильного ответа), состоящая из
16 вопросов. Правильный ответ оценивается 1 баллом
2 часть— задания на соответствие, состоящая из 4 вопросов. Полностью
правильный ответ оценивается 2 баллами, 2 из 4—ых соответствий
оцениваются 1 баллом.
3 часть— задание со свободным ответом, состоящая из 2 вопросов.
Полностью правильный ответ оценивается 3 баллами
ЧАСТЬ 1
Внимательно прочитай вопрос и предложенные к нему варианты
ответов и выбери только один правильный.
Внимательно прочитай задание выбери один правильный ответ и
перенеси в бланк ответов, обметив его «крестиком»
соответствующим правильному ответу
А 1. Число электронов в атоме хлора равно
1) 17 2) 19 3) 35 4) 18
А 2. Основные свойства оксидов в ряду: МgO → CaO → BaO
1) усиливаются
2) ослабевают
3) не изменяются
4) изменяются периодически
А 3. В молекуле хлороводорода химическая связь
1) ковалентная полярная 2) ковалентная неполярная
3) ионная 4) металлическая
А 4. Степень окисления +6 сера имеет в соединении
1) Н
2
SO
3
2) SO
3
3) SO
2
4) H
2
S
А 5. К основному оксиду относится
1) CO 2) СаО
3) NO 4) N
2
O
А 6. Признаком реакции между сульфидом натрия и хлоридом
свинца (II) является
1) выделение газа 2) изменение цвета раствора
3) выпадение осадка 4) появление запаха.
А 7. Оксид калия вступает в реакцию присоединения с
1) серной кислотой
2) водой
3) хлороводородной кислотой
4) магнием
А 8. Реакция ионного обмена возможна между:
1) соляной кислотой и алюминием
2) хлорид алюминия и гидроксидом натрия
3) серой и кислородом
4) оксидом кальция и водой
А 9. Неэлектролитом является
1) хлорид натрия (раствор)
2) гидроксид кальция (раствор)
3) этиловый спирт
4) серная кислота
А 10. Наибольшее число ионов образуется при полной диссоциации
1) Na
2
SO
4
2) NaNO
3
3) Na
3
PO
4
4) Na
2
SiO
3
А 11. Соляная кислота не способна взаимодействовать:
1) оксидом натрия
2) оксидом углерода (IV)
3) гидроксидом калия
4) нитратом серебра
А 12. NaOH может про взаимодействовать с каждым из двух
веществ:
1) НNO
3
и СuО
2) O
2
и Nа
2
О
3) КNО
3
и КOH
4) Н
2
SО
4
и СО
2
А 13. Какие из пар оксидов могут про взаимодействовать:
1) Na
2
O и СаО 2) SО
2
и Н
2
О 3) SiО
2
и СО 4) CuО и Н
2
О
А 14. Какие из всех солей ряда относятся к средним:
1) NaCl, К
2
SО
3
, FеСl
3
2) KNO
3
, ВаНРО
4
, К
3
РО
4
3) (МgОН)
2
SО
3
, (СаОН)
2
SO
4
, (ВаОН)
3
РО
4
4) К
2
SO
4
, СаНSO
4
, СаОНСl
А 15. Смесь воды и чернил можно разделить с помощью
1) перегонки 2) фильтрования
3) выпаривания 4) делительной воронки
А16. Массовая доля калия в гидроксиде калия равна
1) 69,6% 2) 79,4% 3) 59,4% 4) 29,4%
ЧАСТЬ 2
Внимательно прочитай вопрос и варианты ответов и выбери только
правильные 2 ответа
В1. В ряду химических элементов С → N → O → F
1) увеличивается число электронов во внешнем слое
2) ослабевают неметаллические свойства
3) увеличивается радиус атомов
4) уменьшается число протонов в ядре
5) увеличиваются заряды ядер атомов
В2. Оксид серы (IV) вступает в реакцию с
1) оксидом кальция
2) раствором соляной кислоты
3) алюминием
4) хлором
5) водой
В3. Выберите уравнения реакций, которые относятся к
окислительно—восстановительным:
1) СuСl
2
+ 2LiОН = 2LiСl + Сu(ОН)
2
2)NН
3
+ CuO = N
2
+ Cu + Н
2
О
3) NаОН + НСl = NаСl + Н
2
О
4) NH
4
Сl + КОН = NН
3
+ Н
2
O + КСl
5) N
2
+ Н
2
= NН
3
В задании В4 на установление соответствия запишите в таблицу
цифры выбранных вами ответов. Получившуюся
последовательность цифр запишите в строку ответа.
В4. Установите соответствие между исходными веществами и
продуктами реакции
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) NaOH +НСl
→ 1) → NaOH
Б) Na + Cl
2
→ 2) → NaOH +Н
2
В) Na
2
O + H
2
O →
3) → NaCl +Н
2
O
4) → NaCl
5) → NaCl + H
2
ЧАСТЬ 3
С1. Напишите уравнения реакций, с помощью которых можно
осуществить следующие превращения:
Si → SiO
2
→ Na
2
SiO
3
→ H
2
SiO
3
С2. Через 40 г раствора с массовой долей гидроксида натрия 8% пропу—
стили оксид серы (IV). При этом образовался сульфит натрия. Вычисли—
те объём (н. у.) вступившего в реакцию газа.
.
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
ЧАСТЬ 3
С1
1. 4Р+ 5О
2
=2Р
2
О
5
2. Р
2
О
5
+ 3Н
2
О= 2Н
3
РО
4
3. 2Н
3
РО
4
+ 2Са(ОН)
2
= Са
3
(РО
4
)
2
+ Н
2
О
С2 _______________________________________________
Ва(ОН)
2
+ Н
2
SО
4
= ВаSО
4
+ 2Н
2
О
m (Ba(OH)2 вещества)= 100*50/100= 50г
n (Ba(OH)2= 50/171=0,29 моль
n (Ba(OH)2) = n (ВаSО
4
)= 0,29 моль
m (ВаSО
4
)= 0,29 моль* 233 г/моль= 68,13 г
__________________________________________________
ЧАСТЬ 3
С1
1. 2Сu + O2 = 2CuO
2. CuO + 2HCl = CuCl2 + H2O
3. CuCl2 + 2NaOH = Cu(OH)2 + 2NaCl
С2 _______________________________________________
2NaOH + CuSO
4
= Cu(OH)
2
+ Na
2
SO
4
m (NaOH вещества)= 50*20/100= 10г
n (NaOH)= 10/40= 0,25 моль
n (Cu(OH)
2
)= 1/2n (NaOH)=0,125 моль
m (Cu(OH)
2
)=0,125*98= 34,125 г
__________________________________________________
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
Бланк ответов для промежуточной аттестации по химии
Фамилия учащегося
ЧАСТЬ 3
С1 ________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
С2 _______________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
ЧАСТЬ 3
С1 ________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
С2 _______________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
ЧАСТЬ 3
С1 ________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
С2 _______________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
ЧАСТЬ 3
С1 ________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
С2 _______________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
__________________________________________________
Анализ выполнения работы
Работу выполняло _________ учащихся, ________ класса
Замечания и анализ:
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
________________________________________________________________________________________________________________
|
Билет №1
|
|
Билет №2
|
|
Билет № 3
|
|
Билет №4
|
|
Билет №5
|
|
Билет №6
|
|
Билет №7
|
|
Билет №8
|
|
Билет №9
|
|
Билет №10
активный металл + кислота = соль + водород. Напишите уравнения реакций. |
|
Билет №11
|
|
Билет №12
|
|
Билет №13
|
|
Билет №14
|
|
Билет №15
|
|
Билет №16
S +O2→ ? C4H10 + O2→ ?+? H2CO3→ H2O +? MgCO3→ ?+? |
|
Билет №17
|
|
Билет №18
|
|
Билет №19
|
|
Билет №20
CaCO3 = CaO + CO2 – 180 кДж 2С4Н10 + 13О2 = 8СО2 + 10Н2О – 575кДж рассчитайте объем С4Н10, который нужно сжечь, чтобы выделившегося тепла было достаточно для получения 280 кг СаО |
|
Билет № 21
CaO→CaCl2→Ca(OH)2→Ca(NO3)2 |
|
Билет №22
|
|
Билет №23
|
|
Билет №24
|
|
Билет №25
2FeO+C=2Fe+CO2 CaO+H2=Ca+H2O SO2 + 2Mg=2MgO+S Fe+CuSO4=FeSO4 + Cu |
Пояснительная записка
Экзаменационные билеты по химии устной итоговой аттестации учащихся 8 класса составлены на основе государственного стандарта химического образования.
Основная цель: проверить выполнение государственного стандарта уровня подготовки учащихся.
Главные задачи: выявить подготовку химически и экологически грамотной личности, понимающей, что жизнь – это наивысшая ценность, овладевшей химическим и экологическим мышлением, освоившей основы химической культуры, овладевшей необходимыми методами изучения окружающих веществ, умеющей их применять на практике: ведения здорового образа жизни, охраны окружающей среды.
Требования к уровню подготовленности:
Знать / понимать
• химическую символику: знаки химических элементов, формулы химических веществ и уравнения химических реакций;
• важнейшие химические понятия: химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, химическая связь, вещество, классификация веществ, моль, молярная масса, молярный объем, химическая реакция, классификация реакций, электролит и неэлектролит, электролитическая диссоциация, окислитель и восстановитель, окисление и восстановление;
• основные законы химии: сохранения массы веществ, постоянства состава, периодический закон.
Уметь
называть: химические элементы, соединения изученных классов;
• объяснять: физический смысл атомного (порядкового) номера химического элемента, номеров группы и периода, к которым элемент принадлежит в периодической системе Д.И. Менделеева; закономерности изменения свойств элементов в пределах малых периодов
и главных подгрупп; сущность реакций ионного обмена;
• характеризовать: химические элементы (от водорода до кальция) на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов;
связь между составом, строением и свойствами веществ; химические свойства основных классов неорганических веществ;
• определять: состав веществ по их формулам, принадлежность веществ к определенному классу соединений, типы химических реакций, валентность и степень окисления элемента в соединениях, тип химической связи в соединениях, возможность протекания реакций ионного обмена;
• составлять: формулы неорганических соединений изученных классов; схемы строения атомов первых 20 элементов периодической системы Д.И.Менделеева; уравнения химических реакций;
• обращаться с химической посудой и лабораторным оборудованием;
• распознавать опытным путем: кислород, водород, углекислый газ, аммиак; растворы кислот и щелочей, хлорид -, сульфат -, карбонат — ионы;
• вычислять: массовую долю химического элемента по формуле соединения; массовую долю вещества в растворе; количество вещества, объем или массу по количеству вещества, объему или массе реагентов или продуктов реакции.
Использовать приобретенные знания и умения в практической деятельности и повседневной жизни для:
безопасного обращения с веществами и материалами;
экологически грамотного поведения в окружающей среде;
оценки влияния химического загрязнения окружающей среды на организм человека;
критической оценки информации о веществах, используемых в быту;
приготовления растворов заданной концентрации.
Суббота, 11.03.2023, 20:33
Приветствую Вас
Гость | RSS
Сайт учителя химии Егоровой Н. С.
|
Регистрация
|
Вход
Результаты педагогической деятельности
Ответы к билетам по химии 8 класса
Добавлять комментарии могут только зарегистрированные пользователи. [ Регистрация | Вход ] |
Меню сайта
Форма входа Категории раздела
Поиск Наш опрос Что вам нравится в нашей школе? Одноклассники Учителя Оборудование в кабинетах Мероприятия Классная жизнь Уроки Питание Другое Результаты | Архив опросов Всего ответов: 17 Друзья сайта Статистика Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
Copyright MyCorp © 2023
Бесплатный конструктор сайтов — uCoz
Тесты к переводному экзамену по химии в 8 классе
Вариант 1
К каждому из заданий А1-А30 даны 4 варианта ответа, из которых только один правильный
Часть. А
А 1 Заряд ядра атома алюминия равен
1) +2;
2) +13;
3) +12;
4) +20; А 2 В ряду Ca(OH)2 → AI(OH)3→ H2SO4свойства гидроксидов изменяются от
1) амфотерных к основным;
2) кислотных к основным;
3) кислотных к амфотерных;
4) основных к кислотным;
А 3. Химическая связь в оксиде фосфора (Y)
1) ионная;
2) металлическая;
3) ковалентная неполярная;
4) ковалентная полярная
А 4 Валентность азота в соединениях NO2 и N2O5 соответственно равно
1) I и II
2) II и I
3) YIи II
4) IY и Y
А 5. К амфотерным оксидам относится вещество, формула которого
1) Mg(OH)2
2) MgSO4
3) HNO3
4) Fe2O3
А 6. В уравнении реакции между магнием и серной кислотой коэффициент перед формулой
серной кислоты равен
1) 1 3) 2
2) 3 4) 4
А 7. Какое из указанных уравнений соответствует реакции обмена
1) Mg O+HCI=MgCI2+H2O
2) S+O2=SO2
3) 2AgNO3+Mg=2Ag+Mg (NO3)2
4) 2 Fe (OH) 3=Fe2O3+3H2O
А 8. Алюминий реагирует с
1) оксидом магния
2) гидроксидом калия
3) цинком
4) хлоридом калия
А 9. Из приведённого перечня веществ: H2SO4, NaOH, CO2, H2О — с гидроксидом алюминия
реагирует
1) два
2) одно
3) три
4) четыре
А 10. Раствор серной кислоты реагирует с
1) оксидом углерода (IY)
2) оксидом кальция
3) серой
4) хлоридом калия
А 11. Раствор гидроксида натрия реагирует с
1) оксидом серы(IY)
2) водой
3) оксидом кальция
4) медью
А 12. Верны ли следующие суждения о правилах работы в химической лаборатории
А Простое вещество нельзя получить в результате реакции соединения.
Б При физических явлениях изменяется агрегатное состояние и форма
1) верно только. А
2) верно только. Б
3) верны оба суждения
4) оба суждения не верны
А 13. В соединении Na2SO3 окисления серы
1) +4;
2) +6;
3) +2;
4) +1;
А 14. Наименьший радиус у атома
1) AI;
2) В;
3) Ga;
4) Sr;
А 15. Вещество H3PO4-это
1) соль;
2) кислота;
3) основание;
4) оксид;
А 16. Формула хлорида меди (I)-это
1) CuCI;
2) CuСI2;
3) СuCIO;
4) СuCIO3;
А 17. 2 моль кислорода (O2) занимают объём … л (н.у)
1) 67,2
2) 22,4
3) 44,8
4) 64
А 18. Распределение электронов по слоям 2, 8, 8.1 имеет атом
1) Mg
2) S
3) Ca
4) К
А 19. 24,5г фосфорной кислоты составляют … моль
1) 1
2) 0,25
3) 0,5
4) 5
А 20. Запись 2 H2 означает
1) молекулу водорода
2) две молекулы водорода
3) два атома водорода
4) молекулу воды
А 21. Ковалентная неполярная связь осуществляется в веществе
1) H2SO4
2) Р
3) SО2
4) NaBr
А 22. В веществе состава ЭO элемент Э – это
1) K
2) AI
3) H
4) Ca
А 23. Кислотные оксиды – это
1) P2O5 и СO2
2) Li2O и H2O
3) CaO и NO2
47) SO3 и CuO
А 24. В уравнении реакции между оксидом железа (III) и серной кислотой отношение
коэффициентов перед формулами реагирующих веществ соответственно равно
1) 1: 3
2) 1: 2
3) 2: 3
4) 1:1
А 25. Число электронов во внешнем электронном слое атома фосфора
1) 12
2) 4
3) 5
4) 1
А 26. В формуле сульфата алюминия индексы при символе алюминия и кислотном остатке равны соответственно
1) 1 и 2
2) 2 и 3
3) 1 и 3
4) 3 и 1
А 27.Магний реагирует с
1) серной кислотой
2) медью
3) сульфатом натрия
4) оксидом углерода(IY)
А 28Ядро состоит из
1) протонов, нейтронов и электронов
2) протонов и электронов
3) нейтронов и электронов
4) протонов и нейтронов
А 29. Массовая кислорода в воде равна
1) 10,5%
2) 88,88
3) 33,2%
4) 44,1%
А 30 Соли калия, имеющие формулы K3PO4, KNO3 , KCI, называются
1) нитрит, хлорид, фосфид
2) нитрат, хлорат, фосфат
3) нитрид, хлорат, фосфид
4) фосфат, нитрат, хлорид,
Часть. Б
При выполнении заданий В1 и В4 из предложенного перечня ответов выберите два правильных и обведите их номера. Цифры выбранных ответов запишите в указанном месте без дополнительных символов
В 1. В ряду химических элементов N—P—As
1) уменьшаются радиусы атомов
2) увеличиваются радиусы атомов
3) увеличиваются число электронов на внешнем электронном слое
4) увеличиваются число электронных слоёв
5) увеличивается электроотрицательность
Ответ:__________________
B 2. Химические реакции возможны между
1) K2O и H2SO4
2) CaO и NaOH
3) CuO и MgO
4) SO2 и H2O
5) Cu и H2S
Ответ: ___________________
В 3.В реакцию с раствором соляной кислоты вступают
-
медь
-
алюминий
-
оксид калия
-
оксид углероды (IY)
-
сульфат натрия
Ответ: ___________________
В 4. С раствором гидроксида натрия реагируют
1) азотная кислота
2) оксид фосфора (Y)
3) гидроксид магния
4) углерод
5) оксид меди ( II)
Ответ:_____________________
Часть. С
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Na→Na2O→X→Na3PO4
C 2. Какая масса нитрата магния образуется при взаимодействии оксида магния и 196 г азотной кислоты.
Тесты к переводному экзамену по химии в 8 классе.
Вариант 2
К каждому из заданий А1-А30 даны 4 варианта ответа, из которых только один правильный
Часть. А
А 1 Заряд ядра атома калия равен
1) +19;
2) +13;
3) +12;
4) +20; А 2 В ряду AI(OH) →3 Ca(OH)2 → H2SO4свойства гидроксидов изменяются от
1) амфотерных к кислотным;
2) кислотных к основным;
3) кислотных к амфотерных;
4) основных к;
А 3. Химическая связь в оксиде магния
1) ионная;
2) металлическая;
3) ковалентная неполярная;
4) ковалентная полярная
А 4 Валентность углерода в соединениях СO2 и Na2CО3соответственно равно
1) I и II
2) II и I
3) IYи IY
4) IY и II
А 5. К солям относится вещество, формула которого
1) SO3
2) MgSO4
3) HNO3
4) Fe2O3
А 6. В уравнении реакции между гидроксидом магния и фосфорной кислотой коэффициент перед формулой фосфорной кислоты равен
1) 1 3) 2
2) 3 4) 4
А 7. Какое из указанных уравнений соответствует реакции разложения
1) MgO +2HCI=MgCI2+H2O
2) S+O2=SO2
3) 2AgNO3+Mg=2Ag+Mg (NO3)2
4) 2 Fe (OH) 3=Fe2O3+3H2O
А 8. Медь реагирует с
1) оксидом магния
2) соляной кислотой
3) цинком
4) хлоридом ртути
А 9. Из приведённого перечня веществ: H2SO4, NaOH, CO2, K2O, H2O— с оксидом серы(YI)
реагирует
1) два
2) одно
3) три
4) четыре
А 10. Раствор серной кислоты реагирует с
1) оксидом углерода (IY)
2) оксидом кальция
3) серой
4) хлоридом натрия
А 11. Раствор гидроксида кальция реагирует с
1) гидроксидом магния
2) водой
3) оксидом серы(YI)
4) медью
А 12. Верны ли следующие суждения о правилах работы в химической лаборатории
А Простое вещество нельзя получить в результате реакции соединения.
Б При физических явлениях изменяется агрегатное состояние и форма
1) верно только. А
2) верно только. Б
3) верны оба суждения
4) оба суждения не верны
А 13. В соединении К3PO4 окисления фосфора
1) +4;
2) +6;
3) +5;
4) +1;
А 14. Наименьший радиус у атома
1) AI;
2) Mg;
3) P;
4) Si;
А 15. Вещество Mg3(PO4)2-это
1) соль;
2) кислота;
3) основание;
4) оксид;
А 16. Формула хлорида меди (II)-это
1) CuCI;
2) CuСI2;
3) СuCIO;
4) СuCIO3;
А 17. 2 моль кислорода (N2) занимают объём … л (н.у)
1) 67,2
2) 22,4
3) 44,8
4) 64
А 18. Распределение электронов по слоям 2, 8, 2 имеет атом
1) Mg
2) S
3) Ca
4) К
А 19. 24,5г фосфорной кислоты составляют … моль
1) 1
2) 0,25
3) 0,5
4) 5
А 20. Запись 2 H2 означает
1) молекулу водорода
2) две молекулы водорода
3) два атома водорода
4) молекулу воды
А 21. Ковалентная полярная связь осуществляется в веществе
1) H2SO4
2) Р
3) SО2
4) NaBr
А 22. В веществе состава ЭO3 элемент Э – это
1) K
2) AI
3) S
4) Ca
А 23. Кислотные оксиды – это
1) P2O5 и СaO
2) Li2O и H2O
3) CaO и NO2
4) SO3 и P2O5
А 24. В уравнении реакции между оксидом железа (II) и азотной кислотой отношение
коэффициентов перед формулами реагирующих веществ соответственно равно
1) 1: 3
2) 1: 2
3) 2: 3
4) 1:1
А 25. Число электронов во внешнем электронном слое атома кремния
1) 12
2) 4
3) 5
4) 1
А 26. В формуле фосфата калия индексы при символе калия и кислотном остатке равны соответственно
1) 1 и 2
2) 2 и 3
3) 1 и 3
4) 3 и 1
А 27.Ртуть реагирует с
1) серной кислотой
2) медью
3) хлоридом серебра
4) оксидом углерода(IY)
А 28. Массовая кислорода в воде равна
1) 88,88
2) 10,5%
3) 33,2%
4) 44,1%
А 29. Соли калия, имеющие формулы K2SO4, KNO3,3PO4 называются
1) нитрит, хлорид, фосфид
2) сульфат, нитрат, фосфат
3) нитрид, хлорат, фосфид
4) фосфат, нитрат, хлорид,
А 30. Число электронных слоёв в атоме равно
1) номеру группы
2) порядковому номеру
3) номеру периода
4) 8- номер группы
Часть. Б
При выполнении заданий В1 и В4 из предложенного перечня ответов выберите два правильных и обведите их номера. Цифры выбранных ответов запишите в указанном месте без дополнительных символов
В 1. В ряду химических элементов N—P—As
1) уменьшаются радиусы атомов
2) увеличиваются радиусы атомов
3) увеличиваются число электронов на внешнем электронном слое
4) увеличиваются число электронных слоёв
5) увеличивается электроотрицательность
Ответ:__________________
B 2. Химические реакции возможны между
1) K2O и MgO
2) CaO и H2SO4
3) Cu(OH)2 и MgO
4) SO2 и K2O
5) Cu и H2S
Ответ: ___________________
В 3.В реакцию с раствором соляной кислоты вступают
-
медь
-
алюминий
-
оксид углероды (IY)
-
оксид магния
-
сульфат натрия
Ответ: ___________________
В 4. С раствором гидроксида натрия реагируют
1) азотная кислота
2) оксид азота (Y)
3) гидроксид магния
4) углерод
5) оксид меди ( II)
Ответ: _____________________
Часть. С
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Mg→ Х→ Mg(OH)→MgO
C 2. Какая масса сульфата алюминия образуется при взаимодействии гидроксида алюминия и
24,5 г серной кислоты.
Тесты к переводному экзамену по химии в 8 классе.
Вариант 3
К каждому из заданий А1-А30 даны 4 варианта ответа, из которых только один правильный
Часть. А
А 1 Заряд ядра атома хлора равен
1) +19;
2) +13;
3) +17;
4) +20; А 2 В ряду NaOH → Zn(OH)2 → H2SO3свойства гидроксидов изменяются от
1) амфотерных к кислотным;
2) кислотных к основным;
3) кислотных к амфотерных;
4) основных к кислотным;
А 3. Химическая связь в азотной кислоте
1) ионная;
2) металлическая;
3) ковалентная неполярная;
4) ковалентная полярная
А 4 Валентность углерода в соединениях SO2 и SO3 соответственно равно
1) I и II
2) II и I
3) YIи II
4) IY и YI
А 5. К кислотным оксидам относится вещество, формула которого
1) SO3
2) MgSO4
3) HNO3
4) Fe2O3
А 6. В уравнении реакции между оксидом магния и серной кислотой коэффициент перед
формулой серной кислоты равен
1) 1 3) 2
2) 3 4) 4
А 7. Какое из указанных уравнений соответствует реакции замещения
1) MgO +2HCI=MgCI2+H2O
2) S+O2=SO2
3) 2AgNO3+Mg=2Ag+Mg (NO3)2
4) 2 Fe (OH) 3=Fe2O3+3H2O
А 8. Медь реагирует с
1) оксидом магния
2) гидроксидом калия
3) цинком
4) хлоридом серебра
А 9. Из приведённого перечня веществ: H2SO4, NaOH, CO2, CuО — с гидроксидом натрия
реагирует
1) два
2) одно
3) три
4) четыре
А 10. Раствор серной кислоты реагирует с
1) оксидом углерода (IY)
2) гидроксидом кальция
3) серой
4) хлоридом натрия
А 11. Раствор гидроксида кальция реагирует с
1) азотной кислотой
2) водой
3) оксидом кальция
4) медью
А 12. Верны ли следующие суждения о правилах работы в химической лаборатории
А Простое вещество нельзя получить в результате реакции соединения.
Б При физических явлениях изменяется агрегатное состояние и форма
1) верно только. А
2) верно только. Б
3) верны оба суждения
4) оба суждения не верны
А 13. В соединении Na3PO4 окисления фосфора
1) +4;
2) +6;
3) +5;
4) +1;
А 14. Наибольший радиус у атома
1) AI;
2) Mg;
3) P;
4) Si;
А 15. Вещество Mg(OH)2-это
1) соль;
2) кислота;
3) основание;
4) оксид;
А 16. Формула хлорида меди (II)-это
1) CuCI;
2) CuСI2;
3) СuCIO;
4) СuCIO3;
А 17. 2 моль азота (N2) занимают объём … л (н.у)
1) 67,2
2) 22,4
3) 44,8
4) 64
А 18. Распределение электронов по слоям 2, 8, имеет атом
1) Ne
2) S
3) Ca
4) К
А 19. 196 г фосфорной кислоты составляют … моль
1) 1
2) 0,25
3) 0,5
4) 2
А 20. Запись H2 означает
1) молекулу водорода
2) две молекулы водорода
3) два атома водорода
4) молекулу воды
А 21. Ковалентная неполярная связь осуществляется в веществе
1) H2SO4
2) O2
3) SО2
4) NaBr
А 22. В веществе состава ЭO2 элемент Э – это
1) K
2) AI
3) S
4) C
А 23. Кислотные оксиды – это
1) P2O5 и СaO
2) Li2O и H2O
3) CaO и NO2
4) SO3 и P2O5
А 24. В уравнении реакции между оксидом железа (II) и соляной кислотой отношение
коэффициентов перед формулами реагирующих веществ соответственно равно
1) 1: 3
2) 1: 2
3) 2: 3
4) 1:1
А 25. Число электронов во внешнем электронном слое атома натрия
1) 12
2) 4
3) 5
4) 1
А 26. В формуле фосфата магния индексы при символе магния и кислотном остатке равны соответственно
1) 1 и 2
2) 2 и 3
3) 1 и 3
4) 3 и 2
А 27.Ртуть реагирует с
1) серной кислотой
2) медью
3) хлоридом серебра
4) оксидом углерода(IY)
А 28 Ядро состоит из
1) протонов, нейтронов и электронов
2) протонов и электронов
3) нейтронов и электронов
4) протонов и нейтронов
А 29. Массовая кислорода в воде равна
1) 10,5%
2) 88,88
3) 33,2%
4) 44,1%
А 30. Соли калия, имеющие формулы KCI, KNO3, К3PO4 называются
1) нитрит, хлорид, фосфид
2) хлорид, нитрат, фосфат
3) нитрид, хлорат, фосфид
4) фосфат, нитрат, хлорид,
Часть. Б
При выполнении заданий В1 и В4 из предложенного перечня ответов выберите два правильных и обведите их номера. Цифры выбранных ответов запишите в указанном месте без дополнительных символов
В 1. В ряду химических элементов N—P—As
1) уменьшаются радиусы атомов
2) увеличиваются радиусы атомов
3) увеличиваются число электронов на внешнем электронном слое
4) увеличиваются число электронных слоёв
5) увеличивается электроотрицательность
Ответ:__________________
B 2. Химические реакции возможны между
1) K2O и MgO
2) CaO и H2SO4
3) Cu(OH)2 и MgO
4) SO2 и Mg
5) Cu и H2S
Ответ: ___________________
В 3.В реакцию с раствором соляной кислоты вступают
-
медь
-
алюминий
-
оксид углероды (IY)
-
оксид магния
-
сульфат натрия
Ответ: ___________________
В 4. С раствором гидроксида натрия реагируют
1) азотная кислота
2) оксид азота (Y)
3) гидроксид магния
4) углерод
5) оксид меди ( II)
Ответ: _____________________
Часть. С
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
P→P2O5 →X→Na3PO4
C 2. Какая масса нитрата алюминия образуется при взаимодействии гидроксида алюминия и
32,5 г азотной кислоты.
