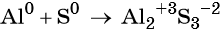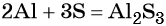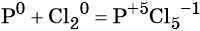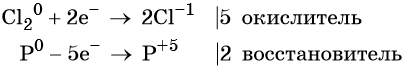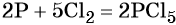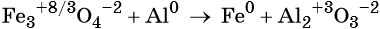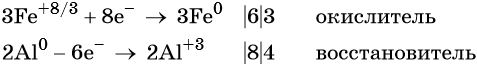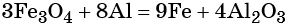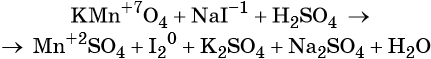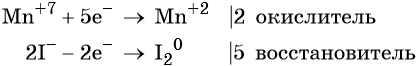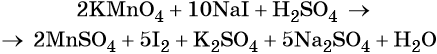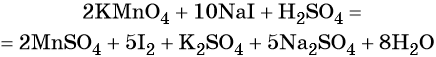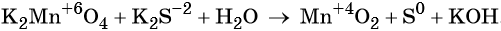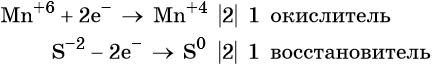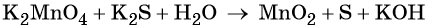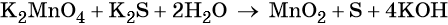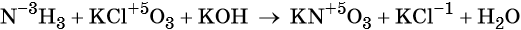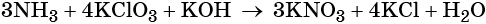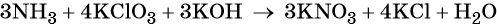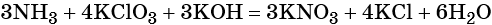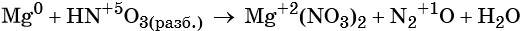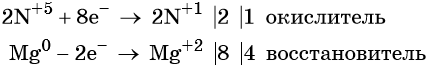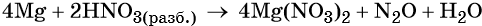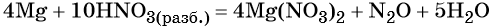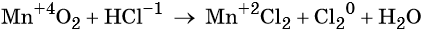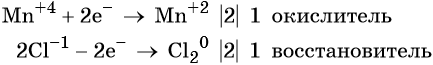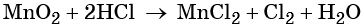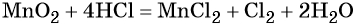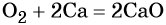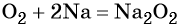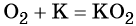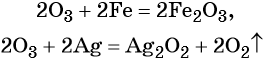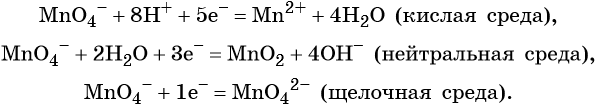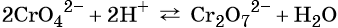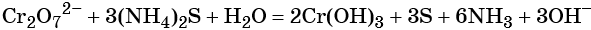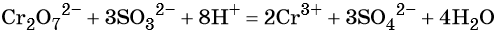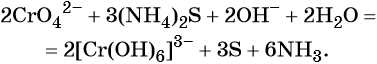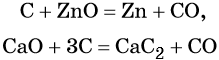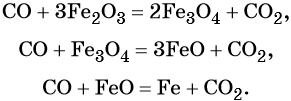100 ОВР, котрые помогут учащимся при сдаче ЕГЭ по химии.
1) 2KMnO4 + 3MnSO4 + 2H2O = 5MnO2 + K2SO4 + 2H2SO4
2) 2KMnO4 + 16HCl = 2MnCl2 + 5Cl2 + 8H2O + 2KCl
3) 5NaNO2 + 2KMnO4 + 3H2SO4 = 2MnSO4 + 5NaNO3 + K2SO4 + 3H2O
4) 10FeSO4 + 2KMnO4 + 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
5) 2KMnO4 + 5H2S + 3H2SO4 = 5S + 2MnSO4 + K2SO4 + 8H2O
6) 2KMnO4 + 5Na2SO3 + 3H2SO4 = MnSO4 + K2SO4 + 5Na2SO4 + 3H2O
7)SO2 + 2KMnO4 + 4KOH = K2SO4 + 2K2MnO4 + 2H2O

9) K2Cr2O7 + 3NaNO2 + 4H2SO4 = 3NaNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
10) K2Cr2O7 + 6KI + 7H2SO4 = 3I2 + Cr2(SO4)3 + 4K2SO4 + 7H2O
11) 4Mg + 10HNO3(оч.разб.) = 4Mg(NO3)2 + NH4NO3 + 3H2O
12) Cr2(SO4)3 + 3Br2 + 16NaOH = 6NaBr + 2Na2CrO4 + 3Na2SO4 + 8H2O
13)Al2S3 + 30HNO3(конц.) = 2Al(NO3)3 + 3H2SO4 + 24NO2 + 12H2O
14) 6FeSO4 + 2HNO3 + 3H2SO4 = 3Fe2(SO4)3 + 2NO + 4H2O
15) FeCl2 + 4HNO3(конц.) = Fe(NO3)3 + 2HCl + NO2 + H2O
16) AlP + 11HNO3(конц.) = H3PO4 + 8NO2 + Al(NO3)3 + 4H2O
17) 6FeSO4 + KClO3 + 3H2SO4 = 3Fe2(SO4)3 + KCl + 3H2O
18) 3MnSO4 + 2KClO3 + 12KOH = 3K2MnO4 + 2KCl + 3K2SO4 + 6H2O
19) 2Al + K2Cr2O7 + 7H2SO4 = Al2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
20) 3P2O3 + 2HClO3 + 9H2O = 6H3PO4 + 2HCl
21) Cr2(SO4)3 + 6KMnO4 + 16KOH = 2K2CrO4 + 6K2MnO4 + 3K2SO4 + 8H2O
22) Cr2O3 + 3KNO3 + 4KOH = 2K2CrO4 + 3KNO2 + 2H2O
23) 2NaNO2 + 2NaI + 2H2SO4 = 2NO + I2 + 2Na2SO4 + 2H2O
24) 8KI + 9H2SO4(конц.) = 4I2 + H2S + 8KHSO4 + 4H2O
25) Cu + 2FeCl3 = CuCl2 + 2FeCl2
26) 3PH3 + 4HClO3 = 3H3PO4 + 4HCl
27) 3NO2 + H2O = NO + 2HNO3
28) I2 + K2SO3 + 2KOH = 2KI + K2SO4 + H2O
29) 2NH3 + 3KClO = N2 + 3KCl + 3H2O
30) 6P + 5HClO3 + 9H2O = 5HCl + 6H3PO4
31) 3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO
32) Ca(ClO)2 + 4HCl = CaCl2 + 2Cl2 + 2H2O
33) 3H2S + HClO3 = 3S + HCl + 3H2O
34) Fe2(SO4)3 + 2KI = 2FeSO4 + I2 + K2SO4
35) 2KMnO4 + KI + H2O = 2MnO2 + KIO3 + 2KOH
36) I2 + 10HNO3(конц.) = 2HIO3 + 10NO2 + 4H2O
37) 3As2S3 + 28HNO3 + 4H2O = 6H3AsO4 + 28NO + 9H2SO4
38) 4Mg + 5H2SO4(конц.) = 4MgSO4 + H2S + 4H2O
39) MnO2 + 2KBr + 2H2SO4 = MnSO4 + Br2 + K2SO4 + 2H2O
40) 5HCOH + 4KMnO4 + 6H2SO4 = 5CO2 + 2K2SO4 + 4MnSO4 + 11H2O
41) 3KNO2 + 2KMnO4 + H2O = 3KNO3 + 2MnO2 + 2KOH
42) NaClO + 2KI + H2SO4 = I2 + NaCl + K2SO4 + H2O
43) 2KNO3 + 6KI + 4H2SO4 = 2NO + 3I2 + 4K2SO4 + 4H2O
44) 14HCl + K2Cr2O7 = 3Cl2 + 2CrCl3 + 2KCl + 7H2O
45) 2Cr(OH)3 + 3Cl2 + 10KOH = 2K2CrO4 + 6KCl + 8H2O
46) K2MnO4 + 8HCl = MnCl2 + 2Cl2 + 2KCl + 4H2O
47) K2Cr2O7 + 3Na2SO3 + 4H2O = 2Cr(OH)3 + 3Na2SO4 + 2KOH
48) 2KMnO4 + 10KBr + 8H2SO4 = 2MnSO4 + 5Br2 + 6K2SO4 + 8H2O
49) 4Zn + KNO3 + 7KOH = NH3 + 4K2ZnO2 + 2H2O
50) 2Fe(OH)3 + 3Br2 + 10KOH = 2K2FeO4 + 6KBr + 8H2O
51) P2O3 + 6KOH + 2NO2 = 2NO + 2K3PO4 + 3H2O
52) 2KMnO4 + 2NH3 = 2MnO2 + N2 + 2KOH + 2H2O
53) 3Na2SO3 + 2KMnO4 + H2O = 3Na2SO4 + 2MnO2 + 2KOH
54) 3NaNO2 + Na2Cr2O7 + 8HNO3 = 5NaNO3 + 2Cr(NO3)3 + 4H2O
55) B + HNO3(конц.) + 4HF = NO + HBF4 + 2H2O
56) 2CuCl2 + SO2 + 2H2O = 2CuCl + 2HCl + H2SO4
57) PH3 + 8AgNO3 + 4H2O = 8Ag + H3PO4 + 8HNO3
58) 2NH3 + 6KMnO4 + 6KOH = N2 + 6K2MnO4 + 6H2O
59) 5Zn + 2KMnO4 + 8H2SO4 = 5ZnSO4 + 2MnSO4 + K2SO4 + 8H2O
60) 3KNO2 + K2Cr2O7 + 8HNO3 = 5KNO3 + 2Cr(NO3)3 + 4H2O
61) FeS + 12HNO3(конц.) = Fe(NO3)3 + H2SO4 + 9NO2 + 5H2O
62) KIO3 + 5KI + 3H2SO4 = 3I2 + 3K2SO4 + 3H2O
63) 2NaCrO2 + 3Br2 + 8NaOH = 2Na2CrO4 + 6NaBr + 4H2O
64) Fe2(SO4)3 + Na2SO3 + H2O = 2FeSO4 + Na2SO4 + H2SO4
65) 3P2O3+ 2H2Cr2O7 + H2O = 2H3PO4 + 4CrPO4
66) 3Si + 4HNO3 + 18HF = 3H2SiF6 + 4NO + 8H2O
67) 5Na2SO3(нед.) + 2KIO3 + H2SO4 = I2 + K2SO4 + 5Na2SO4 + H2O
68) 2CrBr3 + 3H2O2 + 10NaOH = 2Na2CrO4 + 6NaBr + 8H2O
69) 8 KMnO4 + 5 PH3 + 12H2SO4 = 5H3PO4 + 8MnSO4 + 4K2SO4 + 12H2O
70) 3SO2 + K2Cr2O7 + H2SO4 = K2SO4 + Cr2(SO4)3 + H2O
71) 3P2O3 + 4HNO3 + 7H2O = 6H3PO4 + 4NO
72) 2NO + 3KClO + 2KOH = 2KNO3 + 3KCl + H2O
73) 5PH3 + 8KMnO4 + 12H2SO4 = 5H3PO4 + 4K2SO4 + 8MnSO4 + 12H2O
74) 5AsH3 + 8KMnO4 + 12H2SO4 = 5H3AsO4 + 4K2SO4 + 8MnSO4 + 12H2O
75) 2CuI + 4H2SO4(конц.) = 2CuSO4 + I2 + 4H2O + 2SO2
76) Si + 2KOH + H2O = K2SiO3 + 2H2 (to)
77) B + 3HNO3 = H3BO3 + 3NO2
78) 8NH3 + 3Br2 = N2 + 6NH4Br
79) P4 + 3KOH + 3H2O = PH3 + 3KH2PO2
80) Al2O3 + 3C + 3Cl2 = 2AlCl3 + 3CO(to)
81) H2S + HClO = S + HCl + H2O
82) 5KNO3(расплав) + 2P = 5KNO2 + P2O5
83) I2 + 5Cl2 + 6H2O = 2HIO3 + 10HCl
84) H2S + 4Cl2 + 4H2O = H2SO4 + 8HCl
85) 8Zn + 5H2S2O7 = 8ZnSO4 + 2H2S + 3H2O
86) 2FeCl3 + 3Na2S = 2FeS + S + 6NaCl
87) Na2S + 8NaNO3 + 9H2SO4 = 10NaHSO4 + 8NO2 + 4H2O
88) Cr2O3 + 3NaNO3 + 2Na2CO3 = 2Na2CrO4 + 3NaNO2 + 2CO2
89) 5C + Ca3(PO4)2 + 3SiO2 = 2P + 5CO + 3CaSiO3 (to)
90) 2NaI + H2O2 + H2SO4 = Na2SO4 + I2 + 2H2O
91) 14HBr + K2Cr2O7 = 2CrBr3 + 3Br2 + 7H2O + 2KBr
92) 2NH3 + 2KMnO4(тв.) = N2 + 2MnO2 + 2KOH + 2H2O (to)
93) 2FeCl3 + SO2 + 2H2O = 2FeCl2 + H2SO4 + 2HCl
94) 2HMnO4 + 5H2S + 2H2SO4 = 5S + 2MnSO4 + 8H2O
95) 3KNO3 + 8Al + 5KOH + 18H2O = 3NH3 + 8K[Al(OH)4]
96) 5H2O2 + 2KMnO4 + 3H2SO4 = 5O2 + 2MnSO4 + K2SO4 + 8H2O
97) P4 + 20HNO3 = 4H3PO4 + 20NO2 + 4H2O
98) 3NaClO + 4NaOH + Cr2O3 = 2Na2CrO4 + 3NaCl + 2H2O
99) Na2SO3 + 2KMnO4 + 2KOH = 2K2MnO4 + Na2SO4 + H2O
100) Cr2(SO4)3 + 3H2O2 + 10NaOH = 2Na2CrO4 + 3Na2SO4 +8H2O
1. Окислители и восстановители
2. Классификация окислительно–восстановительных реакций
3. Основные правила составления ОВР
4. Общие закономерности протекания ОВР
5. Основные схемы ОВР
5.1. Схема восстановления перманганатов
5.2. Схема восстановления хроматов/бихроматов
5.3. Разложение нитратов
5.4. Окислительные свойства азотной кислоты
5.5. Взаимодействие металлов с серной кислотой
5.6. Пероксид водорода
Окислительно-восстановительные реакции — это химические реакции, сопровождающиеся изменением степени окисления у атомов реагирующих веществ. При этом некоторые частицы отдают электроны, а некоторые получают.
Окислители и восстановители
Окислители — это частицы (атомы, молекулы или ионы), которые принимают электроны в ходе химической реакции. При этом степень окисления окислителя понижается. Окислители при этом восстанавливаются.
Восстановители — это частицы (атомы, молекулы или ионы), которые отдают электроны в ходе химической реакции. При этом степень окисления восстановителя повышается. Восстановители при этом окисляются.
Химические вещества можно разделить на типичные окислители, типичные восстановители, и вещества, которые могут проявлять и окислительные, и восстановительные свойства. Некоторые вещества практически не проявляют окислительно-восстановительную активность.
К типичным окислителям относят:
- простые вещества-неметаллы с наиболее сильными окислительными свойствами (фтор F2, кислород O2, хлор Cl2);
- сложные вещества, в составе которых есть ионы металлов или неметаллов с высокими положительными (как правило, высшими) степенями окисления: кислоты (HN+5O3, HCl+7O4), соли (KN+5O3, KMn+7O4), оксиды (S+6O3, Cr+6O3)
- соединения, содержащие некоторые катионы металлов, имеющих высокие степени окисления: Pb4+, Fe3+, Au3+ и др.
Типичные восстановители – это, как правило:
- простые вещества-металлы (восстановительные способности металлов определяются рядом электрохимической активности);
- сложные вещества, в составе которых есть атомы или ионы неметаллов с отрицательной (как правило, низшей) степенью окисления: бинарные водородные соединения (H2S, HBr), соли бескислородных кислот (K2S, NaI);
- некоторые соединения, содержащие катионы с минимальной положительной степенью окисления (Sn2+, Fe2+, Cr2+), которые, отдавая электроны, могут повышать свою степень окисления;
- соединения, содержащие сложные ионы, состоящие из неметаллов с промежуточной положительной степенью окисления (S+4O3)2–, (НР+3O3)2–, в которых элементы могут, отдавая электроны, повышать свою положительную степень окисления.
Большинство остальных веществ может проявлять как окислительные, так и восстановительные свойства.
Типичные окислители и восстановители приведены в таблице.
В лабораторной практике наиболее часто используются следующие окислители:
-
перманганат калия (KMnO4);
-
дихромат калия (K2Cr2O7);
-
азотная кислота (HNO3);
-
концентрированная серная кислота (H2SO4);
-
пероксид водорода (H2O2);
-
оксиды марганца (IV) и свинца (IV) (MnO2, PbO2);
-
расплавленный нитрат калия (KNO3) и расплавы некоторых других нитратов .
К восстановителям, которые применяются в лабораторной практике относятся:
- магний (Mg), алюминий (Al), цинк (Zn) и другие активные металлы;
- водород (Н2) и углерод (С);
- иодид калия (KI);
- сульфид натрия (Na2S) и сероводород (H2S);
- сульфит натрия (Na2SO3);
- хлорид олова (SnCl2).
Классификация окислительно-восстановительных реакций
Окислительно-восстановительные реакции обычно разделяют на четыре типа: межмолекулярные, внутримолекулярные, реакции диспропорционирования (самоокисления-самовосстановления), и реакции контрдиспропорционирования.
Межмолекулярные реакции протекают с изменением степени окисления разных элементов из разных реагентов. При этом образуются разные продукты окисления и восстановления.
2Al0 + Fe+32O3 → Al+32O3 + 2Fe0,
C0 + 4HN+5O3(конц) = C+4O2 ↑ + 4N+4O2 ↑+ 2H2O.
Внутримолекулярные реакции – это такие реакции, в которых разные элементы из одного реагента переходят в разные продукты, например:
(N-3H4)2Cr+62O7 → N20 ↑+ Cr+32O3 + 4 H2O,
2 NaN+5O-23 → 2 NaN+3O2 + O02↑.
Реакции диспропорционирования (самоокисления-самовосстановления) – это такие реакции, в которых окислитель и восстановитель – один и тот же элемент одного реагента, который при этом переходит в разные продукты:
3Br2 + 6 KOH → 5KBr + KBrO3 + 3 H2O,
Репропорционирование (конпропорционирование, контрдиспропорционирование) – это реакции, в которых окислитель и восстановитель – это один и тот же элемент, который из разных реагентов переходит в один продукт. Реакция, обратная диспропорционированию.
2H2S-2 + S+4O2 = 3S + 2H2O
Основные правила составления окислительно-восстановительных реакций
Окислительно-восстановительные реакции сопровождаются процессами окисления и восстановления:
Окисление — это процесс отдачи электронов восстановителем.
Восстановление — это процесс присоединения электронов окислителем.
Окислитель восстанавливается, а восстановитель окисляется.
В окислительно-восстановительных реакциях соблюдается электронный баланс: количество электронов, которые отдает восстановитель, равно количеству электронов, которые получает окислитель. Если баланс составлен неверно, составить сложные ОВР у вас не получится.
Используется несколько методов составления окислительно-восстановительных реакций (ОВР): метод электронного баланса, метод электронно-ионного баланса (метод полуреакций) и другие.
Рассмотрим подробно метод электронного баланса.
«Опознать» ОВР довольно легко — достаточно расставить степени окисления во всех соединениях и определить, что атомы меняют степень окисления:
K+2S-2 + 2K+Mn+7O-24 = 2K+2Mn+6O-24 + S0
Выписываем отдельно атомы элементов, меняющих степень окисления, в состоянии ДО реакции и ПОСЛЕ реакции.
Степень окисления меняют атомы марганца и серы:
S-2 -2e = S0
Mn+7 + 1e = Mn+6
Марганец поглощает 1 электрон, сера отдает 2 электрона. При этом необходимо, чтобы соблюдался электронный баланс. Следовательно, необходимо удвоить число атомов марганца, а число атомов серы оставить без изменения. Балансовые коэффициенты указываем и перед реагентами, и перед продуктами!
Схема составления уравнений ОВР методом электронного баланса:
Внимание! В реакции может быть несколько окислителей или восстановителей. Баланс необходимо составить так, чтобы ОБЩЕЕ число отданных и полученных электронов было одинаковым.
Общие закономерности протекания окислительно-восстановительных реакций
Продукты окислительно-восстановительных реакций зачастую зависят от условий проведения процесса. Рассмотрим основные факторы, влияющие на протекание окислительно-восстановительных реакций.
Самый очевидный фактор, определяющий — среда раствора реакции — кислая, нейтральная или щелочная. Как правило (но не обязательно), вещество, определяющее среду, указано среди реагентов. Возможны такие варианты:
- окислительная активность усиливается в более кислой среде и окислитель восстанавливается глубже (например, перманганат калия, KMnO4, где Mn+7 в кислой среде восстанавливается до Mn+2, а в щелочной — до Mn+6);
- окислительная активность усиливается в более щелочной среде, и окислитель восстанавливается глубже (например, нитрат калия KNO3, где N+5 при взаимодействии с восстановителем в щелочной среде восстанавливается до N-3);
- либо окислитель практически не подвержен изменениям среды.
Среда протекания реакции позволяет определить состав и форму существования остальных продуктов ОВР. Основной принцип — продукты образуются такие, которые не взаимодействуют с реагентами!
Обратите внимание! Если среда раствора кислая, то среди продуктов реакции не могут присутствовать основания и основные оксиды, т.к. они взаимодействуют с кислотой. И, наоборот, в щелочной среде исключено образование кислоты и кислотного оксида. Это одна из наиболее частых, и наиболее грубых ошибок.
Также на направление протекания ОВР влияет природа реагирующих веществ. Например, при взаимодействии азотной кислоты HNO3 с восстановителями наблюдается закономерность — чем больше активность восстановителя, тем больше восстанавливается азот N+5.
При увеличении температуры большинство ОВР, как правило, проходят более интенсивно и более глубоко.
В гетерогенных реакциях на состав продуктов зачастую влияет степень измельчения твердого вещества. Например, порошковый цинк с азотной кислотой образует одни продукты, а гранулированный — совершенно другие. Чем больше степень измельчения реагента, тем больше его активность, как правило.
Рассмотрим наиболее типичные лабораторные окислители.
Основные схемы окислительно-восстановительных реакций
Схема восстановления перманганатов
В составе перманганатов есть мощный окислитель — марганец в степени окисления +7. Соли марганца +7 окрашивают раствор в фиолетовый цвет.
Перманганаты, в зависимости от среды реакционного раствора, восстанавливаются по-разному.
В кислой среде восстановление происходит более глубоко, до Mn2+. Оксид марганца в степени окисления +2 проявляет основные свойства, поэтому в кислой среде образуется соль. Соли марганца +2 бесцветны. В нейтральном растворе марганец восстанавливается до степени окисления +4, с образованием амфотерного оксида MnO2 — коричневого осадка, нерастворимого в кислотах и щелочах. В щелочной среде марганец восстанавливается минимально — до ближайшей степени окисления +6. Соединения марганца +6 проявляют кислотные свойства, в щелочной среде образуют соли — манганаты. Манганаты придают раствору зеленую окраску.
Рассмотрим взаимодействие перманганата калия KMnO4 с сульфидом калия в кислой, нейтральной и щелочной средах. В этих реакциях продуктом окисления сульфид-иона является S0.
5 K2S + 2 KMnO4 + 8 H2SO4 = 5 S + 2 MnSO4 + 6 K2SO4 + 8 H2O,
3 K2S + 2 KMnO4 + 4 H2O = 2 MnO2↓ + 3 S↓ + 8 KOH,
Распространенной ошибкой в этой реакции является указание на взаимодействие серы и щелочи в продуктах реакции. Однако, сера взаимодействует с щелочью в довольно жестких условиях (повышенная температура), что не соответствует условиям этой реакции. При обычных условиях правильно будет указывать именно молекулярную серу и щелочь отдельно, а не продукты их взаимодействия.
K2S + 2 KMnO4 –(KOH)= 2 K2MnO4 + S↓
При составлении этой реакции также возникают трудности. Дело в том, что в данном случае написание молекулы среды (КОН или другая щелочь) в реагентах не требуется для уравнивания реакции. Щелочь принимает участие в реакции, и определяет продукт восстановления перманганата калия, но реагенты и продукты уравниваются и без ее участия. Этот, казалось бы, парадокс легко разрешим, если вспомнить, что химическая реакция — это всего лишь условная запись, которая не указывает на каждый происходящий процесс, а всего лишь является отображением суммы всех процессов. Как определить это самостоятельно? Если действовать по классической схеме — баланс-балансовые коэффициенты-уравнивание металла, то вы увидите, что металлы уравниваются балансовыми коэффициентами, и наличие щелочи в левой части уравнения реакции будет лишним.
Перманганаты окисляют:
- неметаллы с отрицательной степенью окисления до простых веществ (со степенью окисления 0), исключения — фосфор, мышьяк — до +5;
- неметаллы с промежуточной степенью окисления до высшей степени окисления;
- активные металлы из простых веществ (ст.окисления 0) до соединений со стабильной положительной степенью окисления металла.
KMnO4 + неМе (низшая с.о.) = неМе0 + другие продукты
KMnO4 + неМе (промежуточная с.о.) = неМе(высшая с.о.) + др. продукты
KMnO4 + Ме0 = Ме (стабильная с.о.) + др. продукты
KMnO4 + P-3, As-3= P+5, As+5 + др. продукты
Схема восстановления хроматов/бихроматов
Особенностью хрома с валентностью VI является то, что он образует 2 типа солей в водных растворах: хроматы и бихроматы, в зависимости от среды раствора. Хроматы активных металлов (например, K2CrO4) — это соли, которые устойчивы в щелочной среде. Дихроматы (бихроматы) активных металлов (например, K2Cr2O7) — соли, устойчивые в кислой среде.
Восстанавливаются соединения хрома (VI) до соединений хрома (III). Соединения хрома Cr+3 — амфотерные, и в зависимости от среды раствора они существуют в растворе в различных формах: в кислой среде в виде солей (амфотерные соединения при взаимодействии с кислотами образуют соли), в нейтральной среде — нерастворимый амфотерный гидроксид хрома (III) Cr(OH)3, и в щелочной среде соединения хрома (III) образуют комплексную соль, например, гексагидроксохромат (III) калия K3[Cr(OH)6].
Соединения хрома VI окисляют:
- неметаллы в отрицательной степени окисления до простых веществ (со степенью окисления 0), исключения — фосфор, мышьяк – до +5;
- неметаллы в промежуточной степени окисления до высшей степени окисления;
- активные металлы из простых веществ (ст.окисления 0) до соединений со стабильной положительной степенью окисления металла.
Хромат/бихромат + неМе (отрицательная с.о.) = неМе0 + другие продукты
Хромат/бихромат + неМе (промежуточная положительная с.о.) = неМе(высшая с.о.) + др. продукты
Хромат/бихромат + Ме0 = Ме (стабильная с.о.) + др. продукты
Хромат/бихромат + P, As (отрицательная с.о.) = P, As+5 + другие продукты
Разложение нитратов
Соли-нитраты содержат азот в степени окисления +5 — сильный окислитель. Такой азот может окислять кислород (О-2). Это происходит при нагревании нитратов. При этом в большинстве случаев кислород окисляется до степени окисления 0, т.е. до молекулярного кислорода O2.
В зависимости от типа металла, образующего соль, при термическом (температурном) разложении нитратов образуются различные продукты: если металл активный (в ряду электрохимической активности находятся до магния), то азот восстанавливается до степени окисления +3, и при разложении образуется соли-нитриты и молекулярный кислород.
Например:
2NaNO3 → 2NaNO2 + O2.
Активные металлы в природе встречаются в виде солей (KCl, NaCl).
Если металл в ряду электрохимической активности находится правее магния и левее меди (включая магний и медь), то при разложении образуется оксид металла в устойчивой степени окисления, оксид азота (IV) (бурый газ) и кислород. Оксид металла образует также при разложении нитрат лития.
Например, разложение нитрата цинка:
2Zn(NO3)2 → 2ZnО + 4NO2 + O2.
Металлы средней активности чаще всего в природе встречаются в виде оксидов (Fe2O3, Al2O3 и др.).
Ионы металлов, расположенных в ряду электрохимической активности правее меди являются сильными окислителями. При разложении нитратов они, как и N+5, участвуют в окислении кислорода, и восстанавливаются до простых веществ, т.е. образуется металл и выделяются газы — оксид азота (IV) и кислород.
Например, разложение нитрата серебра:
2AgNO3 → 2Ag + 2NO2 + O2.
Неактивные металлы в природе встречаются в виде простых веществ.
Некоторые исключения!
Разложение нитрата аммония:
В молекуле нитрата аммония есть и окислитель, и восстановитель: азот в степени окисления -3 проявляет только восстановительные свойства, азот в степени окисления +5 — только окислительные.
При нагревании нитрат аммония разлагается. При температуре до 270 оС образуется оксид азота (I) («веселящий газ») и вода:
NH4NO3 → N2O + 2H2O
Это пример реакции контрдиспропорционирования.
Результирующая степень окиcления азота — среднее арифметическое степени окисления атомов азота в исходной молекуле.
При более высокой температуре оксид азота (I) разлагается на простые вещества — азот и кислород:
2NH4NO3 → 2N2 + O2 + 4H2O
При разложении нитрита аммония NH4NO2 также происходит контрдиспропорционирование.
Результирующая степень окисления азота также равна среднему арифметическому степеней окисления исходных атомов азота — окислителя N+3 и восстановителя N-3
NH4NO2 → N2 + 2H2O
Термическое разложение нитрата марганца (II) сопровождается окислением металла:
Mn(NO3)2 = MnO2 + 2NO2
Нитрат железа (II) при низких температурах разлагается до оксида железа (II), при нагревании железо окисляется до степени окисления +3:
2Fe(NO3)2 → 2FeO + 4NO2 + O2 при 60°C
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2 при >60°C
Нитрат никеля (II) разлагается до нитрита при нагревании до 150оС под вакуумом и до оксида никеля при более высоких температурах (разложения нитрата никеля в ЕГЭ по химии не должно быть, но это не точно)).
Окислительные свойства азотной кислоты
Азотная кислота HNO3 при взаимодействии с металлами практически никогда не образует водород, в отличие от большинства минеральных кислот.
Это связано с тем, что в составе кислоты есть очень сильный окислитель — азот в степени окисления +5. При взаимодействии с восстановителями — металлами образуются различные продукты восстановления азота.
Азотная кислота + металл = соль металла + продукт восстановления азота + H2O
Азотная кислота при восстановлении может переходить в оксид азота (IV) NO2 (N+4); оксид азота (II) NO (N+2); оксид азота (I) N2O («веселящий газ»); молекулярный азот N2; нитрат аммония NH4NO3. Как правило, образуется смесь продуктов с преобладанием одного из них. Азот восстанавливается при этом до степеней окисления от +4 до −3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты. При этом работает правило: чем меньше концентрация кислоты и выше активность металла, тем больше электронов получает азот, и тем более восстановленные продукты образуются.
Некоторые закономерности позволят верно определять основной продукт восстановления металлами азотной кислоты в реакции:
- при действии очень разбавленной азотной кислоты на металлы образуется, как правило, нитрат аммония NH4NO3;
Например, взаимодействие цинка с очень разбавленной азотной кислотой:
4Zn + 10HNO3 = 4Zn(NO3)2 + NH4NO3 + 3H2O
- концентрированная азотная кислота на холоде пассивирует некоторые металлы — хром Cr, алюминий Al и железо Fe. При нагревании или разбавлении раствора реакция идет;
пассивация металлов — это перевод поверхности металла в неактивное состояние за счет образования на поверхности металла тонких слоев инертных соединений, в данном случае преимущественно оксидов металлов, которые не реагируют с концентрированной азотной кислотой
- азотная кислота не реагирует с металлами платиновой подгруппы — золотом Au, платиной Pt, и палладием Pd;
- при взаимодействии концентрированной кислоты с неактивными металлами и металлами средней активности азотная кислота восстанавливается до оксида азота (IV) NO2;
Например, окисление меди концентрированной азотной кислотой:
Cu+ 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
- при взаимодействии концентрированной азотной кислоты с активными металлами образуется оксид азота (I) N2O;
Например, окисление натрия концентрированной азотной кислотой:
8Na+ 10HNO3 = 8NaNO3 + N2O + 5H2O
- при взаимодействии разбавленной азотной кислоты с неактивными металлами (в ряду активности правее водорода) кислота восстанавливается до оксида азота (II) NO;
- при взаимодействии разбавленной азотной кислоты с металлами средней активности образуется либо оксид азота (II) NO, либо оксид азота N2O, либо молекулярный азот N2 — в зависимости от дополнительных факторов (активность металла, степень измельчения металла, степень разбавления кислоты, температура).
- при взаимодействии разбавленной азотной кислоты с активными металлами образуется молекулярный азот N2.
Для приближенного определения продуктов восстановления азотной кислоты при взаимодействии с разными металлами я предлагаю воспользоваться принципом маятника. Основные факторы, смещающие положение маятника: концентрация кислоты и активность металла. Для упрощения используем 3 типа концентраций кислоты: концентрированная (больше 30%), разбавленная (30% или меньше), очень разбавленная (меньше 5%). Металлы по активности разделим на активные (до алюминия), средней активности (от алюминия до водорода) и неактивные (после водорода). Продукты восстановления азотной кислоты располагаем в порядке убывания степени окисления:
NO2; NO; N2O; N2; NH4NO3
Чем активнее металл, тем больше мы смещаемся вправо. Чем больше концентрация или меньше степень разбавления кислоты, тем больше мы смещаемся влево.
Например, взаимодействуют концентрированная кислота и неактивный металл медь Cu. Следовательно, смещаемся в крайнее левое положение, образуется оксид азота (IV), нитрат меди и вода.
Взаимодействие металлов с серной кислотой
Разбавленная серная кислота взаимодействует с металлами, как обычная минеральная кислота. Т.е. взаимодействует с металлами, которые расположены в ряду электрохимических напряжений до водорода. Окислителем здесь выступают ионы H+, которые восстанавливаются до молекулярного водорода H2. При этом металлы окисляются, как правило, до минимальной степени окисления.
Например:
Fe + H2SO4(разб) = FeSO4 + H2
Концентрированная серная кислота взаимодействует с металлами, стоящими в ряду напряжений как до, так и после водорода.
H2SO4 (конц) + металл = соль металла + продукт восстановления серы (SO2, S, H2S) + вода
При взаимодействии концентрированной серной кислоты с металлами образуются соль металла (в устойчивой степени окисления), вода и продукт восстановления серы — сернистый газ S+4O2, молекулярная сера S либо сероводород H2S-2, в зависимости от степени концентрации, активности металла, степени его измельчение, температуры и т.д. При взаимодействии концентрированной серной кислоты с металлами молекулярный водород не образуется!
Основные принципы взаимодействия концентрированной серной кислоты с металлами:
1. Концентрированная серная кислота пассивирует алюминий, хром, железо при комнатной температуре, либо на холоду;
2. Концентрированная серная кислота не взаимодействует с золотом, платиной и палладием;
3. С неактивными металлами концентрированная серная кислота восстанавливается до оксида серы (IV).
Например, медь окисляется концентрированной серной кислотой:
Cu0 + 2H2S+6O4(конц) = Cu+2SO4 + S+4O2 + 2H2O
4. При взаимодействии с активными металлами и цинком концентрированная серная кислота образует серу S либо сероводород H2S2- (в зависимости от температуры, степени измельчения и активности металла).
Например, взаимодействие концентрированной серной кислоты с цинком:
8Na0 + 5H2S+6O4(конц) → 4Na2+SO4 + H2S—2 + 4H2O
Пероксид водорода
Пероксид водорода H2O2 содержит кислород в степени окисления -1. Такой кислород может и повышать, и понижать степень окисления. Таким образом, пероксид водорода проявляет и окислительные, и восстановительные свойства.
При взаимодействии с восстановителями пероксид водорода проявляет свойства окислителя, и восстанавливается до степени окисления -2. Как правило, продуктом восстановления пероксида водорода является вода или гидроксид-ион, в зависимости от условий проведения реакции. Например:
S+4O2 + H2O2-1 → H2S+6O4-2
При взаимодействии с окислителями перекись окисляется до молекулярного кислорода (степень окисления 0): O2. Например:
2KMn+7O4 + 5H2O2-1 + 3H2SO4 → 5O20 + 2Mn+2SO4 + K2SO4 + 8H2O
Окислительно-восстановительные реакции
I. ОВР в неорганической химии.
Перекись водорода.
|
4H2O2 + PbS → PbSO4 + 4H2O 5H2O2 + 2KMnO4 + 3H2SO4 → 5O2 + K2SO4 +2MnSO4 + 8H2O 5H2O2 + 2HIO3 → 5 O2 + I2 + 6H2O 3H2O2 + 2AuCl3 → 3 O2 + 6HCl + 2Au H2O2 + H2S → S + 2H2O H2O2 + KI + H2SO4 → I2 + K2SO4 + 2H2O 3H2O2 + 2CrCl3 + 10 KOH → 2K2CrO4 + 8H2O + 6KCl H2O2 + 2NaOH → Na2O2 + 2H2O H2O2 + Ba(OH)2 → BaO2 + 2H2O MnO2 2H2O2 → 2H2O + O2 H2O2 + Cl2 → 2HCl + O2 H2O2 + 2FeSO4 + H2SO4 → Fe2(SO3)3 + 2H2O K3[Cr(OH)6] + 3H2O2 → 2K2CrO4 + 8H2O + 2KOH H2O2 + SO2 → H2SO4 |
Na2O2 + 2CO2 → 2Na2CO3 + O2 Na2O2 + 2H2O → H2O2 + 2NaOH Na2O2 + 2Na → 2Na2O Na2O2 + H2SO4 → H2O2 + Na2SO4 Na2O2 + H2SO4 + 2KI → I2 + Na2SO4 +K2SO4 + 2H2O KO2+ H2SO4→H2O2+K2SO4+O2 надперекись калия 2KO2 + 2H2O → 2KOH +H2O2+ O2 BaO2 + H2SO4 → BaSO4 + H2O2 BaO2 + CO2 + H2O → H2O2 + BaCO3 800oC 2BaO2 → 2BaO + O2 SnO2 + 2H2SO4 →Sn(SO4)2 + 2H2O |
Железо.
|
to сильное 2Fe + 6H2SO4 (к) → Fe2(SO4)3 + 3SO2 + 6H2O to Fe + 6HNO3(к) → Fe(NO3)3 + 3NO2 + 3H2O |
10Fe + 6HNO3(сильно разб.) → Fe(NO3)3 + 3N2 + 18H2O С растворами щелочей в присутствии сильных окислителей to Fe + KClO3 + 2KOH → KCl + H2O + K2FeO4 феррат калия |
Соединения Fe2+.
|
to 2FeO + 4H2SO4 (к) → Fe2(SO4)3 + SO2 + 4H2O to FeO + 4HNO3(к) → Fe(NO3)3 + NO2 + 2H2O to 3FeO + 10HNO3(р) → 3Fe(NO3)3 + NO + 5H2O to Fe(OH)2 + 4HNO3(к) → Fe(NO3)3 + NO2 + 3H2O to 2Fe(OH)2 + 4H2SO4 (к) → Fe2(SO4)3 + SO2 + 6H2O 10FeS + 6KMnO4 + 24H2SO4 → 5Fe2(SO4)3 + 6MnSO4 + + 3K2SO4 + 24H2O 2FeI2 + 6H2SO4 (к) → Fe2(SO4)3 + 2I2 +3SO2 + 6H2O |
to 4FeCl2 + O2 + 2H2O → 4Fe(OH)Cl2 4FeCl2 + O2 + 8NaOH + 2H2O → Fe(OH)3 + 8NaCl to 4FeSO4 → 2Fe2O3 + 4SO2 + O2 2FeSO4 + H2O2 + H2SO4 → Fe2(SO3)3 + 2H2O 10 FeSO4 + 2KIO3 + 6H2SO4 → I2 + 5Fe2(SO4)3 + K2SO4 + + 6H2O 6FeSO4 + KClO3 + 3H2SO4 → 3Fe2(SO4)3 + KCl + 3H2O 10 FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + + K2SO4 + 8H2O to 4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2 |
Соединения Fe3+.
|
to Fe2O3 + 3NaH → 3NaOH + 2Fe В присутствии сильных окислителей со щелочами Fe2O3 + 4KOH + 3KNO3 → 2K2FeO4 + 3 KNO2 +2H2O to Fe2O3 + 4KOH + KClO3 → 2K2FeO4 + KCl + 2H2O Fe2O3 + 6Hl → 2FeI2 + I2 + 3H2O NaFeO2+2H2O→ Fe(OH)3+NaOH 2Fe(OH)3 + 6HI → FeI2 +I2+ 6H2O |
to 2Fe(OH)3 +10NaOH+3Br2 → 2Na2FeO4 + 6NaBr +8H2O 2FeCl3 + 2KI → FeCI2 + I2 + 2KCl 2FeCl3 + H2S → FeCI2 + S + 2HCl 2FeCl3 + FeCl2 + 4(NH4)2S → 3FeS + S + 8NH4Cl to 2FeCl3 +3Br2+16NaOH →2Na2FeO4 + 6NaBr ++6NaCl+8H2Oферрат натрия |
Fe3O4.
|
Fe3O4 + 8HCl → FeCI2 + 2FeCl3 + 4H2O (не ОВР) Fe3O4+8Hl→3FeI2+I2+4H2O Fe3O4+10HNO3(к) →3Fe(NO3)3+ NO2 + 5H2O 3Fe3O4 + 28 HNO3 (р) → 9Fe(NO3)3 + NO+14H2O |
2Fe3O4+10H2SO4(к)→3Fe2(SO4)3 +SO2+10H2O Fe3O4 + 4H2SO4 (р) → Fe2(SO4)3 + FeSO4 + 8H2O to Fe3O4 + Fe → 4FeO |
Соединения марганца.
Оксиды:
MnO Mn2O3 Mn3O4 Mn2O7 MnO3 MnO2
основные кислотные амфотерный
|
Mn(NO3)2 + 5PbO2 + 6HNO3 → 5Pb(NO3)2 + 2HMnO4 +2H2O to Mn(NO3)2 → MnO2 + 2NO2 |
to Mn(NO3)2 +PbO2 →MnO2+ Pb(NO3)2 2KMnO4 + 3MnSO4 + 2H2O → 5MnO2 + K2SO4 +2H2SO4 |
MnO2
↙OH— ↘ H+
-2 +2
MnO4 Mn
манганат
|
2MnO2 +2H2SO4 (к) → 2MnSO4 + 2H2O+ O2 MnO2 + 4HCl → MnCl2 + Cl2+ 2H2O |
2MnO2 + 4HNO3 (к) → 2Mn(NO3)2 + 2H2O +O2 |
MnO2 проявляет кислотные свойства при сплавлении со щелочами или оксидами активных металлов без доступа воздуха.
|
MnO2 + 2KOH → K2MnO3 + H2O (не ОВР) |
Mn(OH)4 + BaO → BaMnO3 + 2H2O (не ОВР) |
В зависимости от условий реакции MnO2 проявляет либо окислительные, либо восстановительные свойства.
В кислой среде:
|
MnO2 +2FeSO4 +2H2SO4 → MnSO4 + Fe2(SO4)3 + 2H2O |
2MnO2+3PbO2+6HNO3→ 2HMnO4 +3Pb(NO3)2 + 2H2O |
В щелочной среде:
to
3MnO2 + KClO3 + 6NaOH → 3Na2MnO4 +KCl + 3H2O
твёрдые сплавление
MnO2 + KNO3 + 2KOH → K2MnO4 + KNO2 + H2O
_
MnO4
↙H+ ↓H2O ↘OH—
+2 2-
Mn +4 MnO4
MnO2 ↓ манганат
оксид марганца (IV)
В кислой среде:
|
2KMnO4+5K2SO3 +3H2SO4→2MnSO4+6K2SO4+3H2O 2KMnO4+5Na2SO3+3H2SO4→2MnSO4+5Na2SO4+ K2SO4 +3H2O 2KMnO4 + 5H2S + 3H2SO4 → 5S + MnSO4 + K2SO4 + 8H2O 2KMnO4 + 5H3PO3 + 3H2SO4 → 5H3PO4 +2MnSO4 + K2SO4 + 3H2O 2KMnO4 + 5N2O + 3H2SO4 → 2MnSO4 + K2SO4 + 10NO + 3H2O 2KMnO4 + 5NaNO2 + 3H2SO4 → 5NaNO3 +2MnSO4 + K2SO4 + 3H2O 2KMnO4 + 10KBr + 8H2SO4 → 2MnSO4 + 5Br2 + 6K2SO4 + 8H2O 8KMnO4 + 5PH3 + 24HCl → 5H3PO4 + 8MnCl2 + 8KCl + 12H2O 2KMnO4 + 16HCl → 5Cl2 + MnCl2 + 2KCl + 8H2O 10 FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O В нейтральной среде: 2KMnO4+5SO2+ 2H2O → 2MnSO4 + K2SO4 + 2H2SO4 |
2KMnO4 + 3K2SO3 + H2O → 2MnO2 + 3K2SO4 + 2KOH
2KMnO4 + 3Na2SO3 + H2O → 2MnO2 + 3Na2SO4 + 2KOH
2KMnO4 + (NH4)2SO4 → 2MnO2 + N2 + K2SO4 + 4H2O
2KMnO4 + 3MnSO4 + 2H2O → 5MnO2 + K2SO4 + 2H2SO4
В щелочной среде:
2KMnO4 + K2SO3 + 2KOH → K2SO4 + 2K2MnO4 + H2O
2KMnO4 + Na2SO3 + 2KOH → Na2SO4 + 2K2MnO4 + H2O
Другие реакции:
to
2KMnO4 → K2MnO4 + MnO2 + O2↑
2HMnO4 + 3H2S → 3S + 2MnO2 + 4H2O
8HMnO4 + 3PH3 → 3H3PO4 + 8MnO2 + 4H2O
K2MnO4 + K2S + 2H2O → S + MnO2 + 4KOH
K2MnO4 + Cl2 → 2KCl + 2KMnO4
MnSO4 + NaClO + 2NaOH → MnO2 + NaCl + Na2SO4 + H2O
Соединения хрома.
Соединения хрома (III).
Cr2O3 – оксид хрома (III), порошок тёмно-зелёного цвета, по твёрдости близок к корунду. Поэтому его вводят в состав полирующих средств. Он нерастворим в воде, имеет аморфный характер, однако в кислотах и щелочах плохо растворим.
Химические свойства.
1. Сплавление со щелочами:
t0 t0
Cr2O3 + 2KOH → 2KCrO2 + H2O Cr2O3 + Ba(OH)2 → Ba(CrO2)2 + H2O
хромит калия хромит бария
2. Сплавление с карбонатами щелочных металлов:
t0
Cr2O3 + Na2CO3 → 2NaCrO2 + CO2
хромит натрия
3. Сплавление с оксидами щелочных и щелочно-земельных металлов:
t0
Cr2O3 + Na2O → 2NaCrO2
4. С концентрированными растворами кислот и щелочей реагирует с трудом:
Cr2O3 + 6HCl → 2CrCl3 + 3H2O
t0
Cr2O3 + 6NaOH + 3H2O → 2Na3[Cr(OH)6]
гексагидроксохромит натрия
5. Взаимодействует со щелочными расплавами окислителей:
t0 +6
Cr2O3 + 3KNO3 + 4KOH → 2K2CrO4 + 3KNO2 + 2H2O
хромат калия
Получение Cr2O3.
1. В лаборатории. 2. В промышленности.
t0 t0
(NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O 2K2Cr2O7+3С→2Cr2O3+
2K2СO3 + СO2
t0
K2Cr2O7 + S → Cr2O3 + K2SO4
Cr(OH)3 – гидроксид хрома (III), серо-зелёного цвета, нерастворим в воде, амфотерный.
Получение Cr(OH)3.
CrCl3 + 3NaOH → Cr(OH)3 + 3NaCl
студенистый серо-зелёный осадок
Химические свойства.
Cr(OH)3 легко взаимодействует с кислотами и со щелочами.
1. Взаимодействие с кислотами:
2Cr(OH)3 + 3H2SO4 → Cr2(SO4)3 + 6H2O
2. Взаимодействие со щелочами:
Cr(OH)3 + 3NaOH → Na3[Cr(OH)6]
гексагидроксохромат (III) натрия
(изумрудно-зелёный раствор)
3. Разложение при нагревании.
t0
2Cr(OH)3 → Cr2O3 + 3H2O
Соли – хромиты и другие — (III).
Химические свойства.
1. С кислотами легко реагируют:
а) недостаток кислоты:
NaCrO2 + HCl + H2O → Cr(OH)3 + NaCl
б) избыток кислоты:
NaCrO2 + 4HCl → CrCl3 + NaCl + 2H2O
2. С кислотными оксидами:
Na3[Cr(OH)6] + 3CO2 → Cr(OH)3 + 3NaHCO3
3. В растворе подвергаются гидролизу:
NaCrO2 + 2H2O → Cr(OH)3↓ + NaOH
Cr2S3 + 6H2O → 2Cr(OH)3↓ + 3H2S↑
4. Окислительные свойства соединений хрома (III):
+3 0 +2 +1
Cr2(SO4)3 + H2 (Zn + H2SO4) → 2CrSO4 + H2SO4
5. Восстановительные свойства соединений хрома (III):
+3 0 +6 -1
2К3[Cr(OH)6] + 3Br2 + 4KOH → 2K2CrO4 + 6KBr + 8H2O
+3 -1 +6 -2
3CrCl3 + 3H2O2 + 10KOH → 2K2CrO4 + 6KCL + 8H2O
-3e—↗ Cr+6 (окисление)
Cr+3
+1e—↘ Cr+2 (восстановление)
Соединения хрома (III):
а) при окислении в щелочной среде образуют хроматы:
to
Cr2O3 + KClO3 + 4KOH → 2K2CrO4 + KCl + 2H2O
спекание хромат калия
б) при окислении в кислой среде образуют дихроматы:
Cr2(SO4)3 + 2K2FeO4 + H2SO4 → K2Cr2O7 + Fe2(SO4)3 + K2SO4 + H2O
дихромат калия
Соединения хрома (VI).
CrO3 – оксид хрома (VI) – кристаллы тёмно-красного цвета, хорошо растворимые в воде, сильно ядовит (действует на почки; 0,6 г – смертельная доза). Кислотный оксид, которому соответствуют кислоты Н2CrO4 и Н2Cr2O7.
Получение CrO3.
K2Cr2O7 + 2H2SO4 → K2SO4 + 2CrO3 + H2O
Химические свойства.
1. Взаимодействие с водой.
OH— H+
CrO3 + H2O → Н2CrO4 2CrO3 + H2O → H2Cr2O7
Формула получающейся кислоты зависит от среды.
CrO3 – сильнейший окислитель.
2. Взаимодействие с углеродом:
4CrO3 + 3C → 3CO2↑ + 2Cr2O3
3. Взаимодействие с серой:
4CrO3 + 3S → 3SO2 + 2Cr2O3
4. Взаимодействие с органическими веществами:
C2H5OH + 4CrO3 → 2CO2↑ + 2Cr2O3 + 3H2O
+6 +3 +4 H C2H5OH + 4CrO3 + 6H2SO4 → 2Cr2(SO4)3 + 2CO2↑ + 9H2O H ↘ ↓
Реакция сопровождается воспламенением. H→C-С→O←H
H↗ ↑
H
5. Соли хромовой и дихромовой кислот – сильнейшие окислители.
Na2CrO4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O (не ОВР)
Na2Cr2O7 + 2NaOH → 2Na2CrO4 + H2O (не ОВР)
6. Хроматы при нагревании устойчивы, дихроматы при нагревании неустойчивы:
t0
4K2Cr2O7 → 4K2CrO4 + 2Cr2O3 + 3 O2↑
7. Взаимодействие с солями:
а) в нейтральной среде
2K2CrO4 + 3(NH4)2S + 2H2O → 2Cr(OH)3↓ + 3S↓ + 6NH3↑ + 4KOH
б) в щелочной среде
2K2CrO4 + 3(NH4)2S + 2KOH + 2H2O → 2K3[Cr(OH)6] + 3S↓ + 6NH3↑
в) в кислой среде:
K2Cr2O7 + 14HCl → 3Cl2 + 2KCL + 2CrCl3 + 7H2O
Cr(OH)3 — серо—зелёный осадок
K2CrO4 (CrO4)2— H2O ↗
}—-OH—— → [Cr(OH)6]3- — р-р изумрудно-зелёного цвета
K2Cr2O7 (Cr2O7)2 ______H+__
↘
Cr3+ — р-р сине-фиолетового цвета
Окисление органических соединений бихроматом калия.
+6 -2 +2 +3
2K2Cr2O7 + 3CH3OH + 8H2SO4 → HCOOH + 2Cr2(SO4)3 +2K2SO4 + 11H2O
+3 +4
K2Cr2O7 + 3HOOC-COOH + 4H2SO4 → 6CO2 + Cr2(SO4)3 + K2SO4 + 7H2O
Соли в кислой среде:
K2Cr2O7 + 2H2SO4 → 2KHSO4 + 2CrO3 + H2O (не ОВР)
Na2CrO4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O (не ОВР)
K2Cr2O7 + 4H2SO4 + 3H2S → 3S + Cr2(SO4)3 + K2SO4 + 7H2O
K2Cr2O7 + 4H2SO4 + 2NO → 2HNO3 + Cr2(SO4)3 + K2SO4 + 3H2O
2K2Cr2O7 + 8H2SO4 + 3C → 3CO2 + 2Cr2(SO4)3 + 2K2SO4 + 8H2O
K2Cr2O7 + 7H2SO4 + 6KI → 3I2 + Cr2(SO4)3 + 4K2SO4 + 7H2O
K2Cr2O7 + 7H2SO4 + 2Al → Al2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
K2Cr2O7 + 14HCl → 3Cl2 + 2KCL + 2CrCl3 + 7H2O
2K2CrO4 + 16HCl → 3Cl2 + 4KCL + 2CrCl3 + 8H2O
2K2CrO4 + 10HNO3 + 3H2S → 4KNO3 + 2Cr(NO3)3 + 3S + 8H2O
Соли в щелочной среде:
Na2Cr2O7 + 2CsOH → Na2CrO4 + Cs2CrO4 + H2O (не ОВР)
K2Cr2O7 + 2RbOH → Rb2CrO4 + K2CrO4 + H2O (не ОВР)
Cr2(SO4)3 + 3Br2 + 16NaOH → Na2CrO4 + 6NaBr + 3Na2SO4 + 8H2O
Соли в нейтральной (или слабокислой) среде:
2K2CrO4 + 3H2S + 2H2O → 2Cr(OH)3 + 3S + 4KOH
(гор.)
K3[Cr(OH)6] + 3H2O2 → 2K2CrO4 + 8H2O + 2KOH
K3[Cr(OH)6] + 3SO2 → Cr(OH)3 + 3KHSO3 (не ОВР)
K3[Cr(OH)6] + FeCl3 → Cr(OH)3 + Fe(OH)3 + 3KCl (не ОВР)
2K2CrO4 + 3K2SO3 + 5H2O → 2Cr(OH)3↓ + 3K2SO4 + 4KOH
Разложение солей:
to
(NH4)2Cr2O7 → N2 + Cr2O3 + 4H2O (вулкан)
Основания:
2Cr(OH)3 + 3Cl2 + 10NaOH → 2Na2CrO4 + 6NaCl + 8H2O
Оксиды:
2CrO3 + 2NH3 + H2O → (NH4)2Cr2O7 (не ОВР)
Cr2O3 + 3KNO3 + 4KOH → 2K2CrO4 + 3KNO2 + 2H2O
+3 +1 -1 +6
Cr2O3 + 3Ca(OCl)Cl + 4NaOH → 3CaCl2 + 2Na2CrO4 + 2H2O
+3 +5 t0 +6 +4
Cr2O3 + Na2CO3 + KClO3 → 2Na2CrO4 + KCl + 2CO2
+3 +1 -1 +6
Cr2O3 + 3Ca(OCl)Cl + 4NaOH → 3CaCl2 + 2Na2CrO4 + 2H2O
+3 +5 t0 +6 +4
Cr2O3 + Na2CO3 + KClO3 → 2Na2CrO4 + KCl + 2CO2
t0
2Cr2O3 +3O2 +4Na2CO3 → 4Na2CrO4 + 4CO2
t0
2Cr2O3 +3O2 +4Na2CO3 → 4Na2CrO4 + 4CO2
Написать уравнения 4-х возможных реакций:
1) р-ры CrSO4; NaOH; Na2CrO4; H2SO4:
3CrSO4 + Na2CrO4 + 16NaOH + 4H2O → 4Na3[Cr(OH)6] + 3Na2SO4
2Na2CrO4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O
2NaOH + H2SO4 → Na2SO4 + 2H2O
CrSO4 + 2NaOH → Na2SO4 + Cr(OH)2
2) р-ры SO2; CsOH; K2Cr2O7; H2SO4:
K2Cr2O7 + 2CsOH → K2CrO4 + Cs2CrO4 + H2O
2CsOH + H2SO4 → Cs2SO4 + 2H2O
K2Cr2O7 + 3SO2 + H2SO4 → Cr2(SO4)3 + K2SO4 + H2O
2CsOH + SO2 → Cs2SO3 + H2O
3) Cr(NO3)3; Na2SO3; Cl2; NaOH:
Cr(NO3)3 + Na2SO3 + 3H2O → 2Cr(OH)3↓ + SO2 + 6NaNO3
6NaOH + 3Cl2 → 5NaCl + NaClO3 + 3H2O
Cr(NO3)3 + 3NaOH → Cr(OH)3 + 3NaNO3
Галогены.
t0
3Cl2 + 6KOH (гор.) → 5KCl + KClO3 + 3H2O
Cl2 + 2KOH (хол.) → KCl + KClO + H2O
3Cl2 + 8NH3 → 6NH4Cl + N2
Cl2 + NaHS → S + NaCl + HCl
t0
3Br2 + 6KOH (гор.) → 5KBr + KBrO3 + 3H2O
Br2 + 2KOH (хол.) → KBr + KBrO + H2O
6Br2 + 6Ba(OH)2 → Ba(BrO3)2 + 5BaBr2 + 6H2O
чистый горячий
Br2 + H2S → 2HI + S
I2 + SO2 + 2H2O → H2SO4 + HI
Соединения галогенов.
KClO3 + 6HCl → KCl + 3Cl2 + 3H2O
KClO + HI → Kl + l2 + H2O
Соединения серы.
Концентрированная H2SO4.
to
5H2SO4 + 8KIтв. → 4 I2 + 3H2S ↑+ 4K2SO4 + 4H2O
3H2SO4 + KIO3 + 5KI → 3I2 + 3K2SO4 + 3H2O
H2SO4 + Na2S2O3 → Na2SO4 + SO2↑ + S↓ + H2O
2H2SO4 + Hg → HgSO4 + SO2 + 2H2O
2H2SO4 + C → CO2 + 2SO2 + 2H2O
Оксид серы (IV).
SO2 + I2 + 2H2O → H2SO4 + 2HI
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
SO2 + 2H2S → 3S + 2H2O
SO2 + H2O2 → H2SO4
Сера.
S + 6HNO3 (к.) → H2SO4 + 6NO2 + 2H2O
S + 2H2SO4 (к.) → 3SO2 + 2H2O
S + 3H2SO4 (к.) → 4SO2 + 4H2O
Соединения фосфора.
Фосфор.
|
to |
|||
|
6P + 5HClO3 + 9H2O → 5HCl + 6H3PO4 |
2P + 5NaNO3 → 5NaNO2 + P2O5 |
||
|
P + KMnO4 + H2SO4 →KH2PO4 + MnSO4 |
|||
|
4P + 3KOH(k.) + 3H2O → 3KH2PO2 + PH3 |
P + 5HNO3 (к.) → H3PO4 + 5NO2 + 5H2O |
Фосфин.
2PH3 + 4O2 → P2O5 + 3H2O
PH3 + 8AgNO3 + 4H2O → 8Ag + H3PO4 + 8HNO3
5PH3 + 8HBrO3 → 5H3PO4 + 4Br2 + 4H2O
3PH3 + 4HClO3 → 3H3PO4 + 4HCl
3PH3 + 8HMnO4 → 3H3PO4 + 8MnO2 + 4H2O
Фосфаты.
Сa3(PO4)2 + 5C + 3SiO2 → 3CaSiO3 + 2P + 5CO
3Сa3(PO4)2 + 16Al → 3Сa3P2 + 8Al2O3
Соединения азота.
Оксид азота (IV).
2NO2 + 2KOH → KNO2 + KNO3 + H2O
to
2NO2 + 4Cu → N2 + 4CuO
Азотная кислота.
H2S + 8HNO3 (к.) → H2SO4 + 8NO2 + 4H2O
H2S + 2HNO3 (к., хол.) → S + 2NO2 + 2H2O
3As2S3 + 28HNO3 + 4H2O → 6H3AsO4 + 28NO + 9H2SO4
S + 6HNO3 (к.) → H2SO4 + 6NO2 + 2H2O
5HNO3 (к.) + P → H3PO4 + 5NO2 + 5H2O
3Si + 4HNO3 + 18HF → 3H2SiF6 + 4NO + 8H2O
8HNO3 (к.) + CuS → CuSO4 + 8NO2 + 4H2O
Нитраты.
4Zn + KNO3 + 7KOH → NH3 + 4K2ZnO2 + 2H2O
(тв.)
Аммиак.
NH3 + Ca(OCl)2 → N2 + H2O + CaCl2
Кремний.
3Si + 4HNO3 + 18HF → 3H2SiF6 + 4NO + 8H2O
Si + 4NaOH → Na4SiO4 + 2H2↑
Si + 2NaOH + H2O → Na2SiO3 + 2H2
Кислород.
2PH3 + 4O2 → P2O5 + 3H2O
2NO2 + O2 + 2KOH → 2KNO3 + H2O
Скачать материал

Скачать материал






- Сейчас обучается 412 человек из 63 регионов


Описание презентации по отдельным слайдам:
-
1 слайд
Мастер – класс «Подготовка к ЕГЭ. Окислительно-восстановительные реакции»
КУЗОВАЯ Т.В., учитель химии МАОУ Гимназия №1 г.Белогорск
-
2 слайд
Информация о ЕГЭ. Мнения учащихся и родителей.
Школьные выпускные экзамены – первая по-настоящему серьезная проверка эффективности той работы, которой ученик занимался несколько лет. С 2001 ЕГЭ в порядке эксперимента введен на территории РФ, а с 2009 года переведен в штатный режим как государственный механизм контроля качества образования.
На мой взгляд введение ЕГЭ в школах имеет свои положительные и отрицательные моменты. -
3 слайд
Положительные стороны ЕГЭ:
Тестирование как форма опроса вводится во все сферы жизни человека, школьники готовятся к особенностям выполнения тестовых заданий, которые позволяют проверить общий уровень грамотности.
Благодаря ЕГЭ молодые люди могут продолжить свое обучение в различных учебных заведениях РФ.
ЕГЭ может защитить ученика от несправедливого учитель. -
4 слайд
Отрицательные стороны ЕГЭ:
Тесты хороши для инертных, ограниченных людей, а не творческих. Значит этим снижается интерес к предмету, интерес поиска своих решений даже у сильно увлеченного человека.
Введение ЕГЭ приведет к натаскиванию выполнения заданий, поэтому снизится целостность восприятия химического образования.
При минимальном количестве учебного времени на подготовку, роль репетиторства будет необходима.
При снижении учебной нагрузки невозможно готовить учащихся к ЕГЭ. -
5 слайд
Количество учебных часов по химии на весь период обучения
8 – 9 классы – 68 часов – 2 часа в неделю – 5,5% всего учебного времени за год.
10 – 11 классы – 34 часа — 1 час в неделю – 2,7% всего учебного времени за год.
10 – 11 классы (профильные) – 170 часов в неделю- 13,8% всего учебного времени за год.На период обучения химии отводится 204 урока за 4 года в непрофильных классах.
-
6 слайд
Некорректные формулировки и ошибки в тестах:
Верны ли следующие суждения о галогенах?
А. Все галогены проявляют высшую степень окисления.
Б. Радиус атома уменьшается от фтора к йоду.
(ответ: верно только Б).
Карбонат натрия в растворе не взаимодействует с
1) серной кислотой, 2) углекислым газом, 3) сульфатом натрия, 4) хлоридом железа (2).
(ответ: 2) -
7 слайд
Вопросы к родителям:
Считаете ли вы ЕГЭ защитой от несправедливости учителя?
Вдруг ваш ребенок не справится с ЕГЭ, кого будите винить?
Какой вопрос вы бы хотели задать авторам этого эксперимента? -
8 слайд
Вопросы к учащимся:
Как вы относитесь к ЕГЭ как системе контроля качества ваших знаний?
Можно ли сказать, что КИМЫ дают объективную оценку качества ваших знаний?
Приведите 3-4 примера наиболее сложных заданий
Расшифруйте аббревиатуру ЕГЭ на современном школьном сленге.
Ваши предложения к проведению контрольного тестирования школьников. -
9 слайд
Результаты опроса учащихся
На 1 вопрос: положительно – 30 % учащихся, отрицательно – 55 % учащихся, затрудняются с ответом – 15% учащихся.
На 2 вопрос: да – ответили 40 % учащихся, нет – 60 %.
На 3 вопрос: наиболее трудными считают- задачи варианта С, цепочки органических превращений, ОВР.
На 4 вопрос: ЕГЭ это: единый государственный эшафот, единая гениальная эйфория, европейская глобальная экзекуция, если готов- экзаменуйся! -
10 слайд
Изучение КИМОВ показало:
Часть А- содержит вопросы, связанные с ОВР- А4, А7,А8, А24. Всего 4 балла.
Часть В – В2, всего 2 балла.
Часть С – С1, С2, всего 7 баллов.
На ОВР приходится 13 набранных баллов. Это 26% ответов от оценки «5», 39% ответов от оценки «4», 81% ответов от оценки «3».
Вывод: Знания об окислительно-восстановительных реакциях влияют на количество баллов при ответах. -
11 слайд
Изучение программ показало:
На изучение темы ОВР в 8 классе отводится :
а) в теме «Строение вещества»- 1 урок,
б) в теме «Типы химических реакций»- 2 урока.
На изучение темы ОВР в 9 классе отводится:
а) в теме «Азот и его соединения» -1 урок
На изучение темы ОВР в 11 классе отводится –2 урока.
Итого 6 уроков за 4 года обучения. -
12 слайд
ТЕМА УРОКА: ОВР. Метод полуреакций и влияние среды на ход ОВР
Цель урока: Формирование умения составлять уравнения окислительно-восстановительных процессов, идущих в разных условиях.
Учащиеся умеют: распознавать ОВР, определять степени окисления, составлять процессы окисления и восстановления, подбирать коэффициенты методом электронного баланса.
Формируемые умения: записывать уравнения полуреакций окислительно-восстановительных превращений, подбирать сопряженные пары окислительной и восстановительной полуреакций для ОВ процесса. -
13 слайд
Девиз к уроку:
БЛАГОДАРЯ ИСТИННОМУ ЗНАНИЮ ТЫ БУДЕШЬ ГОРАЗДО СМЕЛЕЕ И СОВЕРШЕННЕЕ, ЧЕМ БЕЗ НЕГО.ДЮРЕР.
-
14 слайд
Используемые технологии:
Технология интерактивного обучения(использование кластеров, метод « мозгового штурма»).
Здоровьесберегающие технологии(физкульминутка, релаксация).
Информационно-коммуникативные технологии (мультимедийные слайды, интерактивная доска).
Проблемное обучение.
Исследования в группах( лабораторная работа).
Технология сотрудничества. -
15 слайд
Использование кластеров
С каким настроением вы пришли на урок?
С каким настроением вы ушли с урока? -
16 слайд
Основные понятия для изучения данной темы
Окисление
Восстановление
Окислитель
Восстановитель
Степень окисления
Полуреакция
Электронный баланс
Коэффициент
Электрон -
17 слайд
Степень
окисления
ПОЛУРЕАКЦИЯ
ЭЛЕКТРОН
ВОССТАНОВИТЕЛЬ
ОКИСЛИТЕЛЬ
ВОССТАНОВЛЕНИЕ
ОКИСЛЕНИЕ
ОВР -
18 слайд
Прием «мозгового штурма»
Что такое окислитель?
Какой процесс называют окисление?
Что такое восстановитель?
Какой процесс называют восстановление?
Какие реакции называют окислительно-восстановительными?
Что такое степень окисления?
Какой заряд имеет электрон?
Назовите типы ОВР
Назовите способы расстановки коэффициентов в ОВР. -
19 слайд
Методы расстановки коэффициентов в ОВР
1)2)
3)
-
20 слайд
Расставить коэффициенты методом электронного баланса
H2SO4 + Cu = CuSO4 + SO2 + H2O -
21 слайд
ОВР
Физкультурная пауза -
22 слайд
Алгоритм метода полуреакций
Находим элементы, которые изменили степень окисления и определяем в состав какого иона они входят.
В кислой среде атомы кислорода добавляем за счет молекул воды, а атомы водорода за счет катионов водорода.
В щелочной среде атомы кислорода добавляем за счет гидроксогрупп из расчета 1:2, а атомы водорода- добавлением воды.
В нейтральной среде слева всегда вода, а справа протоны или гидроксогруппы.
Восстановитель переходит в соединение с высшей степенью окисления.
Составляем электронный баланс.
Суммируем обе правые части и левые с учетом коэффициентов.
Составляем молекулярное уравнение. -
23 слайд
Лабораторная работа в группах «Превращение хроматов в дихроматы и наоборот» –проблемная ситуация
К раствору хромата калия добавить раствор серной кислоты. Что наблюдаем? Составить уравнение реакции. Является ли она ОВР?К раствору дихромата калия добавить раствор щелочи. Что наблюдаем? Составить уравнение реакции. Является ли эта реакция ОВР?
-
24 слайд
Лабораторная работа в группах «Влияние среды на ОВР»
К раствору сульфита натрия добавьте раствор серной кислоты и раствор перманганат калия? Что наблюдаете? Составьте ОВР. Расставьте коэффициенты методом полуреакций.
К раствору сульфита натрия добавьте раствор перманганата калия. Что наблюдаете? Составьте ОВР. Расставьте коэффициенты методом полуреакций.
К раствору сульфита натрия добавьте раствор щелочи и раствор перманганата калия. Что наблюдаете? Составьте ОВР. Расставьте коэффициенты методом полуреакций. -
25 слайд
Расставить коэффициенты методом полуреакций:
K2SO3 +KMnO4+H2SO4= -
26 слайд
Расставить коэффициенты методом полуреакций
K2SO4 + KMnO4 + H2O=
-
27 слайд
Расставить коэффициенты методом полуреакций
K2SO4 + KMnO4 + KOH =
-
28 слайд
Примеры уравнений для тренировки
CuCI + K2Cr2O7 + HCI =Cr2O3 + KCIO3 + KOH =
H2SO3 + CI2 + H2O =
Na2CrO4 + NaI + NaOH =
-
-
30 слайд
Выводы:
Для изучения данного метода расстановки коэффициентов учащиеся должны обладать необходимыми навыками и оперировать определенными понятиями при изучении ОВР.
Необходимы знания основных окислителей и восстановителей и их переход в другую форму в различной среде.
Данная методика составления ОВР универсальна и проста, ее использование позволяет прогнозировать состав продуктов реакций, что выходит за рамки программы средней школы.
Умения в составлении таких уравнений отрабатываются на нескольких уроках. -
31 слайд
Заключение:
Т.К. ЕГЭ в настоящее время это реалии сегодняшнего дня, необходимо настраивать учеников на такой контроль, начиная с 8 класса.
Психологически готовить школьников и их родителей, настраивать их на успех, учить планировать свое время, расслабляться и отдыхать.
Проводить тренировочные тесты по типу ЕГЭ после изучения каждой темы школьного курса.
По возможности убеждать администрацию школы, что при таком количестве часов по химии результаты ЕГЭ не будут радовать ни нас, ни их, ни учеников и их родителей.
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 154 748 материалов в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Другие материалы
- 31.12.2020
- 3792
- 1
- 31.12.2020
- 4349
- 0
- 31.12.2020
- 5192
- 10
- 31.12.2020
- 4087
- 1
- 31.12.2020
- 3957
- 1
- 31.12.2020
- 5000
- 1
- 31.12.2020
- 4178
- 36
- 31.12.2020
- 2300
- 6
Вам будут интересны эти курсы:
-
Курс повышения квалификации «Формирование компетенций межкультурной коммуникации в условиях реализации ФГОС»
-
Курс повышения квалификации «Экономика предприятия: оценка эффективности деятельности»
-
Курс повышения квалификации «Основы построения коммуникаций в организации»
-
Курс повышения квалификации «Организация практики студентов в соответствии с требованиями ФГОС юридических направлений подготовки»
-
Курс повышения квалификации «Организация практики студентов в соответствии с требованиями ФГОС медицинских направлений подготовки»
-
Курс профессиональной переподготовки «Организация маркетинга в туризме»
-
Курс повышения квалификации «Финансовые инструменты»
-
Курс профессиональной переподготовки «Организация процесса страхования (перестрахования)»
-
Курс повышения квалификации «Информационная этика и право»
-
Курс профессиональной переподготовки «Стратегическое управление деятельностью по дистанционному информационно-справочному обслуживанию»
Основные правила составления окислительно-восстановительных реакций
(скачать pdf файл)
Существует несколько основных правил, которые сильно упрощают составление окислительно-восстановительных реакций. Более подробно эти и другие правила рассматривается на других страницах этого раздела, но для ЕГЭ достаточно знать правила из этого списка.
Правило 1. Реакции простых веществ: металлов и неметаллов с щелочами, кислотами и солями:
1.1) Из металлов только Al, Zn и Be взаимодействуют со щелочами с выделением водорода:
Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
1.2) Из неметаллов только S, P, Si и галогены реагируют с щелочами:
3S + 6NaOH → Na2SO3 + 2Na2S + 3H2O
P4 + 3NaOH + 3H2O → PH3
Si + 2NaOH + H2O → Na2SiO3 + 2H2
Cl2 + 2NaOH → NaCl + NaClO + H2O (аналогично для Br2, I2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании, аналогично для Br2, I2)
2.1) Металлы (стоящие в ряду активности металлов до H2) реагируют с кислотами-неокислителями с выделением водорода:
2HCl + Fe → FeCl2 + H2
H2SO4(р) + Fe → FeSO4 + H2
2.2) Все металлы, кроме Pt и Au, реагируют с кислотами-окислителями без выделения водорода:
2H2SO4(к) + 2Ag → Ag2SO4 + SO2
6H2SO4(к) + 2Fe → Fe2(SO4)3 + 3SO2
2.3) Более сильные металлы вытесняют более слабые из растворов их солей:
Fe + CuSO4 → FeSO4 + Cu
3) Неметаллы не реагируют с кислотами-неокислителями:
C + HCl → реакция не идет
4) Такие неметаллы, как S, C, P могут реагировать с солями, проявляющими окислительные свойства (KClO3, KNO3 в расплавленном состоянии):
6P + 5KClO3 → 3P2O5 + 5KCl
C + 2KNO3 (расплав) → CO2
S + 2KNO3 (расплав) → SO2
5) Важная реакция получения фосфора:
5C + 3SiO2 + Ca3(PO4)2 → 5CO
6) Из неметаллов только S, C, и P реагируют с кислотами-окислителями (в рамках ЕГЭ), а также I2 с HNO3(к):
Правило 2. Фосфор
1) Наиболее устойчивая степень окисления фосфора +5, следовательно, любые другие соединения фосфора окисляются сильными окислителями до этой степени окисления (с образованием P2O5 или фосфат-иона):
PH3 + 8KMnO4 + 11KOH → K3PO4 + 8K2MnO4 + 7H2O
6P + 5KClO3 → 5KCl + 3P2O5
3P2O3 + 4HNO3 + 7H2O → 6H3PO4 + 4NO
Правило 3. Азот
1) Аммиак, как правило, окисляется до азота N2:
8NH3 + 3KBrO4 → 3KBr + 4N2
2NH3 + 3CuO → 3Cu + N2
Исключением является каталитическое окисление аммиака:
4NH3 + 5O2 → 4NO
Обычное горение аммиака протекает с образованием N2 (как и горение любых органических азотсодержащих соединений):
4NH3 + 3O2 → 2N2
2) Нитрит-ионы окисляются до нитрат-ионов:
3KNO2 + K2Cr2O7 + 4H2SO4 → 3KNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
3KNO2 + 2KMnO4 + H2O → 3KNO3 + 2MnO2
3) Нитрит-ионы восстанавливаются до азота в реакциях с солями аммония:
NaNO2 + NH4Cl → N2
Ca(NO2)2 + (NH4)2SO4 → 2N2
4) Нитрит-ионы восстанавливаются до оксида азота (II) в реакциях с типичными восстановителями: HI, йодидами, солями Fe+2 и др.:
2KNO2 + 2KI + 2H2SO4 → 2NO
HNO2 + 2HI → 2NO
Следующий тип реакций встречается в вариантах Ю.Н. Медведева.
5) Нитрат-ионы являются сильными окислителями при сплавлении с соединениями Cr, Mn, Fe в щелочной среде и с некоторыми неметаллами (восстанавливаются до нитритов):
3NaNO3 + Cr2O3 + 4KOH → 3NaNO2 + 2K2CrO4 + 2H2O
KNO3 + MnO2 + K2CO3 → KNO2 + K2MnO4 + CO2
2NaNO3 + FeSO4 + 4NaOH → 2NaNO2 + Na2FeO4 + Na2SO4 + 2H2O
2KNO3(расплав) + C → 2KNO2 + CO2
2KNO3(расплав) + S → 2KNO2 + SO2
6) Нитрат-ионы являются сильными окислителями в кислотной среде:
2KNO3 + Cu + 2H2SO4 → CuSO4 + 2NO2
7) Восстановление нитратов до аммиака в реакциях с такими металлами, как Al, Zn, Mg (встречается очень редко):
3NaNO3 + 8Al + 5NaOH +18H2O → 3NH3
NaNO3 + 4Zn + 7NaOH + 6H2O → NH3
KNO3 + 4Mg + 6H2O → NH3


Правило 4. Кислород
1) Перекись водорода окисляется до кислорода O2 типичными окислителями:
KMnO4, K2Cr2O7, галогены, соли кислородсодержащих кислот хлора (например, KClO3) и некоторыми другими.
5H2O2 + KMnO4 + 3H2SO4 → 2MnSO4 + K2SO4 + 5O2
3H2O2 + 2KNO3 + H2SO4 → K2SO4 + 2NO

2) Перекись водорода восстанавливается до H2O типичными восстановителями:
KI (HI, йодиды), K2SO3 (SO2, сульфиты), KNO2 (нитриты), PbS (H2S, сульфиды), соединения Cr+3 в щелочной среде, соединения Fe+2, NH3 и некоторыми другими.
H2O2 + Na2SO3 → Na2SO4 + H2O
H2O2 + KNO2 → KNO3 + H2O
3H2O2 + 2NaCrO2 + 2NaOH → 2Na2CrO4 + 4H2O
Свойства пероксида водорода с примерами
Правило 5. Галогены
1) Галогены диспропорционируют в щелочах:
Cl2 + 2NaOH → NaCl + NaClO + H2O (аналогично для Br2, I2)
3Cl2 + 6NaOH → 5NaCl + NaClO3 + 3H2O (при нагревании, аналогично для Br2, I2)
2) Простые вещества галогены и соединения галогенов в любой положительной степени окисления восстанавливаются, как правило, до галогенид-ионов (т.е. до ст. ок. -1) в реакциях с типичными восстановителями:
5HClO3 + 6P + 9H2O → 5HCl + 6H3PO4
KClO3 + 6Fe(OH)2 + 18HCl → 6FeCl3 + KCl + 15H2O
2Cl2 + H3PO2 + 7KOH → K3PO4 + 4KCl + 5H2O
2Br2 + CrCl2 + 8NaOH → Na2CrO4 + 2NaCl + 4NaBr + 4H2O
Исключение: соединения йода в высоких степенях окисления могут восстанавливаться до I2, а не до йодид-иона
KIO3 + 5KI + 3H2SO4 → 3I2 + 3K2SO4 + 3H2O.
3) Галогенид-ионы окисляются, как правило, до простых веществ: Cl2, Br2, I2:
14HCl + K2Cr2O7 → 3Cl2 + 2CrCl3 + 2KCl + 7H2O
16HCl + 2KMnO4 → 5Cl2 + 2MnCl2 + 2KCl + 8H2O
4) Йодид меди восстанавливает серную кислоту до SO2, тогда как йодиды активных металлов до H2S:
2CuI + 4H2SO4(конц.) → I2 + 2SO2 + 2CuSO4 + 4H2O
8KI + 5H2SO4(конц.) → 4I2 + H2S + 4K2SO4 + 4H2O
5) Концентрированной серной кислотой окисляются только бромид- и йодид-ионы. В первом случае образуется SO2, во втором H2S.
2KBr + 2H2SO4(конц.) → Br2 + SO2 + K2SO4 + 2H2O
8KI + 5H2SO4(конц.) → 4I2 + H2S + 4K2SO4 + 4H2O.
6) Более сильные галогены вытесняют менее сильные из галогенидов. В ряду F2, Cl2, Br2, I2 окислительные свойства ослабевают.
Cl2 + 2NaI → I2 + 2NaCl
Cl2 + NaF → реакция не идет, так как Cl2 — более слабый окислитель чем F2.
Все галогены вытесняют серу из сульфидов:
(NH4)2S + Br2 → S + 2NH4Br.
Правило 6. Сера
1) Сульфид-ионы обычно окисляются до S типичными окислителями: Br2, I2, растворами солей K2Cr2O7, KMnO4 и др.:
3Na2S + K2Cr2O7 + 7H2SO4 → 3S
5Na2S + 2KMnO4 + 16HCl → 5S
H2S + Br2 → S
H2S + H2O2 → S
2) С H2SO4(к) сероводород и сульфиды реагируют с образованием SO2, аналогично реакции кислоты с серой:
S + H2SO4(конц.) → 3SO2
H2S + 3H2SO4(конц.) → 4SO2
K2S + 4H2SO4(конц.) → K2SO4 + 4SO2
В этой реакции сульфид-ион окисляется до SO2: S–2 -6e → S+4.
Часть сульфат-ионов восстанавливается также до SO2 и часть остается для образования соли K2SO4.
3) Окисление H2S и сульфидов до сульфат-ионов протекает в реакциях с такими окислителями, как Cl2 в воде, H2O2, HNO3(конц.) при нагревании:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
H2S + 8HNO3(конц.) → H2SO4 + 8NO2
PbS + 4H2O2 → PbSO4 + 4H2O (черный сульфид свинца превращается в белый сульфат)
4) Сульфит-ионы любыми окислителями окисляются до сульфат-иона:
3Na2SO3 + 2KMnO4 + H2O → 2MnO2 + 2Na2SO4 + 2KOH
3K2SO3 + 2K2CrO4 + 5H2O → 2Cr(OH)3 + 3K2SO4 + 4KOH.
5) Взаимодействие серной кислоты с простыми и сложными веществами
Правило 7. Медь
1) Соединения Cu+2 окисляют соединения S+4 и I– (восстанавливаясь до Cu+1):
2CuCl2 + SO2 + 2H2O → 2CuCl
2Cu(NO3)2 + 4KI → 2CuI

В реакции с аммиаком выделяется металлическая медь:
3CuO + 2NH3 → N2
2) Йодиды меди реагируют с H2SO4(к) с образованием SO2, тогда как йодиды щелочных металлов с образованием H2S:
2CuI + 4H2SO4 → 2CuSO4 + I2 + 2SO2 + 4H2O
8KI + 5H2SO4(конц.) → 4K2SO4 + 4I2 + H2S + 4H2O
3) Медь по-разному реагирует с галогенами:
Cu + Cl2 → CuCl2
Cu + Br2 → CuBr2
2Cu + I2 → 2CuI (соль меди +1)
4) Медь в степени окисления +2 восстанавливается самой медью:
CuO + Cu → Cu2O (t)
CuCl2 + Cu → 2CuCl (t).
Правило 8. Железо
1) Соединения Fe+3 окисляют соединения S–2, S+4, I– и некоторые слабые металлы (восстанавливаясь до Fe+2):
Fe2O3 + 6HI → 2FeI2 + I2
2FeCl3 + 3Na2S → 2FeS

2FeCl3 + H2S → 2FeCl2 + S
2FeCl3 + Na2SO3 +H2O → 2FeCl2 + Na2SO4 + 2HCl
2FeCl3 + Cu → CuCl2 + 2FeCl2 (соль железа +2)
Fe2(SO4)3 + Cu → CuSO4 + 2FeSO4 (соль железа +2)
2Fe(NO3)3 + Fe → 3Fe(NO3)2 (соль железа +2)
2) В кислой среде соединения Fe+2 окисляются такими окислителями, как KMnO4, K2Cr2O7, Na2O2, HNO3, H2SO4(к) и др. до солей Fe+3:
6FeCl2 + Na2Cr2O7 + 14HCl → 6FeCl3 + 2CrCl3 + 2NaCl + 7H2O
2FeSO4 + Na2O2 + 2H2SO4 → Fe2(SO4)3 + Na2SO4 + 2H2O
3) В щелочной среде образуется гидроксид железа (III):
FeCl2 + KMnO4 + 3KOH → K2MnO4 + Fe(OH)3 + 2KCl
2FeSO4 + 2KMnO4 + 6NaOH → K2MnO4 + 2Fe(OH)3 + Na2MnO4 + 2Na2SO4
4) Железо по-разному реагирует с галогенами:
2Fe + 3F2 → 2FeF3
2Fe + 3Cl2 → 2FeCl3
2Fe + 3Br2 → 2FeBr3
Fe + I2 → FeI2 (соль железа +2)
5) Соединения Fe+2, Fe+3 также могут быть окислены до степени окисления +6 (до ферратов, например, Na2FeO4) очень сильными окислителями, но на ЕГЭ знание этих реакций не проверяется (источник: вебинары от разработчиков экзамена):
3FeSO4 + 2NaClO3 + 12NaOH → 3Na2FeO4 + 2NaCl + 3Na2SO4 + 6H2O.
Правило 9. Марганец
1) В кислой среде образуются соли Mn+2:
K2MnO4 + 8HBr → MnBr2 + 2Br2 + 2KBr + 4H2O
2KMnO4 + 5SO2 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
2) В щелочной среде образуется манганат-ион MnO42– (зеленого цвета):
MnSO4 + 2Br2 + 8KOH → K2MnO4 + 4KBr + Na2SO4 + 4H2O
2KMnO4 + 2FeSO4 + 6NaOH → K2MnO4 + 2Fe(OH)3
3) В нейтральной среде образуется осадок бурого цвета MnO2:
3MnSO4 + 2KMnO4 + 2H2O → 5MnO2
2KMnO4 + 3K2S + 4H2O → 2MnO2

K2MnO4 + Na2S + 2H2O → S

Правило 10. Хром
1) Восстановление дихроматов в кислой среде протекает с образованием солей Cr+3:
Na2Cr2O7 + 6NaI + 7H2SO4 → Cr2(SO4)3 + 3I2
K2Cr2O7 + 6FeSO4 + 7H2SO4 → Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O
K2Cr2O7 + 3KNO2 + 8HNO3 → 2Cr(NO3)3 + 5KNO3 + 4H2O
2) Окисление соединений Cr+2 в кислой среде протекает с образованием солей Cr+3:
6CrCl2 + K2Cr2O7 + 14HCl → 8CrCl3 + 2KCl + 7H2O
2CrCl2 + 4H2SO4(конц.) → Cr2(SO4)3 + SO2 + 4HCl + 2H2O
3) Окисление соединений Cr+3 очень сильными окислителями с щелочами или с карбонатами щелочных металлов протекает с образованием хроматов (типичные окислители: KNO3, Cl2, KClO3, H2O2 и др. в щел. среде):
Cr2O3 + 3KNO3 + 2K2CO3 → 2K2CrO4 + 3KNO2 + 2CO2
Cr2(SO4)3 + 3Cl2 + 16KOH → 2K2CrO4 + 6KCl + 3K2SO4 + 8H2O
2Cr(OH)3 + KClO3 + 4NaOH → 2Na2CrO4 + KCl + 5H2O
2Cr(OH)3 + 3H2O2 + 4KOH → 2K2CrO4 + 8H2O
4) Соединения Cr+6 в различных средах:
В щелочной среде устойчивы соли хромовой кислоты (хроматы, желтого цвета), например, Na2CrO4.
В кислой среде устойчивы соли дихромовой кислоты (дихроматы, оранжевого цвета), например, Na2Cr2O7.
CrO3 + 2KOH → K2CrO4 + H2O
2K2CrO4 + H2SO4 → K2Cr2O7 + K2SO4 + H2O (в кислотной среде желтая окраска переходит в оранжевую).
Na2Cr2O7 + 2NaOH → 2Na2CrO4 + H2O (в щелочной среде оранжевая окраска переходит в желтую).
Правило 11. Среда раствора
1) С карбонатами щелочных металлов реакции протекают аналогично щелочной среде реакции:
Cr2O3 + 3KNO3 + 2K2CO3 → 2K2CrO4 + 3KNO2 + 2CO2
MnO2 + KNO3 + K2CO3 → K2MnO4 + KNO2 + CO2
2) Если в реакцию вступает оксид серы (IV) SO2 в нейтральном растворе, то реакция протекает аналогично кислой среде раствора:
2KMnO4 + 5SO2 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4.
Поэтому очень важно не зубрить окислительно-восстановительные реакции, а знать какие соединения проявляют окислительные, а какие восстановительные свойства, и знать основные правила, приведенные выше.
Пройти тестирование по этим заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
Определите окислитель и восстановитель.
Источник: Демонстрационная версия ГИА—2014 по химии.
2
Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
3
Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
4
Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
5
Используя метод электронного баланса, составьте уравнение реакции по схеме:
Определите окислитель и восстановитель
Пройти тестирование по этим заданиям
Окислительно-восстановительные реакции. Окислитель и восстановитель
Окислительно-восстановительными называют реакции, которые сопровождаются изменением степеней окисления химических элементов, входящих в состав реагентов.
Окислением называют процесс отдачи электронов атомом, молекулой или ионом, который сопровождается повышением степени окисления.
Восстановлением называют процесс присоединения электронов атомом, молекулой или ионом, который сопровождается понижением степени окисления.
Окислителем называют реагент, который принимает электроны в ходе окислительно-восстановительной реакции. (Легко запомнить: окислитель — грабитель.)
Восстановителем называют реагент, который отдаёт электроны в ходе окислительно-восстановительной реакции.
Окислительно-восстановительные реакции делят на реакции межмолекулярного окисления-восстановления, реакции внутримолекулярного окисления-восстановления, реакции диспропорционирования и реакции конмутации.
Для составления окислительно-восстановительных реакций используют метод электронного баланса.
Составление уравнения окислительно-восстановительной реакции осуществляют в несколько стадий.
- Записывают схему уравнения с указанием в левой и правой частях степеней окисления атомов элементов, участвующих в процессах окисления и восстановления.
- Определяют число электронов, приобретаемых или отдаваемых атомами или ионами.
- Уравнивают число присоединённых и отданных электронов введением множителей, исходя из наименьшего кратного для коэффициентов в процессах окисления и восстановления.
- Найденные коэффициенты (их называют основными) подставляют в уравнение реакции перед соответствующими формулами веществ в левой и правой частях.
Пример 1. Реакция алюминия с серой. Записываем схему реакции и указываем изменение степеней окисления:
Атом серы присоединяет два электрона, изменяя свою степень окисления от 0 до –2. Он является окислителем. Атом алюминия отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 2. Окисление фосфора хлором. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления хлора изменяется от 0 до –1, при этом молекула хлора присоединяет два электрона. Хлор является окислителем.
Атом фосфора отдаёт пять электронов, изменяя свою степень окисления от 0 до +5. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Электронное уравнение для хлора записывают именно так, поскольку окислителем является молекула хлора, состоящая из двух атомов, и каждый из этих атомов изменяет свою степень окисления от 0 до –1. Коэффициент 5 относится к молекуле хлора в левой части уравнения, а количество атомов хлора в правой части уравнения 5 × 2 = 10.
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 3. Восстановление оксида железа (II, III) алюминием. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления железа изменяется от +8/3 до 0, при этом три иона железа (поскольку в исходном оксиде их содержится именно три) присоединяют восемь электронов (3 × 8/3 = 8). Железо является окислителем.
Алюминий отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединенных и отданных электронов:
Электронное уравнение для алюминия записывают именно так, поскольку в состав оксида алюминия входят два атома алюминия. Таким образом, в левой части уравнения основной коэффициент перед оксидом железа (II, III) будет равен 3, а перед алюминием 4 × 2 = 8.
Количество атомов железа в правой части уравнения реакции составит 3 × 3 = 9. Количество молекул оксида алюминия будет равно 8/2 = 4. Окончательно получаем:
Проверяем баланс по кислороду. В левой части уравнения 3 × 4 = 12. В правой части уравнения 4 × 3 = 12. Таким образом, число атомов каждого элемента в отдельности в левой и в правой части химического уравнения равны между собой, и реакция уравнена правильно.
Этот пример наглядно показывает, что дробная степень окисления хотя и не имеет физического смысла, но позволяет правильно уравнять окислительно-восстановительную реакцию.
Очень часто окислительно-восстановительные реакции проходят в растворах в нейтральной, кислой или щелочной среде. В этом случае химические элементы, входящие в состав вещества, образующего среду реакции, свою степень окисления не меняют.
Пример 4. Окисление йодида натрия перманганатом калия в среде серной кислоты. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Атом марганца принимает пять электронов, изменяя свою степень окисления от +7 до +2. Перманганат калия является окислителем.
Два йодид-иона отдают два электрона, образуя молекулу I20. Йодид натрия является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Найденные коэффициенты подставим в уравнение реакции перед соответствующими формулами веществ в левой и правой частях.
Серная кислота является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет, но сульфат-анион связывает выделяющиеся в результате реакции катионы калия, натрия и марганца. Подсчитаем число сульфат-ионов в правой части. Оно равно 2 + 1 + 5 = 8. Следовательно, перед серной кислотой следует поставить коэффициент 8. Число атомов водорода в левой части уравнения равно 8 × 2 = 16. Отсюда вычисляем коэффициент для воды: 16/2 = 8.
Таким образом, уравнение реакции будет иметь вид:
Правильность баланса проверяем по кислороду. В левой части его 2 × 4 = 8 (перманганат калия); в правой — 8 × 1 = 8 (вода). Следовательно, уравнение составлено правильно.
Пример 5. Окисление сульфида калия манганатом калия в водной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Ион марганца принимает два электрона, изменяя свою степень окисления от +6 до +4. Манганат калия является окислителем.
Сульфид-ион отдаёт два электрона, образуя молекулу S0. Сульфид калия является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Основные коэффициенты в уравнении реакции равны единице:
Вода является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Гидроксид-ионы связывают выделяющиеся в результате реакции катионы калия. Таких катионов четыре (2 × 2), число атомов водорода также 4 (4 × 1), поэтому перед молекулой воды ставим коэффициент два (4/2 = 2):
Пример 6. Окисление аммиака хлоратом калия в щелочной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Хлор принимает шесть электронов, изменяя свою степень окисления от +5 до –1. Хлорат калия является окислителем.
Азот отдаёт восемь электронов, изменяя свою степень окисления от –3 до +5. Аммиак является восстановителем.
Составляем уравнение электронного баланса, уравниваем число присоединённых и отданных электронов введением множителей, сокращаем кратные коэффициенты:
Проставляем найденные основные коэффициенты в уравнение реакции:
Гидроксид калия является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Катионы калия связывают выделяющиеся в результате реакции нитрат-ионы. Таких анионов три. Следовательно, перед гидроксидом калия ставим коэффициент три:
Число атомов водорода в левой части уравнения равно девяти в аммиаке (3 × 3) = 9 и трём в гидроксиде калия (3 × 1), а их общее число 9 + 3 = 12. Следовательно, перед водой ставим коэффициент (12/2) = 6. Окончательно уравнение реакции будет иметь вид:
Убеждаемся ещё раз в правильности расстановки коэффициентов, сравнивая число атомов кислорода в левой и правой его частях. Оно равно 15.
Довольно часто одно и то же вещество одновременно является окислителем и создаёт среду реакции. Такие реакции характерны для концентрированной серной кислоты и азотной кислоты в любой концентрации. Кроме того, в подобные реакции, но в качестве восстановителя, вступают галогенводородные кислоты с сильными окислителями.
Пример 7. Окисление магния разбавленной азотной кислотой. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления азота изменяется от +5 до +1, при этом два атома азота присоединяют восемь электронов. Азотная кислота является окислителем.
Магний отдаёт два электрона, изменяя свою степень окисления от 0 до +2. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 4 × 2 = 8 нитрат-ионов, не изменивших свою степень окисления. Очевидно, что для этого в правую часть уравнения реакции следует добавить ещё 8 молекул HNO3. Тогда общее количество молекул азотной кислоты в правой части уравнения составит 2 + 8 = 10.
В этих молекулах содержатся 10 × 1 = 10 атомов водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Следовательно, перед молекулой воды следует подставить коэффициент 10/2 = 5, и уравнение окончательно будет иметь вид:
Окончательно проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части 10 × 3 = 30. В правой части (2 × 3) × 4 = 24 в нитрате магния, 1 в оксиде азота (I) и 5 × 1 = 5 в молекуле воды. Итого 24 + 1 + 5 = 30. Таким образом, реакция полностью уравнена.
Пример 8. Взаимодействие соляной кислоты с оксидом марганца (IV). Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления марганца изменяется от +4 до +2, при этом марганец присоединяет два электрона. Оксид марганца (IV) является окислителем.
Два хлорид-иона отдают два электрона, образуя молекулу Cl20, хлористый водород является восстановителем.
Составляем электронное уравнение и уравниваем число присоединённых и отданных электронов, сокращаем кратные коэффициенты:
При этом коэффициент 1 изначально относится к двум хлорид-ионам и к одной молекуле Cl2. Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 1 × 2 = 2 хлорид-иона, не изменивших свою степень окисления. Эти хлорид-ионы в окислительно-восстановительной реакции не участвовали. Очевидно, что для этого в правую часть уравнения реакции следует добавить 2 молекулы HCl. Тогда общее количество молекул HCl в правой части уравнения составит 2 + 2 = 4. В этих молекулах будет содержаться 4 × 1 = 4 атома водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Тогда перед молекулой воды следует подставить коэффициент 4/2 = 2, и уравнение в окончательном виде будет иметь вид:
Проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части оно составляет 1 × 2 = 2 в оксиде марганца (IV), а в правой части 2 × 1 = 2 в молекуле воды. Таким образом, реакция полностью уравнена.
В качестве окислителя могут выступать нейтральные атомы и молекулы, положительно заряженные ионы металлов, сложные ионы и молекулы, содержащие атомы металлов и неметаллов в состоянии положительной степени окисления и др.
Ниже приведены сведения о некоторых наиболее распространенных окислителях, имеющих важное практическое значение.
Кислород. Сильный окислитель, окислительная способность значительно возрастает при нагревании. Кислород взаимодействует непосредственно с большинством простых веществ, кроме галогенов, благородных металлов Ag, Au, Pt и благородных газов, с образованием оксидов:
Взаимодействие натрия с кислородом приводит к пероксиду натрия:
Более активные щелочные металлы (K, Rb, Cs) при взаимодействии с кислородом дают надпероксиды типа ЭО2:
В своих соединениях кислород, как правило, проявляет степень окисления –2. Применяется кислород в химической промышленности, в различных производственных процессах в металлургической промышленности, для получения высоких температур. С участием кислорода идут многочисленные чрезвычайно важные жизненные процессы: дыхание, окисление аминокислот, жиров, углеводов. Только немногие живые организмы, называемые анаэробными, могут обходиться без кислорода.
Реакции, иллюстрирующие окислительные свойства кислорода при его взаимодействии с различными неорганическими веществами, приведены в уроке 14.
Озон. Обладает ещё большей по сравнению с кислородом окислительной способностью. Озон окисляет все металлы, за исключением золота, платины и некоторых других, при этом, как правило, образуются соответствующие высшие оксиды элементов, реже — пероксиды и озониды, например:
Озон окисляет оксиды элементов с промежуточной степенью окисления в высшие оксиды.
Перманганат калия. Является сильным окислителем, широко применяется в лабораторной практике. Характер восстановления перманганата калия зависит от среды, в которой протекает реакция. В кислой среде перманганат калия восстанавливается до солей Mn2+, в нейтральной или слабощелочной — до MnO2, а в сильнощелочной он переходит в манганат-ион MnO42–. Данные переходы описываются следующими уравнениями
Перманганат калия способен окислять сульфиды в сульфаты, нитриты в нитраты, бромиды и йодиды — до брома и йода, соляную кислоту до хлора и т. д.:
Хромат и бихромат калия. Эти соединения широко применяют в качестве окислителей в неорганических и органических синтезах. Взаимные переходы хромат- и бихромат-ионов очень легко протекают в растворах, что можно описать следующим уравнением обратимой реакции:
Соединения хрома (VI) — сильные окислители. В окислительно-восстановительных процессах они переходят в производные Cr (III). В нейтральной среде образуется гидроксид хрома (III), например:
В кислой среде образуются ионы Cr3+:
В щелочной — производные анионного комплекса [Cr(OH)6]3–:
В качестве восстановителя могут выступать нейтральные атомы, отрицательно заряженные ионы неметаллов, положительно заряженные ионы металлов в низшей степени окисления, сложные ионы и молекулы, содержащие атомы в промежуточной степени окисления, электрический ток на катоде и др.
Ниже приведены сведения о некоторых наиболее распространённых восстановителях, имеющих важное практическое значение.
Углерод. Углерод широко применяют в качестве восстановителя в неорганических синтезах. При этом в качестве продуктов окисления может образовываться углекислый газ, или оксид углерода (II). При восстановлении оксидов металлов могут образовываться свободные металлы, реже — карбиды металлов.
Восстановительные свойства углерод проявляет также в реакции получения водяного газа:
Полученную смесь водорода и оксида углерода (II) широко применяют для синтеза органических соединений.
Оксид углерода (II). Широко применяют в металлургии при восстановлении металлов из их оксидов, например:
Водород. Широко применяют в качестве восстановителя в неорганических синтезах (водородотермия) для получения чистого вольфрама, молибдена, галлия, германия и т. д.:
Тренировочные задания
Используя метод электронного баланса, расставьте коэффициенты, определите окислитель и восстановитель в уравнении реакции, схема которой:
1. Al + H2O + KNO3 + KOH → K[Al(OH)4] + NH3↑.
2. KNO3 + Al → KAlO2 + Al2O3 + N2.
3. Na2O2 + H2SO4 + KMnO4 → O2↑ + MnSO4 + Na2SO4 + K2SO4 + H2O.
4. NaCl + H2SO4 + MnO2 → Cl2 + MnSO4 + Na2SO4 + H2O.
5. NaCl + H2SO4 + KMnO4 → Cl2 + MnSO4 + Na2SO4 + K2SO4 + H2O.
6. KNO2 + H2SO4 + MnO2 → MnSO4 + KNO + H2O.
7. KI + H2SO4 + KMnO4 → I2 + MnSO4 + K2SO4 + H2O.
8. KI + K2Cr2O7 + H2SO4 → I2 + Cr2(SO4)3 + K2SO4 + H2O.
9. C + K2Cr2O7 + H2SO4 → CO2 + Cr2(SO4)3 + K2SO4 + H2O.
10. PbO2 + HNO3 + KI → Pb(NO3)2 + I2 + KNO3 + H2O.
11. PbO2 + HNO3 + Mn(NO3)2 → Pb(NO3)2 + HMnO4 + H2O.
12. NaNO2 + KMnO4 + H2SO4 → NaNO3 + MnSO4 + K2SO4 + H2O.
13. KNO2 + KMnO4 + H2SO4 → KNO3 + MnSO4 + K2SO4 + H2O.
14. KNO2 + K2Cr2O7 + H2SO4 → KNO3 + Cr2(SO4)3 + K2SO4 + H2O.
15. KNO2 + KI + H2SO4 → NO + I2 + K2SO4 + H2O.
16. KNO2 + FeSO4 + H2SO4 → NO + Fe2(SO4)3 + K2SO4 + H2O.
17. Ca3(PO4)2 + C + SiO2 → CaSiO3 + P + CO.
18. Sb + HNO3 → Sb2O5 + NO2 + H2O.
19. H2O2 + H2SO4 + KMnO4 → MnSO4 + O2 + H2O + K2SO4.
20. S + HNO3 → H2SO4 + NO2 + H2O.
21. H2S + HNO3 → H2SO4 + NO2 + H2O.
22. H2S + KMnO4 → MnO2 + S + H2O + KOH.
23. H2S + K2Cr2O7 + H2SO4 → S + Cr2(SO4)3 + K2SO4 + H2O.
24. KMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 + H2O.
25. KMnO4 + Na2SO3 + H2O → MnO2 + Na2SO4 + KOH.
26. KMnO4 + Na2SO3 + KOH → K2MnO4 + Na2SO4 + H2O.
27. K2Cr2O7 + K2SO3 + H2SO4 → Cr2(SO4)3 + K2SO4 + H2O.
28. H2SO4 + C → SO2 + CO2 + H2O.
29. H2SO4 + Zn → ZnSO4 + H2S + H2O.
30. H2SO4 + KBr → SO2 + Br2 + KHSO4 + H2O.
31. H2SO4 + KI → H2S + I2 + K2SO4 + H2O.
32. PbO2 + HCl → PbCl2 + Cl2 + H2O.
33. K2Cr2O7 + HCl → CrCl3 + Cl2 + KCl + H2O.
34. KMnO4 + HCl → MnCl2 + Cl2 + KCl + H2O.
35. KClO3 + HCl → KCl + Cl2 + H2O.
36. HClO3 + FeSO4 + H2SO4 → Fe2(SO4)3 + HCl + H2O.
37. NaBrO3 + NaBr + H2SO4 → Br2 + Na2SO4 + H2O.
38. HNO3 + I2 → HIO3 + NO2 + H2O.
39. HNO3 + I2 → HIO3 + NO + H2O.
40. H2SO4 + HI → I2 + H2S + S + H2O.
41. Fe2(SO4)3 + HI → FeSO4 + I2 + H2SO4.
42. HIO3 + FeSO4 + H2SO4 → Fe2(SO4)3 + I2 + H2O.
43. NaIO3 + NaI + H2SO4 → I2 + Na2SO4 + H2O.
44. KMnO4 + Cu2O + H2SO4 → MnSO4 + CuSO4 + K2SO4 + H2O.
45. HNO3 + Cu2S → CuSO4 + Cu(NO3)2 + NO2 + H2O.
46. H2SO4 + Cu2S → CuSO4 + SO2 + H2O.
47. Ag + HNO3 → AgNO3 + NO + H2O.
48. Zn + HNO3 → Zn(NO3)2 + N2O + H2O.
49. PH3 + KMnO4 + H2SO4 → H3PO4 + MnSO4 + K2SO4 + H2O.
50. FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O.
51. H2S + KMnO4 + H2SO4 → S + MnSO4 + K2SO4 + H2O.
52. Ca3P2 + KMnO4 + H2SO4 → CaSO4 + H3PO4 + MnSO4 + K2SO4 + H2O.