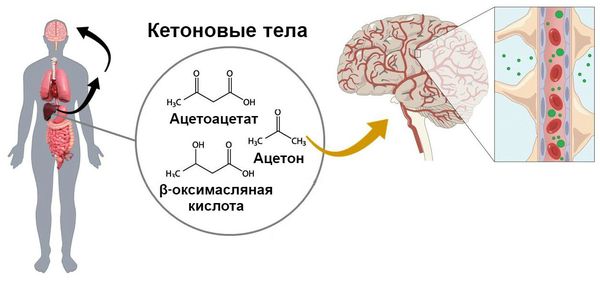
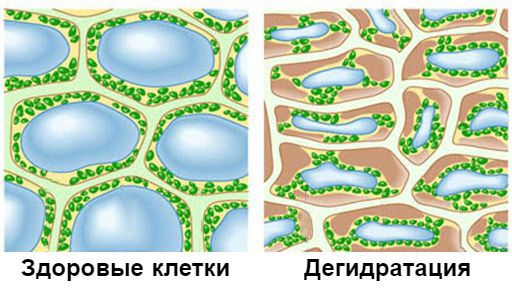
Последствия и причины передозировки инсулином
Последствия передозировки инсулина, cмepтельная доза, первая помощь
Инсулин – это пептидный гормон, который участвует в углеводном метаболизме и предназначен для нормализации уровня глюкозы в крови. Инъекции препаратов гормона используются диабетиками для снижения сахара. Если введение средства проводилось правильно в адекватном количестве, то состояние пациента поддерживается на практически нормальном уровне. Превышение дозы при инсулинотерапии является опасным состоянием. Поэтому если возникает передозировка инсулина, последствия могут быть крайне тяжелыми.
Какое количество инсулина необходимо для передозировки?
Для здорового человека, который не страдает сахарным диабетом, безопасной является доза до 4МЕ. Учитывая анаболические свойства пептида, бодибилдеры превышают это количество. Обычно они используют до 20 МЕ/сутки. Доза у диабетика колeблется от 20 до 50 МЕ за сутки. Все, что выше – может вызвать признаки передозировки. Смертельная доза препаратов инсулина для диабетиков разнообразна. Для большинства из них летальный исход возникает, когда было введено 100 МЕ гормона. Но известны случаи, когда пациенты приняли 3000 МЕ лекарства, и для них это было не cмepтельно.
Внимание! Адекватное количество лекарства подбирается эндокринологом индивидуально для каждого пациента.
Передозировка может случиться по разным причинам. Главным этиологическим фактором является неправильный подбор дозы препарата. Также встречаются такие случаи:
- Врачебные ошибки (введение средства человеку, не страдающему заболеванием).
- Чрезмерные физические занятия без употрeбления углеводных продуктов.
- Неправильная техника инъекции (не подкожно, а внутримышечно).
- Применение нового препарата.
- Использование другого вида шприца для уколов.
- Игнорирование приема еды после инъекции.
- Неправильное использование пациентом препаратов инсулина медленного и быстрого действия.
Кроме того, восприимчивость тканей к молекулам инсулина увеличивается при некоторых физиологических и патологических состояниях. Такое наблюдается при вынашивании ребенка во время первого триместра. Среди патологических состояний выделяют жировую дистрофию печени (стеатоз) и хроническую недостаточность почек.
Также ухудшение состояния возможно при несоблюдении больным рекомендаций доктора относительно употрeбления алкогольных напитков. Если отказать себе пациент не может, то нужно учитывать некоторые важные принципы. Прежде всего, отдавать предпочтение необходимо легким спиртным напиткам. Также важно понимать, что до и после выпивки нужно включить в рацион блюдо, которое содержит медленные углеводы. Дозу инсулина перед употрeблением алкоголя уменьшать по совету с доктором.
Признаки передозировки
Отравление дозой инсулина проявляется понижением показателя глюкозы. Гипогликемия -это состояние, когда уровень сахара снижается до 3,3ммоль/л. Продолжительность развития клинических проявлений зависит от вида применяемого средства. Если пациент вводил инсулин быстрого действия, то и симптоматика возникает спустя краткий промежуток времени.
Первая стадия передозировки характеризуется выраженным чувством голода. Также есть слабость, тахикардия и головная боль. Пациент становится раздражительным, наблюдается эмоциональная лабильность.
При прогрессировании состояния больной будет жаловаться на повышение потливости и саливации (слюноотделения). Слабость и голод будут приобретать большую интенсивность. Появится тремор рук (дрожание), онемение пальцев, расширение зрачков и падение остроты зрения. При осмотре будет определяться бледность пациента.
Дальнейшие патологические изменения соответствуют третьей стадии развития гипогликемической комы. При этом наблюдается значительное ухудшение самочувствия: пациент не способен двигаться, тремор конечностей и частота сердечных сокращений нарастают, потоотделение усиливается. Также это сопровождается психомоторным возбуждением, головокружением, падением артериального давления, потерей сознания и судорогами.
Гипогликемия при четвертой стадии характеризуется снижением уровня глюкозы на 5 ммоль/л от исходного показателя. При этом больной в бессознательном состоянии, внешне выглядит бледным. Кроме того, тахикардия переходит в брадикардию (замедление сокращений сердца), отсутствует зрачковый рефлекс. В таком случае при передозировке инсулином возможна cмepть из-за угнетения жизненно важных систем организма – нервной, дыхательной и кровеносной.
Также возможна хроническая передозировка. Она спровоцирована повышенным синтезом контринсуллярных гормонов – соматотропина, глюкагона, тироксина, адреналина. Такое состояние называют «синдромом Сомоджи».
Такое состояние проявляется тяжелым течением основного заболевания – сахарного диабета. Пациент отмечает повышение аппетита, стремительный набор веса при глюкозурии (повышении концентрации глюкозы в моче). При клинических исследованиях определяются ацетонурия, склонность к развитию кетоацидоза. Измерение уровня сахара в крови указывает на колебания показателя на протяжении суток.
Первая помощь при передозировке инсулином
Неотложной помощь зависит от степени тяжести состояния. Если развитие гипогликемии еще на первой стадии, то необходимо перopaльно принять немного сладкого или мучного. Это может быть 3-4 кусочка сахара, шоколада, ломтик хлеба или просто чай с медом.
Внимание! После употрeбления углеводов требуется срочно вызвать скорую помощь для предотвращения ухудшения состояния больного в дальнейшем.
Больному, который находится без сознания, или не может глотать, требуются внутривенные вливания глюкозы. Это делается с помощью капельницы, вводится до 80 мл 40%-го раствора глюкозы. После этой процедуры можно сделать инъекцию контринсулярного гормона, например 1 миллилитр глюкагона внутримышечно или подкожно, а также адреналина гидрохлорида в дозе 0,1% 0,5-1 мл. Если введение препаратов не было эффективно, и состояние больного не изменяется, процедypa повторяется в количестве глюкозы 60 мл.
Антидотом, чтобы не допустить cмepть от инсулина, является глюкоза. Ее необходимо ввести во время оказания немедленной помощи диабетику, если его состояние тяжелое и он не способен самостоятельно ее принять. При гипогликемии легкой степени, что соответствует первой и второй стадии развития патологического понижения сахара, это может сделать пациент, употребив сладкий чай или кусочек хлеба.
Диабетики, страдающие инсулинозависимым типом заболевания, должны всегда иметь при себе глюкометр. Также необходимо брать с собой фруктовые соки, несколько шоколадных конфет, чтобы при первых проявлениях гипогликемии нормализовать состояние.
Когда необходима медицинская помощь?
Пациенты, у которых патология еще на первых стадиях развития, могу справиться самостоятельно. Но все же, после приема антидота рекомендуется обратиться к эндокринологу. Он поможет определить причину возникновения патологии и, если нужно, скорректирует дозу лекарства.
Если у диабетика наблюдается третья или четвертая стадия развития комы, то требуется немедленная госпитализация. Оказание необходимых мер в виде введения глюкозы с помощью капельниц может спасти больного. Также возможно применение гормонов, у которых действие направлено на снижение концентрации инсулина. Например, глюкагон, адреналин. Если состояние усугубилось до острого инсулинового коматоза, то доктора направят лечение на коррекцию расстройств в организме – нарушения дыхания, кровоснабжения органов.
Пациенту с избытком гормона необходим контроль врачей, чтобы не допустить повторения патологии. Очень важно оставаться под присмотром тем больным, у которых повышена чувствительность клеток к гормону. Это беременные женщины (особенно первый три месяца вынашивания), пациенты с почечной недостаточностью хронического течения. Также восприимчивость к инсулину растет у пациентов со стеатозом печени, когда орган инфильтрирован жировой тканью и не функционирует в полном объеме.
Возможные осложнения
Последствия отравления гормоном отличаются в зависимости от степени передозировки. Если у пациента наблюдались признаки легкой гипогликемии, то осложнения обычно не возникают. Опасность при частых понижениях глюкозы кроется в синдроме Сомоджи. В таком случае нарушается контроль диабета, и самочувствие пациента чаще ухудшается.
Развитие более тяжелых состояний грозит серьезными последствиями. Отравление может спровоцировать неврологические нарушения. Среди расстройств нервной системы выделяют:
- отек головного мозга;
- менингеальные проявления (Брудзинского, Кернига);
- угнетение когнитивных способностей человека (памяти);
- деменция.
Неврологическая симптоматика обусловлена расстройством трофики мозговых структур из-за снижения содержания сахара в крови. Кроме того, возможны психические нарушения. Редко в виде осложнения при тяжелой передозировке возникает эпилептический припадок. У больных, которые страдают расстройствами сердечно-сосудистой системы могут развиться кровоизлияние в сетчатку, инфаркт миокарда или инсульт.
Заключение
Диабетики часто интересуются, можно ли умереть от инсулина. Умереть от передозировки возможно, если не соблюдать рекомендации доктора и игнорировать первичные проявления патологии.
Своевременное обращение к доктору должно быть главной целью пациента при развитии гипогликемии. подробную информацию о состоянии можно получить, просмотрев видеоролик:
Ошибочка вышла: передозировка инсулина и ее последствия
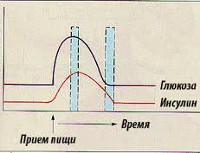
В организм человека при приеме пищи поступают белки, жиры и углеводы. Для расщепления углеводов щитовидная железа выpaбатывает инсулин.
При сахарном диабете 2 типа организм не справляется самостоятельно с выработкой естественного инсулина, и поэтому, порой им приходится стимулировать создание инсулина с помощью медикаментов.
При диабете 1 типа поджелудочная вообще не выpaбатывает инсулин, поэтому углеводы не расщепляются, тогда применяется инсулинотерапия (инъекции или помпа – устройство, которое самостоятельно измеряет уровень сахара в крови и впрыскивает инсулин).
Взаимодействие с алкоголем
Углеводы играют огромную роль в организме человека, они носят и строительную, и питательную функции, поэтому очень важно, чтобы при поступлении их в организм, они выполняли эти роли.
Это возможно лишь тогда, когда инсулин расщепляет их на полезные элементы.
В ином случае, углеводы вызывают загустение крови, образуются тромбы, и многие органы не имеют возможности питания, а значит, и здорового функционирования.
При диабете больным рекомендуется отказаться от вредных привычек, в особенности от употрeбления алкоголя.
Это правило особо значимо для больных, перешедших на инсулинотерапию.
Дело в том, что алкоголь значительно снижает уровень сахара в крови, поэтому привычная доза не применима, ее надо корректировать. В ином случае, снижение сахара доведет до состояния гипогликемии (пониженного содержания сахара в крови), а это может стать причиной и гипогликемической комы, и даже летального исхода (если не обратиться вовремя за квалифицированной медицинской помощью).
Лишь в том случае, когда Вы уже достаточно изучили свой организм и изменения уровня сахара в нем, Вы можете позволить себе алкоголь, но не забывайте при этом о понятии нормы, потому что до сих не выяснено точное влияние алкоголя на организм. Никак нельзя точно сказать, насколько упадет сахар.
Основные правила употрeбления алкоголя при инсулинозависимой диете:
- Алкоголь не чаще 2-х раз в неделю, но не два дня подряд;
- Чтоб избежать резкого падения сахара в организме, стоит сократить дозу инсулина;
- Нельзя пить на голодный желудок. Лучше всего совмещать еду и алкоголь;
- Безопасная доза алкоголя для диабетика составляет 30 гр. чистого спирта в день. Это 50 мл водки, 150 мл сухого вина, 350 мл светлого пива.
В организме человека, не страдающего диабетом, происходит саморегуляция гормонов, в том числе и инсулина.
Однако, из-за неправильно прописанных медикаментов врачами, искусственно введенный инсулин может попасть в организм здорового человека.
А также, нередко, люди, стремящиеся быстро повысить мышечную массу, намеренно вкалывают инсулин. Такие действия могут привести к резкому понижению сахара в крови.
Встречаются случаи гипогликемии и у эмоционально неустойчивых людей, или страдающих булимией, или анорексией. Это вызывает гормональные сбои, а так как инсулин — это тоже гормон, то он может выpaбатываться организмом не в тех количествах, которые необходимы для здорового функционирования.
Если при наступлении гипогликемии вовремя не повысить сахар в организме и не обратиться за профессиональной помощью врачей, возможен летальный исход.
Читать еще: Что такое токсическая энцефалопатия – симптомы, лечение
Чаще всего он наступает от аритмии, инсульта или инфаркта миокарда. Гораздо реже, от cмepти мозговых клеток, потому что мозг должен голодать несколько часов, чтобы это произошло. А это возможно лишь при наступлении гипогликемии во время сна.
У диабетика:
Спровоцировать передозировку у больного СД могут:
- Физические упражнения, после которых вы принимаете привычную дозу инсулина (необходимо уменьшить ее);
- Алкоголь на голодный желудок или в большом количестве (при употрeблении алкогольных напитков также стоит снизить дозу инсулина);
- Недостаточное питание;
- Неправильно рассчитанные Хлебные Единицы (ХЕ);
- Ошибочно принятая доза инсулина;
Также, существует понятие «медовый месяц» — ремиссия при сахарном диабете, это вызвано улучшением функционирование оставшихся бета-клеток поджелудочной железы. Если диабетик не сразу обнаруживает это, то при принятии стандартной дозы инсулина, возможна передозировка.
Основными признаками передозировки являются:
- Слабость;
- Головные боли;
- Резко подступающее чувство стpaxa;
- Чувство голода;
- Потерянность в прострaнcтве;
- Потемнения в глазах;
- Нехарактерно возбужденное, даже агрессивное поведение;
- Повышенное артериальное давление;
- Нарушение координации.
Заметить подобные изменения в человеке несложно, скорее всего, он и сам поймет, что происходит.
Если больной смог оказать себе первую помощь вовремя и грамотно, то в ближайшее время уровень сахара должен нормализоваться. Однако, больному в любом случае необходимо обратиться к лечащему врачу для коррекции дозы.
В случае, когда гипогликемия не проходит, то необходимо обратиться за профессиональной помощью.
Существуют 4 стадии состояния, вызванные передозировкой инсулина в организме:
Легкая: проявляются симптомы, указанные выше. Начинается гипоксия клеток коры головного мозга;
Средняя: поражение гипоталамо-гипофизарной области мозга. Ухудшение состояния, повышается потливость;
Тяжелая: разрушается функциональная активность среднего мозга. Начинаются судороги, зрачки расширяются — поведение человека напоминает состояние при эпилептическом припадке;
Острая (cмepтельная): человек теряет сознание, пульс и сердцебиение учащены. Если до сих пор ничего не предпринято, то возможен отек головного мозга и cмepтельный исход. Нарушение работы головного мозга может привести к развитию слабоумия; для пожилых людей это опасно инсультом, инфарктом или кровоизлиянием в сетчатку глаза.
Как эффективно и быстро повысить уровень сахара
Самое быстродействующее средство — это инъекция глюкозы, которая мгновенно поступит в кровь и сможет поднять уровень сахара. Если такой возможности нет, то необходимо употребить продукты, которые быстро растворяются, расщепляются в крови. Например, кусок сахара, сахар в стиках или сладкие напитки (сладкая вода, сладкий чай и проч.).
Хроническая форма
У некоторых больных диабетом наблюдается хроническая передозировка, иначе синдром хронической передозировки инсулина (СХПИ), феномен Сомоджи — это постоянно низкий уровень сахара в крови, что вызвано большим количеством инсулина. Также она возникает при гормональном сбое в организме.
Симптомы хронической гипогликемии такие же, как и у спонтанной — головная боль, слабость, дезориентация.
Частое нахождение в таком состоянии может привести к массовой гибели клеток головного мозга.
При синдроме Сомоджи сахар ведет себя по-разному — то резко повышается, то падает, то долгое время не меняет значений, несмотря на инъекции и принятые углеводы.
При сахарном диабете опасно частое нахождение в таком состоянии. Постепенно гипогликемия ощущается слабее, и она протекает скрыто. Человек становится замкнутым, в вечно плохом настроении. Лечение таких случаев протекает тяжело.
Расчет дозировки
При расчете дозы инсулина нужно учитывать, что важнейшим пунктом для исполнения является соблюдение низко-углеводной диеты. Если больной ее не соблюдает, то рассчитать определенную дозу будет невозможно. Доза инсулина зависит от количества углеводов в организме. Если постоянно употрeблять разное количество, то и доза инсулина будет меняться.
Основные правила расчета:
- Правило соблюдения низко-углеводной диеты. Необходимо уменьшить в своем рационе те продукты, которые содержат углеводы, к ним относятся: все мучные изделия; крупы, причем светлые крупы более калорийны, чем темные; фрукты; любые продукты, изготовленные не на сахарозаменителях, а на сахаре.
- Важно часто измерять уровень сахара с помощью глюкометра на первых порах заболевания. Изучая, что приводит к изменению уровня сахара крови, Вы сможете вывести зависимость, которой можно руководствоваться в будущем;
- Учитывайте, что после физических упражнений уровень сахара также понижается. Надо изучить и этот процесс для правильной коррекции дозы после физических нагрузок;
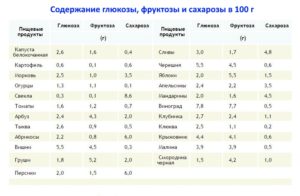
Существует особая система измерения углеводов/калорий, система хлебных единиц (ХЕ). 1 ХЕ равна примерно 10 ед глюкозы. Существуют специальные таблицы, в которых прописано, сколько глюкозы содержится в разных продуктах;
Общепринятые дозировки:
- При только что обнаруженном инсулине на 1 кг веса необходимо 0,5 ед инсулина;
- Диабет, который протекает без осложнений год и больше — 0,6 ед;
- При диабете, протекающем с осложнениями — 0,7;
- Декомпенсированный диабет требует 0,8 ед;
- С осложненным кетоацидозом — 0,9;
- Во время беременности на поздних сроках — 1 ед на 1 кг веса.
Повышают уровень сахара в основном углеводы, белки и жиры играют совсем незначительную роль, так что часто их и вовсе не учитывают;
И помните, что действие инсулина зависит от времени суток — утром он менее эффективен, чем в обед или вечером.
Передозировка инсулина может вызвать самые плачевные последствия — cмepть клеток органов, это вызывает нарушение правильного функционирования организма человека. Если приступы частые, то однажды гипогликемия может стать причиной комы или даже летального исхода.
При передозировке инсулина возможно развитие следующих патологических процессов:
Очень важно соблюдать основные правила недопущения подобного:
- Периодический контроль уровня сахара;
- Иметь при себе глюкозу или продукты, с высоким содержанием сахара (мед, карамель, сладкая вода, сахар);
- Регулированное употрeбление алкоголя и не злоупотрeбление прочими вредными привычками;
- Знакомые и близкие люди должны быть в курсе Вашего заболевания и иметь понимание, что предпринять в случае передозировки.
Полезное видео
Неправильная дозировка и халатное отношение к собственному здоровью могут привести человека к необратимым последствиям:
Совсем несложно контролировать уровень сахара в крови. Нужно лишь иметь всегда под рукой глюкометр, не экономить на тест-полосках, ведь речь идет о Вашем здоровье; придерживаться прописанной врачом диеты и соблюдать распорядок дня.
Передозировка инсулином
Инсулин – это гормон, который регулирует углеводный обмен в организме человека и выpaбатывается клетками Лангерганса поджелудочной железы. С его помощью ткани усваивают глюкозу, вещество, служащее источником энергии в организме. При сахарном диабете I типа (инсулинозависимом) собственный инсулин поджелудочной железой не выpaбатывается, поэтому жизненно важно вводить его извне. Препараты инсулина содержат синтезированный гормон. Их регулярные инъекции – основа поддерживающей терапии сахарного диабета I типа.
Инсулин обладает и анаболическим действием, поэтому его используют и в терапии некоторых других заболеваний, также он применяется бодибилдерами для увеличения мышечной массы.
Какое количество инсулина необходимо для передозировки?
Для здорового (т. е. не страдающего диабетом) взрослого человека безопасной дозой инсулина является 2–4 ЕД.
Нередко бодибилдеры, начиная с безопасной, постепенно увеличивают дозу, доводя ее до 20 ЕД.
При сахарном диабете доза инсулина подбирается эндокринологом индивидуально, с учетом концентрации глюкозы в сыворотке крови и наличия сахара в моче. Средняя терапевтическая доза при сахарном диабете находится в диапазоне 20–40 ЕД, в тяжелых случаях или при развитии осложнений (гипергликемическая кома) она может быть увеличена, и значительно.
Основными причинами передозировки инсулина являются:
- неправильно подобранная доза инсулинсодержащего препарата;
- ошибки при проведении инъекции, которые чаще всего наблюдаются при смене препарата или использовании нового типа шприцов;
- внутримышечное (вместо подкожного) введение;
- пропуск приема пищи после инъекции;
- значительные физические нагрузки при недостаточном поступлении углеводов после инъекции.
Некоторые состояния повышают чувствительность организма к действию инсулина. К ним относятся:
- жировая дистрофия печени;
- хроническая почечная недостаточность;
- первый триместр беременности;
- состояние алкогольного опьянения (в т. ч. и легкой степени).
В этих случаях даже введение привычной дозы лекарственного препарата, подобранной врачом, может стать причиной развития симптомов передозировки инсулином.
Признаки передозировки
При передозировке инсулина в крови резко снижается содержание глюкозы. Если этот показатель опускается ниже 3,3 ммоль/л, говорят о развитии гипогликемии.
Если передозировка возникла при применении инсулина короткого действия, ее признаки начинают проявляться уже через несколько минут после инъекции. Если использовался препарат инсулина длительного действия (депо-инсулин), то симптомы гипогликемии появляются позже и нарастают медленнее.
Заподозрить передозировку инсулина можно при наличии следующих симптомов, возникающих спустя некоторое время после инъекции:
- нарастающая общая слабость;
- тахикардия;
- головная боль;
- сильное чувство голода.
Если в этот момент не предпринять необходимых мер, состояние больного начнет быстро ухудшаться, присоединятся и другие симптомы:
- сильная потливость;
- тремор;
- онемение пальцев рук;
- бледность кожных покровов;
- гиперсаливация;
- расширение зрачков;
- нестерпимый голод;
- преходящие нарушения зрительной функции;
- нарушение способности к самостоятельному передвижению;
- нервное возбуждение или, наоборот, заторможенность;
- затуманивание сознания;
- клонико-тонические судороги.
Самое тяжелое проявление передозировки инсулином – развитие гипогликемической комы, несущей угрозу жизни.
Передозировка инсулином может быть не только острой, но и хронической. Развитие последней связано с проведением длительной гормонозаместительной терапии сахарного диабета. После введения инсулина, даже в правильно подобранной дозировке, у больного на некоторое время снижается уровень глюкозы в крови. Организм стремится компенсировать это увеличением синтеза глюкагона, кортикостероидов и адреналина – гормонов, повышающих концентрацию глюкозы.
Признаки формирования хронической передозировки инсулином:
- постоянно повышенный аппетит;
- повышение массы тела;
- появление в моче ацетона;
- наличие в моче сахара;
- частые случаи развития кетоацидоза;
- резкие скачки уровня глюкозы в крови в течение суток;
- гипогликемия, периодически возникающая в течение дня;
- переход сахарного диабета в тяжелую форму.
Нарушения углеводного обмена, связанные с хронической передозировкой инсулина, приводят к тому, что в утренние часы у пациентов с сахарным диабетом I типа возникает гипергликемия, а в дневные часы уровень глюкозы в крови снижается и развивается гипогликемия.
Первая помощь при передозировке инсулином
При передозировке инсулином, особенно короткого действия, первая помощь должна быть оказана незамедлительно. Она предельно проста: больному следует выпить сладкий чай, съесть конфету, ложку варенья или кусочек сахара. Если его состояние не улучшается в течение 3-5 минут, прием пищи, содержащей быстрые углеводы, следует повторить.
Поскольку при передозировке инсулином происходит резкое снижение концентрации глюкозы в крови, в качестве антидота используют гипертонические (20–40%) растворы глюкозы.
Читать еще: Насколько полезно или вредно использование маргарина в выпечке?
Когда необходима медицинская помощь?
Если при передозировке инсулином оказание первой помощи привело к быстрому улучшению состояния, необходимости в экстренной медицинской помощи нет. Однако больному в ближайшее время следует обязательно посетить лечащего врача для коррекции дозы и кратности введения инсулина.
В тех случаях, когда передозировка инсулином протекает тяжело и прием углеводной пищи не выводит пациента из состояния гипогликемии, необходимо срочно вызвать бригаду скорой помощи.
Лечение пациентов с передозировкой инсулином проводится в отделении эндокринологии. При развитии гипогликемической комы – в отделении реанимации и интенсивной терапии.
В стационаре больным в срочном порядке определяют уровень глюкозы в крови и некоторые другие биохимические показатели. Терапию начинают с внутривенного введения 20–40% растворов глюкозы. При необходимости внутримышечно вводят глюкагон.
При развитии комы проводится коррекция нарушенных функций жизненно важных органов.
Возможные осложнения
Незначительная передозировка инсулином не представляет опасности для жизни и здоровья, легкие степени гипогликемии изредка случаются практически у всех больных сахарным диабетом I типа. Однако если гипогликемия возникает регулярно, то следует заподозрить формирование хронической передозировки инсулином, способной утяжелить течение основного заболевания.
Тяжелая передозировка инсулином может привести к развитию выраженных неврологических нарушений:
- менингеальные симптомы;
- отек головного мозга;
- деменция (нарушение умственной деятельности с формированием слабоумия).
Гипогликемия особенно опасна для людей пожилого возраста, а также тех, кто страдает заболеваниями сердечно-сосудистой системы. У пациентов этих категорий она может осложниться инсультом, инфарктом миокарда, кровоизлиянием в сетчатую оболочку глаза.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
Средняя продолжительность жизни левшей меньше, чем правшей.
Если улыбаться всего два раза в день – можно понизить кровяное давление и снизить риск возникновения инфарктов и инсультов.
Кровь человека «бегает» по сосудам под огромным давлением и при нарушении их целостности способна выстрелить на расстояние до 10 метров.
74-летний житель Австралии Джеймс Харрисон становился донором крови около 1000 раз. У него редкая группа крови, антитела которой помогают выжить новорожденным с тяжелой формой анемии. Таким образом, австралиец спас около двух миллионов детей.
Согласно исследованиям, женщины, выпивающие несколько стаканов пива или вина в неделю, имеют повышенный риск заболеть раком гpyди.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его «мотор» остановился на 4 часа после того как рыбак заблyдился и заснул в снегу.
Первый вибратор изобрели в 19 веке. Работал он на паровом двигателе и предназначался для лечения женской истерии.
Существуют очень любопытные медицинские синдромы, например, навязчивое заглатывание предметов. В желудке одной пациентки, страдающей от этой мании, было обнаружено 2500 инородных предметов.
При регулярном посещении солярия шанс заболеть раком кожи увеличивается на 60%.
Вес человеческого мозга составляет около 2% от всей массы тела, однако потрeбляет он около 20% кислорода, поступающего в кровь. Этот факт делает человеческий мозг чрезвычайно восприимчивым к повреждениям, вызванным нехваткой кислорода.
Для того чтобы сказать даже самые короткие и простые слова, мы задействуем 72 мышцы.
Согласно мнению многих ученых, витаминные комплексы практически бесполезны для человека.
В Великобритании есть закон, согласно которому хирург может отказаться делать пациенту операцию, если он курит или имеет избыточный вес. Человек должен отказаться от вредных привычек, и тогда, возможно, ему не потребуется оперативное вмешательство.
В четырех дольках темного шоколада содержится порядка двухсот калорий. Так что если не хотите поправиться, лучше не есть больше двух долек в сутки.
Образованный человек меньше подвержен заболеваниям мозга. Интеллектуальная активность способствует образованию дополнительной ткани, компенсирующей заболевшую.
Связки – это особые образования, состоящие из соединительной ткани. Их основная функция заключается в удерживании сустава и одновременном обеспечении его подвиж.
Причины возникновения и лечение передозировки инсулина
Диабетикам необходимо ежедневно вводить определенную дозировку инсулина, чтобы поддерживать нормальную жизнедеятельность. Именно поэтому такая категория пациентов чаще других сталкивается с передозировкой инсулина, последствия которой могут быть крайне нeблагоприятными.
Значение инсулинового гормона
На инсулин возложены важнейшие функции, связанные с регулированием сахара в кровотоке. Гормон принимает участие в процессах сохранения энергии, а также преобразует и трaнcпортирует поступающий сахар в клеточные структуры. Не последнее значение гормон имеет и в аминокислотном производстве, а также дальнейших процессах преобразования данных кислот.
У каждого пациента свое содержание инсулинового гормона, нормы которого определены специалистами для всех возрастных категорий. Если же происходит изменение нормальных показателей, то начинаются разного рода расстройства метаболической сферы и прочие нарушения, способные привести к опасным последствиям. Передозировка инсулина влияет на многие процессы в организме, потому как подобный гормональный элемент:
- Улучшает процессы белкового синтеза;
- Способствует сохранению молекулярного структурного строения белковых веществ;
- Участвует в гликогеновом синтезе, эти вещества помогают сохранить глюкозу в мышечных тканях;
- Сохраняет аминокислотные соединения в мышечных структурах, благоприятно воздействуя на рост мышц.
Если же происходит передозировка инсулином, то запускаются негативные внутриорганические процессы: начинается сохранение и отложение жиров, повышается синтез жирных кислот, повышаются АД показатели, снижается сосудистая эластичность и повышаются риски развития опухолевых клеточных структур злокачественной природы.
Причины передозировки
Для сохранения оптимального здоровья нужно правильно рассчитывать инсулиновые дозировки. Точных критериев подбора правильных дозировок инсулина не разработано, потому и передозировки случаются достаточно часто. Превышение инсулиновой дозы может наблюдаться и у лиц, не имеющих диабета. Просто инсулин часто себе вкалывают спортсмены-бодибилдеры и пр.
Самым распространенным фактором инсулиновой передозировки выступает нарушение индивидуально назначенной схемы инсулинотерапии. Чаще рискуют столкнуться с побочными эффектами инсулина пациенты, страдающие диабетом, оттого вынужденные каждодневно вводить дозу гормона по жизненным показаниям. Таким пациентам нужно крайне внимательно отслеживать собственное самочувствие, самостоятельно определять сахар с помощью глюкометра.
Вторыми по степени риска являются профессиональные культуристы, которые тоже вводят себе инсулиновые инъекции. Такие пациенты могут ошибочно ввести дозировку гормона, традиционно назначаемую для диабетических больных. К тому же у культуристов высок риск гипогликемического состояния и cмepтельного исхода в случаях, когда сменяется тип шприца или самой инъекции. Если спортсмены нарушают рекомендованный режим, исключают из рациона углеводную пищу, пропускают трапезы после инсулиновых инъекций, то они также рискуют столкнуться с побочными действиями инсулина:
- Если человек здоров, то в сутки ему достаточно 2-4 МЕ препарата;
- Для спортсменов или культуристов количество назначаемого инсулинового гормона несколько выше – 20 МЕ в сутки;
- Диабетикам гормон назначается в еще более высокой концентрации – 20-50 МЕ.
Передозировка инсулина и даже cмepть возможна и в случае, когда пациент совмещает недопустимую комбинацию инсулинового гормона с алкоголем. Пациентам стоит запомнить простое правило – выпить стакан пива или бокал вина им можно только при компенсированном типе диабета, исключительно после пищи и при условии контроля сахара с помощью глюкометра.
Признаки и симптомы
При превышении рекомендованных дозировок инсулина побочные явления возникают достаточно быстро, обуславливаясь резким снижением глюкозного компонента в кровотоке. Когда сахар падает меньше 5 ммоль/л, начинаются гипогликемические проявления. Скорость развития клинической симптоматики различается в зависимости от типа применяемого медикамента – быстрый инсулин вызывает гипогликемию скорее, нежели медленный. Характерными побочными явлениями инсулиновой передозировки выступают:
- Общеорганическая слабость, сопровождающаяся учащенным биением сердца, мигренозными проявлениями или внезапным обострением аппетита.
- Специалисты в данном случае рекомендуют выпить либо скушать что-то сладкое. Если на начальной стадии развития меры по предотвращению приняты не были, то состояние продолжает усугубляться.
- О прогрессировании говорят симптоматические проявления, связанные с гиперпотливостью и обильным слюноотделением, тремором рук или расширением зрачков и зрительными нарушениями. Но даже сейчас возможность избежать гипогликемического состояния все еще сохраняется, для чего нужно срочно скушать 5-6 кубиков сахара.
- На следующем этапе развития инсулиновой передозировки самостоятельные меры помочь уже не смогут. Пациент все больше слабеет, передвигаться сам не может. Его тахикардия набирает обороты, сознание мутнеет, беспокоит сильный тремор, начинаются проявления психических расстройств. Сейчас необходимо ввести глюкозу внутривенно, иначе у больного возникнет гипогликемическое коматозное состояние.
В дальнейшем пациент становится землисто-белого цвета, сердечный ритм его замедляется и приобретает неравномерный характер, зрачки перестают реагировать на свет. Если пациент не будет экстренно доставлен в реанимацию, то наступит летальный исход, поскольку происходит неизбежное угнетение всех функций (дыхательной, рефлекторной, кровеносной и пр.).
Хронический синдром инсулиновой передозировки
При неизменно повышенной концентрации гормона происходит постоянная выработка контринсулиновых веществ, что при прохождении инсулинотерапии чревато частыми скачками глюкозы и лабильным течением диабета. Синдром хронической инсулиновой передозировки обычно проявляется следующей симптоматикой:
- Повышенным аппетитом и ощущением постоянного голода;
- Головокружениями и частыми мигренями, частой слабостью, которая проходит после употрeбления углеводных продуктов;
- Гиперпотливостью во время сна, бессонницей или частыми кошмарами;
- Разбитостью по утрам, а в течение дня выраженной сонливостью;
- Внезапными зрительными нарушениями, самостоятельно исчезающими в течение короткого времени, появлением затуманивания или пелены перед глазами, раздвоенностью предметов и мельканием мошек;
- Прибавка веса;
- Снижение интеллектуальных способностей и работоспособности.
Первая помощь и лечение
Если в семье имеется диабетик, то домочадцам часто приходится наблюдать побочные проявления инсулиновой передозировки. Будет полезно знать, как таким пациентам помочь, как предотвратить развитие гипогликемического коматозного состояния и наступление cмepти. Специалисты предупреждают, нужно оказать первую помощь в первые минуты после появления патологической симптоматики. При своевременном обнаружении характерной симптоматики пациент даже сам может остановить наступление гипогликемии:
- На раннем этапе рекомендуется скушать кусочек белого хлеба (100 г), который нормализует сахар;
- Если по прошествии 5-7 минут симптоматика не проходит, то нужно скушать быстрые углеводы вроде сахара (2 ч. л.), карамелек или варенья;
- Если симптоматика по прошествии 5 минут также сохраняется, то следует снова скушать быстрые углеводные продукты.
Домочадцам следует вызвать скорую, а пациента нужно уложить в постель, разместив его на боку. Следует обязательно укутать ноги. Нельзя самостоятельно вкалывать Глюкагон, лучше дождаться приезда скорой. Самостоятельно можно бороться с инсулиновой передозировкой только сладкими напитками и сахаром. В дальнейшем лечение должно проходить под контролем специалистов, при необходимости с помещением больного в стационарные условия.
Если первая помощь привела к нормализации состояния, то экстренная медпомощь уже не требуется. Но пациенту все же нужно будет сходить к эндокринологу, чтобы скорректировать дозировку и схему инсулинотерапии. Если передозировка протекает в тяжелой форме, то необходим вызов неотложки. Больного помещают в эндокринологическое отделение или в реанимацию. Проводятся исследования на уровень сахара, внутривенно вводится глюкоза, внутримышечно при необходимости вводят Глюкагон. Если формируется коматозное состояние, то необходима коррекция нарушенных внутриорганических функций.
Читать еще: Признаки и лечение отравления беленой
Опасные осложнения и последствия
Последствия инсулиновой передозировки порой бывают крайне серьезными, вплоть до наступления cмepти больного. Уже указывалось, что вследствие нарушения рекомендованных доз может развиться гипогликемическое коматозное состояние, при наступлении которого у больного наблюдаются проявления:
- Вздутие и боли в животе;
- Прекращение выделения пота;
- От больного начинает пахнуть ацетоном (от мочи или изо рта);
- Выраженная дегидратация;
- Резко снижаются показатели АД;
- Уменьшаются рефлексы и тонус мышц;
- Беспокоит тошнотно-рвотное недомогание;
- Сужаются зрачки.
Легкие проявления гипогликемических приступов периодически встречаются у всех диабетиков. По наблюдениям эндокринологов, около 35% больных регулярно переживают гипогликемическую симптоматику. Если приступ развился до средней тяжести, то его последствия должны нейтрализоваться с применением специализированных инъекционных медикаментов.
Если же передозировка привела к тяжелому приступу, то осложнения неизбежно затрагивают нервносистемные структуры, провоцируя развитие головномозгового отека, менингита или умственной отсталости. Также на фоне повышенного инсулина вполне возможны различные кровоизлияния, инсульты или инфаркты. Имеет место риск кетоацидоза, который сам по себе опасен комой.
Профилактика передозировки
Ведущее значение в профилактике имеет профессиональное назначение дозировок инсулина и грамотный подбор схемы инсулинотерапии. Необходимо строго соблюдать назначения эндокринолога, вводить инъекции по времени. Для удобства пациентов сегодня созданы специальные шприцы-ручки. На шкале нужно набрать количество вводимых единиц и ввести препарат.
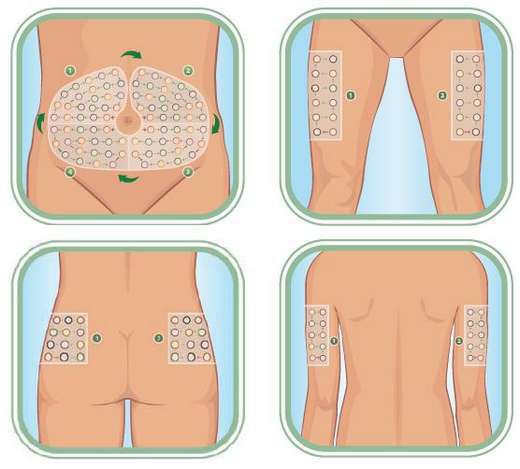
Также важно соблюдать правила введения относительно еды, т. е. вводить препарат только после или до пищи. Инсулиновые инъекции обычно колют в живот, поскольку именно эта область меньше всего подвергается физическим повреждениям или перегрузкам. Если же инъекции вводить в ягoдицы, то усваиваемость препарата будет сильно нарушена и замедлена.
Если пациент по каким-то причинам изменил образ жизнедеятельности, появились повышенные физические нагрузки или, наоборот, работа приобрела малоподвижный, сидячий характер, произошли изменения в режиме рациона либо в психологическом состоянии, то нужно пройти дополнительное обследование и скорректировать схему инсулинотерапии.
При своевременной терапии инсулиновой передозировки практически исключены летальные последствия для пациентов. Только внимательное отношение к процедypaм введения гормона, постоянный контроль сахара, а также своевременное распознавание признаков гипогликемического приступа поможет избежать жизнеугрожающих осложнений или фатальных последствий.
Последствия и помощь при передозировке инсулином
Инсулин позволяет поддерживать работу организма и поджелудочной железы на оптимальном уровне, но его применение в чрезмерных количествах может привести к нежелательным последствиям. В связи с этим передозировки инсулина гораздо проще избежать изначально, чем обеспечивать лечение в будущем. Во избежание осложнений необходимо знать какое количество может спровоцировать передозировку, каковы признаки состояния и другие особенности.
Какое количество инсулина приводит к передозировке
Безопасная дозировка для человека, не страдающего сахарным диабетом, должна составлять больше 4 МЕ. Спортсмены, в частности, бодибилдеры иногда используют гормональный компонент в огромном количестве, увеличивая допустимое соотношение в пять раз. Диабетики в лечебных целях могут использовать от 25 до 50 МЕ инсулина.
Все, что больше указанных показателей, приводит к передозировке.
Чаще всего причины этого заключаются в механической ошибке, разовом внедрении некорректной дозы, путнице в препаратах или некомпетентности специалиста. Также привести к передозировке может:
- нарушение привычного режима активности на фоне применения недостаточного количества углеводов;
- отказ от употрeбления пищи после введения инсулина;
- переход на новый вид гормонального компонента;
- ошибочное введение препарата здоровому человеку;
- несоблюдение врачебных рекомендаций.
Кроме того, использование чрезмерного количества инсулина возможно при одномоментном применении инсулина, употрeблении значительного количества алкоголя. В особенности тяжелые последствия следует ожидать в той ситуации, когда диабетик не употрeбляет необходимые порции пищи на фоне высоких физических нагрузок.
Признаки состояния
Скорость формирования симптомов будет зависеть от типа используемого лекарственного средства. Например, при внедрении быстрого инсулина симптомы будут развиваться через короткий промежуток времени, при использовании медленного – в течение более продолжительного периода.
На первой стадии развития состояния формируется чувство голода, тотальная слабость. Также у диабетика проявляются головные боли и учащенный темп сердцебиения. Если на данном этапе не были предприняты меры для увеличения уровня сахара в крови, то клиническая картина дополняется потливостью, дрожанием рук, повышенным слюноотделением. Не менее выраженными симптомами оказывается прогрессирующая слабость и ощущение голода, значительная бледность, онемение пальцев. Могут идентифицироваться проходящие нарушения зрения и даже расширение зрачков. Следует отметить, что на указанном этапе состояние все еще обратимо.
Однако впоследствии состояние диабетика будет усугубляться все более стремительно. Клиническая картина такова:
- Слабость прогрессирует, в результате человек будет не в состоянии помочь себе самостоятельно.
- Идентифицируется неспособность двигаться, чрезмерное потоотделение, а также учащенное сердцебиение. Может проявляться дрожание верхних и нижних конечностей, усугубление сознания, угнетение или, наоборот, чрезмерное психическое возбуждение.
- Далее формируются клонические (подергивания) или тонические судороги (спазмы). Если на представленном этапе не ввести глюкозу внутривенно, вероятно наступление гипогликемической комы.
- Коматозное состояние идентифицируется по потере сознания, сильному снижению соотношения сахара в крови (больше чем на пять ммоль от привычного уровня). У диабетика будет отмечена постоянная бледность, усугубление сердечного ритма и даже отсутствие зрачкового рефлекса. Не вызывает сомнений, что последствия такого состояния, скорее всего, окажутся весьма серьезными.
Последствия передозировки инсулином
Во многом последствия будут зависеть от степени реакции. Так, с легкими гипогликемическими состояниями сталкиваются все диабетики. В соответствии с врачебными данными, практически 30% пациентов регулярно сталкиваются с гипогликемией и ее последствиями. Наиболее серьезная опасность заключается в формировании синдрома Сомоджи, о котором будет рассказано далее. Следствием этого, в свою очередь, называют неправильное лечение сахарного диабета, что никак не облегчает течение заболевания и с течение времени приводит к возникновению кетоацидоза.
Последствия в случае приступа гипогликемии средней степени тяжести должны ликвидироваться за счет введения соответствующих лекарственных средств. Обычно это занимает достаточно длительное время. В наиболее тяжелых случаях передозировка инсулином может провоцировать нарушения со стороны деятельности нервной системы:
- отек в области мозга;
- менингеальные симптомы (головные боли, боязнь света, упopная тошнота и продуктивные рвотные позывы, ригидность мышц затылка);
- нарушение умственной деятельности, а именно деменция.
Если у диабетика по каким-либо причинам часто повторяются гипогликемические состояния и при этом присутствует расстройство сердечно-сосудистой деятельности, вероятно развитие инфаркта миокарда. Также у больного может быть отмечен инсульт и кровоизлияние в сетчатку глаза.
Смертельная доза инсулина
Смертельная дозировка гормонального компонента у разных людей – разная. Одни диабетики спокойно могут переносить количество в 300-500 ЕД, в то время как для других уже 100 ЕД могут оказаться крайне опасными, спровоцировать кому и даже cмepть. Происходит это в силу самых разных факторов, одним из которых является вес больного.
В ситуациях, когда человек, весящий 60 кг обычно вводит 60 ЕД, дозировка гормона в 100 ЕД уже окажется cмepтельной. Для диабетика же, весящего, например, 90 кг (использующего обычно 90 ЕД), указанная дозировка окажется вполне нормальной. Именно поэтому важно учитывать не только количество инсулина, но и его соотношение с весом диабетика, возрастом, наличием или отсутствием осложнений.
Возможна ли хроническая передозировка инсулином?
Хроническая передозировка инсулином действительно возможна, и называется она синдромом Сомоджи. Перманентный избыток гормонального компонента при лечении диабета провоцирует хроническое состояние, сопровождающееся производством гормонов, которые препятствуют уменьшению показателей сахара в крови. Речь идет об адреналине, кортикостероидах и глюкагоне.
Симптомами хронической передозировки у диабетиков следует считать:
- усугубленное течение заболевания;
- повышенный аппетит;
- увеличение весовой категории при повышенном соотношении сахара в моче;
- склонность к кетоацидозу (нарушение углеводного обмена);
- ацетонурию – появление в моче ацетона.
Дополняют клиническую картину резкие колебания показателей сахара в течение 24 часов, чаще привычного идентифицируется увеличение показателей сахара в крови. Кроме того, симптоматика ассоциируется с постоянными приступами гипогликемии, возникающими до нескольких раз в течение суток.
Первая и медицинская помощь
Безусловно, в случае превышения дозировки инсулина необходимо оказать первую помощь. Далее диабетику может быть предоставлена более специализированная поддержка. Первая помощь при передозировке инсулина начинается с проверки уровня сахара – это поможет диабетику убедиться в том, что причина ухудшения самочувствия определена правильно. Для этого достаточно измерить соотношение глюкозы в крови с помощью глюкометра.
После этого можно приступать к оказанию первой помощи, которая заключается в увеличении уровня глюкозы в крови. С представленной целью диабетику потребуется употребить что-либо сладкое, например, шоколадку, конфету или булочку, сладкий чай. Также больному рекомендуется внутривенно ввести раствор глюкозы – объем лекарственного средства идентифицируется в соответствии с общим состоянием диабетика.
Стремясь увеличить соотношение сахара в крови, очень важно не использовать чрезмерное количество углеводов. Избыточное соотношение сахара у человека с нормальным здоровьем может откладываться в виде гликогена (впоследствии они используются для резервной энергии). Для диабетика подобные отложения опасны дегидратацией тканевых структур, а также обезвоживанием всего организма.
После оказания представленных мер, следует обратиться к специалисту. При инсулинозависимом типе диабета будет проведена повторная проверка уровня сахара, возможно помещение в стационар. В зависимости от возникших осложнений, лечение может быть самым разными, вплоть до пожизненного.
Учитывая высокие риски, важно знать как вводить инсулин, чтобы избежать критических последствий.
- Больной должен строго соблюдать рекомендации эндокринолога и использовать инъекции исключительно в определенное время, то есть строго по часам.
- Зачастую диабетики делают себе уколы самостоятельно, что довольно несложно. Для этого применяют специальные шприцы-ручки, которые не подразумевают дополнительный набор гормонального компонента в шприц.
- Диабетику лишь необходимо набрать на шкале требуемое значение, обозначенное в единицах. Инъекция гормонального компонента проводится до или после употрeбления пищи, все зависит от указаний эндокринолога.
Общие правила внедрения инсулина таковы: в шприц набирают требуемое количество инсулина, непосредственную область введения иглы обpaбатывают при помощи спирта. После осуществления инъекции не рекомендуется сразу же извлекать из тела иголку, важно подождать в течение 10 секунд – до тех пор, пока гормональный компонент полностью усвоится.
Живот – это именно такая часть тела, которая в наименьшей степени подвержена случайным физическим нагрузкам, а потому инъекции гормонального компонента делают именно в указанную область. Если же гормональный компонент вводить в мышечные структуры конечностей, то степень его всасываемости окажется значительно ниже, соответственно, усвоение будет хуже. Именно поэтому такой подход является нежелательным. Соблюдение же всех указанных ранее советов и рекомендаций эндокринолога сведет к минимуму вероятность передозировки инсулином.
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
08 03 2023 15:11:40
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
07 03 2023 17:23:36
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
06 03 2023 14:33:11
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
05 03 2023 18:46:20
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
02 03 2023 6:35:18
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
01 03 2023 15:48:21
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
26 02 2023 22:22:56
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
25 02 2023 15:49:41
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
24 02 2023 7:49:24
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
23 02 2023 8:16:45
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
22 02 2023 18:54:47
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
21 02 2023 17:30:33
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
20 02 2023 2:44:57
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
18 02 2023 15:16:51
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
15 02 2023 13:28:24
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
12 02 2023 0:21:36
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
11 02 2023 12:39:32
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
09 02 2023 14:29:52
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
08 02 2023 7:10:41
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
05 02 2023 22:42:33
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
04 02 2023 4:19:44
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
03 02 2023 16:57:30
Фуросемид таблетки инструкция по применению
Фуросемид таблетки инструкция по применению Инструкция по применению: Цены в интернет-аптеках: Фуросемид – синтетическое диуретическое лекарственное…
31 01 2023 15:43:34
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
30 01 2023 11:26:55
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
29 01 2023 18:36:48
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
28 01 2023 17:16:22
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
25 01 2023 15:19:39
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
24 01 2023 11:43:14
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
21 01 2023 2:32:12
Гиперинсулинизм — клинический синдром, характеризующийся повышением уровня инсулина и снижением сахара в крови. Гипогликемия приводит к слабости, головокружению, повышению аппетита, тремору, психомоторному возбуждению. При отсутствии своевременного лечения развивается гипогликемическая кома. Диагностика причин состояния основывается на особенностях клинической картины, данных функциональных проб, динамическом исследовании глюкозы, ультразвуковом или томографическом сканировании поджелудочной железы. Лечение панкреатических новообразований – хирургическое. При внепанкреатическом варианте синдрома проводят терапию основного заболевания, назначают специальную диету.
Общие сведения
Гиперинсулинизм (гипогликемическая болезнь) — врожденное или приобретенное патологическое состояние, при котором развивается абсолютная или относительная эндогенная гиперинсулинемия. Признаки болезни впервые были описаны в начале ХХ века американским врачом Харрисом и отечественным хирургом Оппелем. Врожденный гиперинсулинизм встречается достаточно редко — 1 случай на 50 тыс. новорожденных. Приобретенная форма заболевания развивается в возрасте 35-50 лет и чаще поражает лиц женского пола. Гипогликемическая болезнь протекает с периодами отсутствия выраженной симптоматики (ремиссия) и с периодами развернутой клинической картины (приступы гипогликемии).
Гиперинсулинизм
Причины гиперинсулинизма
Врожденная патология возникает вследствие внутриутробных аномалий развития, задержки роста плода, мутаций в геноме. Причины возникновения приобретенной гипогликемической болезни разделяют на панкреатические, приводящие к развитию абсолютной гиперинсулинемии, и непанкреатические, вызывающие относительное повышение уровня инсулина. Панкреатическая форма болезни встречается при злокачественных или доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы. Непанкреатическая форма развивается при следующих состояниях:
- Нарушения в режиме питания. Длительное голодание, повышенная потеря жидкости и глюкозы (поносы, рвота, период лактации), интенсивные физические нагрузки без потребления углеводной пищи вызывают резкое снижение уровня сахара в крови. Чрезмерное употребление в пищу рафинированных углеводов увеличивает уровень сахара крови, что стимулирует активную выработку инсулина.
- Поражение печени различной этиологии (рак, жировой гепатоз, цирроз) приводит к снижению уровня гликогена, нарушению обменных процессов и возникновению гипогликемии.
- Бесконтрольный прием сахароснижающих препаратов при сахарном диабете (производных инсулина, сульфанилмочевины) вызывает медикаментозную гипогликемию.
- Эндокринные заболевания, приводящие к снижению уровня контринсулиновых гормонов (АКТГ, кортизол): гипофизарный нанизм, микседема, болезнь Аддисона.
- Недостаток ферментов, участвующих в процессах обмена глюкозы (печеночная фосфорилаза, почечная инсулиназа, глюкозо-6-фосфатаза) вызывает относительный гиперинсулинизм.
Патогенез
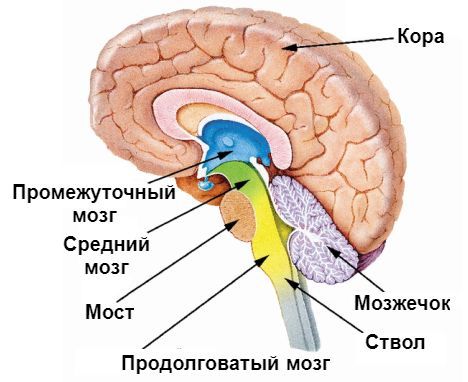
Глюкоза является главным питательным субстратом центральной нервной системы и необходима для нормального функционирования головного мозга. Повышенный уровень инсулина, накопление гликогена в печени и торможение гликогенолиза приводит к снижению уровня глюкозы в крови. Гипогликемия вызывает торможение метаболических и энергетических процессов в клетках головного мозга. Происходит стимуляция симпатоадреналовой системы, увеличивается выработка катехоламинов, развивается приступ гиперинсулинизма (тахикардия, раздражительность, чувство страха). Нарушение окислительно-восстановительных процессов в организме приводит к снижению потребления кислорода клетками коры головного мозга и развитию гипоксии (сонливость, заторможенность, апатия). Дальнейший дефицит глюкозы вызывает нарушение всех обменных процессов в организме, увеличение притока крови к мозговым структурам и спазм периферических сосудов, что может привести к инфаркту. При вовлечении в патологический процесс древних структур мозга (продолговатый и средний мозг, варолиев мост) развиваются судорожные состояния, диплопия, а также нарушение дыхательной и сердечной деятельности.
Классификация
В клинической эндокринологии наиболее часто используется классификация гиперинсулинемии в зависимости от причин возникновения заболевания:
- Первичный гиперинсулинизм (панкреатический, органический, абсолютный) является следствием опухолевого процесса или гиперплазии бета-клеток островкового аппарата поджелудочной железы. Повышению уровня инсулина в 90% способствуют доброкачественные новообразования (инсулинома), реже – злокачественные (карцинома). Органическая гиперинсулинемия протекает в тяжелой форме с выраженной клинической картиной и частыми приступами гипогликемии. Резкое понижение уровня сахара в крови возникает утром, связано с пропуском приема пищи. Для данной формы заболевания характерна триада Уиппла: симптомы гипогликемии, резкое снижение сахара в крови и купирование приступов введением глюкозы.
- Вторичный гиперинсулинизм (функциональный, относительный, внепанкреатический) связан с дефицитом контринсулярных гормонов, поражением нервной системы и печени. Приступ гипогликемии возникает по внешним причинам: голодание, передозировка гипогликемических препаратов, интенсивная физическая нагрузка, психоэмоциональное потрясение. Обострения болезни возникают нерегулярно, практически не связаны с приемом пищи. Суточное голодание не вызывает развернутой симптоматики.
Симптомы гиперинсулинизма
Клиническая картина гипогликемической болезни обусловлена понижением уровня глюкозы в крови. Развитие приступа начинается с повышения аппетита, потливости, слабости, тахикардии и ощущения голода. Позже присоединяются панические состояния: чувство страха, тревога, раздражительность, дрожь в конечностях. При дальнейшем развитии приступа отмечается дезориентация в пространстве, диплопия, парестезии (онемение, покалывание) в конечностях, вплоть до возникновения судорог. При отсутствии лечения наступает потеря сознания и гипогликемическая кома. Межприступный период проявляется снижением памяти, эмоциональной лабильностью, апатией, нарушением чувствительности и онемением в конечностях. Частый прием пищи, богатой легкоусвояемыми углеводами, провоцирует увеличение массы тела и развитие ожирения.
В современной практике выделяют 3 степени гиперинсулинизма в зависимости от тяжести течения болезни: легкую, среднюю и тяжелую. Легкая степень проявляется отсутствием симптоматики межприступного периода и органического поражения коры головного мозга. Обострения болезни проявляются реже 1 раза в месяц и быстро купируются медикаментозными препаратами или сладкой пищей. При средней степени тяжести приступы возникают чаще 1 раза в месяц, возможна потеря сознания и развитие коматозного состояния. Межприступный период характеризуется легкими нарушениями поведенческого характера (забывчивость, снижение мышления). Тяжелая степень развивается при необратимых изменениях коры головного мозга. При этом приступы случаются часто и заканчиваются потерей сознания. В межприступном периоде пациент дезориентирован, память резко снижена, отмечается тремор конечностей, характерна резкая смена настроения и повышенная раздражительность.
Осложнения гиперинсулинизма
Осложнения можно условно разделить на ранние и поздние. К ранним осложнениям, возникающим в ближайшие часы после приступа, относят инсульт, инфаркт миокарда вследствие резкого снижения метаболизма сердечной мышцы и головного мозга. В тяжелых ситуациях развивается гипогликемическая кома. Поздние осложнения проявляются спустя несколько месяцев или лет от начала болезни и характеризуются нарушением памяти и речи, паркинсонизмом, энцефалопатией. Отсутствие своевременного диагностики и лечения заболевания приводит к истощению эндокринной функции поджелудочной железы и развитию сахарного диабета, метаболического синдрома, ожирения. Врожденный гиперинсулинизм в 30% случаев приводит к хронической гипоксии головного мозга и снижению полноценного умственного развития ребенка.
Диагностика гиперинсулинизма
Диагностика основывается на клинической картине (потеря сознания, тремор, психомоторное возбуждение), данных анамнеза заболевания (время начала приступа, его связь с приемом пищи). Эндокринолог уточняет наличие сопутствующих и наследственных заболеваний (жировой гепатоз, сахарный диабет, синдром Иценко-Кушинга), после чего назначает лабораторные и инструментальные исследования. Пациенту проводится суточное измерение уровня глюкозы крови (гликемический профиль). При выявлении отклонений выполняют функциональные пробы. Проба с голоданием используется для дифференциальной диагностики первичного и вторичного гиперинсулинизма. Во время теста измеряют С-пептид, иммунореактивный инсулин (ИРИ) и глюкозу в крови. Повышение данных показателей свидетельствует об органическом характере болезни.
Для подтверждения панкреатической этиологии заболевания проводят тесты на чувствительность к толбутамиду и лейцину. При положительных результатах функциональных проб показано УЗИ, сцинтиграфия и МРТ поджелудочной железы. При вторичном гиперинсулинизме для исключения новообразований других органов выполняют УЗИ брюшной полости, МРТ головного мозга. Дифференциальная диагностика гипогликемической болезни проводится с синдромом Золлингера-Эллисона, началом развития сахарного диабета 2 типа, неврологическими (эпилепсия, новообразования головного мозга) и психическими (неврозоподобные состояния, психоз) заболеваниями.
Лечение гиперинсулинизма
Тактика лечения зависит от причины возникновения гиперинсулинемии. При органическом генезе показано хирургическое лечение: частичная резекция поджелудочной железы или тотальная панкреатэктомия, энуклеация новообразования. Объем оперативного вмешательства определяется местоположением и размерами опухоли. После операции обычно отмечается транзиторная гипергликемия, требующая медикаментозной коррекции и диеты с пониженным содержанием углеводов. Нормализация показателей наступает через месяц после вмешательства. При неоперабельных опухолях проводят паллиативную терапию, направленную на профилактику гипогликемии. При злокачественных новообразованиях дополнительно показана химиотерапия.
Функциональный гиперинсулинизм в первую очередь требует лечения основного заболевания, вызвавшего повышенную продукцию инсулина. Всем больным назначается сбалансированная диета с умеренным снижением потребления углеводов (100-150 гр. в сутки). Отдается предпочтение сложным углеводам (ржаные хлебцы, макароны из твердых сортов пшеницы, цельнозерновые крупы, орехи). Питание должно быть дробным, 5-6 раз в день. В связи с тем, что периодические приступы вызывают у пациентов развитие панических состояний, рекомендована консультация психолога. При развитии гипогликемического приступа показано употребление легкоусвояемых углеводов (сладкий чай, конфета, белый хлеб). При отсутствии сознания необходимо внутривенное введение 40 % раствора глюкозы. При судорогах и выраженном психомоторном возбуждении показаны инъекции транквилизаторов и седативных препаратов. Лечение тяжелых приступов гиперинсулинизма с развитием комы осуществляют в условиях реанимационного отделения с проведением дезинтоксикационной инфузионной терапии, введением глюкокортикоидов и адреналина.
Прогноз и профилактика
Профилактика гипогликемической болезни включает в себя сбалансированное питание с интервалом в 2-3 часа, употребление достаточного количества питьевой воды, отказ от вредных привычек, а также контроль уровня глюкозы. Для поддержания и улучшения обменных процессов в организме рекомендованы умеренные физические нагрузки с соблюдением режима питания. Прогноз при гиперинсулинизме зависит от стадии заболевания и причин, вызывавших инсулинемию. Удаление доброкачественных новообразований в 90% случаев обеспечивают выздоровление. Неоперабельные и злокачественные опухоли вызывают необратимые неврологические изменения и требуют постоянного контроля за состоянием пациента. Лечение основного заболевания при функциональном характере гиперинсулинемии приводит к регрессии симптомов и последующему выздоровлению.
15.09.2021
Головной мозг всегда нуждается в определённом количестве глюкозы, в этом состоит опасность гипогликемии. Гипогликемия – состояние, когда сахар в крови понижается меньше, чем до 3 ммоль на литр. Запущенное состояние гипогликемии может обернуться комой и последующим летальным исходом. Обычно, гипогликемия проявляется лишь у пациентов с сахарным диабетом на инсулинотерапии или приёме других сахароснижающий препаратов. В случае возникновения гипогликемии у диабетика, нужно очень быстро предпринимать меры.
Причины возникновения гипогликемии
- Передозировка инсулина короткого/ультракороткого действия в один из приёмов пищи
- Чрезмерная физическая активность
- Употребление недостаточного количества углеводов
- Употребление алкогольных напитков
Симптоматика гипогликемии
- Беспокойство
- Потеря сознания
- Головокружение
- Слабость
- Нарушение зрения
- Потливость
- Дрожь в теле
- Голод
- Учащённое сердцебиение
- В некоторых случаях могут наблюдаться судороги по всему телу
Что делать, если случился приступ гипогликемии
В первую очередь немедленно прекратить физические нагрузки, измерить уровень сахара крови, употребить быстроусвояемые углеводы (например, 4 ч.л. сахара или стакан фруктового сока). Спустя 10-15 минут снова измерить уровень сахара и убедиться, что он в норме. Не нужно пытаться купировать гипогликемию с помощью медленных углеводов, они медленно повышают уровень сахара, в данном случае этого не нужно! При тяжёлом состоянии гипогликемии необходимо вызвать скорую помощь, из тяжёлого состояния поможет выйти внутривенное введение глюкозы до восстановления сознания.
Профилактика развития гипогликемии
Существует ряд советов, помогающий предотвратить гипогликемию или вовремя среагировать на её симптомы:
- Необходимо постоянно иметь при себе сахар, сок или какие-либо таблетки с высоким содержанием глюкозы
- Перед физической активностью нужно правильно скорректировать дозировку инсулинов
- Обязательно требуется регулярно контролировать сахар в крови
- Нужно соблюдать режим питания
- Рекомендуется ограничить количество употребляемых алкогольных напитков
Особого внимания заслуживают приступы гипо в ночные часы. Причинами могут послужить передозировка инсулина перед последним приёмом пищи или усиленная физическая активность в вечернее время. Чтобы предотвратить ночные приступы можно регулярно (например, раз в неделю) измерять сахар крови в 2-4 часа ночи, для контроля. О ночном приступе гипо может свидетельствовать влажная постель на утро, головные боли, а также ночные кошмары.
Очень важно предупреждать состояние гипогликемии, оно может быть очень опасно. Ведь без необходимого количества глюкозы мозг человека не способен правильно функционировать. Если гипогликемии будут регулярными, возможны и дальнейшие осложнения сахарного диабета, например, нейропатия. Главное – правильно рассчитывать дозы инсулина и не увлекаться физическими упражнениями при сахарном диабете.
Дата публикации 29 апреля 2020Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Диабетическая кома — это опасное состояние, при котором человек длительное время находится без сознания. У него снижается или исчезает реакция на внешние раздражители, нарушается глубина и частота дыхания, изменяется сосудистый тонус, учащается или замедлением пульс. Такое состояние возникает при нарушении углеводного обмена — резком снижении или повышении уровня глюкозы в крови (уровня гликемии) из-за неправильного введения и хранения инсулина, а также острых воспалительных реакций [1][2][7]. Если пациенту вовремя не оказать помощь, кома может привести к летальному исходу.
Норма глюкозы в плазме крови — 4-5,9 ммоль/л, в капиллярной крови — 3,3-5,5 ммоль/л.
Кома начинает развиваться в том случае, если уровень гликемии опускается ниже 2,8 ммоль/л. Однако при длительном стаже диабета и «привычных» организму высоких уровнях глюкозы кома может возникнуть на более высоких цифрах гликемии — 3,3-6,6 ммоль/л и выше [1][3][9][10].
В зависимости от уровня глюкозы в крови диабетическую кому делят на два вида:
- Гипогликемическая кома — связана со снижением уровня гликемии.
- Гипергликемическая кома — вызвана повышением уровня гликемии. Её подразделяют на кетоацидотическую, гиперосмолярную и лактацидемическую комы.
Гипогликемическая кома чаще всего возникает у больных, находящихся на инсулинотерапии, и у пациентов с сахарным диабетом 1-го типа. Причина такой комы — избыток инсулина, который мешает организму поднять уровень глюкозы в крови до нормальных цифр. Избыток инсулина вызывают:
- передозировка инсулина (более половины случаев);
- нарушение режима питания, при котором количество введённого инсулина не соответствует количеству съеденной пищи (мало углеводов, пропуск приёма пищи);
- увеличение физической нагрузки без дополнительного приёма углеводов (во время физнагрузки организм расходует больше углеводов);
- приём таблетированных сахароснижающих средств (например препаратов сульфонилмочевины), действие которых осуществляется через повышение выработки своего инсулина;
- алкогольное опьянение (алкоголь угнетает поступление глюкозы из печени);
- хроническая болезнь почек, печеночная и надпочечниковая недостаточность и другие заболевания;
- автономная нейропатия — повреждение нервных волокон внутренних органов (из-за поражений нервной системы организм не чувствует гипогликемии, поэтому не может среагировать на снижение глюкозы в крови).
Кетоацидотическая кома сопровождается нехваткой инсулина, высоким уровнем гликемии (более 14 ммоль/л) и нарушением углеводного обмена — метаболическим ацидозом: помимо гликемии, в крови повышается уровень кетонов (более 5 ммоль/л), а в моче — уровень ацетона. В результате этого кислотно-щелочного баланс крови сдвигается в сторону кислой среды, т. е. рН крови снижается.
Причины кетоацидотическаяой комы:
- сахарный диабет 1-го типа (часто метаболический ацидоз является первым проявлением этой болезни);
- неправильное хранение инсулина (несоблюдение температурного режима);
- неверное введение инсулина (неправильная доза, неверно выбранное место введения);
- погрешности в питании (избыток жиров в пище, уменьшение доз инсулина);
- острые заболевания, т. е. инфекции (особенно ОРВИ), при которых организм нуждается в увеличении доз инсулина;
- беременность, требующая корректировки инсулина;
- приём глюкокортикостероидов, тиазидных диуретиков и эстрогенов, обладающих противоположным действием к инсулину, без увеличения доз инсулина [1][3][7][8][10].
Гиперосмолярная кома возникает на фоне такого острого состояния, как гиперосмолярный гипергликемический синдром. У больного повышается уровень глюкозы (обычно больше 33 ммоль/л) и концентрация электролитов в плазме (330-500 мосмоль/л), сгущается кровь и утрачивается жидкость, приводя к выраженному обезвоживанию. В результате таких изменений нарушается микроциркуляция в головном мозге. При этом уровень кетонов не превышает норму, а pH крови не уменьшается.
Факторы развития гиперосмолярной комы:
- обезвоживание организма при рвоте, диарее, ожогах, кровотечениях, приёме диуретиков;
- выполнение гемодиализа и перитонеального диализа (очищение крови от токсинов);
- выраженное обезвоживание на фоне нехватки инсулина при сахарном диабете 2-го типа;
- приём глюкокортикоидов на постоянной основе;
- хирургические вмешательства (увеличивают потребность организма в инсулине) [1][2][3][4].
Лактацидемическая кома развивается на фоне сахарного диабета и лактатацидоза — накопления в крови молочной кислоты (лактата). Данное состояние возникает у больных с кислородным голоданием тканей (гипоксией): анемией, отравлением угарным газом, различными видами шока и эпилепсией. Также оно может развиться после приёма метформина, отравления этанолом, салицилатами и на фоне заболеваний, изначально не связанных с тканевой гипоксией: хронической болезни почек, лейкоза и др. [1][2][3][4].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы диабетической комы
Симптомы гипогликемической комы. Перед потерей сознания возникает состояние гипогликемии, в клинике которого выделяют адренергические и нейрогликопенические симптомы.
Адренергические признаки обусловлены запуском контринсулярных гормонов, которые нейтрализуют действие инсулина. Их активность приводит к следующим симптомам:
- тахикардия;
- беспокойство, страх, агрессивность;
- расширение зрачков (мидриаз);
- дрожь;
- бледность кожи и усиленная потливость;
- тошнота, сильный голод.
Нейрогликопенические признаки возникают вследствие дефицита глюкозы в головном мозге. К ним относятся:
- слабость;
- головная боль;
- снижение концентрации внимания;
- головокружение;
- нарушение координации;
- спутанность речи и сознания;
- неконтролируемое поведения (беспричинная агрессия, смех или плаксивость) [1][2][5].
Симптомы кетоацидотической комы. В клинической картине данного вида комы выделяют четыре формы:
- Абдоминальная симптоматика: боли в области живота из-за воздействия кетонов на солнечное сплетение, остановка работы кишечника, увеличение печени.
- Сердечно-сосудистая (коллаптоидная) симптоматика: боли в области сердца, увеличение частоты сердечных сокращений, снижение уровня калия в крови (гипокалиемия), аритмия (нарушение сердечного ритма), резкое снижение артериального давления (коллапс).
- Мозговая симптоматика: поражение головного мозга с увеличением температуры, повышение тонуса затылочных мышц (пациент не может опустить голову к груди).
- Нефротическая симптоматика: уменьшение объёма мочи или прекращение её выделения почками [1][4][5][7][9].
Симптомы гиперосмолярной комы. Клиника развивается постепенно, в течение нескольких дней. У пациента возникают следующие жалобы:
- жажда (не во всех случаях);
- учащённое мочеиспускание;
- сухость кожи и слизистых оболочек;
- тахикардия;
- частое дыхание;
- в дальнейшем могут присоединяться нервно-психические расстройства: возбуждённость, галлюцинации, судороги, заторможенность и потеря сознания.
Симптомы лактацидемической комы. Данное состояние развивается быстро. Ему предшествуют:
- боли в мышцах;
- расстройство стула, боли в животе (не всегда);
- слабость, беспокойство;
- головная боль;
- тошнота, рвота.
Далее прогрессирует сердечно-сосудистая недостаточность, возникает одышка, дыхание и пульс становятся частыми. Кожа при этом бледная, синюшная [1][2][4][5].
Патогенез диабетической комы
Основа развития гипогликемической комы — снижение уровня глюкозы, поступающей к клеткам центральной нервной системы. Это приводит к развитию дефицита энергии, кислородному «голоду».
Первые реакции головного мозга на гипогликемию возникают при снижении глюкозы до 3,8 ммоль/л. По мере падения уровня сахара поражаются различные отделы головного мозга: сначала страдает кора, затем нарушается работа подкорковых структур и мозжечка, что обуславливает симптомы гипогликемии (нарушение координации, головную боль, спутанность речи и др.). В последнюю очередь поражается продолговатый мозг, что и является причиной летального исхода.
Одновременно со снижением гликемии и поражением структур головного мозга активизируются контринсулярные системы: гипофиз, поджелудочная желез и надпочечники. Они начинают активно вырабатывать контрисулярные гормоны, чтобы увеличить продукцию глюкозы. К таким гормонам относятся глюкагон, кортизол, гормон роста, адреналин и норадреналин. Однако у человека с сахарным диабетом такая реакция нарушена, в связи с чем у больного возникает тахикардия, потливость и другие клинические проявления [1][7][10].
Развитие диабетического кетоацидоза, который предшествует кетоацидотической коме, начинается с дефицита инсулина, из-за которого происходят следующие изменения:
- повышается концентрация глюкозы в крови за счёт уменьшения её поступления в клетки печени и мышцы;
- идёт дополнительный синтез глюкозы благодаря повышению уровня контринсулярных гормонов;
- клетки начинают «голодать», так как в них не попадает глюкоза;
- происходит распад белков, которые стараются обеспечить голодные клетки глюкозой;
- расщепляются резервы жиров и образуются свободные жирные кислоты;
- окисление жирных кислот приводит к кетозу — образованию кетоновых тел в печени, которые приводят к нарушению кислотно-щелочного баланса крови (причём жиры, которые поступают с пищей, не участвую в образовании кетоновых тел).
Так как в крови скапливается много глюкозы, она начинает выделяться вместе с мочой и при этом тянет за собой воду, что приводит к обезвоживанию. В результате высокой концентрации кетоновых тел у больного возникает рвота и ещё большее обезвоживание. Все это приводит к гиповолемической недостаточности кровообращения (из-за уменьшения объёма циркулирующей крови) и гипоксии тканей. Повреждаются почки, миокард (сердечная мышца), расширяются сосуды, и затем нарушается сознание [8][9][10].
Патогенез гиперосмолярной гипергликемической комы до конца неясен. Известно, что для него характерно повышение гликемии и осмолярности крови (концентрации её активных элементов, в частности электролитов) натощак. При этом проявления кетоза и ацидоза не возникают. В случае относительной недостаточности инсулина (т. е. сахарного диабета 2-го типа) повышения гликемии и осмолярности не достаточно для расщепления жировой ткани и образования кетоновых тел, но при этом организм не может подавить образование глюкозы печенью.
Гиперосмолярность плазмы поддерживается глюкозой и натрием — соединениями с высокой концентрацией электролитов. Они плохо проникают внутрь клетки и, оставаясь снаружи, притягивают к себе воду, тем самым обезвоживая клетки. Те же самые процессы происходят и в головном мозге, что приводит к дегидратации (обезвоживанию) и потере сознания, а в результате гипоксии повреждаются жизненно важные органы: почки, лёгкие, сердце и др. [1][2][5].
Главный механизм развития лактацидотической комы — тканевая гипоксия. На её фоне запускается анаэробный (бескислородный) путь гликолиза — расщепления глюкозы до молекул молочной кислоты (лактата). В условиях гипоксии в печени тормозится перевод лактата в гликоген. Это приводит к тому, что лактат не утилизируется, а накапливается. В результате молочная кислота провоцирует сдвиг кислотно-основного состояния в сторону ацидоза (увеличения кислотности). А так как лактат обладает токсическим действием, у пациента развивается слабость, тошнота и другие симптомы, вплоть до комы [1][2][4].
Классификация и стадии развития диабетической комы
Развитие гипогликемической комы имеет пять стадий:
- Первая стадия — корковая. Для неё характерен голод и раздражительность.
- Вторая стадия — подкорковая с вегетативными проявлениями. Характерна головная боль, дрожь, повышенная потливость.
- Третья стадия — подкорковая с нарушениями сознания. Характерно нарушение речи, изменение поведения, снижение концентрации внимания, повышенное слюноотделение.
- Четвёртая стадия — вовлечение верхних отделов продолговатого мозга. Характерен гипертонус мышц и судороги.
- Пятая стадия — вовлечение нижних отделов продолговатого мозга (дыхательного и сосудодвигательного центров). Характерна остановка сердца и дыхания, развивается отёк мозга с повышением температуры, рвотой, нарушением ритма сердца и учащением дыхания [1][2][3].
Диабетической кетоацидотической коме предшествует диабетический кетоацидоз, который имеет три степени тяжести [1][7][8].
| Показатели | Лёгкая степень | Средняя степень | Тяжёлая степень |
|---|---|---|---|
| Глюкоза | выше 13 ммоль/л | выше 13 ммоль/л | выше 13 ммоль/л |
| рН артериальной крови |
7,25-7,30 | 7,00-7,34 | меньше 7,00 |
| Бикарбонаты | 15-18 ммоль/л | 10-15 ммоль/л | меньше 10 ммоль/л |
| Ацетон в моче | + | ++ | +++ |
| Количество кетоновых тел |
небольшое | умеренное | большое |
| Сознание | не нарушено | не нарушено, но может возникать оглушённость или сонливость |
нарушено: стопор или кома |
Развитие гиперосмолярной комы происходит медленно: в течение пару дней и даже недель. Начинается с усиленной жажды (у пожилых людей её может не быть), учащённого мочеиспускания, снижения массы тела, головной боли, вялости и слабости. В 25-60 % случаев бывает тошнота и рвота [1].
После этого наступает период олигоурии (уменьшения объёма мочи), а затем — анурии (отсутствия мочи). В дальнейшем наступает обезвоживание, присоединяются неврологические проявления и потеря сознания.
Развитие лактацидотической комы начинается с повышения концентрации лактата в крови, из-за чего у пациента возникают жалобы на боли в мышцах и за грудиной, а также расстройства пищеварения. По мере накопление лактата присоединяется одышка, слабость, тошнота и рвота. При дальнейшем увеличении содержания лактата кислотно-щелочное равновесие сдвигается в сторону ацидоза (кислой среды). Если на этом этапе вовремя не оказать помощь, пациент впадаёт в кому [4][8].
Осложнения диабетической комы
При тяжёлой гипогликемии и длительном пребывании в коме возможны осложнения в виде отёка мозга, сердечно-сосудистых осложнений и расстройств дыхания. Смертность по причине гипогликемической комы составляет порядка 2-4 % [1][6].
При диабетической кетоацидотической коме возможно развитие коллапса, респираторного дистресс-синдрома (нарушение дыхания) и почечной недостаточности, что также может привести к летальному исходу [2][3][8].
При несвоевременном оказании помощи в случае развития гиперосмолярной комы высока вероятность летальности — до 60 % [1]. Это связано с необратимыми поражениями всех органов.
Лактацидотическая кома не осложняется, если концентрация лактата нормализируется за сутки после нарушения сознания. Если уровень молочной кислоты не снижается в течение 1-2 суток, то риск летальности увеличивается до 22 %, а после 2 суток — до 86 % (поражается головной мозг, жизненно важные центры дыхания и кровообращения) [1][4][5].
Диагностика диабетической комы
Диагностика гипогликемической комы проводится на основании информации об истории болезни, наличия сахарного диабета, приёма сахароснижающих таблетированных препаратов или инсулина. По результатам лабораторных исследований наблюдается низкий уровень глюкозы — менее 2,2 ммоль/л.
Для кетоацидотической комы характерна высокая гликемия, повышенная концентрация кетонов в моче и крови. Также в моче возникает белок, а в крови увеличивается уровень мочевины и остаточного азота.
В случае гиперосмолярной комы на себя обращает внимание высокая степень обезвоженности, которая проявляется сухостью кожи и слизистых, снижением упругости кожи и нарушением сознания. Лабораторная диагностика гиперосмолярной комы сводится к определению осмолярности. Для этого используют специальные приборы или определённую формул, в которой учитывается натрий, глюкоза, мочевина и белок. В норме осмолярность находится в пределах 285-300 мосм/л [1][2][4][10].
Диагностика лактацидотической комы сложна. Для постановки правильного диагноза требуется лабораторно подтвердить уровень молочной кислоты в крови. Для этого необходимо взять кровь для биохимического анализа. В норме концентрация лактата не превышает 1,3 ммоль/л, при лактацидотической коме этот уровень больше 8 ммоль/л. Уровень гликемии повышен незначительно — до 13-17 ммоль/л, рН менее 7,25, уровень бикарбонатов снижен, в моче отсутствуют кетоны [1][8].
Лечение диабетической комы
Пациенту с гипогликемической комой нельзя вливать сладкие напитки. Для купирования гипогликемии подкожно или внутримышечно вводят 1-2 мг глюкагона или же внутривенно 20-40 мл 40 % раствора глюкозы. Если даже на фоне внутривенного введения 60-100 мл 40 % раствора глюкозы человек не приходит в сознание, то дальнейшая терапия проводится в стационаре, чтобы восполнить водный баланс и нормализовать уровень гликемии [1][3][6][10].
Лечение кетоацидотической комы состоит из пяти компонентов:
- Инсулинотерапия. С помощью дозатора под контролем гликемии внутривенно вводят инсулин короткого действия из расчёта 0,1 ЕД на кг массы тела со скоростью 6-10 ЕД/ч.
- Регидратация. Для восполнения жидкости в организме необходимо ввести 0,9 % раствор натрия хлорида. В первый час вводят 1-1,5 литра физраствора до нормализации давления и восстановления объёма циркулирующей жидкости, во второй час — один литр. В третий-четвёртый час также вливают один литр жидкости: это может быть 0,9 % раствор натрия хлорида или 5 % раствор глюкозы. В дальнейшем в течение 8 часов вводится около 2 литров жидкости.
- Коррекция электролитных нарушений. Её начинают с введения 0,9 % раствора натрия хлорида. Так как в процессе регидратации и уменьшения глюкозы в крови снижается уровень калия, необходимо внутривенно вводить растворы калия.
- Ликвидация ацидоза. Проводится с помощью введения физрастворов. При низком рН (меньше 6,9) вводят 2 % раствор натрия гидрокарбоната. При этом также нужно следить за уровнем калия, при необходимости вливать его растворы.
- Лечение сопутствующих заболеваний, которые вызвали ацидоз (почечной недостаточности, ОРВИ и др.).
Лечение гиперосмолярной и кетоацидотической комы примерно одинаково. При высоком натрии (более 165 мэкв/л) вводить солевые растворы противопоказано — назначают 2 % раствор глюкозы. При понижении натрия до 145-165 мэкв/л необходимо вводить 0,45 % раствор натрия хлорида. При уровне натрия ниже 145 мэкв/л дальнейшее восполнение водного баланса проводят физраствором. Высокий уровень глюкозы в крови быстро снижать инсулином нельзя (скорость введения должна быть не больше 4-5 ммоль/л в час), а осмолярность плазмы должна снижаться не быстрее чем 10 мосмоль/л в час. Параллельно с этим проводят лечение сопутствующих заболеваний, которые привели к гиперосмолярной коме (острые инфекции и др.) [1][4][8][10].
Лечение лактацидотической комы основано на удалении избытка лактата из крови и восстановлении кислотно-щелочного состояния. Также необходимо снизить уровень глюкозы в крови. С этой целью проводится инсулинотерапия [1][4][6][9][10].
Прогноз. Профилактика
Прогноз при своевременной помощи пациенту с легкой гипогликемией благоприятный. В случае тяжёлой гипогликемии всё зависит от того, в какой стадии комы находился человек и развились ли у него осложнения.
Профилактика гипогликемической комы:
- Всегда иметь при себе быстроусвояемые углеводы не менее 2 ХЕ (хлебных единиц), например леденец, кусочек сахара или глюкозу.
- При незапланированной физической нагрузке обязательно принимать дополнительные углеводы (1-2 ХЕ).
- Перед походом в спортзал необходимо скорректировать инсулин и, если требуется, принять дополнительное количество углеводов в зависимости от уровня гликемии.
При возникновении лёгкой гипогликемии необходимо съесть 4 куска или 4 чайные ложки сахара (2 ХЕ), также допустим приём углеводов в жидкой форме (200 г сладкого сока или чая). Если гипогликемия вызвана приёмом большой дозы инсулина, то необходимо съесть 2 ХЕ быстрых углеводов (например кусок хлеба).
Прогноз при своевременном оказании помощи пациенту с диабетическим кетоацидозом также благоприятный. Летальность у детей и подростков не превышает 7 %, у взрослых — около 2 %. При длительном нарушении сознания, развитии дистресс-синдрома, очень высоких цифрах глюкозы в крови и развитии почечной недостаточности прогноз неблагоприятный [1][4][5][8][10].
Для профилактики кетоацидоза важно постоянно контролировать глюкозу в крови, при необходимости корректировать дозу инсулина, проверять его сроки годности и хранить в прохладном месте. Также важно менять иголку в шприце-ручке и места инъекций (чтобы не допустить истончения жировой ткани). При ОРВИ возможно потребуется увеличение дозы инсулина. Нельзя сидеть на безуглеводных диетах.
Прогноз при гиперосмолярной коме относительно благоприятный. Летальность достигает 15 %. Профилактика заключается в регулярном измерении гликемии крови с помощью глюкометра. В случае стойкого повышения уровня глюкозы в течение пару дней, особенно при тенденции к его росту или невозможности снижения, необходимо обратиться к врачу для подбора правильного лечения [1][2][6].
Лактацидемическая кома чаще всего приводит к летальному исходу. Её профилактика состоит в соблюдении показаний к назначению метформина и контроле лактата у пациентов с сахарным диабетом. При гипоксических состояниях метформин необходимо отменить. Сочетать приём метформина с алкоголем нежелательно [2][3][4][10].
Обморок – не отдельная болезнь и не диагноз, он представляет собой кратковременную потерю сознания вследствие острого снижения кровоснабжения мозга, сопровождаемого падением сердечно-сосудистой деятельности.
Наступает обморок или синкопальное состояние (синкопе), как его называют, внезапно и длится обычно недолго – несколько секунд. От обморока не застрахованы абсолютно здоровые люди, то есть, его не следует торопиться трактовать как признак тяжелого заболевания, лучше попробовать разобраться в классификации и причинах.
Классификация синкопе
К настоящим обморокам относят приступы кратковременной потери сознания, которые можно разделить на следующие виды:
- Нейрокардиогенная (нейромедиаторная) форма включает несколько клинических синдромов, поэтому считается термином собирательным. В основе формирования нейромедиаторного обморока лежит рефлекторное воздействие вегетативной нервной системы на сосудистый тонус и ритм сердечных сокращений, спровоцированное неблагоприятными для данного организма факторами (температура окружающей среды, психоэмоциональное напряжение, испуг, вид крови). Обмороки у детей (при отсутствии каких-либо значительных патологических изменений со стороны сердца и сосудов) или у подростков в период гормональной перестройки нередко имеют нейрокардиогенное происхождение. Также к синкопе такого рода относят вазовагальные и рефлекторные реакции, которые могут иметь место при кашле, мочеиспускании, глотании, физической нагрузке и других обстоятельствах, не связанных с сердечной патологией.
- Ортостатический коллапс или обморок развивается по причине замедления кровотока в головном мозге при резком переходе тела из горизонтального положения в вертикальное.
- Аритмогенный обморок. Этот вариант самый опасный. Он обусловлен формированием морфологических изменений в сердце и сосудах.
- Потеря сознания, в основе которой лежат цереброваскулярные расстройства (изменение сосудов головного мозга, нарушение мозгового кровообращения).

Между тем, некоторые состояния, называемые обмороком, не классифицируются как синкопе, хотя внешне его очень напоминают. К ним относят:
- Потерю сознания, связанную с метаболическими расстройствами (гипогликемия – падение содержания глюкозы в крови, кислородное голодание, гипервентиляция со снижением концентрации углекислого газа).
- Приступ эпилепсии.
- ТИА (транзиторная ишемическая атака) вертеброгенного происхождения.
Существует группа расстройств, напоминающих обморок, но протекающих без потери сознания:
- Кратковременное расслабление мускулатуры (катаплексия) в результате которого человек не может удержать равновесие и падает;
- Внезапно возникающее расстройство координации движений – острая атаксия;
- Синкопальные состояния психогенной природы;
- ТИА, обусловленная нарушением кровообращения в каротидном бассейне, сопровождающаяся потерей способности двигаться.
Самый частый случай

Значительная доля от всех обмороков принадлежит нейрокардиогенным формам. Потеря сознания, спровоцированная обычными бытовыми обстоятельствами (транспорт, душное помещение, стресс) или медицинскими процедурами (разные скопии, венепункция, иногда просто посещение кабинетов, напоминающих операционные), как правило, не имеет в основе развития изменений со стороны сердца и сосудов. Даже артериальное давление, которое в момент обморока снижается, вне приступа находится на нормальном уровне. Стало быть, вся ответственность за развитие приступа возлагается на вегетативную нервную систему, а именно, на ее отделы – симпатический и парасимпатический, которые по каким-либо причинам перестают работать согласованно.
Подобного рода обмороки у детей и подростков вызывают массу тревог со стороны родителей, которых нельзя успокоить только тем, что такое состояние не является следствием серьезной патологии. Повторяющиеся обмороки сопровождаются получением травм, что снижает качество жизни и может быть опасным в целом.
Почему пропадает сознание?
Человеку, далекому от медицины, классификация, в общем-то, не играет никакой роли. Большинство людей в приступе с потерей сознания, бледностью кожных покровов и падении усматривают обморок, но их нельзя обвинить в ошибке. Главное – поспешить на помощь, а какого рода потеря сознания – разберутся врачи, поэтому и мы не станем особенно переубеждать читателей.

Однако, исходя из классификации, но приняв во внимание тот факт, что не все знают ее тонкости, попытаемся определить причины обмороков, которые могут быть как банальными, так и серьезными:
- Жара – понятие для каждого свое, один человек сносно себя чувствует при 40°С, другому 25 – 28 – уже катастрофа, особенно, в закрытом, непроветренном помещении. Пожалуй, чаще всего подобные обмороки случаются в переполненном транспорте, где всем угодить трудно: кому-то дует, а кому-то дурно. Кроме этого, там нередко присутствуют и другие провоцирующие факторы (давка, запахи).
- Длительное отсутствие пищи или воды. Кое-что знают о голодном обмороке любители стремительной потери веса или люди, вынужденные голодать по другим, не зависящим от них причинам. Вызвать синкопе может диарея, упорная рвота или потеря жидкости, обусловленная другими обстоятельствами (частое мочеиспускание, усиленное потоотделение).
- Резкий переход из горизонтального положения тела (встал – перед глазами все поплыло).
- Чувство тревоги, сопровождаемое учащением дыхания.
- Беременность (перераспределение кровотока). Обмороки при беременности – явление нередкое, мало того, иногда именно потеря сознания относится к первым признакам интересного положения женщины. Свойственная беременности эмоциональная нестабильность на фоне гормональных изменений, жара на улице и в доме, боязнь набрать лишний килограмм (голод) провоцируют у женщины снижение артериального давления, которое влечет потерю сознания.
- Боль, шок, пищевое отравление.
- Нервное потрясение (почему, прежде чем сообщить какое-то страшное известие, человека, которому оно предназначается, попросят сначала присесть).
- Быстрая кровопотеря, например, доноры теряют сознание во время кроводачи отнюдь не потому, что ушел какой-то объем драгоценной жидкости, а по причине того, что он покинул кровеносное русло слишком быстро и организм не успел включить механизм защиты.
- Вид ран и крови. Кстати, у мужчин на кровь обмороки бывают чаще, чем у женщин, получается, что прекрасная половина к ней как-то привычнее.
-
Уменьшение объема циркулирующей крови (гиповолемия) при значительной кровопотере или вследствие приема мочегонных и вазодилататоров.
- Снижение артериального давления, сосудистый криз, причиной которого может быть несогласованная работа парасимпатического и симпатического отделов вегетативной нервной системы, ее несостоятельность в выполнении своих задач. Нередки обмороки у подростков, страдающих вегето-сосудистой дистонией по гипотоническому типу или дети в пубертатном периоде с диагностируемой экстрасистолией. А вообще, для гипотоников упасть в обморок – дело обычное, поэтому они сами начинают избегать передвижений в общественном транспорте, особенно, летом, посещений парилок в бане и всяких других мест, с которыми у них связаны неприятные воспоминания.
- Падение уровня сахара в крови (гипогликемия) – кстати, не обязательно при передозировке инсулина у больных сахарным диабетом. «Продвинутая» молодежь нашего времени знает, что этот препарат можно использовать для других целей (увеличить рост и вес, например), что может быть очень опасно (!).
- Анемия или то, что в народе называют малокровием.
- Неоднократно повторяющиеся обмороки у детей могут быть свидетельством серьезных заболеваний, например, синкопальные состояния нередко служат признаком нарушения сердечного ритма, которое довольно трудно распознать у ребенка раннего возраста, поскольку, в отличие от взрослых, сердечный выброс больше зависит от частоты сердечных сокращений (ЧСС), чем от ударного объема.
- Акт глотания при патологии пищевода (рефлекторная реакция, вызванная раздражением блуждающего нерва).
- Вызывающая сужение церебральных сосудов гипокапния, которая представляет собой уменьшение углекислого газа (СО2) за счет усиленного потребления кислорода при частом дыхании, свойственном для состоянии страха, паники, стресса.
- Мочеиспускание и кашель (за счет повышения внутригрудного давления, уменьшения венозного возврата и, соответственно, ограничения сердечного выброса и снижения артериального давления).
- Побочный эффект некоторых лекарственных средств или передозировка гипотензивных препаратов.
- Уменьшение кровоснабжения отдельных участков головного мозга (микроинсульт), хоть и редко, но может вызывать обморочное состояние у пожилых пациентов.
- Серьезная сердечно-сосудистая патология (инфаркт миокарда, субарахноидальное кровоизлияние и др.).
- Некоторые эндокринные заболевания.
- Объемные образования в головном мозге, затрудняющие кровоток.
Таким образом, чаще всего к потере сознания приводят изменения в системе кровообращения, вызванные падением артериального давления. Организм просто не успевает адаптироваться в короткий срок: давление снизилось, сердце не успело увеличить выброс крови, кровь не принесла мозгу достаточного количества кислорода.
Видео: причины обмороков – программа “Жить здорово!”
Причина – сердце
Между тем, не следует особо расслабляться, если синкопальные состояния становятся слишком частыми и причины обмороков не ясны. Обмороки у детей, подростков и у взрослых часто бывают следствием сердечно-сосудистой патологии, где не последняя роль принадлежит аритмиям различного рода (бради- и тахикардия):
- Связанным со слабостью синусового узла, высокой степенью атриовентрикулярной блокады, нарушением проводящей системы сердца (нередко у пожилых людей);
- Вызванным приемом сердечных гликозидов, антагонистов кальция, β-блокаторов, неправильным функционированием клапанного протеза;
- Обусловленным сердечной недостаточностью, интоксикацией лекарственными препаратами (хинидин), электролитным дисбалансом, недостатком углекислого газа в крови.

Сердечный выброс могут уменьшать и другие снижающие мозговой кровоток факторы, которые нередко присутствуют в сочетании: падение артериального давления, расширение периферических сосудов, снижение возврата венозной крови к сердцу, гиповолемия, сужение сосудов выносящего тракта.
Потеря сознания у «сердечников» при физической нагрузке относится к довольно серьезным показателям неблагополучия, поскольку причиной обморока в данном случае могут быть:
- ТЭЛА (тромбоэмболия легочной артерии);
- Легочная гипертензия;
- Стеноз аорты, расслаивающая аневризма аорты;
- Клапанные пороки: стеноз трикуспидального клапана (ТК) и клапана легочной артерии (ЛА);
- Кардиомиопатии;
- Тампонада сердца;
- Инфаркт миокарда;
- Миксома.
Конечно, такие перечисленные болезни редко бывают причиной обмороков у детей, в основном, они формируются в процессе жизни, поэтому являются печальным преимуществом солидного возраста.
Как выглядит обморок?
Обморочные состояния нередко сопровождают нейроциркуляторную дистонию. Гипоксия, вызванная падением артериального давления на фоне сосудистого криза, особо не дает времени для размышлений, хотя люди, для которых потеря сознания не является чем-то сверхъестественным, могут заранее предчувствовать приближение приступа и называют это состояние предобморочным. Симптомы, указывающие на приближение синкопе и сам обморок лучше описать вместе, поскольку начало ощущает сам человек, а собственно обморок видят окружающие. Как правило, придя в сознание, человек чувствует себя нормально, а о потере сознания напоминает лишь легкая слабость.

Итак, симптомы:
- «Мне дурно» – так свое состояние определяет пациент.
- Подступает тошнота, прошибает неприятный липкий холодный пот.
- Все тело слабеет, ноги подкашиваются.
- Кожные покровы бледнеют.
- В ушах звенит, перед глазами мелькают мушки.
- Потеря сознания: лицо сероватое, артериальное давление понижено, пульс слабый, обычно учащенный (тахикардия), хотя не исключена брадикардия, зрачки расширены, но на свет реагируют, хоть и с некоторым опозданием.
В большинстве случаев человек приходит в себя через несколько секунд. При более продолжительном приступе (5 минут и более) возможны судороги и непроизвольное мочеиспускание. Такой обморок незнающие люди могут легко спутать с приступом эпилепсии.
Таблица: как отличить истинный обморок от истерики или эпилепсии
Что делать?
Став очевидцем обморока, каждый человек обязан знать, как себя вести, хотя нередко потеря сознания обходится без всякой доврачебной помощи, если пациент быстро пришел в себя, не получил травм при падении и после синкопе самочувствие его более-менее нормализовалось. Первая помощь при обмороке сводится к выполнению несложных мероприятий:

- Слегка побрызгать на лицо холодной водой
- Уложить человека в горизонтальное положение, под ноги положить валик или подушку, чтобы они оказались выше головы.
- Расстегнуть ворот рубашки, ослабить галстук, обеспечить доступ свежего воздуха.
- Нашатырный спирт. Случись обморок – все бегут за этим средством, однако при этом иногда забывают, что обращаться с ним нужно осторожно. Вдыхание его паров может привести к рефлекторной остановке дыхания, то есть, нельзя подносить ватку, смоченную спиртом, слишком близко к носу потерявшего сознания.
Оказание неотложной помощи при синкопе больше связано с его первопричиной (нарушение ритма) или с последствиями (ушибы, порезы, черепно-мозговая травма). Если к тому же человек не спешит возвращаться в сознание, то следует насторожиться в отношении других причин обморока (падение уровня сахара в крови, эпилептический припадок, истерия). Кстати, что касается истерии, то люди, склонные к ней, способны упасть в обморок специально, главное, чтобы были зрители.
Вряд ли стоит самонадеянно выяснять происхождение затянувшегося обморока, не имея определенных навыков медицинской профессии. Наиболее разумным будет вызов «скорой», которая займется оказанием неотложной помощи и при необходимости доставит пострадавшего в стационар.
Видео: помощь при обмороке – доктор Комаровский
Как упасть в оборок специально / распознать имитацию
Вызвать приступ некоторым удается с помощью дыхания (дышать часто и глубоко) или, присев на корточки на некоторое время, резко подняться. Но тогда это может быть настоящий обморок?! Сымитировать же искусственный обморок довольно сложно, у здоровых людей это все-таки плохо получается.
Синкопе при истерии может ввести в заблуждение тех самых зрителей, но не врача: человек заранее продумывает, как упасть, чтобы не пораниться и это заметно, кожа его остается нормальной (разве что белилами предварительно намазаться?), а если (вдруг?) доходит дело до судорог, но и они вызваны отнюдь не непроизвольными сокращениями мускулатуры. Изгибаясь и принимая различные вычурные позы, больной лишь имитирует судорожный синдром.
Поиск причины
Беседа с доктором обещает быть долгой…

В начале диагностического процесса пациенту следует настроиться на обстоятельный разговор с врачом. Он будет задавать массу различных вопросов, подробный ответ на которые знает сам больной или родители, если дело касается ребенка:
- В каком возрасте появился первый обморок?
- Какие обстоятельства ему предшествовали?
- Как часто появляются приступы, одинаковы ли они по характеру?
- Какие провоцирующие факторы обычно приводят к обморочному состоянию (боль, жара, физическая нагрузка, стресс, голод, кашель и т.д.)?
- Что предпринимает пациент, когда подступает «чувство дурноты» (ложится, поворачивает голову, пьет воду, принимает пищу, пытается выйти на свежий воздух)?
- Каков по времени период до приступа?
- Особенности характера предобморочного состояния (звенит в ушах, кружится голова, темнеет в глазах, тошнит, болит в груди, голове, животе, учащенно бьется сердце или «замирает, останавливается, то стучит, то не стучит…», не хватает воздуха)?
- Продолжительность и клиника самого синкопе, то есть, как выглядит обморок со слов очевидцев (положение тела больного, цвет кожи, характер пульса и дыхания, уровень АД, наличие судорог, непроизвольное мочеиспускание, прикус языка, реакция зрачков)?
- Состояние после обморока, самочувствие пациента (пульс, дыхание, артериальное давление, хочется спать, болит и кружится голова, присутствует общая слабость)?
- Как чувствует себя обследуемый человек вне синкопальных состояний?
- Какие перенесенные или хронические болезни он у себя отмечает (или что рассказывали родители)?
- Какие фармацевтические средства пришлось применять в процессе жизни?
- Указывает ли пациент или его родственники, что в детском возрасте имели место параэпилептические феномены (ходил или говорил во сне, кричал по ночам, просыпался от страха и др.)?
- Семейный анамнез (подобные приступы у родственников, вегето-сосудистая дистония, эпилепсия, проблемы с сердцем и пр.).
Очевидно, то, что на первый взгляд кажется сущим пустяком, может играть ведущую роль в формировании синкопальных состояний, поэтому врач уделяет столь пристальное внимание разным мелочам. Кстати, пациент, отправляясь на прием, тоже должен хорошенько покопаться в своей жизни, чтобы помочь доктору открыть причину своих обмороков.
Осмотр, консультации, помощь оборудования
Осмотр больного, помимо определения конституционных особенностей, измерения пульса, давления (на обеих руках), прослушивания сердечных тонов, предполагает выявление патологических неврологических рефлексов, исследование функционирования вегетативной нервной системы, что, разумеется, без консультации невролога не обойдется.
Лабораторная диагностика предусматривает традиционные анализы крови и мочи (общие), анализ крови на сахар, сахарную кривую, а также ряд биохимических тестов в зависимости от предполагаемого диагноза. На первом этапе поиска пациенту в обязательном порядке делают электрокардиограмму и привлекают R –графические методы, если в этом есть необходимость.

В случае подозрения на аритмогенный характер синкопе основной акцент в диагностике приходится на исследование сердца:
- R –графия сердца и контрастирование пищевода;
- УЗИ сердца;
- холтеровское мониторирование;
- велоэргометрия;
- специальные методы диагностики сердечной патологии (в условиях стационара).
Если врач предполагает, что синкопальные состояния вызывают органические заболевания головного мозга или причина обмороков представляется смутно, спектр диагностических мероприятий заметно расширяется:
- R-графия черепа, турецкого седла (место расположения гипофиза), шейного отдела позвоночника;
- Консультация окулиста (поля зрения, глазное дно);
- ЭЭГ (электроэнцефалограмма), в том числе, мониторная, если имеет место подозрение на приступ эпилептического происхождения;
- ЭхоЭС (эхоэнцефалоскопия);
- Ультразвуковая диагностика с допплером (патология сосудов);
- КТ, МРТ (объемные образования, гидроцефалия).
Порой, даже перечисленные методы в полной мере не дают ответы на вопросы, поэтому не стоит удивляться, если пациенту будет предложено сдать анализ мочи на 17-кетостероидов или кровь на гормоны (щитовидной железы, половые, надпочечников), поскольку искать причину обмороков иногда бывает затруднительно.
Как лечить?
Тактика лечения и профилактики синкопальных состояний выстраивается в зависимости от причины обмороков. И это не всегда медикаментозные средства. Например, при вазовагальных и ортостатических реакциях больного, прежде всего, учат избегать ситуаций, провоцирующих синкопе. Для этого рекомендуют тренировать сосудистый тонус, проводить закаливающие процедуры, избегать душных помещений, резкой перемены положения тела, мужчинам советуют перейти на мочеиспускание сидя. Обычно отдельные моменты оговариваются с лечащим врачом, который учитывает происхождение приступов.

Обмороки, обусловленные падением артериального давления, лечат повышением АД также в зависимости от причины его снижения. Чаще всего этой причиной является нейроциркуляторная дистония, поэтому применяются препараты, воздействующие на вегетативную нервную систему.
Особого внимания заслуживают повторные обмороки, которые могут оказаться аритмогенной природы. Следует иметь в виду, что именно они повышают вероятность внезапной смерти, поэтому в подобных случаях самым серьезным образом лечат аритмию и болезни ее вызывающие.
Об обморочных состояниях нельзя сказать однозначно: безобидны они или опасны. Пока не выяснена причина, а приступы то и дело продолжают беспокоить пациента, прогноз может быть самым различным (даже крайне неблагоприятным), ведь он полностью зависит от природы этого состояния. Насколько высок риск – определит тщательный анамнез и всестороннее физикальное обследование, которое может стать первым шагом к тому, чтобы навсегда забыть об этом неприятном «сюрпризе», способном лишить сознания человека в самый неподходящий момент.
Глюкоза — важнейший компонент процессов метаболизма человека. Являясь источником энергии для жизнедеятельности клеток и, в частности, клеток мозга, она выполняет в организме пластические функции.
Внутри клеток свободная глюкоза практически отсутствует. В клетках глюкоза накапливается в виде гликогена. В ходе окисления она превращается в пируват и лактат (анаэробный путь) или в углекислый газ (аэробный путь), в жирные кислоты в виде триглицеридов. Глюкоза является составной частью молекулы нуклеотидов и нуклеиновых кислот. Глюкоза необходима для синтеза некоторых аминокислот, синтеза и окисления липидов, полисахаридов.
Концентрация глюкозы в крови человека поддерживается в относительно узких пределах — 2,8–7,8 ммоль/л, вне зависимости от пола и возраста, несмотря на большие различия в питании и физической активности (постпрандиальная гипергликемия — повышение уровня глюкозы в крови после приема пищи, стрессовых факторов и ее снижение через 3–4 часа после приема пищи и физической нагрузки). Это постоянство обеспечивает ткани мозга достаточным количеством глюкозы, единственного метаболического топлива, которое они могут использовать в обычных условиях.
В зависимости от способа поступления глюкозы все органы и ткани организма делятся на инсулинозависимые: глюкоза поступает в эти органы и ткани только при наличии инсулина (жировая ткань, мышцы, костная, соединительная ткань); инсулинонезависимые органы: глюкоза попадает в них по градиенту концентрации (головной мозг, глаза, надпочечники, гонады); относительно инсулинонезависимые органы: в качестве питательных веществ ткани этих органов используют свободные жирные кислоты (сердце, печень, почки). Поддержание глюкозы в определенных пределах — важная задача сложной системы гормональных факторов. Каждый раз при приеме пищи повышается уровень глюкозы и параллельно растет уровень инсулина. Инсулин способствует поступлению глюкозы в клетки, что не только предотвращает существенное увеличение ее концентрации в крови, но также обеспечивает глюкозой внутриклеточный метаболизм.
Концентрация инсулина в период голодания колеблется около 10 мкЕд/мл и повышается до 100 мкЕд/мл после обычного приема пищи, достигая максимальных значений через 30–45 минут после еды. Это влияние опосредуется через АТФ-чувствительные калиевые каналы, которые состоят из белковых субъединиц SUR-1 и Kir 6.2. Поступающая в бета-клетку глюкоза при участии фермента глюкокиназы подвергается превращению с образованием АТФ. Повышение АТФ способствует закрытию калиевых каналов. Концентрация калия в цитозоле клетки увеличивается. Таким же образом на эти каналы действуют и метаболиты глютамата, через окисление ферментом глютаматдекарбоксилазой. Повышение калия в клетке вызывает открытие кальциевых каналов, и кальций устремляется в клетку. Кальций способствует переносу секреторных гранул к периферии клетки и последующему выделению инсулина в межклеточное пространство, а затем в кровь [1]. Пищевыми секретогенами инсулина являются аминокислоты (лейцин, валин и др.). Их эффект усиливается гормонами тонкого кишечника (желудочный ингибирующий полипептид, секретин). Другие вещества стимулируют его выделение (препараты сульфанилмочевины, агонисты бета-адренорецепторов).
В кровь глюкоза поступает разными путями. После приема пищи, в течение 2–3 часов, экзогенные углеводы служат основным источником гликемии. У человека, занимающегося физическим трудом, в пище должно содержаться 400–500 г глюкозы. Между приемами пищи большая часть глюкозы в циркулирующую кровь поставляется за счет гликогенолиза (накопленный гликоген в печени разрушается до глюкозы, а гликоген в мышцах до лактата и пирувата). При голодании и истощении запасов гликогена глюконеогенез становятся источником глюкозы в крови (образование глюкозы из неуглеводных субстратов: лактата, пирувата, глицерина, аланина).
Большая часть пищевых углеводов представлена полисахаридами и состоит в основном из крахмалов; меньшая часть содержит лактозу (молочный сахар) и сахарозу. Переваривание крахмалов начинается в ротовой полости с помощью птиалина слюны, который продолжает свое гидролитическое действие и в желудке, пока pH среды не становится слишком низким. В тонком кишечнике амилаза поджелудочной железы расщепляет крахмалы до мальтозы и других полимеров глюкозы. Ферменты лактаза, сахараза и альфа-декстриназа, которые выделяются эпителиальными клетками щеточной каемки тонкой кишки, расщепляют все дисахариды на глюкозу, галактозу и фруктозу. Глюкоза, составляющая более 80% конечного продукта переваривания углеводов, сразу всасывается и поступает в воротный кровоток.
Глюкагон, синтезируемый А-клетками островков Лангерганса, изменяет доступность субстратов в интервалах между приемами пищи. Стимулируя гликогенолиз, он обеспечивает достаточный выход глюкозы из печени в ранний период времени после еды. По мере истощения запасов гликогена в печени, глюкагон вместе с кортизолом стимулируют глюконеогенез и обеспечивают поддержание нормальной гликемии натощак.
Во время ночного голодания глюкоза синтезируется исключительно в печени и ее большую часть (80%) потребляет головной мозг. В состоянии физиологического покоя интенсивность обмена глюкозы составляет примерно 2 мг/кг/мин. Люди с массой тела 70 кг нуждаются в 95–105 г глюкозы на 12-часовой интервал между ужином и завтраком. Гликогенолиз отвечает примерно за 75% ночной продукции глюкозы в печени; оставшуюся часть обеспечивает глюконеогенез. Основными субстратами для глюконеогенеза являются лактат, пируват и аминокислоты, особенно аланин и глицерин. Когда период голодания затягивается и содержание инсулина падает, глюконеогенез в печени становится единственным источником поддержания эугликемии, поскольку все запасы гликогена в печени уже израсходованы. Одновременно из жировой ткани метаболизируются жирные кислоты для обеспечения источника энергии для мышечной деятельности и доступной глюкозы для центральной нервной системы. Жирные кислоты окисляются в печени с образованием кетоновых тел — ацетоацетата и бета-гидроксибутирата.
Если голодание продолжается дни и недели, включаются другие гомеостатические механизмы, которые обеспечивают сохранение белковой структуры организма, замедляя глюконеогенез и переключая мозг на утилизацию кетоновых молекул, ацетоацетата и бета-гидроксибутирата. Сигналом для использования кетонов служит повышение их концентрации в артериальной крови. При длительном голодании и тяжелом течении диабета наблюдаются крайне низкие концентрации инсулина в крови.
Гипогликемия и гипогликемические состояния
Гипогликемией принято считать снижение концентрации глюкозы в крови ниже 2,5–2,8 ммоль/л у мужчин и менее 1,9–2,2 ммоль/л у женщин.
У здоровых людей угнетение эндогенной секреции инсулина после всасывания глюкозы в кровь начинается при концентрации 4,2–4 ммоль/л, при дальнейшем снижении ее — сопровождается выбросом контринсулярных гормонов. Спустя 3–5 часов после приема пищи прогрессивно уменьшается количество всасываемой глюкозы из кишечника и организм переключается на эндогенную выработку глюкозы (гликогенолиз, глюконеогенез, липолиз). Во время этого перехода возможно развитие функциональной гипогликемии: ранней — в первые 1,5–3 часа и поздней — через 3–5 часов. «Голодовая» гипогликемия не связана с приемом пищи и развивается натощак или через 5 часов после ее приема. Нет жесткой корреляции между уровнем глюкозы в крови и клиническими симптомами гипогликемии.
Проявления гипогликемии
Гипогликемия больше клиническое понятие, нежели лабораторное, симптомы которой исчезают после нормализации содержания глюкозы в крови. На развитие симптомов гипогликемии влияет быстрое снижение глюкозы в крови. Об этом свидетельствуют факторы быстрого снижения высокой гликемии у больных сахарным диабетом. Появление клинических симптомов гипогликемии наблюдается у этих больных с высокими показателями гликемии при активной инсулинотерапии.
Симптомы гипогликемии отличаются полиморфизмом и неспецифичностью. Для гипогликемической болезни патогомоничной является триада Уиппла:
- возникновение приступов гипогликемии после длительного голодания или физической нагрузки;
- снижение содержания сахара в крови во время приступа ниже 1,7 ммоль/л у детей до двух лет, ниже 2,2 ммоль/л — старше двух лет;
- купирование гипогликемического приступа внутривенным введением глюкозы или пероральным приемом растворов глюкозы.
Симптомы гипогликемии обусловлены двумя факторами:
- стимуляцией симпатикоадреналовой системы, в результате чего усиливается секреция катехоламинов;
- дефицитом снабжения глюкозой головного мозга (нейрогликемия), что равносильно снижению потребления кислорода нервными клетками.
Такие симптомы, как обильное потоотделение, постоянное чувство голода, ощущение покалывания губ и пальцев, бледность, сердцебиение, мелкая дрожь, мышечная слабость и утомляемость, обусловлены возбуждением симпатоадреналовой системы. Эти симптомы являются ранними предвестниками приступа гипогликемии.
Нейрогликемические симптомы проявляются головной болью, зевотой, невозможностью сосредоточиться, утомляемостью, неадекватностью поведения, галлюцинациями. Иногда возникают и психические симптомы в виде депрессии и раздражительности, дремотного состояния днем и бессонницы по ночам. Из-за разнообразия симптомов гипогликемии, среди которых часто доминирует реакция тревоги, многим больным ставят ошибочные диагнозы невроза или депрессии.
Длительная и глубокая гипогликемическая кома может вызвать отек и набухание головного мозга с последующим необратимым повреждением ЦНС. Частые приступы гипогликемии приводят к изменению личности у взрослых, снижению интеллекта у детей. Отличие симптомов гипогликемии от настоящих неврологических состояний — положительный эффект приема пищи, обилие симптомов, не укладывающихся в клинику неврологического заболевания.
Наличие выраженных нервно-психических нарушений и недостаточная осведомленность врачей о гипогликемических состояниях часто приводят к тому, что вследствие диагностических ошибок больные с органическим гиперинсулинизмом длительно и безуспешно лечатся под самыми разными диагнозами. Ошибочные диагнозы ставятся у 3/4 больных с инсулиномой (эпилепсия диагностируется в 34% случаев, опухоль головного мозга — в 15%, вегетососудистая дистония — в 11%, диэнцефальный синдром — в 9%, психозы, неврастения — в 3% [2]).
Большинство симптомов гипогликемии обусловлены недостаточным снабжением центральной нервной системы глюкозой. Это приводит к быстрому повышению содержания адреналина, норадреналина, кортизола, гормона роста, глюкагона.
Эпизодические гипогликемические состояния могут компенсироваться срабатыванием контринсулярных механизмов или приемом пищи. В том случае, если этого недостаточно, развивается обморочное состояние или даже кома.
Гипогликемическая кома
Гипогликемическая кома — это состояние, которое развивается при снижении уровня глюкозы в крови до 2,2 ммоль/л и ниже. При быстром падении сахара в крови может развиваться стремительно, без предвестников и иногда даже внезапно.
При непродолжительной коме кожа обычно бледная, влажная, ее тургор сохранен. Тонус глазных яблок обычный, зрачки широкие. Язык влажный. Характерна тахикардия. Артериальное давление (АД) нормальное или слегка повышенное. Дыхание обычное. Температура нормальная. Мышечный тонус, сухожильные и периостальные рефлексы повышены. Могут отмечаться мышечная дрожь, судорожные подергивания мимической мускулатуры.
По мере углубления и увеличения продолжительности комы прекращается потоотделение, учащается и становится поверхностным дыхание, снижается АД, иногда появляется брадикардия. Отчетливо нарастают изменения в неврологическом статусе: появляются патологические симптомы — нистагм, анизокория, явления менингизма, пирамидные знаки, снижается мышечный тонус, угнетаются сухожильные и брюшные рефлексы. В затянувшихся случаях возможен летальный исход.
Особую опасность гипогликемические приступы представляют у пожилых лиц, страдающих ишемической болезнью сердца и мозга. Гипогликемия может осложниться инфарктом миокарда или инсультом, поэтому контроль ЭКГ обязателен после купирования гипогликемического состояния. Частые, тяжелые, продолжительные гипогликемические эпизоды постепенно приводят к энцефалопатии, а затем и к деградации личности.
Причины гипогликемии
Гипогликемия — это синдром, который может развиваться как у здоровых людей, так и при различных заболеваниях (таблица).
Гипогликемии при недостаточности продукции глюкозы
Дефицит гормонов
Гипогликемия всегда встречается при пангипопитуитаризме — заболевании, характеризующемся снижением и выпадением функции передней доли гипофиза (секреции адренокортикотропина, пролактина, соматотропина, фоллитропина, лютропина, тиреотропина). В результате резко снижается функция периферических эндокринных желез. Однако гипогликемия встречается и при первичном поражении эндокринных органов (врожденная дисфункция коры надпочечников, болезнь Аддисона, гипотиреоз, гипофункция мозгового слоя надпочечников, дефиците глюкагона). При дефиците контринсулярных гормонов снижается скорость глюконеогенеза в печени (влияние на синтез ключевых ферментов), повышается утилизация глюкозы на периферии, снижается образование аминокислот в мышцах — субстрата для глюконеогенеза.
Дефицит глюкокортикоидов
Первичная надпочечниковая недостаточность является следствием уменьшения секреции гормонов коры надпочечников. Под этим термином подразумевают различные по этиологии и патогенезу варианты гипокортицизма. Симптомы надпочечниковой недостаточности развиваются только после разрушения 90% объема ткани надпочечников.
Причины гипогликемии при надпочечниковой недостаточности схожи с причинами гипогликемии при гипопитуитаризме. Отличием является уровень возникновения блока — при гипопитуитаризме снижается секреция кортизола из-за дефицита АКТГ, а при надпочечниковой недостаточности из-за разрушения ткани самих надпочечников.
Гипогликемические состояния у больных с хронической надпочечниковой недостаточностью могут возникать как натощак, так и через 2–3 часа после приема пищи, богатой углеводами. Приступы сопровождаются слабостью, чувством голода, потливостью. Гипогликемия развивается в результате снижения секреции кортизола, уменьшения глюконеогенеза, запасов гликогена в печени.
Дефицит катехоламинов
Данное состояние может возникать при надпочечниковой недостаточности с поражением мозгового слоя надпочечников. Катехоламины, попадая в кровь, регулируют высвобождение и метаболизм инсулина, снижая его, а также увеличивают высвобождение глюкагона. При снижении секреции катехоламинов наблюдаются гипогликемические состояния, вызванные избыточной продукцией инсулина и пониженной активностью гликогенолиза.
Дефицит глюкагона
Глюкагон — гормон, являющийся физиологическим антагонистом инсулина. Он участвует в регуляции углеводного обмена, влияет на жировой обмен, активируя ферменты, расщепляющие жиры. Основное количество глюкагона синтезируется альфа-клетками островков поджелудочной железы. Однако установлено, что специальные клетки слизистой оболочки двенадцатиперстной кишки и слизистой оболочки желудка также синтезируют глюкагон. При поступлении в кровоток глюкагон вызывает повышение в крови концентрации глюкозы, вплоть до развития гипергликемии. В норме глюкагон предотвращает чрезмерное снижение концентрации глюкозы. Благодаря существованию глюкагона, препятствующего гипогликемическому действию инсулина, достигается тонкая регуляция обмена глюкозы в организме.
Некоторые гипоталамо-гипофизарные синдромы могут сопровождаться гипогликемией: синдром Лоренса–Муна–Бидля–Борде, синдром Дебре–Мари, синдром Пехкранца–Бабинского (адипозогенетальная дистрофия).
- Синдром Лоренса–Муна–Бидля–Борде характеризуется ожирением, гипогонадизмом, умственной отсталостью, дегенерацией сетчатки, полидактилией, глубокими дегенеративными изменениями гипоталамо-гипофизарной системы.
- Синдром Дебре–Мари — заболевание обусловлено гиперфункцией задней доли гипофиза и гипофункцией аденогипофиза. Проявляется в раннем детском возрасте. Больные инфантильны, низкорослы, с избыточной массой. В клинической картине типично нарушение водного обмена с олигурией и олигодипсией, плотность мочи высокая. Психическое развитие не нарушено.
- Синдром Пехкранца–Бабинского — причиной заболевания считают органические и воспалительные изменения гипоталамуса, которые ведут к ожирению, аномалиям развития скелета и гипоплазии половых органов.
При этих синдромах содержание инсулина снижено, а экскреция кетоновых тел с мочой повышена.
Гипогликемии при дефиците ферментов
Дефект фермента глюкозо-6-фосфатазы (болезнь Гирке)
Дефицит глюкозо-6-фосфатазы составляет основу болезни Гирке, или гликогеноза типа 1. Недостаточность этого фермента приводит к невозможности превращения глюкозо-6-фосфата в глюкозу, что сопровождается накоплением гликогена в печени и почках. Болезнь наследуется по аутосомно-рецессивному типу.
Поступление глюкозы в организм с пищей, в принципе, дает возможность поддерживать в крови нормальный уровень глюкозы, однако для этого поступление пищи, содержащей глюкозу, должно быть практически непрерывным. В реальных условиях существования, т. е. при отсутствии непрерывного поступления глюкозы, в здоровом организме последняя депонируется в виде гликогена, который при необходимости используется при его полимеризации.
Первичное нарушение при болезни Гирке происходит на генетическом уровне. Оно состоит в полной или почти полной неспособности клеток продуцировать глюкозо-6-фосфатазу, обеспечивающую отщепление свободной глюкозы от глюкозо-6-фосфата. В результате этого гликогенолиз прерывается на уровне глюкозо-6-фосфата и дальше не идет. Дефосфорилирование с участием глюкозо-6-фосфатазы является ключевой реакцией не только гликогенолиза, но и глюконеогенеза, который, таким образом, при болезни Гирке также прерывается на уровне глюкозо-6-фосфата. Возникновение устойчивой гипогликемии, которая в реальных условиях неизбежна из-за непоступления в кровь глюкозы как конечного продукта гликогенолиза и глюконеогенеза, в свою очередь приводит к постоянной повышенной секреции глюкагона как стимулятора гликогенолиза. Глюкагон, однако, в условиях прерывания этого процесса способен лишь без пользы для организма непрерывно стимулировать его начальные стадии.
Если недостаток фермента умеренный, больные достигают юношеского, а нередко и более старшего возраста. Однако психическое и соматическое развитие, а также биохимический статус (повышение уровня триглицеридов, холестерина, гиперурикемия, гипофосфатемия) у этих больных резко нарушены. Характерными чертами являются олигофрения, задержка роста, ожирение, остеопороз, большой живот (следствие увеличения печени и почек), ксантоматоз, липемия сетчатки, геморрагический диатез. Содержание глюкозы в плазме натощак постоянно снижено, в связи с чем даже при кратковременном голодании развиваются гипогликемические судороги, кетонурия и метаболический ацидоз. Последний обусловлен не только гиперкетонемией, но и повышенным накоплением и образованием в крови пирувата и лактата, что является результатом нарушенного глюконеогенеза. Нарушение обмена липидов сопровождается панкреатитом.
Диагноз основывается на данных клинической картины, сниженного содержания глюкозы и повышенной концентрации липидов и лактата в крови. Уровень глюкозы в плазме практически не меняется после введения глюкагона. Однако содержание лактата в крови после его введения возрастает. Биопсия печени, специальные гистохимические методы подтверждают недостаточность соответствующих ферментов [3].
Дефицит амило-1,6-глюкозидазы
Недостаточность амило-1,6-глюкозидазы, обозначаемая как гликогеноз типа 3 или болезнь Кори, относится к числу наиболее частых гликогенозов и имеет относительно легкое клиническое течение. Функция данного фермента заключается в деградации белковых ветвей гликогена и отщеплении от них свободной глюкозы. Однако снижение содержания глюкозы в крови при этом заболевании не настолько существенное, как при гликогенозе типа 1, так как определенное количество глюкозы образуется активированием фосфорилазы в печени. Для клинической картины заболевания характерны гепатомегалия, мышечная слабость, задержка роста и периодические «голодовые» гипогликемии. При лабораторном исследовании выявляется повышение уровня печеночных трансаминаз. Содержание лактата и мочевой кислоты в плазме крови обычно в норме. В ответ на введение глюкагона отсутствует повышение содержания глюкозы в плазме крови, если проба с глюкагоном проводится натощак, тогда как при введении глюкагона через 2 часа после приема пищи — ответ уже нормальный. Для подтверждения диагноза необходима биопсия печени и мышц, в которых выявляют измененный гликоген и недостаточность соответствующего фермента.
Дефект печеночной фосфорилазы — болезнь Герса
Гликогеноз, вызванный недостаточностью фосфорилазы печени (гликогеновая болезнь типа 6). Фосфорилаза печени катализирует фосфорилирование (расщепление) гликогена с образованием глюкозо-1-фосфата. Нарушение этого механизма приводит к избыточному отложению гликогена в печени. Наследуется предположительно по аутосомно-рецессивному типу.
Проявляется обычно на первом году жизни. Характерны задержка роста, кукольное лицо, значительное увеличение печени в результате гликогенной инфильтрации гепатоцитов, гипогликемия, гиперлипемия, повышенное содержание гликогена в эритроцитах. Диагноз основывается на снижении активности фосфорилазы в лейкоцитах.
Недостаточность гликогенсинтетазы
Очень редкое наследственное заболевание. У больных, имеющих дефект синтеза этого фермента, гликоген вообще не синтезируется. Голодание вызывает тяжелую гипогликемию.
Недостаточность фосфоэнолпируваткарбоксикиназы
Фосфоэнолпируваткарбоксикиназа — ключевой фермент глюконеогенеза. Дефект данного фермента является очень редкой причиной гипогликемии. Фосфоэнолпируваткарбоксикиназа участвует в синтезе глюкозы из лактата, метаболитов цикла Кребса, аминокислот и жирных кислот. Поэтому при недостаточности этого фермента инфузия лактата или аланина не позволяет добиться нормогликемии. Напротив, введение глицерина нормализует концентрацию глюкозы, поскольку для синтеза глюкозы из глицерина фосфоэнолпируваткарбоксикиназа не требуется. При тяжелой гипогликемии проводят инфузию глюкозы.
Голодовые гипогликемии
Тяжелое нарушение питания
Голодание — самая распространенная причина гипогликемии у здоровых людей. При голодании глюкоза не поступает в организм, но продолжает потребляться мышцами и другими органами. Во время кратковременного голодания дефицит глюкозы покрывается за счет гликогенолиза и глюконеогенеза в печени. При длительном голодании запасы гликогена в печени истощаются и возникает гипогликемия.
Гипогликемия нередко случается у людей, соблюдающих религиозные каноны в питании (например, у православных во время Великого Поста и у мусульман во время Рамадана). Понятно, что в таких случаях гипогликемия обусловлена полным или практически полным длительным отсутствием пищи.
Эта же форма гипогликемии развивается на фоне изнуряющей физической нагрузки, например, при беге, плавании и велогонках на длительные дистанции, у многоборцев, альпинистов, лыжников, культуристов. В таких ситуациях основная причина гипогликемии — усиленное потребление глюкозы мышцами.
Гипогликемия во время беременности
Все виды обмена веществ во время беременности претерпевают значительные изменения, перестраиваются ферментативные реакции. Глюкоза является основным материалом для обеспечения энергетических потребностей плода и матери. С прогрессированием беременности расход глюкозы непрерывно увеличивается, что требует постоянной перестройки регулирующих механизмов. Увеличивается секреция как гипергликемических гормонов (глюкагон, эстрогены, кортизол, гипофизарный пролактин, плацентарный лактоген, соматотропин), так и гипогликемического гормона инсулина. Таким образом устанавливается динамическое равновесие механизмов, регулирующих углеводный обмен. Уровень глюкозы в крови у беременных женщин остается в пределах нормы, полностью обеспечивается при этом потребность в глюкозе организмов матери и плода.
На поздних сроках беременности, на фоне истощения компенсаторных механизмов, может возникать гипогликемическое состояние. Клиническая картина гипогликемии беременных включает в себя чувство голода, головную боль, потливость, слабость, тремор, тошноту, парестезии, нечеткость и сужение полей зрения, спутанность сознания, сопор, потерю сознания, кому и судороги.
Приобретенные заболевания печени
Диффузное и тяжелое поражение печени, при котором выходит из строя 80–85% ее массы, может привести к гипогликемии вследствие нарушения гликогенолиза и глюконеогенеза. Это связывают с такими поражениями, как острый некроз печени, острый вирусный гепатит, синдром Рейе и тяжелая пассивная застойная сердечная недостаточность. Метастатическая или первичная опухоль печени (если затрагивается большая часть печеночной ткани) может вызвать гипогликемию, но метастазы в печень обычно не сопровождаются гипогликемией. Гипогликемия была описана как часть синдрома жирового перерождения печени при беременности. Сообщалось также о сочетании гипогликемии с HELLP синдромом (гемолиз, повышенный уровень печеночных ферментов и снижение числа тромбоцитов в периферической крови). Во время беременности могут иметь место самые различные поражения печени — от преэклампсии и HELLP синдрома до острого жирового ее перерождения. Поэтому у всех нездоровых женщин в III триместре беременности следует определять уровень глюкозы. Хроническое заболевание печени очень редко сопровождается гипогликемией. Больные с тяжелой печеночной недостаточностью, способной вызвать гипогликемию, часто находятся в коматозном состоянии. Гипогликемия как причина коматозного состояния может быть пропущена, если кома расценивается как следствие печеночной энцефалопатии.
Гипогликемией может сопровождаться хроническая почечная недостаточность. Это связано с тем, что здоровая почка способна к глюконеогенезу. В некоторых случаях этот процесс составляет до 50% образуемой эндогенной глюкозы. При уремии глюконеогенез может быть подавлен. К тому же почка вырабатывает инсулиназы, разрушающие инсулин, который у больных с хронической почечной недостаточностью кумулируется. По этой же причине опасность гипогликемии увеличивается и у больных с сахарным диабетом, осложненным хронической почечной недостаточностью.
Алкоголь и медикаменты
Употребление спиртных напитков — распространенная причина гипогликемии как у взрослых людей, так и у детей. Расщепление этанола с образованием ацетальдегида в печени катализируется ферментом алкогольдегидрогеназой. Этот фермент работает только в присутствии особого кофактора — никотинамиддинуклеотида (НАД). Но это же вещество необходимо и для печеночного глюконеогенеза. Прием алкоголя приводит к быстрому расходованию НАД и резкому торможению глюконеогенеза. Поэтому алкогольная гипогликемия возникает при истощении запасов гликогена, когда для поддержания нормального уровня глюкозы в крови особенно необходим глюконеогенез. При приеме большого количества алкоголя вечером, симптомы гипогликемии обычно возникают на следующее утро.
Чаще всего алкогольная гипогликемия наблюдается у истощенных больных алкоголизмом, но бывает и у здоровых людей после приемов большого количества алкоголя или при употреблении алкоголя «на голодный желудок».
Алкогольная гипогликемия нередко случается у детей, которые по ошибке или намеренно выпивают пиво, вино или более крепкие напитки. Особенно чувствительны к алкоголю дети до 6 лет — алкогольная гипогликемия встречается после спиртовых компрессов. Смертность при алкогольной гипогликемии у детей достигает 30%, тогда как у взрослых она составляет примерно 10%. [4]. Диагноз алкогольной гипогликемии основывается на данных анамнеза и обнаружении гипогликемии в сочетании с повышенным уровнем алкоголя и молочной кислоты в крови.
Описаны случаи гипогликемии при приеме неселективных бета-блокаторов. Они применяются для лечения ишемической болезни сердца, нарушений сердечного ритма, а также некоторых форм гипертонической болезни. Такой эффект обусловлен повышенной утилизацией глюкозы мышцами, снижением образования глюкозы из гликогена, ингибированием липолиза и снижением содержания неэстерифицированных жирных кислот в крови. Бета-блокаторы не рекомендуется применять в случае инсулинозависимого сахарного диабета, потому что они маскируют большинство симптомов гипогликемии и могут быть токсичными для клеток островков поджелудочной железы. Также стоит помнить, что при одновременном применении пропранолола и гипогликемических препаратов существует риск развития гипогликемии, за счет усиления их действия.
Гипогликемию могут вызвать противовоспалительные и обезболивающие препараты из класса салицилатов (Парацетамол, Аспирин). Салицилаты оказывают влияние на обмен веществ: при введении в больших дозах наблюдаются уменьшение синтеза и увеличение распада аминокислот, белков и жирных кислот. При сахарном диабете салицилаты способствуют снижению содержания глюкозы в крови. Также салицилаты, как и бета-адреноблокаторы, усиливают действие препаратов, применяемых для снижения уровня сахара в крови.
Гипогликемии, связанные с повышением потребления глюкозы
Инсулинома
Инсулинома — инсулинпродуцирующая опухоль, происходящая из бета-клеток островков Лангерганса, обуславливающая развитие гипогликемического синдрома натощак. В опухолевых клетках нарушена секреция инсулина: секреция не подавляется при снижении уровня глюкозы крови. В 85–90% случаев опухоль солитарная и доброкачественная, только в 10–15% случаев опухоли множественные, и крайне редко опухоли расположены вне поджелудочной железы (ворота селезенки, печень, стенка двенадцатиперстной кишки). Частота новых случаев опухоли — 12 на 1 млн человек в год, чаще всего опухоль диагностируется в возрасте от 25 до 55 лет.
В клинике при инсулиноме характерны приступы гипогликемии, связанные с постоянным, независимым от уровня глюкозы в крови, выбросом инсулина. Частые приступы гипогликемии вызывают изменения в центральной нервной системе. У некоторых больных они напоминают эпилептический припадок, с которым госпитализируют в неврологическое отделение. Приступы гипогликемии прерываются приемом пищи, в связи с чем больные постоянно употребляют большое количество продуктов, главным образом углеводов, что способствует развитию ожирения.
Диагностика инсулиномы базируется на выявлении классической и патогомоничной для нее триады Уиппла, а также типичной для гипогликемии клинической картины. «Золотым стандартом» на первом этапе диагностики гипогликемического синдрома и подтверждения эндогенного гиперинсулинизма является проба с голоданием. Проба проводится в течение 72 часов и считается положительной при развитии триады Уиппла. Начало голодания отмечают как время последнего приема пищи. Уровень глюкозы в крови на пробе оценивают исходно через 3 часа после последнего приема пищи, затем через каждые 6 часов, а при снижении уровня глюкозы в крови ниже 3,4 ммоль/л интервал между ее исследованиями сокращают до 30–60 мин.
Скорость секреции инсулина при инсулиноме не угнетается снижением уровня глюкозы в крови. У находящихся в условиях голодания больных инсулиномой гипогликемия развивается в связи с тем, что количество глюкозы в крови натощак зависит от интенсивности гликогенолиза и глюконеогеноза в печени, а избыточная инсулиносекреция блокирует продукцию глюкозы. Рекомендуется вычислить инсулин/гликемический индекс. В норме он составляет не более 0,3, а при инсулиноме превышает 1,0. Концентрация С-пептида также резко повышена.
Вторым этапом в диагностике инсулиномы является топическая диагностика опухоли. Используют УЗИ, компьютерную томографию, магниторезонансную томографию, эндоскопическое УЗИ, сцинтиграфию, ангиографию, интраоперационное УЗИ. Наиболее информативны в диагностике инсулином эндоскопическое ультразвуковое исследование (эндо-УЗИ) и забор крови из печеночных вен после внутриартериальной стимуляции поджелудочной железы кальцием. Многим пациентам, с помощью современных методов исследования, удается на дооперационном этапе установить локализацию опухоли, ее размер, стадию и темпы прогрессирования опухолевого процесса, выявить метастазы.
Определенные трудности в диагностике инсулиномы могут возникнуть у пациентов, применяющих препараты инсулина или сульфанилмочевины. Для доказательства экзогенного введения инсулина необходимо посмотреть анализ крови: при экзогенном введении инсулина в крови обнаружатся антитела к инсулину, низкий уровень С-пептида при высоком уровне общего иммунореактивного инсулина (ИРИ). С целью исключения гипогликемии, вызванной приемом препаратов сульфанилмочевины, целесообразным будет определение содержания сульфанилмочевины в моче.
Лечение инсулиномы в большинстве случаев хирургическое: энуклеация опухоли, дистальная резекция поджелудочной железы. Консервативная терапия проводится в случае нерезектабельной опухоли и ее метастазов, а также при отказе пациента от оперативного лечения и включает в себя:
- химиотерапию (стрептозотоцин, 5-Фторурацил Эбеве, Эпирубицин-Эбеве);
- биотерапию (аналоги соматостатина (Октреотид-депо, Сандостатин Лар);
- иммунотерапию (интерферон альфа);
- устранение или снижение симптомов гипогликемии (диазоксид, глюкокортикоиды, фенитоин).
Пятилетняя выживаемость среди радикально прооперированных пациентов — 90%, при обнаружении метастазов — 20% [5].
Гиперплазия бета-клеток у новорожденных и грудных детей
Инсулиному следует дифференцировать с гиперплазией или увеличением количества островков поджелудочной железы. В норме объем эндокринной части составляет 1–2% у взрослых и 10% у новорожденных. У детей раннего возраста гиперплазия островков встречается при незидиобластозе, фетальном эритробластозе, синдроме Беквита–Видемана, а также у детей, родившихся от матерей с сахарным диабетом.
Незидиобластоз
Незидиобластоз — врожденная дисплазия эндокринных клеток (микроаденоматоз). Из незидиобластов, которые внутриутробно формируются из эпителия панкреатических протоков, образуются островки Лангерганса. Этот процесс начинается с 10–19 недели внутриутробного развития и заканчивается на 1–2 году жизни ребенка. В некоторых случаях формирование эндокринных клеток может ускоряться или образовываются дополнительные клетки в ацинарной ткани поджелудочной железы. Подобные нарушения, которые имеют транзиторный характер, часто встречаются в нормально развивающейся ткани поджелудочной железы. Считается, что до двух лет незидиобластоз является вариантом нормы, у детей старше двух лет представляет патологию. Клетки, формирующие очаг незидиобластоза, дают положительную реакцию на инсулин, глюкагон, соматостатин и панкреатический полипептид. Однако пропорция бета-клеток значительно выше, чем в норме. Дисплазия эндокринной части поджелудочной железы сочетается с множественной эндокринной неоплазией типа 1 (МЭН 1). Незидиобластоз сопровождается нерегулируемой секрецией инсулина и выраженной гипогликемией.
Некоторые авторы предполагают ввести термин «врожденный гиперинсулинизм», под которым понимают все разновидности незидиобластоза, а конкретную форму следует ставить после гистологической диагностики [1]. Гиперинсулинемическая гипогликемия встречается у детей, родившихся от матерей, болеющих сахарным диабетом. Патогенез гипогликемии у таких новорожденных вызван тем, что внутриутробно избыточное количество глюкозы диффундирует от беременной к плоду и вызывает у последнего гипертрофию островкового аппарата. После рождения ребенка бета-клетки продолжают избыточно вырабатывать инсулин, вызывая у части детей симптомы гипогликемии. Следует учитывать, что при длительном введении концентрированных растворов глюкозы беременным возможно развитие транзиторной гипогликемии у новорожденных.
Гиперплазия островкового аппарата у новорожденных может встречаться при гемолитической болезни. Разрушение эритроцитов внутриутробно сопровождается деградацией инсулина, что вызывает гипертрофию бета-клеток. Лечение таких больных заменным переливанием крови прекращает гемолиз, а следовательно, разрушение инсулина. Но транзиторная гипогликемия сохраняется некоторое время [6]. В периоде новорожденности гипогликемия может быть проявлением у детей синдрома Видемана–Беквита. Причиной тяжелой неонатальной гипогликемии является гипертрофия и гиперплазия островков поджелудочной железы. Дети рождаются крупные. Характерно увеличение органов: печени, почек, поджелудочной железы. Типичны наличие кисты пупочного канатика, макроглосия, различные органные аномалии. Если больные не погибают в неонатальном периоде, то отставание в психическом развитии связывают с гипогликемическими состояниями.
Аутосомно-рецессивная гиперинсулинемическая гипогликемия
Семейное заболевание, которое является следствием мутации генов, ответственных за синтез белка SUR-1 и Kir 6.2, которые находятся на хромосоме 11 р151. Изоформа белка SUR-1, обозначаемая как SUR-2, участвует в функции калиевых каналов, локализованных внепанкреатически, т. е. в тканях других органов. Любое нарушение, приводящее к потере функции SUR-1 или Kir 6.2, способствует нерегулярному закрытию АТФ-чувствительных калиевых каналов, деполяризации мембран бета-клетки, увеличению выхода кальция и повышению высокого уровня базальной его концентрации в цитозоле и, наконец, нерегулируемой секреции инсулина.
Гипогликемия при сахарном диабете
У больных сахарным диабетом гипогликемия представляет серьезную проблему при лечении сахароснижающими препаратами. Это связано с тем, что снижены запасы гликогена в печени, который в экстренных случаях должен пополнять глюкозой кровь.
Основные причины гипогликемии при лечении сахарного диабета это передозировка инсулина, т. е. несоответствие дозы инсулина и количества углеводов в пище, задержка приема пищи, чрезмерные физические нагрузки, инъекция инсулина в мышцу, приводящая к более быстрому всасыванию его, или инъекции инсулина в участки липодистрофии, откуда он всасывается с разной скоростью. Риск развития гипогликемии у больных сахарным диабетом увеличивается в связи с внедрением интенсифицированной инсулинотерапии, которая предполагает поддержание гликемии в течение суток близких к нормальным значениям глюкозы в крови. Этим провоцируется риск развития гипогликемии. Нижняя граница концентрации глюкозы рекомендуется ограничить в пределах 4–4,2 ммоль/л.
Не распознанная гипогликемия у больных с длительным сахарным диабетом может возникать во сне (феномен Сомоджи). На это состояние организм реагирует избыточной секрецией контринсулярных гормонов. В утренние часы показатели глюкозы в крови значительно возрастают, и их неправильно оценивают как следствие недостаточной дозы инсулина. В связи с этим увеличивается доза препарата, тем самым ухудшается течение сахарного диабета. В этом случае заболевание протекает с резкими колебаниями гликемии в течение суток [7]. Учитывая большое количество препаратов инсулина, используемых в разных клиниках, стоит помнить отличия животного и синтетического инсулина в проявлениях симптомов гипогликемии при передозировке данных препаратов.
При лечении синтетическими человеческими инсулинами, а также у больных с нейропатией симптомы надвигающейся тяжелой гипогликемии носят нейрогликопенический характер. Она развивается неожиданно и очень быстро. Нарушается координация и концентрация внимания. Больной теряет сознание, или возникает эпилептиформный судорожный припадок. По этой причине больной слишком поздно осознает угрозу гипогликемии. Самостоятельный выход из нее затруднен. С этой формой гипогликемической комы связаны отек и набухание головного мозга и развитие постгликемической энцефалопатии.
При передозировке животным инсулином началу гипогликемического приступа предшествуют так называемые «адреналиновые симптомы»: ранние — острое чувство голода, сердцебиение, холодный пот, дрожь, головная боль. Больной может своевременно принять необходимые меры и избежать переход в гипогликемическую кому.
Искусственно вызванная гипогликемия
Эйфория, вызванная введением инсулина, встречается у здоровых девушек (синдром Мюнхаузена). Некоторые больные с сахарным диабетом также активно вызывают симптомы гипогликемии. Мотив такого поведения связан с особенностями характера и социальной средой. Такие больные весьма изобретательны и активно скрывают препараты. Предполагаемая искусственная гипогликемия диагностируется по наличию ее симптомов, высоких показателей инсулина и низкого С-пептида в крови.
Аутоиммунный гипогликемический синдром
Аутоантитела, направленные против инсулина или его рецепторов, могут провоцировать гипогликемию. У здоровых людей в крови постоянно образуются антитела к инсулину, но выявляются лишь у 1–8%. Аутоантитела к инсулину обнаруживаются в 40% у больных с впервые выявленным сахарным диабетом, не леченных инсулином, и в 30% при сочетании его с аутоиммунными заболеваниями. Аутоантитела, которые связывают инсулин, могут подвергаться несвоевременной диссоциации, обычно в течение короткого периода сразу после приема пищи, и резко повышают концентрацию свободного инсулина в сыворотке, таким образом вызывая гипогликемию в поздний постпрандиальный период. Этому может предшествовать гипергликемия в ответ на прием пищи. Диагноз аутоиммунной гипогликемии ставится на основании сочетания с аутоиммунными заболеваниями, наличия высокого титра антител к инсулину, высоких концентраций инсулина и отсутствия снижения уровня С-пептида на фоне гипогликемии.
Провоцировать гипогликемию могут антитела к рецепторам инсулина. Эти антитела связывают рецепторы и имитируют действие инсулина путем повышения утилизации глюкозы из крови. Чаще антитела к рецепторам инсулина встречаются у женщин и сочетаются со многими аутоиммунными заболеваниями. Приступы гипогликемии, как правило, развиваются натощак.
Гипогликемия при нормальном уровне инсулина
Внепанкреатические опухоли
С гипогликемией могут быть связаны разные мезенхимальные опухоли (мезотелиома, фибросаркома, рабдомиосаркома, лейомиосаркома, липосаркома и гемангиоперицитома) и органоспецифические карциномы (печеночная, адренокортикальная, мочеполовой системы и молочной железы). Гипогликемия может сопутствовать феохромоцитоме, карциноиду и злокачественным заболеваниям крови (лейкемии, лимфоме и миеломе). Механизм ее варьирует в соответствии с типом опухоли, но во многих случаях гипогликемия связана с нарушением питания, обусловленным опухолью, и потерей веса вследствие жирового, мышечного и тканевого истощения, которое нарушает глюконеогенез в печени. В некоторых случаях утилизация глюкозы исключительно большими опухолями может привести к гипогликемии. Опухоли могут также секретировать гипогликемические факторы, такие как неподавляемая инсулиноподобная активность и инсулиноподобные факторы роста. Путем связывания с инсулиновыми рецепторами печени инсулиноподобный фактор-2 тормозит продукцию глюкозы печенью и способствует гипогликемии. Под подозрением находятся также опухолевые цитокины, особенно фактор опухолевого некроза (кахектин). Очень редко опухоль секретирует внепеченочный инсулин.
Системный дефицит карнитина
Тяжелая гипогликемия может возникнуть у больных с системной карнитиновой недостаточностью. Карнитин — биологически активное витаминоподобное вещество. Основными его функциями являются участие в энергетическом обмене, связывание и выведение из организма токсичных производных органических кислот. При системном дефиците карнитина в плазме, мышцах, печени и других тканях снижено содержание карнитина, необходимого для транспорта жирных кислот в митохондрии, где происходит их окисление. В результате периферические ткани лишаются способности утилизировать жирные кислоты для образования энергии, а печень не может производить альтернативный субстрат — кетоновые тела. Все это приводит к тому, что все ткани становятся зависимыми от глюкозы и печень оказывается не в состоянии удовлетворить их потребности. Системная карнитиновая недостаточность проявляется тошнотой, рвотой, гипераммониемией и печеночной энцефалопатией. Эта патология является одной из форм синдрома Рейе.
Реже гипогликемия встречается при недостаточности карнитинпальмитоилтрансферазы — фермента, переносящего жирные кислоты с жирного ацил-КоА на карнитин для окисления. У большинства больных имеет место, по-видимому, частичный дефект, так что окисление жирных кислот в какой-то мере сохраняется и тенденция к гипогликемии сводится к минимуму. Клинически это проявляется миопатией при физической нагрузке с миоглобинурией. Некетозная (или гипокетозная) гипогликемия может встречаться также при снижении активности других ферментов окисления жирных кислот, например, при недостаточности дегидрогеназы средне- или длинноцепочечного ацилкоэнзима А (ацил-КоА).
Дети раннего возраста особенно чувствительны к недостаточности карнитина. Эндогенные запасы у них быстро истощаются при различных стрессовых ситуациях (инфекционные заболевания, желудочно-кишечные расстройства, нарушения вскармливания). Биосинтез карнитина резко ограничен в связи с небольшой мышечной массой, а поступление с обычными пищевыми продуктами не способно поддержать достаточный уровень в крови и тканях.
Диагностика и дифференциальная диагностика гипогликемии
При подозрении на гипогликемию следует срочно определить концентрацию глюкозы в крови или в плазме и начать лечение. При сборе анамнеза заболевания, прежде всего, нужно выяснить, в каких условиях она возникает. У одних больных приступы гипогликемии случаются, если они вовремя не поели (гипогликемия голодания). У других приступы возникают после еды, особенно после приема пищи, богатой углеводами (реактивная гипогликемия). Эти сведения очень важны, так как этиология и механизмы развития гипогликемии голодания и реактивной гипогликемии различаются. Гипогликемия голодания нередко бывает проявлением тяжелого заболевания (например, инсулиномы) и более опасна для головного мозга.
Для установления диагноза необходимо найти связь между появлением симптомов и аномально низким уровнем глюкозы в плазме, а также показать, что при повышении этого уровня симптомы исчезают. Уровень глюкозы в плазме, при котором возникают симптомы, у разных больных и в разных физиологических состояниях неодинаков. Аномально низкой концентрацию глюкозы в плазме обычно называют тогда, когда она не достигает 2,7 ммоль/л у мужчин или 2,5 ммоль/л у женщин (т. е. оказывается ниже нижней границы у здоровых мужчин и женщин после голодания в течение 72 ч) и 2,2 ммоль/л у детей.
У любого больного с нарушениями сознания (или судорогами неизвестной этиологии) необходимо определять содержание глюкозы в крови с помощью тест-полосок, используя для этого каплю крови. Если обнаруживается аномально низкий уровень глюкозы, сразу же начинают вводить глюкозу. Быстрое смягчение симптомов со стороны ЦНС (наблюдаемое у большинства больных) при повышении уровня глюкозы в крови подтверждает диагноз гипогликемии натощак или лекарственной гипогликемии. Часть первоначальной пробы крови следует сохранить в виде замороженной плазмы для определения исходных концентраций инсулина, проинсулина и С-пептида или — при необходимости — для выявления в крови каких-либо соединений, послуживших причиной гипогликемии. Нужно определять также рН крови и содержание в ней лактата и с помощью тест-полосок проверять содержание кетоновых тел в плазме.
Часто вероятную причину гипогликемии удается установить уже с самого начала (запах алкоголя изо рта, применение сахаропонижающих средств в анамнезе, признаки обширного поражения печени или почек, присутствие крупной опухоли в забрюшинном пространстве или в грудной полости, а также существование врожденных причин гипогликемии натощак).
У больных с инсулиносекретирующими опухолями поджелудочной железы (инсулиномы, островковоклеточные карциномы) повышенному уровню инсулина обычно сопутствуют повышенные уровни проинсулина и С-пептида. У больных, получающих препараты сульфанилмочевины, тоже следует ожидать повышения уровня С-пептида, но в этом случае в крови должны присутствовать и значительные количества препарата.
Если гипогликемия связана с передозировкой препаратов инсулина, то уровень проинсулина нормален, а содержание С-пептида снижено. При аутоиммунном инсулиновом синдроме содержание свободного инсулина в плазме во время приступа гипогликемии обычно бывает резко повышено, уровень С-пептида снижен, но в плазме легко определяются антитела к инсулину. Дифференциальный диагноз между аутоиммунной гипогликемией и состоянием, вызванным избыточным введением инсулина, требует специальных исследований.
У пациентов с инсулиномой при обращении к врачу симптомы гипогликемии часто отсутствуют. Обращаться в медицинские учреждения их заставляют приступы внезапного помутнения или потери сознания, которыми они страдали на протяжении ряда лет и которые участились в последнее время. Характерной особенностью таких приступов является то, что они возникают между приемами пищи или после ночного голодания; иногда они провоцируются физической нагрузкой. Приступы могут проходить самопроизвольно, но чаще они быстро исчезают после приема сладких продуктов или напитков. Эта особенность является важнейшим диагностическим признаком.
При обследовании таких больных можно обнаружить несоответственно высокий исходный уровень инсулина в плазме (> 6 мкЕД/мл и тем более > 10 мкЕД/мл) на фоне гипогликемии. Эта находка служит веским аргументом в пользу инсулиносекретирующей опухоли, если удается исключить тайное использование инсулина или препаратов сульфанилмочевины. Обычно в тех случаях, когда гликемия падает до аномально низкого уровня, содержание инсулина в плазме снижается до нормального базального уровня, который все же оказывается слишком высоким для данных условий. Другие состояния, кроме наличия инсулиносекретирующей опухоли, предрасполагающие к гипогликемии натощак, обычно удается исключить при амбулаторном обследовании.
Если у пациента не выявлены объективные причины со стороны других органов и систем, при которых характерны эпизодические появления симптомов со стороны ЦНС, больного госпитализируют в стационар и проводят пробу с голоданием. Целью данной пробы является воспроизведение симптомов в условиях регистрации уровней глюкозы, инсулина, проинсулина и С-пептида в плазме. У 79% больных с инсулиномой симптомы возникают уже в течение 48 ч голодания, а у 98% — в течение 72 ч. Голодание прекращают через 72 ч или в момент появления симптомов. Если голодание провоцирует возникновение характерных для больного симптомов, которые быстро купируются введением глюкозы, или если симптомы появляются на фоне аномально низкого уровня глюкозы и несоответственно высокого уровня инсулина в плазме, то предположительный диагноз инсулиносекретирующей опухоли можно считать подтвержденным. Использование рентгенологического исследования и КТ-сканирования нецелесообразно для диагностики инсулиномы, так как данные опухоли обычно слишком малы, чтобы их удалось обнаружить с помощью данных исследований.
Лечение гипогликемических состояний
Лечение гипогликемических состояний на начальных их этапах включает в себя пероральное введение легко всасываемых углеводов: сахара, варенья, меда, сладкого печенья, конфет, леденцов, белого хлеба или фруктового сока.
При малейшем подозрении на гипогликемическую кому, даже при затруднениях в ее дифференцировке с кетоацидемической комой, врач обязан, взяв кровь для анализа, тут же ввести больному внутривенно струйно 40–60 мл 40% раствора глюкозы. Если гипогликемическая кома неглубока и непродолжительна, то больной приходит в сознание сразу же после окончания инъекции. Если этого не происходит, можно думать, что кома не связана с гипогликемией либо кома гипогликемическая, но функции ЦНС восстановятся позднее. Выполнив этот важнейший лечебный прием, необходимый при гипогликемии, врач получает время для дальнейших диагностических исследований. Введение указанного количества глюкозы не принесет больному вреда, если кома окажется кетоацидемической.
Если сознание возвращается к больному после первой внутривенной инъекции глюкозы, дальнейшую инфузию глюкозы можно прекратить. Больному дают сладкий чай, кормят его с короткими интервалами. При отсутствии сознания после введения 60 мл глюкозы налаживают внутривенное капельное введение 5% раствора глюкозы, которое продолжается часами и сутками. В капельницу добавляют 30–60 мг преднизолона, в/в вводят 100 мг кокарбоксилазы, 5 мл 5% раствора аскорбиновой кислоты.
Уровень гликемии должен поддерживаться в пределах 8–12 ммоль/л. При ее дальнейшем повышении вводят дробно инсулин в малых дозах (4–8 ЕД). Перед капельным введением раствора глюкозы подкожно вводится 1 мл 0,1% раствора адреналина, 1–2 мл глюкагона внутривенно или внутримышечно (последний можно вводить повторно каждые 3 часа).
При длительном отсутствии сознания проводятся мероприятия по профилактике отека головного мозга: в/в капельно вводится 15–20% раствор маннитола, в/в струйно — 60–80 мг Лазикса, 10 мл 25% раствора сульфата магния, 30–60 мг преднизолона. Показана ингаляция увлажненного кислорода. В случае угнетения дыхания больной переводится на искусственную вентиляцию легких.
После выведения больного из комы применяют средства, улучшающие метаболизм клеток ЦНС (глютаминовая кислота, Стугерон, Аминалон, Церебролизин, Кавинтон) в течение 3–5 недель.
Литература
- Балаболкин М. И., Клебанова Е. М., Креминская В. М. Дифференциальная диагностика и лечение эндокринных заболеваний (руководство). М.: «Медицина», 2002, с. 751.
- Dizon A. M. et al. Neuroglycopenic and other symptoms in patients with insulinoma // Am. J. Med. 1999, p. 307.
- Генес С. Г. Гипогликемии. Гипогликемический симптомокомплекс. М.: «Медицина», 1970, с. 236.
- Эндокринология и метаболизм. В 2 томах. Под ред. Фелинга Ф. и соавт. Перевод с английского: Кандрора В. И., Старковой Н. Т. М.: «Медицина», 1985, т. 2, с. 416.
- Калинин А. П. и соавт. Инсулинома. Медицинская газета, 2007, № 45, с. 8–9.
- Кравец Е. Б. и соавт. Неотложная эндокринология. Томск, 2005, с. 195.
- Дедов И. И. и соавт. Сахарный диабет у детей и подростков. М.: «Универсум паблишинг», 2002, с. 391.
В. В. Смирнов, доктор медицинских наук, профессор
А. Е. Гаврилова
РГМУ, Москва
Контактная информация об авторах для переписки: smirnov-web@mail.ru
Инсулин необходим для жизни, но хронически высокий уровень инсулина делает организм менее чувствительным к этому гормону, что увеличивает риск развития серьезных хронических заболеваний.
Помогает снизить уровень инсулина и резистентность к инсулину принятие эффективных изменений образа жизни – таких как низкоуглеводная диета, прерывистое питание, регулярная физическая активность и правильный режим сна. Соблюдая все рекомендации эндокринолога больной может избежать негативных последствий гиперинсулинемии.
Что такое резистентность к инсулину?
Резистентность к инсулину – это состояние когда клетки слабо реагируют на инсулин, который циркулирует в организме. Это заставляет поджелудочную железу выделять еще больше этого важного гормона, чтобы поддерживать стабильный уровень сахара в крови.
Роль инсулина
Инсулин очень важен для организма и выполняет множество функций. Его основная роль – поддерживать уровень глюкозы в крови в очень узком диапазоне – это так называемый гомеостаз глюкозы в крови. Как слишком высокий, так и слишком низкий уровень глюкозы в крови опасны и вредны для организма.
При повышении уровня глюкозы выделяется больше инсулина. Когда уровень глюкозы падает, выделяется меньше инсулина. В целом, поддержание инсулина в низком физиологическом диапазоне необходимо для нормального обмена веществ и здоровья в целом. Под действием инсулина глюкоза может использоваться клетками в качестве энергии или храниться в виде гликогена в клетках мышц и печени.
Если глюкоза определенное время не попадает в кровь, например, при отсутствии приема пищи, выделение инсулина замедляется. Падение уровня инсулина сигнализирует печени о необходимости стабилизации уровня глюкозы до нормального для обеспечения работы тканей. В печени запускается глюконеогенез: образование глюкозы из органических неуглеводных соединений. Повышение уровня инсулина до нормального уровня прекращает этот процесс.
Другая важная роль инсулина – регуляция накопления жира. Когда уровень инсулина высок, он стимулирует жировые клетки поглощать глюкозу и превращать ее в жир (липогенез). Когда уровень инсулина низкий, он позволяет организму использовать этот накопленный жир для производства энергии. То есть запускается липолиз (мобилизация жира) – распад триглицеридов жировой ткани с высвобождением энергии, необходимой всем клеткам организма. В норме наблюдается равновесие этих процессов.
При нормальном метаболизме, этот процесс работает без отклонений, чтобы обеспечить постоянную подачу энергии для организма. Проблема возникает, когда нарушается обмен веществ, что, по оценкам специалистов, происходит у 88% людей.
Когда в организм постоянно поступает глюкоза, инсулин постоянно выделяется и остается постоянно высоким. Это состояние называется гиперинсулинемией. Оно развивается когда ткани перестают правильно реагировать на сигналы инсулина.
Почему возникает резистентность к инсулину?
Установлено три фактора риска, которые способствуют развитию резистентности к инсулину: генетические, окружающей среды и образа жизни.
Предполагается, что у некоторых людей генетически выше вероятность развития резистентности к инсулину, например, при наличии диабета в семье. Но, скорее всего, наибольшее влияние оказывают изменения в питании, которые произошли в последние десятилетия.
Большая доступность дешевых, энергетически насыщенных продуктов питания и напитков привела к тому, что все население перешло на нездоровый образ жизни, характеризующийся потреблением продуктов с высоким содержанием сахара и других рафинированных углеводов. Они распадаются на большое количество глюкозы, которая не нужна для производства энергии при малоподвижном образе жизни. В результате лишние углеводы хранятся в клетках.
Как развивается резистентность к инсулину
Когда в организм каждый день поступает избыток глюкозы, клетки мышц и печени перенасыщаются и не могут больше поглощать и хранить глюкозу. Однако постоянное поступление глюкозы в кровь из пищи с высоким содержанием углеводов требует, чтобы глюкоза использовалась. Поскольку этого не происходит, уровень глюкозы в крови не уменьшается и постепенно растет.
Поджелудочная железа выделяет больше инсулина, чтобы сигнализировать клеткам, что уровень глюкозы в крови слишком высок, и что им нужно поглощать больше глюкозы. Клетки не могут поглощать глюкозу, они переполнены и сопротивляются ее проникновению.
Поджелудочная железа переходит в усиленный режим работы, выделяя еще больше инсулина, пытаясь преодолеть клеточное сопротивление и заставить глюкозу проникать в клетки. Развивается гиперинсулинемия, компенсирующая высокий уровень глюкозы. Некоторые эндокринологи справедливо утверждают, что лучший термин для этого ухудшающегося состояния не резистентность к инсулину, а хроническая гиперинсулинемия, так как мышцы и клетки печени на самом деле не «устойчивы» к инсулину, просто они полны и не могут реагировать, несмотря на усиление работы поджелудочной железы.
В жировой ткани увеличивается гидролиз триглицеридов, которые в ней хранятся и снижается способность поглощения липидов, циркулирующих в крови. Содержание свободных жирных кислот в плазме увеличивается, что может дополнительно ухудшить резистентность.
Как правило, клетки жировой ткани сохраняют чувствительность к инсулину при сопротивлении мышечных и клеток печени, они продолжают поглощать глюкозу и синтезировать из нее жир. Образование новой жировой ткани приводит к увеличению веса и усилению процесса резистентности к инсулину.
Определенное время компенсаторный механизм поддержания уровня глюкозы крови за счет увеличения выделения инсулина сохраняется. Но поджелудочная железа постепенно уменьшает выработку инсулина, поэтому уровень сахара также постепенно растет. Это приводит к увеличению постпрандиальной глюкозы (после приема пищи) и глюкозы в крови натощак. Отсюда нарушение толерантности к глюкозе по результатам ОГТ теста и уровня глюкозы натощак служит одними из методов определения резистентности к инсулину.
Если повышается резистентность, и прекращается работа поджелудочной железы, так как клетки со временем изнашиваются и перестают вырабатывать инсулин, может развиться диабет.
Симптомы инсулинорезистентности
Инсулинорезистентность не имеет явных симптомов плохого самочувствия. Основной симптом этого состояния у многих людей – до того, как ему поставили диагноз предиабет или полномасштабный диабет 2 типа – увеличение жира в брюшной полости (висцеральный жир).
- Висцеральное ожирение. Основная теория о том, как усиливается резистентность к инсулину, заключается в следующем. У каждого есть пороговый уровень жира, который может накапливаться в жировых клетках. Когда он превышен, организм начинает накапливать жир в менее идеальных местах – вокруг печени, поджелудочной железы и других органов брюшной полости. Эти жировые отложения называются висцеральным жиром. Когда этот жир начинает нарастать, это верный признак инсулинорезистентности.
- Изменение кожи. Другими тонкими признаками резистентности к инсулину у некоторых людей служат темные, сухие участки кожи в области паха, подмышек или задней части шеи, известные как черный акантоз. Кожные метки – небольшие мясистые образования – часто на шее или в подмышках также могут быть признаком инсулинорезистентности. Их происхождение связано с тем, что инсулин является стимулятором роста клеток.
Это два основных признака. Большинство людей с ранней резистентностью к инсулину чувствуют себя хорошо. Только после того, как уровень глюкозы в крови наконец начинает расти, могут появиться другие симптомы высокого уровня сахара в крови и диабета 2 типа, такие как частое мочеиспускание, сильная жажда, усталость и чрезмерный голод.
Важно понимать, что уровень инсулина поднимается все выше и выше в попытке контролировать уровень глюкозы в крови. Какое-то время это работает. Но в конечном итоге более высокий уровень инсулина может не компенсироваться полностью, и уровень глюкозы в крови начинает расти. Это может длиться до поздней стадии заболевания.
К тому времени, когда кому-то поставили диагноз диабет 2 типа, у него, вероятно, была резистентность к инсулину – или хроническая гиперинсулинемия – в течение ряда лет, возможно, даже более десяти.
Условия, связанные с инсулинорезистентностью
С инсулинорезистентностью связаны следующие состояния:
Ожирение. Поскольку резистентность к инсулину связана с высоким уровнем инсулина, что вызывает образование новой жировой ткани, это может привести к увеличению массы тела и отложению жира. Ожирение, в свою очередь, ведет к повышению резистентности к инсулину, создавая тем самым порочный круг. Развитие резистентности стимулирует развитие ожирения, развитие ожирения в свою очередь усиливает резистентность.
Осложнения беременности. У многих женщин проявляются признаки резистентности к инсулину во время беременности, особенно в третьем триместре. Предполагается, что это эволюционная адаптация, развивающаяся для обеспечения быстро растущего плода достаточным количеством глюкозы. Однако у некоторых женщин это может привести к гестационному диабету из-за повышенной концентрации глюкозы и высокому артериальному давлению из-за задержки в системе кровообращения жидкости.
Это в принципе нормальная адаптация, разработанная для обеспечения здоровой беременности. Но она делает женщин более восприимчивыми к метаболическим заболеваниям в целом, особенно при современном образе жизни при отсутствии регулярной нагрузки и питания продуктами с высоким содержанием рафинированных углеводов и сахаров.
Метаболический синдром. Описывает набор характеристик, которые встречаются у людей с инсулинорезистентностью. Существует ряд различных определений метаболического синдрома, которые обычно включают: повышенный уровень глюкозы в крови натощак, высокое артериальное давление, повышение уровня триглицеридов и снижение уровня холестерина ЛПВП, увеличение окружности талии.
Предиабет. Резистентность к инсулину связана с преддиабетом. Он возникает, когда уровень глюкозы в крови выше нормы, но еще недостаточно высок для диагностики диабета 2 типа.
Всемирная организация здравоохранения определяет преддиабет как: уровень глюкозы натощак 110-125 мг/дл (6,1-6,9 ммоль/л) или HbA1c 6% (42 ммоль/моль) или выше. США и некоторые другие страны используют другое определение: (FBG выше 100 мг/дл (5,7 ммоль/л) или HbA1c выше 5,7% (39 ммоль/л).
Если повышается резистентность, и прекращается работа поджелудочной железы (клетки со временем изнашиваются и перестают вырабатывать инсулин) может развиться диабет.
Синдром поликистозных яичников (PCOS). Синдром поликистозных яичников считается распространенным нарушением обмена веществ, которым страдают до 10% женщин детородного возраста. Это основная причина бесплодия, которая увеличивает риск развития диабета 2 типа в более позднем возрасте.
У женщин с СПКЯ, как правило, повышенный уровень мужских гормонов, нерегулярные или отсутствующие менструальные периоды, кисты на яичниках, а также инсулинорезистентность. Другими общими симптомами являются: ожирение, прыщи, выпадение волос по мужскому типу и избыточные волосы на лице и теле.
В клетках яичников есть рецепторы к инсулину и рецепторы к ИФР-1. Сродство инсулина к собственным рецепторам выше, чем к рецепторам ИФР-1, но при гиперинсулинемии или когда блокируются ИР, инсулин больше связывается с рецепторами ИФР-1. В обоих случаях выработка гормонов яичниками увеличивается.
При неспецифическом механизме стимуляции стероидогенеза под воздействием инсулина увеличивается жизнеспособность клетки яичника (синтез аминокислот и ДНК) и соответственно выработка гормонов. При специфическом механизме стимуляции инсулин непосредственно увеличивает активность ферментов ответственных за выработку гормонов, либо повышает количество рецепторов к ЛГ, а синтез андрогенов под воздействием ЛГ усиливается.
Под влиянием инсулина (или ИФР-1) концентрация андрогенов в яичнике растет, развивается его атрезия, которая сопровождается уменьшением клеток, продуцирующих эстрогены и прогестерон, и увеличением количества клеток (клеток тека и межуточной ткани яичников), в которых вырабатываются андрогены. Этот механизм объясняет, почему под воздействием инсулина вырабатывается больше мужских половых гормонов, чем женских, что приводит к гиперандрогении и развитию СПКЯ.
Неалкогольная жировая болезнь печени – НАЖБП, означает, что в печени хранится слишком много жира. НАЖБП может быть результатом хронически высокого уровня инсулина, и может способствовать инсулинорезистентности.
Патология чаще встречается у людей, страдающих ожирением, имеющих метаболический синдром или диабет 2-го типа. Однако, обнаружено, что она связана с инсулинорезистентностью и гиперинсулинемией у худых людей с нормальной толерантностью к глюкозе.
Примерно у 20-40 % страдающих НАЖБП может прогрессировать до образования рубцовой ткани (фиброз), в последующем у каждого пятого с фиброзом развивается цирроз (поскольку соединительная ткань разрушает гепатоциты) и в дальнейшем может развиться печеночная недостаточность.
Рак. Инсулинорезистентность связана с повышением риска развития колоректального рака, рака эндометрия, рака поджелудочной железы и рака молочной железы. Точно неизвестно, сама инсулинорезистентность вызывает рак или ее связь с другими факторами, такими как ожирение и высокий уровень глюкозы в крови, которые повышают риск развития рака.
Однако, считается, что хронически высокие уровни инсулина могут способствовать росту раковых клеток, а снижение уровня инсулина может замедлить рост рака. Для роста и развития этих клеток также нужен инсулин и глюкоза. Исследования в этой области продолжаются, например, в США идет исследование, в котором изучают воздействие на раковые клетки мощного противоопухолевого препарата в сочетании с кетогенной диетой.
Сердечно-сосудистые заболевания (ССЗ). Инсулинорезистентность и гиперинсулинемия может повышать риск развития сердечно-сосудистых заболеваний, отчасти потому, что эти состояния тесно связаны с другими факторами риска ССЗ (ожирение и гипертония).
Но некоторые исследования показали, что инсулинорезистентность – независимый фактор риска развития сердечно-сосудистых заболеваний. Большинство теорий предполагают, что процесс хронического воспаления и окисления, а также прямое повреждение сосудов при резистентности к инсулину приводит к ССЗ. В первую очередь развивается атеросклероз.
Болезнь Альцгеймера. Болезнь Альцгеймера также может быть связана с инсулинорезистентностью. Исследования показывают, что у людей с диабетом на 60% чаще развивается деменция. Также, отмечается высокая распространенность изменений головного мозга у больных сахарным диабетом. Точный механизм развития этих заболеваний не установлен.
Предполагается, что клетки мозга тоже постепенно становятся инсулинорезистентными и не могут эффективно использовать глюкозу и находятся в состоянии энергетического голодания. Кроме того, высокое АД, высокий уровень холестерина, сопровождающие резистентность к инсулину – установленные факторы риска заболевания. Результат этого процесса – постепенное прогрессирование болезни Альцгеймера.
Адаптивная устойчивость к инсулину. Применение очень низкоуглеводных диет было связано с состоянием, которое называют адаптивной инсулинорезистентностью (физиологической инсулинорезистентностью или адаптивным сохранением глюкозы.)
Неизвестно, как это происходит, возможный механизм развития следующий: если прекратить потреблять сахар или углеводы, количество глюкозы в крови упадет. Однако происходит изменение обмена углеводов, чтобы мозг получал необходимую для работы глюкозу, а поступление глюкозы в печень, жировые клетки или мышечные клетки не происходило (таким образом, эти клетки становятся “инсулинорезистентными”). Мышечные и печеночные клетки вместо этого используют кетоны в качестве энергии.
Поскольку этот тип инсулинорезистентности происходит с низким, а не высоким уровнем циркулирующего инсулина, он не считается таким же опасным состоянием, как обычная инсулинорезистентность.
Как диагностируется резистентность к инсулину
К сожалению, инсулинорезистентность редко диагностируется, поскольку тесты на уровень инсулина дорогостоящие и доступны не всем.
Можно использовать стандартные тесты на сахарный диабет, которые измеряют уровень глюкозы: глюкозу крови натощак и гемоглобин A1c. Однако к тому времени, когда они повышаются, уровень инсулина был высоким в течение многих лет и могли произойти нарушения, вызванные гиперинсулинемией.
Чтобы не ждать, пока из резистентности разовьется преддиабет или диабет типа 2, эндокринологи назначают для ее определения ряд тестов.
Какие анализы можно сдать, чтобы подтвердить диагноз?
Тест на инсулин и триглицериды натощак. Сочетание незначительно повышенного инсулина с повышенными триглицеридами (>150) может указывать на инсулинорезистентность.
Глюкозотолерантный тест (ПГТТ). Вначале натощак измеряется глюкоза, инсулин, а также С-пептид. Затем дают выпить 75 г растворенной глюкозы и измеряют сахар каждые полчаса в течение 2 часов. (через 30 минут, 60, 90, 120 минут).
Расшифровка результатов:
- Если содержание инсулина натощак больше 12,5 мкМЕ/мл, а при измерении через 2 часа больше 28,5 мкМЕ/мл – гиперинсулинемия.
- Если глюкоза натощак более 5,5 ммоль/л – это гипергликемия натощак.
- Если глюкоза натощак >6,7 ммоль/л – диабет.
- Если С-пептид натощак >1,2 нмоль/л и через 120 минут больше 1,4 нмоль/л – метаболический синдром.
Индекс инсулинорезистентности HOMA (HOMA-IR) – оценка гомеостатической модели инсулинорезистентности. Суть метода: определить насколько высоким станет уровень инсулина, чтобы поддерживать уровень глюкозы натощак. В один и тот же день измеряется глюкоза и уровень инсулина в крови натощак. Затем рассчитывают индекс HOMA: инсулин натощак (мЕд/л)x глюкоза натощак (ммоль/л)/22.5= HOMA-IR. Расшифровка результатов:
- Показатель HOMA-IR менее 1 означает хорошую чувствительность к инсулину.
- HOMA-IR более 1,9 указывает на раннюю резистентность к инсулину.
- Если HOMA-IR превышает 2,9 – выраженная резистентность к инсулину.
Эугликемическое гипергликемическое клэмп тестирование (клэмп-тест). Одновременно инфузионно в/в вводят инсулин (однократно) и глюкозу, затем глюкозу продолжают вводить с многократным измерением ее концентрации для поддержания содержания сахара крови 5,5 ммоль/л. Количество введенной глюкозы соответствует скорости ее поглощения тканями.
При инсулинорезистентности глюкозы требуется меньше. Преимущества: самый точный метод определения инсулинорезистентности, позволяет определить причину ее развития (либо нарушено поглощение глюкозы тканями, либо подавление инсулином выработки глюкозы печенью).
Как самостоятельно можно предположить резистентность к инсулину
При нормальном ИМТ в диапазоне 20-25, может быть резистентность к инсулину если есть висцеральное ожирение.
В домашних условиях тоже можно провести тестирование на резистентность к инсулину. Нужно измерить окружность талии и рост. Отношение окружности талии к росту менее 0,5 указывает на хорошую чувствительность к инсулину, выше 0,5 – на ухудшение инсулинорезистентности.
Хотя это не идеальный тест, его очень легко сделать без врача, причем, не имеет значение возраст, пол, рост, степень развития мышечной массы (мускулистый или жилистый человек). В любом случае показатель выше 0,5 указывает на повышенный риск резистентности к инсулину и повод обратиться за диагностикой.
Как лечить инсулинорезистентность: могут ли помочь лекарства?
К сожалению, нет. Не одобрено ни одного препарата для лечения (устранения) резистентности к инсулину.
Иногда эндокринологи назначают популярный препарат для лечения СД 2 типа метформин (Глюкофаж – Glucophage) не только диабетикам, но и пациентам с инсулинорезистентностью. Снижая производство глюкозы в печени и повышая чувствительность клеток к инсулину, метформин может снизить сахар крови, но не устраняет основные причины резистентности.
Единственный метод, позволяющий остановить инсулинорезистентность – нормализовать обмен веществ и похудеть.
Низкоуглеводная диета
Практически любая диета, которая приводит к потере веса, особенно к потере жира вокруг талии, может временно улучшить чувствительность к инсулину. Лучший вариант – низкоуглеводная диета. Если не есть сладкое или углеводы, которые быстро расщепляются, меньше сахара поступает в кровоток, и, следовательно, не нужно повышать уровень инсулина, чтобы выводить сахар (глюкозу) из крови в клетки.
Вместо углеводов, делают упор на настоящую пищу: белки, натуральные жиры и овощи, что приводит к потере веса.
Некоторые преимущества ограничения углеводов в рационе:
- Доказано, что низкоуглеводная диета эффективна для лечения СД 2 типа, поскольку резистентность к инсулину – основная причина диабета, она также эффективна как на начальных этапах резистентности, так и в более поздних, также позволяет остановить переход преддиабета в СД.
- Исследования показали снижение уровня инсулина на 75% у многих пациентов с ожирением и сахарным диабетом 2 типа, которые придерживались диеты с низким содержанием углеводов.
- В других исследованиях установили, что диета с очень низким содержанием углеводов лучше для снижения уровня инсулина, чем диета с низким содержанием жиров. Обе группы похудели одинаково, но содержание инсулина значительно уменьшилось у первой.
- Диета с низким содержанием углеводов имела лучшие результаты, чем диета с низким содержанием жиров, плюс препарат для похудения и снижения уровня инсулина, глюкозы и HbA1c. Обе группы потеряли одинаковое количество веса, но в первой показатели сахара в крови и уровня инсулина заметно снизились.
Вывод: чтобы снизить резистентность к инсулину, необходимо уменьшить употребление сахара и углеводов, которые перевариваются до сахара. Это изменение рациона приведет к снижению производства инсулина.
Резкое ограничение углеводов может быть трудным, поэтому вначале можно просто изменить план питания. Чтобы снизить резистентность к инсулину необходимо:
- увеличение потребления пищевых волокон,
- есть продукты с низким гликемическим индексом,
- снижение потребления жира с пищей.
Интервальное голодание / ограниченное по времени питание
Интервальное голодание – новая диетическая тенденция, которая может улучшить чувствительность к инсулину, помогает похудеть и увеличить энергию. Суть прерывистого голодания: если определенное время не есть (особенно сахар и углеводы) – инсулин не выделяется для компенсации. Это дает клеткам возможность восстановиться и стать более чувствительными к инсулину, а также делает перерыв работы поджелудочной железы.
Прием пищи с ограничением по времени – это тип прерывистого поста, который включает прием пищи в установленные сроки каждый день, например, только с 11 до 19 часов. Обзор исследований показал, что меньшее количество приемов пищи во время более короткого периода приводит к улучшению уровня глюкозы и инсулина.
Например, у мужчин, которые голодали в течение 20 часов через день в течение 15 дней, усвоилось больше глюкозы при тех же уровнях инсулина, что существенно улучшило чувствительность к инсулину. Среди женщин, использующих прерывистое ограничение калорий (голодание) существенно улучшилась резистентность к инсулину по сравнению с хроническим ограничением калорий.
Вывод: сочетание диеты с низким содержанием углеводов и содержанием жиров с периодическим прерывистым голоданием, вероятно, является наиболее эффективным для лечения гиперинсулинемии и резистентности.
Активность и упражнения
Мышцы сжигают глюкозу для энергии во время сокращения, что сопровождается поглощением сахара из крови, уменьшением секреции инсулина и нагрузки на поджелудочную железу.
Мышцы, которые не работают, не расходуют сахар крови, поэтому уровень инсулина может повышаться, чтобы уменьшить любой избыток сахара. Исследования показывают: что
- простой пятидневный постельный режим вызывает состояние резистентности к инсулину у совершенно здоровых людей,
- длительная бездеятельность тесно связана с инсулинорезистентностью, метаболическим синдромом и предиабетом.
Рекомендуются любые регулярные упражнения. Наиболее эффективны:
- высокоинтенсивный интервальный тренинг (ВИИТ),
- тренировка с отягощениями,
- кардиотренировка – все это улучшает использование глюкозы и тем самым улучшает чувствительность к инсулину.
Независимо от того, какую форму активности вы предпочитаете, движение увеличивает чувствительность к инсулину, пока упражнения продолжаются. Если вы перестаете регулярно двигаться, инсулинорезистентность может вернуться.
Нормализация сна
Существует связь между инсулинорезистентностью и сном. Кратковременное недосыпание повышает уровень глюкозы и ухудшает резистентность к инсулину. Хроническое нарушение сна, например, из-за обструктивного апноэ во сне, также приводит к ухудшению инсулинорезистентности. Важно высыпаться и устранить проблемы со сном (апноэ, бессонница) это может привести к улучшению чувствительности к инсулину.
Устранение стресса
Временная резистентность к инсулину возникает в периоды кратковременного физиологического и психологического стресса, такого как внезапная болезнь или внезапная угроза. Вероятно, это предназначено, чтобы быстрее справиться с болезнью.
Эта резистентность к инсулину восстанавливается, когда внезапный стресс проходит. Такой ответ, скорее всего, не имеет негативных последствий.
Хронический стресс и хроническая активация реакции организма на борьбу с инфекцией – процесс длительный, сопровождается нарушением обмена веществ и гормонального фона, без внезапного начала и быстрой устранении причины. Поэтому он может привести к резистентности к инсулину.
Точных доказательств, что методы снижения стресса могут улучшить чувствительность к инсулину, нет. Однако, тренировка концентрации внимания, йога, медитация и даже танцы, пение и другие методы расслабления, такие как ходьба на природе – эффективные способы снижения стресса, они также могут улучшить резистентность к инсулину.
Отказ от вредных привычек
Активное курение повышает риск резистентности к инсулину с последующим развитием диабета. Никотин сужает сосуды и нарушает кровообращение органов. При курении в сочетании с повышенным уровнем триглицеридов и пониженным ЛПВП во время инсулинорезистентности, значительно увеличивается риск образования холестериновых бляшек и тромбов. Бросив курить вы уменьшите риск метаболических нарушений, инсулинорезистентности, атеросклероза, инфарктов и инсультов.
Можно ли вылечить инсулинорезистентность?
- Нет, если при нормализации показателей крови (уровня сахара, инсулина, холестерина) вернуться к нездоровому образу жизни.
- Да, остановить резистентность и ее переход в диабет и другие осложнения, можно, если постоянно в течение всей жизни ограничивать потребление рафинированных углеводов, правильно питаться и заниматься физкультурой.