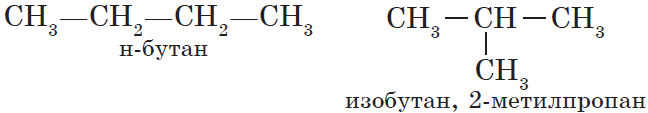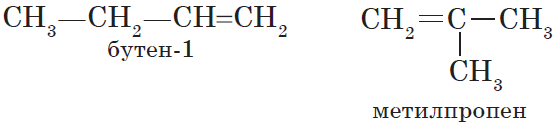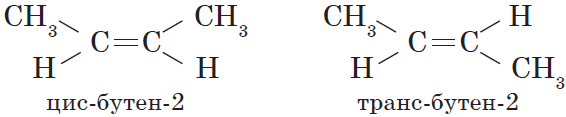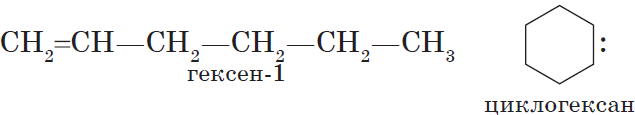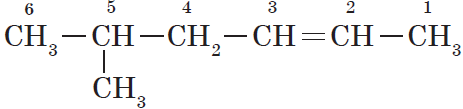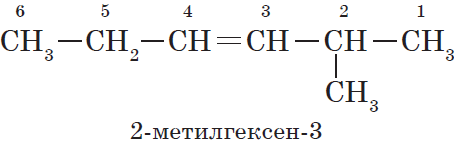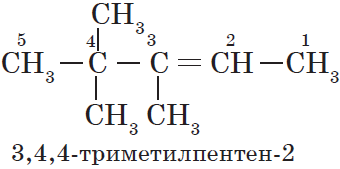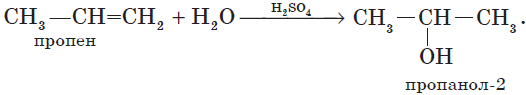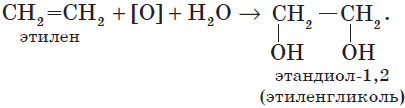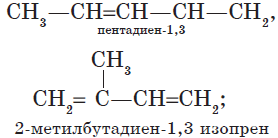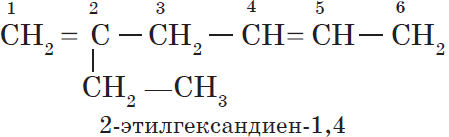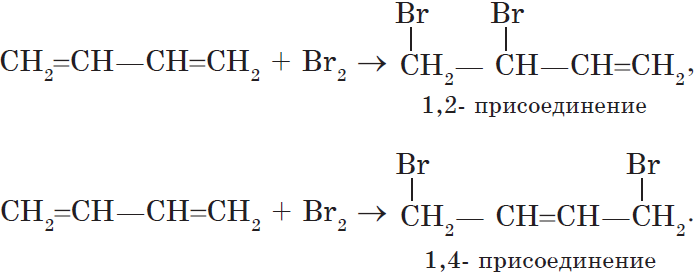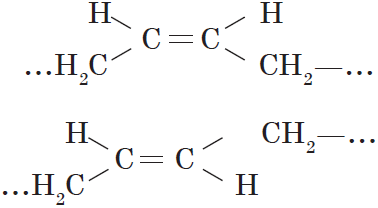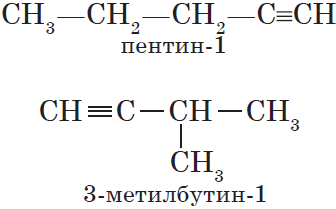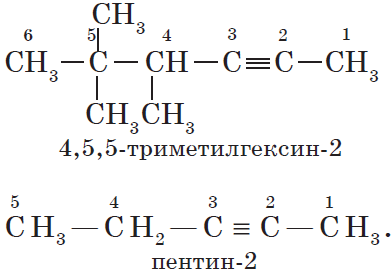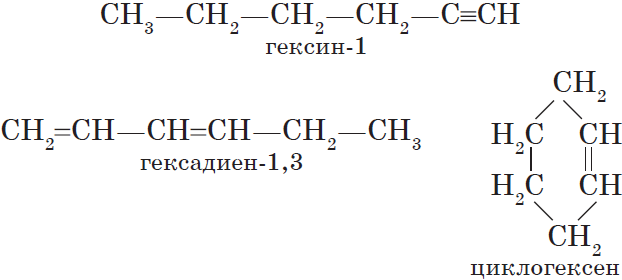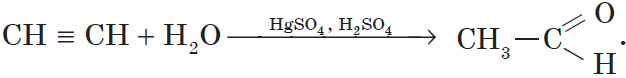Всего: 19 1–19
Добавить в вариант
Верны ли следующие утверждения о способах переработки и использования природного газа?
А. Перед использованием природный газ разделяют на фракции.
Б. Сжигание природного газа используют для получения тепла и электроэнергии.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
Верны ли следующие утверждения о нефти?
А. Нефть состоит преимущественно из предельных углеводородов.
Б. Переработкой нефти получают бензин, керосин, ароматические углеводороды.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Задания Д26 № 257
Основным природным источником бутана является
1) попутный нефтяной газ
2) нефть
3) торф
4) каменный уголь
Задания Д26 № 171
Верны ли следующие суждения о природном газе?
А. Основными составляющими природного газа являются метан и ближайшие его гомологи.
Б. Природный газ служит сырьём для получения ацетилена.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Источник: Демонстрационная версия ЕГЭ—2013 по химии
Верны ли следующие суждения о природном газе?
А. Основными составляющими природного газа являются метан и ближайшие его гомологи.
Б. Природный газ служит сырьём для получения ацетилена.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Источник: Демонстрационная версия ЕГЭ—2014 по химии
Верны ли следующие суждения о способах нефтепереработки?
А. К методам вторичной нефтепереработки относят крекинг-процессы: термический и каталитический.
Б. При каталитическом крекинге наряду с реакциями расщепления происходят реакции изомеризации предельных углеводородов.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Основной составной частью природного газа является
1) ацетилен
2) метан
3) пропан
4) бутан
Задания Д26 № 214
Основной составной частью природного газа является
1) бензол
2) метан
3) этилен
4) бутан
Задания Д26 № 601
Основным компонентом природного газа является
1) этилен
2) ацетилен
3) бензол
4) метан
Основной составной частью природного газа является
1) ацетилен
2) пропан
3) метан
4) этилен
Верны ли следующие утверждения о переработке нефти?
А. Крекинг — химический процесс.
Б. Разделение нефти на фракции — физический процесс.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
Задания Д26 № 558
Верны ли следующие суждения о способах нефтепереработки?
А. К методам вторичной нефтепереработки относят крекинг-процессы: термический и каталитический.
Б. При каталитическом крекинге образуются только предельные углеводороды.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Метан является основным компонентом
1) нефти
2) природного газа
3) коксового газа
4) синтез-газа
Задания Д26 № 859
Уравнение химической реакции
соответствует процессу
1) перегонки
2) риформинга
3) дегидрирования
4) крекинга
В основе крекинга лежат реакции
1) изомеризации
2) присоединения
3) разложения
4) обмена
Задания Д26 № 300
Крекинг нефтепродуктов осуществляется в целях получения
1) бензина
2) сложных эфиров
3) метана
4) мазута
Разделение нефти на фракции осуществляют в процессе
1) перегонки
2) крекинга
3) риформинга
4) коксования
Наиболее токсичны для живого организма ионы:
1) меди
2) натрия
3) ртути
4) магния
5) калия
Запишите номера выбранных ответов.
Для организма человека наиболее токсичным являются каждый из двух ионов:
1)
2)
3)
4)
Источник: Демонстрационная версия ЕГЭ—2014 по химии
Всего: 19 1–19
4.2.3. Природные источники углеводородов, их переработка.
Природный источник углеводородов |
Его основные характеристики |
Нефть |
Многокомпонентная смесь, состоящая преимущественно из углеводородов. Углеводороды представлены в основном алканами, циклоалканами и аренами. |
Попутный нефтяной газ |
Смесь, состоящая практически только из алканов с длинной углеродной цепью от 1 до 6-ти углеродных атомов, образуется попутно при добыче нефти, отсюда и происхождение названия. Имеет место такая тенденция: чем меньше молекулярная масса алкана, тем его процентное содержание в попутном нефтяном газе выше. |
Природный газ |
Смесь, состоящая преимущественно из низкомолекулярных алканов. Основной компонент природного газа — метан. Его процентное содержание в зависимости от месторождения газа может быть от 75 до 99%. На втором месте по концентрации с большим отрывом — этан, еще меньше содержится пропана и т.д. Принципиальное отличие природного газа от попутного нефтяного заключается в том, что в попутном нефтяном газе намного выше доля пропана и изомерных бутанов. |
Каменный уголь |
Многокомпонентная смесь различных соединений углерода, водорода, кислорода, азота и серы. Также в состав каменного угля входит значительное количество неорганических веществ, доля которых существенно выше, чем в нефти. |
Переработка нефти
Нефть представляет собой многокомпонентную смесь различных веществ преимущественно углеводородов. Данные компоненты отличаются друг от друга по температурам кипения. В связи с этим, если нагревать нефть, то сначала из нее будут улетучиваться наиболее легкокипящие компоненты, затем соединения с более высокой температурой кипения и т.д. На данном явлении основана первичная переработка нефти, заключающаяся в перегонке (ректификации) нефти. Данный процесс называют первичным, поскольку предполагается, что при его протекании не происходят химические превращения веществ, а нефть лишь разделяется на фракции с различными температурами кипения. Ниже представлена принципиальная схема ректификационной колонны с кратким описанием самого процесса перегонки:
Перед процессом ректификации нефть специальным образом подготавливают, а именно, избавляют от примесной воды с растворенными в ней солями и от твердых механических примесей. Подготовленная таким образом нефть поступает в трубчатую печь, где нагревается до высокой температуры (320-350 оС). После нагревания в трубчатой печи нефть, обладающая высокой температурой, поступает в нижнюю часть ректификационной колонны, где происходит испарение отдельных фракций и подъем их паров вверх по ректификационной колонне. Чем выше находится участок ректификационной колонны, тем его температура ниже. Таким образом, на разной высоте отбирают следующие фракции:
1) ректификационные газы (отбирают в самой верхней части колонны, в связи с чем их температура кипения не превышает 40 оС);
2) бензиновая фракция (температуры кипения от 35 до 200 оС);
3) лигроиновая фракция (температуры кипения от 150 до 250 оС);
4) керосиновая фракция (температуры кипения от 190 до 300 оС);
5) дизельную фракцию (температуры кипения от 200 до 300 оС);
6) мазут (температуры кипения более 350 оС).
Следует отметить, что средние фракции, выделяемые при ректификации нефти, не удовлетворяют стандартам, предъявляемым к качествам топлив. Кроме того, в результате перегонки нефти образуется немалое количество мазута — далеко не самого востребованного продукта. В связи с этим после первичной переработки нефти стоит задача повышения выхода более дорогих, в частности, бензиновых фракций, а также повышения качества этих фракций. Эти задачи решаются с применением различных процессов вторичной переработки нефти, например, таких как крекинг и риформинг.
Следует отметить, что количество процессов, используемых при вторичной переработке нефти, значительно больше, и мы затрагиваем лишь одни из основных. Давайте теперь разберемся, в чем же заключается смысл этих процессов.
Крекинг (термический или каталитический)
Данный процесс предназначен для повышения выхода бензиновой фракции. Для этой цели тяжелые фракции, например, мазут подвергают сильному нагреванию чаще всего в присутствии катализатора. В результате такого воздействия длинноцепочечные молекулы, входящие в состав тяжелых фракций, рвутся и образуются углеводороды с меньшей молекулярной массой. Фактически это приводит к дополнительному выходу более ценной, чем исходный мазут, бензиновой фракции. Химическую суть данного процесса отражает уравнение:
Риформинг
Данный процесс выполняет задачу улучшения качества бензиновой фракции, в частности повышения ее детонационной устойчивости (октанового числа). Именно эта характеристика бензинов указывается на бензозаправках (92-й, 95-й, 98-й бензин и т.д.).
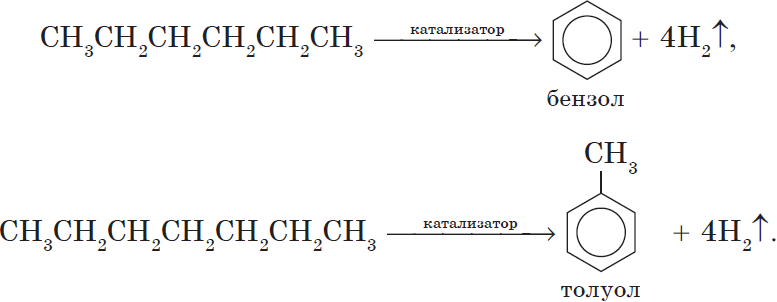
В результате процесса риформинга повышается доля ароматических углеводородов в бензиновой фракции, имеющих среди прочих углеводородов одни из самых высоких октановых чисел. Достигается такое увеличение доли ароматических углеводородов в основном в результате протекания при процессе риформинга реакций дегидроциклизации. Например, при достаточно сильном нагревании н-гексана в присутствии платинового катализатора он превращается в бензол, а н-гептан аналогичным образом — в толуол:
Переработка каменного угля
Основным способом переработки каменного угля является коксование. Коксованием угля называют процесс, при котором уголь нагревают без доступа воздуха. При этом в результате такого нагревания из угля выделяют четыре основных продукта:
1) Кокс
Твердая субстанция, представляющая собой практически чистый углерод.
2) Каменноугольная смола
Содержит большое количество разнообразных преимущественно ароматических соединений, таких как бензол его гомологи, фенолы, ароматические спирты, нафталин, гомологи нафталина и т.д.;
3) Аммиачная вода
Несмотря на свое название данная фракция, помимо аммиака и воды, содержит также фенол, сероводород и некоторые другие соединения.
4) Коксовый газ
Основными компонентами коксового газа являются водород, метан, углекислый газ, азот, этилен и т.д.
Природные источники углеводородов
В природе углеводороды встречаются в виде нефти, природного газа, каменного угля.
Нефть — маслянистая жидкость от светло-бурого до черного цвета с характерным запахом природного происхождения, состоящая из смеси различных углеводородов.
Природный газ — бесцветный газ, состоящий из смеси различных углеводородов (преимущественно из метана).
Каменный уголь — твердое горючее полезное ископаемое, которое имеет сложный состав.
Состав нефти
В зависимости от месторождения нефть имеет различный состав. В неё могут входить: алканы, циклоалканы, ароматические углеводороды.
Фракции нефти
- Фракция, собираемая от 40 до 200°С — фракция бензинов — содержит углеводороды от С6Н12 до С11Н24.
- Лигроиновая фракция, собираемая в пределах от 150 до 250 °С, содержит углеводороды от С8Н18 до С14Н30.
- Керосиновая фракция включает углеводороды от С12Н26 до С18Н38 с температурой кипения от 180 до 300°С.
- В следующей фракции получают газойль (выше 275°С) — дизельное топливо.
- Остаток после перегонки нефти – мазут – содержит углеводороды с большим числом атомов углерода (до многих десятков) в молекуле. После отгонки остается гудрон. Его применяют в дорожном строительстве.
Перегонка нефти
Перегонка – это разделение нефти на отдельные фракции по температуре кипения.
Перегонка нефти осуществляется в ректификационной колонне.
В печи нефть нагревается до 320-350 °С и поступает в ректификационную колонну.
Внутри она имеет горизонтальные перегородки с отверстиями, так называемые тарелки.
Пары нефти подаются в колонну и поднимаются вверх, при этом постепенно охлаждаются и сжижаются.
Менее летучие углеводороды конденсируются внизу, образуя газойлевую фракцию.
Выше собирается керосин, а затем — лигроин. Наиболее летучие углеводороды выходят в виде паров из колонны и сжижаются, образуя бензин.
Главный недостаток перегонки нефти — малый выход бензина (не более 20%).
Крекинг нефтепродуктов
Крекинг — расщепление углеводородов с длинной цепью на углеводороды с меньшей относительной молекулярной массой.
Такой процесс называется крекингом (по англ. crack – расщеплять). Промышленный метод крекинга был изобретен русским инженером В. Г. Шуховым в 1891 г.
Процесс крекинга происходит с разрывом углеродных цепей и образованием более простых предельных и непредельных углеводородов.
Например, при крекинге гексадекана образуются октан и октен:
C16H34 → C8H18 + C8H16
Образовавшиеся вещества могут разлагаться далее. При крекинге октана могут образоваться бутан и бутен:
C8H18 → C4H8 + C4H10
А при крекинге бутана образуются этан и этилен:
C4H10 → C2H4 + C2H6
Различают два основных вида крекинга:
Термический крекинг:
Расщепление углеводородов производится при высокой температуре (470—550°С) и давлении.
Бензин термического крекинга содержит много непредельных углеводородов и обладает большей детонационной стойкостью, чем бензин прямой перегонки. Он менее устойчив при хранении, так как непредельные углеводороды легко окисляются и полимеризуются. Поэтому к бензину термического крекинга добавляют антиокислители.
Каталитический крекинг:
Расщепление углеводородов происходит при несколько более низкой температуре (450- 500°С) с применением катализаторов (алюмосиликатов). Процесс происходит с большей скоростью, чем при термическом крекинге. Бензин каталитического крекинга более высокого качества, чем бензин термического крекинга, так как наряду с реакциями расщепления идет изомеризация и образуются разветвленные углеводороды, которые еще более повышают детонационную стойкость бензина. В бензине каталитического крекинга непредельных углеводородов содержится меньше, и поэтому он более устойчив при хранении.
Ароматизация нефти
Превращение предельных углеводородов и циклоалканов нефти в ароматические углеводороды. Также ароматизацию называют риформингом.
Так как в нефти содержатся также производные циклогексана, например, метилциклогексан, то из него при этих же условиях образуется метилбензол (толуол):
При этих же условиях н-гексан тоже превращается в бензол:
Переработка каменного угля
Каменный уголь подвергают коксованию. Это нагревание без доступа воздуха при температуре 1000-1400оС. При коксовании образуется кокс (почти чистый углерод), коксовый газ (состоит преимущественно из водорода и метана), аммиак, деготь, ароматические углеводорода и др.
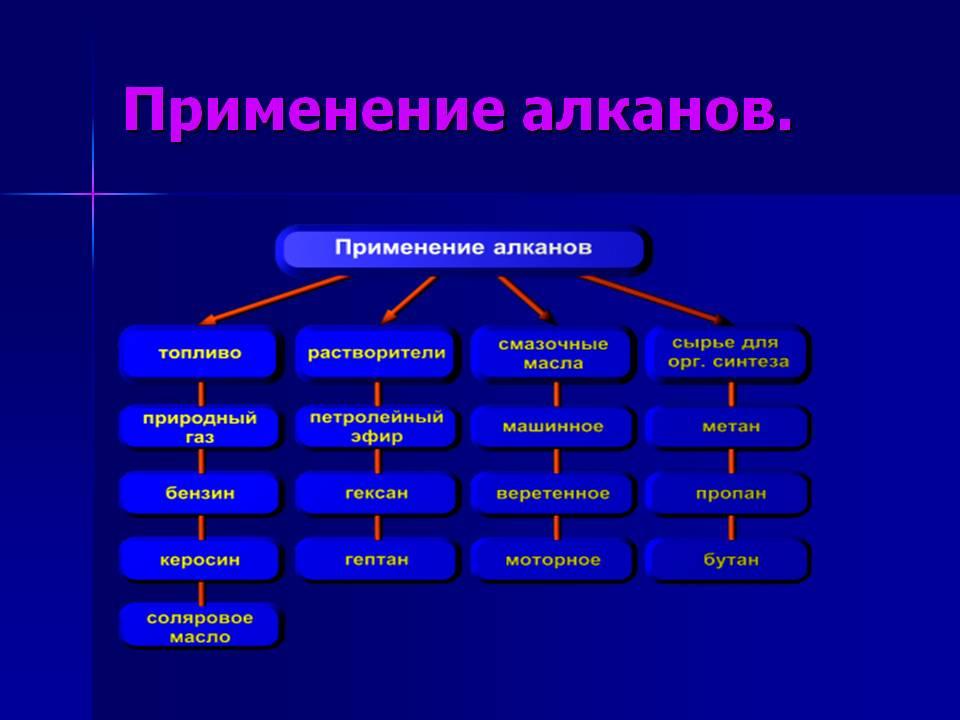
Применение
веществ
Органика
Алканы
Алканы
используются при изготовлении каучука,
синтетических тканей, пластмасс,
поверхностно-активных веществ.
Пропан,
бутан – исп-ся в качестве заправки
баллонов для тушения пожаров в сжиженном
виде
Пропан-бутановая
— смесь в зажигалках
Пропан
— баллоны для дачи
Алканы-газы
– в качестве пропеллентов для изготовления
аэрозолей
СН4
– горючее для газовых плит
С5-С19
– бензин, керосин, смеси для розжига,
топливо
С20
и далее – свечи
С₁₈Н₃₈
до С₃₅Н₇₂ (парафин) — Изготовление
вазелинового масла (смесь жидких
алканов), вазелина (смесь жидких и твёрдых
алканов), свечей, моющих средств, лаков,
эмалей, мыла. В качестве пропитки спичек.
Использование при производстве
органических кислот. В качестве пропитки
упаковочной бумаги. Производство
жевательных резинок
Хлорпроизводные
алканов — изготовление спиртов, альдегидов,
кислот, РАСТВОРИТЕЛИ
Алкены
Циклоалканы
Циклопропан
– анестетик
Циклопентан
— добавка к моторному топливу для
повышения качества.
Циклогексан
используется для синтеза полупродуктов
при производстве синтетических волокон
нейлона и капрона, для получения
циклогексанола, циклогексанона,
адипиновой кислоты, а также в качестве
растворителя.
Алкины
Ацетилен
– газовая сварка, получение технического
карбона; прим-ся в автономных светильниках
и при производстве ракетного топлива
Алкадиены
Синтез
каучуков => пол-е резины, эбонита (не
проводит эл. ток, исп-ся для изоляции),
пвх и т.д.
Бензол
Применяется
в синтезе современных отхаркивающих
средств, препаратов для лечения кожных
заболеваний и других лекарств. В малых
количествах практически не обладает
токсичностью. Применяется в качестве
исходного реагента для синтеза. Он
эффективно растворяет смолы, масла,
жиры, йод и серу.
Бензойная
кислота
Снижает
активность ферментов в структуре
микробов их
Проявляет
дезинфицирующие свойства.
Это
качество нашло активное применение
бензойной кислоты и с успехом используется
для изготовления лекарственных составов
от кашля, отхаркивающих и антисептических
средств
Получение
фунгицид, применяющихся в сельском
хозяйстве для защиты разнообразных
культурных растений.
Консервавнт
Толуол
Лакокрасочные
материалы
Лаки
Краски
РАСТВОРИТЕЛЬ
полимеров
Спирты
—
В
органическом синтезе.
— Биотопливо,
добавки в топливо, ингредиент тормозной
жидкости, гидравлических жидкостей.
—
Растворители.
— Сырье для производства
ПАВ, полимеров, пестицидов, антифризов,
взрывчатых и отравляющих веществ,
бытовой химии.
— Душистые вещества
для парфюмерии. Входят в состав
косметических и медицинских средств.
—
Основа алкогольных напитков, растворитель
для эссенций; сахарозаменитель (маннит
и т.п.); краситель (лютеин), ароматизатор
(ментол).
Этиленгликоль
Производство
теплоносителей и охлаждающих жидкостей,
задачами которых является теплопередача
и теплоотвод соответственно. Производство
пластиковых бутылок. Производство
синтетических волокон. Производство
гидравлических жидкостей. Изготовление
лекарственных средств.
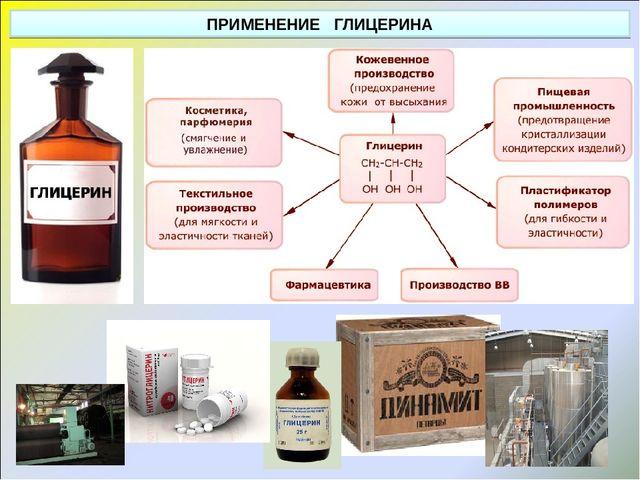
Глицерин
Фенол
АНТИСЕПТИКИ,
лекарства, заменители сахара, красители,
клеи, фенолформальдегидная смола
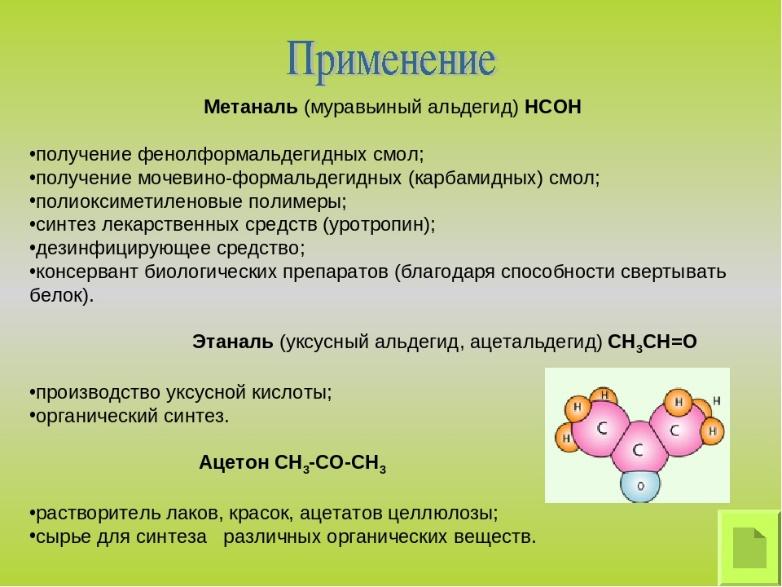
Альдегиды
и ацетон
Альдегиды
нашли широкое применение в качестве
сырья для синтеза различных продуктов.
Так, из формальдегида (крупнотоннажное
производство) получают различные смолы
(фенол-формальдегидные и т.д.), лекарственные
препараты (уротропин); ацетальдегид —
сырье для синтеза уксусной кислоты,
этанола, различных производных пиридина
и т.д. Многие альдегиды (масляный, коричный
и др.) используют в качестве ингредиентов
в парфюмерии
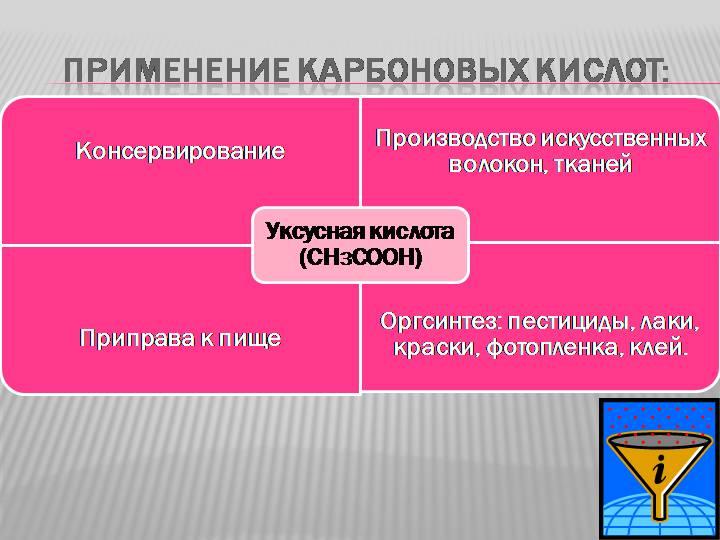
Карб
кислоты
Стеарат/пальмитат
натрия – мыло
Амины
Нитросоединения
Аминокислоты
Жиры
Неорганика
Нитраты
– азотсодержащие удобрения
Фосфат,
гидрофосфат кальция; суперфосфат –
фосфорные удобрения
SiO2
– керамика, стекло
S
– резина
NaHCO3
– разрыхлитель теста, чистящее средство
(NH4)2CO3
– разрыхлитель теста
С
акт. – поглотитель в фильтрах и при
отравлениях
ССl4
– растворитель
NH3
– пол-е удобрений, пол-е азотной к-ты
NH3*H2O
– стеклоочистительные ж-ти и при потере
сознания
O3
– Дезинфекция воды; обнаруживание KI
с крахмалом
Cl2
– Дезинфекция воды; обнаруживание KI
с крахмалом
Лимонная
кислота – удвление накипи с внутр.
пов-ти чайника
H2O2
– антисептик для ран
I2
— антисептик для ран; обнар-е крахмала
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
ПРИРОДНЫЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ
ВАЖНЕЙШИЕ ИСТОЧНИКИ УГЛЕВОДОРОДОВ
1. Природный газ: Россия, Алжир, Иран, США
2. Нефть: Россия, Саудовская Аравия, Кувейт, Иран, Азербайджан
3. Попутный нефтяной газ
4. Каменный уголь
ПРИРОДНЫЙ ГАЗ
смесь газообразных углеводородов различного происхождения, заполняющие поры и пустоты горных пород, рассеянных в почве
Состав: 98%СН4, 2% — С2Н6, С3Н8, С4Н10, N2, CO2, H2, H2S
Применение:
2. Химическое сырье на 10% (сажа, водород, ацетилен, растворители)
ПОПУТНЫЙ НЕФТЯНОЙ ГАЗ — «шапка» над нефтью»
Смесь углеводородов сопутствующие нефти и выделяющиеся при её добыче
Состав: 30-40% — СН4 7,5% — С2Н6, 21,8% — С3Н8, 20,5% -С4Н10
Примеси — N2,CO2, Н2О,Н2S
Раньше сжигали, сейчас улавливают и используют:
2. Химическое сырье — получают: пластмассы, каучуки, сухой газ, пропан- бутановую смесь, газовый бензин
НЕФТЬ — маслянистая горючая жидкость темного цвета, легче воды, имеет специфический запах, не растворяется в воде, не имеет определенной температуры кипения
Сложная смесь углеводородов (150)– алканов, циклоалканов, аренов линейного и разветвленного строения
Физические: ректификация
Химические: алкилирование, крекинг, ароматизация
Происхождение: горная порода осадочного происхождения (каменноугольный период)
Состав: сложная смесь ВМС, С, Н2, N2, O2 ,S
Коксование (пиролиз) – разложение веществ без доступа кислорода при высокой температуре
ПРОДУКТЫ:
Кокс: Чистый уголь С
Коксовый газ: СН4, N2, CO2, CO, Н2, NН3
Каменноугольная смола: C6H6 и его гомологи, C6H5OH, гетероциклические соединения
NH4OH, C6H5OH, H2S
- фракционная перегонка
- термический крекинг
- каталитический крекинг
- риформинг
- гидрокрекинг
- другие процессы
ФРАКЦИОННАЯ ПЕРЕГОНКА НЕФТИ (РЕКТИФИКАЦИЯ НЕФТИ)
Физический способ разделения смеси компонентов с различными температурами кипения.
Перегонка осуществляется в особых установках – ректификационных колоннах.
Ректификация – разделение многокомпонентных жидких смесей на отдельные компоненты.
В них поступающая нефть нагревается примерно до 320° С, и разогретые продукты подаются на промежуточные уровни.
В колонне может быть от 30 до 60 расположенных с определенным интервалом поддонов и желобов, на которых и конденсируются продукты перегонки.
Фракция – часть сыпучего или кускового твердого материала либо жидкой смеси, выделенная по определенному признаку.
Фракции переработки нефти:
- Газовая
- Бензин
- Лигроин
- Керосин
- Дизельное топливо
- Мазут
Самая ценная вторая фракции
КРЕКИНГ
Непрямая переработка нефти- процесс расщепления нефтепродуктов на углеводороды с меньшим числом атомов С
ВИДЫ КРЕКИНГА
1. ТЕРМИЧЕСКИЙ: расщепление молекул углеводородов на алканы и алкены нормального строения
Условия: t=450-5500С, р=2-7 МПА
Продукты крекинга: сырье для получения спиртов, карбоновых кислот, ВМС
Недостаток : бензин малопригоден для использования в качестве моторного топлива, т.к. быстро осмоляется, за счет непредельных углеводородов
2. КАТАЛИТИЧЕСКИЙ – расщепление молекул углеводородов на алканы и алкены разветвленного строения
Условия: t=450-5000С, каt. nAl2O3* mSiO2
Продукты крекинга: углеводороды разветвленного строения(сырье для химической промышленности.
Бензин обладает высоким качеством – с большим октановым числом и детонационной стойкостью.
3. ГИДРОКРЕКИНГ — процесс превращения парообразной нефти в бензин и реактивное топливо под действием водорода при высоком давлении, повышенной температуре и наличии катализатора (на основе вольфрама, никеля или платины).
«Гидроочистка» — гидрирование дистиллятов при невысоких требованиях к выходам продукции, главным образом для удаления серы из сырья.
ПРОЦЕССЫ, ПРОИСХОДЯЩИЕ ПРИ КРЕКИНГЕ
1. АРОМАТИЗАЦИЯ — Пиролиз нефти, риформинг, «облагораживание бензина»
Непрямая химическая переработка бензиновых и лигроиновых фракций при t =500-5400С, каt., p c целью получения высокооктановых бензинов.
Результат: Алканы → циклоалканы→ ароматические (повышение октанового числа бензина)
АЛКИЛИРОВАНИЕ
Процесс введения в молекулы соединений радикалов CH3, C2H5
Используется для получения высокооктанового топлива, ПАВ, инсектицидов, антиокислителей
КАЧЕСТВО БЕНЗИНА определяется детонационной устойчивостью.
Количественным показателем качества бензина является октановое число.
АИ – 92 показывает, что данное горючие имеет такую же детонационную устойчивость, как смесь 92% изооктана и 8% н – гептана.
Для повышения октанового числа используют процесс РИФОРМИНГА низкосортных сортов бензина, который подвергают нагреванию в присутствии катализаторов (платины).
Экологические проблемы использования нефтепродуктов
1.Нефть загрязняет океан при аварийных ситуациях, возникающих на танкерах, разрывах морских трубопроводов, авариях на морских буровых.
2. Ежегодно в океан сливается 2.5 млн.т нефти.
3. Непосредственное отравление живых организмов с летальным исходом.
4. Негативные изменения в среде обитания.
Охрана окружающей среды
1.Необходимо удалять из нефтепродуктов серу и азот, чтобы при сжигании топлива в атмосферу не попадали их оксиды.
2. Необходимо охранять среду от загрязнения отходами производства нефтью и нефтепродуктами.
3. Коксохимические производства обязательно должны быть оборудованы пылеуловителями.
При загрузке шихты и выдаче 1 т. угля выбрасывается 0,75кг. пыли, 0,55кг. сероводорода, 0,07кг. аммиака, 0,0004кг. цианидов, 0,13кг. фенола,0,16кг. аренов.
Нефть самый стойкий загрязнитель океанических вод. Ежегодно в моря и океаны попадает 6-10 млн. тонн нефти. Одна тонна нефти растекаясь образует на поверхности пятно площадью 12 км2.
ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ
И ЕЕ ПОСЛЕДСТВИЯ
ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ — загрязнение газообразными и жидкими химическими соединениями и отдельными элементами, а так же их твердыми фракциями.
ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ АТМОСФЕРЫ
- теплоэлектростанции
- цементные заводы
- металлургические предприятия
- отопления жилищ
- работы транспорта
- сжигания топлива для нужд промышленности
- сжигания и переработки бытовых и промышленных отходов
ПОСЛЕДСТВИЯ:
Фотохимический туман (смог)
Состав :озон, оксиды азота и серы,фотооксиданты .
- наличие в атмосфере
- высокой концентрации оксидов азота;
- углеводородов и других загрязнителей;
- интенсивной солнечной радиации;
- безветрие.
ПУТИ РЕШЕНИЯ:
- контроль за выбросами в атмосферу различных загрязняющих веществ;
- сокращение количества единиц транспорта;
- выведение предприятий за пределы города;
- увеличение высоты труб;
- установка фильтров на предприятиях.
ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ ПРИРОДНЫХ ВОД
- минеральные соли
- кислоты
- щелочи
- глинистые частицы
- нефть
- нефтепродукты
- органические остатки
- пестициды
- тяжелые металлы: ртуть, свинец, кадмий, цинк, медь
ПОСЛЕДСТВИЯ
- происходит повышение температуры воды в водоемах на 6-8°С;
- уменьшается растворимость кислорода;
- ухудшается водообмен между поверхностным и донным слоем.
ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ ПОЧВЫ
- Пестициды
- Кислотные дожди
- Попадание сточных вод
ПОСЛЕДСТВИЯ
- гибель полезных насекомых в почве;
- гибель растений.
ЗАКЛЮЧЕНИЕ:
- Проблема химического загрязнения среды- глобальная проблема человечества.
- Химическое загрязнение затрагивает все сферы географической оболочки Земли.
- Проблема химического загрязнения требует всестороннего изучения и решения, а также участия всех стран мира( в реализации экологических программ).
Органическая химия
Мы приступаем к новому разделу — органической химии. Совершенно необязательно (и даже преступно по отношению к собственному времени!) знать
наизусть, зубрить свойства органических веществ.
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций 
В этой связи особый интерес представляет теория химического строения, которая была создана А.М. Бутлеровым в 1861 году. Она включает в себя несколько
основных положений:
- Атомы в молекуле соединены в определенной последовательности, в соответствии с их валентностью. Порядок связи атомов отражает
химическое строение. - Зная свойства веществ, можно установить их химическое строение, и наоборот, зная строение вещества можно сделать вывод о его
свойствах. - Атомы или группы атомов оказывают взаимное влияние друг на друга непосредственно или через другие атомы
- Свойства вещества зависят от количественного и качественного состава, а также от химического строения молекулы

Алканы (парафины) — насыщенные углеводороды, имеющие линейное или разветвленное строение, содержащие только простые связи. Относятся к
алифатическим углеводородам, так как не содержат ароматических связей.
Алканы являются насыщенными соединениями — содержат максимально возможное число атомов водорода. Общая формула их гомологического ряда
— CnH2n+2.
Номенклатура алканов
Номенклатура (от лат. nomen — имя + calare — созывать) — совокупность названий индивидуальных химических веществ, а также правила составления
этих названий. Названия у алканов формируются путем добавления суффикса «ан»: метан, этан, пропан, бутан и т.д.

Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Перечисленные выше алканы, являются по отношению друг к другу гомологами, то есть составляют один гомологический ряд (греч. homólogos —
соответственный).
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить
читателя с ними. Итак, алгоритм составления названий следующий:
- В структурной формуле вещества необходимо выбрать самую длинную (пусть и изогнутую на рисунке!) цепь атомов углерода
- Атомы выбранной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
- В начале название перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они
связаны. Если в молекуле имеется несколько одинаковых радикалов, то цифрой указывают нахождение каждого из них в главной цепи
и перед их названием соответственно ставят частицы ди-, три-, тетра- и т.д. - Основой названия служит наименование предельного углеводорода с тем же количеством атомов углерода, что и в главной цепи
Внимательно изучите составленные для различных веществ названия ниже.

В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный
атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.
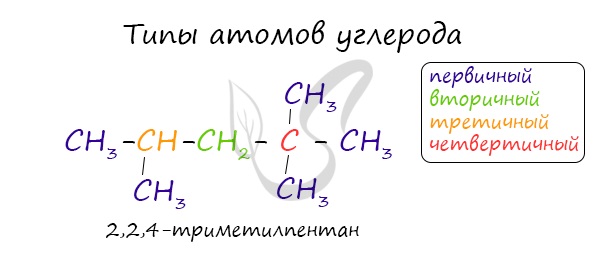
Изомерами (греч. isomeros — составленный из равных частей) называют вещества, имеющие одну молекулярную формулу, но отличающиеся по
строению (структурная изомерия) или расположению атомов в пространстве (пространственная изомерия).
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной
(геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.

В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана
C5H12 существует 3 структурных изомера.
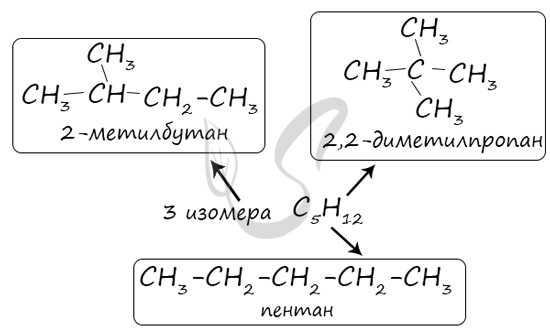
Некоторые данные, касающиеся алканов, надо выучить:
- В молекулах алканов присутствуют одиночные сигма-связи (σ-связи), длина которых составляет 0,154 нм
- Тип гибридизации атомов углерода — sp3
- Валентный угол (между химическими связями) составляет 109°28′
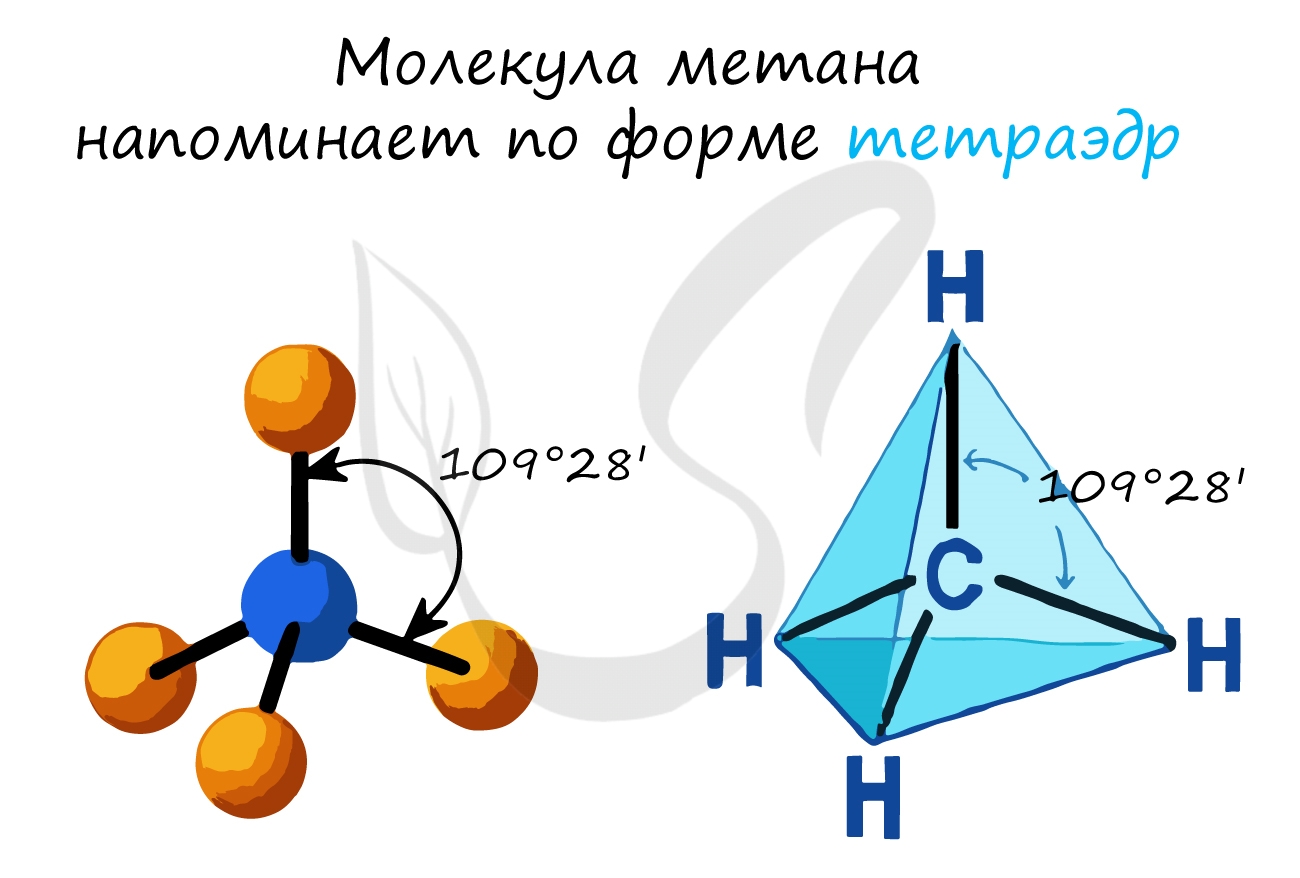
Природный газ и нефть
Алканы входят в состав природного газа: метан 80-97%, этан 0.5-4%, пропан 0.2-1.5% , бутан 0.1-1%, пентан 0-1%. Состав нефти нельзя выразить
одной формулой, он непостоянен и зависит от месторождения.
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем
крекинга из нефти получают алканы.

Получение алканов
В промышленности алканы получают путем:
- Крекинга нефти
- Гидрогенизацией угля (торфа, сланца)
- Гидрированием оксида углерода II
В ходе крекинга нефти получается один алкан и один алкен.
C8H18 → C4H8 + C4H10
C12H26 → C6H12 + C6H14
C + H2 → (t, p) CH4
CO + H2 → (t, p, кат.) CH4 + H2O
В лабораторных условиях алканы получают следующими способами:
- Синтез Дюма
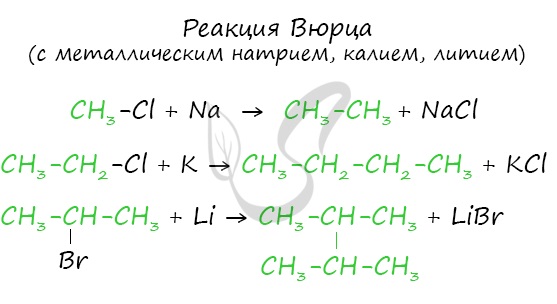
- Реакция Вюрца
- Синтез Гриньяра
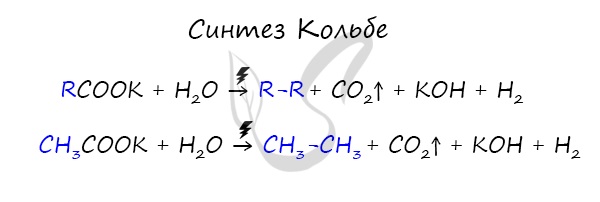
- Синтез Кольбе
- Разложение карбида алюминия
- Гидрированием ненасыщенных углеводородов
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.

Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного
радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
В ходе синтеза Гриньяра с помощью реактива Гриньяра (алкилмагнийгалогенида) получают различные органические соединения, в том числе несимметричные (в отличие от реакции Вюрца).

На схеме выше мы сначала получили реактив Гриньяра, а потом
использовали его для синтеза. Однако можно записать получение реактива Гриньяра и сам синтез в одну реакцию, как показано на примерах ниже.

В результате электролиза солей карбоновых кислот может происходить образование алканов.
В результате разложения карбида алюминия образуется метан и гидроксид алюминия.
Al4C3 + 12H2O → 3CH4 + 4Al(OH)3
CH3-CH=CH2 + H2 → (t, p, Ni) CH3-CH2-CH3
CH2=CH2 + H2 → (t, p, Ni) CH3-CH3
Химические свойства алканов
Алканы — насыщенные углеводороды, не вступают в реакции гидрирования (присоединения водорода), гидратации (присоединения воды). Для
алканов характерны реакции замещения, а не присоединения.
- Галогенирование
- Нитрование (реакция Коновалова)
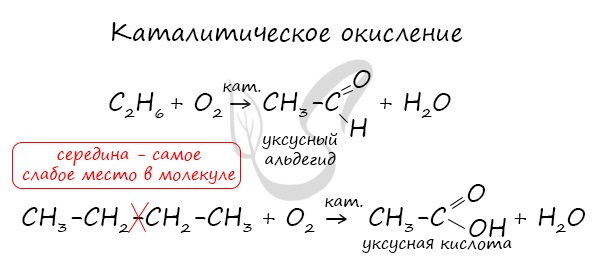
- Окисление
- Пиролиз
- Изомеризация
- Крекинг
Атом галогена замещает атом водорода в молекуле алкана. Запомните, что легче всего идет замещение у третичного атома углерода,
чуть труднее — у вторичного и значительно труднее — у первичного.

Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы,
которые и осуществляют атаку на молекулу углеводорода.

Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция
идет при повышенном давлении, по свободнорадикальному механизму.
CH3-CH3 + HNO3(разб.) → CH3-CH2-NO2 + H2O
Для удобства и более глубокого понимания, азотную кислоту — HNO3 — можно представить как HO-NO2.

Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
С3H8 + O2 → CO2 + H2O
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
CH4 + O2 → CH3-OH (метанол)
Пиролиз (греч. πῦρ — огонь + λύσις — разложение) — термическое разложение неорганических и органических соединений. Принципиальное
отличие пиролиза от горения — в отсутствии кислорода.
CH4 → (t > 1000°С) C + H2
CH4 → (t = 1500-1600°С) CH≡CH + H2↑
CH4 → (t = 1200°С, кат.) CH2=CH2 + H2↑
C2H6 → (t = 1200°С, кат.) CH2=CH2 + H2↑
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.
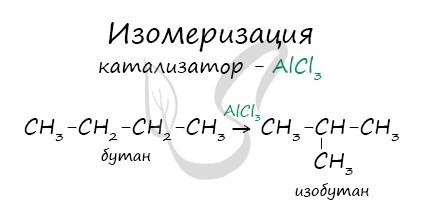
Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их
химическое свойство.
C8H18 → (t) C4H10 + C4H8
C14H30 → (t) C7H14 + C7H16
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Алканы
Алканы — углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле $С_{n}Н_{2n+2}$.
Гомологический ряд метана
Как вы уже знаете, гомологи — это вещества, сходные по строению и свойствам и отличающиеся на одну или более групп $СН_2$.
Предельные углеводороды составляют гомологический ряд метана.
Изомерия и номенклатура
Для алканов характерна так называемая структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Как вам уже известно, простейший алкан, для которого характерны структурные изомеры, — это бутан:
Рассмотрим подробнее для алканов основы номенклатуры ИЮПАК:
1. Выбор главной цепи.
Формирование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
2. Нумерация атомов главной цепи.
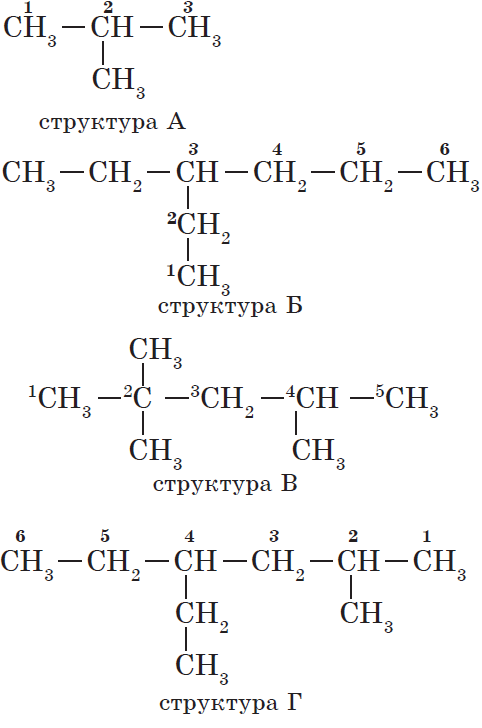
Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (—$СН_3$), затем пропил ($—СН_2—СН_2—СН_3$), этил ($—СН_2—СН_3$) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс -ил в названии соответствующего алкана.
3. Формирование названия.
В начале названия указывают цифры — номера атомов углерода, при которых находятся заместители. Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую ($2.2-$). После номера через дефис указывают количество заместителей (ди — два, три — три, тетра — четыре, пента — пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов — название главной цепи. Главная цепь называется как углеводород — член гомологического ряда метана (метан, этан, пропан и т. д.).
Названия веществ, структурные формулы которых приведены выше, следующие:
— структура А: $2$-метилпропан;
— структура Б: $3$-этилгексан;
— структура В: $2,2,4$-триметилпентан;
— структура Г: $2$-метил $4$-этилгексан.
Физические и химические свойства алканов
Физические свойства. Первые четыре представителя гомологического ряда метана — газы. Простейший из них — метан — газ без цвета, вкуса и запаха (запах газа, почувствовав который, надо звонить $104$, определяется запахом меркаптанов — серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах, для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от $С_5Н_{12}$ до $С_{15}Н_{32}$ — жидкости; более тяжелые углеводороды — твердые вещества.
Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.
Химические свойства.
1. Реакции замещения. Наиболее характерными для алканов являются реакции свободнорадикального замещения, в ходе которого атом водорода замещается на атом галогена или какую-либо группу.
Приведем уравнения наиболее характерных реакций.
Галогенирование:
$CH_4+Cl_2→CH_3Cl+HCl$.
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор:
$CH_3Cl+Cl_2→HCl+{CH_2Cl_2}↙{text»дихлорметан(хлористый метилен)»}$,
$CH_2Cl_2+Cl_2→HCl+{CHСl_3}↙{text»трихлорметан(хлороформ)»}$,
$CHCl_3+Cl_2→HCl+{CCl_4}↙{text»тетрахлорметан(четыреххлористый углерод)»}$.
Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
2. Дегидрирование (отщепление водорода). В ходе пропускания алканов над катализатором ($Pt, Ni, Al_2O_3, Cr_2O_3$) при высокой температуре ($400–600°С$) происходит отщепление молекулы водорода и образование алкена:
$CH_3—CН_3→СH_2=CH_2+Н_2↑$
3. Реакции, сопровождающиеся разрушением углеродной цепи. Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться. Горение предельных углеводородов — это свободнорадикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива:
$СН_4+2О_2→СО_2+2Н_2O+880 кДж.$
В общем виде реакцию горения алканов можно записать следующим образом:
$C_{n}H_{2n+2}+({3n+1}/{2})O_2→nCO_2+(n+1)H_2O$
Термическое расщепление углеводородов:
$C_{n}H_{2n+2}{→}↖{400-500°C}C_{n-k}H_{2(n-k)+2}+C_{k}H_{2k}$
Процесс протекает по свободнорадикальному механизму. Повышение температуры приводит к гомолитическому разрыву углерод-углеродной связи и образованию свободных радикалов:
$R—CH_2CH_2:CH_2—R→R—CH_2CH_2·+·CH_2—R$.
Эти радикалы взаимодействуют между собой, обмениваясь атомом водорода, с образованием молекулы алкана и молекулы алкена:
$R—CH_2CH_2·+·CH_2—R→R—CH=CH_2+CH_3—R$.
Реакции термического расщепления лежат в основе промышленного процесса — крекинга углеводородов. Этот процесс является важнейшей стадией переработки нефти.
При нагревании метана до температуры $1000°С$ начинается пиролиз метана — разложение на простые вещества:
$CH_4{→}↖{1000°C}C+2H_2↑$
При нагревании до температуры $1500°С$ возможно образование ацетилена:
$2CH_4{→}↖{1500°C}CH=CH+3H_2↑$
4. Изомеризация. При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом:
5. Ароматизация. Алканы с шестью и более углеродными атомами в цепи в присутствии катализатора циклизируются с образованием бензола и его производных:
В чем причина того, что алканы вступают в реакции, протекающие по свободнорадикальному механизму? Все атомы углерода в молекулах алканов находятся в состоянии $sp^3$-гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных $С—С$ (углерод — углерод) связей и слабополярных $С—Н$ (углерод — водород) связей. В них нет участков с повышенной и с пониженной электронной плотностью, легко поляризуемых связей, т.е. таких связей, электронная плотность в которых может смещаться под действием внешних факторов (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, т.к. связи в молекулах алканов не разрываются по гетеролитическому механизму.
Алкены
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкадиены (полиены), алкины. Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство непредельности связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных, углеводородов — алканов.
Алкены — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле $С_{n}Н_{2n}$.
Свое второе название — олефины — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел (от лат. oleum — масло).
Гомологический ряд этена
Неразветвленные алкены составляют гомологический ряд этена (этилена):
$С_2Н_4$ — этен, $С_3Н_6$ — пропен, $С_4Н_8$ — бутен, $С_5Н_{10}$ — пентен, $С_6Н_{12}$ — гексен и т. д.
Изомерия и номенклатура
Для алкенов, так же, как и для алканов, характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, — это бутен:
Особым видом структурной изомерии является изомерия положения двойной связи:
$СН_3—{СН_2}↙{бутен-1}—СН=СН_2$ $СН_3—{СН=СН}↙{бутен-2}—СН_3$
Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии — геометрической, или цис-транс изомерии.
Цис-изомеры отличаются от транс-изомеров пространственным расположением фрагментов молекулы (в данном случае метильных групп) относительно плоскости $π$-связи, а следовательно, и свойствами.
Алкены изомерны циклоалканам (межклассовая изомерия), например:
Номенклатура алкенов, разработанная ИЮПАК, схожа с номенклатурой алканов.
1. Выбор главной цепи.
Образование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи.
Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь. Например, правильное название соединения:
$5$-метилгексен-$2$, а не $2$-метилгексен-$4$, как можно было бы предположить.
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей, так же, как для предельных углеводородов.
3. Формирование названия.
Названия алкенов формируются так же, как и названия алканов. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс, обозначающий принадлежность соединения к классу алкенов, — -ен.
Например:
Физические и химические свойства алкенов
Физические свойства. Первые три представителя гомологического ряда алкенов — газы; вещества состава $С_5Н_{10}$ – $С_{16}Н_{32}$ — жидкости; высшие алкены — твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства.
Реакции присоединения. Напомним, что отличительной чертой представителей непредельных углеводородов — алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения.
1. Гидрирование алкенов. Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов — платины, палладия, никеля:
$CH_3—CH_2—CH=CH_2+H_2{→}↖{Pt}CH_3—CH_2—CH_2—CH_3$.
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т.к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция — дегидрирование.
2. Галогенирование (присоединение галогенов). Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе ($CCl_4$) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалоген алканов:
$СН_2=СН_2+Br_2→CH_2Br—CH_2Br$.
3. Гидрогалогенирование (присоединение галогеноводорода).
$CH_3-{CH}↙{пропен}=CH_2+HBr→CH_3-{CHBr}↙{2-бромпропен}-CH_3$
Эта реакция подчиняется правилу Марковникова:
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т.е. атому, при котором находится больше атомов водорода, а галоген — к менее гидрированному.
4. Гидратация (присоединение воды).
Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта:
${CH_2}↙{этен}=CH_2+H_2O{→}↖{t,H_3PO_4}CH_3-{CH_2OH}↙{этанол}$
Обратите внимание на то, что первичный спирт (с гидроксогруппой при первичном углероде) образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты.
Эта реакция протекает также в соответствии с правилом Марковникова — катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа — к менее гидрированному.
5. Полимеризация. Особым случаем присоединения является реакция полимеризации алкенов:
$nCH_2{=}↙{этен}CH_2{→}↖{УФ-свет,R}(…{-CH_2-CH_2-}↙{полиэтилен}…)_n$
Эта реакция присоединения протекает по свободнорадикальному механизму.
6. Реакция окисления.
Как и любые органические соединения, алкены горят в кислороде с образованием $СО_2$ и $Н_2О$:
$СН_2=СН_2+3О_2→2СО_2↑+2Н_2О$.
В общем виде:
$C_{n}H_{2n}+{3n}/{2}O_2→nCO_2↑+nH_2O$
В отличие от алканов, которые устойчивы к окислению в растворах, алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:
Алкадиены (диеновые углеводороды)
Алкадиены — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода и соответствующие общей формуле $С_{n}Н_{2n-2}$.
В зависимости от взаимного расположения двойных связей различают три вида диенов:
— алкадиены с кумулированным расположением двойных связей:
$CH_2=C=CH_2$;
— алкадиены с сопряженными двойными связями;
$CH_2=CH—CH=CH_2$;
— алкадиены с изолированными двойными связями
$CH_2=CH—CH_2—CH=CH_2$.
Эти все три вида алкадиенов существенно отличаются друг от друга по строению и свойствам. Центральный атом углерода (атом, образующий две двойные связи) в алкадиенах с кумулированными связями находится в состоянии $sp$-гибридизации. Он образует две $σ$-связи, лежащие на одной прямой и направленные в противоположные стороны, и две $π$-связи, лежащие в перпендикулярных плоскостях. $π$-Связи образуются за счет негибридизированных р-орбиталей каждого атома углерода. Свойства алкадиенов с изолированными двойными связями весьма специфичны, т.к. сопряженные $π$-связи существенно влияют друг на друга.
р-Орбитали, образующие сопряженные $π$-связи, составляют практически единую систему (ее называют $π$-системой), т.к. р-орбитали соседних $π$-связей частично перекрываются.
Изомерия и номенклатура
Для алкадиенов характерна как структурная изомерия, так и цис-, транс-изомерия.
Структурная изомерия.
— изомерия углеродного скелета:
— изомерия положения кратных связей:
${CH_2=CH—CH=CH_2}↙{бутадиен-1,3}$ ${CH_2=C=CH—CH_3}↙{бутадиен-1,2}$
Цис-, транс-изомерия (пространственная и геометрическая)
Например:
Алкадиены изомерны соединениям классов алкинов и циклоалкенов.
При формировании названия алкадиена указывают номера двойных связей. Главная цепь должна обязательно содержать две кратные связи.
Например:
Физические и химические свойства алкадиенов
Физические свойства.
В обычных условиях пропандиен-1,2, бутадиен-1,3 — газы, 2-метилбутадиен-1,3 — летучая жидкость. Алкадиены с изолированными двойными связями (простейший из них — пентадиен-1,4) — жидкости. Высшие диены — твердые вещества.
Химические свойства.
Химические свойства алкадиенов с изолированными двойными связями мало отличаются от свойств алкенов. Алкадиены с сопряженными связями обладают некоторыми особенностями.
1. Реакции присоединения. Алкадиены способны присоединять водород, галогены, галогеноводороды.
Особенностью присоединения к алкадиенам с сопряженными связями является способность присоединять молекулы как в положениях 1 и 2, так и в положениях 1 и 4.
Соотношение продуктов зависит от условий и способа проведения соответствующих реакций.
2. Реакция полимеризации. Важнейшим свойством диенов является способность полимеризоваться под воздействием катионов или свободных радикалов. Полимеризация этих соединений является основой синтетических каучуков:
$nCH_2={CH—CH=CH_2}↙{бутадиен-1,3}→{(… —CH_2—CH=CH—CH_2— …)_n}↙{text»синтетический бутадиеновый каучук»}$.
Полимеризация сопряженных диенов протекает как 1,4-присоединение.
В этом случае двойная связь оказывается центральной в звене, а элементарное звено, в свою очередь, может принимать как цис-, так и транс-конфигурацию.
Алкины
Алкины — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну тройную связь между атомами углерода и соответствующие общей формуле $С_{n}Н_{2n-2}$.
Гомологический ряд этина
Неразветвленные алкины составляют гомологический ряд этина (ацетилена):
$С_2Н_2$ — этин, $С_3Н_4$ — пропин, $С_4Н_6$ — бутин, $С_5Н_8$ — пентин, $С_6Н_{10}$ — гексин и т. д.
Изомерия и номенклатура
Для алкинов, так же как и для алкенов, характерна структурная изомерия: изомерия углеродного скелета и изомерия положения кратной связи. Простейший алкин, для которого характерны структурные изомеры положения кратной связи класса алкинов, — это бутин:
$СН_3—{СН_2}↙{бутин-1}—С≡СН$ $СН_3—{С≡С}↙{бутин-2}—СН_3$
Изомерия углеродного скелета у алкинов возможна, начиная с пентина:
Так как тройная связь предполагает линейное строение углеродной цепи, геометрическая (цис-, транс-) изомерия для алкинов невозможна.
Наличие тройной связи в молекулах углеводородов этого класса отражается суффиксом -ин, а ее положение в цепи — номером атома углерода.
Например:
Алкинам изомерны соединения некоторых других классов. Так, химическую формулу $С_6Н_{10}$ имеют гексин (алкин), гексадиен (алкадиен) и циклогексен (циклоалкен):
Физические и химические свойства алкинов
Физические свойства. Температуры кипения и плавления алкинов, так же, как и алкенов, закономерно повышаются при увеличении молекулярной массы соединений.
Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены.
Химические свойства.
Реакции присоединения. Алкины относятся к непредельным соединениям и вступают в реакции присоединения. В основном это реакции электрофильного присоединения.
1. Галогенирование (присоединение молекулы галогена). Алкин способен присоединить две молекулы галогена (хлора, брома):
$CH≡CH+Br_2→{CHBr=CHBr}↙{1,2-дибромэтан},$
$CHBr=CHBr+Br_2→{CHBr_2-CHBr_2}↙{1,1,2,2-тетрабромэтан}$
2. Гидрогалогенирование (присоединение галогеноводорода). Реакция присоединения галогеноводорода, протекающая по электрофильному механизму, также идет в две стадии, причем на обеих стадиях выполняется правило Марковникова:
$CH_3-C≡CH+Br→{CH_3-CBr=CH_2}↙{2-бромпропен},$
$CH_3-CBr=CH_2+HBr→{CH_3-CHBr_2-CH_3}↙{2,2-дибромпропан}$
3. Гидратация (присоединение воды). Боль шое значение для промышленного синтеза кетонов и альдегидов имеет реакция присоединения воды (гидратация), которую называют реакцией Кучерова:
4. Гидрирование алкинов. Алкины присоединяют водород в присутствии металлических катализаторов ($Pt, Pd, Ni$):
$R-C≡C-R+H_2{→}↖{Pt}R-CH=CH-R,$
$R-CH=CH-R+H_2{→}↖{Pt}R-CH_2-CH_2-R$
Так как тройная связь содержит две реакционноспособные $π$-связи, алканы присоединяют водород ступенчато:
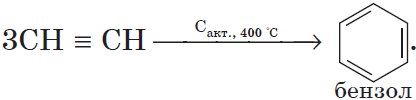
1) тримеризация.
При пропускании этина над активированным углем образуется смесь продуктов, одним из которых является бензол:
2) димеризация.
Помимо тримеризации ацетилена, возможна его димеризация. Под действием солей одновалентной меди образуется винилацетилен:
$2HC≡CH→{HC≡C-CH=CH_2}↙{text»бутен-1-ин-3(винилацетилен)»}$
Это вещество используется для получения хлоропрена:
$HC≡C-CH=CH_2+HCl{→}↖{CaCl}H_2C={CCl-CH}↙{хлоропрен}=CH_2$
полимеризацией которого получают хлоропреновый каучук:
$nH_2C=CCl-CH=CH_2→(…-H_2C-CCl=CH-CH_2-…)_n$
Окисление алкинов.
Этин (ацетилен) горит в кислороде с выделением очень большого количества теплоты:
$2C_2H_2+5O_2→4CO_2↑+2H_2O+2600кДж$ На этой реакции основано действие кислородно-ацетиленовой горелки, пламя которой имеет очень высокую температуру (более $3000°С$), что позволяет использовать ее для резки и сварки металлов.
На воздухе ацетилен горит коптящим пламенем, т.к. содержание углерода в его молекуле выше, чем в молекулах этана и этена.
Алкины, как и алкены, обесцвечивают подкисленные растворы перманганата калия; при этом происходит разрушение кратной связи.














![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)