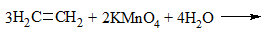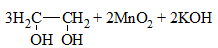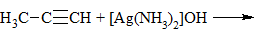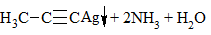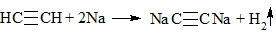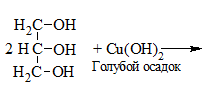| Соединение, функциональная группа | Реагент | Что наблюдается, уравнение реакции |
|
Алкены >C=C< |
Водный раствор KMnO4 |
Наблюдают исчезновение фиолетовой окраски KMnO4 и образование хлопьевидного осадка диоксида марганца бурого цвета 3 >C=C< + 2KMnO4 + 4H2O → 3 >C(OH)-C(OH)< + 2MnO2↓ + 2KOH |
| Раствор Br2 в органическом растворителе или воде (бромная вода) |
Исчезает желто-коричневая окраска раствора брома из-за протекания реакции: >C=C< + Br2 → >C(Br)-C(Br)< |
|
| Алкины -С≡С- | Раствор Br2 в органическом растворителе или воде (бромная вода) |
Исчезает желто-коричневая окраска раствора брома из-за протекания реакции: R-С≡С-R’ + 2Br2 → R-CBr2-CBr2-R’ |
|
Водные растворы аммиачных комплексов Ag(I), например, аммиачный раствор оксида серебра [Ag(NH3)2]OH |
Алкины с тройной связью на конце молекулы дают желтый осадок: R-С≡СН + [Ag(NH3)2]OH → R-С≡СAg↓ + 2NH3 + H2O Алкины, у который при тройной связи нет атомов водорода в такую реакцию не вступают |
|
|
Водный раствор аммиачных комплексов одновалентной меди Cu(I), например, аммиачный раствор оксида меди (I) [Cu(NH3)2]OH |
Алкины с тройной связью на конце молекулы дают красный осадок : R-С≡СН + [Cu(NH3)2]OH → R-С≡СCu↓ + 2NH3 + H2O Алкины, у которых при тройной связи нет атомов водорода в такую реакцию не вступают, что позволяет отличить их друг от друга |
|
| Бензол | Нитрующая смесь – смесь конц. азотной и серной кислот |
Образование желтой жидкости с запахом горького миндаля на дне реакционной смеси |
| Гомологи бензола | Нейтральный водный раствор KMnO4 |
При кипячении с каким-либо гомологом бензола водный раствор перманганата калия обесцвечивается и выпадает бурый осадок оксида марганца (IV). На примере с толуолом и этилбензолом реакции выглядят следующим образом: C6H5CH3 +2KMnO4 = C6H5COOK + 2MnO2↓ + KOH + H2O (при кипячении) C6H5CH2CH3 + 4KMnO4 = C6H5COOK + K2CO3 + 2H2O + 4MnO2↓ + KOH (при нагревании) |
| Подкисленный водный раствор перманганата калия KMnO4(водн.), H+ |
Постепенное обесцвечивание подкисленного раствора KMnO4. Выпадения бурого осадка MnO2 не наблюдается, поскольку марганец восстанавливается до практически бесцветной соли двухвалентного марганца. Чаще всего в качестве подкислителя изпользуют серную кислоту. На примере с толуолом реакция выглядит следующим образом: 5C6H5CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 6MnSO4 + 3K2SO4 +14H2O |
|
| Фенол | Бромная вода |
Исчезновение желто-коричневой окраски бромной воды с одновременным выпадением белого осадка трибромфенола: |
|
Разбавленный водный раствор соли железа (III), например, FeCl3 |
Светло-желтая окраска разбавленного раствора соли трехвалентного железа сменяется на фиолетовую | |
| Анилин | Бромная вода |
Исчезновение желто-коричневой окраски бромной воды с одновременным выпадением белого осадка триброманилина: |
|
Одноатомные первичные и вторичные спирты CH3OH, C2H5OH, (CH3)2CH-OH и т.д. |
Оксид меди (II) CuO |
Черный CuO при нагревании со спиртом изменяет свою окраску на красную в связи с восстановлением до Cu0. Первичный спирт при этом превращается в альдегид: R-CH2-OH + CuO =to=> R-CHO + Cu + H2O, вторичный — в кетон: R-C(OH)-R’+ CuO =to=> R-C(O)-R’ + Cu + H2O, В случае метанола появляется легко узнаваемый запах формальдегида (естественно, чтобы он был узнаваемым, нужно до этого быть знакомым с его запахом:-) ) В случае реакции с CuO этилового спирта чувствуется специфический запах ацетальдегида, схожий с ароматом прелых яблок сорта «антоновка» |
| Многоатомные спирты | Свежеосажденный Cu(OH)2 (II) |
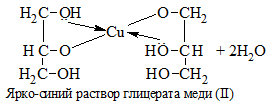
Растворение голубого осадка Cu(OH)2 с образование ярко-синего раствора комплексного соединения меди. На примере с глицерином уравнение реакции выглядит следующим образом: |
|
Альдегиды, —CHO |
Аммиачный раствор оксида серебра [Ag(NH3)2]OH |
Так называемая реакция серебряного зеркала. В результате восстановления Ag+1 в металлическое серебро Ag0 на стенках сосуда образуется зеркало. При небрежном смешении реагентов или в недостаточно чистом сосуде вместо серебряного зеркала может образоваться черный осадок, состоящий из мелкодисперсных частиц металлического серебра. В обоих случаях наблюдаемые явления описываются уравнением в общем виде: R-CHO + 2[Ag(NH3)2]OH = R-СООNH4 + 2Ag↓ + 3NH3↑ + H2O |
|
Свежеосажденный Cu(OH)2 |
Образование оранжево-красного осадка Cu2O при нагревании в результате реакции: R-CHO + 2Cu(OH)2 = R-COOH + Cu2O↓ + 2H2O |
|
|
Карбоновые кислоты, -COOH |
Лакмус | Окрашивание лакмуса в красный цвет |
| Карбонаты, например, K2CO3 |
Выделение углекислого газа в результате разложения образующейся нестойкой угольной кислоты H2CO3: 2R-COOH + CO32- → CO2 + H2O + R-COO— |
|
| Спирт + конц. H2SO4 |
Появление запаха сложного эфира, образующегося в результате реакции: R-COOH + R’-OH → R-COO-R’ + H2O Запахи эфиров весьма разнообразны, но общим является ярко выраженная пахучесть, нередко, могут напоминать ароматы различных фруктов. |
|
|
Муравиная кислота -СНО и -СООН |
Лакмус |
Окрашивание лакмуса в красный цвет, по причине кислой среды, создаваемой муравьиной кислотой: HCOOH ↔ HCOO— + H+ |
|
Аммиачный раствор оксида серебра [Ag(NH3)2]OH |
Молекуле муравьиной кислоты, не смотря на ее малый размер удается сочетать в себе помимо карбоксильной группы также и карбонильную, которая позволяет вступать муравьиной кислоте в реакцию серебряного зеркала подобно альдегидам: HCOOH + 2[Ag(NH3)2]OH → 2Ag↓ + 4NH3↑ + CO2↑ + 2H2O |
|
|
Растворимые соли жирных карб. кислот, например, стеарат натрия CH3(CH2)16COONa (мыло) |
Любая сильная неорганическая кислота или кислота средней силы H2SO4 (разб.) HCl HI HBr HNO3 (разб.) H3PO4 |
Выпадение хлопьевидного белого осадка малорастворимой жирной кислоты: CH3(CH2)16COONa + H+ → Na+ + CH3(CH2)16COOH |
| Раствор соли Ca или Mg |
Выпадение белого осадка нерастворимой кальциевой или магниевой соли жирной кислоты. Ионное уравнение в общем виде: 2R-COO— + Ca2+ → (R-COO)2Ca↓, где R-длинный углеводородный радикал. На примере, стеарата натрия и хлорида кальция молекулярное уравнение реакции выглядит так: 2CH3(CH2)16COONa + CaCl2 → (CH3(CH2)16COONa)2Ca↓ |
|
| Фенолфталеин |
Окрашивание фенолфталеина в малиновый цвет как в щелочах, ввиду того, что соли жирных кислот гидролизуются по аниону: CH3(CH2)16COO— + H2O → CH3(CH2)16COOH + OH— |
|
|
Олеиновая кислота, -COOH; >C=C< |
Водный раствор KMnO4(водн.) |
Наблюдают исчезновение фиолетовой окраски KMnO4 и образование хлопьевидного осадка оксида марганца бурого цвета MnO2 3>C=C< + 2KMnO4 + 4H2O → 3>C(OH)-C(OH)< + 2MnO2↓ + 2KOH |
| Раствор Br2 в орг. растворителе или воде (бромная вода) |
Исчезает желто-коричневая окраска раствора брома из-за протекания реакции (указан структурный фрагмент молекулы олеиновой кислоты): >C=C< + Br2 → C(Br)=C(Br)< |
|
| Раствор щелочи, например, NaOH |
Олеиновая кислота, будучи практически нерастворимой в воде жирной кислотой, растворяется в водных растворах щелочей: C17H33COOH + NaOH → C17H33COONa + H2O |
|
|
Глюкоза, -CHO -C(OH)-C(OH)- |
Аммиачный раствор оксида серебра [Ag(NH3)2]OH |
Глюкоза относится к так называемым альдегидоспиртам, т.к. ее молекулы содержат альдегидную группу и 5 гидроксильных групп. Поэтому она вступает в реакцию «серебряного зеркала» |
|
Свежеосажденный Cu(OH)2 |
Если раствор глюкозы прибавить к свежеосажденному гидроксиду меди без нагревания наблюдается растворение осада гидроксида меди и образование синего раствора. В этом случае глюкоза реагирует как многоатомный спирт — с образованием растворимых комплексов меди. Если же полученный синий раствор нагреть, выпадает оранжево-красный осадок одновалентного оксида меди Cu2O. При этом глюкоза реагирует как альдегид — альдегидная группа молекулы глюкозы окисляется до карбоксильной — образуется глюконовая кислота. | |
| Крахмал |
Йод, I2 |
Появление синей окраски |
| Белок |
концентрированная азотная кислота НNО3(конц.) |
Ксантопротеиновая реакция Появление ярко-желтого окрашивания по причине нитрования бензольных колец молекул белка |
|
Свежеосажденный Cu(OH)2 |
Появляется сине-фиолетовое окрашивание раствора в следствие образование комплексов меди (II) с белком |
-
ЕГЭ по химии 2023
- /
-
Теория по химии
- /
- Теория по теме «Качественные реакции органических соединений»
- /
Качественные реакции органических соединений
Разбор сложных заданий в тг-канале:
Всего: 60 1–20 | 21–40 | 41–60
Добавить в вариант
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) алкадиены
Б) одноатомные спирты
В) карбоновые кислоты
Г) алкены
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО
ОПРЕДЕЛЕНИЯ
1) аммиачный раствор оксида серебра
2) гидрокарбонат натрия
3) оксид меди (II)
4) бромная вода
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между веществом и качественной реакцией на вещества этого класса: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) Ацетальдегид
Б) Сорбит
В) Фенол
Г) Ацетилен
КАЧЕСТВЕННЫЕ РЕАКЦИИ
1) Фиолетовое окрашивание раствора хлорида железа (III)
2) Белый осадок с аммиачным раствором оксида серебра
3) Образование фиолетового раствора с гидроксидом меди (II)
4) Образование раствора с интенсивной синей окраской с гидроксидом меди (II)
5) Реакция «серебряного зеркала»
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Задание Яндекса
Задания Д26 № 815
Качественной реакцией на формальдегид является его взаимодействие с
1) водородом
2) бромной водой
3) хлороводородом
4) аммиачным раствором оксида серебра
Задания Д26 № 987
Реакция с гидроксидом меди (II) является качественной на
1) кетоны
2) фенолы
3) одноатомные спирты
4) многоатомные спирты
Качественной реакцией на многоатомные спирты является реакция с
1) кислородом
2) хлороводородом
3) гидроксидом калия
4) гидроксидом меди (II)
Качественной реакцией на многоатомные спирты является реакция с
1) гидроксидом калия
2) кислородом
3) гидроксидом меди (II)
4) хлороводородом
Источник: ЕГЭ — 20.06.2016 по химии. Основная волна.
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) карбоновые кислоты
Б) многоатомные спирты
В) одноатомные спирты
Г) альдегиды
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО
ОПРЕДЕЛЕНИЯ
1) аммиачный раствор ок-сида серебра
2) карбонат натрия
3) оксид меди(II)
4) кислород
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) многоатомные спирты
Б) одноатомные спирты
В) карбоновые кислоты
Г) алкены
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО
ОПРЕДЕЛЕНИЯ
1) аммиачный раствор оксида серебра
2) карбонат натрия
3) оксид меди (II)
4) бромная вода
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Задания Д26 № 772
Белки приобретают жёлтую окраску под действием
1)
2)
3)
4)
Задания Д26 № 944
Раствор перманганата калия можно использовать для обнаружения
1) циклогексана
2) дихлорэтана
3) гексана
4) этилена
Раствор перманганата калия можно использовать для обнаружения
1) бензола
2) циклопентана
3) бутана
4) пропена
Установите соответствие между классом органических соединений и реактивом, который может быть использован для их качественного определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
A) многоатомные спирты
Б) одноатомные спирты
В) альдегиды
Г) терминальные алкины
РЕАКТИВ ДЛЯ КАЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ
1)
2) аммиачный раствор оксида серебра
3) водород
4) оксид меди(II)
5) кислород
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между органическим соединением и реактивом, который может быть использован для его обнаружения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) 1,2-пропиленгликоль
Б) уксусная кислота
В) этиленгликоль
Г) пропилен
РЕАКТИВ ДЛЯ ОБНАРУЖЕНИЯ
1) гидроксид натрия (в присутствии кислотно-основного индикатора)
2) гидроксид железа (III)
3) бромная вода
4) водород
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Неизвестное органическое вещество взаимодействует и с натрием, и с гидроксидом меди(II). Формула вещества
1) CH3CHO
2) С2Н5ОН
3) HOCH2CH2OH
4) С6Н5СН3
Неизвестное органическое вещество реагирует с натрием и обесцвечивает подкисленный раствор перманганата калия. Формула вещества
1) C6H5CH3
2) C2H4
3) СH3COОН
4) C2H5OH
Установите соответствие между формулой газа и качественной реакцией, позволяющей идентифицировать этот газ.
КАЧЕСТВЕННАЯ РЕАКЦИЯ
1) при пропускании через аммиачный раствор оксида серебра выпадает серый осадок
2) при пропускании через аммиачный раствор оксида серебра на стенках сосуда образуется зеркальный налёт
3) тлеющая лучинка вспыхивает
4) при пропускании через известковую воду выпадает белый осадок
5) влажная лакмусовая бумажка окрашивается в синий цвет
Запишите в таблицу выбранные цифры под соответствующими буквами.
Неизвестное органическое вещество даёт реакцию «серебряного зеркала», а при добавлении соды к раствору этого вещества выделяется газ. Формула вещества
1) СН3СНО
2) НСООН
3) С2Н2
4) СН3СООН
Жидкое органическое вещество не смешивается с водой, но обесцвечивает бромную воду и раствор перманганата калия. Формула вещества
1) С5Н12
2) С6Н5СН=СН2
3) С6Н6
4) С2Н5ОН
Установите соответствие между органическим соединением и реактивом, который может быть использован для его обнаружения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВО
А) глицерин
Б) пропионовая кислота
В) пропилен
Г) ацетилен
РЕАКТИВ ДЛЯ ОБНАРУЖЕНИЯ
1) гидроксид бария
2) гидроксид железа (III)
3) вода
4) бромная вода
5) (в изб.
)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между веществом и реактивом, который служит для качественного определения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) бромид натрия
Б) глицерин
В) пищевая сода
Г) гексен-3
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Всего: 60 1–20 | 21–40 | 41–60
Качественные реакции органических соединений
Таблица. Качественные реакции на органические вещества
| Органическое вещество | Реактив | Наблюдаемая реакция |
| Алкены, алкины, алкадиены
(этилен, ацетилен, дивинил и др.) |
Бромная вода, Br2 (р-р) | Обесцвечивание раствора (видеоопыт реакция этилена с бромной водой, ацетилен с бромной) |
| Алкены, алкины, алкадиены
(этилен, ацетилен, дивинил и др.) |
Перманганат калия KMnO4 | Обесцвечивание раствора (видеоопыт) |
| Алкины с тройной связью на конце цепи
(ацетилен С2Н2, пропин и др.) |
Аммиачный раствор оксида серебра, [Ag(NH3)2]OH | Выпадение осадка соли серебра (видеоопыт) |
| Многоатомные спирты (этиленгликоль, глицерин и др.) | Свежеосажденный гидроксид меди (II) Сu(OH)2 | Образование ярко-синего раствора комплекса (видеоопыт) |
| Фенолы
(С6Н5ОН — фенол и др.) |
Бромная вода, Br2 (р-р) | Выпадение белого осадка |
| Раствор хлорида железа (III) FeCl3 | Образование фиолетового раствора | |
| Альдегиды
(СН2О — муравьиный альдегид и др.) + муравьиная кислота НСООН + глюкоза (и другие углеводы-альдозы) + восстанавливающие дисахариды (мальтоза, лактоза, целлобиоза) |
Свежеосажденный гидроксид меди (II) Сu(OH)2 при нагревании | Образование красного осадка Cu2O |
| Аммиачный раствор оксида серебра, [Ag(NH3)2]OH при нагревании | Выпадение осадка металлического серебра (реакция серебряного зеркала) | |
| Карбоновые кислоты
(уксусная кислота CH3СООН и др.) |
Гидрокарбонат натрия (сода) NaHCO3 | Выделение бесцветного газа СО2 |
| Анилин | Бромная вода, Br2 (р-р) | Выпадение белого осадка 2,4,6-триброманилина |
| Аминокислоты (содержащие ароматическое кольцо) | Азотная кислота, HNO3 | Желтое окрашивание |
| Белки | Азотная кислота, HNO3 | Желтое окрашивание (ксантопротеиновая реакция) |
| Свежеосажденный гидроксид меди (II) Сu(OH)2 | Образование фиолетового раствора (биуретовая реакция) | |
| Крахмал | Раствор йода, I2 (р-р) | Синее окрашивание |
| Первичные амины
(CH3NH2 метиламин и др.) |
Азотистая кислота HNO2 | Выделение бесцветного газ, не поддерживающего горение (азот) |
| Вторичные амины
((CH3)2NH диметиламин и др.) |
Азотистая кислота HNO2 | Желтое окрашивание |
Задание 25. Качественные реакции (подробно)
1. Как распознать алкены и стирол (в случае стирола в реакции вступает только двойная связь боковой цепи, а не бензольное кольцо)
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях)
CH2=CH2 + Br2 → CH2Br-CH2Br
2) + KMnO4 (водный раствор) → обесцвечивание раствора, образование осадка MnO2 бурого цвета:
Раствор перманганат калия фиолетового цвета. В результате реакции окраска исчезает, образуется осадок MnO2 бурого цвета.
2. Как распознать алкины
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях):
C2H2 + 2Br2 → CHBr2-CHBr2
2) + KMnO4 (водный раствор) → обесцвечивание раствора, образование осадка MnO2 бурого цвета:
3C2H2 + 8KMnO4 → 3K2C2O4 + 8MnO2 + 2KOH + 2H2O (K2C2O4 — соль щавелевой кислоты)
3) + [Ag(NH3)2]OH → выпадение осадка в случае концевой тройной связи:
4) + Металл → выпадение осадка и выделение водорода в случае концевой тройной связи
3. Как распознать бензол
1) Бензол горит коптящим пламенем из-за большого содержания углерода.
Благодаря устойчивой ароматической системе бензол не вступает в реакции с водным раствором Br2 и раствором KMnO4.
4. Как распознать одноатомные спирты
1) + CuO → наблюдаем выделение металлической меди:
CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O (t, окисление спиртов до альдегидов)
2) + Na → наблюдаем выделение газа:
2C2H5-OH + 2Na → 2C2H5-ONa + H2
С основаниями одноатомные спирты не взаимодействуют.
5. Как распознать многоатомные спирты
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора:
С щелочами многоатомные спирты не взаимодействуют.
6. Как распознать фенолы
1) + Br2 → выпадение белого осадка 2,4,6-трибромфенола
2) + FeCl3 → раствор фиолетового цвета
7. Как распознать альдегиды
1) + [Ag(NH3)2]OH → восстановление металлического серебра
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета
8. Как распознать карбоновые кислоты
1) раствор лакмуса → изменение окраски на красную
2) + Na2CO3/NaHCO3 → выделение газа CO2
9. Как распознать соли высших карбоновых кислот
1) + HCl (любая сильная кислота) → появление хлопьев нерастворимых высших кислот
10. Как отличить муравьиную кислоту от уксусной
Муравьиная кислота содержит и альдегидную группу тоже, следовательно, возможны реакции, характерные альдегидам:
1) + [Ag(NH3)2]OH → восстановление металлического серебра и выделение газа (так как кислота окисляется до CO2)
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета и выделение газа (так как кислота окисляется до CO2).
11. Как распознать низшие амины
1) раствор лакмуса → изменение окраски на синюю (так как среда раствора щелочная)
1) раствор фенолфталеина → изменение окраски на малиновую
12. Как распознать анилин
1) + Br2 → выпадение белого осадка 2,4,6-триброманилина
13. Как распознать белок
1) + HNO3 → желтое окрашивание (ксантопротеиновая реакция)
2) + Cu(OH)2 → фиолетовое окрашивание (биуретовая реакция)
14. Как распознать глюкозу C6H12O6
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора (реакция на несколько гидроксильных групп)
2) + Cu(OH)2 → при нагревании образуется осадок Cu2O красного цвета (реакция на альдегидную группу)
3) + [Ag(NH3)2]OH → восстановление металлического серебра
15. Как распознать крахмал
1) + I2 → появление синей окраски.
Задание 25 в ЕГЭ-2021 по химии: качественные реакции органических веществ. Признаки протекания реакций с участием органических веществ
Вебинар от издательства Легион.
Ведущий: Доронькин Владимир Николаевич
Презентация к вебинару:
→ предварительный просмотр
→ скачать презентацию
Качественные реакции – это реакции, позволяющие доказать наличие того или иного вещества (иона) в среде или присутствие функциональной группы в веществе. Анализируемые вещества могут находиться в различных агрегатных состояниях (твёрдом, жидком и газообразном). С точки зрения наблюдаемых эффектов все реакции обнаружения можно разделить на несколько групп:
1) образование характерных осадков,
2) растворение вещества,
3) появление (изменение) окраски,
4) выделение газов,
5) изменение запаха,
6) окрашивание пламени.
Различить вещества — это значит провести превращения, которые отличаются признаками протекания реакций или свойствами продуктов реакции. Для решения подобных заданий недостаточно знать только качественные реакции, необходимо учитывать химические и физические свойства веществ.
Вывод:
1) Необходимо знать химические свойства веществ (уметь составлять уравнения реакций)
2) Необходимо знать физические свойства изучаемых веществ (растворимость, цвет, запах, …)
3) Необходимо знать качественные реакции
Примеры заданий:
Пример 1. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) пропановая кислота и литий
Б) пропанол-2 и калий
В) гидроксид цинка и уксусная кислота
Г) бромная вода и ацетилен
ПРИЗНАК РЕАКЦИИ
1) растворение осадка
2) образование осадка
3) видимые признаки реакции отсутствуют
4) выделение газа
5) обесцвечивание раствора
Анализ и решение.
Вывод: Необходимо составить уравнения реакций и отметить наблюдаемые изменения (признаки). Далее решение смотрите в презентации
Смотрите также: