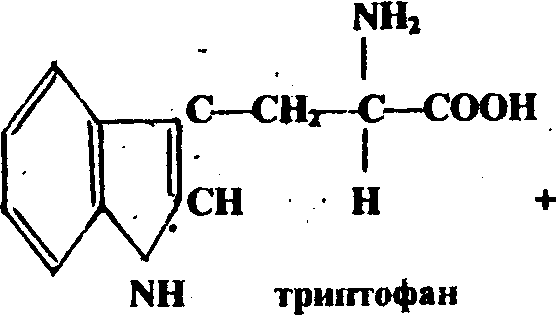
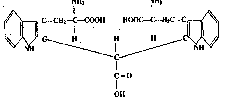
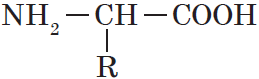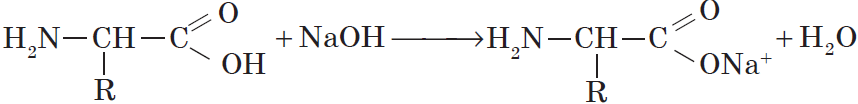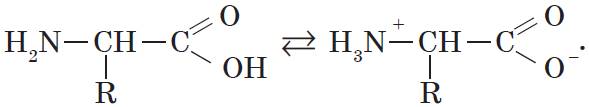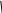Белки (син. протеины) — высокомолекулярные органические вещества, построенные из остатков аминокислот. По
своему биологическому значению принадлежат к числу важнейших составных частей организма.
Несомненно, белки абсолютно необходимы для жизни растений, животных и грибов. Именно вследствие такого
большого значения белки получили названия протеинов (греч. protos — первый, главный).

Качественной реакцией на белки служит ксантопротеиновая реакция. Ее проводят путем добавления к раствору белка HNO3(конц.) до
тех пор, пока не прекратится выпадение осадка. Осадок окрашивается в характерный желтый цвет.

Аминокислота
Аминокислота — органическая кислота, содержащая, по меньшей мере, одну карбоксильную группу (COOH) и одну аминогруппу (NH2).
Аминокислоты являются основной составляющей всех белков.
В построении белков участвуют 20 наиболее распространенных аминокислот. На данном этапе учить их наизусть не обязательно, эта
задача настигнет вас на кафедре биохимии 
И все же для успешного изучения данной темы мы возьмем за основу две аминокислоты: глицин и аланин.

Я хочу вас обрадовать (надеюсь, что обрадую)). Если вы успешно изучили темы: карбоновые кислоты, амины — то вы уже знаете химические
свойства аминокислот!
Они напоминают амфотерные соединения: по аминогруппе вступают в реакции с кислотами, по карбоксильной — с основаниями. Мы разберем их подробнее чуть
ниже.
Получение аминокислот
Аминокислоты можно получить в реакции аммиака с галогенкарбоновыми кислотами.

Химические свойства аминокислот
- Основные свойства
- Кислотные свойства
- Пептидные связи
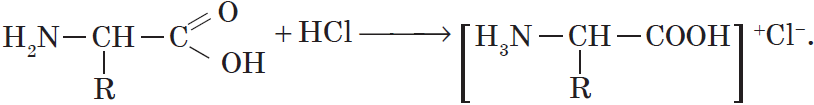
За счет наличия аминогруппы, аминокислоты проявляют основные свойства. Реагируют с кислотами.

По карбоксильной группе аминокислоты способны вступать в реакции с металлами, основными оксидами, основаниями и солями более слабых кислот.

Аминокислоты способны вступать в реакцию этерификации, образуя сложные эфиры.

В молекуле белка аминокислоты связаны друг с другом пептидной связью. Она образуется между карбоксильной группой одной аминокислоты и
аминогруппой другой аминокислоты.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
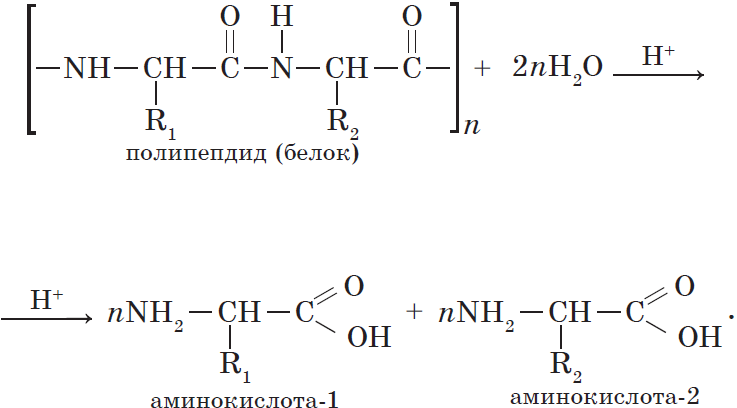
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Структуры белков
Химические свойства белков
Качественные реакции на белки
- Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
Видеоопыт взаимодействия белка с гидроксидом меди (II) можно посмотреть здесь.
- Ксантопротеиновая реакция – желтое окрашивание при действии на белки концентрированной азотной кислоты.
Видеоопыт взаимодействия белка с концентрированной азотной кислотой можно посмотреть здесь.
Денатурация белка
Это разрушение структуры белка при нагревании, изменении кислотности среды, действии излучения, спирта, тяжелых металлов, радиации.
Пример денатурации — свертывание яичных белков при варке яиц.
Видеоопыт денатурации белка можно посмотреть здесь.
Денатурация бывает обратимой и необратимой.
- При обратимой денатурации первичная структура белка не разрушается.
- Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
- При необратимой денатурации происходит также гидролиз белка — необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот или более коротких пептидных фрагментов.
Анализируя продукты гидролиза, можно установить количественный состав белков.
3.8.2. Белки
Белки — высокомолекулярные органические соединения, состоящие из остатков аминокислот, соединённых в длинную цепочку пептидной связью.
В состав белков живых организмов входит всего 20 типов аминокислот, все из которых относятся к альфа-аминокислотами, а аминокислотный состав белков и их порядок соединения друг с другом определяются индивидуальным генетическим кодом живого организма.
Одной из особенностей белков является их способность самопроизвольно формировать пространственные структуры характерные только для данного конкретного белка.
| первичная | последовательность соединения остатков аминокислот | |
| вторичная |
локальное упорядочивание фрагмента полипептидной цепи в спирали |
|
| третичная |
пространственная ориентация полипептидной спирали или способ ее укладки определенном объеме в глобулы (клубки) или фибриллы (нити) |
Из-за специфики своего строения белки могут обладать разнообразными свойствами. Например, белки, имеющие глобулярную четвертичную структуру, в частности белок куриного яйца, растворяются в воде с образованием коллоидных растворов. Белки, обладающие фибриллярной четвертичной структурой в воде не растворяются. Фибриллярными белками, в частности, образованы ногти, волосы, хрящи.
Химические свойства белков
Гидролиз
Все белки способны вступать в реакцию гидролиза. В случае полного гидролиза белков образуется смесь из α-аминокислот:
Белок + nH2O => смесь из α-аминокислот
Денатурация
Разрушение вторичной, третичной и четвертичной структур белка без разрушения его первичной структуры называют денатурацией. Денатурация белка может протекать под действием растворов солей натрия, калия или аммония – такая денатурация является обратимой:
Денатурация же протекающая под действием излучения (например, нагрева) или обработке белка солями тяжелых металлов является необратимой:
Так, например, необратимая денатурация белка наблюдается при термической обработке яиц в процессе их приготовления. В результате денатурации яичного белка его способность растворяться в воде с образованием коллоидного раствора исчезает.
Качественные реакции на белки
Биуретовая реакция
Если к раствору, содержащему белок добавить 10%-й раствор гидроксида натрия, а затем небольшое количество 1 %-го раствора сульфата меди, то появится фиолетовое окрашивание.
раствор белка + NаОН(10%-ный р-р) + СuSO4 = фиолетовое окрашивание
Ксантопротеиновая реакция
растворы белка при кипячении с концентрированной азотной кислотой окрашиваются в желтый цвет:
раствор белка + HNO3(конц.) => желтое окрашивание
Биологические функции белков
| каталитическая | ускоряют различные химические реакции в живых организмах | ферменты |
| структурная | строительный материал клеток | коллаген, белки клеточных мембран |
| защитная | защищают организм от инфекций | иммуноглобулины, интерферон |
| регуляторная | регулируют обменные процессы | гормоны |
| транспортная | перенос жизненно-необходимых веществ от одних частей организма к другим | гемоглобин переносит кислород |
| энергетическая | снабжают организм энергией | 1 грамм белка может обеспечить организм энергией в количестве 17,6 кДж |
| моторная (двигательная) | любые двигательные функции организма | миозин (мышечный белок) |
Приложение
Цветные реакции на белки
Цветные
реакции применяются для установления белковой природы веществ, идентификации
белков и определение их аминокислотного состава в различных биологических
жидкостях. В клинической лабораторной практике эти методы используются для определения
количества белка в плазме крови, аминокислот в моче и крови, для выявления
наследственных и приобретенных патологий обмена у новорожденных.
Биуретовая
реакция на пептидную связь. В основе ее лежит
способность пептидных связей
(– CO–NH– ) образовывать с сульфатом
меди в щелочной среде окрашенные комплексные соединения, интенсивность окраски
которых зависит от длины полипептидной цепи. Раствор белка дает сине-фиолетовое
окрашивание.
Реактивы: 1) яичный белок, 1% р-р (белок куриного яйца
фильтруют через марлю и разводят дист-ой водой 1:10); 2) NaOH,
10% р-р; 3) Cu(OH)2, 1% р-р.
Ход определения. В пробирку вносят 5 капель
р-ра яичного белка, 3 капли NaOH, 1 каплю Cu(OH)2, перемешивают. Содержимое пробирки приобретает
сине-фиолетовое окрашивание.
Нингидриновая реакция.Сущность реакции состоит
в образовании соединения, окрашенного в сине-фиолетовый цвет, состоящего из
нингидрина и продуктов гидролиза аминокислот. Эта реакция характерна для
аминогрупп в a-положении, присутствующих в природных
аминокислотах и белках.
Реактивы: 1) яичный белок, 1% р-р; 2) нингидрин, 0,5%
водный р-р.
Ход определения. В пробирку вносят 5 капель
р-ра яичного белка, затем 5 капель нингидрина, нагревают смесь до кипения. Появляется
розово-фиолетовое окрашивание, переходящее с течением времени в
сине-фиолетовое.
Ксантопротеиновая
реакция.При добавлении к р-ру белка конц-ой азотной к-ты и нагревании
появляется желтое окрашивание, переходящее в присутствии щелочи в оранжевое.
Сущность реакции состоит в нитровании бензольного
кольца циклических аминокислот азотной к-ой с образованием нитросоединений,
выпадающих в осадок.
Реакция выявляет наличие в белке циклических
аминокислот.
Реактивы: 1) яичный белок, 1% р-р; 2) конц. азотная
к-та; 3)NaOH,10% р-р.
Ход определения. К 5 каплям р-ра яичного белка
добавляют 3 капли азотной к-ты и (осторожно!) нагревают. Появляется осадок
желтого цвета. После охлаждения добавляют (желательно на осадок) 10 капель NaOH, появляется оранжевое окрашивание.
Реакция
Адамкевича. Аминокислота триптофан
в кислой среде, взаимодействуя с альдегидами кислот, образует
продукты конденсации красно-фиолетового цвета.
Реактивы: 1) неразбавленные яичный белок; 2)
конц. (ледяная) уксусная к-та; 3) конц. серная к-та.
Ход определения. К
одной капле белка прибавляют 10 капель уксусной к-ты. Наклонив пробирку,
осторожно по стенке добавляют по каплям 0,5 мл серной к-ты так, чтобы жидкости
не смешивались. При стоянии пробирки на границе жидкостей появляется
красно-фиолетовое кольцо.
Реакция Фоля.Аминокислоты, содержащие
сульфгидрильные группы – SH, подвергаются щелочному
гидролизу с образованием сульфида натрия Na2S. Последний, взаимодействуя с плюмбитом натрия ( образуется в ходе
реакции между ацетатом свинца и NaOH), образует осадок
сульфида свинца PbS черного или бурого цвета.
Na2S
+ Na2PbO2 + 2H2O ® PbS¯ + 4NaOH.
Реактивы: 1) яичный белок, 1% р-р; 2) реактив Фоля ( к
5% -р-ру ацетата свинца прибавляют равный объем 30% р-ра NaOH до
растворения образовавшегося осадка).
Ход
определения. К 5 каплям р-ра белка прибавляют 5 капель
реактива Фоля и кипятят 2-3 мин. После отстаивания 1-2 мин появляется черный
или бурый осадок.
Аминокислоты — гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу $—NH_2$ и карбоксильную группу $—СООН$, связанные с углеводородным радикалом.
Общую формулу простейших аминокислот можно записать так:
Так как аминокислоты содержат две различные функциональные группы, которые оказывают влияние друг на друга, характерные реакции отличаются от характерных реакций карбоновых кислот и аминов.
Свойства аминокислот
Аминогруппа $—NH_2$ определяет основные свойства аминокислот, т.к. способна присоединять к себе катион водорода по донорно-акцепторному механизму за счет наличия свободной электронной пары у атома азота.
Группа $—СООН$ (карбоксильная группа) определяет кислотные свойства этих соединений. Следовательно, аминокислоты — это амфотерные органические соединения.
Со щелочами они реагируют как кислоты:
С сильными кислотами — как основания-амины:
Кроме того, аминогруппа в аминокислоте вступает во взаимодействие с входящей в ее состав карбоксильной группой, образуя внутреннюю соль:
Так как аминокислоты в водных растворах ведут себя как типичные амфотерные соединения, то в живых организмах они играют роль буферных веществ, поддерживающих определенную концентрацию ионов водорода.
Аминокислоты представляют собой бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше $200°С$. Они растворимы в воде и нерастворимы в эфире. В зависимости от радикала $R—$ они могут быть сладкими, горькими или безвкусными.
Аминокислоты подразделяют на природные (обнаруженные в живых организмах) и синтетические. Среди природных аминокислот (около $150$) выделяют протеиногенные аминокислоты (около $20$), которые входят в состав белков. Они представляют собой L-формы. Примерно половина из этих аминокислот относятся к незаменимым, т.к. они не синтезируются в организме человека. Незаменимыми являются такие кислоты, как валин, лейцин, изолейцин, фенилаланин, лизин, треонин, цистеин, метионин, гистидин, триптофан. В организм человека данные вещества поступают с пищей. Если их количество в пище будет недостаточным, нормальное развитие и функционирование организма человека нарушаются. При отдельных заболеваниях организм не в состоянии синтезировать и некоторые другие аминокислоты. Так, при фенилкетонурии не синтезируется тирозин.
Важнейшим свойством аминокислот является способность вступать в молекулярную конденсацию с выделением воды и образованием амидной группировки $—NH—CO—$, например:
${nNH_2—(CH_2)_5—COOH}↙{text»аминокапроновая кислота»}→{(…—NH—(CH_2)_5—COO—…)_n}↙{text»капрон»}+(n+1)H_2O$.
Получаемые в результате такой реакции высокомолекулярные соединения содержат большое число амидных фрагментов и поэтому получили название полиамидов.
Для получения синтетических волокон пригодны аминокислоты с расположением аминои карбоксильной групп на концах молекул.
Полиамиды $α$-аминокислот называются пептидами. В зависимости от числа остатков аминокислот различают дипептиды, пептиды, полипептиды. В таких соединениях группы $—NH—CO—$ называют пептидными.
Некоторые аминокислоты, входящие в состав белков.
| Название аминокислоты | Формула |
| Глицин (аминоуксусная) | $NH_2-CH_2-COOH$ |
| Аланин ($α$-аминопропионовая) | 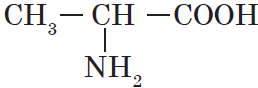 |
| Цистеин ($α$-амино-$β$меркаптопропионовая) | 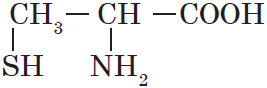 |
| Лизин ($α$, $ε$-диаминокапроновая) | 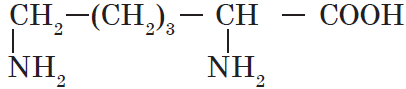 |
| Фенилаланин ($α$-амино-$β$фенилпропионовая) | 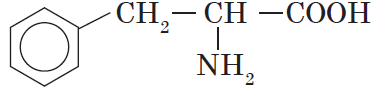 |
Белки
Белками, или белковыми веществами, называют высокомолекулярные (молекулярная масса варьируется от $5–10$ тыс. до $1$ млн и более) природные полимеры, молекулы которых построены из остатков аминокислот, соединенных амидной (пептидной) связью.
Белки также называют протеинами (от греч. protos — первый, важный). Число остатков аминокислот в молекуле белка очень сильно колеблется и иногда достигает нескольких тысяч. Каждый белок обладает своей, присущей ему, по следовательностью расположения аминокислотных остатков.
Белки выполняют разнообразные биологические функции: каталитические (ферменты), регуляторные (гормоны), структурные (коллаген, фиброин), двигательные (миозин), транспортные (гемоглобин, миоглобин), защитные (иммуноглобулины, интерферон), запасные (казеин, альбумин, глиадин) и другие.
Белки — основа биомембран, важнейшей составной части клетки и клеточных компонентов. Они играют ключевую роль в жизни клетки, составляя как бы материальную основу ее химической деятельности.
Исключительное свойство белка — самоорганизация структуры, т.е. его способность самопроизвольно создавать определенную, свойственную только данному белку пространственную структуру. По существу, вся деятельность организма (развитие, движение, выполнение им различных функций и многое другое) связана с белковыми веществами. Без белков невозможно представить себе жизнь.
Белки — важнейшая составная часть пищи человека и животных, поставщик необходимых аминокислот.
Строение белков
Все белки образованы двадцатью разными $α$-аминокислотами, общую формулу которых можно представить в виде
$R-CHNH_2-COOH$
где радикал R может иметь самое разнообразное строение.
Белки представляют собой полимерные цепи, состоящие из десятков тысяч, миллионов и более остатков $α$-аминокислот, связанных между собой пептидными связями. Последовательность аминокислотных остатков в молекуле белка называют его первичной структурой.
Для белковых тел характерны огромные молекулярные массы (до миллиарда) и почти макроразмеры молекул. Такая длинная молекула не может быть строго линейной, поэтому ее участки изгибаются и сворачиваются, что приводит к образованию водородных связей с участием атомов азота и кислорода. Образуется регулярная спиралевидная структура, которую называют вторичной структурой.
В белковой молекуле могут возникать ионные взаимодействия между карбоксильными и аминогруппами различных аминокислотных остатков и образование дисульфидных мостиков. Эти взаимодействия приводят к появлению третичной структуры.
Белки с $M_r > 50000$ состоят, как правило, из нескольких полипептидных цепей, каждая из которых уже имеет первичную, вторичную и третичную структуры. Говорят, что такие белки обладают четвертичной структурой.
Свойства белков
Белки — амфотерные электролиты. При определенном значении $рН$ среды (оно называется изоэлектрической точкой) число положительных и отрицательных зарядов в молекуле белка одинаково.
Это одно из основных свойств белка. Белки в этой точке электронейтральны, а их растворимость в воде наименьшая. Способность белков снижать растворимость при достижении электронейтральности их молекул используется для выделения из растворов, например, в технологии получения белковых продуктов.
Гидратация. Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объем увеличиваются. Набухание отдельных белков зависит от их строения. Имеющиеся в составе и расположенные на поверхности белковой макромолекулы гидрофильные амидные ($—СО—NH—$, пептидная связь), аминные ($—NH_2$) и карбоксильные ($—СООН$) группы притягивают к себе молекулы воды, строго ориентируя их на поверхности молекулы. Окружающая белковые глобулы гидратная (водная) оболочка препятствует агрегации и осаждению, а следовательно, способствует устойчивости растворов белка. В изоэлектрической точке белки обладают наименьшей способностью связывать воду, происходит разрушение гидратной оболочки вокруг белковых молекул, поэтому они соединяются, образуя крупные агрегаты. Агрегация белковых молекул происходит и при их обезвоживании с помощью некоторых органических растворителей, например этилового спирта. Это приводит к выпадению белков в осадок. При изменении $рН$ среды макромолекула белка становится заряженной, и его гидратационная способность меняется.
При ограниченном набухании концентрированные белковые растворы образуют сложные системы, называемые студнями. Студни не текучи, упруги, обладают пластичностью, определенной механической прочностью, способны сохранять свою форму.
Различная гидрофильность клейковинных белков — один из признаков, характеризующих качество зерна пшеницы и получаемой из него муки (так называемые сильные и слабые пшеницы). Гидрофильность белков зерна и муки играет важную роль при хранении и переработке зерна, в хлебопечении. Тесто, которое получают в хлебопекарном производстве, представляет собой набухший в воде белок, концентрированный студень, содержащий зерна крахмала.
Денатурация белков. При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и ряда других факторов) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т.е. ее нативной пространственной структуры. Первичная структура, а следовательно, и химический состав белка не меняются. Изменяются физические свойства: снижается растворимость, способность к гидратации, теряется биологическая активность. Меняется форма белковой макромолекулы, происходит агрегирование. В то же время увеличивается активность некоторых химических групп, облегчается воздействие на белки протеолитических ферментов, а следовательно, он легче гидролизуется.
В пищевой технологии особое практическое значение имеет тепловая денатурация белков, степень которой зависит от температуры, продолжительности нагрева и влажности. Это необходимо помнить при разработке режимов термообработки пищевого сырья, полуфабрикатов, а иногда и готовых продуктов. Особую роль процессы тепловой денатурации играют при бланшировании растительного сырья, сушке зерна, выпечке хлеба, получении макаронных изделий. Денатурация белков может вызываться и механическим воздействием (давлением, растиранием, встряхиванием, ультразвуком). Наконец, к денатурации белков приводит действие химических реагентов (кислот, щелочей, спирта, ацетона). Все эти приемы широко используются в пищевой и биотехнологии.
Пенообразование. Под процессом пенообразования понимают способность белков образовывать высококонцентрированные системы «жидкость — газ», называемые пенами. Устойчивость пены, в которой белок является пенообразователем, зависит не только от его природы и от концентрации, но и от температуры. Белки в качестве пенообразователей широко используются в кондитерской промышленности (пастила, зефир, суфле). Структуру пены имеет хлеб, а это влияет на его вкусовые качества.
Молекулы белков под влиянием ряда факторов могут разрушаться или вступать во взаимодействие с другими веществами с образованием новых продуктов. Для пищевой промышленности можно выделить два важных процесса: 1) гидролиз белков под действием ферментов; 2) взаимодействие аминогрупп белков или аминокислот с карбонильными группами восстанавливающих сахаров. Под влиянием протеаз-ферментов, катализирующих гидролитическое расщепление белков, последние распадаются на более простые продукты (поли- и дипептиды) и в итоге на аминокислоты. Скорость гидролиза белка зависит от его состава, молекулярной структуры, активности фермента и условий.
Гидролиз белков. Реакцию гидролиза с образованием аминокислот в общем виде можно записать так:
Горение. Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев.
Цветные реакции. Используют следующие реакции:
— ксантопротеиновую, при которой происходит взаимодействие ароматических и гетероатомных циклов в молекуле белка с концентрированной азотной кислотой, сопровождающееся появлением желтой окраски;
— биуретовую, при которой происходит взаимодействие слабощелочных растворов белков с раствором сульфата меди (II) с образованием комплексных соединений между ионами $Cu^{2+}$ и полипептидами. Реакция сопровождается появлением фиолетово-синей окраски.
Качественные реакции на белки
Качественные
реакции на аминокислоты, пептиды и белки
можно разделить на две группы:
1)
цветные реакции, обусловленные
аминокислотами и пептидами;
2)
реакции осаждения, в основе которых
лежат изменения физико-хнмических
свойств белковых молекул.
Цветные
реакции. Для
качественного определения белков
применяют следующие характерные реакции:
1.
Биуретовая
реакция на
белки (реакция Пиотровского на пептидную
связь). В разные пробирки наливают по
1-2 см3
раствора
белка с равным объемом 4 %-ного раствора
щелочи и постепенно, по стенке пробирки
добавляют
1-2 капли
0,5 %-ного
раствора медного купороса. Жидкость
окрашивается в фиолетово-синий или
фиолетово-красный цвет (биуретовая
реакция) благодаря присутствию в
молекуле белка пептидной связи (—СО—NH—).
Реакцию дают все белки, а также продукты
их гидролиза − пептоны и полипептиды,
начиная с тетрапептидов.
2.
Ксантопротеиновая
реакция (Мульдера). Эта
реакция на белки обусловлена образованием
нитропроизводных ароматических и
некоторых гетероциклических радикалов.
При взаимодействии
белка с азотной кислотой происходит
нитрование ядра содержащихся в белке
ароматических аминокислот с образованием
окрашенных соединений. Таким образом,
с помощью ксантопротеиновой реакции в
составе белка можно обнаружить такие
циклические аминокислоты, как фенилаланин,
тирозин, триптофан н др.
Реакция протекает
по схеме:
.
−
NH
– CH
– CO
− … … – NH
– CH
– CO
− … … – NH
– CH
– CO
− …
CH2
CH2
CH2
HNO3
NaOH
NO2
N – O Na+
OH
OH
O
O
тирозин
желтый цвет
оранжевый цвет
Реактивы:
1) растворы
белков;
2)
раствор желатина;
3)
HNO3,
концентрированная;
4)
20%-ный раствор NаОН.
Ход
определения.
Реакцию следует проводить под тягой. В
пробирки наливают по
1 мл растворов
белков и желатина и в каждою добавляют
по
5 капель
азотной кислоты. В пробирках выпадает
осадок. Содержимое пробирок осторожно
нагревают при постоянном перемешивании.
Если осадок содержит аминокислоты с
ароматическим или гетероциклическим
радикалом, при нагревании раствор и
осадок окрашиваются в желтый цвет.
Охладив смесь, осторожно, по каплям,
добавляют избыток гидроксида аммония.
При этом желтая окраска раствора
переходит в оранжевую. При обработке
белков корепкой азотной кислотой
появляется желтое окрашивание
(нитрование), которое после добавления
основания переходит в оранжевое. Реакция
указывает на присутствие фенилаланина,
тирозина либо триптофана.
3.
Реакция
обнаружения серы в белке (Фоле)
Белок, содержащий
в своем составе серу, при нагревании с
раствором щелочи гидролизуется, сера
отщепляется а виде сероводорода, который
тут же превращается в сульфид натрия.
Таким образом, для обнаружения серы в
белках требуется разрушение белковой
молекулы. Отщепляющуюся серу можно
определить с помощью ацетата свинца,
который реагирует с сульфидом натрия,
образуя черный осадок сульфида свинца.
HS−CH2
–
CH(NH2)
– COOH + NaOH → −
CH2
– CH (NH2)
– COOH +H2S
H2S
+ NaOH → Na2S
+ H2O
(СН3СОО)2РЬ
+
Na2S
→ 2
CH3COONa
+
PbS↓
Если количество
серы в белке незначительно, вместо
осадка образуется раствор коричневого
цвета.
Реакция обусловлена
присутствием в белке серосодержащих
аминокислот: цистина, цистеина и
метионина.
Реактивы:
1)
растворы белков;
2)
10%-ный раствор NaOH;
3)
10%-ный раствор (CH3COO)2Pb.
Ход
определения.
В пробирки наливают по
1 мл растворов
белков. В каждую пробирку добавляют
двойной объем 10%-ного раствора гидроксида
натрия. Содержимое пробирок перемешивают
и осторожно кипятят в течение
1-2 минут.
Затем в каждую пробирку приливают но
1 мл раствора
ацетата свинца и снова нагревают.
Наблюдают за изменением окраски раствора
в пробирках.
4.
Реакция на
триптофан (Адамкевнча).
Триптофан, реагируя в кислой среде с
альдегидами, образует окрашенные
продукты конденсации. Так, с глиоксиловой
кислотой (являющейся примесью в
концентрированной уксусной кислоте)
реакция протекает но уравнению:
о
II
С
–С =О
Н
ОН
По аналогичной
схеме протекает реакция триптофана с
оксиметилфурфуролом или формальдегидом.
Реактивы:
1)
растворы белков;
2)
1%-иый раствор желатина;
3)
СН3СООН,
концентрированная;
4)
H2SO4,
концентрированная.
Ход
определения.
В пробирку наливают несколько капель
неразбавленного яичного белка, прибавляют
1-2 мл
уксусной кислоты и осторожно нагревают
до растворения выпавшего осадка, после
чего охлаждают и осторожно но стенке
пробирки, наклонив ее, наливают
1 мл серной
кислоты, которую используют в качестве
водоотнимающего средства. На границе
двух несмешивающихся слоев жидкостей
через некоторое время появляется
красно-фиолетовое кольцо.
Эту же реакцию
повторяют с раствором желатина.
Окрашивание не происходит, т.к. триптофан
не входит в состав желатина.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Аминокислоты. Белки
Ключевые слова конспекта: Аминокислоты. Глицин. Пептидная связь. Белки. Качественные реакции на белки. Денатурация белка. ДНК. Ген.
Строение аминокислот
Если проанализировать термин «аминокислоты», то можно прийти к выводу, что так должны называться соединения, содержащие в молекулах две функциональные группы: карбоксильную группу —СООН, определяющую кислотные свойства, и основную аминогруппу —NH2. Вывести общую формулу аминокислот нетрудно:
Органические вещества, содержащие в молекуле карбоксильную группу —СООН и аминогруппу —NH2, называют аминокислотами.
Аминокислоты представляют собой твёрдые кристаллические вещества, многие из них хорошо растворимы в воде, некоторые имеют сладкий вкус.
(с) Цитата из справочного издания «ХИМИЯ. Справочник в таблицах / М.: Издательство АЙРИС-пресс»
Способы получения и химические свойства аминокислот
В промышленности аминокислоты получают биотехнологическим путём как продукты жизнедеятельности микроорганизмов. Кроме того, разработано несколько лабораторных способов получения аминокислот. Один из них может быть представлен следующей схемой:
Простейшую аминокислоту называют аминоуксусной кислотой или глицином, её формула H2N—СН2—СООН.
Какие же свойства проявляют аминокислоты — кислотные или основные? Оказывается, подобно амфотерным неорганическим соединениям, в зависимости от природы реагента аминокислоты могут проявлять свойства как кислоты, так и основания. Например, глицин реагирует со щелочами с образованием солей, проявляя свойства кислоты:
В реакциях с кислотами глицин проявляет свойства органических оснований — аминов:
Понятие о пептидах и белках
Важное химическое свойство аминокислот — способность взаимодействовать друг с другом с отщеплением молекулы воды, образуя пептиды:
Между двумя остатками аминокислот образуется пептидная связь:
Связь, возникающую между карбоксильной группой —СООН одной молекулы аминокислоты и аминогруппой —NH2 другой молекулы аминокислоты, называют пептидной связью.
Получившийся в результате реакции дипептид может вступать в реакции с другими молекулами аминокислот, образуя полимеры — белки. Поскольку в результате этой реакции, помимо высокомолекулярного вещества, образуется второй продукт — вода, такой процесс относят к реакциям поликонденсации.
О важности белков для живых организмов свидетельствует тот факт, что в большинстве иностранных языков соединения такого типа называют протеинами (от греч. protos — первый). На Земле не существует ни одного живого организма, включая простейшие одноклеточные и бактерии, который не состоял бы из белковых молекул.
Белки — это природные полимеры, образованные остатками аминокислот, связанными между собой пептидными связями.
Структура и функции белков
В состав природных белков входит около 20 аминокислот, а разновидностей белков великое множество. Каким же образом эти 20 аминокислот создают такое многообразие белков? Дело в том, что аминокислотные остатки в белковой молекуле повторяются, а их последовательность, называемая первичной структурой белка, уникальна. Подобным образом из 33 букв русского алфавита состоят десятки тысяч различных слов, различающихся порядком чередования букв («первичная структура» слова) и, как следствие, значением.
Молекулы белков имеют также вторичную и третичную структуру. Характеристика этих структур белковых молекул приведена в таблице.
В зависимости от того, какую функцию выполняет белок в организме, различно его отношение к воде. Большинство белков в воде не растворяется, например кератины, которые составляют основу волос, ногтей, перьев, рогов и т. д. Для некоторых белков выполнение их функций невозможно без растворения. Так, в воде растворяются многие белки, выполняющие функции природных катализаторов, — ферменты.
Химические свойства белков
Для обнаружения белка проводят качественные реакции на белки. Белки дают фиолетовое окрашивание в щелочной среде под действием свежеприготовленного осадка гидроксида меди(II). Эту пробу называют биуретовой реакцией.
Вторую качественную реакцию на белки называют ксантопротеиновой. При действии на раствор белка концентрированной азотной кислоты образуется белый осадок, который быстро приобретает жёлтую окраску, а при добавлении водного раствора аммиака становится оранжевым.
Для обнаружения в белках соединений серы используют следующий тест. При горении серосодержащих белков появляется характерный запах жжёного рога.
Одно из важнейших химических свойств белков — реакции гидролиза. В присутствии природных катализаторов (ферментов) или сильных кислот молекулы воды расщепляют полимерную белковую молекулу до аминокислот:
Именно такой процесс протекает при переваривании белковой пищи. Образующиеся аминокислоты попадают в кровь, затем транспортируются в каждую клетку организма, где из них синтезируются белковые молекулы, характерные именно для этого вида живых организмов. Теперь вы понимаете, почему белки, наряду с жирами и углеводами, — основной компонент пищи. Недостаток белка в питании человека может вызвать тяжёлые заболевания. При несбалансированном питании у людей отмечается плохое самочувствие, быстрая утомляемость, снижение иммунитета. Многие юноши и девушки вашего возраста изнуряют себя разными диетами с целью похудеть, а то и вовсе отказываются от еды. Такая «коррекция фигуры» может привести к непоправимым проблемам со здоровьем.
При относительно небольшом нагревании или действии химических реагентов нарушается структура белка, т. е. происходит его денатурация (от лат. denaturatus; de- — приставка, означающая «отделение, удаление», +nature — природа). Для живых организмов денатурация белка — это гибель. Однако в пищевой промышленности тепловая денатурация белков — один из обычных технологических процессов. Варка и обжаривание продуктов, выпечка хлеба, производство макаронных изделий, приготовление творога — все эти операции связаны с денатурацией белков.
Белки играют ключевую роль почти во всех структурах живых организмов и происходящих в них процессах.
В каждой клетке организма синтезируется множество белков. Информация о структуре всех белков организма зашифрована в ещё одних природных биополимерах — молекулах дезоксирибонуклеиновых кислот (ДНК). Мономеры ДНК — нуклеотиды. Молекулы ДНК человека содержат примерно 3,1 млрд пар нуклеотидов. Участок молекулы ДНК, отвечающий за синтез одного белка, называют геном.
Справочная таблица «Аминокислоты»
Конспект урока по химии «Аминокислоты. Белки». В учебных целях использованы цитаты из пособия «Химия. 10 класс : учеб, для общеобразоват. организаций : базовый уровень / О. С. Габриелян, И. Г. Остроумов, С. А. Сладков. — М. : Просвещение». Выберите дальнейшее действие:
- Вернуться к Списку конспектов по химии
- Найти конспект в Кодификаторе ОГЭ по химии
- Найти конспект в Кодификаторе ЕГЭ по химии