Белки (син. протеины) — высокомолекулярные органические вещества, построенные из остатков аминокислот. По
своему биологическому значению принадлежат к числу важнейших составных частей организма.
Несомненно, белки абсолютно необходимы для жизни растений, животных и грибов. Именно вследствие такого
большого значения белки получили названия протеинов (греч. protos — первый, главный).

Качественной реакцией на белки служит ксантопротеиновая реакция. Ее проводят путем добавления к раствору белка HNO3(конц.) до
тех пор, пока не прекратится выпадение осадка. Осадок окрашивается в характерный желтый цвет.

Аминокислота
Аминокислота — органическая кислота, содержащая, по меньшей мере, одну карбоксильную группу (COOH) и одну аминогруппу (NH2).
Аминокислоты являются основной составляющей всех белков.
В построении белков участвуют 20 наиболее распространенных аминокислот. На данном этапе учить их наизусть не обязательно, эта
задача настигнет вас на кафедре биохимии 
И все же для успешного изучения данной темы мы возьмем за основу две аминокислоты: глицин и аланин.

Я хочу вас обрадовать (надеюсь, что обрадую)). Если вы успешно изучили темы: карбоновые кислоты, амины — то вы уже знаете химические
свойства аминокислот!
Они напоминают амфотерные соединения: по аминогруппе вступают в реакции с кислотами, по карбоксильной — с основаниями. Мы разберем их подробнее чуть
ниже.
Получение аминокислот
Аминокислоты можно получить в реакции аммиака с галогенкарбоновыми кислотами.

Химические свойства аминокислот
- Основные свойства
- Кислотные свойства
- Пептидные связи
За счет наличия аминогруппы, аминокислоты проявляют основные свойства. Реагируют с кислотами.

По карбоксильной группе аминокислоты способны вступать в реакции с металлами, основными оксидами, основаниями и солями более слабых кислот.

Аминокислоты способны вступать в реакцию этерификации, образуя сложные эфиры.

В молекуле белка аминокислоты связаны друг с другом пептидной связью. Она образуется между карбоксильной группой одной аминокислоты и
аминогруппой другой аминокислоты.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Тематический тест на белки, жиры и углеводы.
Задание №1
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных жиров. Число верных ответов может быть любым.
1) этиленгликоль
2) серная кислота
3) глицерин
4) ацетон
5) стеариновая кислота
Решение
Ответ: 35
Задание №2
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных углеводов. Число верных ответов может быть любым.
1) глюкоза
2) аланин
3) фосфорная кислота
4) фруктоза
5) сорбит
Решение
Ответ: 14
Задание №3
Из предложенного списка соединений выберите те, которые можно обнаружить среди продуктов гидролиза природных белков. Число верных ответов может быть любым.
1) глицерин
2) анилин
3) олеиновая кислота
4) аланин
5) кофеин
Решение
Ответ: 4
Задание №4
Из предложенного списка соединений выберите те, которые нельзя обнаружить среди продуктов гидролиза природных жиров. Число верных ответов может быть любым.
1) олеиновая кислота
2) линолевая кислота
3) глицерин
4) бензойная кислота
5) пальмитиновая кислота
Решение
Ответ: 4
Задание №5
Из предложенного списка соединений выберите те, которые нельзя обнаружить среди продуктов гидролиза природных белков. Число верных ответов может быть любым.
1) глицин
2) глицерин
3) аланин
4) фенол
5) метиламин
Решение
Ответ: 245
Задание №6
Из предложенного списка функциональных групп выберите те, которые встречаются в моносахаридах. Число верных ответов может быть любым.
1) карбоксильная
2) карбонильная
3) гидроксильная
4) нитрогруппа
5) аминогруппа
Решение
Ответ: 23
Задание №7
Из предложенного списка функциональных групп выберите те, которые не встречаются в моносахаридах. Число верных ответов может быть любым.
1) гидроксильная
2) амидная
3) карбоксильная
4) аминогруппа
5) сложноэфирная
Решение
Ответ: 2345
Задание №8
Из предложенного списка функциональных групп выберите те, которые встречаются в природных аминокислотах. Число верных ответов может быть любым.
1) карбонильная
2) нитрогруппа
3) аминогруппа
4) карбоксильная
5) сложноэфирная
Решение
Ответ: 34
Задание №9
Из предложенного списка типов реакций выберите те, которые характерны для белков. Число верных ответов может быть любым.
1) кислотный гидролиз
2) денатурация
3) присоединение
4) щелочной гидролиз
5) полимеризация
Решение
Ответ: 124
Задание №10
Из предложенного списка типов реакций выберите те, которые характерны для моносахаридов и дисахаридов. Число верных ответов может быть любым.
1) этерификация
2) окисление
3) полимеризация
4) гидролиз
5) нитрование
Решение
Ответ: 12
[adsp-pro-3]
Задание №11
Из предложенного списка типов реакций выберите те, которые характерны для белков и дисахаридов. Число верных ответов может быть любым.
1) горение
2) кислотный гидролиз
3) спиртовое брожение
4) нитрование
5) гидратация
Решение
Ответ: 12
Задание №12
Из предложенного списка типов реакций выберите те, которые характерны для предельных жиров. Число верных ответов может быть любым.
1) гидрирование
2) горение
3) гидратация
4) обесцвечивание бромной воды
5) гидрогалогенирование
Решение
Ответ: 2
Задание №13
Из предложенного списка типов реакций выберите те, которые характерны для жидких жиров. Число верных ответов может быть любым.
1) полимеризация
2) обесцвечивание бромной воды
3) этерификация
4) омыление
5) брожение
Решение
Ответ: 124
Задание №14
Из предложенного списка типов реакций выберите те, которые характерны для твердых и жидких жиров. Число верных ответов может быть любым.
1) омыление
2) полимеризация
3) гидрирование
4) горение
5) нитрование
Решение
Ответ: 14
Задание №15
Из предложенного списка типов реакций выберите те, которые характерны для полисахаридов и твердых жиров. Число верных ответов может быть любым.
1) кислотный гидролиз
2) омыление
3) бромирование
4) реакция «серебряного зеркала»
5) горение
Решение
Ответ: 15
Задание №16
Из предложенного списка соединений выберите те, которые реагируют с глюкозой. Число верных ответов может быть любым.
1) аммиак
2) цинк
3) водород
4) гидроксид меди
5) вода
Решение
Ответ: 34
Задание №17
Из предложенного списка соединений выберите те, которые реагируют с сахарозой. Число верных ответов может быть любым.
1) кислород
2) водород
3) аммиачный раствор оксида серебра
4) никель
5) водный раствор серной кислоты
Решение
Ответ: 15
Задание №18
Из предложенного списка соединений выберите те, которые реагируют с рибозой. Число верных ответов может быть любым.
1) гидроксид натрия
2) гидроксид меди
3) водород
4) вода
5) мел
Решение
Ответ: 23
Задание №19
Из предложенного списка соединений выберите те, которые не реагируют с фруктозой. Число верных ответов может быть любым.
1) кислород
2) водород
3) гидроксид меди
4) аммиачный раствор оксид серебра
5) вода
Решение
Ответ: 45
Задание №20
Из предложенного списка соединений выберите те, которые реагируют с твердыми жирами. Число верных ответов может быть любым.
1) едкий натр
2) кремнезем
3) сероводород
4) гашеная известь
5) пирит
Решение
Ответ: 14
[adsp-pro-3]
Задание №21
Из предложенного списка соединений выберите те, которые реагируют с непредельными жирами. Число верных ответов может быть любым.
1) бромная вода
2) едкое кали
3) графит
4) водород
5) азот
Решение
Ответ: 124
Задание №22
Из предложенного списка соединений выберите те, которые не реагируют с дезоксирибозой. Число верных ответов может быть любым.
1) аргон
2) литий
3) кислород
4) аммиачный раствор оксида серебра
5) гидроксид меди
Решение
Ответ: 1
Задание №23
Из предложенного списка соединений выберите те, которые не реагируют с насыщенными жирами. Число верных ответов может быть любым.
1) бромная вода
2) гидроксид цезия
3) водород
4) гашеная известь
5) хлорид натрия
Решение
Ответ: 135
Задание №24
Из предложенного списка соединений выберите те, которые реагируют с белками. Число верных ответов может быть любым.
1) азотная кислота
2) кислород
3) водород
4) азот
5) железо
Решение
Ответ: 12
Задание №25
Из предложенного списка соединений выберите те, которые не реагируют с глюкозой. Число верных ответов может быть любым.
1) уксусный ангидрид
2) гидроксид меди
3) водород
4) перманганат калия
5) бромид калия
Решение
Ответ: 5
Задание №26
Из предложенного списка соединений выберите те, которые можно использовать для обнаружения глюкозы. Число верных ответов может быть любым.
- 1. [Ag(NH3)2]OH
- 2. NaCl
- 3. Zn
- 4. NaHCO3
- 5. Cu(OH)2
Решение
Ответ: 15
Задание №27
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный и непредельный жиры. Число верных ответов может быть любым.
1) аммиак
2) калий
3) оксид кальция
4) бром
5) йод
Решение
Ответ: 45
Задание №28
Из предложенного списка соединений выберите те, с помощью которых можно различить рибозу и фруктозу. Число верных ответов может быть любым.
- 1. Сu(OH)2
- 2. FeO
- 3. FeCl3
- 4. Na
- 5. [Ag(NH3)2]OH
Решение
Ответ: 15
Задание №29
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и природный белок. Число верных ответов может быть любым.
1) бромная вода
2) азотная кислота
3) водород
4) кислород
5) серная кислота
Решение
Ответ: 2
Задание №30
Из предложенного списка соединений выберите те, с помощью которых можно различить непредельный жир и сахарозу. Число верных ответов может быть любым.
1) раствор брома
2) серная кислота
3) гидроксид меди
4) азот
5) оксид цинка
Решение
Ответ: 13
[adsp-pro-3]
Задание №31
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и глюкозу. Число верных ответов может быть любым.
- 1. [Ag(NH3)2]OH
- 2. I2
- 3. Zn
- 4. K2CO3
- 5. KMnO4
Решение
Ответ: 15
Задание №32
Из предложенного списка реагентов выберите два таких, с помощью которых можно различить природный белок и крахмал.
1) соляная кислота
2) раствор серной кислоты
3) азотная кислота
4) фосфор
5) йод
Решение
Ответ: 35
Задание №33
Из предложенного списка соединений выберите те, с помощью которых можно различить рибозу и глицин. Число верных ответов может быть любым.
1) аммиачный раствор оксида серебра
2) сода
3) ацетон
4) бензол
5) кислород
Решение
Ответ: 12
Задание №34
Из предложенного списка соединений выберите те, с помощью которых можно различить непредельный жир и целлюлозу. Число верных ответов может быть любым.
1) бромная вода
2) аммиак
3) алюминий
4) гидроксид натрия
5) вода
Решение
Ответ: 1
Задание №35
Из предложенного списка соединений выберите те, с помощью которых можно различить предельный жир и уксусную кислоту. Число верных ответов может быть любым.
1) серная кислота
2) азотная кислота
3) сода
4) водород
5) йод
Решение
Ответ: 3
Задание №36
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) глюкоза Б) сахароза В) растительное масло |
1) сорбит 2) глицин 3) фруктоза 4) маргарин |
Решение
Ответ: 134
Задание №37
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) твердый жир Б) крахмал В) целлюлоза |
1) ацетатное волокно 2) глюкоза 3) этиленгликоль 4) глицерин |
Решение
Ответ: 421
Задание №38
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) растительный белок Б) сахароза В) подсолнечное масло |
1) глюкоза 2) азот 3) рибоза 4) твердый жир |
Решение
Ответ: 214
Задание №39
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) глюкоза Б) бараний жир В) животный белок |
1) фруктоза 2) глицин 3) стеариновая кислота 4) этанол |
Решение
Ответ: 432
Задание №40
Установите соответствие между природными соединениями и веществами, которые можно получить из них в одну стадию.
| ВЕЩЕСТВО | ПРОДУКТ |
|
А) растительное масло Б) твердый жир В) гликоген |
1) глюкоза 2) маргарин 3) сорбит 4) мыло |
Решение
Ответ: 241
[adsp-pro-3]
Задание №41
Из предложенного перечня выберите два вещества, которые взаимодействуют и с глюкозой, и с целлюлозой.
1) водород
2) сульфат меди (II)
3) гидроксид железа (III)
4) азотная кислота
5) кислород
Решение
Ответ: 45
Задание №42
Из предложенного перечня выберите два вещества, которые не подвергаются гидролизу.
1) крахмал
2) целлюлоза
3) глюкоза
4) сахароза
5) фруктоза
Решение
Ответ: 35
Задание №43
Из предложенного перечня выберите две реакции, в которые не вступает целлюлоза.
1) горение
2) гидролиз
3) нитрование
4) хлорирование
5) гидрирование
Решение
Ответ: 45
Задание №44
Из предложенного перечня выберите два вещества, с которыми не реагирует крахмал.
1) йод
2) гидроксид меди (II)
3) аммиак
4) вода в присутствии кислот
5) вода в присутствии ферментов
Решение
Ответ: 23
Задание №45
Из предложенного перечня выберите два вещества, которые взаимодействуют с белками.
- 1. Cl2 (H2O)
- 2. HNO3
- 3. Ag2O (р-р NH3)
- 4. Cu(OH)2
- 5. FeCl3
Решение
Ответ: 24
[adsp-pro-10]
Белки (полипептиды) – биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот:
Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Структуры белков
Химические свойства белков
Качественные реакции на белки
- Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
Видеоопыт взаимодействия белка с гидроксидом меди (II) можно посмотреть здесь.
- Ксантопротеиновая реакция – желтое окрашивание при действии на белки концентрированной азотной кислоты.
Видеоопыт взаимодействия белка с концентрированной азотной кислотой можно посмотреть здесь.
Денатурация белка
Это разрушение структуры белка при нагревании, изменении кислотности среды, действии излучения, спирта, тяжелых металлов, радиации.
Пример денатурации — свертывание яичных белков при варке яиц.
Видеоопыт денатурации белка можно посмотреть здесь.
Денатурация бывает обратимой и необратимой.
- При обратимой денатурации первичная структура белка не разрушается.
- Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
- При необратимой денатурации происходит также гидролиз белка — необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот или более коротких пептидных фрагментов.
Анализируя продукты гидролиза, можно установить количественный состав белков.
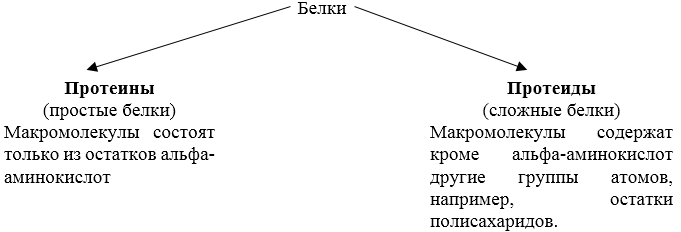
Белки — это природные высокомолекулярные соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков альфа-аминокислот.
Все белки являются полипептидами, но не всякий полипептид является белком.
Физические свойства белков:
Свойства белков также разнообразны, как и функции, которые они выполняют. Одни белки растворятся в воде, образуя, как правило, коллоидные растворы (например, белок яйца); другие растворяются в разбавленных растворах солей; третьи нерастворимы (например, белки покровных тканей).
Химические свойства белков — гидролиз белков:
Белки + H2O = полипептиды + H2O = олигопептиды + H2O = дипептиды + H2O = альфа-аминокислоты
(условия реакций везде: кислая среда и нагревание)
Жиры — это смесь сложных эфиров глицерина и высших карбоновых кислот (ВКК)ю
Общая формула жиров:
Физические свойства жиров:
Жиры — вязкие жидкости или твердые вещества, легче воды; в воде не растворяются, но растворяются в органических растворителях (бензине, бензоле и т.д.)
Химические свойства жиров:
1. Гидролиз: водный, кислотный, ферментативный, щелочной.
2. Гидрирование.
3. Присоединение галогенов.
Функции жиров в организме:
1. Энергетическая.
2. Структурная.
3. Защитная.
Углеводы — обширный класс природных соединений, которые играют важную роль в жизни человека, животных и растений.
Простые углеводы (моносахариды) — это простейшие углеводы, не гидролизующиеся с образованием более простых углеводов.
Сложные углеводы — это углеводы, молекулы которых состоят из двух или большего числа остатков моносахаридов и разлагаются на эти моносахариды при гидролизе.
Физические свойства:
Моносахариды представляют собой бесцветные кристаллические вещества, сладкие на вкус, хорошо растворимы в воде, нерастворимы в эфире, плохо растворимы в спирте. Сладость моносахаридов различна. Например, фруктоза слаще глюкозы в три раза.
Химические свойства моносахаридов:
1. Свойства по карбонильной группе в открытых формах моносахаридов.
2. Свойства по спиртовым группам как в открытых, так и в циклических формах моносахаридов.
3. Свойства по полуацетальной гидроксильной группе.
Вернуться к теме «Строение и функции белков»
Задания по теме «Строение и функции белков» для самостоятельной подготовки к ЕГЭ по биологии
СКОРО! — Видео с объяснениями — СКОРО!
1. Установите соответствие между характеристикой химического вещества и веществом в организме человека
|
ФУНКЦИИ ВЕЩЕСТВ |
ХИМИЧЕСКИЕ ВЕЩЕСТВА |
|
|
А) специфичные катализаторы химических реакций Б) представлены только белками В) бывают белковой и липидной природы Г) необходимы для нормального обмена веществ Д) выделяются непосредственно в кровь Е) в основном поступают вместе с пищей |
1) ферменты 2) гормоны 3) витамины |
2. Выберите примеры функций белков, осуществляемых ими на клеточном уровне жизни
1) обеспечивают транспорт ионов через мембрану
2) входят в состав волос, перьев
3) формируют кожные покровы
4) антитела связывают антигены
5) запасают кислород в мышцах
6) обеспечивают работу веретена деления
3. Выберите особенности строения молекул белков
1) состоят из жирных кислот
2) состоят из аминокислот
3) мономеры молекулы удерживаются пептидными связями
4) состоят из одинаковых по строению мономеров
5) представляют собой многоатомные спирты
6) четвертичная структура молекул состоит из нескольких глобул
4. Выберите три функции, характерные только для белков
1) энергетическая
2) каталитическая
3) двигательная
4) транспортная
5) структурная
6) запасающая
5. Все приведённые ниже признаки, кроме двух, можно использовать для описания значения белков в организме человека и животных. Определите два признака, «выпадающих» из общего списка, и запишите в ответ цифры, под которыми они указаны
1) служат основным строительным материалом
2) расщепляются в кишечнике до глицерина и жирных кислот
3) образуются из аминокислот
4) в печени превращаются в гликоген
5) в качестве ферментов ускоряют химические реакции
6. Все перечисленные ниже признаки, кроме двух, можно использовать для описания молекулы инсулина. Определите два признака, «выпадающие» из общего списка, и запишите в таблицу цифры, под которыми они указаны
1) состоит из аминокислот
2) гормон надпочечников
3) катализатор многих химических реакций
4) гормон поджелудочной железы
5) вещество белковой природы
7. Все перечисленные ниже признаки, кроме двух, можно использовать для описания яичного белка альбумина. Определите два признака, «выпадающих» из общего списка, и запишите в таблицу цифры, под которыми они указаны
1) состоит из аминокислот
2) пищеварительный фермент
3) денатурирует обратимо при варке яйца
4) мономеры связаны пептидными связями
5) молекула образует первичную, вторичную и третичную структуры
8. Белки в организме человека и животных
1) служат основным строительным материалом
2) расщепляются в кишечнике до глицерина и жирных кислот
3) образуются из аминокислот
4) в печени превращаются в гликоген
5) откладываются в запас
6) в качестве ферментов ускоряют химические реакции
9. Установите соответствие между характеристикой и функцией белка, которую он выполняет
|
ХАРАКТЕРИСТИКА БЕЛКА |
ФУНКЦИЯ БЕЛКА |
|
|
А) входит в состав центриолей Б) образует рибосомы В) представляет собой гормон Г) формирует мембраны клеток Д) изменяет активность генов |
1) регуляторная 2) структурная |
10. Найдите ошибки в приведенном тексте, исправьте их. Укажите номера пред-ложений, в которых сделаны ошибки, объясните их
1. Большое значение в строении и жизнедеятельности организмов имеют белки. 2. Это биополимеры, мономерами которых являются азотистые основания. 3. Белки входят в состав плазматической мембраны. 4. Многие белки выполняют в клетке ферментативную функцию. 5. В молекулах белка зашифрована наследственная информация о признаках организма. 6. Молекулы белка и тРНК входят в состав рибосом.
1) 2 — Это биополимеры, мономерами которых являются аминокислоты;
2) 5 — В молекулах ДНК зашифрована наследственная информация;
3) 6 — Молекулы белка и рРНК входят в состав рибосом.
11. Какова природа большинства ферментов и почему они теряют свою активность при повышении уровня радиации?
1) большинство ферментов — белки;
2) под действием радиации происходит денатурация, изменяется структура белка-фермента.
12. Почему человек без опасных последствий употребляет в пищу белки в виде мяса, рыбы, яиц, а вводить белки сразу в кровь для питания больных ни в коем случае нельзя?
1) белки в пищеварительном тракте, в желудке, в кислой среде расщепляются до аминокислот ферментами пептидазами;
2) в кровь попадают уже аминокислоты и разносятся к клеткам тканей;
3) введение в кровь чужеродных белков вызовет иммунную реакцию, отторжение, возможна даже гибель больного.
13. Может ли человек питаться только жирами, исключив из рациона белковую пищу?
1) Не может.
2) Отсутствие белков приведет к тому, что в клетках не будут выполняться следующие функции: ферментативная, двигательная, защитная, транспортная.
3) Синтез белков из жиров невозможен, т.к. белки имеют более сложное строение (их молекулы включают азот и серу).
14. Почему повышение температуры выше 40° опасно для жизни?
При повышении температуры выше 40 градусов, происходит денатурация (разрушение) белков, в том числе ферментов.
Просмотров: 57290
Чтобы поделиться, нажимайте
Белки (полипептиды) — биополимеры, построенные из остатков a-аминокислот, соединенных пептидными связями.
Пептидной связью называют амидную связь –CO–NH–, образованную при взаимодействии a-аминокислот за счет реакции между аминогруппой NH2 одной молекулы и карбоксильной группы COOH – другой. Продуктом реакции двух a-аминокислот является дипептид:
Из трех молекул a-аминокислот (глицин+аланин+глицин) образуется трипептид: H2N-CH2-CO-NH-CH(CH3)-CO-NH-CH2-COOH
Аналогично происходит образование тетра-, пента— и полипептидов.
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов. Макромолекулы белков имеют стеререгулярное строение, исключительно важное для проявления ими определенных биологических свойств. Несмотря на многочисленность белков, в их состав входят остатки лишь 22 a-аминокислот.
Функции белков в природе универсальны:
- каталитические (ферменты);
- регуляторные (гормоны);
- структурные (кератин шерсти, фиброин шелка, коллаген);
- двигательные (актин, миозин);
- транспортные (гемоглобин);
- запасные (казеин, яичный альбумин);
- защитные (иммуноглобулины) и т.д.
Разнообразные функции белков определяются a-аминокислотным составом и строением их высокоорганизованных макромолекул.
Выделяют 4 уровня структурной организации белков.
Первичная структура — определенная последовательность a-аминокислотных остатков в полипептидной цепи
Вторичная структура — конформация полипептидной цепи, закрепленная множеством водородных связей между группами N-H и С=О. Одна из моделей вторичной структуры — a-спираль
Третичная структура — форма закрученной спирали в пространстве, образованная главным образом за счет дисульфидных мостиков -S-S-, водородных связей, гидрофобных и ионных взаимодействий .
Четвертичная структура — агрегаты нескольких белковых макромолекул (белковые комплексы), образованные за счет взаимодействия разных полипептидных цепей.
Состав белков
Макромолекулы природных полипептидов (белков) состоят из остатков a-аминокислот —NH—CН(R)-СO—
В составе радикала R могут быть открытые цепи, карбо- и гетероциклы, а также различные функциональные группы (-SH, -OH, -COOH, -NH2).
Несмотря на многочисленность белков, их макромолекулы содержат остатки лишь 22 a-аминокислот (наиболее часто встречаются 20 a-аминокислот).
Молекулярные массы различных белков составляют от 10 000 до нескольких миллионов.
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации различных a-аминокислот:
Аминокислотный состав белков оказывает определяющее влияние на их биологические свойства.
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
Жиры — сложные эфиры глицерина и высших одноосновных карбоновых кислот (так называемых ЖИРНЫХ кислот).
Общее название таких соединений – триглицериды или триацилглицерины, где ацил – остаток карбоновой кислоты
ФИЗИЧЕСКИЕ СВОЙСТВА
Жидкие или твердые вещества, растворимые в органических растворителях, но не растворимые в воде.
ХИМИЧЕСКИЕ СВОЙСТВА.
ГИДРОЛИЗ ЖИРОВ
проходит в кислой или в щелочной среде, или под действием ферментов:
а) кислотный (водный) гидролиз:
под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
б) щелочной гидролиз – омыление.
Получают глицерин и соли карбоновых кислот (мыла), входивших в состав жира. Мыла – соли высших жирных кислот (натриевые – твёрдые, калиевые – жидкие).
При пищеварении жир омыляется (расщепляется) с помощью ферментов.
ГИДРИРОВАНИЕ (ГИДРОГЕНИЗАЦИЯ)
процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
Остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
Жидкие жиры обесцвечивают бромную воду, что говорит о наличии двойных связей
УГЛЕВОДЫ (САХАРА) — органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3.
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4.
МОНОСАХАРИДЫ — гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (альдегидная или кетонная) и несколько гидроксильных.
ФИЗИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
Моносахариды – твердые вещества, легко растворимые в воде, плохо – в спирте и совсем нерастворимые в эфире.
Водные растворы имеют нейтральную реакцию на лакмус.
Большинство моносахаридов обладают сладким вкусом, однако меньшим, чем свекловичный сахар.
ХИМИЧЕСКИЕ СВОЙСТВА МОНОСАХАРИДОВ
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
СВОЙСТВА ГЛЮКОЗЫ, КАК МНОГОАТОМНОГО СПИРТА
1. Реакция комплексообразование с гидроксидом меди (II).
При взаимодействии свежеосажденного гидроксида меди (II) с моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
2. Глюкоза, как альдегид.
Образование сложных эфиров с ангидридами кислот или галогенангидридами.
3. Реакция с гидроксидом меди (II) при нагревании
4. Окисление бромной водой до глюконовой кислоты.
4. Каталитическое гидрирование (восстановление) глюкозы
происходит восстановление карбонильной группы до спиртового гидроксила, получается шестиатомный спирт – сорбит.
5. РЕАКЦИИ БРОЖЕНИЯ.
а) спиртовое брожение
б) молочнокислое брожение
в) маслянокислое брожение
ФРУКТОЗА— структурный изомер глюкозы — КЕТОНОСПИРТ:
Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп. При гидрировании фруктозы также получается СОРБИТ.
СВОЙСТВА ДИСАХАРИДОВ
это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
1. САХАРОЗА (СВЕКЛОВИЧНЫЙ ИЛИ ТРОСТНИКОВЫЙ САХАР) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
Чистая сахароза — бесцветное кристаллическое вещество сладкого вкуса, хорошо растворимое в воде.
В молекуле сахарозы нет открытой (альдегидной) формы. Вследствие этого сахароза не вступает в реакции альдегидной группы – с аммиачным раствором оксида серебра с гидроксидом меди при нагревании.
Подобные дисахариды называют невосстанавливающими, т.е. не способными окисляться.
2. МАЛЬТОЗА.
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
Мальтоза — является восстанавливающим дисахаридом и вступает в реакции, характерные для альдегидов.
2. Окисление восстанавливающихся дисахаридов
СВОЙСТВА ПОЛИСАХАРИДОВ.
это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — КРАХМАЛ И ЦЕЛЛЮЛОЗА (C6H10O5)n
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы (выделена цветом):
КРАХМАЛ.
Крахмалом называется смесь двух полисахаридов, построенных из остатков циклической α-глюкозы. Крахмал — белый порошок, нерастворимый в холодной воде.
В горячей воде он набухает и образует клейстер. В отличие от моно- и олигосахаридов полисахариды не обладают сладким вкусом
2. Гидролиз крахмала
(ферментативный или кислотный) – ведет к образованию глюкозы.
3. Крахмал не дает реакции «серебряного зеркала» и не восстанавливает гидроксид меди (II)
4. Качественная реакция на крахмал — окрашивание поверхности в синий цвет при добавлении раствора йода.
ЦЕЛЛЮЛОЗА
наиболее распространенный растительный полисахаридМолекулярная масса целлюлозы — от 400 000 до 2 млн.
Чистая целлюлоза — твердое белое вещество, имеющее волокнистую структуру. Она нерастворима в воде и органических растворителях, но хорошо растворяется в аммиачном растворе гидроксида меди (II). Как известно, сладкого вкуса целлюлоза не имеет.
Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
ОБРАЗОВАНИЕ СЛОЖНЫХ ЭФИРОВ.
2. Нитрование целлюлозы
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
3. Взаимодействие с уксусной кислотой
Образуется ацетат целлюлозы — ацетатное волокно.
4. Гидролиз целлюлозы (ферментативный или кислотный) — образуется глюкоза
БЕЛКИ (ПОЛИПЕПТИДЫ) — биополимеры, построенные из остатков α-аминокислот, соединенных пептидными (амидными) связями.
Формально образование белковой макромолекулы можно представить как реакцию поликонденсации α-аминокислот
Молекулярные массы различных белков (полипептидов) составляют от 10 000 до нескольких миллионов.Макромолекулы белков имеют стереорегулярное строение, исключительно важное для проявления ими определенных биологических свойств.
Несмотря на многочисленность белков, в их состав входят остатки не более 22 α-аминокислот.
По физическим свойствам белки делят на два класса:
1.ГЛОБУЛЯРНЫЕ БЕЛКИ- растворяются в воде или образуют коллоидныеnрастворы
2.ФИБРИЛЛЯРНЫЕ БЕЛКИ в воде нерастворимы
ДЕНАТУРАЦИЯ БЕЛКА
разрушение вторичной и третичной структуры белка с сохранением первичной структуры. Происходит при нагревании, изменении кислотности среды, действии излучения.
Пример денатурации — свертывание яичных белков при варке яиц.
ДЕНАТУРАЦИЯ БЫВАЕТ ОБРАТИМОЙ И НЕОБРАТИМОЙ.
Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
3. КАЧЕСТВЕННЫЕ РЕАКЦИИ НА БЕЛКИ:
1)Биуретовая реакция – фиолетовое окрашивание при действии на белки свежеосажденного гидроксида меди (II).
2) Ксантопротеиновая реакция — желтое окрашивание при действии на белки концентрированной азотной кислоты.
3) Реакция с щелочью в присутствии солей свинца – при нагревании выпадает черный осадок PbS, что свидетельствует о присутствии серосодержащих аминокислот.




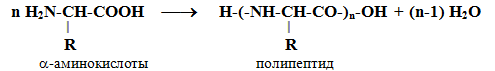
![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)

































