в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 1000 1–20 | 21–40 | 41–60 | 61–80 …
Добавить в вариант
В двух сосудах (1) и (2) объёмом V0 каждый находятся одинаковые идеальные одноатомные газы. Исходные состояния этих газов соответствуют точкам А и В на VT-диаграмме (см. рис.). Известно, что сначала давление в обоих сосудах одинаковое. Затем из исходных состояний газы переводят в новые конечные состояния А‘ и В‘.
Выберите все верные утверждения на основании анализа представленного графика.
1) В исходном состоянии концентрация молекул газа в сосуде (1) равна концентрации молекул газа в сосуде (2).
2) В конечном состоянии средняя кинетическая энергия хаотического движения молекул газа в сосуде (1) больше средней кинетической энергии хаотического движения молекул газа в сосуде (2).
3) Масса газа в сосуде (1) больше массы газа в сосуде (2).
4) Изменение внутренней энергии газа, находящегося в сосуде (1), при его переходе из состояния А в состояние А‘ равно изменению внутренней энергии газа, находящегося в сосуде (2), при его переходе из состояния В в состояние В‘.
5) Работа, совершённая газом, находящимся в сосуде (1) в процессе А→А‘, больше работы, совершённой газом, находящимся в сосуде (2) в процессе В→В‘.
В двух закрытых сосудах одинакового объёма (1 литр) нагревают два различных газа — 1 и 2. На рисунке показаны зависимости давления p этих газов от времени t. Известно, что начальные температуры газов были одинаковы.
Выберите все верные утверждения, соответствующие результатам этих экспериментов.
1) Количество вещества первого газа больше, чем количество вещества второго газа.
2) Так как по условию эксперимента газы имеют одинаковые объёмы, а в момент времени t = 40 мин они имеют и одинаковые давления, то температуры этих газов в этот момент времени также одинаковы.
3) В момент времени t = 40 мин температура газа 1 меньше температуры газа 2.
4) В процессе проводимого эксперимента не происходит изменения внутренней энергии газов.
5) В процессе проводимого эксперимента оба газа не совершают работу.
1 моль одноатомного идеального газа совершает цикл 1−2−3−1, при котором давление p газа изменяется с изменением плотности
газа так, как показано на рисунке. Значения плотности и давления в вершинах цикла представлены на графике. Выберите из предложенного перечня все верные утверждения.
1) Работа газа в процессе 1−2 равна нулю.
2) Внутренняя энергия газа в процессе 2−3 увеличивается.
3) При переходе газа из 3 в 1 внутренняя энергия не меняется.
4) В процессе 3−1 газ отдаёт положительное количество теплоты.
5) Температура газа в состоянии 3 минимальна.
Источник: ЕГЭ по физике 2022. Досрочная волна
На рисунках приведены графики А и Б двух процессов: 1—2 и 3—4, происходящих с 1 моль гелия. Графики построены в координатах V—T и p—V, где p — давление, V — объём и T — абсолютная температура газа. Установите соответствие между графиками и утверждениями, характеризующими изображённые на графиках процессы. К каждой позиции первого столбца подберите соответствующую позицию второго столбца.
ГРАФИКИ
А)
Б)
УТВЕРЖДЕНИЯ
1) Над газом совершают работу, при этом его внутренняя энергия увеличивается.
2) Над газом совершают работу, при этом газ отдаёт положительное количество теплоты.
3) Газ получает положительное количество теплоты и совершает работу.
4) Газ получает положительное количество теплоты, при этом его внутренняя энергия увеличивается.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2015 по физике.
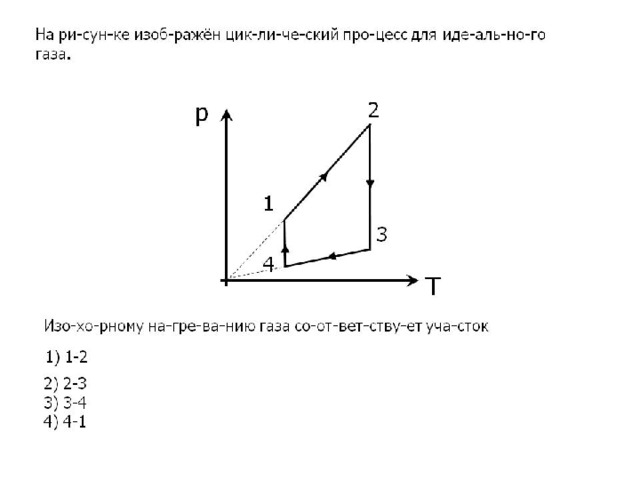
На рисунке показан график циклического процесса, проведённого с одноатомным идеальным газом, в координатах р–Т, где р — давление газа, Т — абсолютная температура газа. Количество вещества газа постоянно.
Из приведённого ниже списка выберите все правильные утверждения, характеризующих процессы на графике, и укажите их номера.
1) Газ за цикл совершает положительную работу.
2) В процессе АВ газ получает положительное количество теплоты.
3) В процессе ВС внутренняя энергия газа уменьшается.
4) В процессе СD над газом совершают работу внешние силы.
5) В процессе DA газ изотермически расширяется.
Источник: Демонстрационная версия ЕГЭ—2018 по физике
Один моль одноатомного идеального газа участвует в циклическом процессе, график которого изображён на TV−диаграмме.
Выберите все верные утверждения на основании анализа представленного графика.
1) Давление газа в состоянии 2 больше давления газа в состоянии 4.
2) Работа газа на участке 2–3 положительна.
3) На участке 1–2 давление газа увеличивается.
4) На участке 4–1 от газа отводится некоторое количество теплоты.
5) Изменение внутренней энергии газа на участке 1−2 меньше, чем изменение внутренней энергии газа на участке 2−3.
На рисунке показан график зависимости модуля среднеквадратичной скорости Vср.кв. атомов одноатомного идеального газа от объёма V газа в некотором процессе 1→2. Количество атомов газа в течение этого процесса не изменяется.
На основании анализа представленного графика выберите все верные утверждения.
1) В процессе 1→2 газ совершает положительную работу.
2) В процессе 1→2 внутренняя энергия газа уменьшается.
3) В процессе 1→2 давление p газа возрастает прямо пропорционально объёму V газа.
4) В процессе 1→2 газ отдаёт некоторое количество теплоты окружающим телам.
5) Процесс 1→2 является изобарическим.
На рисунке показан график циклического процесса, проведённого с одноатомным идеальным газом, в координатах р–Т, где р — давление газа, Т — абсолютная температура газа. Количество вещества газа постоянно. Из приведённого ниже списка выберите все правильные утверждения, характеризующие процессы на графике.
1) Газ за цикл совершает отрицательную работу.
2) В процессе АВ газ получает положительное количество теплоты.
3) В процессе ВС внутренняя энергия газа остаётся неизменной.
4) В процессе DA газ изотермически расширяется.
5) В процессе СD над газом совершают работу внешние силы.
Аналоги к заданию № 9311: 11793 Все
Источник: ЕГЭ по физике 01.04.2019. Досрочная волна. Вариант 3
На рисунках приведены графики А и Б двух процессов: 1—2 и 3—4, происходящих с 1 моль аргона. Графики построены в координатах p—V и V—T, где p — давление, V — объём и T — абсолютная температура газа. Установите соответствие между графиками и утверждениями, характеризующими изображённые на графиках процессы. К каждой позиции первого столбца подберите соответствующую позицию второго столбца.
ГРАФИКИ
А)
Б)
УТВЕРЖДЕНИЯ
1) Внутренняя энергия газа уменьшается, при этом газ отдаёт теплоту.
2) Над газом совершают работу, при этом газ отдаёт теплоту.
3) Газ получает теплоту, но не совершает работу.
4) Газ получает теплоту и совершает работу.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Репетеционные варианты. Гиголо А. И. 2015 г.
Один моль идеального одноатомного газа совершает циклический процесс 1-2-3-4-1, график которого показан на рисунке в координатах p-V. Из предложенного перечня выберите все верные утверждения и укажите их номера.
1) В процессе 1-2 внутренняя энергия газа увеличивается.
2) В процессе 2-3 газ совершает положительную работу.
3) В процессе 3-4 газ отдает некоторое количество теплоты.
4) В процессе 4-1 температура газа увеличивается в 4 раза.
5) Работа, совершённая газом в процессе 1-2, в 3 раза больше работы, совершённой над газом в процессе 3-4.
В вертикальном цилиндре с гладкими стенками под массивным металлическим поршнем находится идеальный газ. В первоначальном состоянии 1 поршень опирается на жёсткие выступы на внутренней стороне стенок цилиндра (рис. 1), а газ занимает объём V0 и находится под давлением p0, равным внешнему атмосферному. Его температура в этом состоянии равна T0. Газ медленно нагревают, и он переходит из состояния 1 в состояние 2, в котором давление газа равно 2p0, а его объём равен 2V0 (рис. 2). Количество вещества газа при этом не меняется. Постройте график зависимости объёма газа от его температуры при переходе из состояния 1 в состояние 2. Ответ поясните, указав, какие явления и закономерности Вы использовали для объяснения.
Источник: Демонстрационная версия ЕГЭ—2016 по физике.
В двух закрытых сосудах одинакового объёма (1 литр) нагревают два различных газа — 1 и 2. На рисунке показаны зависимости давления p этих газов от времени t. Известно, что начальные температуры газов были одинаковы.
Выберите все верные утверждения, соответствующие результатам этих экспериментов.
1) Количество вещества первого газа меньше, чем количество вещества второго газа.
2) Так как по условию эксперимента газы имеют одинаковые объёмы, а в момент времени t = 40 мин они имеют и одинаковые давления, то температуры этих газов в этот момент времени также одинаковы.
3) В момент времени t = 40 мин температура газа 1 больше температуры газа 2.
4) В процессе проводимого эксперимента внутренняя энергия обоих газов увеличивается.
5) В процессе проводимого эксперимента оба газа не совершают работу.
В закрытом сосуде объёмом 8,3 литра находится одноатомный идеальный газ при температуре 127 °C. Начиная с момента времени t = 0 давление p газа изменяется так, как показано на приведённом графике.
На основании анализа графика выберите все верные утверждения.
1) Количество теплоты, переданное газу за первые 10 минут, равно 74,7 Дж.
2) Работа газа за первые 10 минут больше, чем работа газа за следующие 10 минут.
3) Изменение внутренней энергии газа за первые 20 минут равно 149,4 Дж.
4) В момент времени t = 25 мин температура газа станет равной 407,5 °C.
5) По заданным в задаче параметрам определить число молей газа в сосуде не представляется возможным.
Два моля одноатомного идеального газа участвуют в циклическом процессе, график которого изображён на UV-диаграмме (U — внутренняя энергия газа, V — его объём).
Выберите все верные утверждения на основании анализа представленного графика.
1) В процессе 1–2 газ изобарно нагревается.
2) В процессе 2–3 температура газа увеличивается.
3) В процессе 3–4 газ отдаёт некоторое количество теплоты.
4) В процессе 4–1 работа газа отрицательная.
5) В процессе 1–2 газ совершает работу 200 Дж.
На pV-диаграмме показан циклический процесс, состоящий из двух изохор и двух адиабат. В качестве рабочего вещества используется одноатомный идеальный газ.
Из приведённого ниже списка выберите все правильные утверждения.
1) Данный цикл соответствует циклу идеальной тепловой машины (циклу Карно).
2) В процессе 4–1 газ получил количество теплоты 450 Дж.
3) В процессе 2–3 газ отдал в 4 раза большее количество теплоты, чем получил в процессе 4–1.
4) Внутренняя энергия газа в процессе 1–2 уменьшается.
5) В процессах 1–2 и 3–4 газ не совершает работы.
Зависимость температуры 1 моль одноатомного идеального газа от давления показана на рисунке. Выберите из предложенных утверждений все, которые верно отражают результаты этого эксперимента.
1) В процессе 1–2 объём газа увеличился в 3 раза.
2) В процессе 2–3 газ совершал положительную работу.
3) В процессе 2–3 внутренняя энергия газа уменьшалась.
4) В процессе 1–2 газ отдал положительное количество теплоты.
5) В процессе 1–2 концентрация молекул газа не менялась.
Источник: Демонстрационная версия ЕГЭ−2019 по физике
На рисунке показан график циклического процесса, проведённого с одноатомным идеальным газом, в координатах V−Т, где V — объем газа, Т — абсолютная температура газа. Количество вещества газа постоянно.
Из приведенного ниже списка выберите все правильные утверждения, характеризующие процессы на графике, и укажите их номера.
1. В состоянии В концентрация газа максимальна.
2. В процессе АВ газ получает некоторое количество теплоты.
3. В процессе ВС внутренняя энергия газа остается неизменной.
4. Давление газа в процесс СD постоянно, при этом газ совершает положительную работу.
5. В процессе DA давление газа изохорно увеличивается.
Источник: ЕГЭ по физике 13.07.2020. Основная волна
На рисунках А) и Б) приведены графики двух процессов 1−2 и 3−4, каждый из которых проводится с одним молем аргона. Графики построены в координатах и
где p — давление, V — объём и T — абсолютная температура газа.
Установите соответствие между графиками и утверждениями, характеризующими изображённые на графиках процессы. К каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
ГРАФИК
А)
Б)
УТВЕРЖДЕНИЕ
1) Внутренняя энергия газа уменьшается, при этом газ отдаёт теплоту.
2) Над газом совершают работу, при этом газ отдаёт теплоту.
3) Газ получает теплоту, но не совершает работы.
4) Газ получает теплоту и совершает работу.
На рисунках А) и Б) приведены графики двух процессов 1−2 и 3−4, каждый из которых проводится с одним молем аргона. Графики построены в координатах и
где p — давление, V — объём и T — абсолютная температура газа.
Установите соответствие между графиками и утверждениями, характеризующими изображённые на графиках процессы. К каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами.
ГРАФИК
А)
Б)
УТВЕРЖДЕНИЕ
1) Внутренняя энергия газа уменьшается, при этом газ отдаёт теплоту.
2) Газ совершает положительную работу, при этом газ отдаёт теплоту.
3) Газ получает теплоту, но не совершает работы.
4) Газ получает теплоту и совершает работу
В закрытом сосуде находится идеальный газ. Как при охлаждении сосуда с газом изменятся величины: давление газа, его плотность и внутренняя энергия?
Для каждой величины определите соответствующий характер изменения:
1) увеличилась;
2) уменьшилась;
3) не изменилась.
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
| Давление газа | Плотность газа | Внутренняя энергия газа |
Всего: 1000 1–20 | 21–40 | 41–60 | 61–80 …
Пройти тестирование по этим заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Если при сжатии объём идеального газа уменьшился в 2 раза, а давление газа увеличилось в 2 раза, то во сколько раз изменилась при этом абсолютная температура газа?
2
Во сколько раз изменяется давление идеального газа при уменьшении объёма идеального газа в 2 раза и увеличении его абсолютной температуры в 4 раза?
4
Идеальный газ в цилиндре переводится из состояния А в состоянии В так, что его масса при этом не изменяется. Параметры, определяющие состояния газа, приведены в таблице. Какое число должно быть в свободной клетке таблицы?
|
|
|
|
|
| Состояние A |
1,0 |
4 |
|
| Состояние B |
1,5 |
8 |
900 |
5
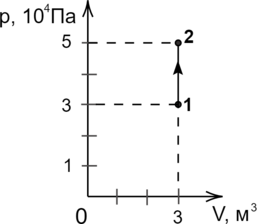
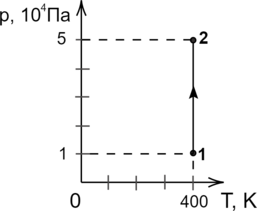
В сосуде находится некоторое количество идеального газа. Во сколько раз изменится температура газа, если он перейдёт из состояния 1 в состояние 2 (см. рис.)?
Пройти тестирование по этим заданиям
8. Молекулярно-кинетическая теория
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
Газовые законы
1 моль гелия изохорно нагревают на 154 К, при этом давление газа увеличивается в 2,1 раза. До какой температуры нагрели газ? Ответ дайте в кельвинах.
Процесс изохорный, т.е. объём не меняется. Запишем закон Шарля: [hspace{ 5 mm} dfrac{p_1}{T_1}=dfrac{p_2}{T_2} hspace{ 5 mm} (1)] Изменение температуры есть разница конечной и начальной температуры газа: [hspace{ 5 mm} Delta T = T_2 — T_1 hspace{3 mm} Rightarrow hspace{3 mm} T_1 = T_2 — Delta T hspace{ 5 mm} (2)] По условию давление газа увеличивается в 2,1 раза: [hspace{ 5 mm}p_2 = 2,1 p_1hspace{ 5 mm} (3)] Подставим (2), (3) в (1) и выразим температуру, до которой нагрели газ: [dfrac{p_1}{T_2 — Delta T}=dfrac{2,1 p_1}{T_2}] [T_2 = dfrac{2,1 p_1 Delta T}{2,1p_1 — p_1} = dfrac{2,1 Delta T}{1,1} = dfrac{2,1 cdot 154text{ K}}{1,1} = 294 text{ K}]
Ответ: 294
Воздух при температуре 27(^{circ})C и давлении 202,65 кПа занимает объём 0,3 м(^3). Газ изобарно нагрели, причём объём газа увеличился до 0,5 м(^3). Найдите конечную температуру воздуха. Ответ дайте в кельвинах.
Т.к. процесс изобарный ((p=const)), используем закон Гей – Люссака: [dfrac{V_1}{T_1}=dfrac{V_2}{T_2}hspace{3 mm}Rightarrow hspace{3 mm} T_2=dfrac{T_1 cdot V_2}{V_1}] Переведём (T_1) в кельвины: 27(^{circ})С + 273 = 300 К. [T_2=dfrac{300 text{ К} cdot 0,5 text{ м$^3$}}{0,3text{ м$^3$}}=500 text{ К}]
Ответ: 500
На графике изображено изменение состояния постоянной массы разреженного аргона. Температура газа в состоянии 1 равна 56(^{circ})C. Какова температура аргона в состоянии 2? Ответ дайте в кельвинах.
Из графика видно, что процесс 1–2 — изобарный ((p=const)). Воспользуемся законом Гей – Люссака: [dfrac{V_1}{T_1}=dfrac{V_2}{T_2}hspace{3 mm}Rightarrow hspace{3 mm} T_2=dfrac{T_1 cdot V_2}{V_1}] Переведём (T_1) в кельвины: 56(^{circ})С + 273 = 329 К. [T_2=dfrac{329text{ К} cdot 14text{ м$^3$}}{7text{ м$^3$}} = 658 text{ К}]
Ответ: 658
На графике изображено изменение состояния постоянной массы разреженного аргона. Температура газа в состоянии 2 равна 212(^{circ})C. Какова температура аргона в состоянии 1? Ответ дайте в кельвинах.
Из графика видно, что процесс 1–2 — изохорный ((V=const)). Воспользуемся законом Шарля: [dfrac{p_1}{T_1}=dfrac{p_2}{T_2}hspace{3 mm}Rightarrow hspace{3 mm} T_1=dfrac{p_1 cdot T_2}{p_2}] Переведём (T_2) в кельвины: 212(^{circ})С + 273 = 485 К. [T_1=dfrac{3cdot 10^4 text{ Па} cdot 485text{ К}}{5 cdot 10^4text{ Па}} = 291 text{ К}]
Ответ: 291
Давление газа при температуре 306 К равно 159 кПа. Газ нагрели до температуры (T_2), при этом объём газа не изменился. После нагревания давление газа стало равно 212 кПа. Найдите, до какой температуры (T_2) нагрели газ. Ответ дайте в кельвинах.
По условию процесс изохорный ((V=const)).
Согласно закону Шарля: [dfrac{p_1}{T_1} = dfrac{p_2}{T_2}hspace{3 mm}Rightarrowhspace{3 mm} T_2 = dfrac{T_1 p_2}{p_1}] [T_2 = dfrac{306 text{ K} cdot 212 cdot 10^3 text{ Па}}{159 cdot 10^3 text{ Па}} = 408 text{ K}]
Ответ: 408
Газ занимает объём 0,03 м(^3) при температуре 418 К. Какой объём займёт этот же газ, если его температура понизится до 209 К? Давление и масса газа не меняются. Ответ дайте в м(^3).
По условию процесс изобарный ((p=const)). По закону Гей – Люссака: [dfrac{V_1}{T_1} = dfrac{V_2}{T_2}hspace{3 mm}Rightarrowhspace{3 mm} V_2 = dfrac{V_1T_2}{T_1}] [V_2 = dfrac{0,03 text{ м$^3$} cdot 209 text{ К}}{418 text{ К}} = 0,015 text{ м$^3$}]
Ответ: 0,015
На рисунке представлен график зависимости давления от температуры газа. Объём газа в состоянии 2 равен 6 л. Какой объём занимает газ в состоянии 1? Масса газа не меняется. Ответ дайте в м(^3).
По графику видно, что процесс 1–2 — изотермический ((T=const)). По закону Бойля – Мариотта: [p_1V_1 = p_2V_2hspace{3 mm}Rightarrowhspace{3 mm} V_1 = dfrac{p_2V_2}{p_1}] Переведём объём газа в м(^3): (; 
Ответ: 0,03

Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Описание презентации по отдельным слайдам:
-
1 слайд
Решение задач ЕГЭ.
10 класс.
Задачи из учебника
(стр.232). -
2 слайд
Идеальный газ изотермически сжали из состояния с объёмом 6 л так, что давление газа изменилось в 3 раза.
На сколько уменьшился объём газа в этом процессе? -
3 слайд
Выразим V2, запишем разность объёмов и подставим:
-
4 слайд
2. Поршень площадью 10 см2 и массой 5 кг может без трения перемещаться в вертикальном цилиндрическом сосуде, обеспечивая при этом его герметичность. Сосуд с поршнем, заполненный газом, покоится на полу неподвижного лифта при атмосферном давлении 100 кПа, при этом расстояние от нижнего края поршня до дна сосуда 20 см. Каким станет это расстояние, когда лифт поедет вверх с ускорением, равным 2 м/с2? Изменение температуры газа не учитывайте.
-
5 слайд
Выразим высоту и подставим давления Р1 и Р2:
-
6 слайд
3. С идеальным газом происходит изобарный процесс, в котором для увеличения объёма газа на 150 дм2 его температуру увеличивают в 2 раза. Масса газа постоянна. Каким был первоначальный объём газа?
-
-
8 слайд
4. Идеальный одноатомный газ в количестве
v = 0,09 моль находится в равновесии в вертикальном цилиндре под поршнем массой
5 кг. Трение между поршнем и стенками цилиндра отсутствует. Внешнее атмосферное давление Р0 = 100 кПа. В результате нагревания газа поршень поднялся на высоту h = 4 см, а температура газа повысилась на Т = 16 К. Чему равна площадь поршня?
∆
∆ -
-
10 слайд
5. Идеальный газ изохорно нагревают так, что его температура изменяется на Т = 240 К, а давление — в 1,8 раза. Масса газа постоянна. Определите начальную температуру газа по шкале Кельвина.
∆ -
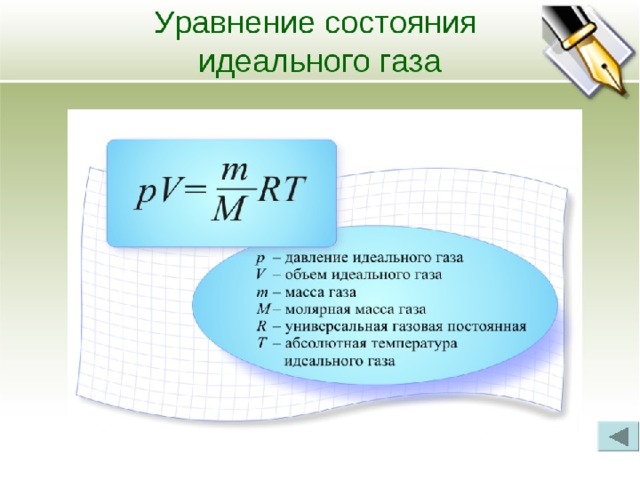
Уравнение Менделеева-Клапейрона и газовые законы: простые задачи
Задачи из пособия Г.А. Никуловой и А.Н. Москалева (2017 г). По теме «Тепловое равновесие, уравнение состояния идеального газа»
Задача 1.
Во сколько раз средняя квадратичная скорость молекул кислорода меньше средней квадратичной скорости молекул водорода, если температуры этих газов одинаковы?
Ответ: в 4 раза
Задача 2.
Три одинаковых сосуда соединены трубками с краном. Первый сосуд содержит 2 моль водорода, второй – 1 моль гелия, третий – 1,5 моль аргона. Как изменится давление в каждом сосуде после того, как краны откроют? Температура неизменна.
Согласно основному уравнению МКТ
Поэтому давление будет определяться концентрацией, а именно количеством вещества, приходящимся на объем. Когда краны откроют, все 4,5 моля газов распределятся по всему объему сосуда – по всем . Поэтому на один объем
станет приходиться по 1,5 моля газов. То есть в первом сосуде давление уменьшится (в нем изначально было 2 моль газа), во втором – увеличится, а в третьем – не изменится.
Задача 3.
В закрытом сосуде вместимостью 2 м находится 280 г азота и 320 г кислорода. Чему равно давление в такой газовой смеси при температуре
?
Согласно уравнению Менделеева-Клапейрона
Ответ: 24 кПа.
Задача 4.
Два баллона объемами 4 и 6 л соединены трубкой с краном. В первом баллоне находится 1,5 моль кислорода под давлением 200 кПа. Второй пуст. Определите давление в сосудах после того, как открыли кран. Температура постоянна.
Если температура постоянна, то можно воспользоваться законом Бойля -Мариотта:
Ответ: 80 кПа
Задача 5.
Воздушный шар радиусом 5 м удерживается веревкой, массой которой можно пренебречь. На сколько изменится натяжение веревки при повышении температуры воздуха с С до
С? Атмосферное давление нормальное.
При повышении температуры увеличится объем шара согласно закону Гей-Люссака, и в связи с этим вырастет сила Архимеда.
Ответ: 482 Н
Задача 6.
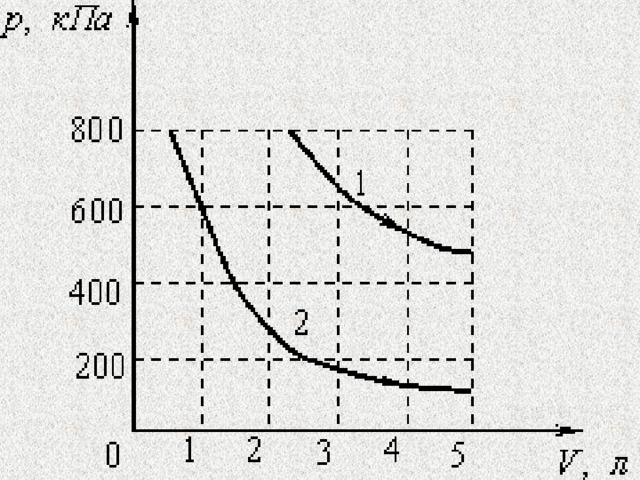
По рисунку определите отношение максимального и минимального объемов газа.
К задаче 6
Согласно уравнению Менделеева-Клапейрона
Тогда для точки 2
Откуда
И для точки 3
Откуда
Отношение объемов будет равно 6.
Ответ: 6.
Изобарный процесс
Заполните пропуск в тексте.
Повторите определение изобарного процесса.
Процесс изменения состояния термодинамической системы данной массы при называют изобарным.
постоянном объёме
постоянной температуре
постоянном давлении
Газовые законы
Заполните таблицу.
Повторите газовые законы.
| Закон | Изопроцесс | Формула |
|---|---|---|
|
$frac{V}{T}=const$ |
||
|
Изотермический |
||
|
Шарля |
$frac{p}{T}=const$
Изобарный
Бойля–Мариотта
Изохорный
Гей-Люссака
$pV=const$
Физические величины
Установите соответствие между физическими величинами и их единицами измерения.
Вспомните основные величины и единицы их измерения.
Уравнение состояния идеального газа
Соедините попарно физическую величину с её значением так, чтобы получились верные ответы.
1. В баллоне объёмом 2 $м^3$ находится 2 кг молекулярного кислорода при давлении $10^5$ Па. Какова температура кислорода (ответ в К)?
2. В баллоне ёмкостью 10 л находится углекислый газ при температуре 17 $^circ$ С под давлением 107 Па. Какой объём займёт этот газ при нормальных условиях (ответ в $м^3$)?
3. В закрытом сосуде объёмом 10 литров находится 2 моль азота. Температура газа равна 27 $^circ$ С. Чему равно давление газа (ответ в кПа)?
Повторите уравнение состояния идеального газа.
Изопроцессы
Соедините попарно фигуры так, чтобы каждому изопроцессу соответствовала формула.
Вспомните определения изопроцессов.
Основные величины МКТ
Решите кроссворд.
Вспомните основные величины МКТ и единицы их измерения.
Физические термины
Выделите мышкой 5 слов, которые относятся к теме урока.
1. Состояние вещества, в котором расстояние между атомами и молекулами в среднем во много раз больше размеров самих молекул.
2. Мельчайшая частица вещества.
3. Итальянский учёный XIX века, в честь которого названа постоянная, показывающая, какое количество атомов или молекул содержится в 1 моле вещества.
4. Синоним слова «корпускула».
5. Единица измерения количества вещества в СИ.
Повторите авторов законов и определения.
Газовые законы
Заполните пропуски в тексте, выбрав правильные варианты ответа из выпадающего меню.
Повторите газовые законы.
В сосуде под поршнем находится газ. При его изотермическом расширении давление газа на стенки сосуда
, температура
, объём газа
.
Измерительные приборы
Установите соответствие между физическими величинами и приборами для их измерения.
Повторите определения давления, температуры.
Экспериментальные исследования
Выберите верные утверждения, которые соответствуют результатам проведённых экспериментальных исследований.
В сосуде неизменного объема при комнатной температуре находилась смесь водорода и гелия, по 1 моль каждого. Половину содержимого сосуда выпустили, а затем добавили в сосуд 1 моль водорода. Газы считаются идеальными, а их температура постоянной.
Вспомните закон Гей-Люссака, закон Дальтона, определение парциального давления.
Парциальное давление водорода уменьшилось
В начале опыта концентрации газов были одинаковые
Давление смеси газов в сосуде не изменилось
Концентрация гелия увеличилась
В начале опыта массы газов были одинаковые
Изотермический процесс
На рисунке приведены графики двух изотермических процессов, проводимых с одной и той же массой газа. На основании графиков выберите верные утверждения о процессах, происходящих с газом.
Вспомните график изотермического процесса, на графике посмотрите направление стрелки.
Никаких выводов по графику сделать нельзя
Процесс 1 идёт при более высокой температуре
В процессе 1 объём увеличивается
Оба процесса идут при одной и той же температуре
Процесс 2 идёт при более высокой температуре
Газовые законы
Выделите мышкой 5 слов, которые относятся к теме урока.
1. Один из учёных, открывших изотермический процесс.
2. Единица измерения абсолютной температуры.
3. Параметр состояния газа постоянный в изохорном процессе.
4. Процессы, происходящие при постоянном значении одного из макропараметров состояния
5. Параметр состояния газа постоянный в изотермическом процессе.
Вспомните газовые законы.
Изопроцессы
Выделите мышкой 4 слова, которые относятся к теме урока.
1. Макроскопический параметр постоянный во всех изопроцессах.
2. Величины, характеризующие состояние газа.
3. График изопроцесса с постоянным объёмом.
4. График изопроцесса с постоянным давлением.
Вспомните изопроцессы.
Газовые законы
Выделите мышкой 4 слова, которые относятся к теме урока.
1. То, из чего состоит молекула.
2. Масса моля вещества.
3. Упрощённая модель реального газа.
4. Учёный, открывший взаимосвязь между давлением и температурой при постоянном объёме.
Повторите конспекты.
Решение задач по темам:
Уравнение состояния идеального газа. Газовые законы.
2.Какая формула соответствует уравнению состояния идеального газа?
P = 1/3 m o v 2 n
P = 2/3nE
PV = m/MRT
PV = 3/2kT
- № 493 (Р) (самостоятельно у доски)
2. В сосуде вместимостью 500 см 3 содержится 0,89 г водорода при температуре 17 0 С. Определить давление газа.
Изопроцессы
Формула изохорного процесса …
PV = const
v/T = const
p/T = const
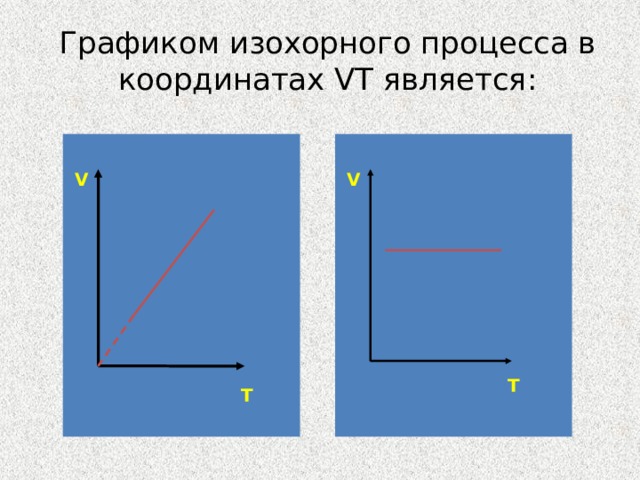
Графиком изохорного процесса в координатах VT является:
V
V
T
T
Формула изобарного процесса …
PV = const
p/T = const
v/T = const
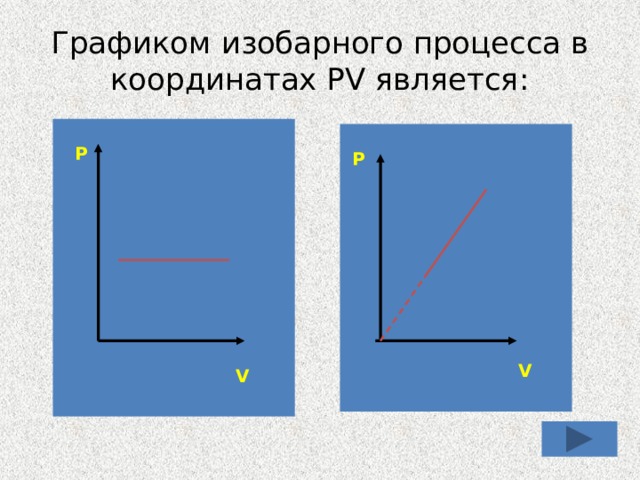
Графиком изобарного процесса в координатах PV является:
P
P
V
V
Процесс изменения состояния системы макроскопических тел (термодинамической системы) при постоянной температуре называется…
изобарный
изотермический
изохорный
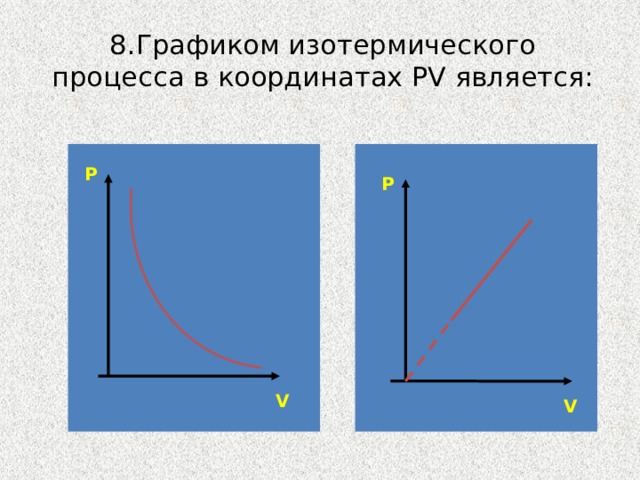
8.Графиком изотермического процесса в координатах PV является:
P
P
V
V
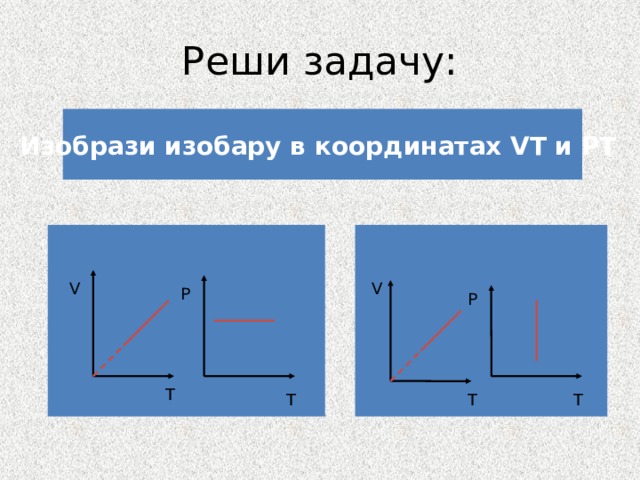
Реши задачу:
Изобрази изобару в координатах VT и PT
V
V
P
P
T
T
T
T
Даны две изохоры для двух идеальных газов. Сравнить объемы V 1 и V 2. Массы газов постоянны.
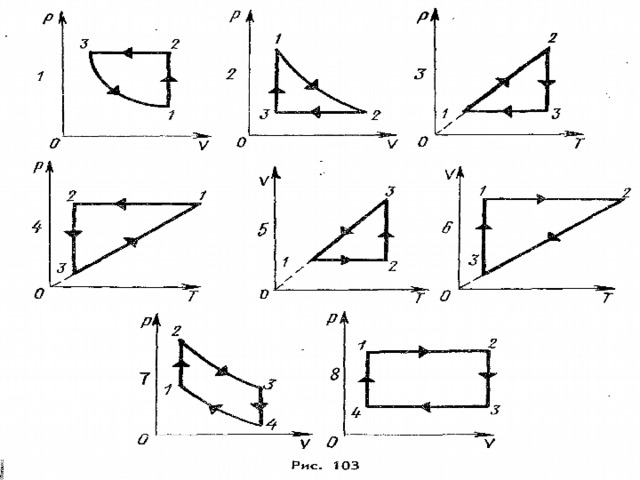
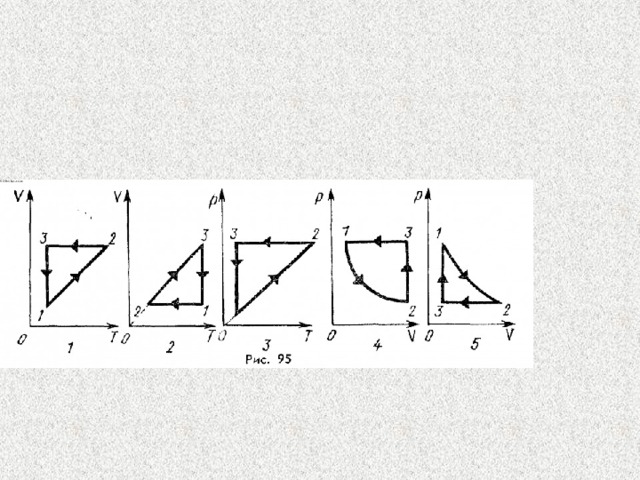
ЦИКЛИЧЕСКИЕ ПРОЦЕССЫ ИДЕАЛЬНОГО ГАЗА
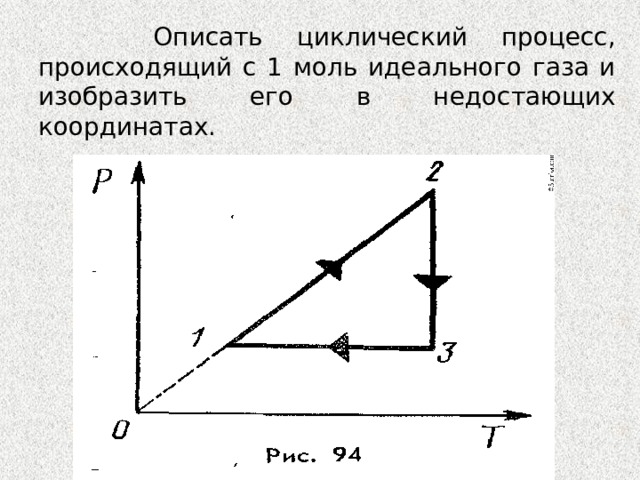
Описать циклический процесс, происходящий с 1 моль идеального газа и изобразить его в недостающих координатах.
Задания
«Решу ЕГЭ»
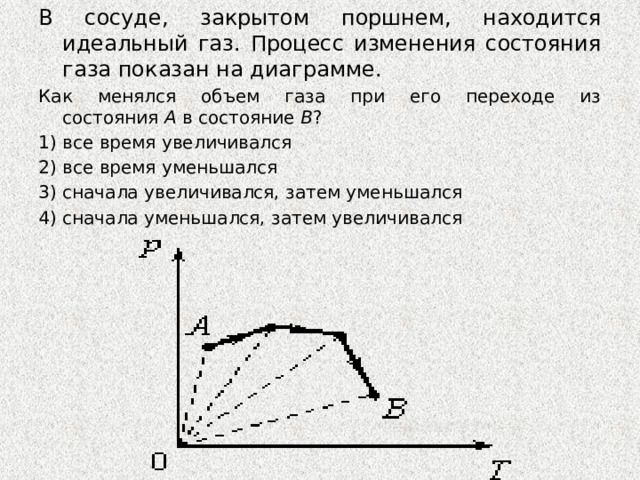
В сосуде, закрытом поршнем, находится идеальный газ. Процесс изменения состояния газа показан на диаграмме.
Как менялся объем газа при его переходе из состояния А в состояние В ?
1) все время увеличивался
2) все время уменьшался
3) сначала увеличивался, затем уменьшался
4) сначала уменьшался, затем увеличивался
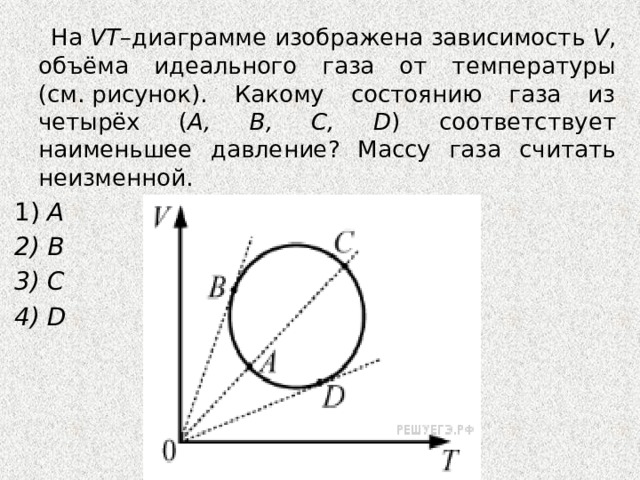
На VT –диаграмме изображена зависимость V , объёма идеального газа от температуры (см. рисунок). Какому состоянию газа из четырёх ( А, В, С, D ) соответствует наименьшее давление? Массу газа считать неизменной.
1) А
2) В
3) С
4) D
Решить задачу
При увеличении давления в 2 раза объем газа уменьшился на 40 мл.
Найти первоначальный объем.