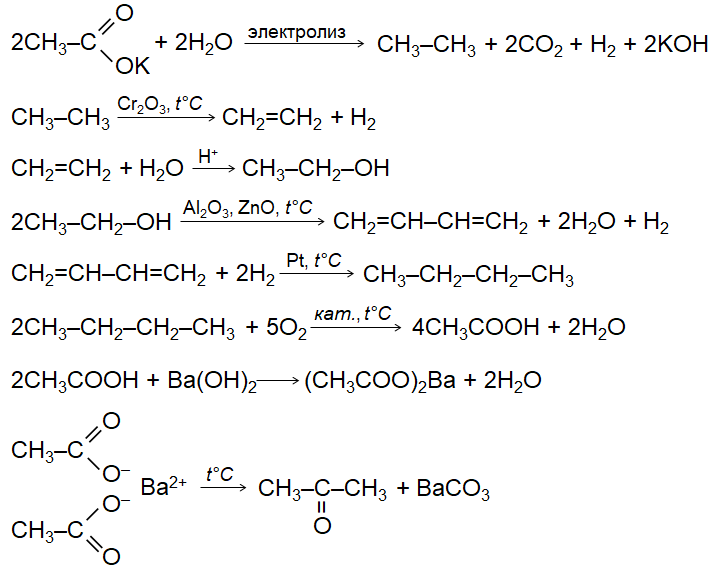
Карбоновые кислоты и сложные эфиры. Тематические задания для подготовки к ЕГЭ.
Задание №1
Выберите два утверждения, справедливые для муравьиной кислоты
1) является изомером уксусной кислоты
2) при нормальных условиях является газом
3) изменяет окраску индикаторов
4) хорошо растворима в воде
5) имеет межклассовые изомеры
Решение
Ответ: 34
Задание №2
Выберите два утверждения, справедливые для уксусной кислоты
1) содержит альдегидную группу
2) является гомологом адипиновой кислоты
3) образует межмолекулярные водородные связи
4) плохо растворима в воде
5) общая формула ее гомологического ряда CnH2nO2
Решение
Ответ: 35
Задание №3
Выберите два утверждения, справедливые для бензойной кислоты
1) является жидкостью с характерным запахом
2) является ароматической карбоновой кислотой
3) при нитровании замещение происходит в орто- и пара-положениях по отношению к карбоксильной группе
4) относится к классу аренов
5) является одноосновной кислотой
Решение
Ответ: 25
Задание №4
Выберите два утверждения, справедливые для олеиновой кислоты
1) ее остатки входят в состав жидких жиров
2) обесцвечивает бромную воду
3) относится к предельным одноосновным кислотам
4) образует простые эфиры
5) имеет твердое агрегатное состояние при обычных условиях
Решение
Ответ: 12
Задание №5
Выберите два утверждения, которые справедливы для стеариновой кислоты
1) относится к непредельным карбоновым кислотам
2) обесцвечивает бромную воду
3) обесцвечивает раствор перманганата калия
4) входит в состав твердых жиров
5) ее натриевая соль является твердым мылом
Решение
Ответ: 45
Задание №6
Выберите два утверждения, которые справедливы для всех карбоновых кислот
1) имеют жидкое агрегатное состояние при нормальных условиях
2) содержат карбоксильную группу
3) хорошо растворимы в воде
4) вступают в реакцию со щелочами
5) содержат только атомы углерода в состоянии sp2-гибридизации
Решение
Ответ: 24
Задание №7
Выберите два утверждения, которые справедливы и для уксусной, и для метановой кислоты
1) жидкости с характерным запахом
2) вступают в реакцию «серебряного зеркала»
3) являются изомерами
4) при этерификации образуют простые эфиры
5) изменяют окраску лакмуса
Решение
Ответ: 15
Задание №8
Выберите два утверждения, которые справедливы и для пропановой, и для этановой кислот
1) плохо растворимы в воде
2) могут быть получены при окислении первичных спиртов
3) способны к полимеризации
4) в водном растворе являются слабыми электролитами
5) реагируют с раствором перманганата калия
Решение
Ответ: 24
Задание №9
Выберите два утверждения, которые справедливы и для олеиновой, и для стеариновой кислот
1) способны вступать в реакции полимеризации
2) обесцвечивают бромную воду
3) вступают в реакцию этерификации
4) реагируют с этиленгликолем
5) в водном растворе являются сильными электролитами
Решение
Ответ: 34
Задание №10
Выберите два утверждения, которые справедливы и для бензойной, и для уксусной кислот
1) жидкости с характерным запахом
2) являются гомологами метановой кислоты
3) являются одноосновными кислотами
4) образуют сложные эфиры с этанолом
5) для их распознавания можно использовать сульфат натрия
Решение
Ответ: 34
[adsp-pro-3]
Задание №11
Выберите два утверждения, которые справедливы и для глицерина, и для уксусной кислоты
1) являются жидкостями без запаха
2) реагируют с гидроксидом меди (II)
3) при их этерификации можно получить жир
4) являются электролитами
5) между молекулами есть водородные связи
Решение
Ответ: 25
Задание №12
Выберите два утверждения, которые справедливы и для ацетальдегида, и для муравьиной кислоты
1) вступают в реакцию серебряного зеркала
2) имеют запах
3) вступают в реакции этерификации
4) изменяют окраску индикаторов
5) плохо растворимы в воде
Решение
Ответ: 12
Задание №13
Из предложенного перечня реакций, выберите две таких, в которые может вступать муравьиная кислота
1) дегидрирование
2) гидролиз
3) изомеризация
4) окисления
5) нейтрализация
Решение
Ответ: 45
Задание №14
Из предложенного перечня реакций, выберите две таких, в которые может вступать уксусная кислота
1) гидрирование
2) гидрогалогенирование
3) галогенирование
4) полимеризация
5) этерификация
Решение
Ответ: 35
Задание №15
Из предложенного перечня выберите два вещества, которые являются гомологами уксусной кислоты
1) метановая
2) бензойная
3) масляная
4) олеиновая
5) щавелевая
Решение
Ответ: 13
Задание №16
Из предложенного перечня выберите два вещества, которые являются гомологами стеариновой кислоты
1) пальмитиновая
2) бензойная
3) пропановая
4) олеиновая
5) этандиовая
Решение
Ответ: 13
Задание №17
Из предложенного перечня выберите два вещества, которые являются структурными изомерами
1) бутаналь
2) бутановая кислота
3) пропаналь
4) метилпропионат
5) этанол
Решение
Ответ: 24
Задание №18
Из предложенного перечня выберите два вещества, которые являются структурными изомерами
1) метановая кислота
2) уксусная кислота
3) метилформиат
4) метилацетат
5) пропаналь
Решение
Ответ: 23
Задание №19
Из предложенного перечня выберите два вещества, которые являются структурными изомерами
1) изопропилацетат
2) бутилформиат
3) метановая кислота
4) бутановая кислота
5) пропилбутират
Решение
Ответ: 12
Задание №20
Из предложенного перечня соединений, выберите два вещества, которые между собой могут вступать в реакцию этерификации
1) этаналь и глицерин
2) этанол и метанол
3) глицерин и азотная кислота
4) уксусная кислота и фенол
5) уксусная кислота и этиленгликоль
Решение
Ответ: 35
[adsp-pro-3]
Задание №21
Из предложенного перечня соединений, выберите два вещества, которые между собой могут вступать в реакцию этерификации
1) метанол и метаналь
2) бутановая кислота и глицерин
3) стеариновая кислота и пропантриол-1,2,3
4) метанол и фенол
5) этаналь и олеиновая кислота
Решение
Ответ: 23
Задание №22
Из предложенного перечня соединений, выберите два вещества, которые между собой могут вступать в реакцию этерификации
1) пропеновая кислота и метанол
2) метаналь и фенол
3) глицерин и олеиновая кислота
4) фенол и соляная кислота
5) масляная кислота и пропаналь
Решение
Ответ: 13
Задание №23
Из предложенного перечня соединений, выберите два вещества, которые между собой могут вступать в реакцию этерификации
1) метилацетат и соляная кислота
2) пропаналь и уксусная кислота
3) фенолят натрия и хлорметан
4) гександиовая кислота и изопропиловый спирт
5) циклогексанол и уксусная кислота
Решение
Ответ: 45
Задание №24
Из предложенного перечня соединений, выберите два вещества, которые между собой могут вступать в реакцию этерификации
1) пропанон и этановая кислота
2) ацетат натрия и хлорэтан
3) глицерин и метанол
4) стеариновая кислота и пропанол-2
5) этиленгликоль и уксусная кислота
Решение
Ответ: 45
Задание №25
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию гидрогалогенирования.
1) пропин
2) уксусная кислота
3) пропеновая кислота
4) бензойная кислота
5) ацетальдегид
Решение
Ответ: 13
Задание №26
Из предложенного перечня соединений, выберите два вещества, которые обесцвечивают бромную воду
1) олеиновая кислота
2) гександиовая кислота
3) стирол
4) глицерин
5) толуол
Решение
Ответ: 13
Задание №27
Из предложенного перечня кислот, выберите две, которые обесцвечивают водный раствор брома
1) пальмитиновая
2) олеиновая
3) пропеновая
4) бутановая
5) уксусная
Решение
Ответ: 23
Задание №28
Из предложенного перечня соединений, выберите два вещества, которые обесцвечивают бромную воду
1) ацетальдегид
2) циклогексанол
3) этиленгликоль
4) бензол
5) 2-метилпропеновая кислота
Решение
Ответ: 15
Задание №29
Из предложенного перечня соединений, выберите два металла, которые могут вступать в реакцию c уксусной кислотой
1) медь
2) цинк
3) серебро
4) калий
5) ртуть
Решение
Ответ: 24
Задание №30
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом натрия
1) пропаналь
2) фенол
3) этандиовая кислота
4) этанол
5) стирол
Решение
Ответ: 23
[adsp-pro-3]
Задание №31
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с водным раствором гидроксида натрия
1) глицерин
2) пропен
3) уксусная кислота
4) бензол
5) хлорэтан
Решение
Ответ: 35
Задание №32
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом натрия
1) ацетат натрия
2) метаналь
3) пропеновая кислота
4) пропанол-1
5) диизопропиловый эфир
Решение
Ответ: 13
Задание №33
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с водным раствором гидроксида калия
1) этилацетат
2) этиленгликоль
3) этанол
4) бензойная кислота
5) пропанон
Решение
Ответ: 14
Задание №34
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с водородом.
1) метанол
2) циклогексан
3) метаналь
4) стеариновая кислота
5) олеиновая кислота
Решение
Ответ: 35
Задание №35
Из предложенного перечня соединений, выберите два вещества, которые могут гидролизоваться в водной среде
1) метилацетат
2) уксусная кислота
3) этанол
4) бензол
5) ацетат натрия
Решение
Ответ: 15
Задание №36
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом меди (II)
1) пропановая кислота
2) этанол
3) гексан
4) ацетальдегид
5) диметиловый эфир
Решение
Ответ: 14
Задание №37
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом меди (II)
1) пропанон
2) пропаналь
3) изопропиловый спирт
4) этилен
5) метановая кислота
Решение
Ответ: 25
Задание №38
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом меди (II)
1) пропен
2) глицерин
3) пропионовая кислота
4) стирол
5) изопрен
Решение
Ответ: 23
Задание №39
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с гидроксидом железа (II)
1) фенол
2) ацетат натрия
3) метановая кислота
4) щавелевая кислота
5) метилацетат
Решение
Ответ: 34
Задание №40
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с оксидом меди (II)
1) этаналь
2) бутадиен-1,3
3) формиат калия
4) уксусная кислота
5) этанол
Решение
Ответ: 45
[adsp-pro-3]
Задание №41
Из предложенного перечня соединений, выберите два вещества, которые могут вступать в реакцию с оксидом меди (II)
1) серная кислота
2) уксусная кислота
3) бутанон
4) пропаналь
5) метилат натрия
Решение
Ответ: 12
Задание №42
Из предложенного перечня соединений, выберите два вещества, с каждым из которых реагирует этановая кислота
1) вода
2) этанол
3) этаналь
4) сульфат меди (II)
5) оксид меди (II)
Решение
Ответ: 25
Задание №43
Из предложенного перечня, выберите две пары веществ, с каждым из которых реагирует муравьиная кислота
- 1. Ag, H2O
- 2. AgCl, H2
- 3. NaOH, Cu(OH)2
- 4. CH3C(O)CH3, NH3
- 5. Br2, NaHCO3
Решение
Ответ: 35
Задание №44
Из предложенного перечня соединений, выберите две пары веществ, с каждым из которых может реагировать бензойная кислота
- 1. HNO3, Cl2
- 2. O2, CH3OH
- 3. NaCl, KOH
- 4. H2, Cu
- 5. CH4, HCl
Решение
Ответ: 12
Задание №45
Из предложенного перечня соединений, выберите две пары веществ, с каждым из которых реагирует ацетат натрия
1) вода, этилен
2) сульфат меди (II), хлорэтан
3) гидроксид натрия, серная кислота
4) хлорид натрия, этанол
5) соляная кислота, хлорметан
Решение
Ответ: 35
Задание №46
Из предложенного перечня соединений, выберите два вещества, с каждым из которых реагирует стеариновая кислота
1) водород
2) глицерин
3) хлороводород
4) этиленгликоль
5) углерод
Решение
Ответ: 24
Задание №47
Из предложенного перечня соединений, выберите два вещества, с каждым из которых реагирует олеиновая кислота
1) водород
2) кремниевая кислота
3) хлорид железа (II)
4) этанол
5) хлорид железа (III)
Решение
Ответ: 14
Задание №48
Из предложенного перечня соединений, выберите два вещества, которые при растворении в воде дают щелочную среду
1) ацетат натрия
2) этанол
3) метилат натрия
4) метановая кислота
5) метилформиат
Решение
Ответ: 13
Задание №49
Из предложенного перечня соединений, выберите два вещества, водные растворы которых имеют щелочную среду
1) фенолят калия
2) глицерин
3) фенол
4) бензойная кислота
5) формиат калия
Решение
Ответ: 15
Задание №50
Из предложенного перечня соединений, выберите два вещества, водные растворы которых могут изменять окраску индикаторов
1) метанол
2) пропанон
3) пропионат бария
4) хлоруксусная кислота
5) бензол
Решение
Ответ: 34
[adsp-pro-3]
Задание №51
Из предложенного перечня, выберите две реакции, которые являются окислительно-восстановительными
1) CH3COOH + NaOH → CH3COONa + H2O
2) 2CH3COOH + 2Na → 2CH3COONa + H2
3) CH3COONa + HCl → CH3COOH + NaCl
4) CH3COOH + CH3OH ⇆ CH3COOCH3 + H2O
5) CH3COOH + Cl2 → ClCH2COOH + HCl
Решение
Ответ: 25
Задание №52
Из предложенного перечня, выберите две реакции, которые не являются реакциями обмена
1) HCOOK + H3PO4(конц.) → HCOOH + KH2PO4
2) HCOOH + 4[Ag(NH3)2]OH → (NH4)2CO3 + 4Ag + 6NH3 + 3H2O
3) CH3COOH + NaHCO3 → CH3COONa + H2O + CO2
4) CH3COOH + NH3 → CH3COONH4
5) 2CH3COOH + Ca(OH)2 → (CH3COO)2Ca + 2H2O
Решение
Ответ: 24
Задание №53
Из предложенного перечня соединений, выберите два вещества, с которыми могут вступать в реакцию как уксусная кислота, так и этанол
1) метанол
2) водород
3) натрий
4) углекислый газ
5) медь
Решение
Ответ: 13
Задание №54
Из предложенного перечня соединений, выберите два вещества, с которыми могут вступать в реакцию как муравьиная кислота, так и метанол
1) оксид меди (II)
2) аммиачный раствор оксида серебра
3) гидроксид натрия
4) хлороводород
5) этанол
Решение
Ответ: 15
Задание №55
Из предложенного перечня соединений, выберите два вещества, с которыми могут вступать в реакцию как стеариновая, так и пальмитиновая кислоты
1) глицерин
2) водород
3) бром
4) медь
5) хлороводород
Решение
Ответ: 13
Задание №56
Из предложенного перечня соединений, выберите два вещества, с которыми могут вступать в реакцию как фенол, так и бензойная кислота
1) соляная кислота
2) азотная кислота
3) гидроксид натрия
4) сульфат натрия
5) хлорид железа (III)
Решение
Ответ: 23
Задание №57
Из предложенного перечня соединений, выберите два вещества, с которыми могут вступать в реакцию как бензойная, так и олеиновая кислота
1) пропанол-1
2) бромоводород
3) водород
4) бромная вода
5) фенол
Решение
Ответ: 13
Задание №58
Из предложенного перечня взаимодействий выберите два таких, в результате которых возможно образование муравьиной кислоты
1) CH3OH + CuO
2) CH4 + O2
3) HCOONa + HCl
4) HCOOCH3 + KOH
5) HCHO + [Ag(NH3)2]OH
Решение
Ответ: 23
Задание №59
Из предложенного перечня реакций выберите две такие, в результате которых образуется уксусная кислота
1) сплавление ацетата натрия с гидроксидом натрия
2) окисление этилового спирта
3) окисление бутана кислородом воздуха
4) гидрирование этаналя
5) окисление этилена подкисленным раствором перманганата калия
Решение
Ответ: 23
Задание №60
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получена бутановая кислота
1) термическое разложение бутаноата бария
2) электролиз водного раствора пропаноата калия
3) сплавление пропионата натрия с гидроксидом калия
4) взаимодействие бутирата натрия с соляной кислотой
5) окисление бутаналя
Решение
Ответ: 45
[adsp-pro-3]
Задание №61
Из предложенного перечня реакций выберите две такие, в результате которых может быть получена уксусная кислота
1) окисление этилена водным раствором перманганата калия
2) окисление этанола оксидом меди (II)
3) гидратация ацетилена
4) окисление этанола подкисленным раствором перманганата калия
5) окисление этаналя гидроксидом меди (II)
Решение
Ответ: 45
Задание №62
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получена стеариновая кислота
1) гидролиз жиров
2) брожение глюкозы
3) гидрирование олеиновой кислоты
4) крекинг октана
5) окисление бутана кислородом
Решение
Ответ: 13
Задание №63
Из предложенного перечня реакций выберите две такие, в результате которых может быть получена муравьиная кислота
1) каталитическое окисление метана кислородом
2) кислотный гидролиз метилформиата
3) окисление метаналя аммиачным раствором оксида серебра
4) окисление формальдегида подкисленным раствором перманганата калия
5) гидрирование муравьиного альдегида
Решение
Ответ: 12
Задание №64
Из предложенного перечня реакций выберите две такие, с помощью которых может быть получена уксусная кислота
1) CH≡C-CH2-CH3 + KMnO4 + H2SO4
2) CH3-CH=CH-CH3 + KMnO4 + H2SO4
3) HC≡CH+KMnO4 + H2SO4
4) CH3-CH=CH-CH2-CH3 + KMnO4 + H2SO4
5) CH2=C(CH3)-CH3 + KMnO4 + H2SO4
Решение
Ответ: 24
Задание №65
Из предложенного перечня реакций выберите две такие, при протекании которых образуется уксусная кислота
1) CH3-CHO + KMnO4 + H2SO4
2) С2H5OH + CuO
3) CH3-C≡C-CH3 + KMnO4 + H2SO4
4) CH3-CHO + [Ag(NH3)2]OH
5) HC≡CH + KMnO4 + H2SO4
Решение
Ответ: 13
Задание №66
Из предложенного перечня взаимодействий выберите два таких, в результате которых возможно образование бензойной кислоты
1) C6H5-CHO + KMnO4 + H2SO4
2) C6H5-CCl3 + NaOH(изб.)
3) C6H5-CHO + KMnO4 + KOH
4) C6H5-CH3 + KMnO4 + H2SO4
5) C6H5-CHO + H2
Решение
Ответ: 14
Задание №67
Из предложенного перечня реакций выберите две такие, при протекании которых образуется бензоат калия
1) C6H5-CH2CH3 + KMnO4 + KOH
2) C6H5-CCl3 + KOH(изб.)
3) C6H5-CHCl2 + KOH
4) C6H5-CH(CH3)2 + KMnO4 + H2SO4
5) C6H11CH3 + KMnO4 + H2SO4
Решение
Ответ: 12
Задание №68
Из предложенного перечня веществ, выберите два таких, которые при реакции с избытком водного раствора гидроксида натрия в качестве конечного продукта образуют соль.
1) хлорэтан
2) 1,1-дихлоэтан
3) этандиовая кислота
4) 1,1,1-трихлорэтан
5) 1,2-дихлорэтан
Решение
Ответ: 34
Задание №69
Из предложенного перечня веществ, выберите два таких, которые при реакции с избытком водного раствора гидроксида натрия в качестве конечного продукта не образуют соль.
1) бензойная кислота
2) хлорметан
3) 2,2-дихлорпропан
4) этандиовая кислота
5) 1,1,1-трихлорэтан
Решение
Ответ: 23
Задание №70
Установите соответствие между формулами веществ и реагентом, с помощью которого их можно различить: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ФОРМУЛЫ ВЕЩЕСТВ | РЕАКТИВ |
|
А) CH3COOH и CH3C(O)СН3 Б) CH3COOH и CH3CН2OH В) CH3CНO и CH3CН2OH |
1) сода 2) HBr 3) FeCl3 4) [Ag(NH3)2]OH 5) H2O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 114
[adsp-pro-3]
Задание №71
Установите соответствие между формулой вещества и реагентом, который используют для его определения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ФОРМУЛЫ ВЕЩЕСТВ | РЕАКТИВ |
|
А) CH3COOH Б) CH3OH В) HC≡CH |
1) [Ag(NH3)2]OH 2) CuO 3) FeCl3 4) NaHCO3 5) H2O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 421
Задание №72
Установите соответствие между формулами веществ и реагентом, применяющимся для обнаружения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛЫ ВЕЩЕСТВ | РЕАКТИВ |
|
А) CH3CНO Б) H2CO В) C2H5COOH |
1) фенолфталеин 2) HBr 3) FeCl3 4) сода 5) Ag2O в NH3(р-р) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 554
Задание №73
Установите соответствие между реагирующими веществами и признаком реакции, протекающей между ними: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРИЗНАК РЕАКЦИИ |
|
А) CH3COOH + NaHCO3 Б) CH3COOH + Cu(OH)2 В) CH3CНO + [Ag(NH3)2]OH |
1) выделение газа с неприятным запахом 2) выпадение черного осадка 3) выпадение кирпично–красного осадка 4) выделение газа без запаха 5) растворение осадка |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 452
Задание №74
Установите соответствие между исходными веществами и продуктом, который образуется в результате реакции между ними: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТ РЕАКЦИИ |
|
А) HCOOH + [Ag(NH3)2]OH Б) HCOOH + KMnO4 + H2SO4 В) HCOOH + CH3OH |
1) ацетат серебра 2) карбонат аммония 3) оксид углерода (IV) 4) метилацетат 5) метилформиат |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 235
Задание №75
Установите соответствие между исходными веществами и продуктом, который образуется в результате их сплавления с гидроксидом натрия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТ РЕАКЦИИ |
|
А) CH3COONa + NaOH(cплавл.) Б) NaOOC-CH2-CH2-COONa + 2NaOH(cплавл.) В) C6H5COONa + NaOH(cплавл.) |
1) бензол 2) этан 3) пропан 4) бутан 5) метан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 521
Задание №76
Установите соответствие между исходными веществами и продуктом, который образуется в результате реакции между ними: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТ РЕАКЦИИ |
|
А) CH3COOH + X → CH3COONa + CO2 + H2O Б) CH3COOH + X → CH3COONa + H2 В) CH3COOH + X → CH3COOCH3 + H2O |
1) Ba 2) Na2CO3 3) Na 4) BaCO3 5) CH4O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 235
Задание №77
Установите соответствие между формулой алкена и продуктом, который образуется при его окислении. К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ |
|
А) пропилен + KMnO4 + H2SO4 Б) бутен-1 + KMnO4 + H2SO4 В) бутен-2 + KMnO4 + H2SO4 |
1) пропаналь 2) пропионовая и уксусная кислоты 3) пропановая кислота и оксид углерода (IV) 4) уксусная кислота и углекислый газ 5) уксусная кислота |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 435
[adsp-pro-3]
Задания с развернутым ответом на карбоновые кислоты и сложные эфиры.
Задание №1
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
HCOOH X1
CH4O
X2
X3
X4
X5
X6
Решение
Задание №2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
CH3COOK X1
X2
X3
X4
X5
X6
X7
Решение
Задание №3
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
хлорэтан н-бутан
C2H4O2
бензилацетат
ацетат кальция
ацетон
Решение
Задание №4
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
угарный газ формиат калия
метановая кислота
X
Решение
Задание №5
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения
этилен ацетальдегид
X1
метилацетат
X2
X3
Решение
[adsp-pro-3]
Задание №6
Навеску неизвестного соединения массой 5,8 г сожгли в избытке кислорода и получили 13,2 г углекислого газа и равное количество вещества воды. Определите молекулярную формулу данного соединения и его структуру, если известно, что оно реагирует с марганцем, а его молекула содержит два третичных атома углерода.
Решение
n(CO2) = m(CO2)/M(CO2) = 13,2/44 = 0,3 моль, следовательно:
n(C) = n(CO2) = 0,3 моль => m(C) = n(C)⋅M(C) = 0,3⋅12 = 3,6 г,
Исходя из условия:
n(H2O) = n(CO2) = 0,3 моль, следовательно:
n(H) = 2n(H2O) = 2⋅0,3 = 0,6 моль,
m(H) = n(H)⋅M(H) = 0,6⋅1 = 0,6 г,
m(O) = m(в-ва) — m(H) — m(C) = 5,8 — 0,6 — 3,6 = 1,6 г,
n(O) = m(O)/M(O) = 1,6/16 = 0,1 моль,
n(C):n(H):n(O) = 0,3:0,6:0,1 = 3:6:1
Таким образом, простейшая формула искомого органического соединения C3H6O
Поскольку ни одно вещество с такой истинной молекулярной формулой не может содержать два третичных атома углерода в молекуле, то, очевидно, простейшую формулу, как минимум, нужно удвоить. В случае удвоения простейшей формулы получаем C6H12O2.
Искомым веществом с такой молекулярной формулой может быть 2,3-диметилбутановая кислота:
Задание №7
Навеску неизвестного органического соединения массой 16,7 г сожгли в избытке кислорода и получили 30,8 г углекислого газа, 4,5 г воды и 1,12 л азота. Определите молекулярную формулу данного соединения и его структуру, если известно, что оно может быть получено взаимодействием ароматического соединения с нитрующей смесью.
Решение
n(CO2) = m(CO2)/M(CO2) = 30,8/44 = 0,7 моль,
n(C) = n(CO2) = 0,7 моль, m(C) = M(C)⋅n(C) = 12⋅0,7 = 8,4 г,
n(H2O) = m(H2O)/M(H2O) = 4,5/18 = 0,25 моль,
n(H) = 2n(H2O) = 2⋅0,25 = 0,5 моль,
m(H) = n(H)⋅M(H) = 0,5⋅1 = 0,5 г,
n(N2) = V(N2)/Vm = 1,12/22,4 = 0,05 моль,
n(N) = 2n(N2) = 2⋅0,05 = 0,1 моль,
m(N) = n(N)⋅M(N) = 0,1⋅14 = 1,4 г,
vm(O) = m(в-ва) – m(H) – m(N) – m(C) = 16,7 – 0,5 – 1,4 – 8,4 = 6,4 г,
n(O) = m(O)/M(O) = 6,4/16 = 0,4 моль,
n(C):n(H):n(N):n(O) = 0,7:0,5:0,1:0,4 = 7:5:1:4
Исходя из условий можно сделать вывод о том, что искомым соединением может являться м-нитробензойная кислота, молекулярная формула которой C7H5NO4, а структурная:
Задание №8
При сжигании навески неизвестного органического вещества массой 1,5 г образовалось 2,016 л углекислого газа и 900 мг воды. Определите молекулярную формулу вещества и его структуру, если известно, что оно гидролизуется в кислой среде с образованием продукта с формулой C7H8O, а при щелочном гидролизе образуется только одна соль.
Решение
n(CO2) = V/Vm = 2,016/22,4 = 0,09 моль,
n(C) = n(CO2) = 0,09 моль,
m(C) = n(C)⋅M(C) = 0,09⋅12 = 1,08 г,
n(H2O) = m(H2O)/M(H2O) = 0,9/18 = 0,05 моль,
n(H) = 2n(H2O) = 2⋅0,05 = 0,1 моль,
m(H) = n(H)⋅M(H) = 0,1⋅1 = 0,1 г,
m(O) = m(в-ва) – m(H) – m(С) = 1,5 – 0,1 – 1,08 = 0,32 г,
n(O) = m(O)/M(O) = 0,32/16 = 0,02 моль,
n(C):n(H):n(O) = 0,09:0,1:0,02 = 4,5:5:1 = 9:10:2
Таким образом, простейшая формула искомого соединения C9H10O2
Предположим, что она также является и истинной молекулярной. В таком случае решением может являться бензилацетат:
Задание №9
Навеску неизвестного органического соединения массой 11,8 г сожгли в избытке кислорода. В результате образовалось 17,6 г углекислого газа и 5,4 г паров воды. Определите молекулярную формулу данного соединения и установите его строение, если известно, что оно гидролизуется в кислой среде с образованием двух продуктов, один из которых вступает в реакцию серебряного зеркала, а другой может быть получен в одну стадию из этилена.
Решение
n(CO2) = m(CO2)/M(CO2) = 17,6/44 = 0,4 моль,
n(C) = n(CO2) = 0,4 моль, m(C) = M(C)⋅n(C) = 12⋅0,4 = 4,8 г,
n(H2O) = m(H2O)/M(H2O) = 5,4/18 = 0,3 моль,
n(H) = 2n(H2O) = 2⋅0,3 = 0,6 моль,
m(H) = n(H)⋅M(H) = 0,6⋅1 = 0,6 г,
m(O) = m(в-ва) – m(H) – m(C) = 11,8 – 0,6 – 4,8 = 6,4 г,
n(O) = m(O)/M(O) = 6,4/16 = 0,4 моль,
n(C):n(H):n(O) = 0,4:0,6: 0,4 = 1:1,5:1 = 2:3:2
Таким образом, простейшая формула искомого органического соединения C2H3O2
Органические соединения, в состав которых входят только углерод, водород и кислород, не могут иметь в составе молекул нечетное число атомов водорода.
В связи с этим, рассчитанную простейшую формулу нужно увеличить в четное число раз.
При удвоении простейшей формулы мы получаем C4H6O4
Исходя из условия о способности искомого органического вещества легко предположить, что оно относится к классу сложных эфиров.
Один из продуктов гидролиза может быть получен в одну стадию из этиленгликоля. По всей видимости, это этиленгликоль, а искомое вещество представляет собой диформиат этиленгликоля со структурной формулой:
[adsp-pro-10]
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций используйте структурные формулы органических веществ.
8
Решение
Авторизуйтесь на сайте, чтобы пройти тест.
Следующий вопрос →
Объяснение понятно.
изменить
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
Видео с разбором теста
Версия для печати
Решаемость этого задания 80%
Карбоновые кислоты — класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп
COOH.
Имеют разнообразное промышленное применение и большое биологическое значение.
Общая формула одноосновных карбоновых кислот CnH2nO2 .
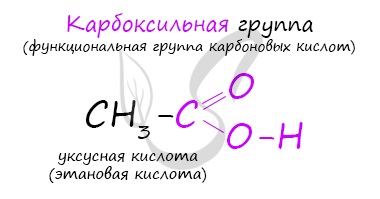
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные — 1 карбоксильная группа
- Двухосновные — 2 карбоксильных группы
- Трехосновные — 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав
которых они входят.
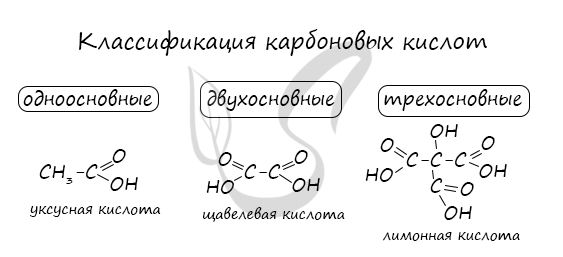
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода
и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая — HCOOH — муравьиная кислота
- Этановая — CH3-COOH — уксусная кислота
- Пропановая — C2H5-COOH — пропионовая кислота
- Бутановая — C3H7-COOH — масляная кислота
- Пентановая — C4H9-COOH — валериановая кислота
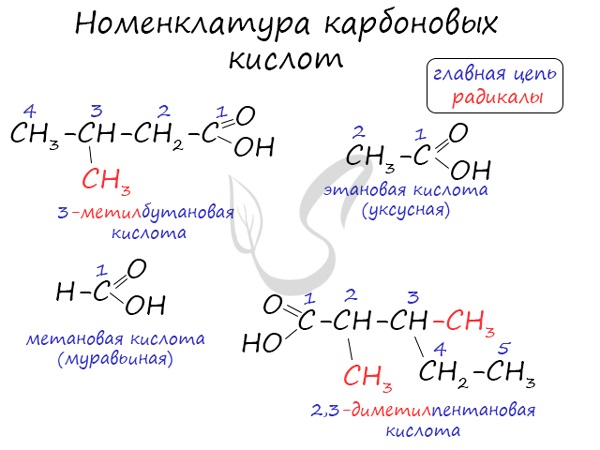
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными
эфирами.
Получение карбоновых кислот
- Окисление алканов
- Окисление спиртов
- Окисление альдегидов
- Синтез муравьиной кислоты
- Синтез уксусной кислоты
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого
образуются кислоты.
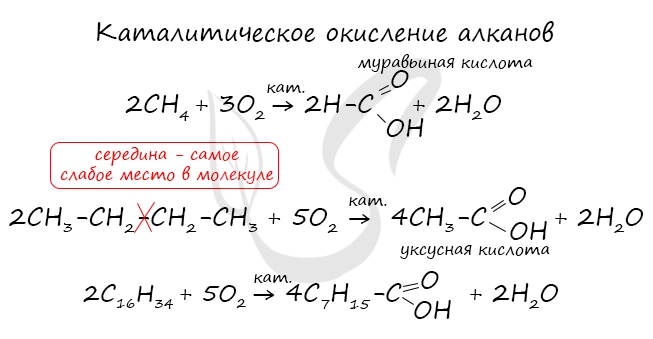
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются
до соответствующих кислот.
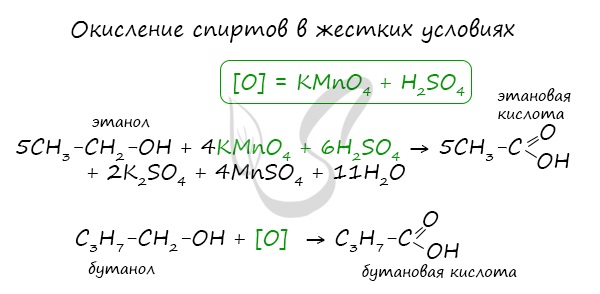
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией
на альдегиды — реакцией серебряного зеркала.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.

Окисление альдегидов также может быть успешно осуществлено другим реагентом — свежеосажденным гидроксидом меди II.
В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.

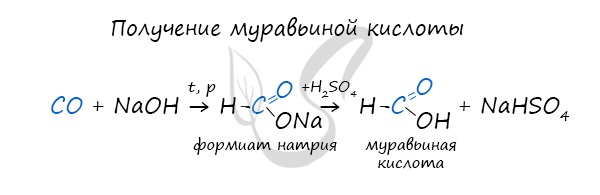
Существует специфический способ получения муравьиной кислоты, который заключается в реакции твердого гидроксида щелочного металла с угарным газом под давлением и температуре 200°С — образуется формиат (соль муравьиной кислоты).
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
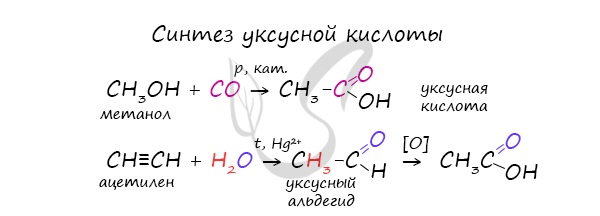
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид.
Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем
спирты.
- Кислотные свойства
- Галогенирование
- Особые свойства муравьиной кислоты
- Разложение муравьиной кислоты
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений
металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.

Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко
замещается водород у третичного, чуть сложнее — у вторичного, и значительно сложнее — у первичного атома углерода.

Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе.
Поэтому самая слабая из трех кислот — уксусная, чуть сильнее — хлоруксусная, за ней — дихлоруксусная и самая сильная —
трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это
перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.

Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот,
способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.

При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
HCOOH → (t, H2SO4) CO↑ + H2O
Сложные эфиры
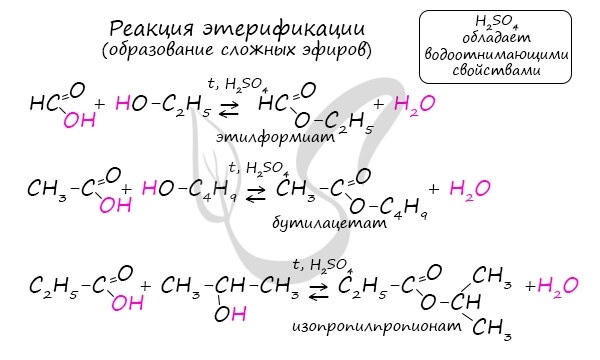
Получение сложных эфиров происходит в реакции этерификации (лат. aether — эфир), заключающейся во взаимодействии карбоновой кислоты
и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислота + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
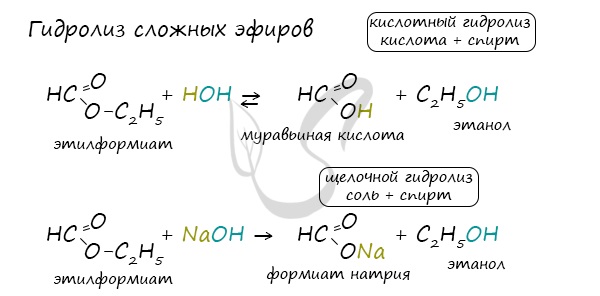
Для сложных эфиров характерной реакцией является гидролиз — их разложение. Возможен щелочной гидролиз, при котором образуется соль
кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной — необратимо.
Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
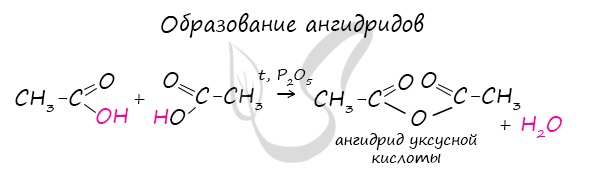
Ангидриды
Ангидриды — химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
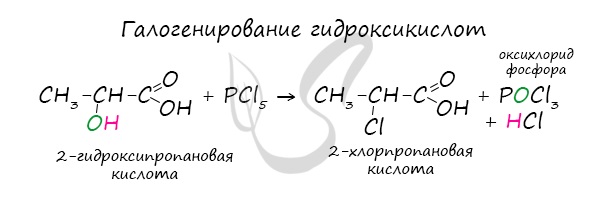
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.

Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания.
Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
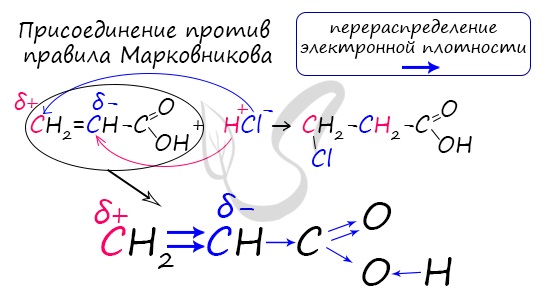
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит
в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Карбоновые кислоты – это вещества, в молекулах которых содержится одна или несколько карбоксильных групп СООН.
Общая формула предельных одноосновных карбоновых кислот: СnH2nO2
Строение, изомерия и гомологический ряд карбоновых кислот
Химические свойства карбоновых кислот
Способы получения карбоновых кислот
Классификация карбоновых кислот
По числу карбоксильных групп:
- одноосновные карбоновые кислоты — содержат одну карбоксильную группу -СООН. Общая формула CnH2n+1COOH или CnH2nO2.
Например, уксусная кислота
- многоосновные карбоновые кислоты — содержат две и более карбоксильные группы СООН. Например, общая формула двухосновных карбоновых кислот CnH2n(СОOH)2 или CnH2n-2O4.
Например, щавелевая кислота
Классификация по строению углеводородного радикала
- Предельные карбоновые кислоты – карбоксильная группа СООН соединена с предельным радикалом. Например, этановая кислота СН3–СООН.
- Непредельные карбоновые кислоты – карбоксильная группа СООН соединена с непредельным радикалом. Например, акриловая кислота: СН2=СН–СООН.
- Ароматические кислоты — карбоксильная группа СООН соединена с непредельным радикалом. Например, бензойная кислота: С6Н5СООН.
- Циклические кислоты — карбоксильная группа СООН соединена с углеводородным циклом. Например, циклопропанкарбоновая кислота: С3Н5СООН.
Строение карбоновых кислот
Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга.
Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4).
Электронная плотность смещена к более электроотрицательному атому кислорода.
Атом углерода карбоксильной группы находится в состоянии sp2-гибридизации, образует три σ-связи и одну π-связь.
Водородные связи и физические свойства карбоновых кислот
В жидком состоянии и в растворах молекулы карбоновых кислот образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул карбоновых кислот.
Молекулы карбоновых кислот с помощью водородных связей соединены в димеры.
Это приводит к увеличению растворимости в воде и высоким температурам кипения низших карбоновых кислот.
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Номенклатура карбоновых кислот
Предельные одноосновные карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Муравьиная | Метановая | Формиат (метаноат) | HCOOH |
| Уксусная | Этановая | Ацетат (этаноат) | CH3COOH |
| Пропионовая | Пропановая | Пропионат (пропаноат) | CH3CH2COOH |
| Масляная | Бутановая | Бутират (бутаноат) | CH3(CH2)2COOH |
| Валериановая | Пентановая | Пентаноат | CH3(CH2)3COOH |
| Капроновая | Гексановая | Гексаноат | CH3(CH2)4COOH |
| Пальмитиновая | Гексадекановая | Пальмитат | С15Н31СООН |
| Стеариновая | Октадекановая | Стеарат | С17Н35СООН |
Таблица. Непредельные одноосновные карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Акриловая | Пропеновая | Акрилат | CH2=CH–COOH |
| Метакриловая | 2-Метилпропеновая | Метакрилат | CH2=C(СH3)–COOH |
| Кротоновая | транс-2-Бутеновая | Кротонат | СН3 -CH=CH–COOH |
| Олеиновая | 9- цис-Октадеценовая | Олеат | СН3(СН2)7СН=СН(СН2)7СООН |
| Линолевая | 9,12-цис-Октадекадиеновая | Линолеат | СН3(СН2)4(СН=СНСН2)2(СН2)6СООН |
| Линоленовая | 9,12,15-цис-Октадекатриеновая | Линоленоат | СН3СН2(СН=СНСН2)3(СН2)6СООН |
Таблица. Двухосновные карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Щавелевая | Этандиовая | Оксалат | НООС – COOH |
| Малоновая | Пропандиовая | Малонат | НООС-СН2-СООН |
| Янтарная | Бутандиовая | Сукцинат | НООС-(СН2)2-СООН |
| Глутаровая | Пентандиовая | Глутарат | НООС-(СН2)3-СООН |
| Адипиновая | Гександиовая | Адипинат | НООС-(СН2)4-СООН |
| Малеиновая | цис-Бутендиовая | Малеинат | цис-НООССН=СНСООН |
| Фумаровая | транс-Бутендиовая | Фумарат | транс-НООССН=СНСООН |
Таблица. Ароматические карбоновые кислоты.
| Тривиальное название | Систематическое название | Название соли и эфира | Формула кислоты |
| Бензойная | Фенилкарбоновая | Бензоат |  |
| Фталевая | Бензол-1,2-дикарбоновая кислота | Фталат |  |
| Изофталевая | Бензол-1,3-дикарбоновая кислота | Изофталат |  |
| Терефталевая | Бензол-1,4-дикарбоновая кислота | Терефталат |  |
Изомерия предельных карбоновых кислот
Структурная изомерия
Для предельных карбоновых кислот характерна структурная изомерия – изомерия углеродного скелета и межклассовая изомерия.
Структурные изомеры – это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета характерна для карбоновых кислот, которые содержат не менее четырех атомов углерода.
Например. Формуле С4Н8О2 соответствуют бутановая и 2-метилпропановая кислота
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Карбоновые кислоты изомерны сложным эфирам. Общая формула и предельных одноосновных карбоновых кислот, и сложных эфиров — CnH2nО2.
Например. Межклассовые изомеры с общей формулой С2Н4О2: уксусная кислота СН3–CОOH и метилформиат H–COOCH3
| Уксусная кислота | Метиловый эфир муравьиной кислоты |
| СН3–CОOH | HCOOCH3 |
Общую формулу СnH2nO2 могут также иметь многие другие полифункциональные соединения, например: альдегидоспирты, непредельные диолы, циклические простые диэфиры и т.п.
Химические свойства карбоновых кислот
.
- кислотные свойства, замещение водорода на металл;
- замещение группы ОН
- замещение атома водорода в алкильном радикале
- образование сложных эфиров — этерификация
1. Кислотные свойства
Кислотные свойства карбоновых кислот возникают из-за смещения электронной плотности к карбонильному атому кислорода и вызванной этим дополнительной (по сравнению со спиртами и фенолами) поляризацией связи О–Н.
В водном растворе карбоновые кислоты частично диссоциируют на ионы:
R–COOH ⇆ R-COO– + H+
1.1. Взаимодействие с основаниями
Карбоновые кислоты реагируют с большинством оснований. При взаимодействии карбоновых кислот с основаниями образуются соли карбоновых кислот и вода.
CH3COOH + NaOH = CH3COONa + H2O
Карбоновые кислоты реагируют с щелочами, амфотерными гидроксидами, водным раствором аммиака и нерастворимыми основаниями.
Например, уксусная кислота растворяет осадок гидроксида меди (II)
Видеоопыт взаимодействия уксусной кислоты с гидроксидом натрия можно посмотреть здесь.
Например, уксусная кислота реагирует с водным раствором аммиака с образованием ацетата аммония
CH3COOH + NH3 = CH3COONH4
1.2. Взаимодействие с металлами
Карбоновые кислоты реагируют с активными металлами. При взаимодействии карбоновых кислот с металлами образуются соли карбоновых кислот и водород.
Например, уксусная кислота взаимодействует с кальцием с образованием ацетата кальция и водорода.
Видеоопыт взаимодействия уксусной кислоты с магнием и цинком можно посмотреть здесь.
1.3. Взаимодействие с основными оксидами
Карбоновые кислоты реагируют с основными оксидами с образованием солей карбоновых кислот и воды.
Например, уксусная кислота взаимодействует с оксидом бария с образованием ацетата бария и воды.
Например, уксусная кислота реагирует с оксидом меди (II)
2СН3СООН + CuO = H2О + ( CH3COO)2 Cu
Видеоопыт взаимодействия уксусной кислоты с оксидом меди (II) можно посмотреть здесь.
1.4. Взаимодействие с с солями более слабых и летучих (или нерастворимых) кислот
Карбоновые кислоты реагируют с солями более слабых, нерастворимых и летучих кислот.
Например, уксусная кислота растворяет карбонат кальция
Качественная реакция на карбоновые кислоты: взаимодействие с содой (гидрокарбонатом натрия) или другими гидрокарбонатами. В результате наблюдается выделение углекислого газа
2. Реакции замещения группы ОН
Для карбоновых кислот характерны реакции нуклеофильного замещения группы ОН с образованием функциональных производных карбоновых кислот: сложных эфиров, амидов, ангидридов и галогенангидридов.
2.1. Образование галогенангидридов
Под действием галогенагидридов минеральных кислот-гидроксидов (пента- или трихлорид фосфора) происходит замещение группы ОН на галоген.
Например, уксусная кислота реагирует с пентахлоридом фосфора с образованием хлорангидрида уксусной кислоты
2.2. Взаимодействие с аммиаком
При взаимодействии аммиака с карбоновыми кислотами образуются соли аммония:
При нагревании карбоновые соли аммония разлагаются на амид и воду:
2.3. Этерификация (образование сложных эфиров)
Карбоновые кислоты вступают в реакции с одноатомными и многоатомными спиртами с образованием сложных эфиров.
Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты):
При этом фенол не вступает в реакцию этерификации с карбоновыми кислотами. Сложные эфиры фенола получают косвенными способами.
2.4. Получение ангидридов
С помощью оксида фосфора (V) можно дегидратировать (то есть отщепить воду) карбоновую кислоту – в результате образуется ангидрид карбоновой кислоты.
Например, при дегидратации уксусной кислоты под действием оксида фосфора образуется ангидрид уксусной кислоты
3. Замещение атома водорода при атоме углерода, ближайшем к карбоксильной группе
Карбоксильная группа вызывает дополнительную поляризацию связи С–Н у соседнего с карбоксильной группой атома углерода (α-положение). Поэтому атом водорода в α-положении легче вступает в реакции замещения по углеводородному радикалу.
В присутствии красного фосфора карбоновые кислоты реагируют с галогенами.
Например, уксусная кислота реагирует с бромом в присутствии красного фосфора
4. Свойства муравьиной кислоты
Особенности свойств муравьиной кислоты обусловлены ее строением, она содержит не только карбоксильную, но и альдегидную группу и проявляет все свойства альдегидов.
4.1. Окисление аммиачным раствором оксида серебра (I) и гидроксидом меди (II)
Как и альдегиды, муравьиная кислота окисляется аммиачным раствором оксида серебра. При этом образуется осадок из металлического серебра.
При окислении муравьиной кислоты гидроксидом меди (II) образуется осадок оксида меди (I):
4.2. Окисление хлором, бромом и азотной кислотой
Муравьиная кислота окисляется хлором до углекислого газа.
4.3. Окисление перманганатом калия
Муравьиная кислота окисляется перманганатом калия до углекислого газа:
5HCOOH + 2KMnO4 + 3H2SO4 → 5CO2 + 2MnSO4 + K2SO4 + 8H2O
Видеоопыт взаимодействия муравьиной кислоты с перманганатом калия можно посмотреть здесь.
4.4. Разложение при нагревании
При нагревании под действием серной кислоты муравьиная кислота разлагается с образованием угарного газа:
Видеоопыт разложения муравьиной кислоты можно посмотреть здесь
5. Особенности бензойной кислоты
5.1. Разложение при нагревании
При нагревании бензойная кислота разлагается на бензол и углекислый газ:
5.2. Реакции замещения в бензольном кольце
Карбоксильная группа является электроноакцепторной группой, она уменьшает электронную плотность бензольного кольца и является мета-ориентантом.
6. Особенности щавелевой кислоты
6.1. Разложение при нагревании
При нагревании щавелевая кислота разлагается на угарный газ и углекислый газ:
6.2. Окисление перманганатом калия
Щавелевая кислота окисляется перманганатом калия до углекислого газа:
7. Особенности непредельных кислот (акриловой и олеиновой)
7.1. Реакции присоединения
Присоединение воды и бромоводорода к акриловой кислоте происходит против правила Марковникова, т.к. карбоксильная группа является электроноакцепторной:
К непредельным кислотам можно присоединять галогены и водород. Например, олеиновая кислота присоединяет водород:
7.2. Окисление непредельных карбоновых кислот
Непредельные кислоты обесцвечивают водный раствор перманганатов. При этом окисляется π-связь и у атомов углерода при двойной связи образуются две гидроксогруппы:
Получение карбоновых кислот
1. Окисление спиртов, алкенов и алкинов
При окислении спиртов, алкенов, алкинов и некоторых других соединений подкисленным раствором перманганата калия образуются карбоновые кислоты.
Например, при окислении этанола в жестких условиях образуется уксусная кислота
2. Окисление альдегидов
Альдегиды реагируют с раствором перманганата или дихромата калия в кислой среде при нагревании, а также с гидроксидом меди при нагревании.
Например, при окислении уксусного альдегида перманганатом калия в серной кислоте образуется уксусная кислота.
Например, при окислении альдегидов гидроксидом меди (II) также образуются карбоновые кислоты
3. Щелочной гидролиз тригалогенидов
Тригалогеналканы, в которых три атома галогена расположены у одного атома углерода, с избытком щелочи образуется соль кислоты. При этом сначала происходит замещение галогенов на группы ОН.
Образуется неустойчивое вещество, которое распадается с отщеплением воды:
Так как щелочь в избытке, то образуется не сама кислота, а её соль:
4. Получение карбоновых кислот из солей
Карбоновые кислоты можно получить из солей действием минеральной кислоты на раствор соли:
Например, муравьиную кислоту можно получить, подействовав на формиат натрия раствором серной кислоты:
5. Гидролиз сложных эфиров
Сложные эфиры подвергаются гидролизу в кислой среде при нагревании:
Например, метилацетат гидролизуется в кислой среде:
6. Кислотный гидролиз жиров
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин
7. Получение муравьиной кислоты из угарного газа
Соль муравьиной кислоты получают нагреванием оксида углерода (II) с твёрдым гидроксидом натрия под давлением:
8. Каталитическое окисление бутана
Уксусную кислоту в промышленности получают каталитическим окислением бутана:
9. Получение бензойной кислоты
Бензойную кислоту получают окислением гомологов бензола раствором перманганата калия в кислой среде.
Например, при окислении толуола образуется бензойная кислота:
10. Взаимодействие реактива Гриньяра с углекислым газом
При взаимодействии реактивов Гриньяра (алкилгалогенидов магния) с углекислым газом и последующем гидролизе образовавшегося промежуточного продукта образуется карбоновая кислота.
Органические кислоты
.
Теоретическое введение
Карбоновые кислоты – производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на карбоксильную группу
Особенности химических свойств карбоновых кислот обусловлены сильным взаимным влиянием карбонильной и гидроксильной групп.
Поэтому все химические реакции карбоновых кислот будут идти по следующим направлениям:
- замещение водорода в гидроксильной группе. Карбоновые кислоты – слабые электролиты и взаимодействуют с активными металлами, оксидами и гидроксидами металлов с образованием солей:
2CH3COOH + Mg → Mg(CH3COO)2 + H2;
уксусная кислота ацетат магния
C2H5COOH + NaOH → C2H5COONa + H2O.
пропионовая кислота пропионат натрия
- Замещение всей гидроксильной группы. Карбоновые кислоты реагируют со спиртами в присутствии сильных неорганических кислот, в результате образуется сложный эфир:
C2H5COOH + CH3OH = C2H5COOCH3
пропионовая метиловый метиловый эфир пропионовой кислоты
кислота спирт (метилпропионат)
Примеры решения задач
Пример 1. Составить уравнения реакций, которые надо провести для осуществления следующих превращений: Метан → X → Y → уксусная кислота. Назвать вещества X и Y.
Решение. При нагревании метана получают ацетилен – вещество Х:
2СН4 → С2Н2 + 3Н2.
Гидратацией ацетилена в присутствии солей ртути (II) синтезируют уксусный альдегид – вещество Y:
C2H2 + H2O → CH3COH.
Окислив уксусный альдегид кислородом воздуха в присутствии катализатора, получают уксусную кислоту:
2СН3СОН + О2 → 2СН3СООН.
Пример 2. В трех пробирках без надписей находятся следующие вещества: этанол, муравьиная кислота, уксусная кислота. Какие химические реакции следует провести, чтобы различить эти вещества?
Решение. Спирт (этанол) можно отличить по действию веществ на индикаторы. Например, кислоты окрашивают синий лакмус в красный цвет, спирт – нет.
Различить муравьиную и уксусную кислоту легко, так как муравьиная кислота проявляет некоторые свойства альдегидов. Например, она вступает в реакцию «серебряного зеркала» (уксусная – нет):
НСООН + Ag2O → CO2↑ + 2Ag + H2O.
Пример 3. Какой объем уксусной эссенции плотностью 1,07 г/мл надо взять для приготовления столового уксуса объмом 200 мл и плотностью 1,007 г/мл? Массовая доля уксусной кислоты в уксусной эссенции равна 80 %, в столовом уксусе – 6 %.
Решение. Определяем массу раствора уксуса, который надо приготовить:
m = V∙ ρ; m = 200 ∙ 1,007 = 201,4 г.
Рассчитаем массу уксусной кислоты, которая содержится в уксусе:
m (CH3COOH) = m ∙ ω (CH3COOH) = 201,4 ∙ 0,06 = 12,1 г.
Вычисляем массу уксусной эссенции m′, которая содержит уксусную кислоту массой 12,1 г: m′ = 12,1/0,8 = 15,1 г.
Находим объем уксусной эссенции: V = 15,1/1,07 = 14,1 мл
Задачи и упражнения для самостоятельного решения
1. Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
С2Н4 → С2Н5СОН → С3Н7ОН → С3Н7СООН.
2. Сколько изомерных карбоновых кислот может соответствовать формуле С5Н10О2? Написать структурные формулы этих изомеров. (Ответ: 4 изомера).
3. При окислении муравьиной кислоты получили газ, который пропустили через избыток раствора гидроксида кальция. При этом образовался осадок массой 20 г. Какая масса муравьиной кислоты взята для окисления?
(Ответ: 9,2 г).
4. В четырех пробирках находятся следующие вещества: пропионовая кислота, раствор формальдегида, раствор фенола в бензоле, метанол. При помощи каких химических реакций можно различить эти вещества?
5. Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
CH4 → CH3Cl → CH3ОH → HCOH → HCOOH → CO2.
6. Какие массы растворов уксусной кислоты с массовой долей СН3СООН
90 и 10 % надо взять для получения раствора массой 200 г с массовой долей кислоты 40 %? (Ответ: раствора с массовой долей 90 % − 75 г; 10 % − 125 г).
7. Сколько изомерных карбоновых кислот может соответствовать формуле С6Н12О2? Написать структурные формулы этих изомеров.
(Ответ: 9 изомеров).
8. Назвать вещества Х и Y и составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) метанол → Х → формиат натрия;
б) уксусный альдегид → Y → ацетат кальция.
9. Какой объем воды надо прибавить к 300 мл 70 %-го раствора уксусной кислоты (ρ = 1,07 г/мл), чтобы получить 30 %-й раствор? (Ответ: 428 мл).
10. Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
СаС2 → С2Н2 → СН3СОН → СН3СООН.
11. Рассчитать объем оксида углерода (II) (условия нормальные), который потребуется для получения раствора муравьиной кислоты массой 16,1 кг. Массовая доля НСООН в растворе, который требуется получить, равна 40 %.
(Ответ: 3136 л).
12. Написать структурные формулы следующих кислот:
а) 3-метил-2-этилгексановая кислота;
б) 4,5-диметилоктановая кислота;
в) 2,2,3,3-тетраметилпентановая кислота.
13. Рассчитать массу бутановой кислоты, которая образуется при окислении бутанола-1 массой 40,7 г. (Ответ: 48,4 г).
14. Какой объем 20 %-го раствора гидроксида калия плотностью 1,2 г/мл потребуется для полной нейтрализации 22,2 г пропионовой кислоты?
(Ответ: 70 мл).
15. Написать уравнение реакции диссоциации бутановой кислоты и реакции получения натриевой соли этой кислоты.
16. Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
пропионовая кислота ← этилен → этанол → уксусная кислота.
17. К раствору муравьиной кислоты массой 36,8 г добавили избыток окислителя. Газ, полученный в результате окисления, пропустили через избыток баритовой воды Ba(OH)2, в результате чего получили осадок массой 39,4 г. Определить массовую долю кислоты в исходном растворе.
(Ответ: 25 %).
18. На нейтрализацию 3,7 г одноосновной предельной кислоты израсходовано 100 мл 0,5 М раствора КОН. Написать структурную формулу этой кислоты.
19. На нейтрализацию 30 г смеси раствора уксусной кислоты и фенола израсходовано 100 мл 2 М раствора NaOH, а при действии бромной воды на эту смесь образовалось 33,1 г осадка. Определить массовую долю (%) кислоты и фенола в растворе. (Ответ: 20 % кислоты и 31,3 % фенола).
20. Определить массовую долю хлоруксусной кислоты, полученной при пропускании хлора в 75 %-й раствор уксусной кислоты.
(Ответ: 82,5 %).
Тест по химии
Тематический тест «Карбоновые кислоты» 2022
-
Главная
-
Тесты по химии
-
Вариант по химии Тематический тест «Карбоновые кислоты» 2022
1
Как для карбонильной, так и для карбоксильной группы, характерно:
- Sp-гибридизация атомов углерода
- Sp2-гибридизация атомов углерода
- Валентный угол связи составляет 120°
- Валентный угол связи составляет 180°
- Углерод имеет валентность равную трём
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
2
Для муравьиной кислоты характерно:
- Газообразное вещество при н.у.
- Образует водородные связи
- Легко смешивается с водой
- Имеет резкий запах
- Легче воздуха
- Твёрдое вещество при н.у.
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
3
К двухосновным карбоновым кислотам относят:
- изофталевую
- бутеновую
- щавелевую
- терефталевую
- капроновую
- бензойную
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
4
И муравьиная, и пропионовая кислота взаимодействуют с:
- водородом
- оксидом натрия
- аммиачным раствором оксида серебра
- гидроксидом калия
- гидрокарбонатом аммония
- водой
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
5
И уксусная кислота, и ацетальдегид при необходимых условиях реагируют с:
- Cu(OH)2
- H2
- CH3OH
- H2O
- FeO
- Cl2
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
6
И муравьиная кислота, и пропаналь реагирует с:
- [Ag(NH3)2]OH
- CH3-I
- HF
- Cu(OH)2
- O2
- Zn(OH)2
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
7
Бутеновая кислота, в отличие от бутановой, реагирует с:
- Бромной водой
- Натрием
- Хлором
- Перманганатом натрия
- Оксидом цинка
- Водой
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
8
Метановая кислота, в отличие от этановой, реагирует с веществами, формулы которых:
- C2H6O
- O2
- C2H4O
- Ag2O(NH3 p-p)
- CH3-Mg-I
- Br2(р-р)
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
9
Этановую кислоту можно получить напрямую из:
- бутана
- бутина-1
- бутадиена-1,3
- бутена-2
- бутадиена-1,2
- бутина-2
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
10
Масляную кислоту нельзя получить
- Гидролизом изопропилбутирата
- Окислением в мягких условиях пентина-1
- Гидролизом 1,1,1-трихлорбутана в избытке щелочи
- Окислением в жестких условиях гексина-2
- Гидролизом метилизовалерата
- Реакцией бутаноата меди с сероводородной кислотой
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
11
Кислоту нельзя получить следующими реакциями:
- CH3‒OH + K2Cr2O7 + H2SO4
- CH3‒CH=CH2 + KMnO4 + H2SO4
- C4H10 + O2(кат)
- C2H4 + KMnO4 + H2SO4
- CH3COOCH3 + H2O
- HCOH + Ag2O(аммиачный р-р)
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
12
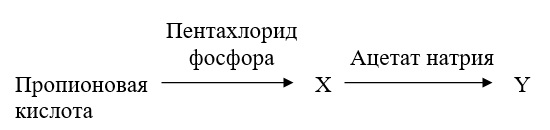
В заданной схеме превращений определите вещества X и Y, запишите их в таблицу ответов (сначала номер, соответствующий веществу X, затем — веществу Y)
- уксуснопропионовый ангидрид
- α-хлорпропионовая кислота
- хлорангидрид пропановой кислоты
- этиловый эфир пропионовой кислоты
- этилпропионат
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
13
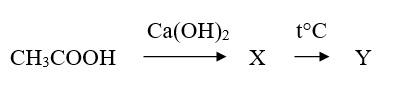
В заданной схеме превращений определите вещества X и Y, запишите их в таблицу ответов (сначала номер, соответствующий веществу X, затем — веществу Y)
- Формиат кальция
- Уксусный ангидрид
- Ацетат калия
- Пропанон
- Ацетат кальция
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
14
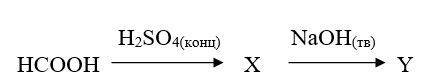
В заданной схеме превращений определите вещества X и Y, запишите их в таблицу ответов (сначала номер, соответствующий веществу X, затем — веществу Y)
- CO
- HCHO
- CH3COOH
- H2CO2
- HCOONa
Ответ:
X_n = Xn
|
X^n = Xn (^ это Shift+6)
Чтобы написать X25 нужно набрать X^2^5
На экзамене нужно использовать Xn и Xn
Ответы
Вы учитель?
Хотите получать новые уникальные тесты раньше других?
Вы можете получать новые тесты в формате КИМ 2023 с ответами, которых нет в публичном доступе!
- Только уникальные задания
- Полное соответствие требованиям ФИПИ
- Хитрости и «ловушки», используемые на реальном ЕГЭ
И всё это здесь и только здесь