в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 187 1–20 | 21–40 | 41–60 | 61–80 …
Добавить в вариант
Какие изменения произошли с эритроцитом в пробирке А? Какие изменения произошли с эритроцитом в пробирке Б? Объясните данное явление. Раствор какой концентрации NaCl был добавлен в пробирку на рис. А, а какой — в пробирку на рис. Б?
Показать
1
Какая переменная в этом эксперименте будет зависимой (изменяющейся), а какая — независимой (задаваемой)? Объясните, как в данном эксперименте можно поставить отрицательный контроль*. С какой целью необходимо такой контроль ставить?
*Отрицательный контроль — это экспериментальный контроль, при котором изучаемый объект не подвергается экспериментальному воздействию).
Как зависит частота сердечных сокращений от концентрации ионов кальция в растворе? Какой эффект можно наблюдать, если в культуру дафний, взятых из пруда, добавить ацетилхолин? (Считать реакцию сердца дафнии на химические вещества аналогичной реакции человека). Ответ поясните.
Показать
1
Какую нулевую гипотезу* смог сформулировать исследователь перед постановкой эксперимента? Какая переменная в этом эксперименте будет зависимой (изменяющейся), а какая — независимой (задаваемой)? Объясните, почему в эксперименте используется хлорид кальция.
*Нулевая гипотеза — принимаемое по умолчанию предположение, что не существует связи между двумя наблюдаемыми событиями, феноменами.
Почему при увеличении концентрации удобрений в воде скорость зарастания постепенно уменьшается? Какие параметры необходимо контролировать в данном эксперименте? Ответ поясните.
Показать
1
Какая переменная в этом эксперименте будет зависимой (изменяющейся), а какая — независимой (задаваемой)? Объясните, как в данном эксперименте можно поставить отрицательный контроль*? С какой целью необходимо
такой контроль ставить?
(*Отрицательный контроль — это экспериментальный контроль, при котором изучаемый объект не подвергается экспериментальному воздействию.)
В каком из листьев крахмала будет меньше? Ответ поясните. Почему через три дня концентрация кислорода в колбе значительно возрастет?
Показать
1
Какую нулевую гипотезу* смог сформулировать исследователь перед постановкой эксперимента? Какой параметр был задан экспериментатором (независимая переменная), какой параметр менялся в зависимости от заданного (зависимая переменная)? Объясните, почему лист был помещён в герметичную колбу?
*Нулевая гипотеза — принимаемое по умолчанию предположение, что не существует связи между двумя наблюдаемыми событиями, феноменами.
Почему при увеличении концентрации углекислого газа свыше 0,1% скорость фотосинтеза не растёт? Как изменится скорость фотосинтеза, если сильно снизить температуру в теплице? Объясните, почему произойдёт изменение. Какую роль играет углекислый газ в процессе фотосинтеза?
Показать
1
Какая переменная в этом эксперименте будет зависимой (изменяющейся), а какая — независимой (задаваемой)? Объясните, как в данном эксперименте можно поставить отрицательный контроль*. С какой целью необходимо такой контроль ставить?
* Отрицательный контроль — это экспериментальный контроль, при котором изучаемый объект не подвергается экспериментальному воздействию).
Источник: Демонстрационная версия ЕГЭ—2023 по биологии
Существует множество факторов, влияющих на эффективность фотосинтеза у наземных растений. Учёные решили исследовать влияние концентрации углекислого газа на рост проростков пшеницы. Проростки растили при трёх различных концентрациях углекислого газа, а эффективность фотосинтеза (измерялась по количеству поглощенного СO2) определялась при различной интенсивности светового потока. Результаты были занесены в таблицу.
Изучите таблицу 1 и выберите верные ответы
1. При концентрации СO2 1300 частей на миллион фотосинтез идёт наиболее эффективно.
2. Сила света, при которой эффективность фотосинтеза при 500 частей/миллион перестаёт расти = 10000 люмен.
3. При концентрации СO2 280 частей/миллион эффективность фотосинтеза не зависит от силы света.
4. Сила света, при которой эффективность фотосинтеза при 500 частей/миллион перестаёт расти = 5000 люмен.
5. При концентрации СO2 500 частей на миллион фотосинтез идёт наиболее эффективно.
Ответ впишите в порядке возрастания.
Источник: РЕШУ ОГЭ
Исследователь решил изучить рост колоний только что выделенного штамма кишечной палочки на агаризованной среде с ампициллином. Он посеял культуру кишечной палочки на среды с разной концентрацией ампициллина — 0 мкг/мл, 10 мкг/мл и 100 мкг/мл, поставил в оптимальные для роста колоний условия и на следующий день обнаружил, что на среде без ампициллина выросло восемьдесят колоний, на среде с концентрацией 10 мкг/мл выросло две колонии, на среде с концентрацией 100 мкг/мл не выросло ни одной колонии. Исследователь взял колонии, выросшие на концентрации 10 мкг/мл, и некоторое время выращивал их при этой концентрации, после чего пересадил их на среду с концентрацией ампициллина 100 мкг/мл и обнаружил, что выросло шесть колоний. Какой параметр задаётся экспериментатором (независимая переменная), а какой меняется в зависимости от него (зависимая переменная)? Объясните, почему при первом посеве на 100 мкг/мл ампициллина рост колоний отсутствовал, а при последующем посеве — появился. Объясните, почему не стоит прекращать приём антибиотиков при первых признаках улучшения самочувствия пациента и нужно принимать полный курс антибиотиков.
Проанализируйте график «Гликемическая кривая в норме (1) и при сахарном диабете (2)». В двух группах испытуемых оценивалась концентрация глюкозы в крови через определённое время после приёма пищи.
Выберите утверждения, которые можно сформулировать на основании анализа представленных данных.
Запишите в ответе цифры, под которыми указаны выбранные утверждения.
1) При диабете концентрация сахара в крови не может снижаться за счёт выделения инсулина.
2) На второй час после приёма пищи в норме начинается снижение концентрации глюкозы в крови.
3) При диабете концентрация глюкозы снижается медленнее, чем в норме.
4) В норме инсулина выделяется больше, чем при диабете.
5) При диабете концентрация глюкозы в крови не может снизиться до нормальных значений.
Экспериментатор решил исследовать изменения, происходящие с эритроцитами, помещёнными в растворы с различной концентрацией хлорида натрия (NaCl). Перед началом эксперимента он выяснил, что концентрация NaCl в плазме крови составляет 0,9%. В рамках эксперимента он распределил кровь по двум пробиркам, в каждую из которых добавил растворы NaCl с различной концентрацией в соотношении 1 : 1 (на 1 мл крови — 1 мл раствора NaCl). По результатам наблюдений экспериментатор сделал рисунки эритроцитов А и Б. Какой параметр задаётся экспериментатором (независимая переменная), а какой параметр меняется в зависимости от этого (зависимая переменная)? Какие изменения произошли с эритроцитом в пробирке Б? Объясните данное явление. Раствор какой концентрации NaCl был добавлен в пробирку на рис. А, а какой — в пробирку на рис. Б?
Источник: Демонстрационная версия ЕГЭ—2022 по биологии
Экспериментатор измельчил семена гороха, добавил воды, прокипятил, остудил до температуры 37 °C и добавил слюну человека. Как изменились концентрация свободных жирных кислот и концентрация свободных моносахаридов?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация свободных жирных
кислот |
Концентрация свободных
моносахаридов |
|---|---|
| Группа | Контрольная группа | Экспериментальная группа |
|---|---|---|
| Объём мочи (мл/сутки) | 0,9 | 0,031 |
Экспериментатор решил изучить процесс образования мочи у домовой мыши (Mus musculs). Для этого он измерял количество мочи, образуемой у контрольной группы мышей. Параллельно он измерял количество мочи у экспериментальной группы мышей, которым он вводил в кровь гормон вазопрессин, регулирующий объём выделяемой мочи. Результаты эксперимента представлены в таблице. Какой параметр был задан экспериментатором (независимая переменная), а какой параметр менялся в зависимости от заданного (зависимая переменная)? Предположите, у мышей из какой группы концентрация солей в моче была выше. Ответ поясните. Почему у мышей из экспериментальной группы концентрация собственного вазопрессина будет понижена?
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
| Вода из пруда | Раствор, концентрация ионов кальция (г/л) | ||||
| 0,2 | 0,4 | 0,6 | 0,8 | ||
| ЧСС/10 минут | 250 | 293 | 347 | 412 | 432 |
Экспериментатор провел эксперимент с дафниями в целях изучения работы сердца. Для этого он взял культуру дафний из пруда и поместил их в растворе с восходящей концентрацией хлорида кальция. Результаты эксперимента показаны в таблице. Какой параметр был задан экспериментатором (независимая переменная), а какой параметр менялся в зависимости от заданного (зависимая переменная)? Как зависит частота сердечных сокращений от концентрации ионов кальция в растворе? Какой эффект можно наблюдать, если в культуру дафний, взятых из пруда, добавить ацетилхолин? (Считать реакцию сердца дафнии на химические вещества аналогичной реакции человека). Ответ поясните.
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Во время эксперимента учёный измерял скорость фотосинтеза в зависимости от света. Концентрацию углекислого газа и температуру он поддерживал постоянными. Объясните, почему при повышении интенсивности света активность фотосинтеза сначала растёт, но начиная с определённой интенсивности перестаёт расти и выходит на плато (см. график).
Экспериментатор измельчил семена гороха и поместил их в желудочный сок человека. Как изменились концентрация пептидов (продукт частичного гидролиза белков) и концентрация свободных моносахаридов?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация пептидов | Концентрация свободных
моносахаридов |
|---|---|
Известно, что уровень глюкозы в крови взрослого человека в норме составляет 4,1-5,9 ммоль/л. На концентрацию глюкозы влияет ряд органов, например промежуточный мозг, надпочечники, двуглавая мышца плеча. Используя знания о функциях этих органов, объясните их роль в регуляции концентрации уровня глюкозы.
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Ученый провел эксперимент с клетками эпидермиса листа тюльпана. Клетки помещались в 3%, 7% и 10% раствор поваренной соли (хлорида натрия). Ученый зарисовал строение исходной клетки и строение клеток через две минуты от начала эксперимента. Результаты изображены на рисунках. Какой параметр был задан экспериментатором (независимая переменная), а какой менялся в зависимости от заданного (зависимая переменная)? Почему в ходе эксперимента изменяется объем живой части клетки (протопласта)? Изменится ли объем живой части клетки (протопласта), если в эксперименте вместо 10% раствора поваренной соли (хлорида натрия) использовать раствор с равной протопласту концентрацией соли? Ответ поясните.
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Растение гинкго, относящееся к голосеменным растениям, называют палеонтологическим барометром. Плотность устьиц на его листьях зависит от концентрации углекислого газа в атмосфере. На графике показано изменение концентрации углекислого газа в различные геологические периоды. Предположите, каким образом изменяется плотность устьиц у гинкго в зависимости от концентрации углекислого газа в атмосфере. Ответ поясните. Как согласно графику изменилась плотность устьиц на листьях гинкго к середине юрского периода относительно его начала?
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Известно, что концентрация солей в плазме крови соответствует концентрации 0,9% хлорида натрия в физиологическом растворе. В стеклянный стакан, заполненный раствором поваренной соли, поместили эритроциты. Сравните изображения нормального эритроцита в плазме (рис. А) и эритроцита в растворе (рис. Б). Объясните наблюдаемое явление. Определите концентрацию соли в стакане (0,9%, более 0,9%, менее 0,9%).
Источник: Демонстрационная версия ЕГЭ—2017 по биологии
Пользуясь таблицей 1 «Сравнительный состав плазмы крови, первичной и вторичной мочи организма человека», а также используя знания из курса биологии, выберите верные утверждения.
Сравнительный состав плазмы крови, первичной и вторичной мочи
организма человека (в %)
| Составные
вещества |
Плазма крови | Первичная моча | Вторичная моча |
|---|---|---|---|
| Белки, жиры,
гликоген |
7–9 | Отсутствуют | Отсутствуют |
| Глюкоза | 0,1 | 0,1 | Отсутствует |
| Натрий (в составе
солей) |
0,3 | 0,3 | 0,4 |
| Хлор (в составе
солей) |
0,37 | 0,37 | 0,7 |
| Калий (в составе
солей) |
0,02 | 0,02 | 0,15 |
| Мочевина | 0,03 | 0,03 | 2,0 |
| Мочевая кислота | 0,004 | 0,004 | 0,05 |
1) Концентрация натрия практически остаётся неизменной по мере превращения плазмы крови во вторичную мочу.
2) Концентрация белков в плазме ниже, чем в первичной и вторичной моче.
3) Глюкоза отсутствует в составе вторичной мочи по сравнению с первичной.
4) В извитых каналах нефрона глюкоза активно всасывается обратно в лимфу.
5) Мочевина отсутствует в составе вторичной мочи по сравнению с первичной.
Источник: РЕШУ ОГЭ
Экспериментатор поместил кусочек печени кролика в дистиллированную воду. Как изменится объем клеток печени и концентрация раствора минеральных солей в них через минуту после начала эксперимента?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Объем клеток печени | Концентрация |
|---|---|
Всего: 187 1–20 | 21–40 | 41–60 | 61–80 …
в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 187 1–20 | 21–40 | 41–60 | 61–80 | 81–100 …
Добавить в вариант
Исследователь решил изучить процесс прорастания клубней картофеля. Он поместил клубни в тёмные влажные места с разной температурой –5 °С, 8 °С и 11 °С. Через неделю он измерил длину побегов, выросших из клубней, и
концентрацию углеводов в клубнях. Какой параметр задаётся экспериментатором (независимая переменная), а какие меняются в зависимости от него (зависимые переменные)? При какой температуре относительная длина побегов будет максимальной? При какой температуре относительная концентрация углеводов будет максимальной? Ответ поясните. Видоизменением какого органа является клубень картофеля? Аргументируйте свой ответ.
Экспериментатор решил установить зависимость качество корнеплодов свеклы от количества вносимых азотных удобрений. Он высадил семена свеклы в лотки и внёс в каждый лоток вместе с водой азотные удобрения. В каждый лоток вносился раствор удобрений разной концентрации. В конце вегетационного периода, экспериментатор выкопал корнеплоды и взвесил. Какой параметр задаётся экспериментатором (независимая переменная), а какой параметр меняется в зависимости от этого (зависимая переменная)? Как масса корнеплодов зависит концентрации удобрений? Для чего растениям необходим азот? Как азотные удобрения влияют на рост растения?
Почему в ходе эксперимента изменяется объем живой части клетки (протопласта)? Изменится ли объем живой части клетки (протопласта), если в эксперименте вместо 10% раствора поваренной соли (хлорида натрия) использовать раствор с равной протопласту концентрацией соли? Ответ поясните.
Показать
1
Какая переменная в этом эксперименте будет зависимой (изменяющейся), а какая — независимой (задаваемой)? Объясните, как в данном эксперименте можно поставить отрицательный контроль*. С какой целью необходимо такой контроль ставить?
*Отрицательный контроль — это экспериментальный контроль, при котором изучаемый объект не подвергается экспериментальному воздействию).
Предположите, у мышей из какой группы концентрация солей в моче была выше. Ответ поясните. Почему у мышей из экспериментальной группы концентрация собственного вазопрессина будет понижена? Как изменится объём формируемой мочи при инъекции кофеина в организм, если известно, что он блокирует выделение вазопроссина?
Показать
1
Какую нулевую гипотезу* смог сформулировать исследователь перед постановкой эксперимента? Какой параметр был задан экспериментатором (независимая переменная), какой параметр менялся в зависимости от заданного (зависимая переменная)? К каким биологически активным веществам, регулирующий обмен веществ в организме, относится вазопрессин? В каком органе эндокринной системе формируется вазопрессин у млекопитающих?
*Нулевая гипотеза — принимаемое по умолчанию предположение, что не существует связи между двумя наблюдаемыми событиями, феноменами.
Ручьевая форель живёт в воде с концентрацией кислорода не менее 2 мг/л. При понижении его содержания до 1,6 мг/л и меньше форель гибнет. Объясните причину гибели форели, используя знания о норме реакции признака.
Источник: ЕГЭ по биологии 05.05.2014. Досрочная волна. Вариант 2.
К крови прилили такой же объем раствора поваренной соли с концентрацией 0,1%.
Что произойдет с эритроцитами.
Источник: ЕГЭ- 2017
Проанализируйте диаграмму «Влияние уровня засоления на интенсивность транспирации листьев кукурузы». По оси абсцисс отложены даты измерений, а по оси ординат интенсивность транспирации в процентах, за 100% принята интенсивность транспирации листьев контрольных растений.
Запишите в ответе номера выбранных утверждений.
1) Фактор засоления обуславливает уменьшение листовой пластинки.
2) Испаряемость воды у листьев растений, выращенных на почве с 0,1% NaCl растёт в последних пробах.
3) Ширина моторных клеток и пучков, толщина эпидермы и мезофилла уменьшаются с повышением уровня засоления.
4) При увеличении концентрации соли в субстрате транспирация снижается во всех пробах.
5) В условиях засоления растения испытывают недостаток снабжения водой и у них наблюдаются изменения в сторону усиления ксероморфизма.
Ответ:
При всасывании питательных веществ в кишечнике человека резко меняется концентрация этих веществ в крови. Объясните, каким образом эта концентрация стабилизируется? Какой орган играет главную роль в этом процессе?
Установите последовательность процессов вдоха и выдоха у человека, начиная с повышения концентрации СО2 в крови. Запишите в таблицу соответствующую последовательность цифр.
1) насыщение кислородом капилляров альвеол
2) повышение концентрации кислорода в тканях и клетках
3) возбуждение хеморецепторов продолговатого мозга
4) расслабление диафрагмы и наружных межрёберных мышц, сокращение внутренних межрёберных мышц
5) сокращение диафрагмы и наружных межрёберных мышц
Экспериментатор поместил семена гороха в стакан с небольшим количеством воды. Как изменились концентрация солей и количество воды в клетках семян на следующий день?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация солей | Количество воды |
|---|---|
Ученые-агрономы внесли в почву опытной делянки препарат, содержащий клубеньковые бактерии. Как изменится концентрация аммонийных солей в почве и урожайность сои, возделываемой на опытной делянке?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация аммонийных солей | Урожайность сои |
|---|---|
Экспериментатор ввел путем инъекции в кровь лабораторных крыс инсулин. Как изменятся у животных концентрация глюкозы в крови и содержание гликогена в печени?
Для каждой величины определите соответствующий характер её изменения:
1) повысилась
2) понизилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация глюкозы в крови | Содержание гликогена в печени |
|---|---|
Экспериментатор поместил зерновки пшеницы в сушильный шкаф. Как изменились концентрация солей и количество воды в клетках семян?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация солей | Количество воды |
|---|---|
Источник: Демонстрационная версия ЕГЭ—2022 по биологии, Демонстрационная версия ЕГЭ—2023 по биологии
Экспериментатор поместил эритроциты в дистиллированную воду. Как изменилась концентрация ионов натрия внутри клеток и объём клеток?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация ионов натрия | Объём клеток |
|---|---|
Экспериментатор исследовал изменения, происходящие с клетками клубней картофеля в растворах сахарозы различной концентрации. Он вырезал из клубней полоски одинакового размера, поместил их в растворы сахарозы концентрацией 0,01М и 1М на 30 минут и измерил длину полосок. Экспериментатор обнаружил, что полоски, помещённые в 0,01М раствор,
увеличились, а полоски, помещённые в 1М раствор, уменьшились. Какой параметр задаётся экспериментатором (независимая переменная), а какой параметр меняется в зависимости от этого (зависимая переменная)? Почему изменилась длина полосок в каждом из случаев? Какими по отношению к клеткам клубня картофеля являются использованные растворы? Почему плазматическая мембрана клетки картофеля, в отличие от плазматической мембраны эритроцитов, не разрывается в дистиллированной воде?
Исследователь поместил на два предметных стекла по капле воды с культурой амёб. На первое стекло он добавил каплю водного раствора с 10%-ной концентрацией NaCl, а на второе — каплю воды с хламидомонадами. Две капли на каждом стекле он соединил водным мостиком. Какое поведение амёб наблюдал исследователь в первом и во втором случаях? Как называют способность амёб реагировать на внешние воздействия и каково её значение для организма?
Источник: ЕГЭ по биологии 2022. Досрочная волна
Экспериментатор решил изучить процесс фотосинтеза. Он взял ветку растения с листьями. Лист № 1 он поместил в герметичную колбу, концентрация углекислого газа в которой была в 10 раз выше по сравнению с атмосферой, лист № 2 находился в естественных условиях. Через три дня экспериментатор измерил количество крахмала в листьях. Какой параметр был задан экспериментатором (независимая переменная), а какой параметр менялся в зависимости от заданного (зависимая переменная)? В каком из листьев крахмала будет меньше? Ответ поясните. Почему через три дня концентрация кислорода в колбе значительно возрастет?
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Известно, что у прибрежных водорослей, обитающих в арктических морях, концентрация органических веществ (липидов, аминокислот и сахаров) в цитоплазме клеток существенно выше, чем у родственных им групп из экваториальных и субэкваториальных вод. Как можно объяснить такое различие? Температура плавления ненасыщенных жирных кислот ниже, чем у насыщенных. Предположите, в какое время года концентрация ненасыщенных жирных кислот в составе мембранных липидов у водорослей северных морей будет максимальной. Поясните свой ответ. Почему для водорослей опасно изменение агрегатного состояния внутренней среды?
Источник: ЕГЭ по биологии 14.06.2022. Основная волна. Разные задачи
Экспериментатор поместил каплю крови человека в гипертонический раствор. Как при этом изменились концентрация солей и количество воды в эритроцитах?
Для каждой величины определите соответствующий характер её изменения:
1) увеличилась
2) уменьшилась
3) не изменилась
Запишите в таблицу выбранные цифры для каждой величины. Цифры в ответе могут повторяться.
| Концентрация солей | Количество воды в эритроците |
|---|---|
Растения, участвуя в круговороте веществ в биосфере,
1) уменьшают запасы свободного азота
2) потребляют готовые органические вещества
3) увеличивают запасы неорганического углерода
4) увеличивают концентрацию свободного кислорода
Всего: 187 1–20 | 21–40 | 41–60 | 61–80 | 81–100 …
Как решать задание 23 в ЕГЭ по химии в 2022-2023? Установить исходную концентрацию веществ, найти известное вещество, по которому будут проводиться расчеты. Затем провести расчеты по уравнению реакции и найти неизвестные концентрации.
Особенности задания
Как решать новое задание 23 в ЕГЭ по химии, которое появилось только в 2022 году? Разумеется, хорошенько подготовившись – аналогов этой задаче до сих пор не было, в 2023 году она будет использоваться лишь второй раз. Поэтому важно заранее получить максимум информации о том, как можно найти правильный ответ.
Прежде чем разбираться, как решать номер 23 в ЕГЭ по химии, отметим, что задание относится к повышенному уровню сложности. Соответственно, за правильное решение можно заработать два первичных балла. На выполнение отводится в среднем 5-7 минут.
В задании проверяются ваши знания и умения в следующих областях:
- Обратимые и необратимые химические реакции;
- Химическое равновесие и его смещение под воздействием различных факторов;
- Расчеты количества вещества, его массы или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ.
Если вкратце: вот как делать 23 задание на ЕГЭ по химии: проанализировать исходные данные и установить известные концентрации вещества. После этого произвести расчеты по уравнению реакции и вычислить неизвестные вещества.
Демонстрационные задания
А теперь на практике покажем, как решать задачи 23 в ЕГЭ по химии – используем несколько демонстрационных вариантов. Помните, что нет никакой гарантии, что именно эти задачки попадутся в вашем комплекте заданий. Но ими можно руководствоваться как примером.
Итак, первый вариант решения 23 номера ЕГЭ по химии.
Дано:
В замкнутый реактор поместили газообразную смесь оксида азота (II) с кислородом и нагрели. В результате протекания обратимой реакции 2NO(г) + O2(г) ⇄ 2NO2(г) в системе установилось равновесие.
Используя данные, приведенные в таблице, определите равновесные концентрации оксида азота (II) (Х) и кислорода (Y).
| Реагент | NO | O2 | NO2 |
| Исходная концентрация (моль/л) | 0,5 | 0,8 | |
| Равновесная концентрация (моль/л) | 0,2 |
На основании приведенных данных рассказываем, как решать 23 задание ЕГЭ по химии:
Сначала производим базовый расчет: исходя из приведенной информации, следует, что в реакторе не было NO2, а значит, исходная концентрация NO2 равна нулю.
Известное вещество (с известной исходной и равновесной концентрацией) – это NO2, которого образовалось 0,2 моль.
Теперь переходим к стехиометрическим расчетам. Подставляем нужные цифры:
- 2NO(г) + O2(г) ⇄ 2NO2(г)
- 0,2 + 0,1 ⇄ 0,2
Из уравнения реакции становится ясно, что прореагировали 0,2 моль NO и 0,1 моль О2.
Наконец, переходим к окончательным расчетам. Еще раз представим перед собой таблицу и подставим нужные значения:
| Реагент | NO | O2 | NO2 |
| Исходная концентрация (моль/л) | 0,5 | 0,8 | 0 |
| Равновесная концентрация (моль/л) | 0,3 | 0,7 | 0,2 |
Итого, получаем следующий ответ:
- х = 0,5 – 0,2 = 0,3
- у = 0,8 – 0,1 = 0,7
Еще один разбор 23 задачи ЕГЭ по химии 2022-2023. Хороший пример, который может помочь вам разобраться.
Дано:
В реактор для синтеза метанола постоянного объема поместили водород и угарный газ. В результате протекания обратной химической реакции 2Н2(г) + СО(г) ⇄ СН3ОН(г) в системе установилось химическое равновесие.
Используя данные, приведенные в таблице, определите равновесную концентрацию угарного газа (Х) и исходную концентрацию водорода (Y).
| Реагент | Н2 | СО | СН3ОН |
| Исходная концентрация (моль/л) | Y | 2 | 0 |
| Равновесная концентрация (моль/л) | 1,2 | Х | 0,4 |
Решение демо 23 задания ЕГЭ по химии 2022 выглядит так:
Так как в первоначальный момент в системе не было метанола (а в состоянии равновесия метанола стало 0,4 моль), соответственно, изменения в ходе реакции по метанолу будет равно +0,4 моль.
Далее необходимо определить, сколько угарного газа было потрачено на реакцию. Концентрация угарного газа в ходе реакции уменьшается, из уравнения реакции следует, что n(CH3ОН):n(CO) = 1:1. Отсюда следует, что n(CO) = n(CH3ОН) = 0,4 моль.
Равновесную концентрацию угарного газа можно посчитать так: [СО]равн = [СО]исх – [CO]измен = 2 моль/л = 0,4 моль/л = 1,6 моль/л.
Первая часть разбора 23 задания ЕГЭ по химии 2022г. окончена, теперь посчитаем второе неизвестное значение:
Из уравнения реакции следует, что n(CH3ОН):n(Н2) = 1:2, отсюда следует, что n(Н2) = 2n(CH3ОН) = 2х0,4 = 0,8 моль.
Концентрация водорода в ходе реакции уменьшается. Чтобы найти исходную концентрацию водорода: [H2]исх – [H2]измен = 1,2 моль/л.
[H2]исх = [H2]измен + [H2]равн = 1,2 моль/л + 0,8 моль/л = 2 моль/л.
Ответ: х = 1,6 моль/л, у = 2 моль/л.
Как вам такое объяснение 23 задания ЕГЭ по химии 2022 года? Как видите, задачи действительно сложные – нужно знать довольно много вещей и свободно оперировать химическими формулами. Что может быть довольно сложно, если на уроках вы уделяли недостаточно внимания этим темам. Хорошо, что еще есть время на подготовку!
Решение задачи 23 в ЕГЭ по химии 2022-2023 вполне доступно каждому. Конечно, если вы понимаете смысл нужных понятий и умеете пользоваться вычислениями по химическим формулам и уравнениям. Задание это новое, поэтому лучше прорешать все доступные демонстрационные варианты перед экзаменом, чтобы хорошенько подготовиться!
Задачи ЕГЭ на сплавы, смеси, растворы.
Задачи на сплавы, смеси, растворы встречаются и в математике, и в химии. У химиков сложнее – там вещества еще и взаимодействуют, превращаясь во что-то новое. А в задачах по математике мы просто смешиваем растворы различной концентрации. Покажем правила решения на примере задач на растворы. Для сплавов и смесей – действуем аналогично.
. В сосуд, содержащий
литров
-процентного водного раствора некоторого вещества, добавили
литров воды. Сколько процентов составляет концентрация получившегося раствора?
В решении подобных задач помогает картинка. Изобразим сосуд с раствором схематично — так, как будто вещество и вода в нем не перемешаны между собой, а отделены друг от друга, как в коктейле. И подпишем, сколько литров содержат сосуды и сколько в них процентов вещества. Концентрацию получившегося раствора обозначим .
Первый сосуд содержал литра вещества. Во втором сосуде была только вода. Значит, в третьем сосуде столько же литров вещества, сколько и в первом:
.
. Смешали некоторое количество
-процентного раствора некоторого вещества с таким же количеством
-процентного раствора этого вещества. Сколько процентов составляет концентрация получившегося раствора?
Пусть масса первого раствора равна . Масса второго — тоже
. В результате получили раствор массой
. Рисуем картинку.
Получаем:
Ответ: .
. Виноград содержит
влаги, а изюм —
. Сколько килограммов винограда требуется для получения
килограммов изюма?
Внимание! Если вам встретилась задача «о продуктах», то есть такая, где из винограда получается изюм, из абрикосов урюк, из хлеба сухари или из молока творог — знайте, что на самом деле это задача на растворы. Виноград мы тоже можем условно изобразить как раствор. В нем есть вода и «сухое вещество». У «сухого вещества» сложный химический состав, а по его вкусу, цвету и запаху мы могли бы понять, что это именно виноград, а не картошка. Изюм получается, когда из винограда испаряется вода. При этом количество «сухого вещества» остается постоянным. В винограде содержалось воды, значит, «сухого вещества» было
. В изюме
воды и
«сухого вещества». Пусть из
кг винограда получилось
кг изюма. Тогда
от
от
Составим уравнение:
и найдем .
Ответ: .
. Имеется два сплава. Первый сплав содержит
никеля, второй —
никеля. Из этих двух сплавов получили третий сплав массой
кг, содержащий
никеля. На сколько килограммов масса первого сплава меньше массы второго?
Пусть масса первого сплава равна x, а масса второго равна y. В результате получили сплав массой .
Запишем простую систему уравнений:
Первое уравнение — масса получившегося сплава, второе — масса никеля.
Решая, получим, что .
Ответ: .
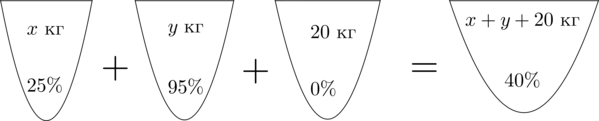
. Смешав
-процентный и
-процентный растворы кислоты и добавив
кг чистой воды, получили
-процентный раствор кислоты. Если бы вместо
кг воды добавили
кг
-процентного раствора той же кислоты, то получили бы
-процентный раствор кислоты. Сколько килограммов
-процентного раствора использовали для получения смеси?
Пусть масса первого раствора , масса второго равна
. Масса получившегося раствора равна
. Запишем два уравнения, для количества кислоты.
Решаем получившуюся систему. Сразу умножим обе части уравнений на , поскольку с целыми коэффициентами удобнее работать, чем с дробными. Раскроем скобки.
Ответ: .
Спасибо за то, что пользуйтесь нашими публикациями.
Информация на странице «Задачи ЕГЭ на сплавы, смеси, растворы.» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать необходимые и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
09.03.2023
Один из способов решения задания 23 по химии по демоверсии 2022 года.




А также учитываем коэффициенты пред формулами веществ. А теперь решим задания, например, с сайта «Решу ЕГЭ»:
1. Задание 23 № 28983
(https://chem-ege.sdamgia.ru/test?filter=all&category_id=176&print=true&svg=0&num=true)
В реактор постоянного объёма поместили некоторое количество азота и кислорода. В результате протекания обратимой реакции
в реакционной системе установилось химическое равновесие. Используя данные, приведённые в таблице, определите равновесные концентрации и
|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
0,7 |
0,5 |
|
|
Равновесная концентрация (моль/л) |
0,5 |
Выберите из списка номера правильных ответов.
1) 0 моль/л
2) 0,1 моль/л
3) 0,25 моль/л
4) 0,35 моль/л
5) 0,45 моль/л
6) 0,55 моль/л
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
|
X |
Y |
Решение:
Составим новую таблицу для решения этого задания, добавив в нее графу изменение концентрации:
|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
0,7 |
0,5 |
0 |
|
Равновесная концентрация (моль/л) |
X |
Y |
0,5 |
|
Изменение концентрации(моль/л) |
Из условия задачи мы видим, что исходная концентрация NO нам не дана, а реакция началась между N2 и O2. Отсюда следует, что исходная концентрация NO равна 0. Таким образом можно найти изменение концентрации NO по формуле:

Подставим значение в соответствующую графу
|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
0,7 |
0,5 |
0 |
|
Равновесная концентрация (моль/л) |
X |
Y |
0,5 |
|
Изменение концентрации(моль/л) |
0,5 |
Она получилась положительной и с правой стороны больше нет веществ, значит с левой стороны в уравнении будут отрицательные значения концентрации веществ, так как вещества реагируют между собой и концентрация их уменьшается. Численно соотношение будет таким же, как и коэффициенты в уравнении. Т.е. по уравнению 1 моль вступает в реакцию с 1 моль
и получается 2 моль NO. Значит изменение концентрации азота и кислорода будут в 2 раза меньше, чем у оксида азота(II), но с обратным знаком.
|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
0,7 |
0,5 |
0 |
|
Равновесная концентрация (моль/л) |
X |
Y |
0,5 |
|
Изменение концентрации(моль/л) |
-0,25 |
-0,25 |
0,5 |
А сейчас получилось, что не известно только по одной величине из столбика, которые легко найти подставив в формулу:



Ответ:
|
X |
Y |
|
5 |
3 |
Это полностью соответствует ответам на сайте «Решу ЕГЭ», хотя само решение отличается.
2. Задание 23 № 28984
(https://chem-ege.sdamgia.ru/test?filter=all&category_id=176&print=true&svg=0&num=true)
В реактор постоянного объёма поместили некоторое количество водорода и кислорода. В результате протекания обратимой реакции
в реакционной системе установилось химическое равновесие. Используя данные, приведённые в таблице, определите равновесную концентрацию и исходную концентрацию
|
Реагент |
|
|
|
|
|
Исходная концентрация (моль/л) |
2,5 |
|||
|
Равновесная концентрация (моль/л) |
0,3 |
0,8 |
Выберите из списка номера правильных ответов.
1) 0 моль/л
2) 0,2 моль/л
3) 0,7 моль/л
4) 1,4 моль/л
5) 1,7 моль/л
6) 3,6 моль/л
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
|
X |
Y |
Решение:
Составим новую таблицу, добавив в нее графу изменение концентрации:
|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
2,5 |
Y |
0 |
|
Равновесная концентрация (моль/л) |
X |
0,3 |
0,8 |
|
Изменение концентрации(моль/л) |
Так как вода получилась в результате реакции, то ее исходная концентрация равна 0. Изменение концентрации отсюда будет:

|
Реагент |
|
|
|
|
Исходная концентрация (моль/л) |
2,5 |
Y |
0 |
|
Равновесная концентрация (моль/л) |
X |
0,3 |
0,8 |
|
Изменение концентрации(моль/л) |
-0,8 |
-0,4 |
0,8 |
Теперь по коэффициентам в уравнении найдем изменение концентрации остальных веществ. Так как вода единственный продукт реакции и ее изменение концентрации положительное, то у исходных продуктов (кислорода и водорода) они будут отрицательными. Количество вещества водорода по уравнению равно количеству вещества воды, значит, изменение концентрации будет таким же, но с обратным знаком, т.е. -0,8 моль/л. А у кислорода коэффициент в 2 раза меньше, поэтому изменение концентрации кислорода будет -0,4 моль/л. Теперь по формулам легко найти неизвестные величины:


Ответ:
|
X |
Y |
|
5 |
3 |
Все вычисления можно проводить устно, остается только правильно записать все в таблицу.
Опыт подготовки обучающихся к ЕГЭ показал, что, решая, задание 23 данным способом, ребята лучше с ним справляются. А значит получат более высокий балл на экзамене!
11. Сюжетные текстовые задачи
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
Задачи на растворы, смеси и сплавы
(blacktriangleright) Концентрация вещества в растворе (сплаве) – это процент содержания этого вещества в растворе (сплаве): [text{концентрация вещества}=dfrac{text{масса вещества}}{text{масса раствора}}cdot 100%]
(blacktriangleright) Заметим, что в задачах из данной подтемы зачастую удобно составлять уравнения относительно кислоты или активного вещества.
Задание
1
#846
Уровень задания: Равен ЕГЭ
Сергей смешал раствор, содержащий (20%) кислоты и раствор, содержащий (40%) той же кислоты. В итоге у него получился раствор, содержащий (32,5%) кислоты, причём объём полученного раствора (4) литра. Сколько литров раствора, содержащего (20%) кислоты, использовал Сергей при смешивании?
Пусть (x) литров раствора, содержащего (20%) кислоты использовал Сергей при смешивании, тогда
(4 — x) литров раствора, содержащего (40%) кислоты использовал Сергей при смешивании,
(dfrac{20}{100}x) – объём кислоты в растворе, содержащем (20%) кислоты, (dfrac{40}{100}(4 — x)) – объём кислоты в растворе, содержащем (40%) кислоты.
Так как в итоге кислоты оказалось (dfrac{32,5}{100} cdot 4 = 1,3) литра, то:
[dfrac{20}{100}x + dfrac{40}{100}(4 — x) = 1,3,] откуда находим (x = 1,5).
Ответ: 1,5
Задание
2
#844
Уровень задания: Равен ЕГЭ
Один газ в сосуде А содержал (21%) кислорода, второй газ в сосуде В содержал (5%) кислорода. Масса первого газа в сосуде А была больше массы второго газа в сосуде В на 300 г. Перегородку между сосудами убрали так, что газы перемешались и получившийся третий газ теперь содержит (14,6%) кислорода. Найдите массу третьего газа. Ответ дайте в граммах.
Пусть (x) грамм – масса второго газа, тогда
(x + 300) грамм – масса первого газа,
(dfrac{21}{100}(x + 300)) грамм – масса кислорода в первом газе,
(dfrac{5}{100}x) грамм – масса кислорода во втором газе,
тогда масса кислорода в третьем газе составляет (dfrac{14,6}{100}(2x + 300)) грамм.
Так как третий газ возник в результате смешивания первого и второго, то:
[dfrac{21}{100}(x + 300) + dfrac{5}{100}x = dfrac{14,6}{100}(2x + 300),] откуда находим (x = 600). Таким образом, масса третьего газа равна (600 + 600 + 300 = 1500) грамм.
Ответ: 1500
Задание
3
#843
Уровень задания: Равен ЕГЭ
Иван случайно смешал молоко жирностью (2,5%) и молоко жирностью (6%). В итоге у него получилось 5 литров молока жирностью (4,6%). Сколько литров молока жирностью (2,5%) было у Ивана до смешивания?
Пусть (x) литров молока жирностью (2,5%) было у Ивана, тогда
(5 — x) литров молока жирностью (6%) было у Ивана,
(dfrac{2,5}{100}x) – объём жира в молоке жирностью (2,5%), (dfrac{6}{100}(5 — x)) – объём жира в молоке жирностью (6%).
Так как в итоге жира оказалось (dfrac{4,6}{100} cdot 5 = 0,23) литра, то:
(dfrac{2,5}{100}x + dfrac{6}{100}(5 — x) = 0,23), откуда находим (x = 2).
Ответ: 2
Задание
4
#841
Уровень задания: Равен ЕГЭ
В сосуде А содержится 3 литра 17-процентного водного раствора вещества Х. Из сосуда В в сосуд А перелили 7 литров 19-процентного водного раствора вещества Х. Сколько процентов составляет концентрация полученного в сосуде А раствора?
Концентрация в процентах – это отношение объёма вещества к объёму смеси, умноженное на 100(%). До переливания в сосуде А было (3 cdot 0,17 = 0,51) литра вещества Х, в сосуде В было (7 cdot 0,19 = 1,33) литра вещества Х.
После переливания объём вещества Х в сосуде А стал (0,51 + 1,33 = 1,84) литра, а объём всего раствора (3 + 7 = 10) литров. Тогда концентрация в процентах составила [dfrac{1,84}{10} cdot 100% = 18,4%.]
Ответ: 18,4
Задание
5
#2133
Уровень задания: Равен ЕГЭ
Во сколько раз больше должен быть объём (5)-процентного раствора кислоты, чем объём (10)-процентного раствора той же кислоты, чтобы при смешивании получить (7)-процентный раствор?
Пусть объём (5)-процентного раствора кислоты равен (x) литров, а объём (10)-процентного раствора равен (y) литров, тогда требуется найти значение величины (dfrac{x}{y}) при условии [0,05x + 0,1y = 0,07(x + y)
qquadLeftrightarrowqquad
dfrac{x}{y} = dfrac{3}{2} = 1,5,,] таким образом, ответ: (1,5).
Ответ: 1,5
Задание
6
#2134
Уровень задания: Равен ЕГЭ
Во сколько раз больше должен быть объём (20)-процентного раствора кислоты, чем объём (14)-процентного раствора той же кислоты, чтобы при смешивании получить (18)-процентный раствор?
Пусть объём (20)-процентного раствора кислоты равен (x) литров, а объём (14)-процентного раствора равен (y) литров, тогда требуется найти значение величины (dfrac{x}{y}) при условии [0,2x + 0,14y = 0,18(x + y)
qquadLeftrightarrowqquad
dfrac{x}{y} = 2,,] таким образом, ответ: (2).
Ответ: 2
Задание
7
#2629
Уровень задания: Равен ЕГЭ
Смешав (25)-процентный и (95)-процентный растворы кислоты и добавив (20) кг чистой воды, получили (40)-процентный раствор кислоты. Если бы вместо (20) кг воды добавили (20) кг (30)-процентного раствора той же кислоты, то получили бы (50)-процентный раствор кислоты. Сколько килограммов (25)-процентного раствора использовали для получения смеси?
Заметим, что вода – это раствор, не содержащий кислоту, то есть содержащий (0%) кислоты.
Пусть (x) кг – масса раствора с (25)-процентным содержанием кислоты, (y) кг – масса раствора с (95)-процентным содержанием кислоты. Составим схему, описывающую получение (40)-процентного раствора:
Заметим, что количество кислоты во всех трех растворах равно количеству кислоты в получившемся растворе. Найдем количество кислоты в первом растворе.
Если раствор весит (x) кг, а в нем (25%) кислоты, то в килограммах в нем (dfrac{25}{100}cdot x) кислоты.
Таким же образом можно посчитать количество кислоты в остальных растворах. Получим первое уравнение:
[dfrac{25}{100}cdot x+dfrac{95}{100}cdot y+
dfrac{0}{100}cdot 20=dfrac{40}{100}cdot (x+y+20)]
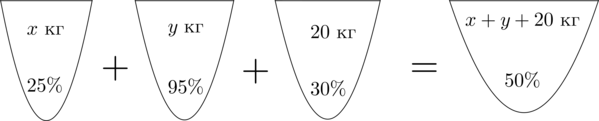
Аналогично составим схему, описывающую получение (50)-процентного раствора:
Значит, уравнение, описывающее эту ситуацию, будет выглядеть так:
[dfrac{25}{100}cdot x+dfrac{95}{100}cdot y+
dfrac{30}{100}cdot 20=dfrac{50}{100}cdot (x+y+20)]
Таким образом, решив систему из полученных двух уравнений, найдем (x). Для этого можно умножить оба уравнения на (100), чтобы сделать их проще на вид:
[begin{cases}
25x+95y+0=40(x+y+20)\
25x+95y+30cdot 20=50(x+y+20)
end{cases}]
Вычтем из второго уравнения первое и получим новую систему:
[begin{aligned} &begin{cases}
25x+95y=40(x+y+20)\
30cdot 20=10(x+y+20)
end{cases} quad Rightarrow quad begin{cases}
5x+19y=8(x+y+20)\
y=40-x end{cases} quad Rightarrow \[2ex] Rightarrow quad
&begin{cases}
3x-11(40-x)+160=0\
y=40-x end{cases} quad Rightarrow quad begin{cases}
x=20\y=20end{cases} end{aligned}]
Таким образом, раствора с (25%) кислоты было (20) кг.
Ответ: 20

Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Тренировочные упражнения по теме «Расчетные задачи на химическое равновесие» в формате ЕГЭ по химии (тренажер задания 23 ЕГЭ по химии).
Теория по теме «Расчетные задачи на химическое равновесие» (теория для решения задания 23 ЕГЭ по химии):
«Обратимые и необратимые химические реакции. Химическое равновесие. Расчёты количества вещества, массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ»
Тренировочный тест «Расчетные задачи на химическое равновесие» 10 вопросов, при каждом прохождении новые.
115
Создан на
16 января, 2022 От Admin
Тренажер задания 23
Тренажер задания 23 ЕГЭ по химии
1 / 10
В реактор постоянного объёма поместили некоторое количество оксида серы(VI). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида серы (VI) и оксида серы (IV) составили 0,05 моль/л и 0,20 моль/л соответственно.
Определите исходную концентрацию SO3 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
2 / 10
В реактор постоянного объёма поместили кислород и азот и подвергли воздействию электрического тока. В результате протекания обратимой реакции
N2(г) + O2(г) ↔ 2NO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация О2 составила 0,4 моль/л, равновесная концентрация N2 составила 0,3 моль/л, а равновесная концентрация NO составила 0,2 моль/л.
Определите исходную концентрацию N2 (Х) и равновесную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
3 / 10
В реактор постоянного объёма поместили некоторое количество оксида серы(IV). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы (VI) составила 0,8 моль/л, а равновесная концентрация оксида серы (IV) – 0,6 моль/л.
Определите равновесные концентрации SO3 (Х) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
4 / 10
В реактор постоянного объёма поместили метан и углекислый газ. В результате протекания обратимой реакции
CH4(г) + CO2(г) ⇄ 2CO(г) + 2H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,1 моль/л, а равновесная концентрация CO2 составила 0,2 моль/л
Определите исходную концентрацию CH4 (X) и равновесную концентрацию H2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
5 / 10
В реактор постоянного объёма поместили некоторое количество водорода и паров йода. В результате протекания обратимой реакции
H2(г) + I2(г) ↔ 2HI(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация йода составила 0,9 моль/л, а равновесные концентрации водорода и йода – 0,2 моль/л и 0,6 моль/л соответственно.
Определите исходную концентрацию Н2 (Х) и равновесную концентрацию НI (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
6 / 10
В реактор постоянного объёма поместили некоторое количество серы и водяного пара. В результате протекания обратимой реакции
2S(ж) + 2H2O(г) ↔ 2H2S(г) + SO2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация Н2О составила 0,8 моль/л, а равновесная концентрация Н2S составила 0,6 моль/л.
Определите равновесные концентрации H2O (Х) и SO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
7 / 10
В реактор постоянного объёма поместили некоторое количество монооксида азота и озона. В результате протекания обратимой реакции
NO(г) + О3(г) ↔ NO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации оксида азота (II) и кислорода составили 0,25 моль/л и 0,3 моль/л соответственно, а равновесная концентрации оксида азота (II) составила 0,05 моль/л.
Определите равновесные концентрации О3 (Х) и NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
8 / 10
В реактор постоянного объёма поместили некоторое количество оксида азота(II) и хлора. В результате протекания обратимой реакции
2NO(г) + Cl2(г) ↔ 2NOCl(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация хлора составила 0,15 моль/л, а равновесные концентрации оксида азота (II) и хлора составили 0,05 моль/л и 0,05 моль/л соответственно.
Определите исходную концентрацию NO (Х) и равновесную концентрацию NOCl (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
9 / 10
В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
2CH4(г) + O2(г) = 2CO(г) + 4H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация O2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,2 моль/л, равновесная концентрация CO составила 0,4 моль/л, а равновесная концентрация H2 составила 0,8 моль/л
Определите исходную концентрацию CH4 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
10 / 10
В реактор постоянного объёма поместили некоторое количество оксида углерода(II) и водорода. В результате протекания обратимой реакции
CO(г) + 3H2(г) ↔ СH4(г) + H2O(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CО составила 0,5 моль/л, а равновесные концентрации Н2, СН4 и Н2О составили 0,1 моль/л, 0,2 моль/л и 0,2 моль/л соответственно.
Определите равновесную концентрацию СО (Х) и исходную концентрацию Н2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,5 моль/л 5) 0,9 моль/л
2) 0,3 моль/л 4) 0,7 моль/л 6) 1,1 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Ваша оценка
The average score is 21%
Полный тематический тест по теме «Расчетные задачи на химическое равновесие» — полный тест из всех вопросов.
38
Создан на
03 апреля, 2022 От Admin
Полный тематический тест Тренажер задания 23
Тренажер задания 23 ЕГЭ по химии
1 / 43
В реактор постоянного объёма поместили некоторое количество водорода и паров йода. В результате протекания обратимой реакции
H2(г) + I2(г) ↔ 2HI(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация йода составила 0,9 моль/л, а равновесные концентрации водорода и йода – 0,2 моль/л и 0,6 моль/л соответственно.
Определите исходную концентрацию Н2 (Х) и равновесную концентрацию НI (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
2 / 43
В реактор постоянного объёма поместили некоторое количество водорода и углекислого газа. В результате протекания обратимой реакции
H2(г) + СO2(г) ↔ H2O(г) + СO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация водорода составила 0,9 моль/л, а равновесные концентрации углекислого газа, угарного газа и воды – 0,1 моль/л, 0,6 моль/л и 0,6 моль/л соответственно.
Определите равновесную концентрацию Н2 (X) и исходную концентрацию СО2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,5 моль/л 5) 0,9 моль/л
2) 0,3 моль/л 4) 0,7 моль/л 6) 1,1 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
3 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + O2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида азота (II), кислорода и оксида азота (IV) составила 0,2 моль/л, 0,4 моль/л и 0,8 моль/л соответственно.
Определите исходные концентрации NО (X) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
4 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + O2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации оксида азота (II) и кислорода составили 0,9 моль/л и 0,5 моль/л соответственно, а равновесная концентрация кислорода – 0,2 моль/л.
Определите равновесные концентрации NO (Х) и NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
5 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + О2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация кислорода составила 0,20 моль/л, а равновесные концентрации оксида азота (II) и оксида азота (IV) – 0,05 моль/л и 0,20 моль/л соответственно.
Определите исходную концентрацию NO (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 2) 0,10 моль/л 3) 0,15 моль/л
4) 0,20 моль/л 5) 0,25 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
6 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(IV). В результате протекания обратимой реакции
2NO2 ↔ 2NO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида азота (IV) составила 1,4 моль/л, а равновесная концентрация оксида азота (II) – 0,8 моль/л.
Определите равновесные концентрации NO2 (Х) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
7 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(IV). В результате протекания обратимой реакции
2NO2(г) ↔ 2NO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида азота (IV) и кислорода составили 0,4 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию NO2 (Х) и равновесную концентрацию NO (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
8 / 43
В реактор постоянного объёма поместили некоторое количество оксида серы(IV). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы (VI) составила 0,8 моль/л, а равновесная концентрация оксида серы (IV) – 0,6 моль/л.
Определите равновесные концентрации SO3 (Х) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
9 / 43
В реактор постоянного объёма поместили некоторое количество оксида серы(VI). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида серы (VI) и оксида серы (IV) составили 0,05 моль/л и 0,20 моль/л соответственно.
Определите исходную концентрацию SO3 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
10 / 43
В реактор постоянного объёма поместили некоторое количество оксида азота(II) и хлора. В результате протекания обратимой реакции
2NO(г) + Cl2(г) ↔ 2NOCl(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация хлора составила 0,15 моль/л, а равновесные концентрации оксида азота (II) и хлора составили 0,05 моль/л и 0,05 моль/л соответственно.
Определите исходную концентрацию NO (Х) и равновесную концентрацию NOCl (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
11 / 43
В реактор постоянного объёма поместили некоторое количество диоксида серы и озона. В результате протекания обратимой реакции
SO2(г) + О3 ↔ SO3(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация озона составила 0,4 моль/л, а равновесные концентрации оксида серы (IV), оксида серы (VI) и кислорода составили 0,2 моль/л, 0,3 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию SO2 (Х) и равновесную концентрацию О3 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
12 / 43
В реактор постоянного объёма поместили некоторое количество диоксида серы и диоксида азота. В результате протекания обратимой реакции
SO2(г) + NO2(г) ↔ SO3(г) + NO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы (IV) составила 0,5 моль/л, а равновесные концентрации оксида азота (IV) и оксида азота (II) составили 0,1 моль/л и 0,3 моль/л соответственно.
Определите равновесную концентрацию SO2 (Х) и исходную концентрацию NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
13 / 43
В реактор постоянного объёма поместили некоторое количество монооксида азота и озона. В результате протекания обратимой реакции
NO(г) + О3(г) ↔ NO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации оксида азота (II) и кислорода составили 0,25 моль/л и 0,3 моль/л соответственно, а равновесная концентрации оксида азота (II) составила 0,05 моль/л.
Определите равновесные концентрации О3 (Х) и NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
14 / 43
В реактор постоянного объёма поместили некоторое количество диоксида хлора. В результате протекания обратимой реакции
ClO2(г) ↔ 1/2Cl2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация ClO2 составила 0,7 моль/л, а равновесная концентрация кислорода – 0,4 моль/л.
Определите равновесные концентрации ClO2 (Х) и Сl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
15 / 43
В реактор постоянного объёма поместили некоторое количество фторида азота(III). В результате протекания обратимой реакции
2NF3(г) ↔ N2(г) + 3F2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация NF3 составила 0,8 моль/л, а равновесная концентрация фтора – 0,6 моль/л.
Определите равновесные концентрации NF3 (Х) и N2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
16 / 43
В реактор постоянного объёма поместили некоторое количество азота и фтора. В результате протекания обратимой реакции
N2(г) + 3F2(г) ↔2NF3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация фтора составила 1,2 моль/л, а равновесные концентрации азота и NF3 составили 0,2 моль/л и 0,4 моль/л соответственно.
Определите исходную концентрацию N2 (Х) и равновесную концентрацию F2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
17 / 43
В реактор постоянного объёма поместили некоторое количество оксида хлора(I). В результате протекания обратимой реакции
4Cl2O(г) ↔ 2Сl2(г) + 2ClO2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации Cl2O и ClO2 составили 0,05 моль/л и 0,10 моль/л соответственно.
Определите исходную концентрацию Cl2O (Х) и равновесную концентрацию Cl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
18 / 43
В реактор постоянного объёма поместили некоторое количество фторида хлора(I). В результате протекания обратимой реакции
3ClF(г) ↔ СlF3(г) + Сl2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации ClF и Cl2 составили 0,2 моль/л и 0,1 моль/л соответственно.
Определите исходную концентрацию СlF (Х) и равновесную концентрацию СlF3 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
19 / 43
В реактор постоянного объёма поместили некоторое количество трифторида хлора. В результате протекания обратимой реакции
2ClF3(г) ↔ Сl2(г) + 3F2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации ClF3 и Cl2 составили 0,1 моль/л и 0,2 моль/л соответственно.
Определите исходную концентрацию СlF3 (Х) и равновесную концентрацию F2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
20 / 43
В реактор постоянного объёма поместили некоторое количество хлора и трифторида хлора. В результате протекания обратимой реакции
ClF3(г) + Сl2(г) ↔ 3СlF(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации ClF3 и Cl2 составили 0,45 моль/л и 0,35 моль/л соответственно, а равновесная концентрация ClF3 составила 0,30 моль/л.
Определите равновесные концентрации Cl2 (Х) и ClF (Y)
Выберите из списка номера правильных ответов.
1) 0,20 моль/л 3) 0,30 моль/л 5) 0,40 моль/л
2) 0,25 моль/л 4) 0,35 моль/л 6) 0,45 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
21 / 43
В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
CH4(г) + 1/2O2(г) ↔ СO(г) + 2H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CH4 составила 0,8 моль/л, а равновесные концентрации кислорода, угарного газа и водорода составили 0,2 моль/л, 0,6 моль/л и 1,2 моль/л соответственно.
Определите равновесную концентрацию СН4 (Х) и исходную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
22 / 43
В реактор постоянного объёма поместили некоторое количество метана и углекислого газа. В результате протекания обратимой реакции
1/2CH4(г) + 1/2CO2(г) ↔ СO(г) + H2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации метана и углекислого газа составили 0,7 моль/л и 0,5 моль/л соответственно, а равновесная концентрация углекислого газа составила 0,2 моль/л.
Определите равновесные концентрации СН4 (X) и СО (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
23 / 43
В реактор постоянного объёма поместили некоторое количество пропана и водорода. В результате протекания обратимой реакции
C3H8(г) + 2H2(г) ↔ 3CH4(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации пропана и водорода составили 0,30 моль/л и 0,50 моль/л соответственно, а равновесная концентрация пропана составила 0,15 моль/л.
Определите равновесные концентрации Н2 (Х) и равновесную концентрацию СН4 (Y).
Выберите из списка номера правильных ответов.
1) 0,20 моль/л 3) 0,30 моль/л 5) 0,40 моль/л
2) 0,25 моль/л 4) 0,35 моль/л 6) 0,45 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
24 / 43
В реактор постоянного объёма поместили некоторое количество оксида углерода(II) и водорода. В результате протекания обратимой реакции
CO(г) + 3H2(г) ↔ СH4(г) + H2O(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CО составила 0,5 моль/л, а равновесные концентрации Н2, СН4 и Н2О составили 0,1 моль/л, 0,2 моль/л и 0,2 моль/л соответственно.
Определите равновесную концентрацию СО (Х) и исходную концентрацию Н2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,5 моль/л 5) 0,9 моль/л
2) 0,3 моль/л 4) 0,7 моль/л 6) 1,1 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
25 / 43
В реактор постоянного объёма поместили некоторое количество пропана и водяного пара. В результате протекания обратимой реакции
C3H8(г) + 3H2O(г) ↔ 3СO(г) + 7H2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации С3Н8, Н2О и СО составили 0,2 моль/л, 0,2 моль/л и 0,6 моль/л соответственно.
Определите исходную концентрацию С3Н8 (Х) и равновесную концентрацию Н2 (Y).
Выберите из списка номера правильных ответов.
1) 0,4 моль/л 3) 0,8 моль/л 5) 1,2 моль/л
2) 0,6 моль/л 4) 1,0 моль/л 6) 1,4 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
26 / 43
В реактор постоянного объёма поместили некоторое количество порошка графита и водяного пара. В результате протекания обратимой реакции
C(тв.) + H2O(г) ↔ H2(г) + СO(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации Н2О и Н2 составили 0,2 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию Н2О (Х) и равновесную концентрацию СО (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
27 / 43
В реактор постоянного объёма поместили некоторое количество S2Cl2 и водорода. В результате протекания обратимой реакции
S2Cl2(г) + H2(г) ↔ 2HCl(г) + 2S(ж)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация S2Cl2 составила 0,4 моль/л, а равновесные концентрации S2Cl2 и Н2 составили 0,2 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию Н2 (Х) и равновесную концентрацию НСl (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
28 / 43
В реактор постоянного объёма поместили некоторое количество серы и водяного пара. В результате протекания обратимой реакции
2S(ж) + 2H2O(г) ↔ 2H2S(г) + SO2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация Н2О составила 0,8 моль/л, а равновесная концентрация Н2S составила 0,6 моль/л.
Определите равновесные концентрации H2O (Х) и SO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
29 / 43
В реактор постоянного объёма поместили некоторое количество вещества А. В результате протекания обратимой реакции
3A(г) ↔ 2В(г) + С(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации А и С составили 0,1 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию А (Х) и равновесную концентрацию В (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
30 / 43
В реактор постоянного объёма поместили вещества А и В. В результате протекания обратимой реакции
A(тв.) + 3В(г) ↔ С(г) + 2D(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация В составила 0,9 моль/л, а равновесная концентрация D составила 0,4 моль/л.
Определите равновесные концентрации веществ В (Х) и С (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
31 / 43
В реактор постоянного объёма поместили оксид углерода(II) и водород. В результате протекания обратимой реакции
CO(г) + 2H2(г) = CH3OH(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO составила 0,3 моль/л, равновесная концентрация CO составила 0,1 моль/л, а равновесная концентрация H2 составила 0,8 моль/л.
Определите равновесные концентрации веществ Н2 (Х) и СН3ОН (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
32 / 43
В реактор постоянного объёма поместили кислород и азот и подвергли воздействию электрического тока. В результате протекания обратимой реакции
N2(г) + O2(г) ↔ 2NO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация О2 составила 0,4 моль/л, равновесная концентрация N2 составила 0,3 моль/л, а равновесная концентрация NO составила 0,2 моль/л.
Определите исходную концентрацию N2 (Х) и равновесную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
33 / 43
В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
2CH4(г) + O2(г) ↔ 2CO(г) + 4H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CH4 составила 0,8 моль/л, равновесная концентрация O2 составила 0,2 моль/л, равновесная концентрация CO составила 0,6 моль/л, а равновесная концентрация H2 составила 1,2 моль/л
Определите равновесную концентрацию CH4 (Х) и исходную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
34 / 43
В реактор постоянного объёма поместили оксид углерода(IV) и нагрели. В результате протекания обратимой реакции
2CO2(г) ↔ 2CO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO2 составила 0,23 моль/л, а равновесная концентрация CO2 составила 0,15 моль/л
Определите равновесную концентрацию CO (Х) и равновесную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,02 моль/л 3) 0,08 моль/л 5) 0,20 моль/л
2) 0,04 моль/л 4) 0,15 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
35 / 43
В реактор постоянного объёма поместили некоторое количество оксида углерода(II) и водорода. В результате протекания обратимой реакции
CO(г) + 2H2(г) ↔ CH3OH(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO составила 0,7 моль/л, исходная концентрация H2 составила 0,8 моль/л, а равновесная концентрация H2 составила 0,4 моль/л
Определите равновесную концентрацию CO (Х) и равновесную концентрацию CH3OH (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
36 / 43
В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
2CH4(г) + O2(г) = 2CO(г) + 4H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация O2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,2 моль/л, равновесная концентрация CO составила 0,4 моль/л, а равновесная концентрация H2 составила 0,8 моль/л
Определите исходную концентрацию CH4 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
37 / 43
В реактор постоянного объёма поместили оксид серы(VI) и нагрели. В результате протекания обратимой реакции
2SO3(г) ↔ 2SО2(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация SO3 составила 0,28 моль/л, а равновесная концентрация SO3 составила 0,3 моль/л
Определите равновесную концентрацию SO2 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,02 моль/л 3) 0,08 моль/л 5) 0,2 моль/л
2) 0,04 моль/л 4) 0,15 моль/л 6) 0,3 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
38 / 43
В реактор постоянного объёма поместили угарный газ и хлор. В результате протекания обратимой реакции
CO(г) + Cl2(г) ↔ COCl2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация СО составила 0,4 моль/л, равновесная концентрация Cl2 составила 0,2 моль/л, а равновесная концентрация COCl2 составила 0,3 моль/л
Определите равновесную концентрацию CО (Х) и исходную концентрацию Cl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
39 / 43
В реактор постоянного объёма поместили оксид серы(IV) и кислород. В результате протекания обратимой реакции
2SO2(г) + O2(г) ↔ 2SO3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы(VI) составила 0,6 моль/л, концентрации кислорода и оксида серы(VI) составили 0,3 моль/л и 0,4 моль/л соответственно.
Определите исходную концентрацию SO2 (X) и исходную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
40 / 43
В реактор постоянного объёма поместили метан и углекислый газ. В результате протекания обратимой реакции
CH4(г) + CO2(г) ⇄ 2CO(г) + 2H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,1 моль/л, а равновесная концентрация CO2 составила 0,2 моль/л
Определите исходную концентрацию CH4 (X) и равновесную концентрацию H2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
41 / 43
В реактор постоянного объёма поместили пары циклогексана и нагрели в присутствии катализатора. В результате протекания обратимой реакции
C6H12(г) ⇄ C6H6(г) + 3H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация C6H12 составила 0,3 моль/л, а равновесная концентрация H2 составила 0,3 моль/л
Определите равновесную концентрацию C6H12 (X) и равновесную концентрацию С6H6 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
42 / 43
В реактор постоянного объёма поместили водород и пары брома. В результате протекания обратимой реакции
H2(г) + Br2(г) ⇄ 2HBr(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация H2 составила 0,32 моль/л, равновесная концентрация Br2 составила 0,1 моль/л, а равновесная концентрация HBr составила 0,32 моль/л
Определите равновесную концентрацию H2 (X) и исходную концентрацию Br2 (Y).
Выберите из списка номера правильных ответов.
1) 0,08 моль/л 3) 0,2 моль/л 5) 0,32 моль/л
2) 0,16 моль/л 4) 0,26 моль/л 6) 0,42 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
43 / 43
В реактор постоянного объёма поместили оксид углерода(IV) и кислород. В результате протекания обратимой реакции
2SO2(г) + O2(г) ↔ 2SO3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация SO2 составила 0,6 моль/л, равновесная концентрация O2 составила 0,3 моль/л, а равновесная концентрация SO3 составила 0,4 моль/л
Определите равновесную концентрацию SO2 (Х) и исходную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Ваша оценка
The average score is 8%
Задание 1. В реактор постоянного объёма поместили некоторое количество водорода и паров йода. В результате протекания обратимой реакции
H2(г) + I2(г) ↔ 2HI(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация йода составила 0,9 моль/л, а равновесные концентрации водорода и йода – 0,2 моль/л и 0,6 моль/л соответственно.
Определите исходную концентрацию Н2 (Х) и равновесную концентрацию НI (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 2. В реактор постоянного объёма поместили некоторое количество водорода и углекислого газа. В результате протекания обратимой реакции
H2(г) + СO2(г) ↔ H2O(г) + СO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация водорода составила 0,9 моль/л, а равновесные концентрации углекислого газа, угарного газа и воды – 0,1 моль/л, 0,6 моль/л и 0,6 моль/л соответственно.
Определите равновесную концентрацию Н2 (X) и исходную концентрацию СО2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,5 моль/л 5) 0,9 моль/л
2) 0,3 моль/л 4) 0,7 моль/л 6) 1,1 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 3. В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + O2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида азота (II), кислорода и оксида азота (IV) составила 0,2 моль/л, 0,4 моль/л и 0,8 моль/л соответственно.
Определите исходные концентрации NО (X) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 4. В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + O2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации оксида азота (II) и кислорода составили 0,9 моль/л и 0,5 моль/л соответственно, а равновесная концентрация кислорода – 0,2 моль/л.
Определите равновесные концентрации NO (Х) и NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 5. В реактор постоянного объёма поместили некоторое количество оксида азота(II) и кислорода. В результате протекания обратимой реакции
2NO(г) + О2(г) ↔ 2NO2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация кислорода составила 0,20 моль/л, а равновесные концентрации оксида азота (II) и оксида азота (IV) – 0,05 моль/л и 0,20 моль/л соответственно.
Определите исходную концентрацию NO (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 2) 0,10 моль/л 3) 0,15 моль/л
4) 0,20 моль/л 5) 0,25 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 6. В реактор постоянного объёма поместили некоторое количество оксида азота(IV). В результате протекания обратимой реакции
2NO2 ↔ 2NO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида азота (IV) составила 1,4 моль/л, а равновесная концентрация оксида азота (II) – 0,8 моль/л.
Определите равновесные концентрации NO2 (Х) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 7. В реактор постоянного объёма поместили некоторое количество оксида азота(IV). В результате протекания обратимой реакции
2NO2(г) ↔ 2NO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида азота (IV) и кислорода составили 0,4 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию NO2 (Х) и равновесную концентрацию NO (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 8. В реактор постоянного объёма поместили некоторое количество оксида серы(IV). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы (VI) составила 0,8 моль/л, а равновесная концентрация оксида серы (IV) – 0,6 моль/л.
Определите равновесные концентрации SO3 (Х) и O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 9. В реактор постоянного объёма поместили некоторое количество оксида серы(VI). В результате протекания обратимой реакции
2SO3(г) ↔ 2SO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации оксида серы (VI) и оксида серы (IV) составили 0,05 моль/л и 0,20 моль/л соответственно.
Определите исходную концентрацию SO3 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 10. В реактор постоянного объёма поместили некоторое количество оксида азота(II) и хлора. В результате протекания обратимой реакции
2NO(г) + Cl2(г) ↔ 2NOCl(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация хлора составила 0,15 моль/л, а равновесные концентрации оксида азота (II) и хлора составили 0,05 моль/л и 0,05 моль/л соответственно.
Определите исходную концентрацию NO (Х) и равновесную концентрацию NOCl (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 11. В реактор постоянного объёма поместили некоторое количество диоксида серы и озона. В результате протекания обратимой реакции
SO2(г) + О3 ↔ SO3(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация озона составила 0,4 моль/л, а равновесные концентрации оксида серы (IV), оксида серы (VI) и кислорода составили 0,2 моль/л, 0,3 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию SO2 (Х) и равновесную концентрацию О3 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 12. В реактор постоянного объёма поместили некоторое количество диоксида серы и диоксида азота. В результате протекания обратимой реакции
SO2(г) + NO2(г) ↔ SO3(г) + NO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы (IV) составила 0,5 моль/л, а равновесные концентрации оксида азота (IV) и оксида азота (II) составили 0,1 моль/л и 0,3 моль/л соответственно.
Определите равновесную концентрацию SO2 (Х) и исходную концентрацию NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 13. В реактор постоянного объёма поместили некоторое количество монооксида азота и озона. В результате протекания обратимой реакции
NO(г) + О3(г) ↔ NO2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации оксида азота (II) и кислорода составили 0,25 моль/л и 0,3 моль/л соответственно, а равновесная концентрации оксида азота (II) составила 0,05 моль/л.
Определите равновесные концентрации О3 (Х) и NO2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 14. В реактор постоянного объёма поместили некоторое количество диоксида хлора. В результате протекания обратимой реакции
ClO2(г) ↔ 1/2Cl2(г) + О2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация ClO2 составила 0,7 моль/л, а равновесная концентрация кислорода – 0,4 моль/л.
Определите равновесные концентрации ClO2 (Х) и Сl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 15. В реактор постоянного объёма поместили некоторое количество фторида азота(III). В результате протекания обратимой реакции
2NF3(г) ↔ N2(г) + 3F2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация NF3 составила 0,8 моль/л, а равновесная концентрация фтора – 0,6 моль/л.
Определите равновесные концентрации NF3 (Х) и N2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 16. В реактор постоянного объёма поместили некоторое количество азота и фтора. В результате протекания обратимой реакции
N2(г) + 3F2(г) ↔2NF3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация фтора составила 1,2 моль/л, а равновесные концентрации азота и NF3 составили 0,2 моль/л и 0,4 моль/л соответственно.
Определите исходную концентрацию N2 (Х) и равновесную концентрацию F2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 17. В реактор постоянного объёма поместили некоторое количество оксида хлора(I). В результате протекания обратимой реакции
4Cl2O(г) ↔ 2Сl2(г) + 2ClO2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации Cl2O и ClO2 составили 0,05 моль/л и 0,10 моль/л соответственно.
Определите исходную концентрацию Cl2O (Х) и равновесную концентрацию Cl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,05 моль/л 3) 0,15 моль/л 5) 0,25 моль/л
2) 0,10 моль/л 4) 0,20 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 18. В реактор постоянного объёма поместили некоторое количество фторида хлора(I). В результате протекания обратимой реакции
3ClF(г) ↔ СlF3(г) + Сl2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации ClF и Cl2 составили 0,2 моль/л и 0,1 моль/л соответственно.
Определите исходную концентрацию СlF (Х) и равновесную концентрацию СlF3 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 19. В реактор постоянного объёма поместили некоторое количество трифторида хлора. В результате протекания обратимой реакции
2ClF3(г) ↔ Сl2(г) + 3F2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации ClF3 и Cl2 составили 0,1 моль/л и 0,2 моль/л соответственно.
Определите исходную концентрацию СlF3 (Х) и равновесную концентрацию F2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 20. В реактор постоянного объёма поместили некоторое количество хлора и трифторида хлора. В результате протекания обратимой реакции
ClF3(г) + Сl2(г) ↔ 3СlF(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации ClF3 и Cl2 составили 0,45 моль/л и 0,35 моль/л соответственно, а равновесная концентрация ClF3 составила 0,30 моль/л.
Определите равновесные концентрации Cl2 (Х) и ClF (Y)
Выберите из списка номера правильных ответов.
1) 0,20 моль/л 3) 0,30 моль/л 5) 0,40 моль/л
2) 0,25 моль/л 4) 0,35 моль/л 6) 0,45 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 21. В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
CH4(г) + 1/2O2(г) ↔ СO(г) + 2H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CH4 составила 0,8 моль/л, а равновесные концентрации кислорода, угарного газа и водорода составили 0,2 моль/л, 0,6 моль/л и 1,2 моль/л соответственно.
Определите равновесную концентрацию СН4 (Х) и исходную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 22. В реактор постоянного объёма поместили некоторое количество метана и углекислого газа. В результате протекания обратимой реакции
1/2CH4(г) + 1/2CO2(г) ↔ СO(г) + H2(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации метана и углекислого газа составили 0,7 моль/л и 0,5 моль/л соответственно, а равновесная концентрация углекислого газа составила 0,2 моль/л.
Определите равновесные концентрации СН4 (X) и СО (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 23. В реактор постоянного объёма поместили некоторое количество пропана и водорода. В результате протекания обратимой реакции
C3H8(г) + 2H2(г) ↔ 3CH4(г)
в реакционной системе установилось химическое равновесие. При этом исходные концентрации пропана и водорода составили 0,30 моль/л и 0,50 моль/л соответственно, а равновесная концентрация пропана составила 0,15 моль/л.
Определите равновесные концентрации Н2 (Х) и равновесную концентрацию СН4 (Y).
Выберите из списка номера правильных ответов.
1) 0,20 моль/л 3) 0,30 моль/л 5) 0,40 моль/л
2) 0,25 моль/л 4) 0,35 моль/л 6) 0,45 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 24. В реактор постоянного объёма поместили некоторое количество оксида углерода(II) и водорода. В результате протекания обратимой реакции
CO(г) + 3H2(г) ↔ СH4(г) + H2O(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CО составила 0,5 моль/л, а равновесные концентрации Н2, СН4 и Н2О составили 0,1 моль/л, 0,2 моль/л и 0,2 моль/л соответственно.
Определите равновесную концентрацию СО (Х) и исходную концентрацию Н2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,5 моль/л 5) 0,9 моль/л
2) 0,3 моль/л 4) 0,7 моль/л 6) 1,1 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 25. В реактор постоянного объёма поместили некоторое количество пропана и водяного пара. В результате протекания обратимой реакции
C3H8(г) + 3H2O(г) ↔ 3СO(г) + 7H2(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации С3Н8, Н2О и СО составили 0,2 моль/л, 0,2 моль/л и 0,6 моль/л соответственно.
Определите исходную концентрацию С3Н8 (Х) и равновесную концентрацию Н2 (Y).
Выберите из списка номера правильных ответов.
1) 0,4 моль/л 3) 0,8 моль/л 5) 1,2 моль/л
2) 0,6 моль/л 4) 1,0 моль/л 6) 1,4 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 26. В реактор постоянного объёма поместили некоторое количество порошка графита и водяного пара. В результате протекания обратимой реакции
C(тв.) + H2O(г) ↔ H2(г) + СO(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации Н2О и Н2 составили 0,2 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию Н2О (Х) и равновесную концентрацию СО (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 27. В реактор постоянного объёма поместили некоторое количество S2Cl2 и водорода. В результате протекания обратимой реакции
S2Cl2(г) + H2(г) ↔ 2HCl(г) + 2S(ж)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация S2Cl2 составила 0,4 моль/л, а равновесные концентрации S2Cl2 и Н2 составили 0,2 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию Н2 (Х) и равновесную концентрацию НСl (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 28. В реактор постоянного объёма поместили некоторое количество серы и водяного пара. В результате протекания обратимой реакции
2S(ж) + 2H2O(г) ↔ 2H2S(г) + SO2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация Н2О составила 0,8 моль/л, а равновесная концентрация Н2S составила 0,6 моль/л.
Определите равновесные концентрации H2O (Х) и SO2 (Y)
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 29. В реактор постоянного объёма поместили некоторое количество вещества А. В результате протекания обратимой реакции
3A(г) ↔ 2В(г) + С(г)
в реакционной системе установилось химическое равновесие. При этом равновесные концентрации А и С составили 0,1 моль/л и 0,3 моль/л соответственно.
Определите исходную концентрацию А (Х) и равновесную концентрацию В (Y).
Выберите из списка номера правильных ответов.
1) 0,2 моль/л 3) 0,6 моль/л 5) 1,0 моль/л
2) 0,4 моль/л 4) 0,8 моль/л 6) 1,2 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 30. В реактор постоянного объёма поместили вещества А и В. В результате протекания обратимой реакции
A(тв.) + 3В(г) ↔ С(г) + 2D(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация В составила 0,9 моль/л, а равновесная концентрация D составила 0,4 моль/л.
Определите равновесные концентрации веществ В (Х) и С (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 31. В реактор постоянного объёма поместили оксид углерода(II) и водород. В результате протекания обратимой реакции
CO(г) + 2H2(г) = CH3OH(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO составила 0,3 моль/л, равновесная концентрация CO составила 0,1 моль/л, а равновесная концентрация H2 составила 0,8 моль/л.
Определите равновесные концентрации веществ Н2 (Х) и СН3ОН (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 32. В реактор постоянного объёма поместили кислород и азот и подвергли воздействию электрического тока. В результате протекания обратимой реакции
N2(г) + O2(г) ↔ 2NO(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация О2 составила 0,4 моль/л, равновесная концентрация N2 составила 0,3 моль/л, а равновесная концентрация NO составила 0,2 моль/л.
Определите исходную концентрацию N2 (Х) и равновесную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 33. В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
2CH4(г) + O2(г) ↔ 2CO(г) + 4H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CH4 составила 0,8 моль/л, равновесная концентрация O2 составила 0,2 моль/л, равновесная концентрация CO составила 0,6 моль/л, а равновесная концентрация H2 составила 1,2 моль/л
Определите равновесную концентрацию CH4 (Х) и исходную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 34. В реактор постоянного объёма поместили угарный газ и хлор. В результате протекания обратимой реакции
CO(г) + Cl2(г) ↔ COCl2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация СО составила 0,4 моль/л, равновесная концентрация Cl2 составила 0,2 моль/л, а равновесная концентрация COCl2 составила 0,3 моль/л
Определите равновесную концентрацию CО (Х) и исходную концентрацию Cl2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 35. В реактор постоянного объёма поместили оксид серы(VI) и нагрели. В результате протекания обратимой реакции
2SO3(г) ↔ 2SО2(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация SO3 составила 0,28 моль/л, а равновесная концентрация SO3 составила 0,3 моль/л
Определите равновесную концентрацию SO2 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,02 моль/л 3) 0,08 моль/л 5) 0,2 моль/л
2) 0,04 моль/л 4) 0,15 моль/л 6) 0,3 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 36. В реактор постоянного объёма поместили некоторое количество метана и кислорода. В результате протекания обратимой реакции
2CH4(г) + O2(г) = 2CO(г) + 4H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация O2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,2 моль/л, равновесная концентрация CO составила 0,4 моль/л, а равновесная концентрация H2 составила 0,8 моль/л
Определите исходную концентрацию CH4 (Х) и равновесную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 37. В реактор постоянного объёма поместили некоторое количество оксида углерода(II) и водорода. В результате протекания обратимой реакции
CO(г) + 2H2(г) ↔ CH3OH(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO составила 0,7 моль/л, исходная концентрация H2 составила 0,8 моль/л, а равновесная концентрация H2 составила 0,4 моль/л
Определите равновесную концентрацию CO (Х) и равновесную концентрацию CH3OH (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 38. В реактор постоянного объёма поместили оксид углерода(IV) и нагрели. В результате протекания обратимой реакции
2CO2(г) ↔ 2CO(г) + O2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO2 составила 0,23 моль/л, а равновесная концентрация CO2 составила 0,15 моль/л
Определите равновесную концентрацию CO (Х) и равновесную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,02 моль/л 3) 0,08 моль/л 5) 0,20 моль/л
2) 0,04 моль/л 4) 0,15 моль/л 6) 0,30 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 39. В реактор постоянного объёма поместили оксид углерода(IV) и кислород. В результате протекания обратимой реакции
2SO2(г) + O2(г) ↔ 2SO3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация SO2 составила 0,6 моль/л, равновесная концентрация O2 составила 0,3 моль/л, а равновесная концентрация SO3 составила 0,4 моль/л
Определите равновесную концентрацию SO2 (Х) и исходную концентрацию O2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 40. В реактор постоянного объёма поместили водород и пары брома. В результате протекания обратимой реакции
H2(г) + Br2(г) ⇄ 2HBr(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация H2 составила 0,32 моль/л, равновесная концентрация Br2 составила 0,1 моль/л, а равновесная концентрация HBr составила 0,32 моль/л
Определите равновесную концентрацию H2 (X) и исходную концентрацию Br2 (Y).
Выберите из списка номера правильных ответов.
1) 0,08 моль/л 3) 0,2 моль/л 5) 0,32 моль/л
2) 0,16 моль/л 4) 0,26 моль/л 6) 0,42 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 41. В реактор постоянного объёма поместили пары циклогексана и нагрели в присутствии катализатора. В результате протекания обратимой реакции
C6H12(г) ⇄ C6H6(г) + 3H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация C6H12 составила 0,3 моль/л, а равновесная концентрация H2 составила 0,3 моль/л
Определите равновесную концентрацию C6H12 (X) и равновесную концентрацию С6H6 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 42. В реактор постоянного объёма поместили метан и углекислый газ. В результате протекания обратимой реакции
CH4(г) + CO2(г) ⇄ 2CO(г) + 2H2(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация CO2 составила 0,5 моль/л, равновесная концентрация CH4 составила 0,1 моль/л, а равновесная концентрация CO2 составила 0,2 моль/л
Определите исходную концентрацию CH4 (X) и равновесную концентрацию H2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Задание 43. В реактор постоянного объёма поместили оксид серы(IV) и кислород. В результате протекания обратимой реакции
2SO2(г) + O2(г) ↔ 2SO3(г)
в реакционной системе установилось химическое равновесие. При этом исходная концентрация оксида серы(VI) составила 0,6 моль/л, концентрации кислорода и оксида серы(VI) составили 0,3 моль/л и 0,4 моль/л соответственно.
Определите исходную концентрацию SO2 (X) и исходную концентрацию О2 (Y).
Выберите из списка номера правильных ответов.
1) 0,1 моль/л 3) 0,3 моль/л 5) 0,5 моль/л
2) 0,2 моль/л 4) 0,4 моль/л 6) 0,6 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.