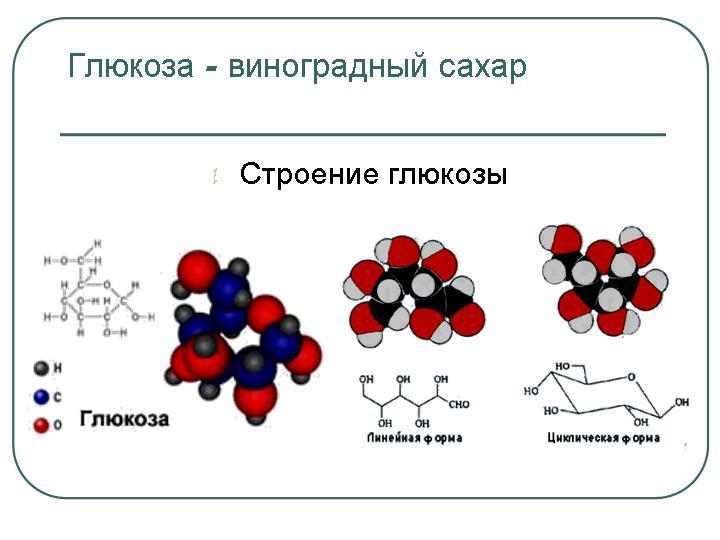
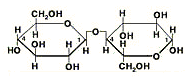
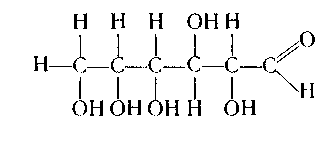Углеводы — группа природных органических соединений, химическая структура которых отвечает формуле
Cm(H2O)n. Входят в состав всех без исключения живых организмов.

Классификация
Углеводы подразделяются на
- Моносахариды
- Олигосахариды
- Полисахариды
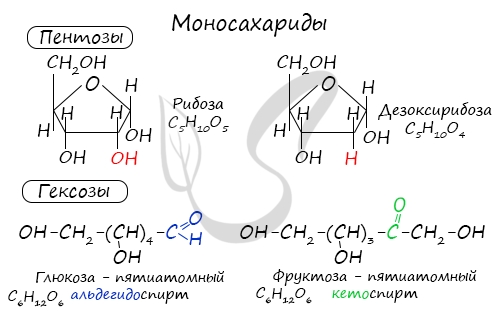
Моносахариды (греч. monos — единственный + sacchar — сахар) — наиболее распространенная группа углеводов в природе,
содержащие в молекулах пять (пентозы) или шесть (гексозы) атомов углерода.
Из наиболее известных представителей к пентозам относятся рибоза и дезоксирибоза, к гексозам — глюкоза и фруктоза.
Олигосахариды (греч. ὀλίγος — немногий) — группа углеводов, в молекулах которых, содержится от 2 до 10 моносахаридных
остатков. Если в молекуле содержатся два моносахаридных остатка, ее называют дисахарид.
Наиболее известны следующие дисахариды: сахароза, лактоза, мальтоза. Они являются изомерами, их молекулярная
формула одинакова — C12H22O11.

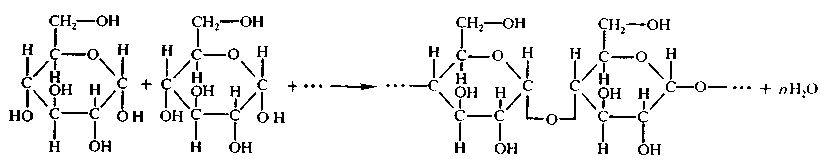
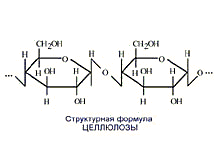
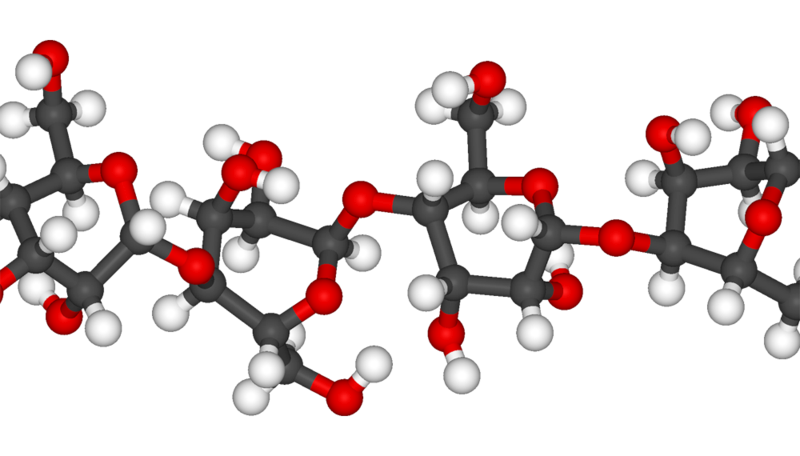
Полисахариды (греч. poly — много) — природные биополимеры, молекулы которых состоят из длинных цепей (десятки, сотни
тысяч) моносахаридов.
Например, глюкоза — моносахарид, а крахмал, гликоген и целлюлоза — ее полимеры. Также к полимерам относится
хитин, пектин. Формула крахмала, целлюлозы — (C6H10O5)n

Моносахариды
Получение глюкозы возможно несколькими способами:
- Реакция Бутлерова
- Гидролиз крахмала
- Фотосинтез
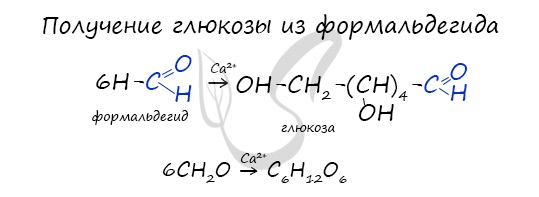
В присутствии ионов металла, молекулы формальдегида соединяются, образуя различные углеводы, например, глюкозу.
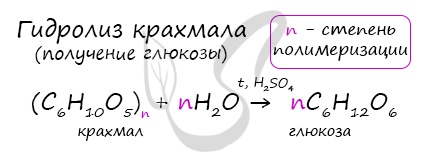
В присутствии кислоты и при нагревании, крахмал (полимер) распадается на мономеры — молекулы глюкозы.
Эту реакцию изобрела природа, для нее существует необыкновенный катализатор — солнечный свет (hν).
6CO2 + 6H2O → (hν) C6H12O6 + 6O2↑
По химическому строению глюкоза является пятиатомным альдегидоспиртом, а, значит, для нее характерны реакции и
альдегидов, и многоатомных спиртов.
- Реакции по альдегидной группе
- Реакции по гидроксогруппам
- Брожение глюкозы
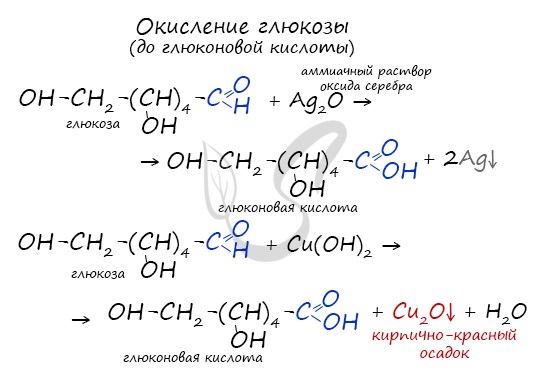
Окисление глюкозы идет до глюконовой кислоты. Это можно осуществить с помощью реакций серебряного зеркала,
с гидроксидом меди II.
Обратите особое внимание на то, что при написании формулы аммиачного раствора в полном виде будет правильнее указать в продуктах не кислоту, а соль — глюконат аммония. Это связано с тем, что аммиак, обладающий основными свойствами, реагирует с глюконовой кислотой с образованием соли.
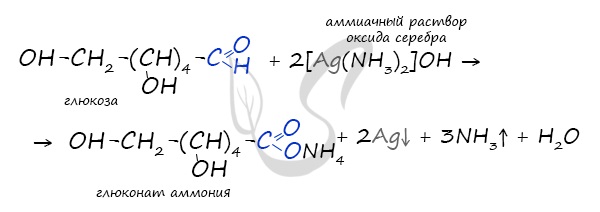
Восстановление глюкозы возможно до шестиатомного спирта сорбита (глюцита), применяемого в пищевой промышленности в
качестве сахарозаменителя. На вкус сорбит менее приятен, менее сладок, чем сахар.
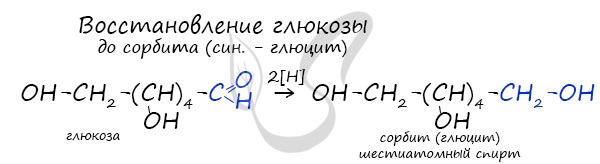
Глюкоза содержит пять гидроксогрупп, является многоатомным спиртом. Она вступает в качественную реакцию
для многоатомных спиртов — со свежеприготовленным гидроксидом меди II.
В результате такой реакции образуется характерное голубое окрашивание раствора.

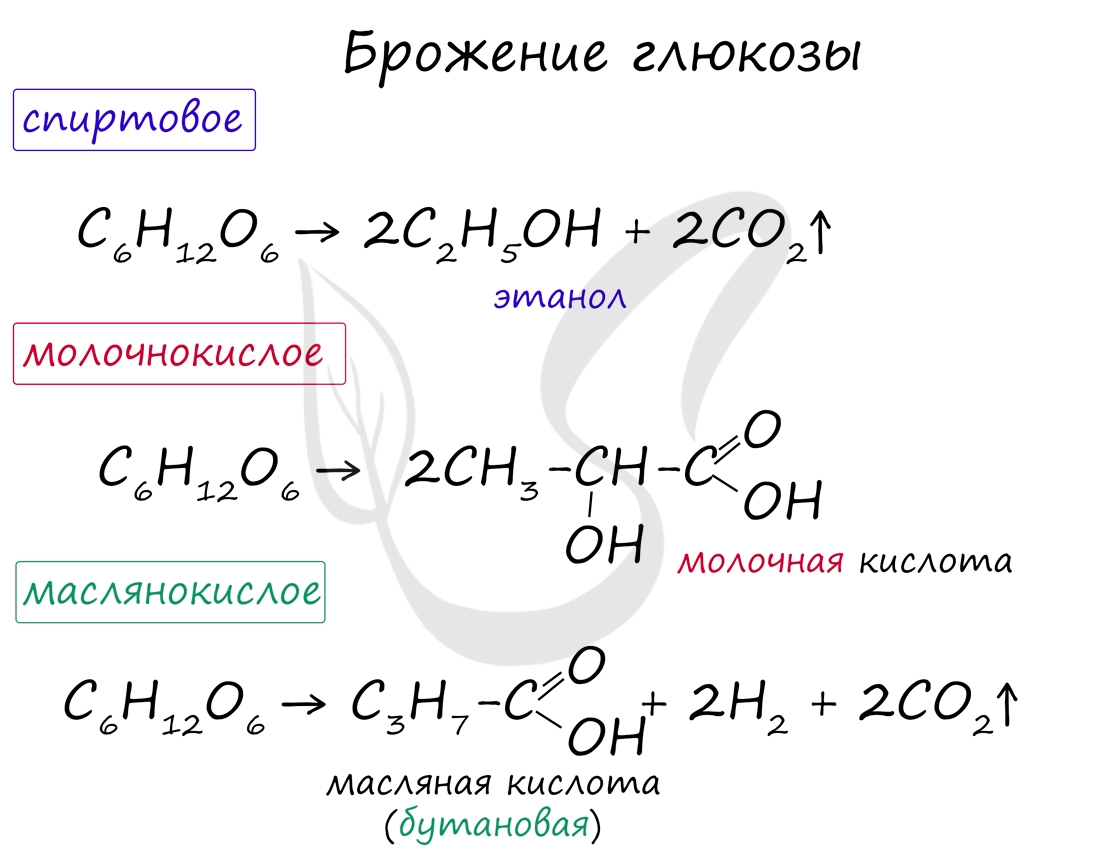
Возможны несколько вариантов брожения глюкозы: спиртовое, молочнокислое, маслянокислое. Эти виды брожения
имеют большое практическое значение и характерны для многих живых организмов, в частности бактерий.
Фруктоза является изомером глюкозы. В отличие от нее не вступает в реакции окисления — она является кетоспиртом,
а кетоны окислению до кислот не подвергаются.
Для нее характерна качественная реакция как многоатомного спирта — со свежеприготовленным гидроксидом меди II.
В реакцию серебряного зеркала фруктоза не вступает.
Применяется фруктоза как сахарозаменитель. Она в 3 раза слаще глюкозы и в 1,5 раза слаще сахарозы.

Дисахариды
Как уже было сказано ранее, наиболее известные дисахариды: сахароза, лактоза и мальтоза — имеют одну и ту же формулу —
C12H22O11.
При их гидролизе получаются различные моносахариды.
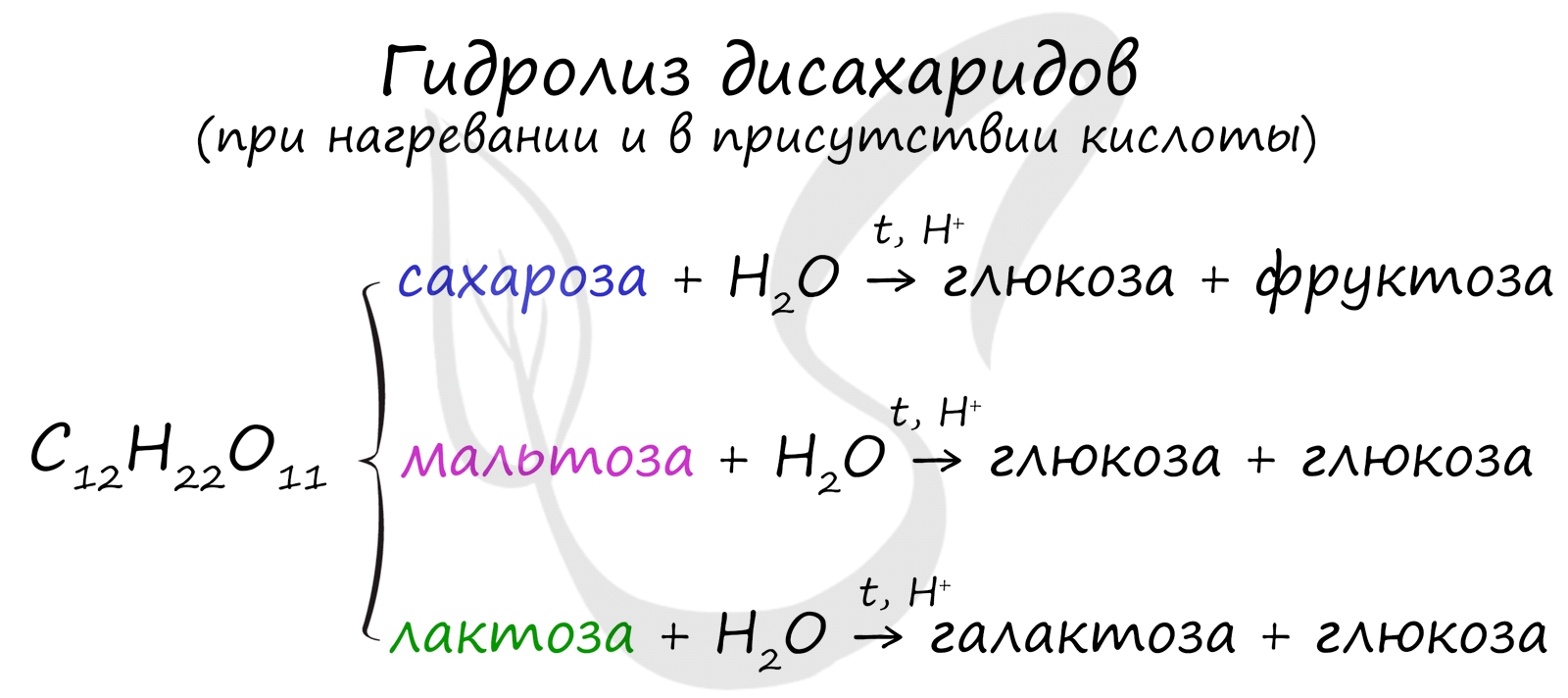
Полисахариды
Из множества реакций, более всего мне хотелось бы выделить гидролиз крахмала. В результате образуется глюкоза.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Теория по теме Углеводы. Краткие конспект по углеводам. Классификация углеводов, химические свойства углеводов, способы получения углеводов. Свойства и получение моносахаридов (глюкоза, фруктоза), олигосахаридов (сахароза и др.), полисахаридов.
Углеводы (сахара) – органические соединения, имеющие сходное строение, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3.
Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4 (на один атом кислорода меньше, чем рибоза).
Классификация углеводов
По числу структурных звеньев
- Моносахариды — содержат одно структурное звено.
- Олигосахариды — содержат от 2 до 10 структурных звеньев (дисахариды, трисахариды и др.).
- Полисахариды — содержат n структурных звеньев.
Некоторые важнейшие углеводы:
| Моносахариды | Дисахариды | Полисахариды |
| Глюкоза С6Н12О6
Фруктоза С6Н12О6 Рибоза С5Н10О5 Дезоксирибоза С5Н10О4 |
Сахароза С12Н22О11
Лактоза С12Н22О11 Мальтоза С12Н22О11 Целлобиоза С12Н22О11 |
Целлюлоза (С6Н10О5)n
Крахмал(С6Н10О5)n |
По числу атомов углерода в молекуле
- Пентозы — содержат 5 атомов углерода.
- Гексозы — содержат 6 атомов углерода.
- И т.д.
По размеру кольца в циклической форме молекулы
- Пиранозы — образуют шестичленное кольцо.
- Фуранозы — содержат пятичленное кольцо.
Химические свойства, общие для всех углеводов
1. Горение
Все углеводы горят до углекислого газа и воды.
Например, при горении глюкозы образуются вода и углекислый газ
C6H12O6 + 6O2 → 6CO2 + 6H2O
2. Взаимодействие с концентрированной серной кислотой
Концентрированная серная кислота отнимает воду от углеводов, при этом образуется углерод С («обугливание») и вода.
Например, при действии концентрированной серной кислоты на глюкозу образуются углерод и вода
C6H12O6 → 6C + 6H2O
Моносахариды
Моносахариды – гетерофункциональные соединения, в состав их молекул входит одна карбонильная группа (группа альдегида или кетона) и несколько гидроксильных.
Моносахариды являются структурными звеньями олигосахаридов и полисахаридов.
Важнейшие моносахариды
| Название и формула | Глюкоза
C6H12O6 |
Фруктоза
C6H12O6 |
Рибоза
C5H10O5 |
| Структурная формула |  |
 |
 |
| Классификация |
|
|
|
Глюкоза
Глюкоза – это альдегидоспирт (альдоза).
Она содержит шесть атомов углерода, одну альдегидную и пять гидроксогрупп.
Глюкоза существует в растворах не только в виде линейной, но и циклических формах (альфа и бета), которые являются пиранозными (содержат шесть звеньев):
Химические свойства глюкозы
Водный раствор глюкозы
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими формами — α и β и линейной формой:
Качественная реакция на многоатомные спирты: реакция со свежеосажденным гидроксидом меди (II)
При взаимодействии свежеосажденного гидроксида меди (II) с глюкозой (и другими моносахаридами происходит растворение гидроксида с образованием комплекса синего цвета.
Реакции на карбонильную группу — CH=O
Глюкоза проявляет свойства, характерные для альдегидов.
- Реакция «серебряного зеркала»
- Реакция с гидроксидом меди (II) при нагревании. При взаимодействии глюкозы с гидроксидом меди (II) выпадает красно-кирпичный осадок оксида меди (I):
- Окисление бромной водой. При окислении глюкозы бромной водой образуется глюконовая кислота:
- Также глюкозу можно окислить хлором, бертолетовой солью, азотной кислотой.
Концентрированная азотная кислота окисляет не только альдегидную группу, но и гидроксогруппу на другом конце углеродной цепи.
- Каталитическое гидрирование. При взаимодействии глюкозы с водородом происходит восстановление карбонильной группы до спиртового гидроксила, образуется шестиатомный спирт – сорбит:
- Брожение глюкозы. Брожение — это биохимический процесс, основанный на окислительно-восстановительных превращениях органических соединений в анаэробных условиях.
Спиртовое брожение. При спиртовом брожении глюкозы образуются спирт и углекислый газ:
C6H12O6 → 2C2H5OH + 2CO2
Молочнокислое брожение. При молочнокислом брожении глюкозы образуется молочная кислота:
Маслянокислое брожение. При маслянокислом брожении глюкозы образуется масляная кислота (внезапно):
- Образование эфиров глюкозы (характерно для циклической формы глюкозы).
Глюкоза способна образовывать простые и сложные эфиры.
Наиболее легко происходит замещение полуацетального (гликозидного) гидроксила.
Например, α-D-глюкоза взаимодействует с метанолом.
При этом образуется монометиловый эфир глюкозы (α-O-метил-D-глюкозид):
Простые эфиры глюкозы получили название гликозидов.
В более жестких условиях (например, с CH3-I) возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные эфиры как с минеральными, так и с карбоновыми кислотами.
Например, β-D-глюкоза реагирует с уксусным ангидридом в соотношении 1:5 с образованием пентаацетата глюкозы (β-пентаацетил-D-глюкозы):
Получение глюкозы
Гидролиз крахмала
В присутствии кислот крахмал гидролизуется:
(C6H10O5)n + nH2O → nC6H12O6
Синтез из формальдегида
Реакция была впервые изучена А.М. Бутлеровым. Синтез проходит в присутствии гидроксида кальция:
6CH2=On → C6H12O6
Фотосинтез
В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
6CO2 + 6H2O → C6H12O6 + 6O2
Фруктоза
Фруктоза — структурный изомер глюкозы. Это кетоноспирт (кетоза): она тоже может существовать в циклических формах (фуранозы).
Она содержит шесть атомов углерода, одну кетоновую группу и пять гидроксогрупп.
Фруктоза – кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза.
В свободном виде содержится в мёде и фруктах.
Химические свойства фруктозы связаны с наличием кетонной и пяти гидроксильных групп.
При гидрировании фруктозы также получается сорбит.
Дисахариды
Дисахариды – это углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных или одной полуацетальной и одной спиртовой).
Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Молекула сахарозы состоит из остатков α-глюкозы и β-фруктозы, соединенных друг с другом:
В молекуле сахарозы гликозидный атом углерода глюкозы связан из-за образования кислородного мостика с фруктозой, поэтому сахароза не образует открытую (альдегидную) форму.
Такие дисахариды называют невосстанавливающими, т.е. не способными окисляться.
Сахароза подвергается гидролизу подкисленной водой. При этом образуются глюкоза и фруктоза:
C12H22O11 + H2O → C6H12O6 + C6H12O6
глюкоза фруктоза
Мальтоза С12Н22О11
Это дисахарид, состоящий из двух остатков α-глюкозы, она является промежуточным веществом при гидролизе крахмала.
Мальтоза является восстанавливающим дисахаридом (одно из циклических звеньев может раскрываться в альдегидную группу) и вступает в реакции, характерные для альдегидов.
При гидролизе мальтозы образуется глюкоза.
C12H22O11 + H2O → 2C6H12O6
Полисахариды
Полисахариды — это природные высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные представители — крахмал и целлюлоза — построены из остатков одного моносахарида — глюкозы.
Крахмал и целлюлоза имеют одинаковую молекулярную формулу: (C6H10O5)n, но совершенно различные свойства.
Это объясняется особенностями их пространственного строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из β-глюкозы, которые являются пространственными изомерами и отличаются лишь положением одной гидроксильной группы:
Крахмал
Крахмалом называется полисахарид, построенный из остатков циклической α-глюкозы.
В его состав входят:
- амилоза (внутренняя часть крахмального зерна) – 10-20%
- амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 — 1000 остатков α-глюкозы (средняя молекулярная масса 160 000) и имеет неразветвленное строение.
Амилопектин имеет разветвленное строение и гораздо большую молекулярную массу, чем амилоза.
Свойства крахмала
- Гидролиз крахмала: при кипячении в кислой среде крахмал последовательно гидролизуется:
- Крахмал не дает реакцию “серебряного зеркала” и не восстанавливает гидроксид меди (II).
- Качественная реакция на крахмал: синее окрашивание с раствором йода.
Целлюлоза
Целлюлоза (клетчатка) – наиболее распространенный растительный полисахарид. Цепи целлюлозы построены из остатков β-глюкозы и имеют линейное строение.
Свойства целлюлозы
- Образование сложных эфиров с азотной и уксусной кислотами.
Нитрование целлюлозы.
Так как в звене целлюлозы содержится 3 гидроксильные группы, то при нитровании целлюлозы избытком азотной кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества пироксилина:
Ацилирование целлюлозы.
При действии на целлюлозу уксусного ангидрида (упрощённо-уксусной кислоты) происходит реакция этерификации, при этом возможно участие в реакции 1, 2 и 3 групп ОН.
Получается ацетат целлюлозы – ацетатное волокно.
- Гидролиз целлюлозы.
Целлюлоза, подобно крахмалу, в кислой среде может гидролизоваться, в результате тоже получается глюкоза. Но процесс идёт гораздо труднее.
ГОТОВИМСЯ К ЕГЭ
УГЛЕВОДЫ
Углеводы (сахара) – органические соединения, имеющие сходное строение и свойства, состав
большинства которых отражает формула Cx(H2O)y,
где x, y ≥ 3.
Исключение
составляет дезоксирибоза, которая имеют формулу С5Н10O4.
НЕКОТОРЫЕ ВАЖНЕЙШИЕ УГЛЕВОДЫ
|
Моносахариды |
Олигосахариды |
Полисахариды |
|
Глюкоза С6Н12О6 Фруктоза С6Н12О6 Галактоза С6Н12О6 Рибоза С5Н10О5 Дезоксирибоза С5Н10О4 |
Дисахариды: Сахароза С12Н22О11 Лактоза (молочный сахар) С12Н22О11 Мальтоза (солодовый сахар) С12Н22О11 |
Целлюлоза Крахмал Гликоген |
Физические
свойства
Моно- и олигосахариды – твердые, белые
кристаллические вещества, имеют сладкий вкус, хорошо растворимы в воде.
Полисахариды – твердые, без сладкого вкуса, практически нерастворимые в воде
(кроме крахмала).
Моносахариды
Моносахариды
– гетерофункциональные
соединения, в состав их молекул входит одна карбонильная группа
(альдегидная или кетонная) и несколько гидроксильных.
ГЛЮКОЗА
Строение
В водном растворе глюкозы существует динамическое равновесие между двумя циклическими
формами — α и β и линейной формой:
Циклические α- и
β-формы глюкозы представляют собой пространственные изомеры, отличающиеся положением
полуацетального гидроксила относительно плоскости кольца. В α-глюкозе этот гидроксил находится втранс-положении
к гидроксиметильной группе -СН2ОН,
в β-глюкозе – в цис-положении.
Явление существования веществ в нескольких
взаимопревращающихся изомерных формах было названо А. М. Бутлеровым динамической изомерией.
Позднее это явление было названо таутомерией
В твёрдом состоянии глюкоза имеет циклическое строение.
Обычная кристаллическая глюкоза – это α- форма. В растворе более устойчива
β-форма (при установившемся равновесии на неё приходится более 60% молекул).
Доля альдегидной формы в равновесии незначительна. Это объясняет отсутствие
взаимодействия с фуксинсернистой кислотой (качественная реакция альдегидов).
Для глюкозы кроме явления таутомерии характерны структурная изомерия с кетонами (глюкоза и фруктоза –
структурные межклассовые изомеры) и оптическая
изомерия:
Физические свойства
Глюкоза
– бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на
вкус (лат. «глюкос» – сладкий):
1)
она встречается почти во всех органах растения: в плодах, корнях, листьях,
цветах;
2)
особенно много глюкозы в соке винограда и спелых фруктах, ягодах;
3)
глюкоза есть в животных организмах;
4) в
крови человека ее содержится примерно 0,1 %.
Получение.
В
промышленности
Гидролиз крахмала:
(C6H10O5)n +
nH2O t,H+→ nC6H12O6
крахмал глюкоза
В лаборатории
Из формальдегида (1861 г А.М. Бутлеров):
6 HCOH Ca(OH)2→ C6H12O6
формальдегид
В природе
Фотосинтез:
6CO2 + 6H2O hν, хлорофилл → C6H12O6 + 6O2
Другие способы
Гидролиз дисахаридов:
C12H22O11 + H2O t,H+→ 2 C6H12O6
мальтоза
глюкоза
C12H22O11 + H2O t,H+→ C6H12O6 + C6H12O6
сахароза глюкоза фруктоза
Химические
свойства глюкозы.
1. Реакция комплексообразования с гидроксидом
меди (II).
Глюкоза как многоатомный спирт
При взаимодействии свежеосажденного гидроксида меди (II) с моносахаридами
происходит растворение гидроксида с образованием комплекса синего цвета.
(глюкозат меди (II) – синий
раствор)
2. Глюкоза как
альдегид
а) реакция серебряного зеркала. Образуется соль глюконовой кислоты.
б) реакция с
гидроксидом меди (II) при нагревании. Образуется глюконовая кислота.
в) Глюкозу также
можно окислить до глюконовой кислоты бромной водой, хлором, азотной кислотой
(разб.):
г)
Каталитическое гидрирование глюкозы – происходит
восстановление карбонильной группы до спиртового гидроксила, получается шестиатомный
спирт – сорбит.
д) С NaHSO3 – НЕ реагирует!!!
3. Реакции
брожения.
а) спиртовое брожение C6H12O6
à 2C2H5OH
+ 2CO2
этанол
б) молочнокислое брожение C6H12O6
à 2CH3-CH(OH)-COOH
молочная кислота
в) маслянокислое брожение C6H12O6
à C3H7COOH
+ 2CO2 + 2H2O
масляная кислота
г) лимоннокислое брожение
4. Реакции
образования эфиров глюкозы.
Глюкоза способна образовывать простые и
сложные эфиры. Наиболее легко происходит замещение полуацетального (гликозидного)
гидроксила:
Простые эфиры
получили название гликозидов.
В более жестких условиях (например, с CH3—I )
возможно алкилирование и по другим оставшимся гидроксильным группам.
Моносахариды способны образовывать сложные
эфиры с карбоновыми кислотами (реакция проходит с ангидридами, а не с
самими кислотами) и с минеральными кислотами.
5. Реакция
горения глюкозы.
C6H12O6 +
6О2 à 6CO2 + 6H2O
Фруктоза
Это структурный изомер глюкозы — кетоноспирт:
СН2— СН- СН- СН — С — СН2
| | | | ║ |
OH OH OH OH O OH
Кристаллическое
вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном
виде содержится в мёде и фруктах.
Химические свойства фруктозы обусловлены
наличием кетонной и пяти гидроксильных групп. Так же, как и глюкоза, реагирует с
гидроксидом меди (ярко-синий раствор) без нагревания; образует простые и
сложные эфиры, горит. При гидрировании фруктозы также получается
СОРБИТ. С бромной водой, Сu(OH)2 при нагревании, аммиачным раствором оксида серебра – не
реагирует.
Реакция
восстановления:
Реакция
многоатомных спиртов:
Образование
сложных эфиров:
Дисахариды
Дисахариды – это
углеводы, молекулы которых состоят из двух остатков моносахаридов, соединенных
друг с другом за счет взаимодействия гидроксильных групп (двух полуацетальных
или одной полуацетальной и одной спиртовой).
1.
Сахароза (свекловичный или тростниковый сахар) С12Н22О11
Физические
свойства и нахождение в природе
1.
Она представляет собой бесцветные кристаллы сладкого вкуса, хорошо растворима в
воде.
2.
Температура плавления сахарозы 160 °C.
3.
При застывании расплавленной сахарозы образуется аморфная прозрачная масса – карамель.
4.
Содержится во многих растениях: в соке березы, клена, в моркови, дыне, а также
в сахарной свекле и сахарном тростнике.
Строение
Молекула сахарозы состоит из
остатков α-глюкозы и β-фруктозы, соединенных друг с другом.
Химические свойства
В молекуле сахарозы гликозидный атом углерода глюкозы СВЯЗАН,
поэтому она не образует ОТКЫТУЮ (альдегидную) форму. (альдегидная группа α-глюкозы, входящей в состав сахарозы,
участвует в образовании связи с β-фруктозой)
Вследствие этого
сахароза не вступает в реакции альдегидной группы – с аммиачным раствором
оксида серебра с гидроксидом меди при нагревании. Подобные дисахариды
называют невосстанавливающими, т.е. не способными окисляться.
Сахароза реагирует
с Сu(OH)2 без нагревания
(ярко-синий раствор), с Са(ОН)2 (образуется сахарат кальция).
Сахароза подвергается гидролизу подкисленной водой:
С12Н22О11
+ Н2О à С6Н12О6 (глюкоза) + С6Н12О6
(фруктоза)
Из числа изомеров сахарозы, имеющих молекулярную формулу
С12Н22О11, можно выделить мальтозу и лактозу.
При гидролизе различные дисахариды расщепляются на
составляющие их моносахариды за счёт разрыва связей между ними (гликозидных
связей):

Таким образом, реакция гидролиза дисахаридов является
обратной процессу их образования из моносахаридов.
Применение
сахарозы
· Продукт питания;
· В кондитерской промышленности;
· Получение искусственного мёда
2. Мальтоза
Это дисахарид, состоящий из двух
остатков α-глюкозы, она является промежуточным веществом при гидролизе
крахмала.
остаток остаток
α-глюкозы α-глюкозы
Мальтоза – является восстанавливающим
дисахаридом и вступает в реакции, характерные для альдегидов.
2.
К восстанавливающим сахаром относятся также целлобиоза
и лактоза
Эти дисахариды так же могут
гидролизоваться.
Полисахариды.
Полисахариды — это природные
высокомолекулярные углеводы, макромолекулы которых состоят из остатков моносахаридов.
Основные
представители — крахмал и целлюлоза — построены из остатков одного моносахарида
— глюкозы. Крахмал и целлюлоза имеют одинаковую молекулярную формулу (C6H10O5)n,
но совершенно различные свойства. Это объясняется особенностями их пространственного
строения.
Крахмал состоит из остатков α-глюкозы, а целлюлоза – из
β-глюкозы, которые являются
пространственными изомерами и отличаются лишь положением одной гидроксильной
группы (выделена цветом):
Крахмал.
Крахмалом
называется смесь двух полисахаридов, построенных из остатков циклической
α-глюкозы.
В его состав входят:
·
амилоза (внутренняя часть крахмального зерна) –
10-20%
·
амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200-1000
остатков α-глюкозы (средняя Mr=160 000) и имеет неразветвленное
строение.
Макромолекула амилозы представляет собой
спираль, каждый виток которой состоит из 6 звеньев α-глюкозы.
Свойства
крахмала:
1.
Гидролиз крахмала: при
кипячении в кислой среде крахмал последовательно гидролизуется.
2. Крахмал не
дает реакцию “серебряного зеркала” и не восстанавливает гидроксид
меди (II).
3. Качественная
реакция на крахмал: синее окрашивание с раствором йода.
Получение
Получают крахмал из природных
крахмалосодержащих продуктов, чаще всего картофеля и кукурузы. Он широко
используется в качестве продукта питания, а также как сырье для производства
глюкозы и этилового спирта.
Целлюлоза
Физические
свойства
Это вещество белого цвета, без вкуса и запаха,
нерастворимое в воде, имеющее волокнистое строение. Растворяется в аммиачном
растворе гидроксида меди (II)
Нахождение
в природе
Этот биополимер обладает большой механической прочностью
и выполняет роль опорного материала растений, образуя стенку растительных
клеток. В большом количестве целлюлоза содержится в тканях древесины (40-55%),
в волокнах льна (60-85%) и хлопка (95-98%). Основная составная часть оболочки
растительных клеток. Образуется в растениях в процессе фотосинтеза.
Древесина состоит на 50% из целлюлозы, а хлопок и лён,
конопля практически чистая целлюлоза.
Хитин (аналог целлюлозы) – основной компонент наружного
скелета членистоногих и других беспозвоночных, а также в составе клеточных
стенок грибов и бактерий.
Получение
Получают
из древесины
Целлюлоза
(клетчатка) – наиболее
распространенный растительный полисахарид. Цепи целлюлозы построены из остатков
β-глюкозы и имеют линейное строение.
Молекулярная масса целлюлозы – от 400 000 до 2
млн.
Свойства
целлюлозы.
1. Горение
(С6Н10О5)n
+ О2 à CO2
+ Н2О
Без доступа кислорода – до угля и воды
(С6Н10О5)n
à C + Н2О
2. С йодом целлюлоза сине-фиолетовое окрашивание не дает.
3. Образование сложных
эфиров с азотной и уксусной кислотами.
а) нитрование целлюлозы. Т.к. в звене
целлюлозы содержится 3 гидроксильные группы, то при нитровании избытком азотной
кислоты возможно образование тринитрата целлюлозы, взрывчатого вещества
пироксилина:
(С6Н7О2(ОН)3)n + 3n HNO3 à 3nH2O + (С6Н7О2(ОNO2)3)n
целлюлоза тринитрат
целлюлозы (пироксилин)
б) ацилирование целлюлозы. При действии на
целлюлозу уксусного ангидрида происходит реакция этерификации, при этом
возможно участие в реакции 1, 2 и 3 групп ОН. Получается ацетат целлюлозы – ацетатное
волокно.
(С6Н7О2(ОН)3)n +3n(СН3СО)2Оà
3nСН3-СООН + (С6Н7О2(ОСОСН3)3)n
целлюлоза уксусный ангидрид
уксусная кислота триацетат целлюлозы
|
|
+ 3n |
|
→ |
|
+ 3n СH3СOOН |
4. Гидролиз
целлюлозы.
Целлюлоза, подобно крахмалу, в кислой
среде гидролизуется:
Применение
Целлюлоза
используется в производстве бумаги, искусственных волокон, пленок, пластмасс,
лакокрасочных материалов, бездымного пороха, взрывчатки, твердого ракетного
топлива, для получения гидролизного спирта и др.
· Получение ацетатного шёлка –
искусственное волокно, оргстекла, негорючей плёнки из ацетилцеллюлозы.
· Получение бездымного пороха из
триацетилцеллюлозы (пироксилин).
· Получение коллодия (плотная плёнка для
медицины) и целлулоида ( изготовление киноленты, игрушек) из
диацетилцеллюлозы.
· Изготовление нитей, канатов, бумаги.
· Получение глюкозы, этилового спирта
(для получения каучука)
25 марта 2022
В закладки
Обсудить
Жалоба
Углеводы
Конспект по химии.
Углеводы (сахара) – органические соединения, имеющие сходное строение и свойства, состав большинства которых отражает формула Cx(H2O)y, где x, y ≥ 3. Исключение составляет дезоксирибоза, которая имеют формулу С5Н10O4.
ugl.doc
ugl.pdf
Автор: Скиба Ольга Николаевна.
3.8.3. Углеводы (моносахариды, дисахариды, полисахариды).
Углеводы — органические соединения, чаще всего природного происхождения, состоящие только из углерода, водорода и кислорода.
Углеводы играют огромную роль в жизнедеятельности всех живых организмов.
Свое название данный класс органических соединений получил за то, что первые изученные человеком углеводы имели общую формулу вида Cx(H2O)y . Т.е. их условно посчитали соединениями углерода и воды. Однако позднее оказалось, что состав некоторых углеводов отклоняется от этой формулы. Например, такой углевод как дезоксирибоза имеет формулу С5Н10О4. В то же время существуют некоторые соединения, формально соответствующие формуле Cx(H2O)y, однако к углеводам не относящиеся, как, например, формальдегид (СН2О) и уксусная кислота (С2Н4О2).
Тем не менее, термин «углеводы» исторически закрепился за данным классом соединений, в связи с чем повсеместно используется и в наше время.
Классификация углеводов
В зависимости от способности углеводов расщепляться при гидролизе на другие углеводы с меньшей молекулярной массой их делят на простые (моносахариды) и сложные (дисахариды, олигосахариды, полисахариды).
Как легко догадаться, из простых углеводов, т.е. моносахаридов, нельзя гидролизом получить углеводы с еще меньшей молекулярной массой.
При гидролизе одной молекулы дисахарида образуются две молекулы моносахарида, а при полном гидролизе одной молекулы любого полисахарида получается множество молекул моносахаридов.
Химические свойства моносахаридов на примере глюкозы и фруктозы
Самыми распространенными моносахаридами являются глюкоза и фруктоза, имеющие следующие структурные формулы:
Как можно заметить, и в молекуле глюкозы, и в молекуле фруктозы присутствует по 5 гидроксильных групп, в связи с чем их можно считать многоатомными спиртами.
В составе молекулы глюкозы имеется альдегидная группа, т.е. фактически глюкоза является многоатомным альдегидоспиртом.
В случае фруктозы можно обнаружить в ее молекуле кетонную группу, т.е. фруктоза является многоатомным кетоспиртом.
Химические свойства глюкозы и фруктозы как карбонильных соединений
Все моносахариды могут реагировать в присутствии катализаторов с водородом. При этом карбонильная группа восстанавливается до спиртовой гидроксильной. Так, в частности, гидрированием глюкозы в промышленности получают искусственный подсластитель – гексаатомный спирт сорбит:
Молекула глюкозы содержит в своем составе альдегидную группу, в связи с чем логично предположить, что ее водные растворы дают качественные реакции на альдегиды. И действительно, при нагревании водного раствора глюкозы со свежеосажденным гидроксидом меди (II) так же, как и в случае любого другого альдегида, наблюдается выпадение из раствора кирпично-красного осадка оксида меди (I). При этом альдегидная группа глюкозы окисляется до карбоксильной – образуется глюконовая кислота:
Также глюкоза вступает и в реакцию «серебряного зеркала» при действии на нее аммиачного раствора оксида серебра. Однако, в отличие от предыдущей реакции вместо глюконовой кислоты образуется ее соль – глюконат аммония, т.к. в растворе присутствует растворенный аммиак:
Фруктоза и другие моносахариды, являющиеся многоатомными кетоспиртами, в качественные реакции на альдегиды не вступают.
Химические свойства глюкозы и фруктозы как многоатомных спиртов
Поскольку моносахариды, в том числе глюкоза и фруктоза, имеют в составе молекул несколько гидроксильных групп. Все они дают качественную реакцию на многоатомные спирты. В частности, в водных растворах моносахаридов растворяется свежеосажденный гидроксид меди (II). При этом вместо голубого осадка Cu(OH)2 образуется темно-синий раствор комплексных соединений меди.
Реакции брожения глюкозы
Спиртовое брожение
При действии на глюкозу некоторых ферментов глюкоза способна превращаться в этиловый спирт и углекислый газ:
Молочнокислое брожение
Помимо спиртового типа брожения существует также и немало других. Например, молочнокислое брожение, которое протекает при скисании молока, квашении капусты и огурцов:
Особенности существования моносахаридов в водных растворах
Моносахариды существуют в водном растворе в трех формах – двух циклических (альфа- и бета-) и одной нециклической (обычной). Так, например, в растворе глюкозы существует следующее равновесие:
Как можно видеть, в циклических формах отсутствует альдегидная группа, в связи с тем что она участвует в образовании цикла. На ее основе образуется новая гидроксильная группа, которую называют ацетальным гидроксилом. Аналогичные переходы между циклическими и нециклической формами наблюдаются и для всех других моносахаридов.
Дисахариды. Химические свойства.
Общее описание дисахаридов
Дисахаридами называют углеводы, молекулы которых состоят из двух остатков моносахаридов, связанных между собой за счет конденсации двух полуацетальных гидроксилов либо же одного спиртового гидроксила и одного полуацетального. Связи, образующиеся таким образом между остатками моносахаридов, называют гликозидными. Формулу большинства дисахаридов можно записать как C12H22O11.
Наиболее часто встречающимся дисахаридом является всем знакомый сахар, химиками называемый сахарозой. Молекула данного углевода образована циклическими остатками одной молекулы глюкозы и одной молекулы фруктозы. Связь между остатками дисахаридов в данном случае реализуется за счет отщепления воды от двух полуацетальных гидроксилов:
Поскольку связь между остатками моносахаридов образована при конденсации двух ацетальных гидроксилов, для молекулы сахара невозможно раскрытие ни одного из циклов, т.е. невозможен переход в карбонильную форму. В связи с этим сахароза не способна давать качественные реакции на альдегиды.
Подобного рода дисахариды, которые не дают качественные реакции на альдегиды, называют невосстанавливающими сахарами.
Тем не менее, существуют дисахариды, которые дают качественные реакции на альдегидную группу. Такая ситуация возможна, когда в молекуле дисахарида остался полуацетальный гидроксил из альдегидной группы одной из исходных молекул моносахаридов.
В частности, в реакцию с аммиачным раствором оксида серебра, а также гидроксидом меди (II) подобно альдегидам вступает мальтоза. Связано это с тем, что в её водных растворах существует следующее равновесие:
Как можно видеть, в водных растворах мальтоза существует в виде двух форм – с двумя циклами в молекуле и одним циклом в молекуле и альдегидной группой. По этой причине мальтоза, в отличие от сахарозы, дает качественную реакцию на альдегиды.
Гидролиз дисахаридов
Все дисахариды способны вступать в реакцию гидролиза, катализируемую кислотами, а также различными ферментами. В ходе такой реакции из одной молекулы исходного дисахарида образуется две молекулы моносахарида, которые могут быть как одинаковыми, так и различными в зависимости от состава исходного моносахарида.
Так, например, гидролиз сахарозы приводит к образованию глюкозы и фруктозы в равных количествах:
А при гидролизе мальтозы образуется только глюкоза:
Дисахариды как многоатомные спирты
Дисахариды, являясь многоатомными спиртами, дают соответствующую качественную реакцию с гидроксидом меди (II), т.е. при добавлении их водного раствора ко свежеосажденному гидроксиду меди (II) нерастворимый в воде голубой осадок Cu(OH)2 растворяется с образованием темно-синего раствора.
Полисахариды. Крахмал и целлюлоза
Полисахариды — сложные углеводы, молекулы которых состоят из большого числа остатков моносахаридов, связанных между собой гликозидными связями.
Есть и другое определение полисахаридов:
Полисахаридами называют сложные углеводы, молекулы которых образуют при полном гидролизе большое число молекул моносахаридов.
В общем случае формула полисахаридов может быть записана как (C6H10O5)n.
Крахмал – вещество, представляющее собой белый аморфный порошок, не растворимый в холодной воде и частично растворимый в горячей с образованием коллоидного раствора, называемого в быту крахмальным клейстером.
Крахмал образуется из углекислого газа и воды в процессе фотосинтеза в зеленых частях растений под действием энергии солнечного света. В наибольших количествах крахмал содержится в картофельных клубнях, пшеничных, рисовых и кукурузных зернах. По этой причине указанные источники крахмала и являются сырьем для его получения в промышленности.
Целлюлоза – вещество, в чистом состоянии представляющее собой белый порошок, не растворимый ни в холодной, ни в горячей воде. В отличие от крахмала целлюлоза не образует клейстер. Практически из чистой целлюлозы состоит фильтровальная бумага, хлопковая вата, тополиный пух. И крахмал, и целлюлоза являются продуктами растительного происхождения. Однако, роли, которые они играют в жизни растений, различны. Целлюлоза является в основном строительным материалом, в частности, главным образом ей образованы оболочки растительных клеток. Крахмал же несет в основном запасающую, энергетическую функцию.
Химические свойства крахмала и целлюлозы
Горение
Все полисахариды, в том числе крахмал и целлюлоза, при полном сгорании в кислороде образуют углекислый газ и воду:
Образование глюкозы
При полном гидролизе как крахмала, так и целлюлозы образуется один и тот же моносахарид – глюкоза:
Качественная реакция на крахмал
При действии йода на что-либо, в чем содержится крахмал, появляется синее окрашивание. При нагревании синяя окраска исчезает, при охлаждении появляется вновь.
При сухой перегонке целлюлозы, в частности древесины, происходит ее частичное разложение с образованием таких низкомолекулярных продуктов как метиловый спирт, уксусная кислота, ацетон и т.д.
Поскольку и в молекулах крахмала, и в молекулах целлюлозы имеются спиртовые гидроксильные группы, данные соединения способны вступать в реакции этерификации как с органическими, так и с неорганическими кислотами:
Углеводы подготовка к егэ химия
Углеводы
Углеводы — группа природных органических соединений, химическая структура которых отвечает формуле Cm(H2O)n. Входят в состав всех без исключения живых организмов.
Классификация
Моносахариды (греч. monos — единственный + sacchar — сахар) — наиболее распространенная группа углеводов в природе, содержащие в молекулах пять (пентозы) или шесть (гексозы) атомов углерода.
Из наиболее известных представителей к пентозам относятся рибоза и дезоксирибоза, к гексозам — глюкоза и фруктоза.
Олигосахариды (греч. ὀλίγος — немногий) — группа углеводов, в молекулах которых, содержится от 2 до 10 моносахаридных остатков. Если в молекуле содержатся два моносахаридных остатка, ее называют дисахарид.
Наиболее известны следующие дисахариды: сахароза, лактоза, мальтоза. Они являются изомерами, их молекулярная формула одинакова — C12H22O11.
Полисахариды (греч. poly — много) — природные биополимеры, молекулы которых состоят из длинных цепей (десятки, сотни тысяч) моносахаридов.
Например, глюкоза — моносахарид, а крахмал, гликоген и целлюлоза — ее полимеры. Также к полимерам относится хитин, пектин. Формула крахмала, целлюлозы — (C6H10O5)n
Моносахариды
В присутствии ионов металла, молекулы формальдегида соединяются, образуя различные углеводы, например, глюкозу.
В присутствии кислоты и при нагревании, крахмал (полимер) распадается на мономеры — молекулы глюкозы.
Эту реакцию изобрела природа, для нее существует необыкновенный катализатор — солнечный свет (hν).
- Реакции по альдегидной группе
Окисление глюкозы идет до глюконовой кислоты. Это можно осуществить с помощью реакций серебряного зеркала, с гидроксидом меди II.
Обратите особое внимание на то, что при написании формулы аммиачного раствора в полном виде будет правильнее указать в продуктах не кислоту, а соль — глюконат аммония. Это связано с тем, что аммиак, обладающий основными свойствами, реагирует с глюконовой кислотой с образованием соли.
Восстановление глюкозы возможно до шестиатомного спирта сорбита (глюцита), применяемого в пищевой промышленности в качестве сахарозаменителя. На вкус сорбит менее приятен, менее сладок, чем сахар.
Глюкоза содержит пять гидроксогрупп, является многоатомным спиртом. Она вступает в качественную реакцию для многоатомных спиртов — со свежеприготовленным гидроксидом меди II.
В результате такой реакции образуется характерное голубое окрашивание раствора.
Возможны несколько вариантов брожения глюкозы: спиртовое, молочнокислое, маслянокислое. Эти виды брожения имеют большое практическое значение и характерны для многих живых организмов, в частности бактерий.
Фруктоза является изомером глюкозы. В отличие от нее не вступает в реакции окисления — она является кетоспиртом, а кетоны окислению до кислот не подвергаются.
Для нее характерна качественная реакция как многоатомного спирта — со свежеприготовленным гидроксидом меди II. В реакцию серебряного зеркала фруктоза не вступает.
Применяется фруктоза как сахарозаменитель. Она в 3 раза слаще глюкозы и в 1,5 раза слаще сахарозы.
Дисахариды
Как уже было сказано ранее, наиболее известные дисахариды: сахароза, лактоза и мальтоза — имеют одну и ту же формулу — C12H22O11.
При их гидролизе получаются различные моносахариды.
Полисахариды
Из множества реакций, более всего мне хотелось бы выделить гидролиз крахмала. В результате образуется глюкоза.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
- Реакции по альдегидной группе
Копирование, распространение в том числе путем копирования на другие сайты и ресурсы в Интернете или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону.
Studarium. ru
13.07.2019 1:37:31
2019-07-13 01:37:31
Источники:
Https://studarium. ru/article/192
Углерод, подготовка к ЕГЭ по химии » /> » /> .keyword { color: red; } Углеводы подготовка к егэ химия
Углеводы подготовка к егэ химия
Углерод
Углерод — неметаллический элемент IV группы периодической таблицы Д. И. Менделеева, является важнейшей частью всех органических веществ в природе.
Общая характеристика элементов IVa группы
От C к Pb (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Из элементов IVа группы углерод и кремний относятся к неметаллам, германий, олово и свинец — металлы.
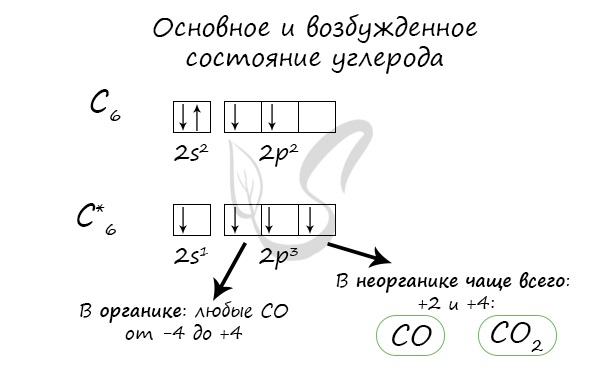
- C — 2s 2 2p 2 Si — 3s 2 3p 2 Ge — 4s 2 4p 2 Sn — 5s 2 5p 2 Pb — 6s 2 6p 2
Природные соединения
- Аллотропных модификаций — графит, алмаз, фуллерен MgCO3 — магнезит CaCO3 — кальцит (мел, мрамор) CaCO3*MgCO3 — доломит
Получение
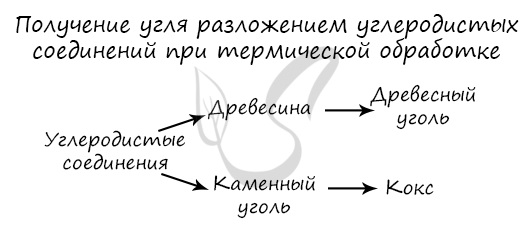
Углерод получают в ходе пиролиза углеводородов (пиролиз — нагревание без доступа кислорода). Также применяется получение углеродистых соединений: древесины и каменного угля.
Химические свойства
- Реакции с неметаллами
При нагревании углерод реагирует со многими неметаллами: водородом, кислородом, фтором.
2С + O2 → (t) 2CO (угарный газ — продукт неполного окисления углерода, образуется при недостатке кислорода)
С + O2 → (t) CO2 (углекислый газ — продукт полного окисления углерода, образуется при достаточном количестве кислорода)
При нагревании углерод реагирует с металлами, проявляя свои окислительные свойства. Напомню, что металлы могут принимать только положительные степени окисления.
Ca + C → CaC2 (карбид кальция, СО углерода = -1)
Al + C → Al4C3 (карбид алюминий, СО углерода -4)
Очевидно, что степень окисления углерода в соединении с различными металлами может отличаться.
Углерод — хороший восстановитель. С помощью него металлургическая промышленность справляется с задачей получения чистых металлов из их оксидов:
Углерод восстанавливает не только металлы из их оксидов, но и неметаллы подобным образом:
SiO2 + C → (t) Si + CO
Может восстановить и собственный оксид:
Известная реакция взаимодействия угля с водяным паром, называемая также газификацией угля, торфа, сланца — крайне важна в промышленности:
В реакциях с кислотами углерод проявляет себя как восстановитель:
Оксид углерода II — СO
Оксид углерода II — продукт неполного окисления углерода. Несолеобразующий оксид. Это чрезвычайно опасное вещество часто образуется при пожарах в замкнутых помещениях, при прогревании машины в гараже.
Растворяясь в крови угарный газ (имеющий в 300 раз большее сродство к гемоглобину, чем кислород) легко выигрывает конкуренцию у кислорода и занимает его место в эритроцитах. Отравление угарным газом нередко заканчивается летальным исходом.
В промышленности угарный газ получают восстановлением оксида углерода IV или газификацией угля (t = 1000 °С).
В лаборатории угарный газ получают при разложении муравьиной кислоты в присутствии серной:
Химические свойства
Полностью окисляется до углекислого газа в реакции с кислородом, восстанавливает оксиды металлов.
FeO + CO → Fe + CO2
Образование карбонилов — чрезвычайно токсичных веществ.
Оксид углерода IV — CO2
Продукт полного окисления углерода. Относится к кислотным оксидам, соответствует угольной кислоте H2CO3. Бесцветный газ, без запаха.
В промышленности углекислый газ получают при разложении известняка, в ходе производства алкоголя, при спиртовом брожении глюкозы.
В лабораторных условиях используют реакцию мела (мрамора) с соляной кислотой.
Углекислый газ образуется при горении органических веществ:
Химические свойства
- Реакция с водой
В результате реакции с водой образуется нестойкая угольная кислота, которая сразу же распадается на воду и углекислый газ.
В ходе реакций с основаниями и основными оксидами углекислый газ образует соли угольной кислоты: средние — карбонаты (при избытке основания), кислые — гидрокарбонаты (при избытке кислотного оксида).
2KOH + CO2 → K2CO3 + H2O (соотношение основание — кислотный оксид 2:1)
KOH + CO2 → KHCO3 (соотношение основание — кислотный оксид 1:1)
При нагревании способен окислять металлы до их оксидов.
Zn + CO2 → (t) ZnO + CO
Угольная кислота
Слабая двухосновная кислота, существующая только в растворах, разлагается на воду и углекислый газ.
Химические свойства
Определить наличие карбонат-иона можно с помощью кислоты: такая реакция сопровождается «закипанием» — появлением пузырьков бесцветного газа без запаха.
Я не раз встречал описание реакций, связанных с этой кислотой, которое заслуживает нашего внимания. В задании было сказано, что при добавлении к раствору гидроксида кальция углекислого газа осадок появлялся, при дальнейшем пропускании углекислого газа — помутнение исчезало.
Это можно легко объяснить, вспомнив про способность угольной кислоты образовывать кислые соли, которые растворимы.
Чтобы сделать из средней соли (карбоната) — кислую соль (гидрокарбонат) нужно добавить угольную кислоту. Однако написать ее формулу H2CO3 — ошибка. Ее следует записать в виде воды и углекислого газа.
Li2CO3 + CO2 + H2O → LiHCO3 (средняя соль + кислота = кислая соль)
Чтобы вернуть среднюю соль, следует добавить к кислой соли щелочь.
При нагревании карбонаты распадаются на соответствующий оксид металла и углекислый газ, гидрокарбонаты — на карбонат металла, углекислый газ и воду.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
- Реакция с водой
Оксид углерода IV — CO2
Химические свойства.
Studarium. ru
19.05.2020 11:32:12
2020-05-19 11:32:12
Источники:
Https://studarium. ru/article/166
Полисахариды. Крахмал и целлюлоза — Углеводы: моносахариды, дисахариды, полисахариды — ОРГАНИЧЕСКАЯ ХИМИЯ » /> » /> .keyword { color: red; } Углеводы подготовка к егэ химия
Полисахариды. Крахмал и целлюлоза — Углеводы: моносахариды, дисахариды, полисахариды — ОРГАНИЧЕСКАЯ ХИМИЯ
Полисахариды. Крахмал и целлюлоза — Углеводы: моносахариды, дисахариды, полисахариды — ОРГАНИЧЕСКАЯ ХИМИЯ
Крахмал — белый аморфный порошок, не растворяется в холодной воде. В горячей воде он разбухает и образует коллоидный раствор — крахмальный клейстер.
Крахмал содержится в цитоплазме растительных клеток в виде зерен запасного питательного вещества. В картофельных клубнях содержится около 20 % крахмала, в пшеничных и кукурузных зернах — около 70 %, а в рисовых — почти 80 %.
Целлюлоза (от лат. cellula — клетка), выделенная из природных материалов (например, вата или фильтровальная бумага), представляет собой твердое волокнистое вещество, нерастворимое в воде.
Оба полисахарида имеют растительное происхождение, однако играют в клетке растений разную роль: целлюлоза — строительную, конструкционную функцию, а крахмал — запасающую. Поэтому целлюлоза является обязательным элементом клеточной оболочки растений. Волокна хлопка содержат до 95 % целлюлозы, волокна льна и конопли — до 80 %, а в древесине ее содержится около 50 %.
Строение крахмала и целлюлозы
Состав этих полисахаридов можно выразить общей формулой (C6H10O5)n. Число повторяющихся звеньев в макромолекуле крахмала может колебаться от нескольких сотен до нескольких тысяч. Целлюлоза же отличается значительно большим числом звеньев и, следовательно, молекулярной массой, которая достигает нескольких миллионов.
— ЗАПОМНИ. В крахмале доля амилозы составляет 10-20 %, а доля амилопектина составляет 80-90 %о. Амилоза крахмала растворяется в горячей воде, а амилопектин только набухает.
Различаются углеводы не только молекулярной массой, но и структурой. Для крахмала характерны два вида структур макромолекул: линейная и разветвленная. Линейную структуру имеют более мелкие макромолекулы той части крахмала, которую называют амилозой, а разветвленную структуру имеют молекулы другой составной части крахмала — амилопектина.
В крахмале на долю амилозы приходится 1020 %, а на долю амилопектина — 80-90 %. Амилоза крахмала растворяется в горячей воде, а амилопектин только набухает.
Структурные звенья крахмала и целлюлозы построены по-разному. Если звено крахмала включает остатки α-глюкозы, то целлюлоза — остатки β-глюкозы, ориентированные в природные волокна:
1. Образование глюкозы. Крахмал и целлюлоза подвергаются гидролизу с образованием глюкозы в присутствии минеральных кислот, например серной:
В пищеварительном тракте животных крахмал подвергается сложному ступенчатому гидролизу:
Крахмал → декстрины → мальтоза → глюкоза
Организм человека не приспособлен к перевариванию целлюлозы, так как не имеет ферментов, необходимых для разрыва связей между остатками β-глюкозы в макромолекуле целлюлозы.
Лишь у термитов и жвачных животных (например, коров) в пищеварительной системе живут микроорганизмы, вырабатывающие необходимые для этого ферменты.
2. Образование сложных эфиров. Крахмал может образовывать эфиры за счет гидроксигрупп, однако эти эфиры не нашли практического применения.
Каждое звено целлюлозы содержит три свободных спиртовых гидроксигруппы. Поэтому общую формулу целлюлозы можно записать таким образом:
За счет этих спиртовых гидроксигрупп целлюлоза и может образовывать сложные эфиры, которые широко применяются.
При обработке целлюлозы смесью азотной и серной кислот получают в зависимости от условий мо — но-, ди — и тринитроцеллюлозу:
Смесь моно — и динитроцеллюлозы называют коллоксилином. Раствор коллоксилина в смеси спирта и диэтилового эфира — коллодий — применяют в медицине для заклеивания небольших ран и для приклеивания повязок к коже.
При высыхании раствора коллоксилина и камфары в спирте получается целлулоид — одна из пластмасс, которая впервые стала широко использоваться в повседневной жизни человека (из нее делают фото — и кинопленку, а также различные предметы широкого потребления). Растворы коллоксилина в органических растворителях применяются в качестве нитролаков. А при добавлении к ним красителей получаются прочные и эстетичные нитрокраски, широко используемые в быту и технике.
Как и другие органические вещества, содержащие в составе молекул нитрогруппы, все виды нитроцеллюлозы огнеопасны. Особенно опасна в этом отношении тринитроцеллюлоза — сильнейшее взрывчатое вещество. Под названием «пироксилин» она широко применяется для производства оружейных снарядов и проведения взрывных работ, а также для получения бездымного пороха.
С уксусной кислотой (в промышленности для этих целей используют более мощное этерифицирующее вещество — уксусный ангидрид) получают аналогичные (ди — и три-) сложные эфиры целлюлозы и уксусной кислоты, которые называются ацетилцеллюлозой:
Ацетилцеллюлозу используют для получения лаков и красок, она служит также сырьем для изготовления искусственного шелка. Для этого ее растворяют в ацетоне, а затем этот раствор продавливают через тонкие отверстия фильер (металлических колпачков с многочисленными отверстиями). Вытекающие струйки раствора обдувают теплым воздухом. При этом ацетон быстро испаряется, а высыхающая ацетилцеллюлоза образует тонкие блестящие нити, которые идут на изготовление пряжи.
Крахмал, в отличие от целлюлозы, дает синее окрашивание при взаимодействии с иодом. Эта реакция является качественной на крахмал или иод в зависимости от того, наличие какого вещества требуется доказать.
Библиотека образовательных материалов для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы из сети Интернет, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
При обработке целлюлозы смесью азотной и серной кислот получают в зависимости от условий мо — но-, ди — и тринитроцеллюлозу.
Compendium. school
26.10.2019 11:55:26
2019-10-26 11:55:26
Источники:
Https://compendium. school/chemistry/universal/97.html
|
Углеводы в зависимости от строения можно подразделить на моносахариды, дисахариды и полисахариды: ( см. приложение 1) 1. Моносахариды: — глюкоза С6Н12О6 — фруктоза С6Н12О6 — рибоза С5Н10О5 Из шестиуглеродных моносахаридов – гексоз – наиболее важное значение имеют глюкоза, фруктоза и галактоза. Если в одной молекуле объединяются два моносахарида, такое соединение называется дисахаридом. 2. Дисахариды: — сахароза С12Н22О11 Сложные углеводы, образованные многими моносахаридами, называются полисахаридами. 3. Полисахариды: — крахмал (С6Н10О5)n — целлюлоза (С6Н10О5)n В молекулах моносахоридов может содержаться от 4-х до 10-ти атомов углерода. Названия всех групп моносахаридов, а также названия отдельных представителей оканчиваются на –оза. Поэтому в зависимости о числа атомов углерода в молекуле моносахариды подразделяют на тетрозы, пентозы, гексозы и т.д. наибольшее значение имеют гексозы и пентозы. Классификация углеводов. |
|
Пентозы |
Гексозы |
Дисахариды |
Полисахариды |
|
Глюкоза Рибоза Дезоксирибоза Арабиноза Ксилоза Ликсоза Рибулоза Ксилулоза |
Глюкоза Галактоза Манноза Гулоза Идоза Талоза Аллоза Альтроза Фруктоза Сорбоза Такатоза Псикоза Фукоза Рамноза |
Сахароза Лактоза Трегалоза Мальтоза Целлобиоза Аллолактоза Гентиобиоза Ксилобиоза Мелибиоза |
Гликоген Крахмал Целлюлоза Хитин Амилоза Амилопектин Стахилоза Инулин Декстрин Пектины |
Животные и человек не способны синтезировать сахара и получают их с различными пищевыми продуктами растительного происхождения.
В растениях углеводы образуются из двуокиси углерода и воды в процессе сложной реакции фотосинтеза, осуществляемой за счет солнечной энергии с участием зелёного пигмента растений — хлорофилла.
I.Моносахариды.
Из шестиуглеродных моносахаридов – гексоз – важное значение имеют глюкоза, фруктоза и галактоза.
Глюкоза.
Основные понятия. Строение молекулы.
Для установления структурной формулы молекулы глюкозы необходимо знать её химические свойства. Экспериментально доказали, что один моль глюкозы реагирует с пятью молями уксусной кислоты с образованием сложного эфира. Это означает, что в молекуле глюкозы имеется пять гидроксильных групп. Так как глюкоза в аммиачном растворе оксида серебра (II) дает реакцию «серебрянного зеркала», то в её молекуле должна быть альдегидная группа.
Опытным путем так же одказали, что глюкоза имеет неразветвленную углеродную цепь. На основании этих данных строение молекулы глюкозы можно выразить следующей формулой:
Как видно из формулы, глюкоза является одновременно многоатомным спиртом а альдегидом, т.е альдегидоспиртом.
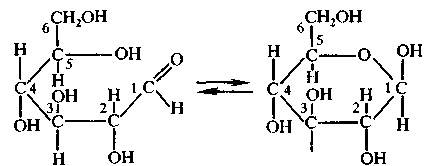
Дальнейшие исследование показали, что кроме молекул с открытой цепью, для глюкозы характерны молекулы циклического строения. Это объясняется тем, что молекулы глюкозы, вследствие вращения атомов углерода вокруг связей могут принимать изогнутую форму и гидроксильная группа 5 углерода может приблизиться к гидроксильной группе. В последней под действием гидроксильной группы разрывается π-связь. К свободной связи присоединяется атом водорода, и образуется шестичленное кольцо, в котором альдегидная группа отсутствует. Доказано, что в водном растворе существуют обе формы молекул глюкозы – альдегидная и циклическая, между которыми устанавливается химическое равновесие:
В молекулах глюкозы с открытой цепью альдегидная группа может свободно вращаться вокруг σ-связи, которая находится между первым и вторым атомами углерода. В молекулах циклической формы такое вращение не возможно. По этой причине циклическая форма молекулы может иметь различное пространственное строение:
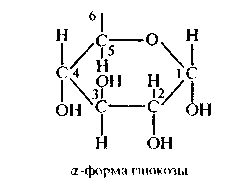
-
α-форма глюкозы — гидроксильные группы (-ОН) при первом и втором атомах углерода расположены по одну сторону кольца.
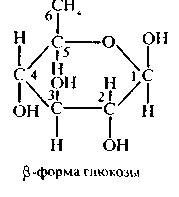
-
б — форма глюкозы — гидроксильные группы находятся по разные стороны кольца молекулы.
Физические свойства.
Глюкоза — бесцветное кристаллическое вещество со сладким вкусом, хорошо растворимое в воде. Из водного раствора кристаллизуется. По сравнению со свекловичным сахаром менее сладкая. Глюкоза пищевая.
Химические свойства.
Глюкоза обладает химическими свойствами, характерными для спиртов (гидроксильная (-ОН) группа) и альдегидов ( группа альдегида (-СНО). Кроме того, она обладает и некоторыми специфическими свойствами.
1. Свойства, характерные для спиртов:
а) взаимодействие с оксидом меди (II):
C6H12O6 + Cu(OH)2 → C6H10O6Cu + H2O
алкоголят меди (II)
б) взаимодействие с карбоновыми кислотами с образованием сложных эфиров (реакция этерификации).
C6H12O6+5CH3COOH→C6H7O6(CH3CO)5
2. Свойства, характерные для альдегидов
а) взаимодействие с оксидом серебра ( I ) в аммиачном растворе (реакция «серебряного зеркала»):
C6H12O6 + Аg2O → C6H12O7 +2Ag↓
глюкоза глюконовая кислота
б)восстановление (гидрирование) — до шестиатомного спирта (сорбита):
C6H12O6 + H2 → C6H14O6
глюкоза сорбит
3. Специфические реакции — брожение:
а) спиртовое брожение (под действием дрожжей):
С6Н12О6 → 2С2Н5ОН + 2СО2
глюкоза этиловый спирт
б) молочнокислые брожение (под действие молочнокислых бактерий):
С6Н12О6 → С3Н6О3
глюкоза молочная кислота
в) маслянокислое брожение:
С6Н12О6 → С3Н7СООН +2Н2 +2СО2
глюкоза масляная кислота
Получение глюкозы.
Первый синтез простейших углеводов из формальдегида в присутствии гидроксида кальция был произведен А.М.Бутлеровым в 1861 году:
са(он)2
6НСОН → С6Н12О6
формальдегид люкоза
На производстве глюкозу чаще всего получают гидролизом крахмала в присутствии серной кислоты:
Н2SО4
(С6Н10О5)n + nН2О → nC6H12O6
крахмал глюкоза
Применение глюкозы.
 Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим превращениям, в результате которых освобождается энергия, которая накопилась в процессе фотосинтеза. Упрощено процесс окисления глюкозы в организме можно выразить следующим уравнением:
Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим превращениям, в результате которых освобождается энергия, которая накопилась в процессе фотосинтеза. Упрощено процесс окисления глюкозы в организме можно выразить следующим уравнением:
С6Н12О6 + 6О2→6СО2+6H2O+Q
Так как глюкоза легко усваивается организмом, ее используют в медицине в качестве укрепляющего лечебного средства. Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников).
Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же, как при силосований кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению.
На практике используется также спиртовое брожение глюкозы, например при производстве пива.
Нахождение в природе и организме человека.
В организме человека глюкоза содержится в мышцах, в крови и в небольших количествах во всех клетках. Много глюкозы находится во фруктах, ягодах, нектаре цветов, особенно много в винограде.
В природе глюкоза образуется в растениях в результате фотосинтеза в присутствии зелёного вещества — хлорофилла, содержащего атом магния. В свободном виде глюкоза содержится почти во всех органах зеленых растений. Особенно ее много в соке винограда, поэтому глюкозу иногда называют виноградным сахаром. Мед в основном состоит из смеси глюкозы с фруктозой.
II Дисахариды. 
Простейшими представителями дисахаридов являются обычный свекловичный или тростниковый сахар — сахароза, солодовый сахар — мальтоза, молочный сахар — лактоза и целлобиоза. Все эти дисахариды имеют одну и туже формулу С12Н22О11. Кристаллы коричневого
(тростникового) сахара
Сахароза.
Основные понятия. Строение молекулы
Опытным путем доказано, что молекулярная формула сахарозы C12H22O11. При исследовании химических свойств сахарозы можно убедиться, что для нее характерна реакция многоатомных спиртов: при взаимодействии с гидроксидом меди (II) образуется ярко-синий раствор. Реакцию «серебряного зеркала» с сахарозой осуществить не удается. Следовательно, в ее молекуле имеются гидроксильные группы, но нет альдегидной.
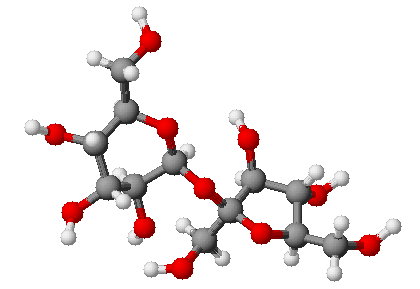
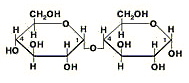
Физические свойства.
Чистая сахароза — бесцветное кристаллическое вещество сладкого вкуса, хорошо растворимое в воде.
Химические свойства.
Главным свойством дисахаридов, отличающим их от моносахаридов, является способность к гидролизу в кислой среде (или под действием ферментов в организме):
С12Н22О11+Н2О→ С6Н12О6+ С6Н12О6
сахароза глюкоза фруктоза
Образовавшуюся в процессе гидролиза глюкозу можно обнаружить реакцией «серебряного зеркала» или при взаимодействии ее с гидроксидом меди (II).
Получение сахарозы.
Сахарозу C12H22O11 (сахар) получают в основном из сахарной свеклы и сахарного тростника. При производстве сахарозы не происходят химические превращения, ибо она уже имеется в природных продуктах. Ее лишь выделяют из этих продуктов по возможности в более чистом виде.

-
Очищенную сахарную свеклу в механических свеклорезках превращают в тонкую стружку и помещают ее вспециальные сосуды — диффузоры, через которые пропускают горячую воду. В результате из свеклы вымывается почти вся сахароза, но вместе с ней в раствор переходят различные кислоты, белки и красящие вещества, которые требуется отделить от сахарозы.
-
Образовавшийся в диффузорах раствор обрабатывают известковым молоком.
С12Н22О11+Ca(OH)2→ С12Н22О11∙2CaO∙H2O

3. Чтобы разложить образовавшийся сахарат кальция и нейтрализовать избыток гидроксида кальция, через их раствор пропускают оксид углерода (IV). В результате кальций осаждается в виде карбоната:
С12Н22О11∙2CaO∙H2O + 2СО2 → С12Н22О11 + 2CaСO3↓ 2Н2О
4. Полученный после осаждения карбоната кальция раствор фильтруют, затем упаривают в вакуумных аппаратах и кристаллики сахара отделяют центрифугированием.
Однако выделить весь сахар из раствора не удается. Остается бурый раствор (меласса), который содержит еще до 50% сахарозы. Мелассу используют для получения лимонной кислоты и некоторых других продуктов.
5. Выделенный сахарный песок обычно имеет желтоватый цвет, так как содержит красящие вещества. Чтобы их отделить, сахарозу вновь растворяют в воде и полученный раствор пропускают через активированный уголь. Затем раствор снова упаривают и подвергают кристаллизации. ( см. приложение 2)
Применение сахарозы.
Сахароза в основном используется в качестве продукта питания и в кондитерской промышленности. Путем гидролиза из нее получают искусственный мед.
Нахождение в природе и организме человека.
Сахароза входит в состав сока сахарной свеклы (16 — 20%) и сахарного тростника (14 — 26%). В небольших количествах она содержится вместе с глюкозой в плодах и листьях многих зеленых растений.
III Полисахариды. Некоторые углеводы представляют собой природные полимеры, состоящие из многих сотен и даже тысяч моносахаридных звеньев, входящих в состав одной макромолекулы. Поэтому такие вещества получили название полисахариды. Наиболее важными среди полисахаридов являются крахмал и целлюлоза. Оба они образуются в растительных клетках из глюкозы, основного продукта процесса фотосинтеза.
Крахмал
Основные понятия. Строение молекулы.
Экспериментально доказано, что химическая формула крахмала (C6H10O5)n, где п достигает нескольких тысяч. Крахмал является природным полимером, молекулы которого состоят из отдельных звеньев C6H10O5. Так как при гидролизе крахмала образуется только глюкоза, то можно сделать вывод, что эти звенья являются остатками молекул α-глюкозы.
Ученым удалось доказать, что макромолекулы крахмала состоят из остатков молекул циклической глюкозы. Процесс образования крахмала можно представить так:
Кроме того, установлено, что крахмал состоит не только из линейных молекул, но и из молекул разветвленной структуры. Этим объясняется зернистое строение крахмала.
Физические свойства.
Крахмал — белый порошок, нерастворимый в холодной воде. В горячей воде он набухает и образует клейстер. В отличие от моно- и олигосахаридов полисахариды не обладают сладким вкусом.
Химические свойства.
-
Качественная реакция на крахмал.
Характерной реакцией крахмала является его взаимодействие с йодом. Если к охлажденному крахмальному клейстеру добавить раствор йода, то появляется синее окрашивание. При нагревании клейстера оно исчезает, а при охлаждении появляется вновь. Этим свойством пользуются при определении крахмала в пищевых продуктах. Так, например, если каплю йода поместить на срез картофеля или ломтик белого хлеба, то появляется синее окрашивание.
-
Реакция гидролиза:
(С6Н6О5)n + nH2O → nC6H12O6
 Получение крахмала.
Получение крахмала.
В промышленности крахмал получают в основном из картофеля, риса или кукурузы.
Применение крахмала.

В промышленности крахмал путем гидролиза превращают в патоку и глюкозу. Для этого его нагревают с разбавленной серной кислотой, избыток которой затем нейтрализуют мелом. Образовавшийся осадок сульфата кальция отфильтровывают, раствор упаривают и выделяют глюкозу. Если гидролиз крахмала не доводить до конца, то образуется смесь декстринов с глюкозой — патока, которую применяют в кондитерской промышленности. Получаемые из крахмала декстрины используются в качестве клея, для загустения красок при нанесении рисунков на ткань.
Крахмал применяется для накрахмаливания белья. Под горячим утюгом происходит частичный гидролиз крахмала и превращение его в декстрины. Последние образуют на ткани плотную пленку, которая придает блеск ткани и предохраняет ее от загрязнения.
Нахождение в природе и организме человека.

В клубнях крахмальные зерна плавают в клеточном соке, поэтому картофель является основным сырьем для получения крахмала. В злаках частицы крахмала плотно склеены белковым веществом клейковиной.
Для организма человека крахмал наряду с сахарозой служит основным поставщиком углеводов — одного из важнейших компонентов пищи. Под действием ферментов крахмал гидролизуется до глюкозы, которая окисляется в клетках до углекислого газа и воды с выделением энергии, необходимой для функционирования живого организма. Из продуктов питания наибольшее количество крахмала содержится в хлебе, макаронных и других мучных изделиях, крупах, картофеле.
Целлюлоза.
Вторым наиболее распространенным в природе полисахаридом является целлюлоза или клетчатка (см. приложение 4).
Основные понятия. Строение молекулы.
.Формула целлюлозы, как и крахмала — (С6Н10О5)n, элементарным звеном этого природного полимера также служат остатки глюкозы. Степень полимеризации у целлюлозы намного больше, чем у крахмала.
Макромолекулы целлюлозы, в отличие от крахмала, состоят из остатков молекул б-глюкозы и имеют только линейное строение. Макромолекулы целлюлозы располагаются в одном направлении и образуют волокна (лен, хлопок, конопля).
 Физические свойства.
Физические свойства.
Чистая целлюлоза — твердое белое вещество, имеющее волокнистую структуру. Она нерастворима в воде и органических растворителях, но хорошо растворяется в аммиачном растворе гидроксида меди (II). Как известно, сладкого вкуса целлюлоза не имеет.
Химические свойства.
-
Горение. Целлюлоза легко горит с образованием углекислого газа и воды.
(С6Н10О5)n + 6nО2 → nСО2 + nН2О + Q
-
Гидролиз. В отличие от крахмала клетчатка гидролизуется с трудом. Только очень длительное кипячение в водных растворах сильных кислот приводит к заметному расщеплению макромолекулы до глюкозы:
(С6Н10О5)n + nH2O → nC6H12O6
-
Образования сложных эфиров. Каждое элементарное звено молекулы целлюлозы имеет три гидроксильные группы, которые могут участвовать в образовании сложных эфиров как с органическими, и с неорганическими кислотами.
Нитраты целлюлозы. При обработке целлюлозы смесью концентрированных азотной и серной кислот (нитрующая смесь) образуются нитраты целлюлозы. В зависимости от условий проведении реакции и соотношения реагирующих веществ можно получить продукт по двум (динитрат) или трем (тринитрат) гидроксильным группам
Получение целлюлозы.
Образцом почти чистой целлюлозы является вата, полученная из очищенного хлопка. Основную массу целлюлозы выделяют из древесины, в которой она содержится вместе с другими веществами. Наиболее распространенным методом получения целлюлозы в нашей стране является так называемый сульфитным. По этому методу, измельченную древесину в присутствии раствора гидросульфита кальция или гидросульфита натрия нагревают в автоклавах при давлении 0,5-0,6 МПа и температуре 150 °С. При этом все другие вещества разрушаются, а целлюлоза выделяется в сравнительно чистом виде. Ее промывают водой, сушат и направляют на дальнейшую переработку, большей частью на производство бумаги.

Применение целлюлозы.
Целлюлоза используется человеком с очень древних времен. Ее применение весьма разнообразно. Из целлюлозы изготавливают многочисленные искусственные волокна, полимерные пленки, пластмассы, бездымный порох, лаки. Большое количество целлюлозы идет на производство бумаги. Большое значение имеют продукты этерификации целлюлозы. Так, например, из ацетилцеллюлозы получают ацетатный шелк. Для этого триацетилцеллюлозу растворяют в смеси дихлорметана и этанола. Образовавшийся вязкий раствор продавливают через фильеры — металлические колпачки с многочисленными отверстиями. Тонкие струи раствора опускаются в шахту, через которую противотоком проходит нагретый воздух. В результате растворитель испаряется и триацетилцеллюлоза выделяется в виде длинных нитей, из которых прядением изготовляют ацетатный шелк .Ацетилцеллюлоза идет также на производство негорючей пленки и органического стекла, пропускающего ультрафиолетовые лучи.
Тринитроцеллюлоза (пироксилин) используется как взрывчатое вещество и для производства бездымного пороха. Для этого тринитроцеллюлозу растворяют в этил-ацетате или в ацетоне. После испарения растворителей компактную массу размельчают и получают бездымный порох. Исторически это был первый полимер, из которого была изготовлена промышленная пластмасса — целлулоид. Ранее пироксилин использовался для изготовления кино- и фотопленки и лаков. Его главный недостаток — легкая горючесть с образованием токсичных оксидов азота.
Динитроцеллюлоза (коллоксилин) применяется также для получения коллодия. В этих целях ее растворяют в смеси спирта и эфира. После испарения растворителей образуется плотная пленка — коллодий, применяемый в медицине. Динитроцеллюлоза идет также на производство пластмассы целлулоида. Его получают путем сплавления ди-нитроцеллюлозы с камфорой.
Нахождение в природе и организме человека.
Целлюлоза является основной частью стенок растений. Относительно чистой целлюлозой являются волокна хлопчатника, джута и конопли. Древесина содержит от 40 до 50% целлюлозы, солома — 30%. Целлюлоза растений служит питательным веществом для травоядных животных, в организме которых имеются расщепляющие клетчатку ферменты. Целлюлоза, так же как и крахмал, образуется в растениях при реакции фотосинтеза. Она является основной составной частью оболочки растительных клеток; отсюда происходит ее название —- целлюлоза («целлула» — клетка). Волокна хлопка — это почти чистая целлюлоза (до 98%). Волокна льна и конопли тоже состоят главным образом из целлюлозы. В древесине ее содержится примерно 50%.


Биологическое значение углеводов очень велико:
-
Углеводы выполняют пластическую функцию, то есть участвуют в построении костей, клеток, ферментов. Они составляют 2-3 % от веса.
-
Углеводы выполняют две основные функции: строительную и энергетическую. Целлюлоза образует стенки растительных клеток. Сложный полисахарид хитин служит главным структурным компонентом наружного скелета членистоногих. Строительную функцию хитин выполняет и у грибов.
-
Углеводы являются основным энергетическим материалом (см. ). При окислении 1 грамма углеводов выделяются 4,1 ккал энергии и 0,4 воды. Крахмал у растений и гликоген у животных откладываются в клетках и служат энергетическим резервом.
-
В крови содержится (0,1-0,12%) глюкозы. От концентрации глюкозы зависит осмотическое давление крови.
-
Пентоза (рибоза и дезоксирибоза) участвуют в постоении АТФ.
В суточном рационе человека и животных преобладают углеводы. Животные получают крахмал, клетчатку, сахарозу. Хищники получают гликоген с мясом.
Ежедневная потребность человека в сахарах составляет около 500 граммов, но она пополняется в основном за счет крахмала, содержащегося в хлебе, картофеле, макаронных изделиях. При рациональном питании суточная доза сахарозы не должна превышать 75 граммов (12 – 14 стандартных кусочков сахара, включая тот, что расходуется на приготовление пищи).
Кроме того, углеводы играют значительную роль в современной промышленности – технологии и продукты, в которых используются углеводы, не загрязняют окружающей среды, не приносят ей ущерба.
Приложения. Приложение 1:
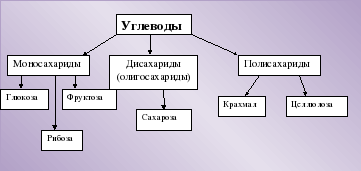
История открытия и производства сахара из свёклы.
Родиной сахарного тростника считается Индия (слово «сахар» тоже «родом» из Индии: «сакхара» на языке одного из древних народов полуострова означало сначала просто «песок», а затем – «сахарный песок»). Из Индии это растение было вывезено в Египет и Персию; оттуда через Венецию сахар поступал в европейские страны. Долгое время он стоил очень дорого и считался роскошью.
Культивировалась свекла с давних времен. В древних Ассирии и Вавилоне свекла выращивалась уже за 1,5 тыс. лет до н.э. Окультуренные формы свеклы известны на Ближнем Востоке с VIII-VI вв. до н.э. А в Египте свекла служила главной пищей рабов. Так, из диких форм свеклы, благодаря соответствующей селекции, постепенно были созданы сорта кормовой, столовой и белой свеклы. Из белых сортов столовой свеклы были выведены первые сорта сахарной свеклы.
Появление нового альтернативного тростнику, сахароноса историки науки связывают с эпохальным открытием немецкого ученого-химика, члена Прусской академии наук А. С. Маргграфа (1705-1782). В докладе на заседании Берлинской академии наук в 1747 г. он изложил результаты опытов по получению кристаллического сахара из свеклы.
Полученный сахар, как утверждал Маргграф, по своим вкусовым качествам не уступал тростниковому. Однако Маргграф не видел широких перспектив практического применения своего открытия.
Дальше в исследовании и изучении данного открытия пошел ученик Маргграфа — Ф. К. Ахард (1753-1821). Он с 1784 года активно взялся за усовершенствование, дальнейшую разработку и внедрение в практику открытия своего учителя.
Ахард прекрасно понимал, что одним из важнейших условий успеха нового, весьма перспективного дела, является улучшение сырья-свеклы, т.е. повышение ее сахаристости. Уже в 1799 году труды Ахарда увенчались успехом. Появилась новая ветвь культурной свеклы – сахарная. В 1801 году в своем имении в Кюцерне (Силезия) Ахард построил один из первых сахарных заводов в Европе, на котором освоил получение сахара из свеклы.
Комиссия, направленная Парижской академией наук, провела обследование ахардовского завода и пришла к выводу, что выработка сахара из свеклы нерентабельна.
Лишь единственные на то время английские промышленники, которые являлись монополистами по производству и продаже тростникового сахара, усмотрели в сахарной свекле серьезного конкурента и несколько раз предлагали Ахарду крупные суммы при условии, что он откажется от проведения своих работ и публично заявит бесперспективности производства сахара из свеклы.
Но Ахард, свято веривший в перспективность нового сахароноса, на компромисс не шел.С 1806 года Франция отказывается от производства сахара из тростника и переходит на свеклосахарное, которое со временем получало все большее распространение. Наполеон оказывал большую поддержку тем, кто проявлял желание выращивать свеклу и производить из нее сахар, т.к. увидел в развитии новой отрасли возможность одновременного развития сельского хозяйства и промышленности
Старинный русский способ получения сахара из растений, содержащих сахарозу.
Этот простой метод получения сахара, рассчитан специально для домашних условий. Способ содержит элементы старинных русских рецептов получения сахара, в том числе использованы методики, предложенные еще в 1850-1854 г. инженером Толпыгиным. Сырьем для получения сахара служат растения — сахароносы, содержащие сахарозу. Для получения сахара следует использовать ягоды, фрукты, овощи с наибольшим содержанием сахара, т.е. наиболее сладкие.
Последовательность получения сахара следующая:
-
Измельчение продукта;
-
Получение сока;
-
Отделение от примесей;
-
Сгущение сока до сиропа;
-
Извлечение кристаллического сахара.
Первый этап: Итак, превращение сахаросодержащего продукта в сахар основано на добывании сока из него.
Если вы используете нежные плоды (земляника, клубника и др. ягоды), то достаточно их размять. Если это, например, абрикосы, персики, то их следует разломить, вынуть косточки. Если применяется арбуз или дыня, то содержимое плода извлекается из оболочки и освобождается от семечек. Также рекомендуется свежесорванные ягоды, плоды выдержать предварительно 2-3 часа для повышения выхода сока. Если это сахарная свекла, яблоки или морковь и др., продукт измельчается в стружку. Чем тоньше и длиннее стружка, тем больше факторов, благоприятствующих ее обессахариванию. Хорошая стружка рекомендуется с шириной полоски 2-3 мм, а толщина 1-1,5 мм.
Второй этап: Измельченный продукт заливается водой до полного его покрытия и проваривается при температуре 70-72 °С. Если температура будет ниже 70°С, то не убиваются возможные микробы, если выше 72°С, то начинается размягчение стружки.
Время варки 45-60 минут при помешивании деревянной лопаткой. Сахар из стружки переходит в воду, которая становится соком. Стружка после извлечения из нее сахара называется жом. Из жома отжимается сок и жом убирается.
Третий этап: Полученный сок имеет темный цвет и высокое содержание примесей. Темная окраска, если от нее не избавиться, передается потом кристаллам сахара. Если на этой стадии выпарить из сока воду, вы получите сахар, но он будет иметь привкус исходного продукта, его цвет и запах. Сок имеет кислую реакцию, поэтому необходима его нейтрализация. Если этого не сделать, сок будет сильно пениться при выпаривании и тем затруднять этот процесс. Наиболее дешевый способ счистки сока — его обработки обожженой гашенной известью СА (ОН)2. В сок, подогретый до 80-90 °С, добавляем известь (в крайнем случае можно использовать строительную известку). На 10 л сока требуется примерно 0,5 кг извести. Известь следует добавлять постепенно, постоянно помешивая сок. Дать раствору выдержку 10 минут. Затем для того, чтобы осадить известь нужно пропустить через сок углекислый газ СО2. Можно использовать углекислый газ из баллончиков к бытовым сифонам (для получения газированной воды), промышленные баллоны с газом для сатураторов или из огнетушителей серии ОУ и ОВП. Газ из баллончика по трубке подается в нижнюю часть сосуда с горячим соком. На конце трубки следует установить распылитель (рассеиватель) с множеством мелких отверстий для более эффективного использования газа. Еще лучшего результата можно добиться одновременно помешивая раствор. Хорошее распыление газа гарантирует высокий коэффициент его использования и сокращает время процесса (около 10 минут). Раствору надо отстояться, затем профильтровать. Более эффективными являются фильтры с использованием активизированного древесного или костяного угля. Но в крайнем случае можно использовать тканевый фильтр.
Для окончательного осветления сока и удаления запаха сырья предлагаю русский проверенный способ. Через сок следует пропустить сернистый газ SO2. Обработку сернистым газом важно провести именно перед выпариванием, т. к. действие газа сказывается и при выпарке, что способствует меньшему потемнению сиропа. Необходимо иметь серу. Сера при нагревании плавится и в смеси с воздухом образуется сернистый газ. Старыми мастерами применялись два герметичных сосуда, соединенных между собой трубкой. В одном — вода, в другой закладывалась сера. Из сосуда с серой выходила 2-я трубка к рассеивателю на дно емкости с соком. При нагревании обоих сосудов водяной пар, проходя по трубке, вытеснял сернистый газ из 2-го сосуда и поступал к рассеивателю. Рассеиватель можно взять тот же.
Эту схему можно несколько упростить: взять только один сосуд с серой, к входной трубке его подсоединить компрессор для аквариума или другой насос и продувать воздухом газ, скапливающийся в сосуде с серой. Продувку газом надо проводить до полного осветления сока. Для ускорения процесса лучше одновременно подмешивать сок. Сернистый газ бесследно улетучивается из раствора в открытом сосуде, но работать следует в хорошо проветриваемом помещении.
Сернистый газ SO2 является лучшим антисептиком. Он сильно коррозирует металлическую посуду, поэтому следует использовать эмалированную. Очень большим достоинством этого газа, в значительной мере перекрывающим его недостатки, является возможность полостью удалить его из продукта. При нагревании продукта, обработанного сернистым газом, последний улетучивается, не оставляя ни запаха, ни привкуса. Газ широко используется на консервных заводах для консервирования различных продуктов.
Серу можно купить в хозяйственном магазине или в магазине для садоводов, она там продается как «Сера садовая» — содержит 99,9 % серы. Если найти серу Вам не удалось, не расстраивайтесь. Ваш сахар будет не такой белый, сохранит оттенок исходного продукта, но по вкусовым качествам будет не хуже белого.
Четвертый этап: Следующий этап — сгущение очищенного и обесцвеченного сока в сироп. Необходимо удалить из сока большое количество воды. Лучше всего это сделать выпариванием сока на русской печи, на малом огне плиты, ни в коем случае не доводя сироп до кипения (во избежание его потемнения).
В процессе выпаривания сироп все более сгущается. Если в пересыщенный раствор, не имеющий кристаллов сахара, ввести затравку в виде нескольких граммов сахарной пудры, то она вызовет образование новых кристаллов. Определение момента заводки в раствор пудры является очень ответственным и заключается с следующем простейшем способе: капля сиропа, зажатая между пальцами, при их раздвигании образует тонкую нить (волос), тогда наступает момент затравки. На 10 литров сиропа количество затравки составит половину чайной ложки пудры. Если завести мало пудры, то кристаллы образующегося сахара будут крупными, если много — мелкими. Достаточное количество кристаллов образуется примерно через 10-15 минут после внесения затравки. Дальнейшую кристаллизацию следует проводить при непрерывном охлаждении и перемешивании продукта,
Полученный продукт называется «утфель», в нем содержится до 7-10% воды и 50-60% выкристаллизовавшегося сахара и межкристаллическая жидкость (патока).
Пятый этап: Следующая операция отделение кристаллов от патоки. После окончания кристаллизации всю массу нужно выгрузить в ткань с ячейкой 0,3 мм, подвесить ее за углы в один узел над емкостью для слива патоки. При этом постараться отжать массу. Для увеличения процента выхода сахара патоку лучше использовать повторно в качестве добавки к сиропу.
Сахар после слива патоки получается желтоватого цвета. Далее можно использовать метод пробелки, отлично зарекомендовавший себя в 1854 г. и предложенный инженером Толпыгиным. Этот метод, внедренный в России, быстро распространился в мировой сахарной промышленности и именовался «русским». Сейчас метод незаслуженно забыт. Он заключается в пробелке утфеля паром и позволяет получить белый сахар высокого качества. Ткань с сахаром надо плотно подвязать на таз с малым количеством кипящей воды. Пар, поднимаясь, будет проходить через сахар, очищая его от белой патоки. Полученный белый сахар даже на ощупь влажный при хранении будет комковаться и превратится в сплошную глыбу. Поэтому пред долговременным хранением сахар следует высушить.
Особенности производства сахара.
Сахарное производство относится к непрерывно-поточному механизированному производству с высоким уровнем автоматизации основных процессов.
Особенностью территориального размещения сахарных заводов является их жёсткая привязка к посевным площадям сахарной свеклы, поскольку перевозка свеклы на значительные расстояния экономически неэффективна. В ряде случаев, сахарные заводы имеют собственные посевные площади, расположенные непосредственно вблизи предприятия. Отходы сахарной промышленности (жом, барда, дефекационная грязь) могут быть использованы как удобрения, в некоторых случаях — и как корм для скота.
Приложение 3:
Углеводы – важнейший источник энергии в организме.
Из всех потребляемых человеком пищевых веществ углеводы, несомненно, являются главным источником энергии. В среднем на их долю приходится от 50 до 70% калорийности дневных рационов. Несмотря на то, что человек потребляет значительно больше углеводов, чем жиров и белков, их резервы в организме невелики. Это означает, что снабжение ими организма должно быть регулярным.
Основными углеводами пищи являются сложные сахара, так называемые полисахариды: крахмал и гликоген, построенные из большого числа остатков глюкозы. Сама глюкоза содержится в больших количествах в винограде и сладких фруктах. В меде и фруктах, помимо глюкозы, содержатся значительные количества фруктозы. Обычный сахар, который мы покупаем в магазинах, относится к дисахаридам, так как его молекула построена из остатков глюкозы и фруктозы. В молоке и молочных продуктах содержатся большие количества менее сладкого, молочного сахара – лактозы, в состав которого наряду с глюкозой входит и моносахарид галактоза.
Потребности в углеводах в очень большой степени зависят от энергетических трат организма. В среднем у взрослого мужчины, занятого преимущественно умственным или легким физическим трудом, суточная потребность в углеводах колеблется от 300 до 500 г. У работников физического труда и спортсменов она значительно выше. В отличие от белков и в известной степени жиров, количество углеводов в рационах питания без вреда для здоровья может быть существенно снижено. Тем, кто хочет похудеть, стоит обратить на это внимание: углеводы имеют главным образом энергетическую ценность. При окислении 1 г углеводов в организме освобождается 4,0 – 4,2 ккал. Поэтому за их счет легче всего регулировать калорийность питания.
Какие же продукты следует считать главными источниками углеводов? Наиболее богаты углеводами многие растительные продукты: хлеб, крупы, макароны, картофель. Чистым углеводом является сахар. Мед, в зависимости от происхождения, содержит 70-80% моно- и дисахаридов. Его высокая сладость объясняется значительным содержанием фруктозы, сладкие свойства которой примерно в 2,5 раза выше глюкозы и в 1,5 выше сахарозы. Конфеты, пирожные, торты, варенье, мороженое и другие сладости являются наиболее привлекательными источниками углеводов и представляют несомненную опасность для полнеющих людей. Отличительной особенностью этих продуктов является высокая калорийность и низкое содержание незаменимых факторов питания.
К группе углеводов тесно примыкают встречающиеся в большинстве растительных продуктов, плохо усвояемые организмом человека вещества – клетчатка и пектины.
Важнейшие источники углеводов:
|
Продукты |
Содержание углеводов, г в 100 г продукта |
|
Хлеб ржаной |
42-45 |
|
Хлеб пшеничный |
43-50 |
|
Крупа гречневая |
64 |
|
Крупа манная |
70 |
|
Рис |
72 |
|
Сахар |
95-99 |
|
Картофель |
20 |
|
Капуста белокочанная |
5 |
|
Арбуз |
9 |
|
Морковь |
7-8 |
|
Свекла |
10 |
|
Виноград |
17 |
|
Яблоки |
11 |
Приложение 4:
Клетчатка – это полисахарид, входящий в состав массивных оболочек растительных клеток. Большие ее количества обнаружены во многих овощах, фруктах, листьях и стеблях растений. Только незначительная часть клетчатки может подвергнуться пищеварению в организме человека под влиянием находящихся в кишечнике микроорганизмов. Поэтому клетчатка и пектины большей частью проходят желудочно-кишечный тракт без изменений. Но они играют важную роль –пищевые массы быстрее продвигаются вдоль кишечника. Из-за этого тем, кто хочет похудеть, советуют есть много овощей и фруктов. Большие количества балластных веществ содержатся в хлебе из муки грубого помола, как уже сказано, в различных овощах, фруктах, особенно в свекле, моркови и черносливе.
22