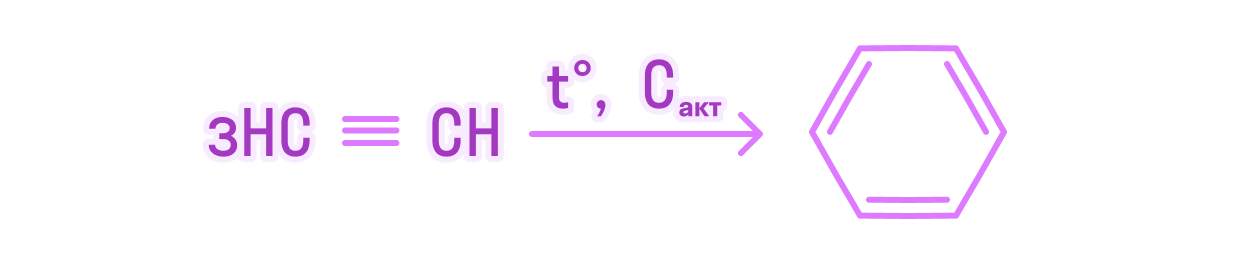Подготовка к ЕГЭ по химии
Как проходит ЕГЭ по химии в 2023 году
На ЕГЭ по химии, как и в случае с большинством других предметов, ученик 11 класса должен будет справиться с 2 частями экзамена:
-
1-я часть: 28 заданий с кратким ответом;
-
2-я часть: 6 заданий с развернутым ответом.
Чтобы решить все 34 задания единого государственного экзамена, у ученика будет 210 минут. За это время нужно будет успеть ответить на вопросы обеих частей, подготовить полное решение для задач 2-й части и перенести ответы в бланк.
Кстати, в отличие от ОГЭ, на ЕГЭ по химии не будет задания-эксперимента. Только обычные химические задания разной сложности. В таблице ниже можно посмотреть, сколько будет легких, средних и сложных вопросов.
| Уровень сложности заданий на ЕГЭ по химии | |
|---|---|
| Базовая | 17 |
| Повышенная | 11 |
| Высокая | 6 |
Если вы хотите больше узнать об особенностях экзамена и подготовки к нему, советуем заглянуть в раздел «Демоверсии, спецификации, кодификаторы» сайта ФИПИ. Там вы найдете всю актуальную информацию о ЕГЭ по химии и методические рекомендации. Все это поможет распланировать подготовку к экзамену так, чтобы сдать его на 100 баллов.
Изменения в ЕГЭ по химии
По сравнению с 2022 годом экзамен по химии немного изменится. Вот список нововведений:
-
Немного поменялось условие задания 23, в котором нужно рассчитать концентрацию веществ. Теперь данные в нем будут записаны текстом, а не в таблице.
-
Задания 33 и 34 поменялись местами.
-
Задания 9, 12 и 16 теперь станут повышенной сложности.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
Демоурок по подготовке к экзаменам
Составим ваш личный путь к высоким баллам — учтем сроки, уровень знаний и цель.
Как хорошо сдать ЕГЭ по химии: разбор сложных задач
Как мы узнали из таблицы в предыдущем разделе, экзамен по химии — один из самых сложных. На 34 задания в нем приходится целых 11 повышенной сложности и 6 — высокой. Но если вы хотите поступить в вуз мечты, советуем научиться их решать так, чтобы не упустить ни одного балла. А потому предлагаем начать подготовку прямо сейчас и вместе разобрать несколько таких задач.
Задание 7
Это задание проверяет буквально все ваши знания в области неорганической химии. Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Установите соответствие между веществом и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Вещество | Реагенты |
|---|---|
| А) S | 1) AgNO3, K3PO4, Cl2 |
| Б) SO3 | 2) BaO, NaOH, H2O |
| В) Zn(OH)2 | 3) H2, Cl2, O2 |
| Г) ZnBr2 | 4) HBr, LiOH, CH3COOH (p-p) |
| 5) H3PO4 (p-p), BaCl2, CuO |
Решение:
-
Вариант под буквой А — простое вещество, сера. Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
-
Вещество под буквой Б — кислотный оксид. Кислотные оксиды не реагируют с кислотами, поэтому смело вычеркиваем варианты, где присутствует хоть одна кислота. Остаются варианты № 1–3. Реагенты под цифрой 3 тоже можем вычеркнуть, так как кислотный оксид уже в своей максимальной степени окисления и дальше взаимодействовать с кислородом не может. Остаются варианты № 1 и № 2. Оксид серы (VI) может реагировать с основным оксидом с образованием соли, со щелочью с образованием соли и воды, и с водой, при этом образуя кислоту. Выбираем № 2.
-
Амфотерный нерастворимый в воде гидроксид цинка может взаимодействовать только с теми, что способны его растворить. Единственно верный вариант под № 4, где указаны кислоты и щелочь.
-
При взаимодействии соли с другими сложными веществами надо помнить про три признака протекания химической реакции: выпадения осадка, выделение газа и образование малодиссоциирующего вещества — воды. Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Ответ: 3241.
Задание 15
Это задание Единого государственного экзамена проверит ваши знания химических свойств органических соединений. Чтобы справиться с ним, нужно по записанным словами реагирующим веществам составить уравнение реакции и выбрать из перечня один из получившихся продуктов. Давайте рассмотрим на примере, как решать такую задачу.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Реагирующие вещества | Продукт взаимодействия |
|---|---|
| А) уксусная кислота и сульфид калия | пропионат калия |
| Б) муравьиная кислота и гидроксид калия | этилат калия |
| В) муравьиный альдегид и гидроксид меди (II) при нагревании | формиат меди (II) |
| Г) этанол и калий | формиат калия |
| ацетат калия | |
| углекислый газ |
Решение:
-
Органические кислоты могут реагировать с солями, если те имеют летучий анион. В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
-
Муравьиная кислота проявляет свойства неорганической кислоты и может взаимодействовать с щелочами с образованием соли и воды. Соль муравьиной кислоты — формиат. Правильный ответ № 4.
-
Под буквой В описана качественная реакция на альдегиды с образованием соответствующей кислоты, оксида меди (I) и воды. Исключение — муравьиный альдегид. Он окисляется до углекислого газа, а остальные продукты реакции те же. Соответственно, правильный ответ № 6.
-
Калий как активный металл может замещать протон водорода в гидроксогруппе у спиртов с образованием алкоголята. Правильный ответ: № 2.
Ответ: 5462.
Задание 16
Это задание всё так же проверяет ваши знания по химическим свойствам и, как следствие, умение записывать превращения в рамках органической химии. Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами х и у:
-
2-бромбутан;
-
этаналь;
-
этен;
-
метилпропан;
-
хлорэтан.
Решение:
Посмотрим, что случилось с известными нам веществами.
-
У спирта исчезла ОН-группа, затем что-то произошло, и углеродная цепочка увеличилась вдвое. Мы помним, что когда цепочка увеличивается вдвое, то, скорее всего, это реакция Вюрца. А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
-
Бутан подвергают нагреванию с использованием катализатора. Нужно помнить, что в таких условиях проводится изомеризация алканов. Из бутана получается метилпропан. Ответ: № 4.
Ответ: 54.
Задание 26
Теперь разберем задачи, которые заканчивают тестовую часть ЕГЭ по химии. Рассмотрим условие одной из них на нахождение массы соли, которую необходимо добавить для получения раствора с новой заданной массовой долей.
Вычислите массу нитрата калия (в граммах), которую следует растворить в 160 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. Ответ округлите до десятых.
Чтобы решить эту задачу, вспомним основную формулу нахождения массовой доли:
-
Найдем массу изначально растворенного нитрата калия в растворе, выразив из формулы выше:
подставим значения:
-
Чтобы увеличить массовую долю соли в растворе, необходимо ее добавить еще. Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
-
Далее в дело вступает чистая математика. Разделим обе части уравнения на 100%:
-
По пропорции перемножим крест-накрест:
0,12 * (160 + X) = 16 + X.
-
Раскроем скобки:
19,2 + 0,12Х = 16 + Х.
-
Приведем подобные: с Х в одну сторону, без Х — в другую:
3,2 = 0,88Х.
-
Найдем Х:
Масса нитрата калия, которую необходимо добавить для увеличения массовой доли раствора до 12%, равна 3,6 граммам.
Ответ: 3,6.
Задание 28
Эта задача может встретиться на экзамене в нескольких вариантах. Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
В результате реакции тримеризации ацетилена объемом 26,88 л (н.у) получили 24,96 г бензола. Вычислите массовую долю выхода продукта реакции от теоретически возможного.
Решение:
-
Для начала напишем формулу, по которой считается доля выхода продукта:
Как определить, какая масса практическая, а какая — теоретическая? Значения, которые даются после слова «получили», — это практическая масса. Та, которая получилась в результате проведения химической реакции в реальных условиях. Масса теоретическая — та, которую рассчитывают из уравнения реакции, зная массу исходных реагентов.
-
Напишем уравнение химической реакции тримеризации ацетилена:
-
Найдем количество вещества ацетилена:
подставим значения:
-
Перейдем на количество вещества бензола, получаемого из ацетилена:
-
Зная количество вещества бензола, найдем его массу:
подставим значения:
m = 0,4 * 78 = 31,2 грамма.
-
Масса, рассчитываемая по уравнению реакции, является теоретической. Масса практическая дана нам по условию. Подставим полученные данные по массам в формулу для нахождения доли выхода продукта реакции:
Доля выхода бензола из данного объема ацетилена составляет 80%.
Ответ: 80.
Как оценивают готовые работы на ЕГЭ по химии
1-я часть
В 1-й части Единого государственного экзамена по химии задания 1–5, 9–13, 16–21, 25–28 оценивают 1 баллом, если вы запишете верный ответ по эталону. При этом в заданиях 1, 3, 4, 11, 12, 13, 17 и 18 ответ — это ряд цифр. То, в каком порядке вы их запишете, не влияет на оценку. Например, если в задании верны варианты под номерами 1 и 4, их можно записать как 14 или как 41. И в обоих случаях ответ засчитают как верный.
За правильные ответы в заданиях 6, 7, 8, 14, 15, 22, 23 и 24 можно получить по 2 балла. Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
2-я часть
В этой части нужно записать не только ответ, но и решение. А значит, и оценивать такие задания будут сразу по нескольким критериям. Зато за верный ответ в некоторых вопросах можно получить больше баллов, чем за любое задание 1-й части. Максимум — 5 баллов. А теперь давайте разберемся, как именно их будут оценивать.
| Задание № 29 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества и записал уравнение химической реакции, составил электронный баланс, указал окислитель и восстановитель | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 30 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества, записал все нужные уравнения реакции | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 31 | Баллы |
|---|---|
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 4 |
| Задание № 32 | Баллы |
|---|---|
| Правильно записаны 5 уравнений реакции | 5 |
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 5 |
| Задание № 33 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 3 элемента | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 3 |
| Задание № 34 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 4 элемента | 4 |
| Правильно записаны только 3 элемента ответа | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 4 |
Как сдать ЕГЭ по химии на 3, 4 и 5
Мы уже познакомились с критериями, по которым будут оценивать работы на ЕГЭ. А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
Будьте внимательны: баллы из таблиц выше — первичные, а требования к абитуриентам на поступление выражены в тестовых. Чтобы понять, сколько заданий точно нужно решить, чтобы поступить, надо перевести баллы из одной системы в другую. Это можно сделать по таблице ниже.
| Первичные баллы | Тестовые баллы | Оценка |
|---|---|---|
| <11 | <36 | 2 |
| 11–25 | 36–55 | 3 |
| 26–38 | 56–72 | 4 |
| 39–56 | 73–100 | 5 |
6 рекомендаций, как подготовиться к ЕГЭ по химии
Единый государственный экзамен — это ответственная задача, от результатов подготовки к которой иногда многое зависит. Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
-
Узнайте все о структуре ЕГЭ и научитесь работать с КИМами.
-
Начинайте готовиться заранее. Но если получилось так, что осталось мало времени, составьте новый экспресс-план с помощью вашего преподавателя.
-
Ведите календарь подготовки к экзамену. Отмечайте на нем запланированные темы, разные методики, занятия у репетитора, пробные ЕГЭ и самоподготовку.
-
Распределяйте время на темы, исходя из ваших знаний. Больше учите то, что «западает», остальное — повторяйте.
-
Советуйтесь с учителем. Это может быть ваш преподаватель по химии или репетитор. Круто, если он сможет поделиться с вами опытом подготовки к ЕГЭ.
-
Заботьтесь о своем здоровье, не забывайте отдыхать, не лишайте себя живого общения. Все это может сказаться на вашем самочувствии, а значит, и баллах тоже.
Если вы хотите сдать ЕГЭ по химии на 100 баллов, советуем тщательно продумать, как вы будете готовиться к нему. Лучший из них — совмещать самостоятельную работу и дополнительные занятия.
На курсах подготовки к ЕГЭ по химии в Skysmart школьники отрабатывают все типы задач и разбирают критерии оценок. Для каждого из них мы составляем индивидуальный план, который приведет к нужным баллам. Он учитывает уровень знаний ученика и время до экзамена, что позволяет «выжать» максимум из подготовки. А еще мы рассказываем о ЕГЭ без «страшилок» и прикрас, чтобы школьник точно знал, что его ждет на экзамене. Ждем на первом бесплатном занятии!
Химия – предмет, не относящийся к обязательным для сдачи ЕГЭ, и выбирают его выпускники, которые хорошо в нем разбираются. Но и у них даже, казалось бы, самые легкие задания могут вызвать затруднения. На каких моментах часто спотыкаются участники экзамена и как можно избежать ошибок, рассказывает Наталия Покровская, эксперт Московского центра качества образования, ответственный секретарь предметной комиссии ЕГЭ по химии.
Вариант контрольно-измерительных материалов единого государственного экзамена по химии состоит из 35 заданий: 29 в первой части – с выбором ответа или кратким ответом, и 6 во второй – высокого уровня сложности с развернутым ответом.
Задания 1–3
– Первые три задания не относятся к разряду трудных, но и в них выпускники могут допустить ошибки: иногда ребят сбивает с толку простое изменение формулировки вопроса, – рассказывает Наталия Покровская. – Например, если в задании 3 написано «Выберите элементы, проявляющие высшую степень окисления +5», всем ясно, о чем идет речь. А нестандартная формулировка вроде «Выберите элементы, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления» вызывает непонимание, хотя суть задания не изменилась! Таким образом, старшеклассники должны быть готовы к тому, что вопрос может звучать по-разному.
Задание 7
Это задание также нельзя назвать трудным. Главное при его выполнении быть внимательными. Например, в условии может быть сказано: «Добавили раствор вещества Х». Значит, выбирая из предложенного списка вещество Х, сразу нужно исключить все нерастворимые вещества. Поскольку задание чаще всего направлено на проверку знаний о реакциях, протекающих в растворах, следует вспомнить, в каких случаях выделяются газы: разложение получившихся непрочных кислот (сернистой, угольной) или гидрата аммиака, появление в продуктах сероводорода, совместный полный гидролиз, вытеснение водорода из кислоты металлом. Всю информацию, касающуюся осадков, можно найти в таблице растворимости. Написание схемы реакции поможет визуализировать условие задания и не допустить ошибок.
Задания 8, 30, 31 и 32
Задания 8, 30, 31 и 32 направлены на проверку знаний свойств неорганических веществ. Изменившийся формат заданий 30 и 31 ограничивает экзаменуемых в выборе веществ, между которыми идет реакция. Теперь уравнение должно соответствовать указанным в условии признакам: меняется ли цвет раствора, образуется или не образуется осадок либо газ. Поэтому не любое правильно написанное уравнение будет считаться верным: оценивается уравнение только той реакции, которая полностью соответствует условию. Для выполнения задания 30 нужно хорошо знать, какие конкретно вещества являются окислителями и восстановителями, а для задания 31 – вспомнить формулы малодиссоциирующих веществ (их нельзя записывать в виде ионов).
Важно помнить: если в исходных веществах есть кислота, то в продуктах не может получиться основание или основная соль, и наоборот. Следует проверять, чтобы получившиеся продукты реакции не реагировали между собой и с реагентами. Если есть возможность дальнейшего протекания реакции, значит, уравнение неверно. Больше информации о выполнении этих заданий можно найти на сайте Московского образовательного телеканала в видеоролике «Учимся вместе. Я сдам ЕГЭ!».
Задания 8 и 32 различаются тем, что первое предполагает только выбор возможных реакций, а во втором требуется написание уравнений (при этом даются подсказки в виде признаков протекания реакций). Приступая к выполнению задания 8, нужно рассмотреть предложенные формулы веществ с двух позиций: их кислотно-основных и окислительно-восстановительных свойств. Это позволит сразу понять, от какого списка реагентов можно отказаться: например, кислота не реагирует с кислотой, а восстановитель – с восстановителем. Для выполнения задания 32 особенно важно знать цвета осадков и растворов – это может быть хорошей подсказкой для определения продуктов реакции. Выучить палитру довольно просто, если раскрасить таблицу растворимости, отмечая все известные цветовые признаки соединений. Дополнительную информацию о задании 32 можно посмотреть по ссылке.
Задание 13
Очень много ошибок выпускники делают в задании 13 (свойства углеводородов), особенно если вопрос заключается в определении механизма реакции. Рекомендую обратить внимание на то, что ионный механизм всегда связан с присутствием ионов, то есть разноименно заряженных частиц. Но есть вещества, которые при разных условиях могут образовывать и частицы-ионы, и частицы-радикалы. Например, молекула хлора при облучении распадается на радикалы, а вот катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи, и получаются ионы.
Гораздо легче запомнить свойства углеводородов, если учитывать возможность веществ с определенным типом связи вступать в соответствующие реакции: кратная связь – реакции присоединения, одинарная связь – реакции замещения. Но не следует забывать также, что при изменении условий могут быть исключения даже в основных законах: с перекисью водорода в качестве катализатора реакция присоединения идет вопреки правилу Марковникова, а если хлорирование алкена проводить при температуре 600 0С, то вместо реакции присоединения пойдет замещение у атома углерода в sp3-гибридизации.
Задания 15 и 17
Не менее сложны задания 15 (азотсодержащие органические вещества и углеводы) и 17 (кислородсодержащие органические вещества). При изучении свойств этих соединений нужно обратить внимание, что реакции могут идти как по функциональной группе, так и по радикалу. Чтобы выучить как можно больше свойств органических соединений, можно составить конспект, выписать побольше уравнений для каждого класса. И конечно же, нужно выполнять цепочки на взаимосвязь органических веществ. Рекомендую посмотреть видеоролики по этим заданиям на Московском образовательном телеканале – «Химия, ЕГЭ. Задание № 15» и «Химия, ЕГЭ. Задание № 17», а также видео «Химия, 10 класс. Взаимосвязь классов органических веществ».
Затруднения вызывают и вопросы по окислительно-восстановительным реакциям в органической химии, особенно если нужно расставить коэффициенты. Справиться с такими заданиями поможет консультация эксперта: «Химия, 11 класс. Окислительно-восстановительные реакции в органической химии».
Задания 34 и 35
Самыми трудными для выполнения являются задания 34 и 35 – это расчетные задачи с химическим содержанием.
Ошибки в задании 35 чаще всего случаются из-за неправильного определения структурной формулы. Обычно это связано с недостаточным знанием химических свойств органических веществ. Поэтому здесь только один совет: стараться каждый день выполнять хотя бы одну цепочку превращений, писать уравнения реакций.
Задание 34 сложно тем, что для него нет единого алгоритма решения. Есть задачи на электролиз, смеси, атомистику, а бывает, что в условии переплетается несколько типов задач. Я бы советовала сначала отработать какой-то один тип задач, разобраться в его логике. Потом подключить задачи другого типа и понять, в чем отличие, определить последовательность действий.
При решении этих задач требуется повышенное внимание: лучше прочитать условие несколько раз, возвращаться к нему по мере выполнения задания, отмечать массы веществ, которые уходят из раствора, чтобы исключить их при нахождении массы конечного раствора. Формулы, применяемые для решения задачи 34, простые и хорошо известные, например: массовая доля равна массе растворенного вещества, деленной на массу раствора. Сложности – в деталях: при вычислении массы раствора нужно не забыть сложить все массы добавляемых веществ, вычесть массы осадков и выделившихся газов. Важно помнить, что амфотерные гидроксиды в избытке щелочи растворяются, и если в начале задачи трудно определить избыток или недостаток щелочи, можно написать два возможных уравнения – образования гидроксида и образования комплексной соли.
Полезные ссылки
Для успешной сдачи экзамена по химии нужно готовиться, повторять теорию и выполнять упражнения. Найти их можно в открытом банке заданий на сайте Федерального института педагогических измерений.
Также я рекомендую посмотреть видеоролики Московского образовательного телеканала, где в рубриках «Субботы московского выпускника» (совместный проект с Московским центром качества образования), «Спроси эксперта», «Учимся вместе. Я сдам ЕГЭ!» ведущие эксперты предметных комиссий разбирают задания ЕГЭ и дают рекомендации, как лучше подготовиться. А все новости, касающиеся ЕГЭ, можно найти на сайте Московского центра качества образования.
Источник: Activityedu.ru
ЕГЭ по химии состоит из тестовой и письменной частей. Из 34 заданий 28 тестовых и 6 письменных. Всего на экзамене по химии можно набрать 56 баллов — 36 в первой части и 20 во второй. Чтобы оставить себе место для ошибки, рекомендуем решать всю первую и всю вторую части. В статье разберем пять полезных советов преподавателей, чтобы успешно сдать экзамен.
Содержание:
- Лайфхак №1. Тренируйтесь в решении заданий блоками
- Лайфхак № 2. Ищите сходства и придумывайте ассоциации в неорганике
- Лайфхак №3. Заучивайте исключения
- Лайфхак №4. Тайм-менеджмент
- Лайфхак №5. Пользуйтесь шпаргалками из КИМа
- Что нужно взять на ЕГЭ по химии в 2023?
- Вывод
Лайфхак №1. Тренируйтесь в решении заданий блоками
В спецификаторах на сайте ФИПИ указаны темы, знание которых будет проверяться на экзамене. Экзаменационный материал разделен на следующие блоки:
- Теоретические основы химии (Общая химия).
- Неорганическая химия:
- оксиды;
- основания;
- амфотерные гидроксиды;
- кислоты;
- соли;
- соединения галогенов, кислорода, азота, фосфора, серы, углерода, кремния, металлов IA- и IIA-групп, алюминия, цинка, хрома, марганца, железа, меди, серебра.
- Органическая химия:
- алканы;
- алкены;
- алкины;
- алкадиены;
- циклоалканы;
- циклоалкены;
- арены;
- одноатомные и многоатомные спирты;
- фенолы;
- альдегиды;
- кетоны;
- карбоновые кислоты;
- амины;
- аминокислоты;
- жиры;
- белки;
- углеводы.
- Химия и жизнь.
- Расчетные задания / Математика.
Рассмотрим подробнее, что проверяют задания. Красным цветом отмечены задания, за которые дается 1 балл, желтым — 2 балла, зеленым 3 и более баллов.
| № | Общая химия | Неорганическая химия | Органическая химия | Расчетные задания |
| 1 | электронная конфигурация | |||
| 2 | закономерности таблицы Менделеева | |||
| 3 | валентность и степень окисления | |||
| 4 | химические связи и кристаллические решетки | |||
| 5 | номенклатура (тривиальная и международная) | |||
| 6 | свойства простых веществ
реакции ионного обмена (РИО) |
|||
| 7 | соотнесение вещества с рядом веществ | |||
| 8 | составление уравнения реакции | |||
| 9 | взаимосвязь неорганических веществ | |||
| 10 | номенклатура (тривиальная и международная) | |||
| 11 | гомологи и изомеры в органике | |||
| 12 | свойства УВ и кислородсодержащих производных | |||
| 13 | свойства азотсодержащих производных БИО | |||
| 14 | составление уравнения (углеводороды) | |||
| 15 | свойства кислородсодержащих производных УВ | |||
| 16 | составление уравнений (производные УВ) | |||
| 17 | классификация химических реакций | |||
| 18 | скорость химической реакции | |||
| 19 | окислительно-восстановительные реакции | |||
| 20 | электролиз | |||
| 21 | гидролиз | |||
| 22 | химическое равновесие | |||
| 23 | расчеты по уравнению обратимой реакции | |||
| 24 | качественные реакции | качественные реакции | ||
| 25 | блок «Химия и жизнь»: вещества и области их применения | |||
| 26 | расчеты массовой доли | |||
| 27 | расчет теплового эффекта реакции | |||
| 28 | расчеты по уравнению реакции | |||
| 29 | окислительно-восстановительные реакции | |||
| 30 | реакции ионного обмена | |||
| 31 | цепочка из четырех реакций (4 балла) | |||
| 32 | цепочка из пяти реакций (5 баллов) | |||
| 33 | органическая расчетная задача (3 балла) | |||
| 34 | неорганическая расчетная задача (4 балла) |
Рекомендуем расписать подготовку к сдаче ЕГЭ таким образом, чтобы наращивать знания от простого к сложному. Начните с общей химии. Это база, без знания которой можно потерять баллы на заданиях, посвященных органической и неорганической химии. О расписании расскажем в лайфхаке №4.
Лайфхак № 2. Ищите сходства и придумывайте ассоциации в неорганике
Вы могли заметить, что в органической химии больше логики, чем в неорганической. Однако в неорганике также можно проследить аналогии. Например, если вы знаете классификацию веществ, вам проще определить свойства конкретного вещества:
- способность реагировать с другими веществами;
- способность к разложению;
- способность к диссоциации.
Ассоциации — это более творческий подход к запоминанию материала. Вы можете продумать ассоциации для конкретного вещества или группы веществ, наделяя их «характером», манерой поведения или другими образными признаками. Рисуйте на их основе схемы, иллюстрации, придумывайте рифму, используйте свой творческий потенциал, чтобы облегчить обучение и сделать подготовку увлекательнее и интереснее.
Обратите внимание, подготовка к сдаче ЕГЭ часто сводится к выводу четких алгоритмов решений, которые проще вспомнить и применить на экзамене. Тем не менее в экзамене по химии прослеживается тенденция к тому, чтобы оценивать, как ученик понимает материал, а не владеет алгоритмами.
Лайфхак №3. Заучивайте исключения
Многие составители и преподаватели объединяют два первых раздела общую и неорганическую химию. Однако здесь важно учитывать следующее: в теоретических основах химии есть четкие алгоритмы, как заучивать материал при подготовке. При этом в ЕГЭ по химии много заданий построено на исключениях. Преимущественно они сконцентрированы именно в блоке неорганической химии.
Помните, что без знания теоретических основ очень сложно решать задания на неорганическую химию, но не пренебрегайте исключениями при подготовке к экзамену. Запомнить их можно, прибегая к ассоциациям, о которых мы говорили в предыдущем лайфхаке.
Лайфхак №4. Тайм-менеджмент
Сколько нужно готовиться к ЕГЭ по химии?
Период подготовки зависит от уровня знаний о предмете и расписания. С нуля рекомендуется начинать готовиться за 2 года до экзамена. Если у вас есть база, начните готовиться к экзамену с сентября одиннадцатого класса.
Подготовку эксперты рекомендуют разделить по месяцам:
| Месяц | Теория | Практика |
| Сентябрь | Основы общей химии | |
| Октябрь | Неорганическая химия | |
| Ноябрь | Органическая химия | |
| Декабрь | Расчетные задачи | |
| Январь | Комплексные задачи* | |
| Февраль | Основы общей химии | |
| Март | Неорганическая химия | |
| Апрель | Органическая химия | |
| Май | Повторение всего изученного материала | Письменная часть экзамена |
*К комплексным задачам рекомендуется переходить после того, как освоили разделы общей, неорганической и органической химии и математики.
Что если до подготовки к экзамену остался один триместр. Можно ли подготовиться к ЕГЭ по химии за 3 месяца?
Если до экзамена осталось три месяца, их желательно посвятить повторению пройденного материала на практике. Подготовка к ЕГЭ по химии за 3 месяца с нуля потребует высокого темпа ежедневной тренировки, изучения большого объема теории и его отработке. Чтобы подготовиться к ЕГЭ за 3 месяца найдите компетентного специалиста — частного репетитора или курсы.
Специалист поможет выстроить программу обучения. Вне зависимости от сроков это необходимый этап подготовки. Важно составить подробную схему — какие темы изучаете, в какой последовательности и сколько по времени. Заранее выстроенная логика прохождения материала позволит без стресса и спешки готовиться к экзамену.
Следует уделять подготовке 1,5—2 часа в день 3—4 раза в неделю.
Чтобы приучить себя к структуре экзамена, важно не только решать задания из пособий, демоверсии 2023 года и вариантов экзамена, которые сдавали выпускники 2022 года и предыдущих лет. Необходимо максимально приблизить условия экзамена во время тренировки — не подглядывать и не списывать, а также четко отводить 3 ч 30 мин на написание экзамена.
Другой метод работы со временем, которые советуют эксперты — фиксировать время, потраченное на каждое задание. Это позволит отследить, какие задания являются для вас наиболее времязатратными.
Лайфхак №5. Пользуйтесь шпаргалками из КИМа
- ручка;
- документ, удостоверяющий личность;
- лекарства и питание при необходимости;
- непрограммируемый калькулятор.
Остальные необходимые материалы для экзамена выпускникам выдаст организатор. В КИМах помимо бланков можно будет найти Периодическую систему, Таблицу растворимости и Электрохимический ряд напряжений.
Рассмотрим, как они помогут на экзамене.
Периодическая система химических элементов Д.И. Менделеева
Помимо периода, группы и порядкового номера по таблице можно сказать многое. Например:
- количество протонов, электронов в атоме элемента;
- количество оболочек;
- распределение электронов по оболочкам;
- количество электронов на валентной оболочке;
- подгруппу элемента;
- химические свойства простого вещества;
- сведения о соединении элемента.
Периодическая система нужна преимущественно для решения первых четырех заданий: №1 — строение атома, № 2 — периодический закон, №3 — электроотрицательность и степень окисления, №4 — связи и кристаллические решетки.
Электрохимический ряд напряжений
Он показывает:
- как от лития Li до золота Au уменьшается активность металлов;
- поведение оксидов в пирометаллургии;
- поведение солей в гидрометаллургии;
- взаимодействие простого вещества с кислотами;
- поведение соли в гидролизе и электролизе;
- поведение нитрата при разложении.
Эта шпаргалка пригодится во всех заданиях блока неорганической химии — №5—9; задания на электролиз и гидролиз №20, 21; качественные реакции — №24; химия и жизнь — 25; неорганические цепочки — №31.
Таблица растворимости кислот, солей и оснований в воде
В этой таблице собрано большое количество важной информации, например:
- заряд иона;
- степень окисления элемента в ионе;
- поведение при гидролизе;
- поведение в реакциях ионного обмена;
- поведение в качественных реакциях.
Таблица будет полезна для решения заданий на степень окисления в ионе — №3, 19, 29. Для решения всего блока неорганической химии — №5—9; задания на гидролиз — №21, качественные реакции — 24, реакции ионного обмена 30, неорганические цепочки — №31 и сложной комплексной задачи — №34.
Вывод
Мы рассмотрели 5 лайфхаков для ЕГЭ по химии от экспертов и преподавателей. Они помогут ученикам продумать и построить верный курс к успешной сдаче ЕГЭ. Резюмируя, мы предлагаем при подготовке разделить задания экзамена на тематические блоки:
- общую химию;
- неорганическую химию;
- органическую химию;
- математику;
- химию и жизнь (задание №25).
На основе выявленных блоков мы рекомендуем вам составить четкое расписание. При подготовке важно идти по запланированному пути — знать, с чего начинать готовиться, и как последовательно выстроить темы. Кроме того, мы выявили, что эксперты рекомендуют подбирать ассоциации, продумывать аналогии при изучении и повторении материала.
Последнее, чему важно научиться в процессе подготовки — это пользоваться тремя ключевыми таблицами:
- Периодической системой;
- Таблицей растворимости;
- Электрохимическим рядом напряжений металлов.
Рекомендуем сразу скачать те варианты таблиц, что будут в КИМах. Их можно найти на сайте ФИПИ в разделе «Демоверсии, спецификаторы и кодификаторы». Умение работать с этими материалами позволит существенно сэкономить время на экзамене.
Главное при подготовке к экзамену — научиться понимать задачи, а не только зазубривать теорию и структуру. Если вы видите, что не понимаете определенные темы, задавайте вопросы учителю химии в школе, подберите репетитора или курсы. Компетентный специалист построит программу с учетом ваших пробелов в определенных темах и поможет успешно сдать ЕГЭ по химии.
Подготовка к егэ по химии глазами 11-классника или
как я сдал егэ на 97 баллов
Реальная история, которая вдохновляет
Всем привет! Я Лёша Богданов, студент биологического факультета Санкт-Петербургского государственного университета, в прошлом — выпускник 11 класса. Если вы читаете эту статью, вероятно вас мучает мысль о егэ, как это было и у меня.
Я сдавал на егэ 3 предмета в 2021 году — химию, биологию и русский язык. Сдал я эти предметы суммарно на 272 балла, а химию – на 97 баллов! Вот за такой короткой фразой кроется годовая история моей подготовки, которой я хочу поделиться с вами.
Выбор предметов на егэ
Для меня это не составило труда, с 8 класса я мечтал научиться медицине — работа человеческого организма меня всегда поражала своей сложностью и многогранностью.
Так что мой выбор безоговорочно пал на химию, биологию и профильную математику. Да, профильную математику, я сам не до конца понимал зачем я её выбрал, но тем не менее, она мне нравилась, и я решил — пусть будет.
Как всё закрутилось…
Наш учитель математики — очень ответственная женщина — начала проводить дополнительные занятия в первую неделю обучения в школе. И где-то через 3 недели я решил — хочу отдыхать, зачем мне эта математика, все равно для вуза она не нужна.
И после этих мыслей я со спокойной душой прогулял последние теплые деньки со своими друзьями. Я всегда считал, что химия и биология мой конек и что я их прекрасно знаю. Но мой отдых и уверенность в том, что я знаю эти две науки разбились в дребезги ноябрьским вечером.
Я решил свои первые пробники. 41 балл по биологии, 37 по химии. Меня накрыл страх и ужас, до экзаменов осталось примерно 7 месяцев, а я, как оказалось, ничего не знаю. Судорожный поиск репетиторов, проверка всех онлайн школ, паника перед экзаменом, все это сопровождало меня, когда я писал репетитору, с которым готовился к ОГЭ — Яне Павловне.
Тогда же мои друзья дали мне наводку на групповые занятия, которые ведёт преподаватель биологии в вузе. Я был вне себя от радости, казалось бы, все прекрасно, меня обучают два сильнейших педагога, но всё только начиналось.
Учебный процесс — подготовка к егэ по химии началась!
Начал я с завидным энтузиазмом, в некоторые дни я уделял химии 10-12 часов. Честно говоря, до сих пор поражаюсь себе. Я пробовал разные способы изучения и запоминания материала: смотрел вебинары, конспектировал, читал, делал таблицы, вешал стикеры по дому, слушал лекции в аудио формате.
Тогда я нашел множество книг и сайтов, в которых был материал для успешной подготовки к ЕГЭ по химии. Я садился за стол, разбирал какую-то тему, потом решал пару сотен заданий, чтобы наверняка запомнить материал и понять принцип решения подобных заданий.
Спустя пару недель такой работы я чувствовал себя амебой, я хотел бесконечно лежать на диване и листать тикток, но все-таки находил в себе силы, чтобы ходить на занятия и делать необходимый минимум, с трудом, но находил.
Вскоре наступил этап полной апатии — тогда я просто ел и спал, от одной мысли об учебе моя голова наливалась свинцом — я понял, что нужно взять паузу.
Таких кругов было несколько, постоянные моральные подъёмы и спады очень истощали. Сегодня ты готов свернуть горы, а завтра не можешь поднять себя с кровати.
Через пару месяцев такой жизни у меня начало получаться совмещать учебу и отдых, я все равно уставал, но главное — стабильно и почти систематично усваивал новый материал и закреплял старый. На этом этапе моя продуктивность резко выросла, баллы подскочили до 70-80. Я ликовал!
Чем выше были мои результаты, тем сильнее я хотел учиться.
Учеба начала становиться хобби — споры с друзьями и учителями по поводу какого-то задания — приятным разговором. Я забыл про экзамены, мне нравилось развиваться и учиться новому. В таком состоянии я пробыл до апреля. Тогда меня снова осенило — осталось всего 60 дней. Но уже тогда меня не пугала эта мысль, я хотел проверить и показать себя.
Оставшиеся 2 месяца я начал наращивать темпы — вместо привычных 3-4 часов в день я занимался 5-6. Я бегло повторял весь материал, чтобы убедиться, что ничего не забыл и принимался решать еще больше заданий, чем в начале года.
Тематические задания и пробники занимали 80% от учебного времени, и я начинал следить за маленькими деталями: оформлением задач, необходимыми записями во второй части, в целом, разбирал структуру критериев, чтобы понять, чего от меня ждут эксперты. Я уставал, но мысль о том, что до экзамена осталось уже пару недель была отличным пинком, и я продолжал учиться.
Уже двадцатые числа мая, до дня сдачи химии буквально неделя. Я сажусь решать пробник — в голове пелена. Снова паника, снова страх. В то же время я вспомнил ради чего я все это делаю — моя будущая специальность, возможно, дело моей жизни.
Тогда я снова спросил себя: «Кем я хочу стать?».
Я не смог ответить на этот вопрос, передо мной открылись двери химии, биологии и их прикладных наук, у меня был выбор из более чем 10 программ обучения, которые мне нравились, но, увы, для большинства из них нужна была профильная математика…
Да, та от которой я отказался еще в начале года. Все эти мысли в преддверии экзаменов пошатнули мою уверенность в своем выборе, своих силах. Мне было невероятно страшно.
За день до экзамена я решил отдохнуть — это было одно из лучших решений!
За этот день я полностью успел восстановиться, информация, которую я беспорядочно находил, успела уложиться у меня в голове.
Учеба стала хобби, я забыл про экзамены — мне нравилось развиваться и учиться новому…
День Х — сдаю егэ по химии
Утром, с легкой головой я собрался и пошёл на экзамен. Как вчера помню — идешь в аудиторию, ноги трясутся, сердце колотится, ладошки потеют. Но после 5 минут в аудитории все страхи исчезли — организаторы, как оказалось, очень добрые люди, и атмосфера экзамена не так уж и угнетает.
Когда нам выдали кимы и все принялись за дело, было ощущение, будто я сижу на простой контрольной работе.
Я даже вышел пару раз прогуляться по коридору и размяться, чтобы с новыми силами приняться решать какое-то сложное задание. Насчет самого кима — я не встретил ни одного задания, которое я когда-то решал, но по сложности он был как обычный средний пробник — мои знания позволили мне ощущать себя в своей тарелке, не волноваться лишний раз и сконцентрироваться на задачах.
Постэкзаменное состояние
Когда я только вышел из аудитории у меня был миллион вопросов. Чувство, будто я ошибся везде. Я сразу же позвонил Яне Павловне — большая часть вопросов отпала, но всё равно меня преследовало ощущение, что выше 90 баллов мне не видать.
Следующие несколько дней я провел в шоковом состоянии, мысль о моих возможных ошибках не давала мне покоя…Наступил не менее важный день, чем тот, когда я сдавал экзамен — день, когда приходили результаты. Страх, который ты испытываешь при открытии чек егэ не передать словами — весь мир замирает.
Когда я увидел свои результаты, сначала я не поверил, несколько раз обновил страницу, проверил данные. «95…» — пробормотал я себе под нос. «ДЕВЯНОСТО ПЯТЬ!!!» — спустя 5 секунд я кричал в трубку всем знакомым и друзьям!
Моему счастью не было предела! Хотя, все-таки был, для достоверности я решил проверить свои ответы и найти ошибки. 5 задание — ответ в бланке «321», компьютер прочитал эти цифры как «311». Тогда меня захватила новая волна паники. Что делать? 95 баллов — высокий результат, но если апеллировать, можно получить 97, а можно и потерять, если будут проверять всю работу….
Я позвонил всем учителям, которых знал. Все настаивали -» Не рискуй, ты можешь потерять в 2 раза больше, чем получишь». Но мне хотелось рискнуть, толчком к этому послужила Яна Павловна. Она проделала невероятную работу, чтобы уточнить все детали, знать обо всех нюансах.
Я написал заявление на апелляцию, через несколько дней я уже стоял на входе в школу, где повторно рассматривалась моя работа. Мы с Яной Павловной были настроены серьезно — я должен был получить свои законные баллы. Апелляция прошла гладко и быстро — стоило мне сказать, что у меня в бланке допущена техническая ошибка (по вине компьютера), эксперты со счастливыми лицами отпустили меня и сказали не переживать.
Радостный я выбежал к Яне Павловне. Это была победа, мой результат был выше, чем у всех знакомых – 97 баллов!
Я поверил в свой успех. Похожая ситуация была с другими экзаменами, я также был на апелляции по биологии, но баллы отбить не смог, увы.

Чем всё закончилось — я учусь в лучшем ВУЗе страны
Сейчас я пишу этот текст после практики по альгологии в лучшем ВУЗе страны. Когда это испытание позади, я с уверенностью могу сказать:
Всё что вы делаете сейчас ради своего будущего стоит того, каждое приложенное усилие вернётся вам пятикратным удовольствием, как только вы добьётесь своей цели.
Определённо, это потребует большого количества сил, возможно, вы потеряете веру в себя (на какое-то время), возможно, совершите множество ошибок, но стоит помнить, что не ошибается только тот, кто ничего не делает. Так что дерзайте, стремитесь, работайте! Все обязательно получится!
Воспользуйтесь советами моего репетитора — профессионала своего дела Шапошниковой Яны Павловны, которыми она делится в статье «Как подготовиться к егэ по химии».
Пройти тестирование по 10 заданиям
Пройти тестирование по всем заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне четыре электрона. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке возрастания их металлических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Источник: Демонстрационная версия ЕГЭ—2017 по химии, Демонстрационная версия ЕГЭ—2018 по химии, Демонстрационная версия ЕГЭ−2019 по химии
2
Из числа указанных в ряду элементов выберите два элемента, которые проявляют низшую степень окисления, равную –4. Запишите в поле ответа номера выбранных элементов.
Источник: Демонстрационная версия ЕГЭ—2017 по химии, Демонстрационная версия ЕГЭ−2019 по химии
Источник: Демонстрационная версия ЕГЭ—2017 по химии, Демонстрационная версия ЕГЭ−2019 по химии
2
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне один электрон. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке возрастания их металлических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Источник: РЕШУ ЕГЭ
2
Из числа указанных в ряду элементов выберите два элемента, которые проявляют высшую степень окисления, равную +1. Запишите в поле ответа номера выбранных элементов.
Источник: РЕШУ ЕГЭ
Источник: РЕШУ ЕГЭ
3
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне пять электронов. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке возрастания их металлических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Источник: РЕШУ ЕГЭ
2
Из числа указанных в ряду элементов выберите два элемента, которые проявляют низшую степень окисления, равную −2. Запишите в поле ответа номера выбранных элементов.
Источник: РЕШУ ЕГЭ
Источник: РЕШУ ЕГЭ
4
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне два электрона. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке возрастания их неметаллических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Источник: РЕШУ ЕГЭ
2
Из числа указанных в ряду элементов выберите два элемента, которые проявляют высшую степень окисления, равную +2. Запишите в поле ответа номера выбранных элементов.
Источник: РЕШУ ЕГЭ
Источник: РЕШУ ЕГЭ
5
Определите, атомы каких двух из указанных в ряду элементов имеют на внешнем энергетическом уровне три электрона. Запишите в поле ответа номера выбранных элементов.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д. И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке возрастания их металлических свойств. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Источник: РЕШУ ЕГЭ
2
Из числа указанных в ряду элементов выберите два элемента, которые проявляют высшую степень окисления, равную +3. Запишите в поле ответа номера выбранных элементов.
Источник: РЕШУ ЕГЭ
Источник: РЕШУ ЕГЭ
Пройти тестирование по этим заданиям