Skip to content
- Главная
- Университеты
- БашГМУ
- Теория
- Биохимия, теория
Башкирский государственный медицинский университет
- Пособия
- Схемы
- Лекции
- Ответы на вопросы
- Теория для экзамена
Пособия
Схемы
Лекции
Ответы на вопросы
Теория к экзамену
Перед отправкой формы внимательно прочитайте то, что находится под каждым из них. В противном случае, ваше обращение может не дойти до нас.
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ БУРЯТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
БИОХИМИЯ В ТАБЛИЦАХ, СХЕМАХ, ГРАФИКАХ
Составители: С.Д. Жамсаранова Ю.А. Капустина Н.А. Тыхеева Н.Б. Болданова
Улан– Удэ Издательство Бурятского госуниверситета
2009
1
УДК 577.1 Б 638
Рекомендовано к печати редакционно-издательским советом
Бурятского госуниверситета
Рецензенты
С.Н. Лебедева, д-р. биол. наук, проф.
С.В. Жигжитжапова канд.биол. наук
Биохимия в таблицах схемах и графиках:
Б 638 учеб. пособие /сост. С.Д. Жамсаранова, Ю.А. Капустина, Н.А. Тыхеева, Н.Б. Болданова. – Улан-Удэ: Издательство Бурятского государственного университета, 2009. 106 с.
Данное пособие — это содержательный раздаточный материал, позволяющий оперативно получать наглядную информацию по центральным проблемам биохимии.
Пособие предназначено для студентов специальности 060101.65 – лечебное дело.
© С.Д. Жамсаранова, Ю.А. Капустина, Н.А. Тыхеева, Н.Б. Болданова, составление, 2009 © Бурятский госуниверситет, 2009
2
|
СОДЕРЖАНИЕ |
||||
|
Список сокращений ……………………………………………… |
..…… |
…5 |
||
|
Строение и характеристика протеиногенных |
||||
|
амнокислот |
7 |
|||
|
Структура белков……………………………… |
………… |
.….….………. 10 |
||
|
Ферменты…… |
………….…14 |
|||
|
Классификация ферментов………………… |
…… ……………………… |
.14 |
||
|
Коферменты и витамины, входящие в их состав…………………… |
.…15 |
|||
|
Механизм действия ферментов…………………… |
……………….….…18 |
|||
|
Ингибиторы ферментов……………………………………………… |
.…..22 |
|||
|
Применение ферментов в медицине……………………………………..24 |
||||
|
Энергетический обмен……………………………………… |
……… |
.….26 |
||
|
Митохондриальная цепь переноса электронов………………………….28 |
||||
|
Биологическое значение цикла |
||||
|
трикарбоновых кислот………………………………… |
…….…… |
…… |
…34 |
|
|
Гипоэнергетическое состояние……………………………… |
……… |
……35 |
||
|
Связь общего пути катаболизма с цепью |
||||
|
переноса электронов ………………………………………………………36 |
||||
|
Обмен и функции углеводов……………………… |
…….….…. ……….37 |
|||
|
Транспорт глюкозы в клетки ……… |
……………………………… |
.…….39 |
||
|
Катаболизм глюкозы. ……….…………………………………..…… |
..…41 |
|||
|
Гликогенез……… |
||||
|
Гликогенолиз………………………………………………………………47 |
||||
|
Глюконеогенез…………………………… |
………………………… |
…….49 |
||
|
Метаболизм фруктозы и галактозы…………………………………… |
…55 |
|||
|
Обмен и функции ……………липидов………………………… |
………… |
57 |
||
|
Этапы расщепления липидов |
||||
|
в пищеварительном тракте………………………………………….…… 60 |
||||
|
Строение липопротеинов……………………………………………… |
. . 63 |
|||
|
Катаболизм жирных кислот…………………………………………… |
…68 |
|||
|
Реакции синтеза кетоновых тел…………………………………..…… |
….70 |
|||
|
Биосинтез жирных кислот…………………………………………… |
……71 |
|||
|
Метаболизм холестерина и желчных кислот………………………… |
….76 |
|||
|
Эйкозаноиды……………………………………………………………… |
.76 |
|||
|
Трансмембранная ………………………………………………передача сигнала |
77 |
|||
|
Структура нуклеиновых кислот……………………………………… |
.79 |
|||
|
Репликация……………………………………… |
………………… |
….…..84 |
||
|
Репарация ошибок и повреждений ДНК……………………………… |
…86 |
|||
|
Транскрипция. ……………………………………… |
………………… |
.…87 |
||
|
Трансляция…………………………………………………………… |
..….90 |
|||
|
Ингибиторы матричных биосинтезов………………………… …………91 |
||||
|
Обмен аминокислот……………………………………… |
…… …… |
…… 93 |
||
|
3 |
|
Источники и способы обезвреживания аммиака |
|
|
в разных тканях……………………………………………………………97 |
|
|
Наследственные нарушения орнитинового цикла ……………………..99 |
|
|
Кето- и гликогенные аминокислоты…………………….…………… |
…100 |
|
Особенности метаболизма фенилаланина |
|
|
и тирозина в разных тканях………………………………….……… |
.…101 |
4
|
Список сокращений |
|
|
А |
-аденин |
|
АДФ |
-аденозиндифосфат |
|
Ала |
-аланин |
|
Альбумин-НЭЖК |
-альбумин-неэтерифицированные |
|
жирные кислоты |
|
|
цАМФ |
— циклический аденозинмонофосфат |
|
Арг |
— аргинин |
|
Асн |
— аспарагиновая кислота |
|
Асп |
— аспарагин |
|
АТФ |
— аденозинтрифосфат |
|
Вал |
— валин |
|
ВЖК |
— высшие жирные кислоты |
|
Г |
— гуанин |
|
Гал |
— галактоза |
|
ГДФ |
— гуанозиндифосфат |
|
Гис |
— гистидин |
|
ГК |
— гексокиназа |
|
Гли |
— глицин |
|
Глк |
— глюкоза |
|
Глн |
— глутамин |
|
Глу |
— глутаминовая кислота |
|
ГМГ-КоА |
— β-гидроксиметилглутарил-КоА |
|
ГМГ-КоА-редуктаза |
— β-гидроксиметилглутарил-КоА-редуктаза |
|
ГТФ |
— гуанозинтрифосфат |
|
ДАГ |
— диацилглицерины |
|
ДНК |
— дезоксирибонуклеиновая кислота |
|
ДОФА |
— дигидроксифенилаланин |
|
ЖК |
— жирная кислота |
|
ЛВП |
— липопротеины высокой плотности |
|
Лей |
— лейцин |
|
Лиз |
— лизин |
|
ЛНП |
— липопротеины низкой плотности |
|
ЛОНП |
— липопротеины очень низкой плотности |
|
ЛП-липаза |
— липопротеинлипаза |
|
ЛХАТ |
— лецитинхолестеролацилтрансфераза |
|
Мет |
— метионин |
|
МАО |
— моноаминоксидаза |
|
НАД+ |
— никотинамидадениндинуклеотид |
|
НК |
— нуклеиновые кислоты |
|
ОМФ |
— оротидинмонофосфат |
|
5 |
|
Про |
— пролин |
|
РНК |
— рибонуклеиновая кислота |
|
мРНК |
— матричная РНК |
|
рРНК |
— рибосомальная РНК |
|
тРНК |
— транспортная РНК |
|
Сер |
— серин |
|
Т |
— Тимин |
|
ТАГ |
— Триацилглицерин |
|
ТАГ-липаза |
— триацилглицеролипаза |
|
Тир |
— тирозин |
|
ТГФК |
— тетрагидрофолиевая кислота (Н4-фолат) |
|
Три |
— триптофан |
|
У |
— урацил |
|
УДФ |
— уридиндифосфат |
|
УТФ |
— уридинтрифосфат |
|
ФАД |
— флавинадениндинуклеотид |
|
Фен |
— фенилаланин |
|
Фру |
— фруктоза |
|
ФФК |
— фосфофруктокиназа |
|
ХМ ост |
— хиломикроны остаточные |
|
Ц |
— цитозин |
|
ЦДФ |
— цитидиндифосфат |
|
ЦПЭ |
— цепь переноса электронов |
|
ЦТК |
— цикл трикарбоновых кислот |
|
Нb |
— гемоглобин |
|
НbА |
-нормальный гемоглобин взрослого |
|
человека |
|
|
Км |
— константа Михаэлиса |
|
VMAХ |
— максимальная скорость |
6
СТРОЕНИЕ И ХАРАКТЕРИСТИКА ПРОТЕИНОГЕННЫХ АМИНОКИСЛОТ
α
ΝН ─ СН ─ СООН
│
R
КЛАССИФИКАЦИЯ АМИНОКИСЛОТ ПО ИХ ХИМИЧЕСКОМУ СТРОЕНИЮ
|
Амино- |
Символы |
Константы |
||||||
|
кислоты |
М |
диссоциации |
ИЭТ |
|||||
|
русск. |
лат. |
рК1 |
рК2 |
рК3 |
||||
|
Глицин |
Гли |
Gly,G |
75 |
— |
— |
— |
5,97 |
|
|
Аланин |
Ала |
Ala,A |
89 |
2,39 |
9,69 |
— |
6,0 |
|
|
Валин |
Вал |
Val,V |
117 |
2,32 |
9,62 |
— |
6,0 |
|
|
Лейцин |
Лей |
Leu,L |
113 |
2,36 |
9,60 |
— |
6,0 |
|
|
Изолей- |
Иле |
Ile,I |
113 |
2,26 |
9,62 |
— |
5,9 |
|
|
цин |
||||||||
|
Серин |
Сер |
Ser,S |
105 |
2,21 |
9,35 |
— |
5,7 |
|
|
Треонин |
Тре |
Thr,T |
119 |
2,15 |
9,12 |
— |
5,6 |
|
|
Цистеин |
Цис |
Cys,C |
121 |
1,71 |
8,33 |
10,8 |
5,0 |
|
|
Метио- |
Мет |
Met,M |
149 |
2,28 |
9,21 |
— |
5,7 |
|
|
нин |
||||||||
|
Фенил- |
Фен |
Phe,F |
165 |
1,83 |
9,13 |
— |
5,3 |
|
|
аланин |
||||||||
|
Тирозин |
Тир |
Tyr,Y |
181 |
2,2 |
9,11 |
10,1 |
5,7 |
|
|
Трипто- |
Три |
Trp,W |
204 |
2,38 |
9,30 |
— |
5,9 |
|
|
фан |
||||||||
|
Пролин |
Про |
Pro,P |
115 |
1,99 |
10,0 |
— |
6,3 |
|
|
Аспара- |
Асн |
Asn, N |
132 |
2,19 |
9,11 |
— |
5,41 |
|
|
гин |
||||||||
|
Глутамин |
Глн |
Gln,Q |
146 |
1,98 |
9,10 |
— |
5,65 |
|
|
Гистидин |
Гис |
His,H |
155 |
1,78 |
5,97 |
8,97 |
7,6 |
|
|
Лизин |
Лиз |
Lys,K |
146 |
2,20 |
8,90 |
10,3 |
9,7 |
|
|
Аргинин |
Арг |
Arg,R |
174 |
2,18 |
9,09 |
13,2 |
10,9 |
|
|
Аспара- |
Асп |
Asp,D |
133 |
1,88 |
3,65 |
9,00 |
2,8 |
|
|
гиновая |
||||||||
|
кислота |
||||||||
|
Глута- |
Глу |
Glu,E |
147 |
2,19 |
4,25 |
9,07 |
3,2 |
|
|
миновая |
||||||||
|
кислота |
||||||||
|
7 |

КЛАССИФИКАЦИЯ АМИНОКИСЛОТ, ОСНОВАННАЯ НА
ПОЛЯРНОСТИ БОКОВЫХ ЦЕПЕЙ
Боковые цепи неполярных аминокислот
|
Глицин (Gly,G) |
Аланин (Ala,A) |
Валин (Val,V) |
Пролин (Pro, P) |
|||||||
|
│ |
│ |
│ |
СОО |
|||||||
|
Н |
СН3 |
Н3С─СН |
│ |
|||||||
|
│ |
СН |
|||||||||
|
СН3 |
⁄ |
|||||||||
|
НN |
СН2 |
|||||||||
|
/ |
||||||||||
|
Н2С— СН2 |
||||||||||
|
Лейцин (Leu,L) |
Изолейцин (Ile, I) |
|||||||||
|
│ |
│ |
|||||||||
|
СН2 |
Н3С─СН |
|||||||||
|
│ |
│ |
|||||||||
|
Н3С─СН |
СН2 |
|||||||||
|
│ |
│ |
|||||||||
|
СН3 |
СН3 |
|||||||||
|
Боковые цепи полярных, незаряженных аминокислот |
||||||||||
|
Серин (Ser,S) |
Цистеин (Cys, C) |
Метионин (Met, M) |
||||||||
|
│ |
│ |
│ |
||||||||
|
СН2 |
СН2 |
СН2 |
||||||||
|
│ |
│ |
│ |
||||||||
|
ОН |
SН |
СН2 |
||||||||
|
│ |
||||||||||
|
S |
||||||||||
|
│ |
||||||||||
|
СН3 |
||||||||||
|
Глутамин (Gln, Q) |
Аспарагин (Asn,N) |
Треонин (Thr, T) |
||||||||
|
│ |
│ |
│ |
||||||||
|
СН2 |
СН2 |
Н3С─СН |
||||||||
|
│ |
│ |
│ |
||||||||
|
СН2 |
СОΝН2 |
ОН |
||||||||
|
│ |
||||||||||
|
СОΝН2 |
||||||||||
|
Боковые цепи отрицательно заряженных аминокислот |
||||||||||
|
Глутаминовая кислота (Glu, E) |
Аспарагиновая кислота (Asp, D) |
|||||||||
|
│ |
│ |
|||||||||
|
СН2 |
СН2 |
|||||||||
|
│ |
│ |
|||||||||
|
СН2 |
СОО |
|||||||||
|
│ |
||||||||||
|
СОО |
||||||||||
|
8 |
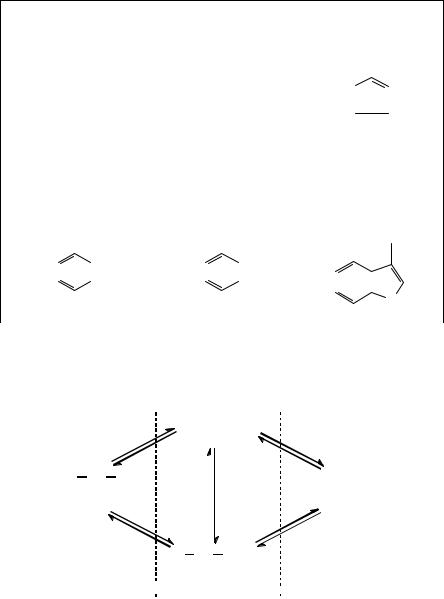
Положительно заряженные
|
Лизин (Lys, K) |
Аргинин (Arg, R) |
Гистидин (His, H) |
|||||||||||||||||||
|
│ |
│ |
│ |
|||||||||||||||||||
|
СН2 |
СН2 |
СН2 |
|||||||||||||||||||
|
│ |
│ |
│ |
|||||||||||||||||||
|
СН2 |
СН2 |
HN |
CH |
||||||||||||||||||
|
│ |
│ |
||||||||||||||||||||
|
СН2 |
СН2 |
||||||||||||||||||||
|
│ |
│ |
CH |
N |
||||||||||||||||||
|
СН2 |
ΝН |
||||||||||||||||||||
|
│ |
│ |
||||||||||||||||||||
|
ΝН2 |
С |
||||||||||||||||||||
|
/ |
|||||||||||||||||||||
|
Н2Ν ΝН2 |
|||||||||||||||||||||
|
Ароматические боковые цепи |
|||||||||||||||||||||
|
Фенилаланин |
Тирозин |
Триптофан |
|||||||||||||||||||
|
│ |
│ |
||||||||||||||||||||
|
СН2 |
СН2 |
||||||||||||||||||||
|
│ |
│ |
CH |
|||||||||||||||||||
|
NH |
|||||||||||||||||||||
|
│ |
|||||||||||||||||||||
|
ОН |
|||||||||||||||||||||
|
КИСЛОТНО—ОСНОВНОЕ РАВНОВЕСИЕ В РАСТВОРЕ |
|||||||||||||||||||||
|
α−АМИНОКИСЛОТ |
|||||||||||||||||||||
|
Цвиттер—ион |
|||||||||||||||||||||
|
R |
CH |
COO– |
|||||||||||||||||||
|
K1 |
+ |
||||||||||||||||||||
|
NH3 |
|||||||||||||||||||||
|
Катион |
K3 |
Анион |
|||||||||||||||||||
|
R CH |
COOH |
R |
CH |
– |
|||||||||||||||||
|
COO |
|||||||||||||||||||||
|
+ |
Kz |
||||||||||||||||||||
|
NH3 |
NH2 |
||||||||||||||||||||
|
K2 |
K4 |
||||||||||||||||||||
|
R |
CH COOH |
||||||||||||||||||||
|
Кислая среда |
Щелочная |
||||||||||||||||||||
|
NH2 |

Нейтральная
9

ПЕНТАПЕПТИД
|
O |
R2 |
H |
O |
R4 |
H |
O |
|||||||||||||||
|
N-Конец H2N |
H |
H |
|||||||||||||||||||
|
C |
C |
N |
C |
C |
N |
C |
|||||||||||||||
|
C |
H |
N |
C |
CH |
N |
C |
CH OH С-Конец |
||||||||||||||
|
R1 |
R3 |
R5 |
|||||||||||||||||||
|
H |
O |
H |
O |
R1, R2 и т.д. — боковые радикалы аминокислот. Пептидный остов молекулы выделен утолщенными линиями.
СТРУКТУРА БЕЛКОВ
Пептидные цеп и содержат десятки, сотни и тысячи аминокислотных остатков, соединенных прочными пептидными связями. За счет внутримолекулярных взаимодействий белки образуют определенную пространственную структуру, называемую «конформация белков». Различают 4 уровня структурной организации белков.
Первичная структура – это линейная последовательность аминокислотных остатков в полипептидной цепи.
Вторичная структура белков – это пространственная структура, образующаяся в результате взаимодействий между функциональными группами пептидного остова. При этом пептидная цепь может приобретать структуры двух типов: α—спирали и ß- структуры.
Третичная структура белка – это трехмерная пространственная структура, образующаяся за счет взаимодействий между радикалами
10
Соседние файлы в предмете Биохимия
- #
09.02.201510.18 Mб16Pethrick. Monomers, Olygomers, Polymers.pdf
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
09.02.201512.17 Mб16095Биохимия. Ленинджер. 1 том.pdf
БИОХИМИЯ В СХЕМАХ И ТАБЛИЦАХ
Библиотека

БИОХИМИЯ В СХЕМАХ И ТАБЛИЦАХ
Биохимия в схемах и таблицах: пособие для студентов биол. фак. / сост.: И.В. Семак (и др.). – Минск: БГУ, 2011. – 91 с.
Резюме. В работе наглядно изображается динамическая биохимия. Приводятся понятные рисунки, известные формулы и биохимические пути.
Скачать PDF
Биологическая библиотека — материалы для студентов, учителей, учеников и их родителей.
Все материалы доступны по лицензии Creative Commons Attribution-Sharealike 3.0 Unported CC BY-SA 3.0 и GNU Free Documentation License (GFDL)
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
© 2018-2023 Все права на дизайн сайта принадлежат С.Є.А.
- Электронный архив библиотеки Витебского государственного медицинского университета ( ISSN 2524-0242 )
- Факультеты
- Лечебный факультет
- Кафедра общей и клинической биохимии с курсом ФПК и ПК
- Учебные материалы
Please use this identifier to cite or link to this item:
https://elib.vsmu.by/handle/123/9869
| Title: | Биохимия в схемах и таблицах |
| Authors: | Фомченко, Г. Н. Ядройцева, И. А. |
| Keywords: | Биологическая химия |
| Issue Date: | 2009 |
| Publisher: | ВГМУ |
| Citation: | Коневалова, Н. Ю. Биохимия в схемах и таблицах : учебное пособие для студентов медицинских вузов / Н. Ю. Коневалова, Г. Н. Фомченко, И. А. Ядройцева ; Министерство здравоохранения Республики Беларусь, Витебский государственный медицинский университет. — Витебск : [ВГМУ], 2009. — 297 с. |
| Abstract: | Представлены таблицы по двадцати темам научной дисциплины «Биохимия». |
| Description: | БИОХИМИЯ |
| URI: | http://elib.vsmu.by/handle/123/9869 |
| ISBN: | 978-985-466-337-1 |
| Appears in Collections: | Учебные материалы |
Items in DSpace are protected by copyright, with all rights reserved, unless otherwise indicated.

