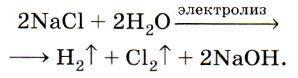Сочинение: Галогены
Галогены
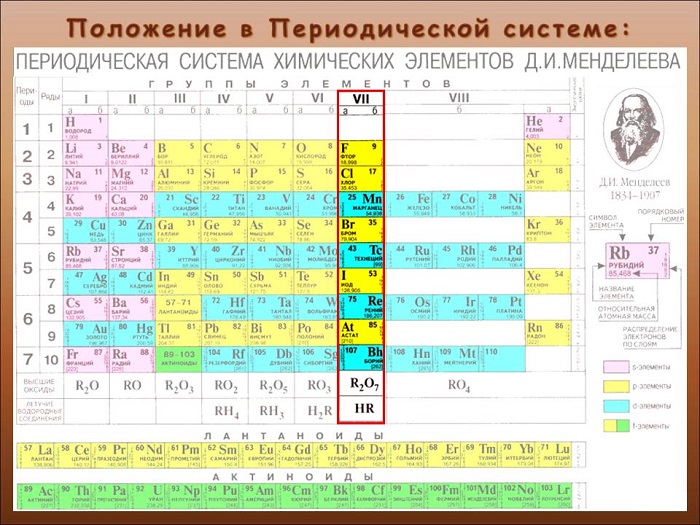
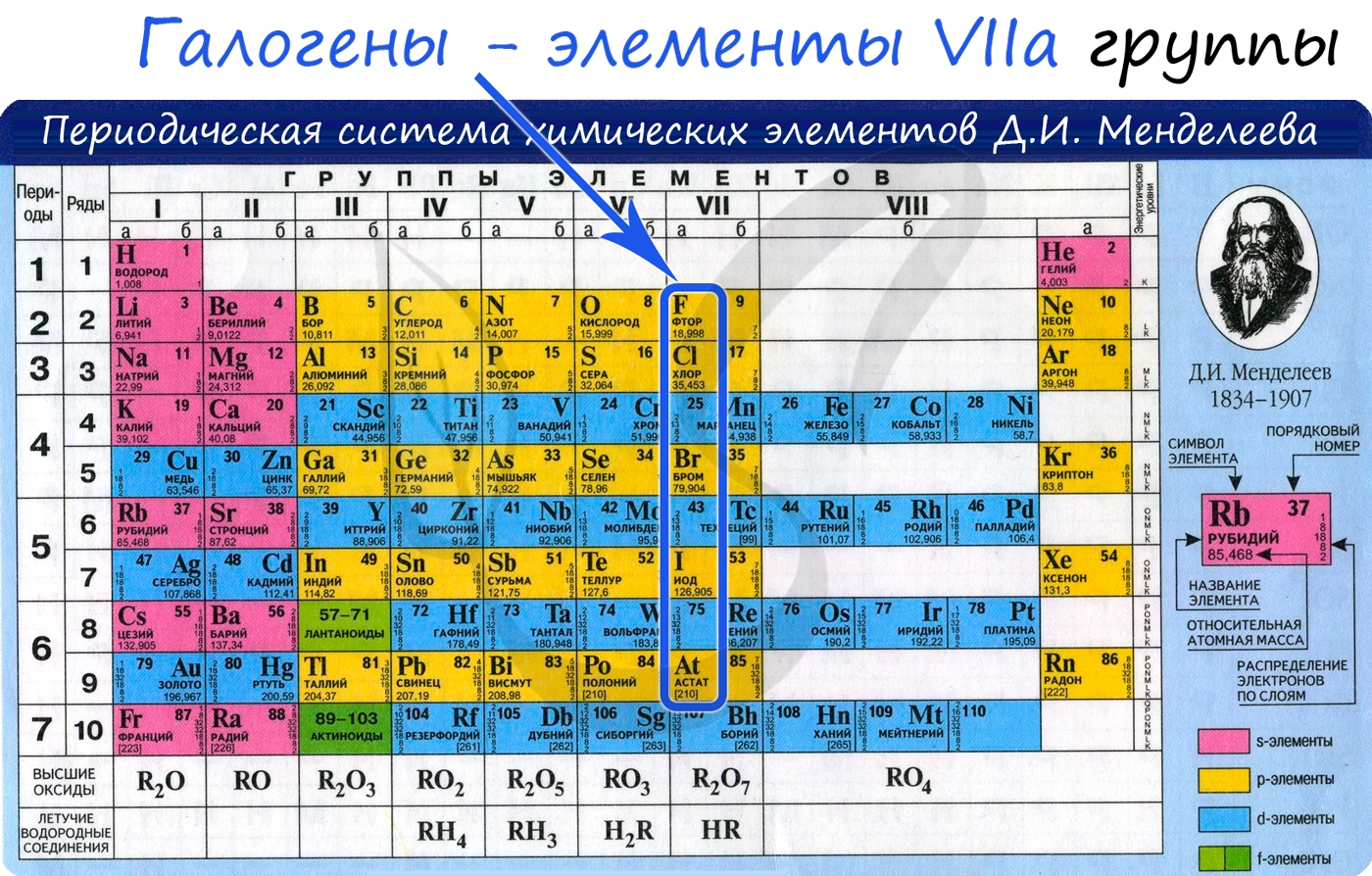
Всем известно, что фтор вводят в состав зубной пасты, а хлором дезинфицируют воду в плавательных бассейнах. Бром применяют в качестве успокоительного средства, а спиртовой раствор йода как антисептическое средство. Фтор, хлор, бром и йод образуют семейство галогенов. Галогены относятся к неметаллическим элементам. Они входят в VII группу периодической системы (см. рис.).
О происхождении названий галогенов
Названия всех галогенов, за исключением фтора, происходят от греческих слов:
|
Название |
Исходное слово |
Значение |
|
Галоген |
галс (греч.) ген (греч.) |
Соль Образующий |
|
Фтор |
флуо (лат.) |
Течь, текучий (в старину минерал полевой шпат CaF, использовали в металлургии в качестве флюса для придания легкоплавкости шлакам) |
|
Хлор |
хлорос (греч.) |
Зеленовато-желтый |
|
Бром |
бромос (греч.) |
Зловонный |
|
Иод |
иодес (греч.) |
Фиолетовый |
|
Астат |
астатос (греч.) |
Неустойчивый |
Слог «ген» в качестве приставки либо суффикса входит во многие научные термины, например в слова генератор и антиген. Обычно он означает рост или образование чего-либо. Таким образом, слово галоген (гало + ген) означает «образующий соль».
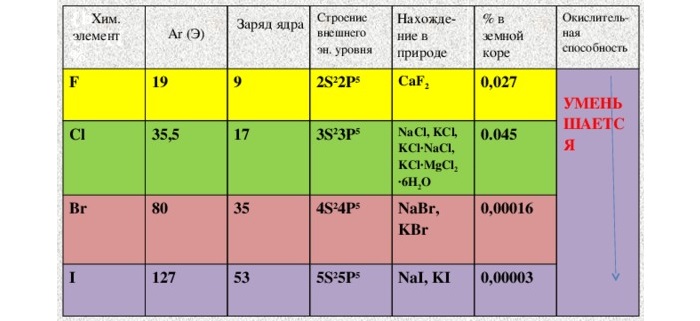
ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
Атомы всех галогенов имеют во внешней оболочке семь электронов. Они легко присоединяют еще один электрон, образуя галогенидные ионы. Галогенид-ион имеет устойчивый октет электронов. Галогены характеризуются высокой электроотрицательностью и реакционной способностью и поэтому в свободном виде не встречаются в природе. Однако галогенид-ионы широко распространены в природе.
Галогены в свободном виде существуют в форме двухатомных молекул. Атомы в этих молекулах связаны между собой простой ковалентной связью. Каждая такая связь образуется в результате обобществления пары электронов — по одному от каждого атома:
В табл. 1 приведены некоторые данные о структуре атомов и молекул галогенов. Обратим внимание на то, что атомные и ионные радиусы галогенов, а также длины связи в их молекулах последовательно возрастают при перемещении к нижней части группы. Однако энергии диссоциации связи и, следовательно, прочность связи в молекулах галогенов при этом, наоборот, уменьшаются. Исключением в этом отношении является только фтор. Небольшая прочность связи фтора, по-видимому, обусловлена слишком близким расположением атомов в его молекуле. Это приводит к сильному отталкиванию между несвязывающими электронами, что вызывает ослабление связи.
Таблица 1. Электронное строение и свойства галогенов
|
Элемент |
Атомный номер |
Электронная конфигурация атомов |
Конфигурация внешней оболочки |
Атомный радиус, нм |
Ионный радиус, нм |
Длина связи, нм |
Энергия диссоциации связи, кДж/моль |
|
Фтор |
9 |
2.7 |
2s2 2p5 |
0,072 |
0,136 |
0,142 |
158 |
|
Хлор |
17 |
2.8.7 |
Зs2 3p5 |
0,099 |
0,181 |
0,200 |
242 |
|
Бром |
35 |
2.8.18.7 |
4s2 4р5 |
0,114 |
0,195 |
0,229 |
193 |
|
Иод |
53 |
2.8.18.18.7 |
5s2 5р5 |
0,133 |
0,216 |
0,266 |
151 |
ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
Хлор. Хлор можно получить в лабораторных условиях окислением концентрированной соляной кислоты манганатом( VII ) калия:
Выделяющийся хлор пропускают через воду, чтобы удалить следы хлороводородов, а затем через концентрированную серную кислоту, чтобы осушить его. Полученный хлор собирают в перевернутом сосуде, из которого он вытесняет воздух.
Другой способ лабораторного получения хлора основан на реакции между отбеливающим порошком (гипохлоритом кальция) и разбавленной соляной кислотой:
Бром. Для получения брома в лабораторных условиях добавляют оксид марган-Ha(IV) к смеси концентрированной серной кислоты с бромидом калия. Бромоводород-ная кислота, обоазуюшаяся в оеакции между сеоной кислотой и бромидом калия:
окисляется оксидом марганца( IV )
Бром отделяют от реакционной смеси перегонкой.
Иод. Иод получают тем же способом, что и бром, только вместо бромида калия используется иодид калия. Полученный иод отделяют от реакционной смеси возгонкой.
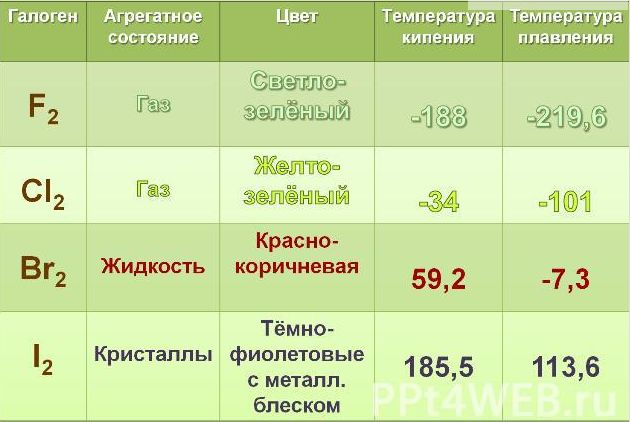
ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
Все галогены — токсичные вещества.
Отравление хлором. Жидкий хлор вызывает серьезные ожоги кожи. Газообразный хлор оказывает сильное раздражающее действие, особенно на глаза и дыхательную систему. Он реагирует с водой, содержащейся в глазах, легких и слизистых оболочках органов дыхания, образуя соляную кислоту и хлорноватистую кислоту (см. ниже «Реакции с водой и щелочами»). Симптомами отравления хлором являются жжение глаз и органов дыхания, непрекращающийся кашель и, в тяжелых случаях, кровавая мокрота. В легких, отравленных хлором, может развиваться бронхиальная пневмония. Предельно допустимая концентрация хлора в воздухе составляет 0,005 мг/дм3. Уровень 0,2 мг/дм3 считается опасным, а концентрация 2 мг/дм3 может вызвать быструю смерть. Однако случаи отравления хлором со смертельным исходом в аварийной обстановке нечасты, поскольку людей, надышавшихся этим газом, обычно удается вовремя удалить из отравленной зоны.
Галогены имеют характерный резкий запах, хорошо знакомый тем, кто посещает плавательные бассейны.
Все галогены имеют большую летучесть. Она объясняется тем, что их молекулы удерживаются вместе лишь слабыми вандерваальсовыми силами. Хотя вандерваальсовы силы постепенно возрастают при перемещении к нижней части группы галогенов, они остаются очень слабыми даже в кристаллах иода, которые поэтому легко возгоняются при нагревании. При этом образуются фиолетовые пары иода. Температуры плавления и кипения галогенов указаны в табл. 2.
Таблица 2. Физические свойства галогенов
|
Элемент |
Температура плавления, °С |
Температура кипения, °С |
Агрегатное состояние и внешний вид при 20°С |
|
Фтор |
-220 |
-188 |
Бледно-желтый газ |
|
Хлор |
-101 |
-34 |
Желто-зеленый газ |
|
Бром |
-7 |
58 |
Коричневая жидкость с тяжелыми коричневыми парами |
|
Иод |
114 |
183 |
Блестящие серо-черные кристаллы |
Все галогены — окрашенные вещества. Интенсивность их окраски возрастает по мере перемещения к нижней части группы.
Галогены обладают небольшой растворимостью в воде. Раствор хлора в воде называется хлорной водой. Галогены хорошо растворяются в органических растворителях, образуя окрашенные растворы. Например, хлор растворяется в тетрахлоро-метане, образуя желтый раствор, бром образует красный раствор, а иод-фиолетовый.
РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
Галогены представляют собой наиболее реакционноспособную группу элементов в периодической системе. Они состоят из молекул с очень низкими энергиями диссоциации связи (см. табл. 1), а их атомы имеют во внешней оболочке семь электронов и поэтому очень электроотрицательны. Фтор-наиболее электроотрицательный и наиболее реакционноспособный неметаллический элемент в периодической системе. Реакционная способность галогенов постепенно уменьшается при перемещении к нижней части группы. В следующем разделе будет рассмотрена способность галогенов окислять металлы и неметаллы и показано, как эта способность уменьшается в направлении от фтора к иоду.
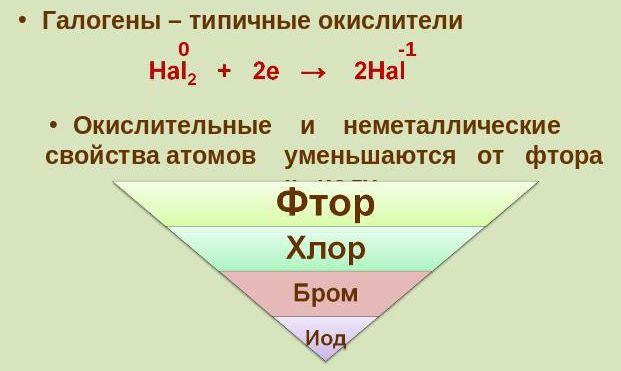
ГАЛОГЕНЫ КАК ОКИСЛИТЕЛИ
При пропускании газообразного сероводорода через хлорную воду происходит осаждение серы. Реакция протекает по уравнению
В этой реакции хлор окисляет сероводород, отнимая у него водород. Хлор окисляет также железо (II) до железа (III). Например, если перемешивать встряхиванием хлор с водным раствором сульфата железа (II), образуется сульфат железа (III):
Происходящая при этом окислительная полуреакция описывается уравнением
В качестве другого примера окислительного действия хлора приведем синтез хлорида натрия при сжигании натрия в хлоре:
В этой реакции происходит окисление натрия, поскольку каждый атом натрия теряет электрон, образуя ион натрия:
Хлор присоединяет эти электроны, образуя хлорид-ионы:
Таблица 3. Стандартные электродные потенциалы галогенов
|
Электродная реакция |
Стандартный электродный потенциал Е ° , В |
|
F 2 (г.)+2 e – « 2 F – (водн.) |
+2,87 |
|
Cl 2 (г.)+2 e – « 2 Cl – (водн.) |
+1,36 |
|
Br2 ( ж .)+2e– « 2Br– (водн.) |
+1,09 |
|
I2 ( тв .)+2e– « 2I– ( водн .) |
+0,54 |
Таблица 4. Стандартные энтальпии образования галогенидов натрия
|
Галогенид |
Стандартная энтальпия образования, D H ° обр, m , кДж/моль |
|
NaF |
-573 |
|
Na Cl |
-414 |
|
NaBr |
-361 |
|
Nal |
-288 |
Окислителями являются все галогены, из них фтор-самый сильный окислитель. В табл. 3 указаны стандартные электродные потенциалы галогенов. Из этой таблицы видно, что окислительная способность галогенов постепенно уменьшается в направлении к нижней части группы. Эту закономерность можно продемонстрировать, добавляя раствор бромида калия в сосуд с газообразным хлором. Хлор окисляет бромид-ионы, в результате чего образуется бром; это приводит к появлению окраски у прежде бесцветного раствора:
Таким образом, можно убедиться, что хлор более сильный окислитель, чем бром. Точно так же, если смешать раствор иодида калия с бромом, образуется черный осадок из твердого иода. Это означает, что бром окисляет иодид-ионы:
Обе описанные реакции являются примерами реакций вытеснения (замещения). В каждом случае более реакционноспособный, то есть являющийся более сильным окислителем, галоген вытесняет из раствора менее реакционноспособный галоген.
Окисление металлов. Галогены легко окисляют металлы. Фтор легко окисляет все металлы, исключая золото и серебро. Мы уже упоминали о том, что хлор окисляет натрий, образуя с ним хлорид натрия. Приведем еще один пример: когда поток газообразного хлора пропускают над поверхностью нагретых железных опилок, образуется хлорид железа (III), твердое коричневое вещество:
Даже иод способен, хотя и медленно, окислять металлы, расположенные в электрохимическом ряду ниже его. Легкость окисления металлов различными галогенами уменьшается при перемещении к нижней части VII группы. В этом можно убедиться, сравнивая энергии образования галогенидов из исходных элементов. В табл. 4 указаны стандартные энтальпии образования галогенидов натрия в порядке перемещения к нижней части группы.
Окисление неметаллов. За исключением азота и большинства благородных газов, фтор окисляет все остальные неметаллы. Хлор реагирует с фосфором и серой. Углерод, азот и кислород не вступают в реакции непосредственно с хлором, бромом или иодом. Об относительной реакционной способности галогенов к неметаллам можно судить, сравнивая их реакции с водородом (табл. 5).
Окисление углеводородов. При определенных условиях галогены окисляют углеводороды. Например, хлор полностью отщепляет водород от молекулы скипидара:
Окисление ацетилена может протекать со взрывом:
Таблица 5. Реакции галогенов с водородом
|
Реакция |
Характер и условия протекания |
|
Н2 (г.)+ F 2 (г.) ® 2Н F (г.) |
Протекает со взрывом |
|
Н2 (г.)+С l 2 (г.) ® 2НС l (г.) |
Протекает со взрывом на свету, но медленно в темноте |
|
Н2 (г.)+В r 2 (г.) ® 2НВ r (г.) |
Протекает только при нагревании и в присутствии катализатора |
|
Н2 (г.)+ I 2 (г.) ® 2Н I (г.) |
Протекает медленно даже при нагревании |
Реакции с водой и щелочами
Фтор реагирует с холодной водой, образуя фтороводород и кислород:
Хлор медленно растворяется в воде, образуя хлорную воду. Хлорная вода имеет небольшую кислотность вследствие того, что в ней происходит диспропорционирование хлора с образованием соляной кислоты и хлорноватистой кислоты:
Бром и иод диспропорционируют в воде аналогичным образом, но степень диспропорционирования в воде уменьшается от хлора к иоду.
Хлор, бром и иод диспропорционируют также в щелочах. Например, в холодной разбавленной щелочи бром диспропорционирует на бромид-ионы и гипобромит-ионы (бромат (I)-ионы):
При взаимодействии брома с горячими концентрированными щелочами диспропорционирование протекает дальше:
Иодат (I), или гипоиодит-ион, неустойчив даже в холодных разбавленных щелочах. Он самопроизвольно диспропорционирует с образованием иодид-иона и иодат(V)-иона.
Реакция фтора со щелочами, как и его реакция с водой, не похожа на аналогичные реакции других галогенов. В холодной разбавленной щелочи протекает следующая реакция:
В горячей концентрированной щелочи реакция с фтором протекает так:
Анализ на галогены и с участием галогенов
Качественный и количественный анализ на галогены обычно выполняется с помощью оаствора нитрата серебра. Например
Для качественного и количественного определения иода может использоваться раствор крахмала. Поскольку иод очень мало растворим в воде, его обычно анализируют в присутствии иодида калия. Так поступают по той причине, что иод образует с иодид-ионом растворимый трииодидный ион I3– :
Растворы иода с иодидами используются для аналитического определения различных восстановителей, например тиосульфат (VI)-ионов, а также некоторых окислителей, например манганат(VII)-ионов. Окислители смещают указанное выше равновесие влево, высвобождая иод. Иод затем титруют тиосульфатом (VI).
Автор:
Ларикова Алина, Конобеева Ирина
В творчестве учащиеся пытаются найти в себе какие-либо скрытые у них таланты…
Скачать:
Предварительный просмотр:
Ларикова Алина
Ученица 9 класса
МОУ СОШ №12
г. Новоалександровска
Ставропольского края
БРОМ
Жил- был Бром и было у него много друзей неметаллов — это и Фтор, и Хлор, и Иод…
Неметаллы не очень любили металлов, да и металлы в свою очередь не проявляли к ним большой любви и дружбы. И как- то раз поздно вечером гулял Бром со своими друзьями ,но отстал он от них и увидел, что на скамейке в парке кто-то сидит. Подошел поближе и увидел он Серебро — очень красивый металл. Бром подошел к ней познакомился. Узнав друг-друга поближе они стали настоящими друзьями. Решили он видится только по вечерам ,чтобы их некто не узнал. Через какое -то время они про взаимодействовали друг с другом и создали соль — Бромид Серебра. Друзья решили что останутся такими навсегда и родные не смогут их разлучить, но лишь взошло солнце и свет попал на них они снова отделились друг от друга. С тех пор Бром и Серебро видятся и взаимодействуют только в темное время суток, а умные люди начали применять эту реакцию в создании фотографий.
Конобеева Ирина
Ученица 9 класса
МОУ СОШ №12
г. Новоалександровска
Ставропольского края
ГАЛОГЕНЫ
Жил — был маленький химический элемент Хлор. Он сильно отличался от своих знакомых и сверстников — таких, как Углерод, Азот, Бор, Кислород и многих других. Отличался он тем, что у него был жёлто — зелёный окрас, а многим не нравился его резкий, удушливый запах.
Надоело Хлору слушать насмешки его знакомых, вот он и решил отправиться в путешествие и найти себе новых друзей. Долго шёл Хлор, многих элементов повстречал на своем пути, хороших и плохих. И вот набрел он на дом, в котором было 5 этажей. На каждом этаже было только 1 окошко. Постучался Хлор в окошко на 1 этаже, открыл ему дружелюбный Астат. Он и созвал всех остальных жителей домика. Поговорили они, обсудили, что да, как решили, что Хлор останется жить с ними. Тем более, что комната на 3 этаже пустовала. Новые друзья Хлора были такими же, как и он — необычные. С необычным окрасом и запахом.
Вот так и сейчас живут друзья галогены в 7 группе, главной подгруппы Периодической системы Д.И. Менделеева.
Обновлено: 11.03.2023
Молекулы галогенов двухатомны: F2, Cl2, Br2, I2. С ростом заряда ядра атома химического элемента, т.е. при переходе от фтора к йоду окислительная способность галогенов снижается, что подтверждается способностью вытеснения нижестоящих галогенов вышестоящими из галогеноводородных кислот и их солей:
Физические свойства галогенов
При н.у. фтор – газ светло-желтого цвета, обладающий резким запахом. Ядовит. Хлор – газ светло-зеленого цвета, также как и фтор имеет резкий запах. Сильно ядовит. При повышенном давлении и комнатной температуре легко переходит в жидкое состояние. Бром – тяжелая жидкость красно-бурого цвета с характерным неприятным резким запахом. Жидкий бром, а также его пары сильно ядовиты. Бром плохо растворяется в воде и хорощо в неполярных растворителях. Йод – твердое вещество темно-серого цвета с металлическим блеском. Пары йода имеют фиолетовый цвет. Йод легко возгоняется, т.е. переходит в газообразное состояние из твердого, при этом минуя жидкое состояние.
Получение галогенов
Галогены можно получить при электролизе растворов или расплавов галогенидов:
Наиболее часто галогены получают по реакции окисления галогенводородных кислот:
Химические свойства галогенов
Наибольшей химической активностью обладает фтор. Большинство химических элементов даже при комнатной температуре взаимодействует с фтором, выделяя большое количество теплоты. Во фторе горит даже вода:
Свободный хлор менее реакционноспособен, чем фтор. Он непосредственно не реагирует с кислородом, азотом и благородными газами. Со всеми остальными веществами он взаимодействует подобно фтору:
При взаимодействии хлора с водой на холоде происходит обратимая реакция:
Смесь, представляющую собой продукты реакции, называют хлорной водой.
При взаимодействии хлора с щелочами на холоде образуются смеси хлоридов и гипохлоритов:
При растворении хлора в горячем растворе щелочи происходит реакция:
Йод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие йода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
Галогены — элементы (VIIA) группы периодической системы: фтор F , хлор Cl , бром Br , иод I и астат At .
Валентные электроны галогенов образуют три электронные пары, а один электрон внешнего энергетического уровня остаётся неспаренным.
С возрастанием порядкового номера от фтора к иоду увеличиваются радиусы атомов, снижается их электроотрицательность. Значит, неметаллические свойства галогенов по группе сверху вниз ослабевают .
До завершения внешнего электронного слоя атомам галогенов не хватает только одного электрона, поэтому им наиболее характерна степень окисления (–1).
У фтора электроотрицательность больше, чем у остальных элементов, и поэтому степень окисления (–1) — его единственная возможная степень окисления в соединениях.
Галогены образуют с металлами соединения с ионной связью, а с другими неметаллами — соединения с ковалентной полярной связью.
Связь в молекулах ковалентная неполярная, одинарная. Кристаллическая решётка — молекулярная. Поэтому у галогенов невысокие температуры кипения и плавления.
При обычных условиях фтор представляет собой светло-жёлтый газ, хлор — жёлто-зелёный газ, бром — красно-коричневую жидкость, иод — тёмно-фиолетовые кристаллы.
Твёрдый иод при нагревании легко возгоняется (переходит в газообразное состояние и обратно в твёрдое, не превращаясь в жидкость).
В ряду галогенов с увеличением относительной молекулярной массы возрастают температуры кипения и плавления, увеличивается плотность, более интенсивной становится окраска.
Хлор знаком любой домохозяйке и сотруднику клининговой компании. А уж его запах знают все, кто посещал бассейн или лечебные учреждения России. Не пустой звук для советских школьников. Даже не из курса химии, а из уроков химзащиты в рамках начальной военной подготовки (НВП).
Что такое галогены
Перечень и общая характеристика галогенов
С первыми четырьмя элементами из списка некоторое знакомство имеется. Надо заметить, что вещества хоть и достаточно распространенные, но в чистом виде в природе не встречаются. Только в составе соединений.
Теннессин существует скорее теоретически. На Земле, по крайней мере, не нашли. Рекордное зафиксированное (и признанное) в лаборатории количество – 6 ядер. Включая изотоп.
Физические свойства
Хлор – настоящее боевое отравляющее вещество. И применялось в таком качестве. Попадая в незащищенные глаза и органы, образует кислоты. С соответствующими последствиями. Для летального исхода достаточно концентрации в воздухе 2 мг/л.
В воде растворимость ограничена. Лучше ведёт себя с органическими растворителями. Растворы оригинально окрашены: от слабо желтого до фиолетового.
Химические свойства галогенов
Общее уравнение:
Можно сказать, что F реагирует со всеми простыми субстанциями, кроме отдельных благородных газов. А так (с облучением):
К галогенам относятся пять основных неметаллических элементов, которые расположены в VII группе таблицы Менделеева. В эту группу входят такие химические элементы, как фтор F, хлор Cl, бром Br, иод I, астат At.
Галогены вступают в реакцию практически со всеми простыми веществами, за исключением только нескольких металлов. Они являются довольно таки энергичными окислителями, имеют очень сильный и резкий запах, прекрасно взаимодействуют с водой, а также имеют большую летучесть и высокую электроотрицательность. А вот в природе их можно встретить лишь в качестве соединений.
Физические свойства галогенов
1. Такие простые химические вещества, как галогены, состоят из двух атомов;
2. Если рассматривать галогены в обычных условиях, то следует знать, что фтор и хлор, находятся в газообразном состоянии, тогда как бром является жидким веществом, а йод и астат относятся к твердым веществам.
3. У галогенов температура плавления, кипения и плотность повышаются с увеличением атомной массы. Также при этом и меняется их окраска, она становиться более темной.
4. При каждом увеличении порядкового номера, уменьшается химическая активность, электроотрицательность и более слабыми становятся неметаллические свойства.
5. Галогены обладают способностью образовывать соединения между собой, как например BrCl.
6. Галогены при комнатной температуре могут находиться во всех трех состояниях материи.
7. Так же важно запомнить то, что галогены относятся к довольно таки токсичным химическим веществам.
Химические свойства галогенов
При химической реакции с металлами, галогены действуют, как окислители. Если, к примеру, взять фтор, то даже в обычных условиях он дает реакцию с большинством металлов. А вот алюминий и цинк воспламеняется даже в атмосфере: +2-1:ZnF2.
Получение галогенов
При получении фтора и хлора в масштабах промышленности используют электролиз или растворы солей.
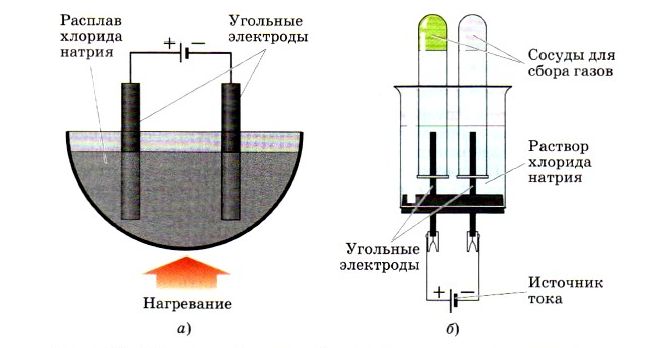
Если вы внимательно рассмотрите рисунок, изображенный внизу, то увидите, как в лабораторных условиях с помощью установки для электролиза можно получить хлор:
На первом рисунке изображена установка для расплава хлорида натрия, а на втором уже для получения раствора хлорида натрия.
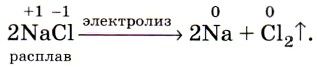
Такой процесс электролиза расплава хлорида натрия можно представить в виде даного уравнения:
При помощи такого электролиза, кроме получения хлора еще образуются также водород и гидроксид натрия:
Конечно же, водород получают более простым и дешевым способом, чего не скажешь об гидроксиде натрия. Его, так же, как и хлор получают практически всегда только с помощью электролиза раствора поваренной соли.
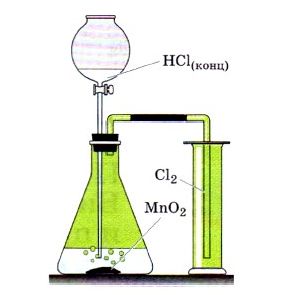
Если вы рассмотрите рисунок, изображенный вверху, то увидите, как лабораторным способом можно получить хлор. А получают его с помощью взаимодействия соляной кислоты с оксидом марганца:
В промышленности бром и йод получают с помощью реакции вытеснения этих веществ хлором из бромидов и йодидов.
Применение галогенов
Фтор или правильнее будет назвать фторид меди (CuF2) имеет довольно таки широкое применение. Его используют при изготовлении керамики, эмалей и различных глазурей. Имеющая в каждом доме тефлоновая сковородка и хладагент в холодильниках и кондиционере, также появились благодаря фтору.
Кроме бытовых нужд тефлон также используют в медицинских целях, так как его применяют при производстве имплантатов. Фтор необходим при изготовлении лизн в оптике и в зубных пастах.
Хлор также в нашей жизни встречается буквально на каждом шагу. Самым массовым и распространенным применением хлора, является, конечно же, поваренная соль NaCl. Она так же выступает в роли дезинтоксикационного средства и используется в борьбе с гололедом.
Кроме этого, хлор незаменим в производстве пластика, синтетического каучука и поливинилхлорида, благодаря которым мы получаем одежду, обувь и другие, нужные в нашей повседневной жизни вещи. Его используют при производстве отбеливателей, порошков, красителей, а также другой бытовой химии.
Бром, как правило, необходим, как светочувствительное вещество при печатании фотографий. В медицине он применяется, как успокаивающее средство. Также бром используют при производстве инсектицидов и пестицидов и т.д.
Ну, а всем известный йод, который имеется в аптечке у каждого человека, в первую очередь используется, как антисептик. Кроме своих антисептических свойств, йод присутствует в источниках света, а также является помощником для обнаружения отпечатков пальцев на бумажной поверхности.
Роль галогенов и их соединений для организма человека
Выбирая в магазине зубную пасту, наверное, каждый из вас обращал внимание на то, что на ее этикетке указывается содержание соединений фтора. И это неспроста, так как этот компонент участвует в построении зубной эмали и костей, повышает устойчивость зубов к кариесу. Также он играет важную роль в процессах обмена веществ, участвует в построении скелета костей и предупреждает появление такого опасного заболевания, как остеопороз.
Важная роль в организме человека отведена и хлору, так как он принимает активное участие в сохранении водно-солевого баланса и поддерживание осмотического давления. Хлор участвует в обмене веществ человеческого организма, построении тканей, ну и что тоже немаловажно – в избавление от лишнего веса. Соляная кислота, находящаяся в составе желудочного сока большое значение имеет для пищеварения, так как без нее невозможен процесс переваривания пищи.
Хлор необходим нашему организму и должен ежедневно в необходимых дозах поступать в него. Но если, же его норму поступления в организм превысить или резко снизить, то мы сразу же это ощутим в виде отеков, головных болей и других неприятных симптомов, которые способны не только нарушить обмен веществ, но и вызвать заболевания кишечника.
У человека в мозге, почках, крови и печени присутствует небольшое количество брома. В медицинских целях бром применяют, как успокоительное средство. Но при его передозировке могут быть неблагоприятные последствия, которые могут привести к угнетенному состоянию нервной системы, а в некоторых случаях и к психическим расстройствам. А недостаток брома в организме ведет к дисбалансу между процессами возбуждения и торможения.
Без йода наша щитовидная железа не может обходиться, так как он способен убивать микробы, поступающие в наше тело. При дефиците йода в организме человека может начаться заболевание щитовидной железы, под названием зоб. При этом заболевании появляются довольно неприятные симптомы. Человек, у которого появился зоб, чувствует слабость, сонливость, повышение температуры, раздражительность и упадок сил.
Из всего этого можно сделать вывод, что без галогенов человек мог бы не только лишиться многих необходимых в повседневной жизни вещей, но без них и не смог бы нормально функционировать наш организм.
Читайте также:
- Сообщение про специи краткое
- Сообщение от 3410 что это такое
- Наводнение в крыму сообщение
- Сообщение о заповеднике канады
- Александровский заповедник ставропольский край сообщение
§ 24. Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. В промышленности фтор и хлор получают электролизом расплавов или растворов их солей. Модели лабораторных установок для электролитического получения хлора изображены на рисунке 103. Например, процесс электролиза расплава хлорида натрия можно отразить уравнением:
Рис. 103.
Модель лабораторной установки для электролиза:
а — расплава хлорида натрия; б — раствора хлорида натрия
При получении хлора электролизом раствора хлорида натрия кроме хлора образуются также водород и гидроксид натрия:

Но если водород можно получить другими, более удобными и дешёвыми способами, например из природного газа, то гидроксид натрия, как и хлор, получают почти исключительно электролизом раствора поваренной соли.
В лаборатории (рис. 104) хлор получают взаимодействием соляной кислоты с оксидом марганца:
Рис. 104.
Получение хлора лабораторным способом
Бром и иод получают в промышленности по реакции вытеснения их хлором соответственно из бромидов и иодидов.
Биологическое значение и применение галогенов. Фтор. Вы не могли не обратить внимания, что на этикетках многих марок зубных паст указывают содержание в них фтора — конечно, не свободного, а его соединений. Благодаря этому важному компоненту, участвующему в построении зубной эмали и костей, предотвращается такое заболевание, как кариес зубов.
Кроме того, фтор является необходимым элементом в процессах обмена веществ в железах, мышцах и нервных клетках.
Важное значение имеет фтор и в промышленном производстве, где основные потребители его — ядерная промышленность и электротехника. Его соединение Na3AlF6 (как его называют?) используют для производства алюминия. А в быту всё более широкое применение находит посуда с тефлоновым покрытием (тефлон — фторсодержащая пластмасса).
Хлор. Один из химических элементов, без которых немыслимо существование живых организмов. Основная форма его поступления в организм — это хлорид натрия, который стимулирует обмен веществ, рост волос, придаёт бодрость и силу. Больше всего хлорида натрия NaCl содержится в плазме крови.
Особую роль в пищеварении играет соляная кислота НСl, которая входит в состав желудочного сока. Без 0,2%-й соляной кислоты практически прекращается процесс переваривания пищи. И хотя почти все пищевые продукты содержат некоторое количество поваренной соли, человек вынужден добавлять к пище ежедневно около 20 г соли.
По масштабам промышленного применения хлор намного превосходит все галогены. Хлор и его соединения необходимы для отбеливания льняных и хлопчатобумажных тканей, бумаги и т. д. (рис. 105). Особенно много его расходуют в органическом синтезе для производства пластмасс, каучуков, красителей и растворителей.
Рис. 105.
Хлор и его соединения применяют для производства химических продуктов:
1 — синтетического каучука; 2 — пластмасс; 3 — химических средств защиты растений; 4 — соляной кислоты; 5 — брома и иода; 6 — лекарственных средств; 7 — синтетических волокон; 8—10 — хлорной извести, используемой для отбеливания тканей (8) и бумаги (9), хлорирования воды (10); 11 — органических растворителей
Многие хлорсодержащие соединения используют для борьбы с вредителями сельского хозяйства. В больших количествах соединения хлора (хлорная известь) необходимы для обеззараживания питьевой воды, правда, далеко не без отрицательных последствий (какое вещество безопаснее применять для этой цели?). В цветной металлургии методом хлорирования из руд извлекают некоторые металлы (титан, ниобий, тантал).
Хлор нашёл применение и в военных целях в качестве боевого отравляющего вещества. Позднее он был заменён другими, более эффективными хлорсодержащими отравляющими веществами, например фосгеном СОСl2.
Хлор содержится в очень опасном для жизни и здоровья веществе — диоксине. Летучие соединения хлора — одна из причин разрушения озонового слоя Земли.
Бром. Ещё один галоген — бром также весьма важен для организма человека. Соединения этого элемента регулируют процессы возбуждения и торможения центральной нервной системы, поэтому для лечения нервных болезней (бессонницы, истерии, неврастении и т. д.) врачи прописывают бромсодержащие препараты.
Бром активно накапливают некоторые растения, в том числе морские водоросли. Именно в море сосредоточена большая часть брома на нашей планете, и море служит главным поставщиком брома. Подсчитано, что ежегодно вместе с морской водой в воздух переходит около 4 млн т брома. Понятно, что содержание его в воздухе приморских районов всегда больше, чем в районах, далёких от моря.
Не менее важную роль бром, а точнее, бромид серебра AgBr играет в фотографии. Фотобумага содержит нанесённый на неё с помощью желатина слой бромида серебра, который легко разлагается под действием света:
Иод. Последний из рассматриваемых нами галогенов — иод — элемент, без которого человек не может жить: недостаток его в воде и пище снижает выработку гормонов щитовидной железы и приводит к заболеванию эндемическим зобом. Гормоны щитовидной железы регулируют мышечную деятельность, работу сердца и мозга, а также аппетит, пищеварение.
Иод поступает в организм вместе с водой, воздухом и пищей: хлебом, яйцами, молоком, водой, морской капустой (рис. 106).
Рис. 106.
Иод поступает в организм человека с пищей
Спиртовой раствор иода (5—10%-й), называемый йодной настойкой, применяют для обработки ран (рис. 107). Иод входит в состав многих лекарств.
Рис. 107.
Спиртовая настойка иода есть в каждой аптечке
Главными потребителями иода являются фармацевтическая и химическая промышленность, а также производство светочувствительных фотоматериалов.
Новые слова и понятия
- Получение галогенов электролизом расплавов и растворов солей.
- Биологическое значение галогенов.
- Применение хлора и соединений фтора, хлора и иода.
Задания для самостоятельной работы
- Вычислите объём хлора (н. у.) и массу натрия, которые можно получить при электролизе 585 г хлорида натрия, содержащего 2% примесей.
- Рассчитайте, сколько граммов 40%-го раствора щёлочи можно получить из натрия, массу которого вы определили в предыдущей задаче.
- Французский химик К. Шееле получил хлор по реакции оксида марганца (IV) с соляной кислотой. В результате этой реакции образуются также хлорид марганца (II) и вода. Составьте уравнение этой реакции, рассмотрите окислительно-восстановительные процессы и рассчитайте массу оксида марганца (IV) и количество хлороводорода, необходимых для получения 100 л хлора (н. у.), если выход его составляет 95% от теоретически возможного.
- Подготовьте сообщение о положительном и отрицательном значении галогенов и их соединений в жизни человека.
- Извечная заповедь медицины: «Малые дозы — лекарство, а большие — яд». Докажите её на примерах из химии галогенов.
- Английский поэт Уилфред Оуэн, погибший в сражениях Первой мировой войны, написал такие строки:
Газ! Газ! Скорей! — неловкие движенья,
Напяливание масок в едкой мгле!
Один замешкался, давясь и спотыкаясь,
Барахтаясь, как в огненной смоле,
В просветах мутного зелёного тумана.
Бессильный, как во сне, вмешаться и помочь,
Я видел только — вот он зашатался,
Рванулся и поник — бороться уж невмочь.
Какое событие описывает поэт? Какой галоген выступает в страшной роли убийцы? Какие его свойства упоминаются в стихотворении?
Используя свои знания по химии галогенов, напишите сочинение на тему «Художественный образ вещества или процесса». Для того чтобы иметь представление, как это делают другие ученики, прочитайте сочинение ученика 9 класса 531-й школы Москвы Ильи Горшкова (1990).
Самый сильный окислитель
Жил-был Кислород. И был он таким сильным, что, с кем ни встретится, сразу окислит. И назвали Кислород окислителем, а вещества, получающиеся в реакции с Кислородом, — оксидами, сам процесс — окислением. Ходит Кислород по таблице Менделеева и со всеми в реакцию вступает. Стал он хвастливым, заносчивым и решил, будто в химическом мире нет никого сильнее его. И всё же Кислород ошибся. Как-то раз встретил он в таблице Фтор. Решил Кислород окислить Фтор. Позвал он на помощь Водород и, образовав в соединении с ним воду, пошёл в наступление на Фтор. И произошло чудо. Вода, которой тушат пожары, сама загорелась во Фторе. Кислород, считавшийся окислителем, в этой реакции стал восстановителем. Так Фтор превзошёл Кислород и оказался самым сильным из окислителей.
Какие химические понятия осветил Илья в своём сочинении? Выпишите их и дайте их определения.
Галогены. Химия галогенов и их соединений
Галогены
Положение в периодической системе химических элементов
Галогены расположены в главной подгруппе VII группы (или в 17 группе в современной форме ПСХЭ) периодической системы химических элементов Д.И. Менделеева.
Электронное строение галогенов
Электронная конфигурация галогенов в основном состоянии соответствует формуле ns 2 np 5 .
Например , электронная конфигурация фтора :
Электронная концигурация хлора :
Атомы галогенов содержат на внешнем энергетическом уровне 1 неспаренный электрон и три неподеленные электронные пары в основном энергетическом состоянии. Следовательно, в основном состоянии атомы галогенов могут образовывать 1 связи по обменному механизму.
При этом у фтора возбужденного состояния нет, т.е. максимальная валентность фтора в соединения равна I.
Однако, в отличие от фтора, за счет вакантной d-орбитали атомы хлора, брома и йода могут переходить в возбужденное энергетическое состояние.
Таким образом, максимальная валентность галогенов (кроме фтора) в соединениях равна VII. Также для галогенов характерны валентности I, III, V.
Степени окисления атома галогенов – от -1 до +7. Характерные степени окисления -1, 0, +1, +3, +5, +7. Для фтора характерная степень окисления -1 и валентность I.
Физические свойства и закономерности изменения свойств
Галогены образуют двухатомные молекулы состава Hal2. В твёрдом состоянии имеют молекулярную кристаллическую решетку. Плохо растворимы в воде, все имеют запах, летучи.
| Галоген | F | Cl | Br | I |
| Электронная формула | … 2s 2 2p 5 | … 3s 2 3p 5 | … 4s 2 4p 5 | … 5s 2 5p 5 |
| Электроотрицательность | 4,0 | 3,0 | 2,8 | 2,5 |
| Степени окисления | -1 | -1, +1, +3, +5, +7 | -1, +1, +3, +5, +7 | -1, +1, +3, +5, +7 |
| Агрегатное состояние | Газ | Газ | Жидкость | Твердые кристаллы |
| Цвет | Светло-желтый | Жёлто-зелёный | Буровато-коричневый | Тёмно-серый с металлическим блеском |
| Запах | Резкий | Резкий, удушливый | Резкий, зловонный | Резкий |
| T плавления | –220 о С | –101 о С | –7 о С | 113,5 о С |
| Т кипения | –188 о С | –34 о С | 58 о С | 185 о С |
Внешний вид галогенов:
Фтор
Хлор
Бром
Йод
В природе галогены встречаются в виде соединений, в основном, в виде галогенидов.
Соединения галогенов
Типичные соединения хлора:
| Степень окисления | Типичные соединения |
| +7 | Хлорная кислота HClO4
Перхлораты MeClO4 |
| +5 | Хлорноватая кислота HClO3
Хлораты MeClO3 |
| +3 | Хлористая кислота HClO2 |
| +1 | Хлорноватистая кислота HClO
Гипохлориты MeClO |
| –1 | Хлороводород HCl, Хлориды MeCl |
Бром и йод образуют подобные соединения.
Способы получения галогенов
1. Получение хлора.
В промышленности хлор получают электролизом расплава или раствора хлорида натрия.
Электролиз расплава хлорида натрия.
В расплаве хлорид натрия диссоциирует на ионы:
NaCl → Na + + Cl −
На катоде восстанавливаются ионы натрия:
K(–): Na + +1e → Na 0
На аноде окисляются ионы хлора:
A(+): 2Cl − ̶ 2e → Cl2 0
Ионное уравнение электролиза расплава хлорида натрия:
2Na + + 2Cl − → 2Na º + Cl2º
Суммарное уравнение электролиза расплава хлорида натрия:
2NaCl → 2Na + Cl2
Электролиз раствора хлорида натрия.
В растворе хлорид натрия диссоциирует на ионы:
NaCl → Na + + Cl −
На катоде восстанавливаются молекулы воды:
K(–): 2H2O + 2e → H2° + 2OH −
На аноде окисляются ионы хлора:
A(+): 2Cl − ̶ 2e → Cl2 0
Ионное уравнение электролиза раствора хлорида натрия:
Суммарное уравнение электролиза раствора хлорида натрия:
2NaCl + 2H2O → H2↑ + 2NaOH + Cl2↑
В лаборатории хлор получают взаимодействием концентрированной соляной кислоты с сильными окислителями.
Например , взаимодействием соляной кислоты с оксидом марганца (IV)
Или перманганатом калия:
2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2↑ + 8H2O
Бертолетова соль также окисляет соляную кислоту:
KClO3 + 6HCl → KCl + 3Cl2↑ + 3H2O
Бихромат калия окисляет соляную кислоту:
2. Получение фтора.
Фтор получают электролизом расплава гидрофторида калия.
3. Получение брома.
Бром можно получить окислением ионов Br – сильными окислителями.
Например , бромоводород окисляется хлором:
2HBr + Cl2 → Br2 + 2HCl
Соединения марганца также окисляют бромид-ионы.
Например , оксид марганца (IV):
4. Получение йода.
Йод получают окислением ионов I – сильными окислителями.
Например , хлор окисляет йодид калия:
2KI + Cl2 → I2 + 2KCl
Соединения марганца также окисляют йодид-ионы.
Например , оксид марганца (IV) в кислой среде окисляет йодид калия:
Химические свойства галогенов
Химическая активность галогенов увеличивается снизу вверх – от астата к фтору.
1. Галогены проявляют свойства окислителей . Галогены реагируют с металлами и неметаллами .
1.1. Галогены не горят на воздухе. Фтор окисляет кислород с образованием фторида кислорода:
1.2. При взаимодействии галогенов с серой образуются галогениды серы:
1.3. При взаимодействии фосфора и углерода с галогенами образуются галогениды фосфора и углерода:
1.4. При взаимодействии с металлами галогены проявляют свойства окислителей, образуя галогениды.
Например , железо реагирует с галогенами с образованием галогенидов. При этом фтор, хлор и бром образуются галогениды железа (III), а c йодом — соединение железа (II):
3Cl2 + 2Fe → 2FeCl3
Аналогичная ситуация с медью : фтор, хлор и бром окисляют медь до галогенидов меди (II),а йод до йодида меди (I):
I2 + 2Cu → 2CuI
Активные металлы бурно реагируют с галогенами, особенно с фтором и хлором (горят в атмосфере фтора или хлора).
Еще пример : алюминий взаимодействует с хлором с образованием хлорида алюминия:
3Cl2 + 2Al → 2AlCl3
1.5. Водород горит в атмосфере фтора:
С хлором водород реагирует только при нагревании или освещении. При этом реакция протекает со взрывом:
Бром также реагирует с водородом с образованием бромоводорода:
Взаимодействие йода с водородом происходит только при сильном нагревании, реакция протекает обратимо, с поглощением теплоты (эндотермическая):
1.6. Галогены реагируют с галогенами. Более активные галогены окисляют менее активные.
Например , фтор окисляет хлор, бром и йод:
2. Со сложными веществами галогены реагируют, также проявляя преимущественно окислительные свойства. Галогены охотно диспропорционируют при растворении в воде или в щелочах.
2.1. При растворении в воде хлор и бром частично диспропорционируют, повышая и понижая степень окисления. Фтор окисляет воду.
Например , хлор при растворении в холодной воде диспропорционирует до ближайших стабильных степеней окисления (+1 и -1), образует при этом соляную кислоту и хлорноватистую кислоту (хлорная вода):
Cl2 + H2O ↔ HCl + HClO
При растворении в горячей воде хлор диспропорционирует до степеней окисления -1 и +5, образуя соляную кислоту и хлороватую кислоту:
Фтор реагирует с водой со взрывом:
2.2. При растворении в щелочах хлор, бром и йод диспропорционируют с образованием различных солей. Фтор окисляет щелочи.
Например , хлор реагирует с холодным раствором гидроксидом натрия:
При взаимодействии с горячим раствором гидроксида натрия образуются хлорид и хлорат:
Еще пример : хлор растворяется в холодном растворе гидроксида кальция:
2.3. Более активные галогены вытесняют менее активные галогены из солей и галогеноводородов.
Например , хлор вытесняет йод и бром из раствора йодида калия и бромида калия соответственно:
Cl2 + 2NaI → 2NaCl + I2
Cl2 + 2NaBr → 2NaCl + Br2
Еще одно свойство: более активные галогены окисляют менее активные.
Например , фтор окисляет хлор с образованием фторида хлора (I):
Cl2 + F2 → 2Cl + F –
В свою очередь, хлор окисляет йод. При этом в растворе образуется соляная кислота и йодная кислота:
2.4. Галогены проявляют окислительные свойства, взаимодействуют с восстановителями.
Например , хлор окисляет сероводород:
Cl2 + H2S → S + 2HCl
Хлор также окисляет сульфиты:
Также галогены окисляют пероксиды:
Или, при нагревании или на свету, воду:
2Cl2 + 2H2O → 4HCl + O2 (на свету или кип.)
Галогеноводороды
Строение молекулы и физические свойства
Галогеноводороды HHal – это бинарные соединения водорода с галогенами, которые относятся к летучим водородным соединениям. Галогеноводороды – бесцветные ядовитый газы, с резким запахом, хорошо растворимые в воде.
В ряду HCl – HBr – HI увеличивается длина связи и ковалентности связи уменьшается полярность связи H – Hal.
Растворы галогеноводородов в воде (за исключением фтороводорода) – сильные кислоты. Водный раствор фтороводорода – слабая кислота.
Способы получения галогеноводородов
В лаборатории галогеноводороды получают действием нелетучих кислот на хлориды металлов.
Например , действием концентрированной серной кислоты на хлорид натрия:
Галогеноводороды получают также прямым взаимодействием простых веществ:
Химические свойства галогеноводородов
1. В водном растворе галогеноводороды проявляют кислотные свойства . Взаимодействуют с основаниями, основными оксидами, амфотерными гидроксидами, амфотерными оксидами . Кислотные свойства в ряду HF – HCl – HBr – HI возрастают.
Например , хлороводород реагирует с оксидом кальция, оксидом алюминия, гидроксидом натрия, гидроксидом меди (II), гидроксидом цинка (II), аммиаком:
2HCl + CaO → CaCl2 + H2O
HCl + NaOH → NaCl + H2O
Как типичные минеральные кислоты, водные растворы галогеноводородов реагируют с металлами , расположенными в ряду активности металлов до водорода. При этом образуются соль металла и водород.
Например , соляная кислота растворяет железо. При этом образуется водород и хлорид железа (II):
Fe + 2HCl → FeCl2 + H2
2. В водном растворе галогеноводороды диссоциируют , образуя кислоты. Водный раствор фтороводорода (плавиковая кислота) – слабая кислота:
HF ↔ H + + F –
Водные растворы хлороводорода (соляная кислота), бромоводорода и йодоводорода – сильные кислоты, в разбавленном растворе диссоциируют практически полностью:
HCl ↔ H + + Cl –
3. Водные растворы галогеноводородов взаимодействуют с солями более слабых кислот и с некоторыми растворимыми солями (если образуется газ, осадок, вода или слабый электролит).
Например , соляная кислота реагирует с карбонатом кальция:
Качественная реакция на галогенид-ионы – взаимодействие с растворимыми солями серебра.
При взаимодействии соляной кислоты с нитратом серебра (I) образуется белый осадок хлорида серебра:
HCl + AgNO3 = AgCl↓ + HNO3
Осадок бромида серебра – бледно-желтого цвета:
HBr + AgNO3 = AgBr↓ + HNO3
Осадок иодида серебра – желтого цвета:
HI + AgNO3 = AgI↓ + HNO3
Фторид серебра – растворимая соль, поэтому реакция плавиковой кислоты и ее солей с нитратом серебра не является качественной.
Видеоопыты качественных реакций на хлорид-, бромид- и йодид-ионы (взаимодействие с нитратом серебра) можно посмотреть здесь.
4. Восстановительные свойства галогеноводородов усиливаются в ряду HF – HCl – HBr – HI.
Галогеноводороды реагируют с галогенами . При этом более активные галогены вытесняют менее активные.
Например , бром вытесняет йод из йодоводорода:
Br2 + 2HI → I2 + 2HBr
А вот хлор не может вытеснить фтор из фтороводорода.
Фтороводород практически невозможно окислить.
Концентрированная соляная кислота окисляется соединениями марганца с валетностью выше II или соединениями хрома (VI).
Например : концентрированная соляная кислота окисляется оксидом марганца (IV):
Бромоводород – сильный восстановитель и окисляется соединениями марганца, хрома (VI), концентрированной серной кислотой и другими сильными окислителями:
Например , бромоводород окисляется концентрированной серной кислотой:
Бромоводород реагирует с бихроматом калия с образованием молекулярного брома:
Или с оксидом марганца (IV):
Пероксид водорода также окисляет бромоводород до молекулярного брома:
Йодоводород – еще более сильный восстановитель, и окисляется другими неметаллами и даже такими окислителями, как соединения железа (III) и соединения меди (II).
Например , йодоводород реагирует с хлоридом железа (III) с образованием молекулярного йода:
2HI + 2FeCl3 → I2 + 2FeCl2 + 2HCl
или с сульфатом железа (III):
Йодоводород легко окисляется соединениями азота, например , оксидом азота (IV):
или молекулярной серой при нагревании:
2HI + S → I2 + H2S
5. Плавиковая кислота реагирует с оксидом кремния (IV) (растворяет стекло):
Галогениды металлов
Галогениды – это бинарные соединения галогенов и металлов или некоторых неметаллов, соли галогеноводородов.
Способы получения галогенидов
1. Галогениды металлов получают при взаимодействии галогенов с металлами . При этом галогены проявляют свойства окислителя.
Например , хлор взаимодействует с магнием и кальцием:
При взаимодействии железа с хлором образуется хлорид железа (III):
3Cl2 + 2Fe → 2FeCl3
2. Галогениды металлов можно получить при взаимодействии металлов с галогеноводородами.
Например , соляная кислота реагирует с железом с образованием хлорида железа (II):
Fe + 2HCl → FeCl2 + H2
3. Галогениды металлов можно получить при взаимодействии основных и амфотерных оксидов с галогеноводородами.
Например , при взаимодействии оксида кальция и соляной кислоты:
2HCl + CaO → CaCl2 + H2O
Еще пример : взаимодействие оксида алюминия с соляной кислотой:
4. Галогениды металлов можно получить при взаимодействии оснований и амфотерных гидроксидов с галогеноводородами.
Например , при взаимодействии гидроксида натрия и соляной кислоты:
HCl + NaOH → NaCl + H2O
Или при взаимодействии гидроксида меди (II) с соляной кислотой:
Гидроксид цинка (II) также взаимодействует с соляной кислотой:
5. Некоторые соли взаимодействуют с галогеноводородами с образованием галогенидов металлов.
Например , гидрокарбонат натрия реагирует с бромоводородом с образованием бромида натрия:
HBr + NaHCO3 → NaBr + CO2↑ + H2O
Взаимодействие с нитратом серебра – качественная реакция на соляную кислоту, бромодоводород и йодоводород:
HCl + AgNO3 → AgCl↓ + HNO3
HBr + AgNO3 → AgBr↓ + HNO3
HI + AgNO3 → AgI↓ + HNO3
Химические свойства галогенидов
1. Растворимые галогениды вступают в обменные реакции с растворимыми солями, кислотами и основаниями , если образуется осадок, газ или вода.
Например , бромиды, йодиды и хлориды реагируют с нитратом серебра с образованием желтого, желтого и белого осадков соответственно.
NaCl + AgNO3 → AgCl↓ + NaNO3
Фторид серебра – растворимая соль, поэтому реакция фторидов с нитратом серебра не является качественной.
Видеоопыты качественных реакций на хлорид-, бромид- и йодид-ионы (взаимодействие с нитратом серебра) можно посмотреть здесь.
2. Галогениды тяжелых металлов реагируют с более активными металлами . При этом более активные металлы вытесняют менее активные.
Например , магний вытесняет медь из расплава хлорида меди (II):
Mg + CuCl2 → MgCl2 + Cu
Обратите внимание! В растворе более активные металлы вытесняют менее активные только если более активные металлы не взаимодействуют с водой (металлы, расположенные в ряду активности до магния). Если добавляемый металл слишком активен, то он провзаимодействует с водой, а не с солью.
Например , натрий не вытесняет цинк из раствора хлорида цинка. Т.к. натрий реагирует с водой, а реакция с хлоридом цинка не идет.
Na + ZnCl2(раствор) ≠
3. Галогениды подвергаются электролизу в растворе или расплаве. При этом на аноде образуются галогены.
Например , при электролизе расплава бромида калия на катоде образуется клий, а на аноде – бром:
2KBr → 2K + Br2
При электролизе раствора бромида калия на катоде выдялется водород, а на аноде также образуется бром:
4. Галогениды металлов проявляют восстановительные свойства . Хлориды окисляются только сильными окислителями, а вот йодиды уже являются очень сильными восстановителями. В целом, восстановительные свойства галогенидов аналогичны свойствам галогеноводородов.
Например , бромид калия окисляется концентрированной серной кислотой:
Еще пример : йодид калия окисляется соединениями меди (II) и соединениями железа (III):
4KI + 2CuCl2 → 2CuI↓ + I2↓ + 4KCl
2KI + 2FeCl3 → I2↓ + 2FeI2 + 2KCl
Еще несколько примеров восстановительных свойств галогенидов:
KI + 3H2O + 3Cl2 → HIO3 + KCl + 5HCl
Более активные галогены вытесняют менее активные из солей.
При этом галогениды металлов не горят в кислороде.
5. Нерастворимые галогениды металлов растворяются под действием избытка аммиака .
Например , хлорид серебра (I) растворяется под действием избытка раствора аммиака:
6. Нерастворимые галогениды под действием света разлагаются на галоген и металл.
Например , хлорид серебра разлагается под действием ультрафиолета:
2AgCl → 2Ag + Cl2
Кислородсодержащие кислоты галогенов
Рассмотрим кислородсодержащие кислоты галогенов на примере хлора:
| Степень окисления галогена | +1 | +3 | +5 | +7 |
| Формула | HClO | HClO2 | HClO3 | HClO4 |
| Название кислоты | Хлорноватистая | Хлористая | Хлорноватая | Хлорная |
| Устойчивость и сила | Существует только в растворах, слабая кислота | Существует только в растворах, слабая кислота | Существует только в растворах, сильная кислота | Сильная кислота |
| Название соответствующей соли | Гипохлориты | Хлориты | Хлораты | Перхлораты |
Хлорноватистая кислота и ее соли
Хлорноватистая кислота HClO устойчива только в разбавленном водном растворе.
Cпособ получения хлорноватистой кислоты:
1. Диспропорционирование хлора в холодной воде :
Cl2 + H2O ↔ HCl + HClO
Химические свойства хлорноватистой кислоты:
Хлорноватистая кислота HClO – это слабая кислота, но сильный окислитель.
1. Под действием ультрафиолета (на свету) хлорноватистая кислота разлагается :
2HClO → 2HCl + O2
2. Как кислота, хлорноватистая кислота реагирует с сильными основаниями .
Например , с гидроксидом калия:
HClO + KOH → KClO + H2O
3. Ярко выражены окислительные свойства хлорноватистой кислоты за счет атома хлора в степени окисления +1. При взаимодействии с восстановителями хлор, как правило, восстанавливается до степени окисления -1.
Например , хлорноватистая кислота окисляет йодоводород:
HClO + 2HI → HCl + I2 + H2O
Хлорноватистая кислота также окисляет, например , пероксид водорода:
4. Хлорноватистая кислота диспропорционирует:
3HClO → 2HCl + НСlO3
Химические свойства солей хлорноватистой кислоты (гипохлоритов):
1. Более сильные кислоты вытесняют гипохлориты из солей.
Например , соляная кислота реагирует с гипохлоритом натрия:
NaClO + 2HCl → NaCl + Cl2 + H2O
Серная кислота реагирует с гипохлоритом кальция при нагревании или под действием излучения:
Даже угольная кислота вытесняет гипохлориты:
2. Гипохлориты вступают в обменные реакции с другими солями , если образуется слабый электролит.
Например , гипохлорит кальция реагирует с растворимыми карбонатами:
3. При нагревании гипохлориты разлагаются :
Хлористая кислота и ее соли
Хлористая кислота HClO2 – существует только в водных растворах.
Способы получения:
Хлористую кислоту можно получить окислением оксида хлора пероксидом водорода:
Химические свойства хлористой кислоты:
1. Хлористая кислота является также слабой. Реагирует с щелочами с образованием хлоритов:
2. При длительном хранении разлагается:
Хлорноватая кислота и ее соли
Хлорноватая кислота HClO3 – также существует только в водных растворах.
Способы получения:
Хлорноватую кислоту можно получить из солей хлорноватой кислоты – хлоратов.
Например , из хлората бария под действием серной кислоты:
Химические свойства хлорноватой кислоты:
1. Хлорноватая кислота – сильная кислота. Реагирует с щелочами с образованием хлоратов:
2. Хлорноватая кислота – сильный окислитель.
Например , хлорноватая кислота окисляет фосфор:
Химические свойства солей хлорноватой кислоты – хлоратов:
1. Хлораты – сильные окислители.
Например , хлорат калия (бертолетова соль) при нагревании разлагается. При этом без катализатора хлорат диспропорционирует:
4KClO3 → 3KClO4 + KCl
В присутствии катализатора (оксид марганца (IV)) хлорат калия разлагается, окисляя кислород:
2KClO3 → 2KCl + 3O2↑
Еще пример : хлорат калия окисляет серу и фосфор:
2KClO3 + 3S → 2KCl + 3SO2
Хлорная кислота и ее соли
Хлорная кислота HClO4 – это бесцветная жидкость, хорошо растворимая в воде.
Способы получения:
Хлорную кислоту можно получить из солей хлорной кислоты – перхлоратов.
Например , из перхлората натрия под действием серной кислоты:
Химические свойства хлорной кислоты:
1. Хлорная кислота – сильная кислота. Реагирует с щелочами с образованием перхлоратов:
2. Хлорная кислота – сильный окислитель.
Например , хлорная кислота окисляет углерод:
3. При нагревании хлорная кислота разлагается:
Химические свойства солей хлорной кислоты – перхлоратов:
1. Перхлораты – сильные окислители.
Например , перхлорат калия при нагревании разлагается. При этом хлор окисляет кислород:
Еще пример : перхлорат калия окисляет алюминий:
Галогены
Галогены (греч. hals — соль + genes — рождающий) — химические элементы VIIa группы: F, Cl, Br, I, At. Реагируют с большинством других элементов и органических соединений.
Галогены широко распространены в природе. Их химическая активность падает от фтора к астату.
Общая характеристика элементов VIIa группы
От F к At (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Все галогены относятся к неметаллам, являются сильными окислителями.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 5 :
- F — 2s 2 2p 5
- Cl — 3s 2 3p 5
- Br — 4s 2 4p 5
- I — 5s 2 5p 5
- At — 6s 2 6p 5
Для галогенов характерны нечетные степени окисления: -1, +1, +3, +5, +7. Это связано с электронной конфигурацией атомов в возбужденном состоянии.
Природные соединения
- NaCl — галит (каменная соль)
- CaF2 — флюорит, плавиковый шпат
- NaCl*KCl — сильвинит
- 3Ca3(PO4)2*CaF2 — фторапатит
- MgCl2*6H2O — бишофит
- KCl*MgCl2*6H2O — карналлит
Простые вещества — F2, Cl2, Br2, I2
Галогены в чистом виде можно получить путем электролиза водных растворов и расплавов их солей. Например, хлор в промышленности получают электролизом водного раствора хлорида натрия.
Электролизом расплава гидрофторида калия KHF2 в безводной плавиковой кислоте — HF — был впервые получен фтор.
Более активные галогены способны вытеснять менее активные. Активность галогенов убывает: F → Cl → Br → I.
В лабораторных условиях галогены могут быть получены следующими реакциями.
- Реакции с металлами
Для галогенов характерна высокая реакционная способность. Фтор реагирует со всеми металлами без исключения, некоторые из них в атмосфере фтора самовоспламеняются.
Реакции с неметаллами
Хлор, как и фтор, химически весьма активен. Не реагирует только с кислородом, азотом и благородными газами.
F2 + H2 → HF (в темноте со взрывом)
Галогены вступают в реакцию друг с другом. Чтобы определить степени окисления в получающихся соединениях, вспомните электроотрицательность 😉
Br2 + F2 → BrF (фтор более электроотрицателен, чем бром — F — )
Br2 + I2 → IBr3 (бром более электроотрицателен, чем йод — Br — )
Реакции с водой
Реакция фтора с водой протекает очень энергично, носит взрывной характер.
Хлор реагирует с водой обратимо, образуя хлорную воду — смесь хлорноватистой и соляной кислоты. Бром вступает в те же реакции, что и хлор.
Замечу, что активность йода существенно ниже, чем у остальных галогенов. С неметаллами йод почти не реагирует, а с металлами — только при нагревании.
Реакции с щелочами
Cl2 + NaOH → NaCl + NaClO + H2O
Галогены способны вытеснять друг друга из солей. Более активные вытесняют менее активные.
KBr + I2 ⇸ (реакция не идет, так как йод менее активен, чем бром)
Галогеноводороды
Соединения, образованные из галогенов и водорода. К галогеноводородам относятся следующие вещества:
- HF — фтороводород (газ), фтороводородная (плавиковая) кислота (жидкость)
- HCl — хлороводород (газ), соляная кислота (жидкость)
- HBr — бромоводород, бромоводородная кислота
- HI — йодоводород, йодоводородная кислота
- HAt — астатоводород, астатоводородная кислота
При н.у. HCl, HBr, HI — газы, хорошо растворимые в воде.
В промышленности применяют получение прямым методом: реакцией водорода с галогенами.
В лабораторных условиях галогеноводороды можно получить в реакциях обмена между галогенсодержащими солями и сильными кислотами.
HF — является слабой кислотой, HCl, HBr, HI — сильные кислоты. Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Галогеноводороды реагируют с основными, амфотерными оксидами и основаниями с образованием соответствующих солей.
KOH + HCl → KCl + H2O (реакция нейтрализации)
Реакции протекают в тех случаях, если в результате выпадает осадок, выделяется газ или образуется слабый электролит (вода).
В некоторых реакциях проявляют себя как сильные восстановители, особенно HI.
В целом взаимодействие галогеноводородов с оксидами неметаллов нехарактерно. В этой связи важно выделить реакцию SiO2 с плавиковой кислотой.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
источники:
http://chemege.ru/halogens/
http://studarium.ru/article/175