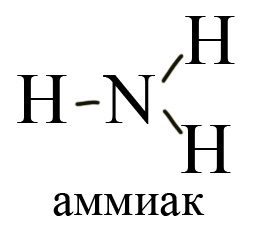
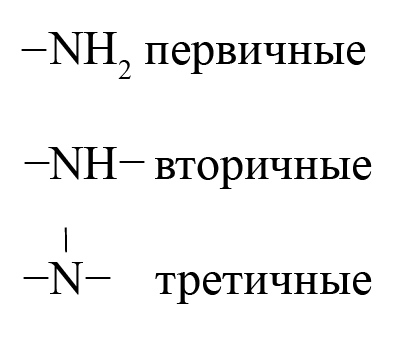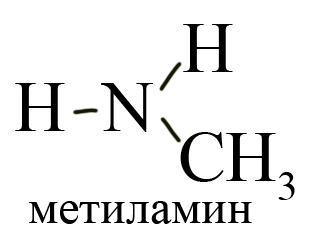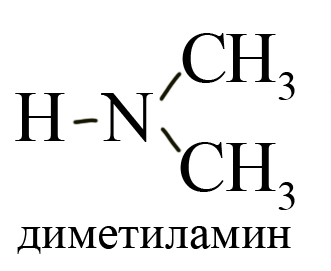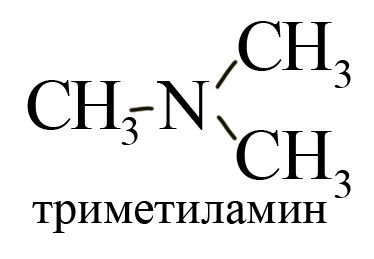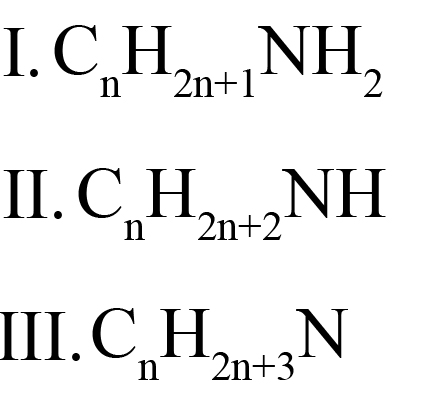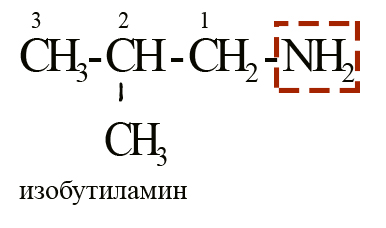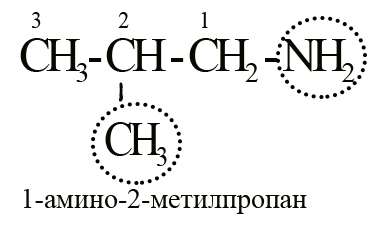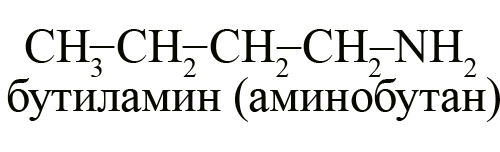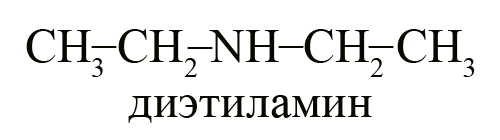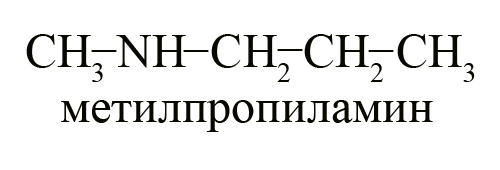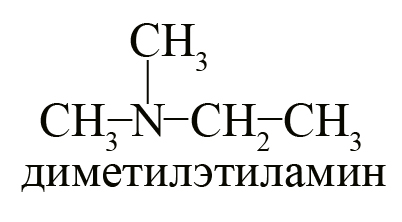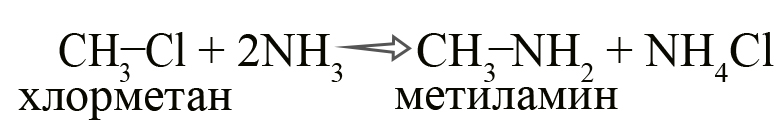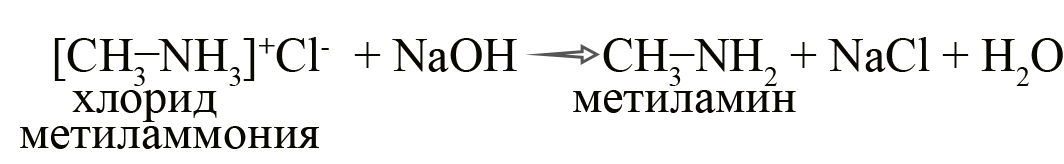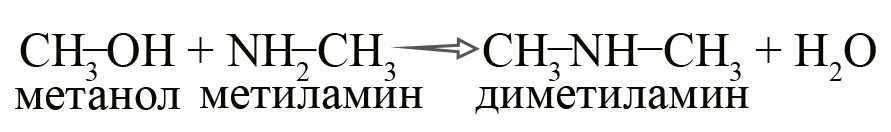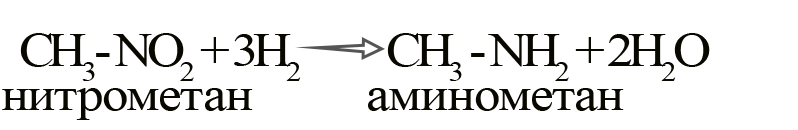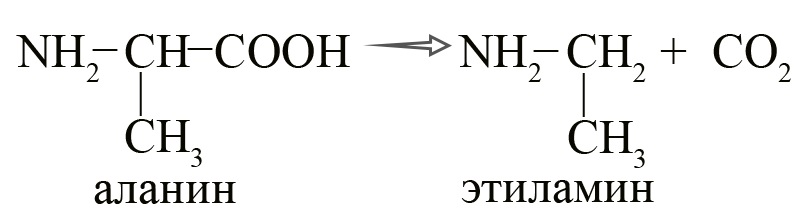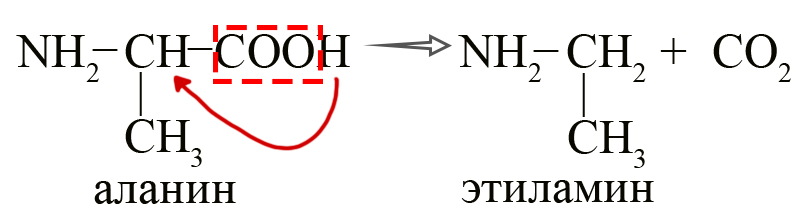Амины — органические соединения, продукты замещения атомов водорода в аммиаке NH3 различными углеводородными радикалами. Функциональная
группой аминов является аминогруппа — NH2.

Классификация аминов
По числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные.

Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций.
Таким образом,
у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены).

Номенклатура и изомерия аминов
Названия аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин,
пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке.
Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации.

Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы.

Получение
- Нагревание галогеналканов с аммиаком
- Восстановление нитросоединений
- Восстановление амидов
- Восстановление нитрилов
- Реакция аммиака со спиртами
- Реакция галогеналканов с аминами
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония.

При такой реакции нитрогруппа превращается в аминогруппу, образуется вода.

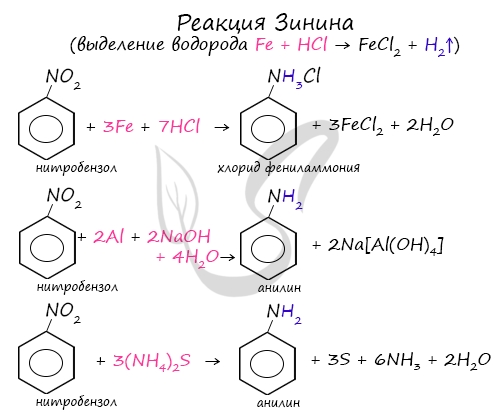
Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина
и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород.
Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды.

Этим способом в промышленности получают гексаметилендиамин, используемый в изготовлении волокна — нейлон.

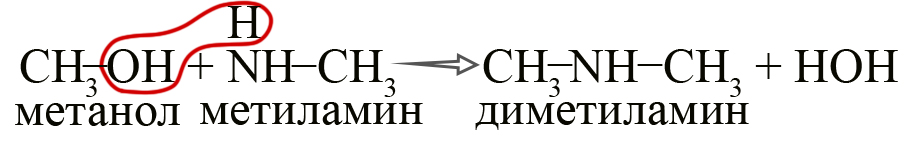
В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу.

В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов.


Химические свойства аминов
- Основные свойства
- Реакция с азотистой кислотой
- Конденсация аминов с альдегидами и кетонами
- Разложение солей аминов
- Горение аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет.
В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием.

Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония.

Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют.

При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C».

Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода.

При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая
температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ.
4C2H5NH2 + 15O2 → 8CO2 + 14H2O + 2N2
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Амины – это органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы.
R-NH2, R1-NH-R2, R1-N(R2)-R3
Строение аминов
Атом азота находится в состоянии sp3-гибридизации, поэтому молекула имеет форму тетраэдра.
Также атом азота в аминах имеет неподелённую электронную пару, поэтому амины проявляют свойства органических оснований.
Классификация аминов
По количеству углеводородных радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины.
По типу радикалов амины делят на алифатические, ароматические и смешанные.
| Амины | Первичные | Вторичные | Третичные |
| Алифатические | Метиламин
CH3-NH2 |
Диметиламин
CH3-NH-CH3 |
Триметиламин
(CH3)3N |
| Ароматические | Фениламин
C6H5-NH2 |
Дифениламин
(C6H5)2NH |
Трифениламин
(C6H5)3N |
| Смешанные | Метилфениламин
CH3-NH-C6H5 |
Диметилфениламин
(CH3)2N-C6H5 |
Номенклатура аминов
- Названия аминов образуют из названий углеводородных радикалов и суффикса амин. Различные радикалы перечисляются в алфавитном порядке.
При наличии одинаковых радикалов используют приставки ди и три.
CH3-NH2 Метиламин
СH3CH2-NH2 Этиламин
CH3-CH2-NH-CH3 Метилэтиламин
(CH3)2NH Диметиламин
- Первичные амины могут быть названы как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -NH2.
В этом случае аминогруппа указывается в названии приставкой амино-:
| 1-Аминопропан | 1,3-Диаминобутан |
| CH3-CH2-CH2-NH2 | NH2-CH2-CH2-CH(NH2) -CH3 |
- Для смешанных аминов, содержащих алкильные и ароматические радикалы, за основу названия обычно берется название первого представителя ароматических аминов – анилин.
Например, N-метиланилин:
Символ N- ставится перед названием алкильного радикала, чтобы показать, что этот радикал связан с атомом азота, а не является заместителем в бензольном кольце.
Изомерия аминов
Для аминов характерна изомерия углеродного скелета, изомерия положения аминогруппы и изомерия различных типов аминов.
Изомерия углеродного скелета
Для аминов характерна изомерия углеродного скелета (начиная с С4H9NH2).
Например. Формуле С4Н9NH2 соответствуют два амина-изомера углеродного скелета.
Изомерия положения аминогруппы
Для аминов характерна изомерия положения аминогруппы (начиная с С3H9N).
Например.Формуле С4Н11N соответствуют амины положения аминогруппы.
| 1-Аминобутан (н-бутиламин) |
2-Аминобутан (втор-бутиламин) |
 |
Изомерия между типами аминов
Например. Формуле С3Н9N соответствуют первичный, вторичный и третичный амины.
| Пропиламин
(первичный амин) |
Метилэтиламин (вторичный амин) | Триметиламин
(третичный амин) |
 |
 |
 |
Физические свойства аминов
При обычной температуре низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха.
Ароматические амины – бесцветные жидкости с высокой температурой кипения или твердые вещества.
Первичные и вторичные амины образуют слабые межмолекулярные водородные связи:
Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой.
Амины также способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо растворимы в воде.
С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Ароматические амины в воде не растворяются.
Химические свойства аминов
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов:
|
Аммиак :NH3 |
Первичный амин R–:NH2 |
 |
 |
Поэтому амины и аммиак обладают свойствами оснований.
1. Основные свойства аминов
Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми.
Это объясняется тем, что радикалы СН3–, С2Н5– увеличивают электронную плотность на атоме азота:
Это приводит к усилению основных свойств.
Основные свойства аминов возрастают в ряду:
1.1. Взаимодействие с водой
В водном растворе амины обратимо реагируют с водой. Среда водного раствора аминов — слабощелочная:
1.2. Взаимодействие с кислотами
Амины реагируют с кислотами, как минеральными, так и карбоновыми, и аминокислотами, образуя соли (или амиды в случае карбоновых кислот):
При взаимодействии аминов с многоосновными кислотами возможно образование кислых солей:
1.3. Взаимодействие с солями
Амины способны осаждать гидроксиды тяжелых металлов из водных растворов.
Например, при взаимодействии с хлоридом железа (II) образуется осадок гидроксида железа (II):
2. Окисление аминов
Амины сгорают в кислороде, образуя азот, углекислый газ и воду. Например, уравнение сгорания этиламина:
3. Взаимодействие с азотистой кислотой
Первичные алифатические амины при действии азотистой кислоты превращаются в спирты:
Это качественная реакция на первичные амины – выделение азота.
Вторичные амины (алифатические и ароматические) образуют нитрозосоединения — вещества желтого цвета:
4. Алкилирование аминов
Первичные амины способны взаимодействовать с галогеналканами с образованием соли вторичного амина:
Из полученной соли щелочью выделяют вторичный амин, который можно далее алкилировать до третичного амина.
Особенности анилина
Анилин С6H5-NH2 – это ароматический амин.
Анилин – бесцветная маслянистая жидкость с характерным запахом. На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. В воде практически не растворяется.
При 18 оС в 100 мл воды растворяется 3,6г анилина. Раствор анилина не изменяет окраску индикаторов.
Видеоопыт изучения среды раствора анилина можно посмотреть здесь.
Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу.
- Бензольное кольцо уменьшает основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком:
Анилин не реагирует с водой, но реагирует с сильными кислотами, образуя соли:
- Бензольное кольцо в анилине становится более активным в реакциях замещения, чем у бензола.
Реакция с галогенами идёт без катализатора во все три орто- и пара- положения.
Качественная реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок ↓).
Видеоопыт бромирования анилина можно посмотреть здесь.
Получение аминов
Восстановление нитросоединений
Первичные амины можно получить восстановлением нитросоединений.
- Гидрирование водородом:
- Восстановление сульфидом аммония:
- Алюминий в щелочной среде.
Алюминий реагирует с щелочами с образованием гидроксокомплексов.
В щелочной и нейтральной среде получаются амины.
Восстановлением нитробензола получают анилин.
- Металлами в кислой среде – железом, оловом или цинком в соляной кислоте.
При этом образуются не сами амины, а соли аминов:
Амины из раствора соли выделяют с помощью щелочи:
Алкилирование аммиака и аминов
При взаимодействии аммиака с галогеналканами происходит образование соли первичного амина, из которой действием щелочи можно выделить сам первичный амин.
Если проводить реакцию с избытком аммиака, то сразу получится амин, а галогеноводород образует соль с аммиаком:
Гидрирование нитрилов
Таким образом получают первичные амины. Возможно восстановление нитрилов водородом на катализаторе:
.
Соли аминов
- Соли аминов — это твердые вещества без запаха, хорошо растворимые в воде, но не растворимые в органических растворителях (в отличие от аминов).
- При действии щелочей на соли аминов выделяются свободные амины:
Видеоопыт взаимодействия хлорида диметиламмония с щелочью с образованием диметиламина можно посмотреть здесь.
- Соли аминов вступают в обменные реакции в растворе:
- Взаимодействие с аминами.
Соль амина с более слабыми основными свойствами может реагировать с другим амином, образуя новую соль (более сильные амины вытесняют менее сильные из солей):
План урока:
Строение аминов
Классификация аминов
Номенклатура аминов
Изомерия аминов
Способы получения аминов
Физические свойства аминов
Химические свойства аминов
Особенности анилина
Особенности аминокислот
Применение аминов
Вредное воздействие аминов
Серотонин улучшает аппетит, повышает настроение и контролирует эмоции человека. Адреналин стимулирует центральную нервную систему. Все эти соединения – амины. Без них невозможно представить жизнь человека.
Амины – углеводородные производные аммиака, в которых вместо водородных атомов располагаются радикалы. Функциональная группа аминов: аминогруппа (-NH2).
Строение аминов
Аммиак и амины схожи по многим параметрам. Для азота в этих соединениях свойственна sp3-гибридизация.
Строение аминов определяет свойства. Для представителей этого класса соединений свойственна основность. Это связано с расположением неподеленной электронной пары на азоте.
Классификация аминов
Группировка по количеству радикалов
Основные свойства соотносятся с количеством электронной плотности на азоте. Чем плотность выше, тем основность выше. Но у третичных аминов обилие радикалов создает пространственные затруднения, поэтому их основные свойства ослаблены.
Группировка по строению органического радикала
Номенклатура аминов
Согласно международной номенклатуре название представителей этого класса соединений формируется из радикала и суффикса«-амин». Если в соединении несколько радикалов, то они располагаются в названии согласно алфавиту.
Амины также можно назвать как производные аммиака. Для этого к радикалу прибавляется приставка «амино-».
Например, молекула CH3-CH2-СН2-CH2-CH2-CH2-NH2называется 1-аминогексан (гексамин).
Изомерия аминов
Для аминов свойственно несколько видов изомерии.
Способы получения аминов
Существует несколько методов получения аминов.
Реакции нитросоединений
С помощью восстановления нитросоединений синтезируются амины.
- Гидрирование (взаимодействие с молекулами водорода) при нагревании
СН3-СН2-СН2-СН2-NO2 + 3H2 →СН3-СН2-СН2-СН2-NH2 + 2 H2O
- Реакция с сульфидом аммония
СН3-СН2-NO2 +3 (NH4)2S → СН3-СН2-NH2 + 3 S + 6 NH3 + 2 H2O
- Взаимодействие с алюминием в щелочи
СН3-СН2-NO2 +2 Al + 2 KOH + 4 H2O → СН3-СН2-NH2 +2 K[Al(OH)4]
- Реакции с металлами (железом, оловом, цинком) и кислотой
СН3-СН2-NO2 + 3 Fe + 7 HCl → [СН3-СН2-NH3]Cl + 2 H2O + 3 FeCl3
В результате образуется соль. При ее взаимодействии с щелочью образуется амин.
[СН3-СН2-NH3]Cl + KOH → СН3-СН2-NH2 + H2O + KCl
Алкилирование (взаимодействие с галогеналканами) аммиака
При недостатке аммиака образуется соль. При ее взаимодействии с щелочью получается амин.
СН3-СН2-СН2-СН2-Br + NH3 → [СН3-СН2-СН2-СН2-NH3]Br
[СН3-СН2-СН2-NH3]Br + KOH → СН3-СН2-СН2 -NH2 + H2O + KBr
При избытке аммиака амин образуется сразу.
R-Br + 2 NH3 → R-NH2 + NH4Br
Гидрирование нитрилов
Данная реакция протекает при наличии никеля.
Физические свойства аминов
Первые представители всех типов аминов существуют в виде газов с аммиачным ароматом, средние представители гомологического ряда– жидкостей с запахом рыбы, а высшие существуют в твердом агрегатном состоянии. Ароматические амины – это прозрачные жидкости с большими температурами кипения или твердые соединения.
Первичным и вторичным аминам свойственны высокие температуры плавления и кипения. Это связано с тем, что амины формируют свободные связи между молекулами.
Растворимость аминов обусловлена тем, что они создают связи с молекулами воды. Чем выше молекулярная масса соединения, тем ниже растворимость. Молекулы ароматических аминов не растворяются в воде.
Химические свойства аминов
Основные свойства
Из-за неподеленной электронной пары на азоте амины выражают основные свойства. Основность возрастает в следующем ряду:
Ароматические амины>аммиак>алифатические амины
По мере увеличения электронной плотности на азоте основность увеличивается.
- Гидратация (взаимодействие с водой)
- Взаимодействие с кислотами
Амины взаимодействуют с органическими, минеральными кислотами, аминокислотами. В результате образуются соли.
СН3-СН2-СН2—СН2-NH2 + HCl → [СН3-СН2-СН2-СН2-NH3]+Cl—
- Взаимодействие с солями
2СН3-СН2-СН2-СН2-NH2 + FeCl2 + 2 H2O → 2 [СН3-СН2-СН2-СН2-NH3]+Cl— + Fe(OH)3
Окисление
Амины при взаимодействии с кислородом (горении) образуют свободный азот.
4 CH3-CH2-NH2 + 15 O2→ 8 CO2 + 2 N2 + 14 H2O
Реакция с азотистой кислотой
Из первичных спиртов синтезируются спирты.
R-NH2 + NaNO2 + HCl → R-OH + N2 + NaCl + H2O
Из вторичных спиртов синтезируются нитрозосоединения (вещества желтого цвета).
Алкилирование аминов
В результате реакции первичных аминов и галогеналканов синтезируются соли вторичных аминов, а из вторичных – соли третичных аминов.
Анилин
Анилин – прозрачная жидкость с особенным запахом. При взаимодействии с кислородом (окислении) анилин становится красно-бурым. Анилин токсичен и не растворим в воде.
Реакции могут идти как по боковой цепи, так и по ароматическому кольцу.
Основные свойства анилина
У ароматических аминов самые низкие основные свойства. Они также не реагируют с водой, но взаимодействуют с кислотами.
Для анилина характерны реакции замещения. В эти реакции он вступает легче, чем бензол. Реакция идет без катализаторов. Бром замещается в орто- и параположениях. В результате образуется белый осадок.
Аминокислоты
Аминокислоты – элементарная структура белков, из которых состоят все тела животных. Аминокислоты включают две функциональные группы – аминогруппу (-NH2) и карбоксильную группу (-СООН). Эти две группы не соединены между собой непосредственно.
Общая формула аминокислот
Для аминокислот характерна оптическая изомерия. Белки включают только α-аминокислоты. На нашей планете существует только 20 аминокислот, из которых строится все живое.
Аминокислоты – амфотерные соединения, которые могут реагировать как по карбоксильной группе, так и по аминогруппе.
Аминокислоты. Источник
Применение аминов
Амины в свободном виде в природе встречаются редко. Они образуются при гниении органических остатков. В этом процессе синтезируются такие соединения как путресцин и кадаверин.
Путресцин и кадаверин
Для средних представителей гомологического ряда аминов характерен рыбный запах. Запах селедочного рассола определяется триметиламином.
Амины используются также в промышленности. Например, как:
- отвердитель эпоксидной смолы,
- ускоритель реакции в металлургической промышленности,
- исходное вещество для производства полиамидных волокон,
- вещество для синтеза анилина,
- сырье для получения фенолформальдегидных смол,
- вещество для получения пестицидов, инсекцидов, фунгицидов,
- добавка к машинным топливам и маслам и др.
Метиламин – первичный амин. Он применяется в производстве лекарственных препаратов, красителей, пестицидов.
Метиламин
Диэтиламин – вторичный амин. С его помощью получают пестициды, красители, лекарственные препараты, добавки к машинным маслам и т.д. Также он служит сырьем для изготовления веществ от коррозии металлов. Он может отвердевать эпоксидные смолы и играть роль катализатора при вулканизации.
Диэтиламин
Триэтиламин – третичный алифатический амин. Он применяется при получении резин, эпоксидных смол и пенополиуретанов. Из него также производят лекарственные препараты, минеральные удобрения, краски и т.д.
Триэтиламин
Анилин – ароматический амин. Он широко применяется в качестве сырья для получения красителей, лекарственных препаратов, взрывчаток и т.д.
Анилин
Амины образуются в растениях и животных в результате биохимического распада аминокислот под действием ферментов. Они обладают высокой биологической активности.
Амины животного происхождения – серотонин, адреналин, мелатонин, тирамин и др. Амины растительного происхождения – кофеин, кокаин, никотин, хинин и др.
Вредное воздействие аминов
Практически все амины ядовиты. Ароматический амин анилин проникает через кожу, окисляет гемоглобин, угнетает работу центральной нервной системы. Его действие может привести к гибели.
Отравление можно выявить по следующим признакам:
- трудности при дыхании,
- посинение носа, губ, кончиков пальцев,
- сильное сердцебиение,
- обмороки.
Первая помощь:
- смыть анилин спиртом,
- дать возможность дышать чистым воздухом,
- вызвать медицинских специалистов.
Алифатические амины оказывают негативное влияние на нервную систему, нарушают работу печени, развивают дистрофию. Некоторые ароматические амины — канцерогены, способные вызвать рак мочевого пузыря. Опасны даже пары аминов.
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Амины: классификация, номенклатура и способы получения
Материал по химии
- Определение и классификация
Амины – предельные органические вещества, содержащие аминогруппу, которая, в зависимости от амина может иметь следующий вид:
Амины: классификация, номенклатура и способы получения
Аминогруппа
Эту группу можно рассматривать как производные аммиака, в котором атомы водорода заместили на углеводородный радикал.
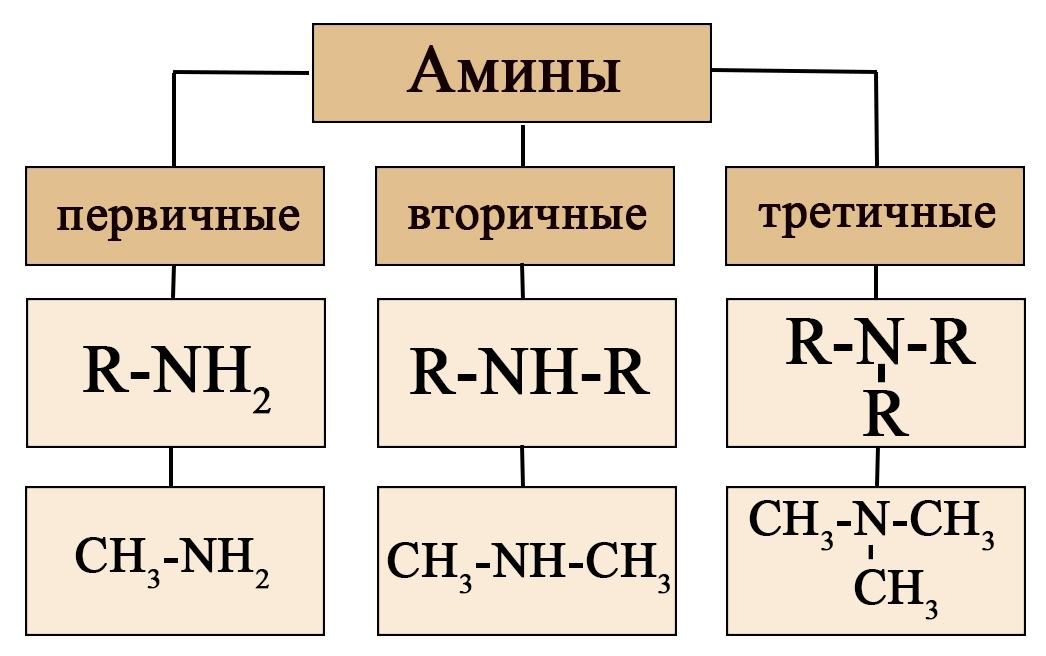
По количеству замещенных атомов водорода можно классифицировать амины на первичные (замещен только один атом водорода), например, метиламин:
Вторичные (замещены два атома водорода), например, диметиламин:
Третичные (замещены все три атома водорода), например, триметиламин:
Общая формула всех аминов CnH2n+3N, однако, если выделять аминогруппу, то общие формулы первичных, вторичных и третичных аминов будут отличаться: (I – у первичных, II – у вторичных, III – у третичных):
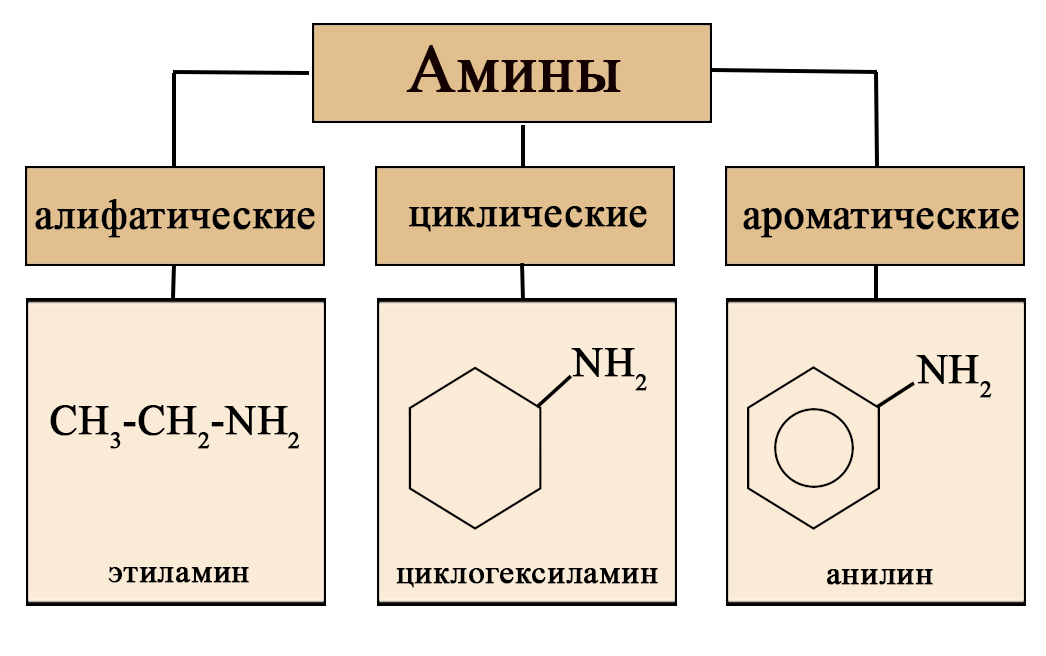
Так же амины можно классифицировать по характеру радикалов на алифатические (амины жирного ряда, содержащие в качестве радикала остаток предельного линейного углеводорода), циклические и ароматические.
- Номенклатура аминов
Номенклатура первичных аминов
- Радикало-функциональная номенклатура
При наименовании аминов чаще всего используется радикало-функциональная номенклатура органических веществ, особенно это характерно для вторичных и третичных аминов.
За основу берется аминогруппа, а всё, что с ней связано считается радикалом. Сначала дается наименование радикалу, а затем добавляется суффикс «-амин». Например, вещество с формулой CH3-CH2-CH2-NH2 можно назвать пропиламином. Представленный на рисунке изобутиламин можно назвать 2-метилпропиламином-1.
- Заместительная номенклатура
Есть и другие методы, которыми можно воспользоваться при наименовании амина, например, заместительная номенклатура. Для этого выделяется самая длинная углеводородная цепь, всё остальное, включая амино-группу, является радикалами-заместителями, которые перечисляют в алфавитном порядке с указанием их мест (номер атома углерода, которому принадлежит данный радикал). Таким образом изобутиламин можно назвать 1-амино-2-метилпропаном.
Номенклатура вторичных и третичных аминов
Для вторичных и третичных аминов характернее радикало-функциональная номенклатура, например:
- Изомерия аминов
Первичные, вторичные и третичные амины с одинаковым количеством углерода являются изомерами друг другу, например, формуле C4H11N соответствуют следующие вещества:
- Бутиламин (1-аминобутан) – первичный амин.
- Два вторичных амина – диэтиламин и метилпропиламин.
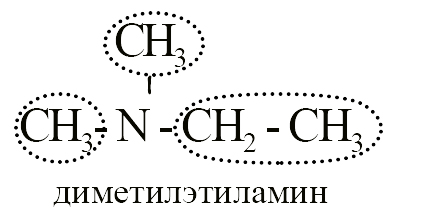
- Один третичный амин – диметилэтиламин.
- Получение аминов
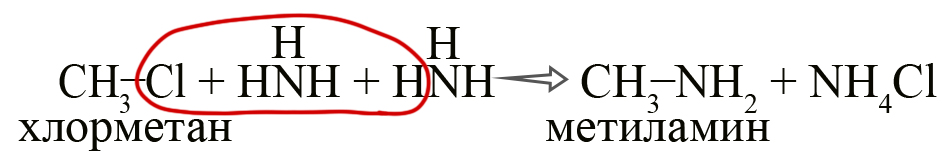
- Алкилирование аммиака галогеналканами (Реакция Гофмана). Одна из первых реакций, использованных для синтеза аминов. В настоящее время в промышленности не используется так как при этой реакции образуется не один необходимый амин, а смесь разных аминов и их солей. В лаборатории амины получают реакцией галогеналкана с избытком аммиака:
Чтобы легче запомнить данную реакцию, можно изобразить её следующим образом (не отображающим реального процесса):
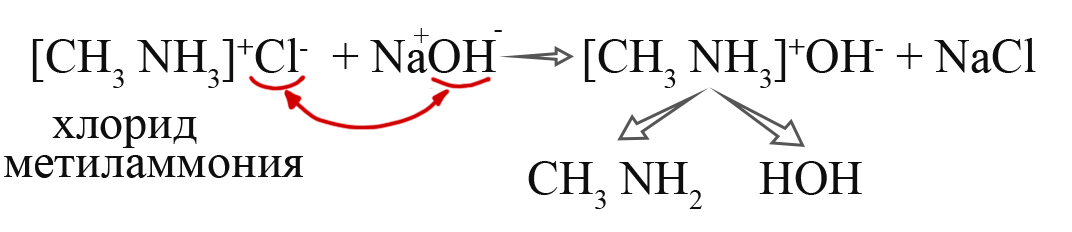
- Получение аминов из солей. При взаимодействии солей со щелочами происходит обменная реакция, при которой образуется гидроксид алкиламмония, разлагающийся как разлагается гидроксид аммония:
- Получение аминов из спиртов. Эта реакция осуществима в более жестких условиях – в присутствии Al2O3 и ThO2 при нагревании до 300ºС.
Эту же реакцию можно представить следующим образом:
- Получение аминов восстановлением нитросоединений. Нитросоединение обрабатывают водородом в присутствии катализаторов (Pt, Pd, Ni) при нагревании. Так же используют водород, полученный в момент его выделения из реакций кислоты с металлом (Fe + HCl) или щелочи с амфотерным металлом (Al + NaOH).
- Получение аминов из аминокислот путем их декарбоксилирования (потерей CO2) в присутствии ферментов.
Процесс можно представить следующим образом:
АМИНЫ
Амины – органические производные аммиака NH3, в
молекуле которого один, два или три атома водорода замещены на углеводородные
радикалы:
R-NH2,
R2NH, R3N
Простейший представитель – метиламин:
Строение
Атом азота находится в
состоянии sp3-гибридизации,
поэтому молекула имеет форму тетраэдра.
Также
атом азота имеет два неспаренных электрона, что обуславливает свойства аминов
как органических оснований.
КЛАССИФИКАЦИЯ АМИНОВ.
По количеству и типу
радикалов, связанных с атомом азота:
|
АМИНЫ |
Первичные амины |
Вторичные амины |
Третичные амины |
|
Алифатические |
CH3— |
(CH3)2NH |
(CH3)3N |
|
Ароматические |
|
(C6H5)2NH |
|
НОМЕНКЛАТУРА АМИНОВ.
1. В большинстве случаев названия аминов
образуют из названий углеводородных радикалов и суффикса амин.
Различные радикалы перечисляются в алфавитном порядке. При наличии одинаковых радикалов
используют приставки ди и три.
CH3-NH2 Метиламин СH3CH2-NH2
Этиламин
CH3-CH2-NH-CH3 Метилэтиламин
(CH3)2NH Диметиламин
2. Первичные амины часто называют как
производные углеводородов, в молекулах которых один или несколько атомов
водорода замещены на аминогруппы -NH2.
В этом случае аминогруппа
указывается в названии приставкой амино-:
CH3-CH2-CH2-NH2 1-аминопропан
H2N-CH2-CH2-CH(NH2)-CH3 1,3-диаминобутан

смешанных аминов, содержащих алкильные и ароматические радикалы, за основу
названия обычно берется название первого представителя ароматических аминов анилин.
Символ N-
ставится перед названием алкильного радикала, чтобы показать, что этот радикал
связан с атомом азота, а не является заместителем в бензольном кольце.
ИЗОМЕРИЯ АМИНОВ
1) углеродного скелета, начиная с С4H9NH2:
СН3-СН2— СН2-СН2
–NH2 н-бутиламин (1-аминобутан)
CH3—CH— СН2—NH2 изо-бутиламин (1-амин-2-метилпропан)
│
СН3
2) положения аминогруппы, начиная с С3H7NH2:
СН3-СН2— СН2-СН2
–NH2 1-аминобутан (н-бутиламин)
CH3—CH— СН2-СH3 2-аминобутан (втор-бутиламин)
│
NН2
3) изомерия
между типами аминов – первичный, вторичный, третичный:
ФИЗИЧЕСКИЕ СВОЙСТВА
АМИНОВ.
Первичные и вторичные амины образуют слабые
межмолекулярные водородные связи:

Это объясняет относительно более высокую
температуру кипения аминов по сравнению с алканами с близкой молекулярной
массой. Например:
|
Пропиламин (М=59) t кип = 49оС |
Бутан (М=58) t кип = -0,5оС |
Третичные амины не
образуют ассоциирующих водородных связей (отсутствует
группа N–H). Поэтому их температуры кипения ниже, чем у изомерных первичных и
вторичных аминов:
|
Триэтиламин t кип = 89 °С |
н-Гексиламин tкип = 133 °С |
По сравнению со спиртами алифатические амины
имеют более низкие температуры кипения, т.к. в спиртах водородная связь
более прочная:
|
Метиламин t кип = -6 °С |
Метанол t кип = +64,5 °С |
При
обычной температуре только низшие алифатические амины CH3NH2,
(CH3)2NH и (CH3)3N – газы (с
запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие
– твердые вещества без запаха.
Ароматические амины – бесцветные
высококипящие жидкости или твердые вещества.
Амины способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо
растворимы в воде.
С увеличением числа и размеров
углеводородных радикалов растворимость аминов в воде уменьшается, т.к.
увеличиваются пространственные препятствия образованию водородных связей.
Ароматические амины в воде практически не растворяются.
Анилин: С6H5-NH2 – важнейший из ароматических аминов:
Он находит широкое применение в
качестве полупродукта в производстве красителей, взрывчатых веществ и
лекарственных средств (сульфаниламидные препараты).
Анилин — бесцветная маслянистая
жидкость с характерным запахом. На воздухе окисляется и приобретает
красно-бурую окраску. Ядовит.
ПОЛУЧЕНИЕ АМИНОВ.
|
1. Первичные а) Гидрирование водородом: R—NO2 + H2 —tà R—NH2 + H2O б) Восстановление: в щелочной и нейтральной R-NO2 + 3(NH4)2S R-NO2 + 2Al + 2KOH + 4H2O à R- NH2 + 2K[Al(OH)4] Восстановлением нитробензола получают в) в кислой среде (железо, олово или цинк в Амины из раствора выделяют с помощью щелочи: [RNH3+]Cl— +КОН = H2O + КCl + R— NH2 |
|
2. Алкилирование СH3Br + NH3 à [CH3NH3]Br -(+KOH)à CH3—NH2 + C2H5Br à [CH3NH2+]Br— —(+KOH)à CH3 — NH + KBr + H2O вторичный амин Возможно дальнейшее алкилирование до третичного |
|
3.Восстановление нитрилов с R–C Этим способом в промышленности получают гексаметилендиамин, |
|
4. Взаимодействие аммиака со |
ХИМИЧЕСКИЕ
СВОЙСТВА АМИНОВ.
Амины имеют сходное с аммиаком
строение и проявляют подобные ему свойства.
Как в аммиаке, так и в аминах атом азота имеет
неподеленную пару электронов:
Поэтому амины и аммиак обладают свойствами оснований.
|
1. Основные свойства. Будучи производными аммиака, все амины Алифатические амины являются более Это СН3 Это приводит к усилению основных свойств. Фенильный В водном растворе амины обратимо |
|
2. Амины реагируют с кислотами, образуя Cоли аминов — твердые вещества без запаха, хорошо растворимые в воде, но не При действии щелочей на соли аминов [CH3NH3]Cl Соли аминов вступают в обменные реакции [CH3NH3]Cl |
|
3. Амины |
|
4. Горение. 4 С2Н5NH2 + 15O2 à 8CO2 + 2N2 + 14 H2O |
|
5. Реакции с а) Первичные алифатические амины при действии азотистой кислоты превращаются в спирты: R—NH2 + NaNO2 + HCl à R—OH +N2 + NaCl + H2O б) Вторичные амины (алифатические и ароматические) |
Особенности
свойств анилина:
Для анилина
характерны реакции как по аминогруппе, так и по бензольному кольцу.
Особенности этих реакций обусловлены взаимным
влиянием атомов.
— бензольное кольцо ослабляет
основные свойства аминогруппы по сравнению алифатическими аминами и
даже с аммиаком.
— бензольное кольцо становится более
активным в реакциях замещения, чем бензол.
Аминогруппа — заместитель 1-го рода
(активирующий орто-пара-ориентант в реакциях электрофильного замещения
в ароматическом ядре).
Качественная
реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина
(белый осадок ↓).
Способы получения аминов (часть 2)
Чтобы получить доступ к бесплатным материалам, пожалуйста зарегистрируйтесь.
Извините, у Вас нет прав просматривать контент!
Регистрация
Войти