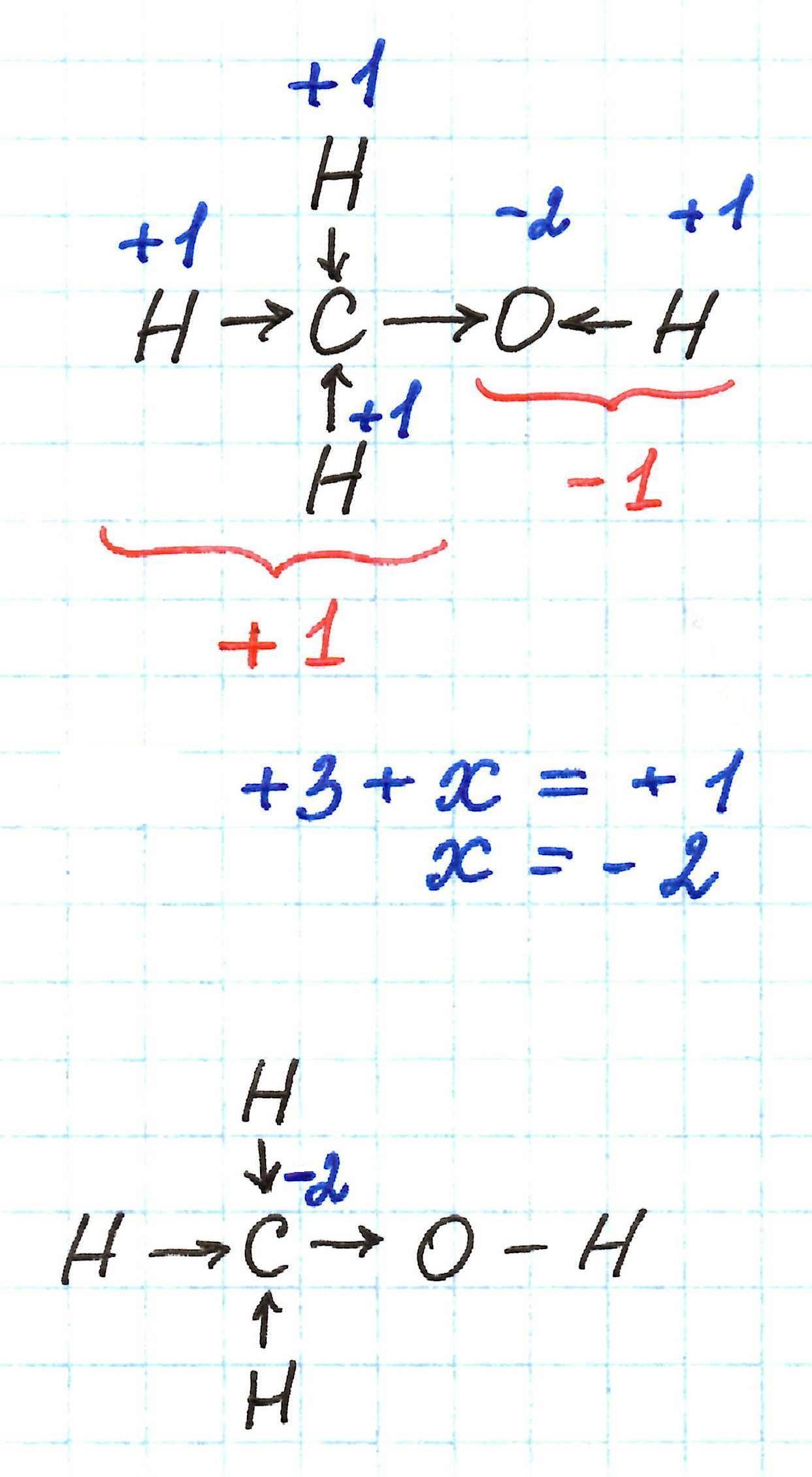Как расставлять степени окисления в органических соединениях?.
Степени окисления в органических соединениях требуется уметь расставлять для решения заданий ЕГЭ по химии, в которых дается цепочка превращений органических веществ, часть из которых неизвестна. На данный момент это задания номер 32.
Для определения степени окисления в органических соединениях существует два метода. Суть их одинакова, но выглядят применение данных методов по-разному.
Первый способ я бы назвал методом блоков.
Метод блоков
Берем органическую молекулу, например, такого вещества, как 2-гидроксипропаналь
и изолируем друг от друга все фрагменты молекулы, содержащие по одному атому углерода следующим образом:
Суммарный заряд каждого такого блока принимаем равным нулю, как у отдельной молекулы. В органических соединениях водород всегда имеет степень окисления, равную +1, а кислород — -2. Обозначим степень окисления атома углерода в первом блоке переменной х. Таким образом, мы можем найти степень окисления первого атома углерода, решив уравнение:
x + 3∙(+1) = 0, где x – степень окисления атома углерода, +1 – степень окисления атома водорода, а 0 – заряд выбранного блока.
Решаем далее:
x + 3 = 0, отсюда x = -3.
Таким образом, степень окисления атома углерода в первом блоке равна -3.
Во второй блок, помимо одного атома углерода и двух атомов водорода, входит также и атом кислорода, который, как мы уже сказали, имеет в органических соединениях практически всегда степень окисления, равную -2. Как и в первом случае, обозначим степень окисления атома углерода второго блока через х, тогда получим следующее уравнение:
x+2∙(+1)+(-2) = 0, решая которое находим, что х = 0. Т.е. степень окисления второго атома углерода в молекуле равна нулю.
Третий блок состоит из одного атома углерода, одного атома водорода и одного атома кислорода. Аналогично составим уравнение:
x +1∙(-2)+ 1 = 0, отсюда х, то есть степень окисления атома углерода в третьем блоке равна +1.
Второй метод расстановки степеней окисления в органических веществах я называю «метод стрелок».
Метод стрелок
Для того, чтобы его использовать, нужно нарисовать сначала развернутую структурную формулу органического вещества:
Под черточками между символами элементов понимают их общие электронные пары, которые между одинаковыми атомами можно считать распределенными поровну, а между разными – смещенными к одному из атомов, обладающему большей электроотрицательностью. Среди трех элементов С, Н и О наибольшую элетроотрицательность имеет кислород, затем углерод, а самое малое значение электроотрицательности у водорода. Поэтому, если показать стрелочкой смешение электронов в сторону более электроотрицательных атомов, мы получим следующую картинку:
Как можно заметить, между атомами углерода мы не стали рисовать стрелку, оставив обычную черточку, поскольку считается, что общая электронная пара между двумя атомами углерода практически не смещена ни к одному из них.
Будет интерпретировать последний рисунок следующим образом: каждый атом, из которого стрелка исходит, «теряет» один электрон, а каждый атом, в который стрелка входит, «принимает» электрон. При этом помним, что заряд электрона отрицателен и равен -1.
Таким образом, первому атому углерода достается от трех атомов водорода по одному электрону (три входящих стрелки), в результате чего он приобретает условный заряд, т.е. степень окисления, равную -3, а каждый атома водорода — +1 (по одной исходящей стрелке).
Второму атому углерода достается от «верхнего» атома водорода один электрон (стрелка от H к С), и еще один электрон атом углерода «теряет», передавая его атому кислорода (стрелка от С к О). Таким образом, в атом углерода «входит» один электрон и один из него «выходит». Поэтому степень окисления второго атома углерода равна 0, как в отдельном атоме.
К атому кислорода направлены две стрелки, значит, он имеет степень окисления, равную -2, а от всех атомов водорода исходит по одной стрелке. То есть степень окисления всех атомов водорода равна +1.
В последний атом углерода входит одна стрелка от Н и исходит две стрелки к О, таким образом, «входит» один электрон и «выходят» два. Значит, степень окисления равна +1.
Нужно отметить, что на самом деле оба описанных метода весьма условны, как, собственно, и условно само понятие «степень окисления» в случае органических веществ. Тем не менее, в рамках школьной программы данные методы вполне справедливы и, главное, позволяют использовать их при расстановке коэффициентов в реакциях ОВР с органическими веществами. Лично мне нравится больше метод «стрелок». Советую усвоить оба метода: одним из них вы можете определять степени окисления, а вторым — убедиться в правильности полученных значений.
Возможные степени окисления элементов
Перед тем как начать писать окислительно-восстановительные реакции, необходимо знать какие степени окисления может проявлять тот или иной химический элемент. Рассмотрим степени окисления, знание которых необходимо для успешной сдачи ЕГЭ.
Элементы с постоянными степенями окисления в сложных соединениях:
| Степень окисления | Элементы | Примеры соединений | Названия соединений |
|---|---|---|---|
| -1 | F | NaF OF2 |
Фторид натрия Фторид кислорода |
| +1 | Все металлы 1-ой группы главной подгруппы (Li-Fr) | Na2O KH |
Оксид натрия Гирид калия |
| +2 | Все металлы 2-ой группы главной подгруппы (Be-Ra), а также Zn и Cd | BeO CaH2 |
Оксид бериллия Гидрид кальция |
| +3 | Al | Al2O3 Al(OH)3 Al2(SO4)3 |
Оксид алюминия Гидроксид алюминия Сульфат алюминия |
Элементы с переменными степенями окисления:
1. Водород
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | H2 | Водород (простое вещество) | В твердом состоянии, как и все газы, образует молекулярную кристаллическую решетку |
| +1 | H2O H2O2 H2SO4 KOH NaHSO3 |
Вода Пероксид водорода Серная кислота Гидроксид калия Гидросульфит натрия |
В таких соединениях, как вода, пероксид водорода, все кислоты, основания, кислые соли, все органические соединения |
| -1 | NaH CaH2 |
Гидрид натрия Гидрид кальция |
Только с металлами водород может проявлять степень окисления -1 |
2. Кислород
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | O2 | Кислород (простое вещество) | В твердом состоянии, как и все газы, образует молекулярную кристаллическую решетку |
| -2 | H2O Na2O H2SO4 KOH NaHSO3 |
Вода Оксид натрия Серная кислота Гидроксид калия Гидросульфит натрия |
В таких соединениях, как вода, все оксиды, кислоты, основания, кислые соли, все органические соединения |
| -1 | H2O2 Na2O2 BaO2 |
Пероксид водорода Пероксид натрия Пероксид бария |
В пероксиде водорода и всех других пероксидах |
| -1/2 | KO2 | Супероксид калия (надпероксид калия) |
Во всех супероксидах |
| -1/3 | KO3 Sr(O3)2 |
Озонид калия Озонид стронция |
Во всех озонидах |
| +1 | O2F2 | Дифторид кислорода |
Положительные степени окисления кислород проявляет только в соединениях с фтором |
| +2 | OF2 | Фторид кислорода |
3. Сера
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | S8 | Сера | Светло-желтый порошок; нерастворим в воде, тяжелее её, но в воде не тонет, плавает на её поверхности, так как ею не смачивается. Молекулы S8 образуют молекулярную кристаллическую решетку. Сера существует в виде нескольких аллотропных модификаций: ромбическая, моноклинная, пластическая. |
| -2 | H2S CaS |
Сероводородная кислота Сульфид кальция |
Все сульфиды |
| -1 | FeS2 | Персульфид железа (II) (пирит, серный колчедан, железный колчедан) |
Единственное соединение со ст. ок. -1 |
| +4 | SO2 H2SO3 CaSO3 |
Оксид серы (IV) Сернистая кислота Сульфит кальция |
В таких соединениях как оксид серы (IV), сернистой кислоте и всех её солях |
| +6 | SO3 H2SO4 CaSO4 |
Оксид серы (VI) Серная кислота Сульфат кальция |
В таких соединениях как оксид серы (VI), серной кислоте и всех её солях |
4. Азот
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | N2 | Азот (простое вещество) | В твердом состоянии, как и все газы, образует молекулярную кристаллическую решетку |
| -3 | NH3 Na3N Ca3N2 |
Аммиак Нитрид натрия Нитрид кальция |
В таких соединениях, как аммиак и все нитриды |
| -2 | N2H4 | Гидразин | Степени окисления -2 и -1 встречаются только в органических соединениях |
| -1 | NH2OH | Гидроксиламин | |
| +1 | N2O | Оксид азота (I) | Азот проявляет положительные степени окисления только в соединениях с кислородом и фтором |
| +2 | NO | Оксид азота (II) | |
| +3 | N2O3 HNO2 NF3 |
Оксид азота (III) Азотистая кислота Фторид азота (III) |
В таких соединениях, как оксид азота (III), азотистой кислоте и всех её солях, фториде азота (III) |
| +4 | NO2 | Оксид азота (IV) | Смешанный оксид азота (IV) |
| +5 | N2O5 HNO3 |
Оксид азота (V) Азотная кислота |
В таких соединениях, как оксид азота (V), азотной кислоте и всех её солях |
5. Галогены*
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | F2 Cl2 Br2 I2 |
Фтор Хлор Бром Йод |
Светло-зеленый газ Желто-зеленый газ Темно-красная жидкость Серо-черные кристаллы |
| -1 | HF HCl HBr HI |
Фтороводород (соли кислоты: фториды) Хлороводород (соли кислоты: хлориды) Бромоводород (соли кислоты: бромиды) Йодоводород (соли кислоты: йодиды) |
Бесцветные ядовитые газы. При растворении в воде образуют соответствующие кислоты. |
| +1 | HClO HBrO HIO |
Хлорноватистая кислота (соли: гипохлориты) Бромноватистая кислота (соли: гипобромиты) Йодноватистая кислота (соли: гипоиодиты) |
В приведенных кислотах, а также всех их солях |
| +3 | HClO2 HBrO2 HIO2 |
Хлористая кислота (соли: хлориты) Бромистая кислота (соли: бромиты) Йодистая кислота (соли: иодиты) |
В приведенных кислотах, а также всех их солях |
| +5 | HClO3 HBrO3 HIO3 |
Хлорноватая кислота (соли: хлораты) Бромноватая кислота (соли: броматы) Йодноватая кислота (соли: иодаты) |
В приведенных кислотах, а также всех их солях |
| +7 | HClO4 HBrO4 HIO4 |
Хлорная кислота (соли: перхлораты) Бромная кислота (соли: перброматы) Йодная кислота (соли: периодаты) |
В приведенных кислотах, а также всех их солях |
* Для фтора только 0 и -1; At также является галогеном, но его не рассматриваем, так как в природе его практически нет.
6. Углерод**
| Степень окисления | Примеры соединений | Названия соединений | Комментарий |
|---|---|---|---|
| 0 | C | Углерод | Аллотропные модификации: алмаз, графит, карбин (черный порошок, полимерные цепи -C=C-, =С=С=), фуллерены (темные, похожие на сажу, C60-C200) |
| +2 | CO | Оксид углерода (II) (угарный газ) |
В таких соединениях как CO, а также в некоторых органических соединениях |
| +4 | CO2
H2CO3 |
Оксид углерода (IV) (углекислый газ) Угольная кислота |
В таких соединениях как оксид углерода (IV), угольная кислота и все ее соли |
** В органических соединениях углерод проявляет все степени окисления от -4 (например, CH4) до +3 (например, CH3COOH).
7. Фосфор
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | P | Фосфор | Неметалл | В природе в свободном состоянии не встречается. Наиболее устойчивые аллотропные модификации: белый фосфор (P4, молекулярная кристаллическая решетка), красный и черный фосфор (атомные кристаллические решетки) |
| -3 | PH3 | Фосфин | Летучее водородное соединение | Бесцветный ядовитый газ с запахом чеснока |
| +1 | H3PO2 NaH2PO2 |
Фосфорноватистая кислота Гипофосфит натрия |
Кислота Средняя соль |
Только в кислоте и ее солях |
| +3 | P2O3 H3PO3 Na2HPO3 |
Оксид фосфора (III) Фосфористая кислота Фосфит натрия |
Кислотный оксид Кислота Средняя соль |
В таких соединениях, как оксид фосфора (III), фосфористая кислота и все её соли |
| +5 | P2O5 H3PO4 Na3PO4 |
Оксид фосфора (V) (Орто)фосфорная кислота Фосфат натрия |
Кислотный оксид Кислота Средняя соль |
В таких соединениях, как оксид фосфора (V), фосфорная кислота и все её соли |
8. Хром
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | Cr | Хром | Металл | Голубовато-белый металл. В обычных условиях покрыт оксидной пленкой и поэтому инертен по отношению к кислороду воздуха и воде. |
| +2 | CrO Cr(OH)2 |
Оксид хрома (II) Гидроксид хрома (II) |
Основный оксид Нерастворимое основание |
Нестабильная степень окисления, сильные восстановители |
| +3 | Cr2O3 Cr(OH)3 H3CrO3 HCrO2 NaCrO2 |
Оксид хрома (III) Гидроксид хрома (III) Хромистая кислота (соли: хромиты) Метахромистая кислота (соли: (мета)хромиты) Метахромит натрия Гексагидроксохромат (III) натрия |
Амфотерный оксид Амфотерный гидроксид Кислота Кислота Средняя соль |
Степень окисления стабильная, проявляется в оксиде, гидроксиде, хромитах и гидроксокомплексах с хромом |
| +6 | CrO3 H2CrO4 H2Cr2O7 |
Оксид хрома (VI) Хромовая кислота (соли: хроматы, желтые) Дихромовая кислота (соли: дихроматы, оранжевые) |
Кислотный оксид Кислота Кислота |
Степень окисления стабильная (соединения являются сильными окислителями) проявляется в оксиде, кислотах (хромовой, дихромовой) и их солях |
9. Железо
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | Fe | Железо | Металл | Серебристо-белый, блестящий металл |
| +2 | FeO Fe(OH)2 |
Оксид железа (II) Гидроксид железа (II) |
Основный оксид Нерастворимое основание |
Оксид черного цвета Гидроксид серо-зеленого цвета |
| +3 | Fe2O3 Fe(OH)3 HFeO2 KFeO2 K3[Fe(OH)6] |
Оксид железа (III) Гидроксид железа (III) Железистая кислота Феррит калия Гексагидроксоферрат (III) калия |
Амфотерный оксид Амфотерный гидроксид Кислота Средняя соль Гидроксокомплекс |
Оксид и гидроксид бурого цвета (цвет ржавчины) |
| +6 | K2FeO4 | Феррат калия | Средняя соль | Кислота H2FeO4 как индивидуальное вещество не выделена |
10. Медь
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | Cu | Медь | Металл | Розово-красный, пластичный металл |
| +1 | Cu2O CuOH |
Оксид меди (I) Гидроксид меди (I) |
Основный оксид |
Кирпично-красного цвета |
| +2 | CuO Cu(OH)2 |
Оксид меди (II) Гидроксид меди (II) |
Основный оксид Нерастворимое основание |
Оксид черного цвета Гидроксид голубого цвета |
11. Марганец
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | Mn | Марганец | Металл | Металл серебристо-белого цвета |
| +2 | MnO Mn(OH)2 |
Оксид марганца (II) Гидроксид марганца (II) |
Основный оксид Нерастворимое основание |
Оксид зеленого цвета Основание светло-розового цвета |
| +3 | Mn2O3 | Оксид марганца (III) | Амфотерный оксид | Коричнево-чёрные кристаллы, не растворимые в воде |
| +4 | MnO2 | Оксид марганца (IV) | Амфотерный оксид | Порошок тёмно-коричневого цвета, нерастворимый в воде |
| +6 | MnO3 K2MnO4 |
Оксид марганца (VI) Манганат калия |
Кислотный оксид Средняя соль |
Оксид тёмно-красного цвета Соль темно-зеленого цвета |
| +7 | Mn2O7 HMnO4 KMnO4 |
Оксид марганца (VII) Марганцовая кислота Перманганат калия |
Кислотный оксид Кислота Средняя соль |
Красная маслянистая жидкость Кислота и соль фиолетово-красного цвета |
12. Кремний
| Степень окисления | Примеры соединений | Названия соединений | Тип соединения | Комментарий |
|---|---|---|---|---|
| 0 | Si | Кремний | Неметалл | Две аллотропные модификации: кристаллический (серый) и аморфный (белый порошок) |
| -4 | Mg2Si | Силицид магния | Бинарное соединение | Темно-синие кристаллы (Mg2Si). Ст. окисления -4 в соединениях кремния с металлами |
| +2 | SiO | Оксид кремния (II) | Несолеобразующий оксид | Смолоподобное аморфное вещество |
| +4 |
SiO2 SiC |
Оксид кремния (IV) Силан Карборунд |
Кислотный оксид Летучее водородное соединение Бинарное соединение |
Кремнезём (SiO2) Бесцветный неустойчивый газ (SiH4) Кристаллическое вещество (SiC) Степень окисления +4 в соединениях кремния с неметалами |
Как определить степень окисления в органических соединениях? Чем отличается определение степени окисления в органических соединениях от определения степени окисления в неорганических? Как составить уравнение окислительно-восстановительной реакции, в которой участвуют соединения углерода, и правильно расставить коэффициенты?
Обо всем этом в данной статье подробно и по порядку.
Содержание:
1. Что такое электроотрицательность, степень окисления и ковалентная связь
2. Как определить степень окисления в органических соединениях: примеры
3. Как расставить коэффициенты в окислительно-восстановительных реакциях с органическими веществами
Проблема, как определить степень окисления в органических соединениях, вытекает из школьного курса химии. Определенное (но не достаточное) внимание уделяется этому вопросу на примере неорганических веществ. Об органических же веществах в этой связи речь практически не идет.
Тем не менее, об окислении соединений углерода в курсе органической химии (10 класс) говорится достаточно часто. 33 задание в ЕГЭ по химии практически всегда подразумевает хотя бы одну ОВР с участием органического вещества и необходимость не только составить схему реакции, но и расставить коэффициенты.
Придя в колледж или университет, изучая курс органической химии на более серьезном уровне, студент сталкивается все с той же проблемой: как определить степень окисления в органических соединениях. Подразумевается, что бывший выпускник школы получил эти знания в школьном курсе химии, поэтому нет надобности останавливаться на данном вопросе в профессиональном образовании.
Налицо потеря взаимосвязи и преемственности разных ступеней образования: среднего основного и профессионального (СПО и ВПО).
Итак, разберемся по порядку как определить степень окисления в органических соединениях.
Что такое электроотрицательность, степень окисления и ковалентная связь
Для того чтобы правильно определить степень окисления в органическом соединении, необходимо четко и ясно усвоить три основных понятия: собственно само понятие степень окисления, электроотрицательность и ковалентная связь.
Остановимся на них кратко, так как их рассмотрение не является основной целью данной статьи.
Что такое электроотрицательность
Понятие электроотрицательности (ЭО) впервые было введено американским химиком Л.Полингом в 1932 г.
Кстати, ЭО – это еще одна относительная величина в химии. Ее правильнее называть относительной электроотрицательностью (ОЭО). Абсолютные значения ЭО очень не удобны в расчетах, поэтому их вычисляют относительно значения ЭО лития Li. Относительные величины не имеют единиц измерения.
Были получены вполне приемлемые для расчетов и анализа числа, которые сведены в удобную таблицу, в общих чертах похожую на периодическую систему химических элементов.
Способность атомов химических элементов притягивать к себе электроны других атомов в процессе образования химической связи называется электроотрицательностью.
Почему нейтральные атомы притягиваются
Раз атомы притягивают к себе электроны, то закономерно возникает следующий вопрос. Если атом, по определению, – это электронейтральная частица, то как он может вообще к себе что-то притягивать, в частности электроны – отрицательно заряженные частицы?
Вообще этот вопрос можно бы переадресовать ученым, специалистам, занимающимся проблемами квантовой механики (один из разделов современной физики).
А мы же лишь крайне упрощенно поясним, почему такое может быть.
Необходимо вспомнить, что силовые линии электрического поля положительного заряда (а им является ядро атома) всегда заканчиваются на отрицательном заряде (электроны атома).
У атомов большинства химических элементов внешний уровень не завершен. То есть в нем есть своеобразная «дырка», сквозь которую выходят силовые линии ядра. Выходят они за пределы атома и заканчиваются на электронах другого атома. В подобной ситуации, несмотря на свою общую электронейтральность, атом ведет себя как положительная частица.
Примерно так это выглядит
При всем при этом атомы полностью не «слипаются». Это не возможно, так как положительно заряженные ядра атомов будут отталкиваться. Но поскольку расстояние между ядром одного атома и электронами другого меньше расстояния между ядрами, то можно утверждать, что силы притяжения все-таки преобладают над силами отталкивания.
Для чего необходимо понятие относительной электроотрицательности
Знание и понимание понятия ОЭО дает возможность определить тип химической связи между атомами. Для этого необходимо найти разность ОЭО двух элементов, атомы которых и образуют связь.
Если разность электроотрицательностей менее 0,5, то связь считается ковалентной неполярной. При разности от 0,5 до 1,6 – связь ковалентная полярная. Если более 2,0 – ионная. А если разность в промежутке от 1,6 до 2,0, то в присутствии металла связь считается ионной, при его отсутствии – ковалентной полярной.
Что такое ковалентная связь
Почему мы говорим здесь о ковалентной связи? Потому, что большинство органических соединений – ковалентные. А это очень важно при определении с.о. углерода в них.
Если коротко, то
ковалентная связь – связь между атомами элементов, возникающая за счет обобществления электронов, т.е. образования общих электронных пар.
Если связь образована между атомами с одинаковой ОЭО, то связь будет считаться ковалентной неполярной. Это потому, что между атомами не происходит перераспределения электронной плотности. Иными словами обобществленная электронная пара не смещается к какому-либо атому.
Такая ситуация возможна, если в образовании связи участвуют атомы одного и того же химического элемента-неметалла:
Но есть и редкие исключения. Молекула фосфина PH3 характеризуется ковалентной неполярной связью, так как относительные электроотрицательности водорода и фосфора равны: ОЭО(Н)=2,1 и ОЭО(Р)=2,1.
Если же связь образована элементами-неметаллами с разной ОЭО, то она считается ковалентной полярной. Происходит перераспределение электронной плотности между атомами, т.е. общая электронная пара смещается к атому с большей ОЭО. И чем сильнее будет разность в электроотрицательностях атомов элементов, тем полярнее будет и связь.
И еще одно понятие, связанное с ковалентностью, – это валентность, означающая количество общих электронных пар (или иными словами, количество связей между атомами).
Что такое степень окисления и какие значения она может принимать
Степень окисления (с.о.) – важнейшее понятие в теории окислительно-восстановительных процессов. И это условная величина.
Известно, что при образовании ковалентной связи электроны общей электронной пары смещаются к атому более электроотрицательного элемента. Но лишь смещаются, а не полностью переходят к нему!
В итоге на более электроотрицательном атоме возникнет частичный (точнее дробный) отрицательный заряд (δ-), например, -0,73, -2/3 и т.п. А на менее электроотрицательном атоме – частичный положительный (δ+) заряд. Такими дробными числами крайне неудобно пользоваться при вычислениях и составлении формул веществ.
Классифицировать с.о. можно по разным признакам. Один из них – это постоянство для одного и того же химического элемента.
Согласно данному признаку, существуют элементы, проявляющие во всех без исключения сложных веществах одну и ту же (постоянную) степень окисления. Например:

А вот теперь самое интересное! Мы прекрасно знаем, что химический элемент углерод проявляет две степени окисления: +2 (в соединении СО) и +4 (СО2, например).
И настолько прочно это закрепляется в сознании, что мы и не предполагаем, что на самом деле у углерода может быть весь спектр степеней окисления от -4 до +4.
Более того, находясь в составе сложного органического соединения, углерод может иметь и нулевую степень окисления! Уж это совсем не вяжется с устоявшимися представлениями, выработанными на основе знаний о неорганических веществах. Для них мы знаем, что с.о. равная нулю возможна у атомов элементов в составе простых веществ (О3, P4, H2, N2 и т.д.)
Подведем некоторый итог.
В органических соединениях:
1) с.о. углерода принимает значения от -4 до +4;
2) с.о. углерода может быть равна 0;
3) валентность углерода постоянна, равна IV и не всегда совпадает по значению со степенью окисления.
Как определить степень окисления в органических соединениях: примеры
Методы, которыми мы пользуемся для определения с.о. в неорганических веществах, применимы к органическим лишь в очень редких случаях.
Напомним, что при этом мы всегда исходим из положения, что молекула вещества электронейтральна, то есть алгебраическая сумма всех зарядов (степеней окисления), как положительных, так и отрицательных, внутри нее равна нулю. Например:


Особенности определения с.о. в органических веществах
Определить степень окисления в органических веществах можно разными способами. Разберем самый простой и удобный, на наш взгляд. Именно для этого мы вспомнили, что такое относительная электроотрицательность, ковалентная связь и ее виды.
Вернемся к ранее упомянутому пропану С3Н8 и рассмотрим, какие виды ковалентной связи присутствуют в его молекуле.
Для этого:
1) запишем полную структурную формулу вещества и пронумеруем атомы углерода;
2) определим, какие связи в молекуле будут ковалентными полярными и ковалентными неполярными;
3) для ковалентных полярных связей покажем смещение общей электронной пары с помощью стрелки (так как ОЭО(С) > ОЭО(Н), то смещение происходит от Н к С);



Но даже и такой вполне удобный способ определения с.о. не всегда бывает справедлив. Все дело во влиянии атомов кислорода на распределение зарядов в молекуле.
Например, если применять указанный выше способ к определению с.о. углерода в молекуле метанола, то можно ожидать, что она буде равна -3. Однако это не так. В данной молекуле углерод имеет с.о. -2.
Молекулу метанола можно рассматривать как связанные между собой метильную –СН3 и гидроксильную –ОН группы. В таком случае суммарные заряды каждой из них в итоге должны дать ноль, так как молекула в целом электронейтральна.
Атом кислорода, как самый электроотрицательный в молекуле метанола, оттягивает к себе электронные плотности связей С-О и Н-О, принимая с.о. -2. Таким образом, суммарный заряд гидроксильной –ОН группы равен -1. Тогда суммарный заряд метильной –СН3 группы должен быть равен +1. А такое возможно только в том случае, если атом углерода имеет с.о. -2.
Ясно, что подобная ситуация будет возникать всегда в тех случаях, когда атом углерода связан с гидроксильной –ОН группой, образуя первичный спирт.
Нечто подобное происходит со степенью окисления углерода в молекуле диметилового эфира. Здесь также можно ожидать с.о. углерода -3. Но она равна -2 на обоих атомах.
Молекула диметилового эфира – это две метильные группы, связанные через атом кислорода (его с.о. -2). Каждая –СН3 должна иметь суммарный заряд +1. Это возможно в случае с.о. углерода -2.
Приведем другие примеры.
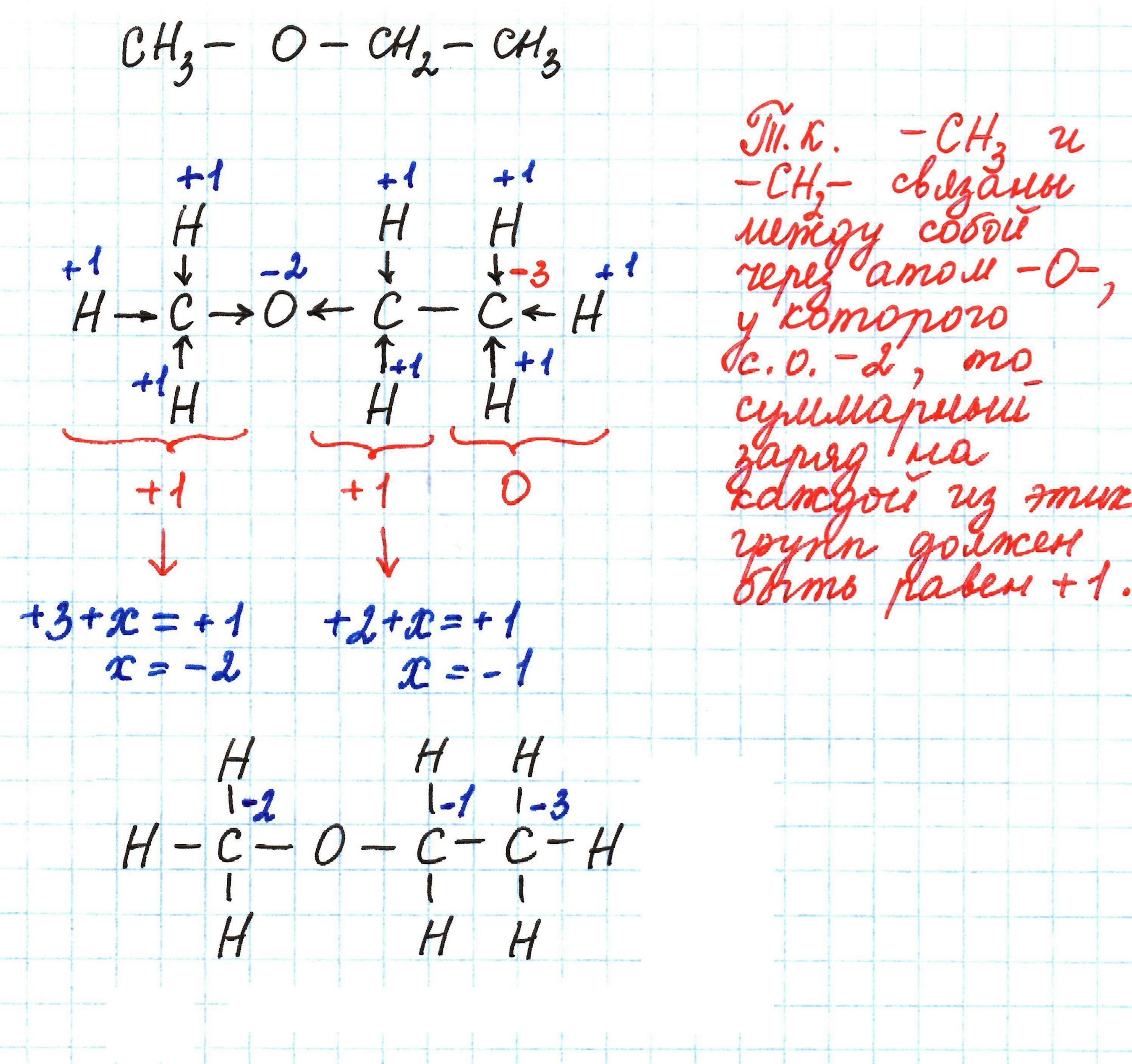
Метилэтиловый эфир – последовательно связанные друг с другом метильная группа –СН3, атом кислорода О, гомологическая разность –СН2– и еще одна метильная группа –СН3.
Таким образом, с. о. углерода в молекуле метилэтилового эфира: -2, -1, -3.
Степень окисления углерода в молекуле уксусного альдегида принимает значения -3 и +1:



Приведенные примеры позволяют сделать общие выводы о том, как определить степень окисления в органических соединениях.
1) Каждая ковалентная полярная связь, электронная плотность которой смещается К атому углерода (Н→С), добавляет в значение его с.о. -1.
2) Каждая ковалентная полярная связь, электронная плотность которой смещается ОТ атома углерода (С→О, С→N и т.д.), добавляет в его значение с.о. +1.
3) Определяя конечное значение с.о. углерода, необходимо посчитать количество смещенных ОТ него и К нему связей с учетом знака (+ или -).
! При этом не следует забывать о влиянии более электроотрицательных атомов на распределение электронной плотности (а, значит, и зарядов), что приводит в некоторых случаях к несоблюдению указанных общих выводов.
Как расставить коэффициенты в окислительно-восстановительных реакциях с органическими веществами
Существует два основных метода составления схемы ОВР и подбора коэффициентов в таких реакциях: метод электронного баланса и ионно-электронный метод (полуреакций). Каждый из них удобнее использовать в той или иной ситуации. В данной статье мы не рассматриваем суть этих методов, а останавливаемся на применении их к ОВР с участием органических веществ.
Итак, начнем с самых простых окислительно-восстановительных реакций, в которых реагентами выступают органические соединения. Для определения степени окисления углерода будем использовать выше описанный метод. В каждом конкретном примере на этом останавливаться уже не будем.
Пример 1. СН4 + О2 → СО2 + Н2О
При расстановке коэффициентов в данном случае лучше воспользоваться методом электронного баланса:
1) определим с.о. элементов;
2) составим схемы полуреакций с элементами, изменяющими свою с.о.;
3) используя данные по числу отданных и принятых электронов в полуреакциях, найдем наименьшее общее кратное и определим множители для каждой из полуреакций;
4) просуммируем полуреакции с учетом найденных множителей (коэффициентов);
5) перенесем коэффициенты в схему реакции, поставив их перед соответствующими веществами;
6) подберем коэффициенты для всех остальных химических элементов;
7) помним, что баланс количества атомов кислорода проверяем в последнюю очередь. Обычно, если число атомов кислорода слева (до стрелки) и справа (после стрелки) сходится, то это означает, что реакция составлена правильно и все остальные коэффициенты верны.
Пример 2. С3Н8 + О2 → СО2 + Н2О
В данном случае также удобнее использовать метод электронного баланса.
Расстановку коэффициентов проводим, как и в предыдущем случае. Однако есть некоторый нюанс. После определения с.о. углерода в пропане обнаруживаем, что их две: -2 и -3. Поэтому составленных схем полуреакций для углерода будет две.
Пример 3. Н2C2O4 + KMnO4 → СО2 + K2CO3 + MnO2 + Н2О
Для расстановки коэффициентов вновь воспользуемся методом электронного баланса.
Пример 4. CH3OH + K2Cr2O7 + H2SO4 → HCOOH + Cr2(SO4)3 + K2SO4 + Н2О
В данном случае метанол и дихромат калия реагируют в кислой среде. Для расстановки коэффициентов можно воспользоваться любым из методов. Еще раз применим метод электронного баланса.
Пример 5. C6H12O6 + KMnO4 + H2SO4 → CO2 + MnSO4 + K2SO4 + Н2О
Расставим коэффициенты тремя разными способами.
Способ 1. В молекуле глюкозы степень окисления углерода -1, 0 и +1. Примем, что средняя с.о. равна 0. Имейте ввиду, что такой подход не всегда и не для всех веществ будет оправдан. В данном случае это вполне возможно.
Способ 2. Расставим коэффициенты методом электронного баланса, используя все три с.о. углерода.
Способ 3. Поскольку реакция между глюкозой и перманганатом калия проходит в кислой среде (в H2SO4), расставим коэффициенты ионно-электронным методом (полуреакций):
1) молекулярные вещества (а к ним относится и глюкоза) на ионы не диссоциируют, поэтому в схемах полуреакций записываются в исходном виде;
2) количество недостающих кислорода и водорода в полуреакциях компенсируем, дописывая по необходимости молекулы воды H2O или ионы водорода Н+;
3) считаем слева и справа в каждой полуреакции суммарный заряд (он создается ионами, образовавшимися при диссоциации реагирующих веществ, и ионами водорода Н+);
4) разницу зарядов компенсируем отдаваемыми или принимаемыми электронами;
5) так же, как и в методе электронного баланса, находим наименьшее общее кратное, определяем множители для каждой из полуреакций;
6) просуммируем полуреакции с учетом найденных множителей (коэффициентов);
7) перенесем коэффициенты в схему реакции, поставив их перед соответствующими веществами;

9) помним, что баланс количества атомов кислорода проверяем в последнюю очередь.
Пример 6. C3H4 + KMnO4 + H2SO4 → CH3COOH + CO2 + MnSO4 + K2SO4 + Н2О
В исходном веществе C3H4 (пропин) степени окисления углерода принимают значения -3, -1 и 0. В образовавшейся уксусной кислоте CH3COOH: -3 и +3. Кроме того, в углекислом газе CO2 с.о. углерода равна +4.
Такое разнообразие степеней окисления одного элемента затрудняет применение метода электронного баланса. Поэтому лучше воспользоваться методом полуреакций.
Действие окислителей на органические вещества
В зависимости от строения и состава органических веществ (разветвленность углеродного скелета, наличие функциональных групп и их количество), а также от условий процесса (избыток или недостаток окислителя, его концентрация, рН раствора, нагревание или охлаждение) окисление происходит по-разному.
Так, например, при окислении алкена раствором KMnO4 в мягких условиях (без нагревания и в нейтральной или слабощелочной среде) образуется двухатомный спирт. А при окислении алкена раствором KMnO4 в жестких условиях (с нагреванием и в кислой или сильнощелочной среде) молекула по двойной связи разрушается, и образуются совершенно иные продукты. Это могут быть и карбоновая кислота, и ее соль и СО2.
Знание действия окислителей на органические вещества тех или иных классов поможет верно определить продукты окислительно-восстановительной реакции и правильно расставить в них коэффициенты.
Итак, ответ на вопрос: «Как определить степень окисления в органических веществах», – позволяет правильно составить схему реакции с участием органических веществ и подобрать наиболее оптимальный метод расстановки коэффициентов.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
Темы кодификатора ЕГЭ: Электроотрицательность. Степень окисления и валентность химических элементов.
Когда атомы взаимодействуют и образуют химическую связь, электроны между ними в большинстве случаев распределяются неравномерно, поскольку свойства атомов различаются. Более электроотрицательный атом сильнее притягивает к себе электронную плотность. Атом, который притянул к себе электронную плотность, приобретает частичный отрицательный заряд δ—, его «партнер» — частичный положительный заряд δ+. Если разность электроотрицательностей атомов, образующих связь, не превышает 1,7, мы называем связь ковалентной полярной. Если разность электроотрицательностей, образующих химическую связь, превышает 1,7, то такую связь мы называем ионной.
Степень окисления – это вспомогательный условный заряд атома элемента в соединении, вычисленный из предположения, что все соединения состоят из ионов (все полярные связи – ионные).
Что значит «условный заряд»? Мы просто-напросто договариваемся, что немного упростим ситуацию: будем считать любые полярные связи полностью ионными, и будем считать, что электрон полностью уходит или приходит от одного атома к другому, даже если на самом деле это не так. А уходит условно электрон от менее электроотрицательного атома к более электроотрицательному.
Например, в связи H-Cl мы считаем, что водород условно «отдал» электрон, и его заряд стал +1, а хлор «принял» электрон, и его заряд стал -1. На самом деле таких полных зарядов на этих атомах нет.
Наверняка, у вас возник вопрос — зачем же придумывать то, чего нет? Это не коварный замысел химиков, все просто: такая модель очень удобна. Представления о степени окисления элементов полезны при составлении классификации химических веществ, описании их свойств, составлении формул соединений и номенклатуры. Особенно часто степени окисления используются при работе с окислительно-восстановительными реакциями.
Степени окисления бывают высшие, низшие и промежуточные.
Высшая степень окисления равна номеру группы со знаком «плюс».
Низшая определяется, как номер группы минус 8.
И промежуточная степень окисления — это почти любое целое число в интервале от низшей степени окисления до высшей.
Например, для азота характерны: высшая степень окисления +5, низшая 5 — 8 = -3, а промежуточные степени окисления от -3 до +5. Например, в гидразине N2H4 степень окисления азота промежуточная, -2.
Чаще всего степень окисления атомов в сложных веществах обозначается сначала знаком, потом цифрой, например +1, +2, -2 и т.д. Когда речь идет о заряде иона (предположим, что ион реально существует в соединении), то сначала указывают цифру, потом знак. Например: Ca2+, CO3 2-.
Для нахождения степеней окисления используют следующие правила:
- Степень окисления атомов в простых веществах равна нулю;
- В нейтральных молекулах алгебраическая сумма степеней окисления равна нулю, для ионов эта сумма равна заряду иона;
- Степень окисления щелочных металлов (элементы I группы главной подгруппы) в соединениях равна +1, степень окисления щелочноземельных металлов (элементы II группы главной подгруппы) в соединениях равна +2; степень окисления алюминия в соединениях равна +3;
- Степень окисления водорода в соединениях с металлами (солеобразные гидриды — NaH, CaH2 и др.) равна -1; в соединениях с неметаллами (летучие водородные соединения) +1;
- Степень окисления кислорода равна -2. Исключение составляют пероксиды – соединения, содержащие группу –О-О-, где степень окисления кислорода равна -1, и некоторые другие соединения (супероксиды, озониды, фториды кислорода OF2 и др.);
- Степень окисления фтора во всех сложных веществах равна -1.
Выше перечислены ситуации, когда степень окисления мы считаем постоянной. У всех остальных химических элементов степень окисления — переменная, и зависит от порядка и типа атомов в соединении.
Примеры:
Задание: определите степени окисления элементов в молекуле дихромата калия: K2Cr2O7.
Решение: степень окисления калия равна +1, степень окисления хрома обозначим, как х, степень окисления кислорода -2. Сумма всех степеней окисления всех атомов в молекуле равна 0. Получаем уравнение: +1*2+2*х-2*7=0. Решаем его, получаем степень окисления хрома +6.
В бинарных соединениях более электроотрицательный элемент характеризуется отрицательной степенью окисления, менее электроотрицательный – положительной.
Обратите внимание, что понятие степени окисления – очень условно! Степень окисления не показывает реальный заряд атома и не имеет реального физического смысла. Это упрощенная модель, которая эффективно работает, когда нам необходимо, например, уравнять коэффициенты в уравнении химической реакции, или для алгоритмизации классификации веществ.
Степень окисления – это не валентность! Степень окисления и валентность во многих случаях не совпадают. Например, валентность водорода в простом веществе Н2 равна I, а степень окисления, согласно правилу 1, равна 0.
Это базовые правила, которые помогут Вам определить степень окисления атомов в соединениях в большинстве случаев.
В некоторых ситуациях вы можете столкнуться с трудностями при определении степени окисления атома. Рассмотрим некоторые из этих ситуаций, и разберем способы их разрешения:
- В двойных (солеобразных) оксидах степень у атома, как правило, две степени окисления. Например, в железной окалине Fe3O4 у железа две степени окисления: +2 и +3. Какую из них указывать? Обе. Для упрощения можно представить это соединение, как соль: Fe(FeO2)2. При этом кислотный остаток образует атом со степенью окисления +3. Либо двойной оксид можно представить так: FeO*Fe2O3.
- В пероксосоединениях степень окисления атомов кислорода, соединенных ковалентными неполярными связями, как правило, изменяется. Например, в пероксиде водорода Н2О2, и пероксидах щелочных металлов степень окисления кислорода -1, т.к. одна из связей – ковалентная неполярная (Н-О-О-Н). Другой пример – пероксомоносерная кислота (кислота Каро) H2SO5 (см. рис.) содержит в составе два атома кислорода со степенью окисления -1, остальные атомы со степенью окисления -2, поэтому более понятной будет такая запись: H2SO3(O2). Известны также пероксосоединения хрома – например, пероксид хрома (VI) CrO(O2)2 или CrO5, и многие другие.
- Еще один пример соединений с неоднозначной степенью окисления – супероксиды (NaO2) и солеобразные озониды KO3. В этом случае уместнее говорить о молекулярном ионе O2 с зарядом -1 и и O3 с зарядом -1. Строение таких частиц описывается некоторыми моделями, которые в российской учебной программе проходят на первых курсах химических ВУЗов: МО ЛКАО, метод наложения валентных схем и др.
- В органических соединениях понятие степени окисления не очень удобно использовать, т.к. между атомами углерода существует большое число ковалентных неполярных связей. Тем не менее, если нарисовать структурную формулу молекулы, то степень окисления каждого атома также можно определить по типу и количеству атомов, с которыми данный атом непосредственно связан. Например, у первичных атомов углерода в углеводородах степень окисления равна -3, у вторичных -2, у третичных атомов -1, у четвертичных — 0.
Потренируемся определять степень окисления атомов в органических соединениях. Для этого необходимо нарисовать полную структурную формулу атома, и выделить атом углерода с его ближайшим окружением — атомами, с которыми он непосредственно соединен.
Полезные советы:
- Для упрощения расчетов можно использовать таблицу растворимости – там указаны заряды наиболее распространенных ионов. На большинстве российских экзаменов по химии (ЕГЭ, ГИА, ДВИ) использование таблицы растворимости разрешено. Это готовая шпаргалка, которая во многих случаях позволяет значительно сэкономить время.
- При расчете степени окисления элементов в сложных веществах сначала указываем степени окисления элементов, которые мы точно знаем (элементы с постоянной степенью окисления), а степень окисления элементов с переменной степенью окисления обозначаем, как х. Сумма всех зарядов всех частиц равна нулю в молекуле или равна заряду иона в ионе. Из этих данных легко составить и решить уравнение.
Тренировочный тест по теме «Степени окисления и валентность» 10 вопросов, при каждом прохождении новые.
132
Создан на
07 января, 2022 От Admin
Тренировочный тест «Степени окисления»
1 / 10
1) S 2) Cl 3) N 4) Na 5) P
Из числа указанных в ряду элементов выберите два элемента, которые в составе образованных ими водородных соединений с общей формулой ЭНх могут иметь одинаковую степень окисления.
Запишите в поле ответа номера выбранных элементов.
2 / 10
1) O 2) P 3) Si 4) Cr 5) S
Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в оксидах может принимать значение +3.
3 / 10
1) Mn 2) Fe 3) Al 4) Si 5) P
Из указанных в ряду элементов выберите два элемента, которые в оксидах проявляют степень окисления +4.
4 / 10
1) Sn 2) Ca 3) С 4) K 5) B
Из указанных в ряду элементов выберите два элемента, которые в соединениях могут проявлять степень окисления, равную +4.
5 / 10
1) Cr 2) Na 3) P 4) As 5) N
Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в оксидах может принимать значение +2.
6 / 10
1) Na 2) Si 3) Mg 4) C 5) O
Из числа указанных в ряду элементов выберите два элемента, проявляющих во всех соединениях только положительную степень окисления.
7 / 10
1) F 2) O 3) N 4) S 5) Cl
Из числа указанных в ряду элементов выберите два элемента, которые не проявляют степени окисления, равной номеру группы.
8 / 10
1) Ca 2) P 3) N 4) О 5) Ti
Из числа указанных в ряду элементов выберите два элемента, у каждого из которых разность между значениями их высшей и низшей степеней окисления равна 4.
9 / 10
1) S 2) Ca 3) Mn 4) Al 5) Cl
Из числа указанных в ряду элементов выберите два элемента, которые в высших оксидах проявляют одинаковую степень окисления.
10 / 10
1) Cr 2) P 3) Al 4) Mn 5) S
Из числа указанных в ряду элементов выберите два элемента, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления.
Ваша оценка
The average score is 54%
II. ОВР в органической химии.
Степени окисления атомов в органических соединениях.
|
Углеводороды |
Спирты |
Альдегиды, кетоны |
Карбоновые кислоты |
|
-2 +1 -2 +1 CH2=CH2 |
-2 +1 -2 +1 CH3-OH |
0 ⸗O-2 0 -2 H-C-H (HCHO) |
+2 -2-2 HCOOH |
|
-2 -1 -3 CH2=CH-CH3 |
-3 -1 -2 CH3-CH2-OH |
-3 +1 ⸗O-2 CH3-C- H -3 +1 -2 (CH3CHO) |
-3 +3-2- 2 CH3COOH |
|
-3 -1 -1 -3 CH3-CH=CH-CH3 |
-1 -1 CH2-CH2 І І OH OH |
-3 +2 -3 CH3-C- CH3 ǁ O-2 |
+3 -2 -2 C OOH І+3-2-2 C OOH |
|
-3 0 -1 -3 CH3-C=CH-CH3 І -3 CH3 |
-1 0 -3 CH2-CH-CH3 І І OH OH |
||
|
-3 0 0 -3 CH3-CH2-CH-CH3 І І OH OH |
Углеводороды.
В кислой среде:
1) CH2=CH2 + KMnO4 + H2SO4 → K2SO4 + MnSO4 + H2O + CO2
-2 -2 +7 +2 +4
5CH2=CH2 + 12KMnO4 + 18H2SO4 → 6K2SO4 + 12MnSO4 + 10CO2 + 28H2O
2C-2 – 12e— → 2C+4 | 12 | 5 – окисляется, восстановитель;
Mn+7 + 5e— → Mn+2 | 5 |12 — восстанавливается, окислитель
2) C2H2 – окисляется окислителями в кислой среде до щавелевой кислоты.
-1 -1 k. H2SO4, KMnO4 (K2Cr2O7) COOH
CHΞCH ―――――――→ І (HOOC-COOH)
COOH
-2 -1 -3 +7 +4 -3 +3
3)CH2=CH-CH3 + 2KMnO4 + 3H2SO4 → CO2 + CH3-COOH + K2SO4 +
+2
2MnSO4 + 4H2O
Mn+7 + 5e— → Mn+2 | 5e— | 2 — восст-тся, окислитель;
C-1 — 4e— → C+3 |} 10e—| 1 — окисляется, восстановитель
-3 -1 -1 -3 +7 -3 +3
4) 5CH3-CH=CH-CH3 + 8KMnO4 + 12H2SO4 → 10CH3-COOH + 4K2SO4 +
+2
8MnSO4 + 12H2O
Mn+7 + 5e— → Mn+2 |4| | 8Mn+7 +40e— →8Mn+2 — восстанавливается, окислитель;
| |× 2 |
C-1 — 4e— → C+3 |5| | 10C-1 — 40e— → 10C+3 — окисляется, восстановитель
-3 0 -1 -3 -3 +3 -2 -2 -3 +2 -3
5) CH3-C‡ CH-CH3 + 6KMnO4 + 9H2SO4 → 5CH3-COOH + 5CH3-C-CH3
+ 3K2SO4 + 6MnSO4 +9H2O
| ǁ
-3 O-2
CH3
Mn+7 + 5e— → Mn+2 |× 6| 6Mn+7+30e—→ 6Mn+2
C-1 — 4e— → C+3 | | 5C-1— 20e— → 5C+3
C0 — 2e— → C+2 | | 5C0 10e— → 5C+2
↙͞ ͞͞͞ ͞ ͞͞ ͞ ͞ ͞ ͞ ͞ ͞͞ ͞ ͞↘
-1 -1 +7 C+3OOH +2
6) 5CHΞCH + 8KMnO4 + 12H2SO4 → 5 І +4K2SO4 +8MnSO4+ 12H2O C+3OOH
только ацетилен!
2C-1 — 8e— → 2C+3 |× 5
Mn+7 + 5e— → Mn+2 |× 8
Гомологи ацетилена окисляются до одноосновных карбоновых кислот.
-1 0 -3 +7 -3 +3 +4 +2
7)5CHΞC-CH3 +8KMnO4 +12H2SO4 → 5CH3-COOH +5CO2 +4K2SO4+ 8MnSO4 + 12H2O
—3 0 0 -3 +7 -3 +3 +2

Ароматические углеводороды.
-1 -3 +7 -1 +3 +2
9) 5C6H5 -CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 3K2SO4 + 6MnSO4 + 14H2O
Mn+7 + 5e— → Mn+2 |× 6
C-3 — 6e— → C+3 |× 5
—1 -2 -3 +7 -1 +3 +4 +2
10) 5C6H5 -CH2CH3 + 12KMnO4 + 18H2SO4 → 5C6H5-COOH + 5CO2 + 6K2SO4 + 12MnSO4 + 28H2O
Mn+7 + 5e— → Mn+2 | 5e—|× 12
C-2 — 6e— → C+4 | |
|}12e—|× 5
C-3 — 6e— → C+3 | |
-1 -3 +7 -1 +3 +2
11) 5 C6H4(CH3)2 + 12KMnO4 + 18H2SO4 → 5 C6H4(COOH)2 + 6K2SO4 + 12MnSO4 + 28H2O
1,2-диметилбензол орто-фталевая кислота
2C-3 — 12e— → 2C+3 |12e—|× 5
Mn+7 + 5e— → Mn+2 | 5e— |× 12
-1 -1 -2 +7 -1 +3 +4 +2
12) C6H5—CH=CH2 + 2KMnO4 + 3H2SO4 → C6H5COOH + CO2 + K2SO4 + 2MnSO4 + 4H2O
Mn+7 + 5e— → Mn+2 | 5e—|× 2
C-1 — 4e— → C+3 | |
|} 10e—|× 1
C-2 — 6e— → C+4 | |
В нейтральной среде:
-2 -2 +7 -1 -1 +4
1) 3CH2=CH2 + 2KMnO4 + 4H2O → CH2-CH2 + 2MnO2 + 2KOH 2C-2 — 2e— → 2C-1 |× 3
І І Mn+7 + 3e— → Mn+4 |× 1
OH OH
2) 3CH3–CH=CH– CH3 + 2KMnO4 + 4H2O → 3CH3–CH–CH– CH3 + 2MnO2 + 2KOH
І І
OH OH
3) C6H5—CH=CH2 + 2KMnO4 + 4H2O → C6H5—CH– CH2 + 2MnO2 + 2KOH
І І
OH OH
00C
4) 3CH3–CH=CH2 + 2KMnO4 + 4H2O —→ 3CH3–CH–CH + 2MnO2 + 2KOH
І І
OH OH
C+3OOK
5) 3CHΞCH + 8KMnO4 → 5 І + 8MnO2 + 2KOH + 2H2O
C+3OOK
только ацетилен!
6) 3CH3–CH=CH–СH2– CH3 + 2KMnO4 + 4H2O → 3CH3–CH–CH– СH2– CH3 + 2MnO2 + 2KOH
І І
OH OH
7) CH3–CH=C– CH3 + 2KMnO4 → CH3-C- CH3 + CH3-COOH + 2MnO2 + 2KOH
І ǁ
CH3 O
Реакция присоединения против правила Марковникова:
+ — H2O2
CH3—CH=CH2 + HBr ——→ CH3—CH2—CH2 — 1-бромпропан
|
Br
При наличии атома хлора в молекуле реакция также идёт против правила, т.к. меняется поляризация молекулы:
— + + —
CH2—CH=CH2 + HBr ——→ CH2—CH2—CH2 — 1-бром-3-хлорпропан
| | |
Cl Cl Br
Спирты.
-3 -1 -2 +7 -3 +3 +2
1) CH3-CH2-OH + 4KMnO4 + 6H2SO4 → 5CH3-COOH + 2K2SO4 + 4MnSO4 + 11H2O
-3 -1 -2 +6 -3 +3 +3
2) CH3-CH2-OH + 2K2Cr2O7 + 8H2SO4 → 3CH3-COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
+6 -2 +2 +3
3) 2K2Cr2O7 + 3CH3OH + 8H2SO4 → HCOOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
-3 +1 -2 -3 +7 -3 +2 -2 -3 +4
4) 5CH3-CH-CH2-CH3 + 2KMnO4 → 5CH3-C-CH2-CH3 + 2MnO2 + 2KOH + 4H2O
І ǁ
OH O
-1 -1 -2 +7 -1 +3 +2
5) 5C6H5 -CH2OH + 4KMnO4 + 6H2SO4 → 5C6H5-COOH + 2K2SO4 + 4MnSO4 + 11H2O
-2 +7 +4 +2
6) 5CH3-OH + 6KMnO4 + 9H2SO4 → 5CO2 + 3K2SO4 + 6MnSO4 + 19H2O
-3 -1 -2 +7 +4 -3 +3
7) 3CH3-CH2-OH + 4KMnO4 → 4MnO2 + KOH + 4H2O + 3CH3-COOK
Альдегиды.
0 +7 +4 +2
1) 5HCHO + 4KMnO4 + 6H2SO4 → 5CO2 + 2K2SO4 + 4MnSO4 + 11H2O
-3 +1 +6 -3 +3 +3
2) 3CH3CHO + K2Cr2O7 + 4H2SO4 → 3CH3-COOH + Cr2(SO4)3 + K2SO4 + 4H2O
-3 +1 +7 -3 +3 +2
3) 5CH3CHO + 2KMnO4 + 3H2SO4 → 5CH3-COOH + K2SO4 + 2MnSO4 + 3H2O
-3 +1 +7 -3 +3 +4
4) 3CH3CHO + 2KMnO4 + KOH → 3CH3-COOK + 2MnO2 + 2H2O
OH
|
5) HC-(CH2)7 -CH3 HC-(CH2)7 -CH3
3 ǁ + 2KMnO4 + 4H2O → 3 | + 2KOH + 2MnO2
HC-(CH2)7 –COOH HC-(CH2)7 -COOH
стеариновая кислота |
OH
9,10 — диоксистеариновая кислота
Другие реакции органических соединений.
Углеводороды.
t0, кат.
1) 2C4H10 + 5 O2 ——→ 4CH3-COOH + 2H2O
2) 3CH3–CH=CH– CH3 + 2KMnO4 + 4H2O → 3CH3–CH–CH– CH3 + 2MnO2 + 2KOH
І І
OH OH
Pd+2
3) 2CH2=CH2 + O2 —→ 2CH3CHO
Ароматические углеводороды.
1) 5С6H4ClC2H5 +12KMnO4 +18H2SO4 → 5C6H4СlCOOH+ 5CO2 +6K2SO4 +12MnSO4+ 28H2O
(орто-,пара- изомеры) (орто-, пара- изомеры)
t0
2) 5 O2N-С6H4-CH3 + 6KMnO4 + 9H2SO4 → 5 O2N-С6H4-COOH + 3K2SO4 + 6MnSO4 + 14H2O
(пара- изомер) (пара- изомер)
3) 5С6H5CH(CH3)2 +18KMnO4 + 27H2SO4 →5C6H5COOH +10CO2+9K2SO4 +18MnSO4+48H2O
KMnO4
4) CHΞC-С6H4-CH3 ——→ С6H4-(COOH)2
(орто — изомер) орто – фталевая кислота
5) 3С6H5-CH2 -CH=CH2 + 2KMnO4 + 4H2O → 3С6H5-CH2 –CH–CH2 + 2KOH + 2H2O
| |
OH OH
6) 5C6H5—CH2 — CH=CH2 + 16KMnO4 + 24H2SO4 → 5C6H5COOH + 10CO2 + 8K2SO4 + 16MnSO4 + 34H2O
+ —
7) O2N-С6H4-COOH + 3Fe + 7HCl → С6H4(COOH)NH3Cl + 3FeCl3 + 2H2O
Получение.
1) Al4C3 + 12H2O → 4Al(OH)4 + 3CH4
2) Al4C3 + 12HCl → 4AlCl3 + 3CH4
3) CaC2 + 2H2O → Ca(OH)2 + C2H2
Спирты.
1) 3CH2–CH=CH–CH2 + 2KMnO4 + 4H2O → 3CH2–CH–CH–CH2 + 2KOH + 2MnO2
| | | | | |
OH OH OH OH OH OH
2) 3CH3-CH2-OH + K2Cr2O7 + 4H2SO4 → 3CH3-CHO + 2Cr2(SO4)3 + K2SO4 + 7H2O
ацеталь
Альдегиды.
1) CH3CHO + 2NaMnO4 + 3NaOH → CH3-COONa + 2Na2MnO4 + 2H2O
Карбоновые кислоты.
+6 +3 +4 +3
1)K2Cr2O7 +3HOOC-COOH +4H2SO4 → 6CO2 + Cr2(SO4)3 + K2SO4 +7H2O
Соли карбоновых кислот.
электролиз
1) 2CH3-COONa ———→ H2 + C2H6 + 2NaOH + 2CO2