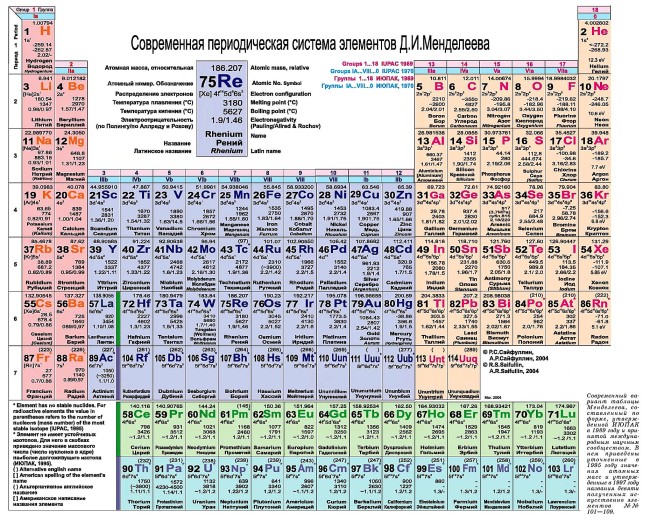
Таблицы на ЕГЭ и ОГЭ по химии
На сдаче ЕГЭ и ОГЭ по химии можно использовать три таблицы:
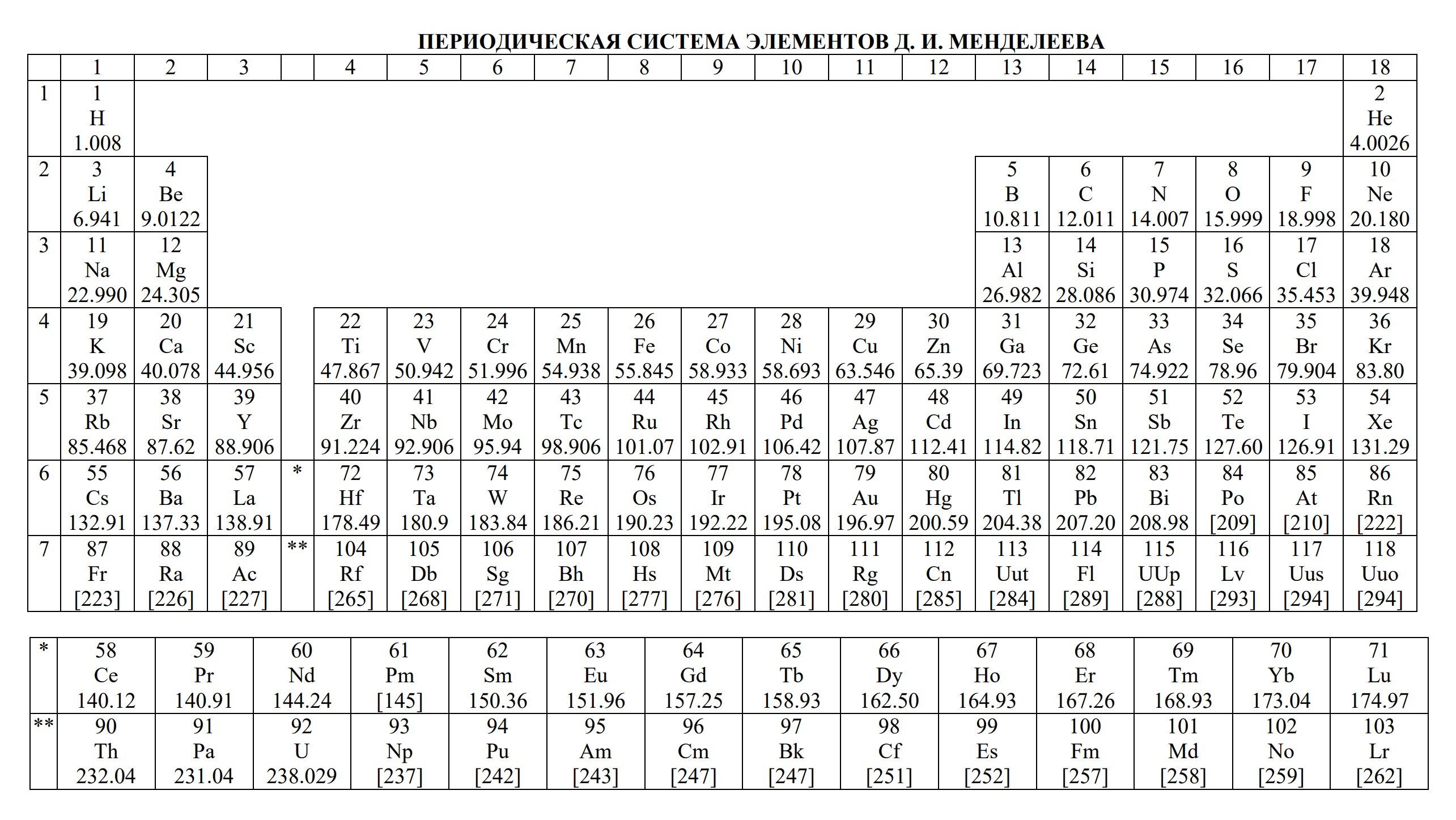
- периодическая система химических элементов Д.И. Менделеева
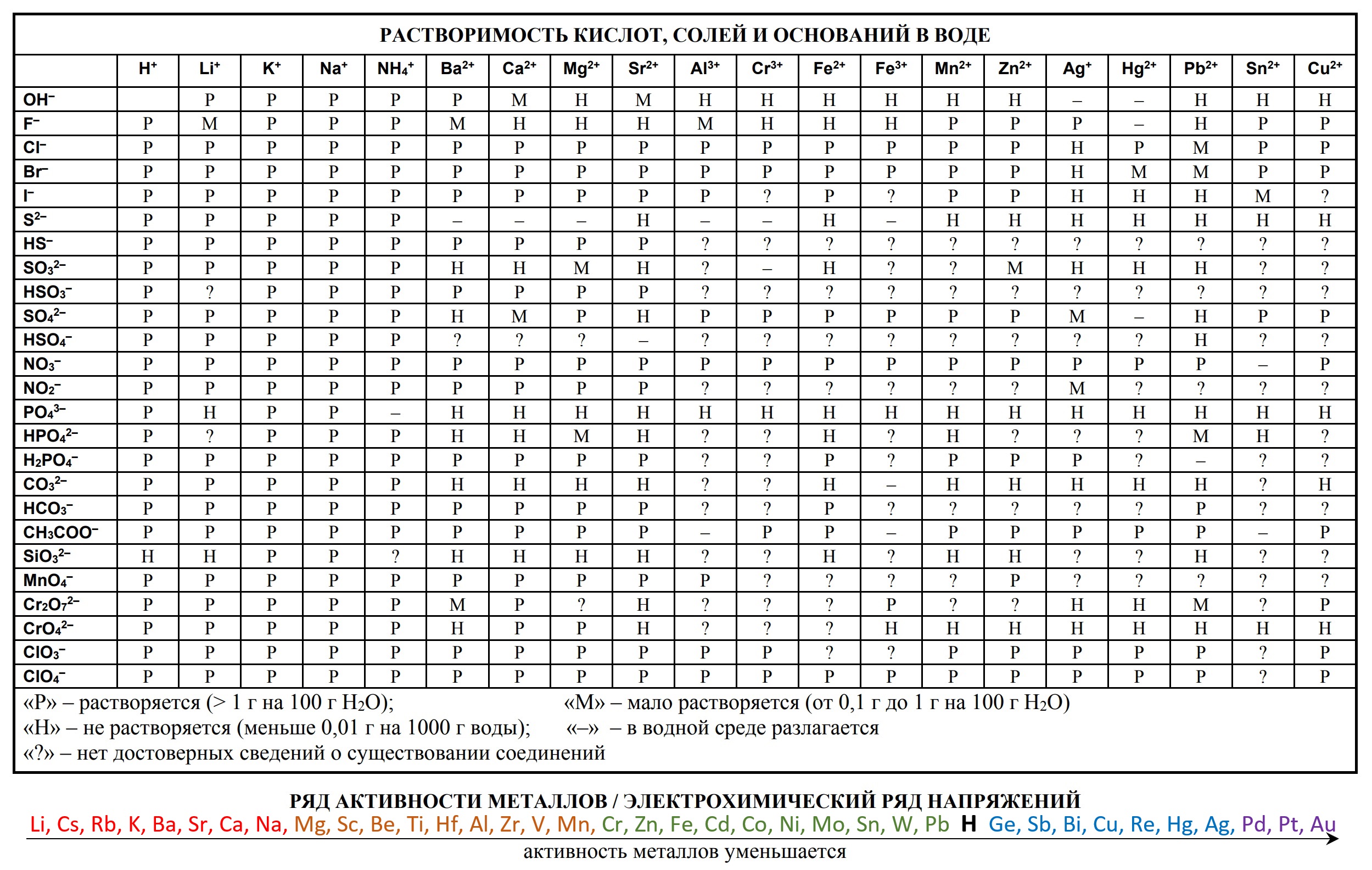
- таблица растворимости
- ряд активности металлов.
Они содержат в себе 80% информации, необходимой для решения большинства заданий.
Однако таблицы на форзацах разных учебников, продаваемые в книжных магазинах, располагающиеся на просторах интернета отличаются не только оформлением, но и содержанием. Что бы они оказались надёжно шпаргалкой, а не приятной неожиданностью, лучше с самого начала начинать работать с тем форматом, который официально разрешен на ЕГЭ твоего года.
Скачать эти таблицы можно ниже. А как сделать эти безликие таблицы наиболее информационными для тебя я расскажу на уроке.
- Таблица Д.И. Менделеева для ОГЭ и ЕГЭ
- Таблица растворимости и ряд активности для ОГЭ и ЕГЭ
- Таблица растворимости с расширенным рядом активности
- Таблица Д.И. Менделеева длиннопериодная для олимпиады
Ниже приведены таблицы, идентичные используемым на ЕГЭ по химии: «Периодическая система химических элементов Д.И.Менделеева»
«Растворимость солей, кислот и оснований в воде» и «Электрохимический ряд напряжений металлов»:
Опубликовано
admin
в 14:10
При выполнении работы ЕГЭ 2021 по химии разрешено использовать:
— периодическую систему химических элементов Д.И. Менделеева,
— таблицу растворимости солей, кислот и оснований в воде,
— электрохимический ряд напряжений металлов.
→ скачать и распечатать таблицы
Эти сопроводительные материалы прилагаются к тексту работы.
Для вычислений используйте непрограммируемый калькулятор.
Перечень дополнительных устройств и материалов, пользование которыми разрешено на ЕГЭ, утверждается приказом Минпросвещения России и Рособрнадзора.
Смотрите также:
2 досрочных варианта ЕГЭ 2020 по химии с ответами от ФИПИ
ЕГЭ 2021. Химия. Баллы за задания
Демоверсия ЕГЭ по химии 2021 года от ФИПИ
Тренировочные варианты ЕГЭ 2020 по химии СтатГрад
Распечатать для школы
Ниже Вы можете скачать таблицу Менделеева в хорошем качестве для печати на принтере.
Таблица пригодится на уроках химии. Ниже расположены ссылки на скачивание таблицы для печати разных размеров без потери качества (большой размер до А3 формата).
Скачать для А4
Скачать для печати А3 формата
Еще один вариант таблицы элементов Менделеева в высоком разрешении:
Скачать для печати А3 формата
Скачать для печати А3 формата
Понедельник, 20 Январь 2014 15:49
-
Печать
Периодическая таблица химических элементов Д.И. Менделеева и таблица растворимости кислот, оснований и солей, используемые на итоговой аттестации обучающихся по химии (скачать)
Наверх
Цитата дня
Учитесь так, словно вы постоянно ощущаете нехватку своих знаний, и так, словно вы постоянно боитесь растерять свои знания.
Конфуций
Таблица Менделеева — общепринятое графическое выражение Периодического закона, открытого Д.И. Менделеевым в 1869 г. Первоначальный вариант таблицы был разработан Менделеевым в 1869—1871 годах. За время существования было предложено более сотни вариантов её изображения, однако наиболее общепринятый вариант представляет собой двумерную таблицу в которой каждый столбец (группа) определяет основные физико-химические свойства, а строки представляют собой периоды, в определённой мере подобные друг другу.
Мы постарались описать основные химические элементы Таблицы Менделеева, для подробной информации о них переходите по соответствующей ссылке в таблице. Обращаем ваше внимание, что целью нашего сайта Занимательная химия не является описание химических элементов с научной точки зрения, мы больше сконцентрировались на интересных фактах, которые будут интересны даже детям, не углубляясь в непонятные термины и цифры. Однако, для каждого элемента приводится краткое описание химических свойств в простой и доступной форме.
| ГРУППЫ ЭЛЕМЕНТОВ | |||||||||
| I | II | III | IV | V | VI | VII | VIII | ||
| 1 H водород |
2 He гелий |
||||||||
| 3 Li литий |
4 Be бериллий |
5 B бор |
6 С углерод |
7 N азот |
8 O кислород |
9 F фтор |
10 Ne неон |
||
| 11 Na натрий |
12 Mg магний |
13 Al алюминий |
14 Si кремний |
15 P фосфор |
16 S сера |
17 Cl хлор |
18 Ar аргон |
||
| 19 K калий |
20 Ca кальций |
21 Sc скандий |
22 Ti титан |
23 V ванадий |
24 Cr хром |
25 Mn марганец |
26 Fe железо |
27 Co кобальт |
28 Ni никель |
| 29 Cu медь |
30 Zn цинк |
31 Ga галлий |
32 Ge германий |
33 As мышьяк |
34 Se селен |
35 Br бром |
36 Kr криптон |
||
| 37 Rb рубидий |
38 Sr стронций |
39 Y иттрий |
40 Zr цирконий |
41 Nb ниобий |
42 Mo молибден |
43 Tc технеций |
44 Ru рутений |
45 Rh родий |
46 Pd палладий |
| 47 Ag серебро |
48 Cd кадмий |
49 In индий |
50 Sn олово |
51 Sb сурьма |
52 Te теллур |
53 I иод |
54 Xe ксенон |
||
| 55 Cs цезий |
56 Ba барий |
57 La лантан × |
72 Hf гафний |
73 Ta тантал |
74 W вольфрам |
75 Re рений |
76 Os осмий |
77 Ir иридий |
78 Pt платина |
| 79 Au золото |
80 Hg ртуть |
81 Tl таллий |
82 Pb свинец |
83 Bi висмут |
84 Po полоний |
85 At астат |
86 Rn радон |
||
| 87 Fr франций |
88 Ra радий |
89 Ac актиний ×× |
104 Rf резерфордий |
105 Db дубний |
106 Sg сиборгий |
107 Bh борий |
108 Hs хассий |
109 Mt мейтнерий |
110 Ds дармштадтий |
| 111 Rg рентгений |
112 Сn коперниций |
113 Nh нихоний |
114 Fl флеровий |
115 Mc московий |
116 Lv ливерморий |
117 Tn теннесин |
118 Og оганессон |
| 57 La лантан |
58 Ce церий |
59 Pr празеодим |
60 Nd неодим |
61 Pm прометий |
62 Sm самарий |
63 Eu европий |
64 Gd гадолиний |
65 Tb тербий |
66 Dy диспрозий |
67 Ho гольмий |
68 Er эрбий |
69 Tm тулий |
70 Yb иттербий |
71 Lu лютеций |
| 89 Ac актиний |
90 Th торий |
91 Pa протактиний |
92 U уран |
93 Np нептуний |
94 Pu плутоний |
95 Am америций |
96 Cm кюрий |
97 Bk берклий |
98 Cf калифорний |
99 Es эйнштейний |
100 Fm фермий |
101 Md менделевий |
102 No нобелий |
103 Lr лоуренсий |
Таблица Менделеева и её значение
Открытие Периодического закона стало важнейшей вехой в развитии атомно-молекулярного учения. Благодаря ей сложилось современное понятие о химическом элементе, были уточнены представления о простых веществах и соединениях. Появление периодической системы и открытие периодического закона открыло новую, подлинно научную эру в истории химии и ряде смежных наук — взамен разрозненных сведений об элементах и соединениях была создана стройная таблица Менделеева, на основе которой стало возможным обобщать, делать выводы и предвидеть открытие новых химических элементов.
Список химических элементов Таблицы Менделеева
Список химических элементов упорядочен в порядке возрастания атомных номеров, приводятся обозначения элемента в Таблице Менделеева, латинское и русское названия.
| Z | Символ | Name | Название |
| 1 | H | Hydrogen | Водород |
| 2 | He | Helium | Гелий |
| 3 | Li | Lithium | Литий |
| 4 | Be | Beryllium | Бериллий |
| 5 | B | Boron | Бор |
| 6 | C | Carbon | Углерод |
| 7 | N | Nitrogen | Азот |
| 8 | O | Oxygen | Кислород |
| 9 | F | Fluorine | Фтор |
| 10 | Ne | Neon | Неон |
| 11 | Na | Sodium | Натрий |
| 12 | Mg | Magnesium | Магний |
| 13 | Al | Aluminium | Алюминий |
| 14 | Si | Silicon | Кремний |
| 15 | P | Phosphorus | Фосфор |
| 16 | S | Sulfur | Сера |
| 17 | Cl | Chlorine | Хлор |
| 18 | Ar | Argon | Аргон |
| 19 | K | Potassium | Калий |
| 20 | Ca | Calcium | Кальций |
| 21 | Sc | Scandium | Скандий |
| 22 | Ti | Titanium | Титан |
| 23 | V | Vanadium | Ванадий |
| 24 | Cr | Chromium | Хром |
| 25 | Mn | Manganese | Марганец |
| 26 | Fe | Iron | Железо |
| 27 | Co | Cobalt | Кобальт |
| 28 | Ni | Nickel | Никель |
| 29 | Cu | Copper | Медь |
| 30 | Zn | Zinc | Цинк |
| 31 | Ga | Gallium | Галлий |
| 32 | Ge | Germanium | Германий |
| 33 | As | Arsenic | Мышьяк |
| 34 | Se | Selenium | Селен |
| 35 | Br | Bromine | Бром |
| 36 | Kr | Krypton | Криптон |
| 37 | Rb | Rubidium | Рубидий |
| 38 | Sr | Strontium | Стронций |
| 39 | Y | Yttrium | Иттрий |
| 40 | Zr | Zirconium | Цирконий |
| 41 | Nb | Niobium | Ниобий |
| 42 | Mo | Molybdenum | Молибден |
| 43 | Tc | Technetium | Технеций |
| 44 | Ru | Ruthenium | Рутений |
| 45 | Rh | Rhodium | Родий |
| 46 | Pd | Palladium | Палладий |
| 47 | Ag | Silver | Серебро |
| 48 | Cd | Cadmium | Кадмий |
| 49 | In | Indium | Индий |
| 50 | Sn | Tin | Олово |
| 51 | Sb | Antimony | Сурьма |
| 52 | Te | Tellurium | Теллур |
| 53 | I | Iodine | Иод |
| 54 | Xe | Xenon | Ксенон |
| 55 | Cs | Caesium | Цезий |
| 56 | Ba | Barium | Барий |
| 57 | La | Lanthanum | Лантан |
| 58 | Ce | Cerium | Церий |
| 59 | Pr | Praseodymium | Празеодим |
| 60 | Nd | Neodymium | Неодим |
| 61 | Pm | Promethium | Прометий |
| 62 | Sm | Samarium | Самарий |
| 63 | Eu | Europium | Европий |
| 64 | Gd | Gadolinium | Гадолиний |
| 65 | Tb | Terbium | Тербий |
| 66 | Dy | Dysprosium | Диспрозий |
| 67 | Ho | Holmium | Гольмий |
| 68 | Er | Erbium | Эрбий |
| 69 | Tm | Thulium | Тулий |
| 70 | Yb | Ytterbium | Иттербий |
| 71 | Lu | Lutetium | Лютеций |
| 72 | Hf | Hafnium | Гафний |
| 73 | Ta | Tantalum | Тантал |
| 74 | W | Tungsten | Вольфрам |
| 75 | Re | Rhenium | Рений |
| 76 | Os | Osmium | Осмий |
| 77 | Ir | Iridium | Иридий |
| 78 | Pt | Platinum | Платина |
| 79 | Au | Gold | Золото |
| 80 | Hg | Mercury | Ртуть |
| 81 | Tl | Thallium | Таллий |
| 82 | Pb | Lead | Свинец |
| 83 | Bi | Bismuth | Висмут |
| 84 | Po | Polonium | Полоний |
| 85 | At | Astatine | Астат |
| 86 | Rn | Radon | Радон |
| 87 | Fr | Francium | Франций |
| 88 | Ra | Radium | Радий |
| 89 | Ac | Actinium | Актиний |
| 90 | Th | Thorium | Торий |
| 91 | Pa | Protactinium | Протактиний |
| 92 | U | Uranium | Уран |
| 93 | Np | Neptunium | Нептуний |
| 94 | Pu | Plutonium | Плутоний |
| 95 | Am | Americium | Америций |
| 96 | Cm | Curium | Кюрий |
| 97 | Bk | Berkelium | Берклий |
| 98 | Cf | Californium | Калифорний |
| 99 | Es | Einsteinium | Эйнштейний |
| 100 | Fm | Fermium | Фермий |
| 101 | Md | Mendelevium | Менделевий |
| 102 | No | Nobelium | Нобелий |
| 103 | Lr | Lawrencium | Лоуренсий |
| 104 | Rf | Rutherfordium | Резерфордий |
| 105 | Db | Dubnium | Дубний |
| 106 | Sg | Seaborgium | Сиборгий |
| 107 | Bh | Bohrium | Борий |
| 108 | Hs | Hassium | Хассий |
| 109 | Mt | Meitnerium | Мейтнерий |
| 110 | Ds | Darmstadtium | Дармштадтий |
| 111 | Rg | Roentgenium | Рентгений |
| 112 | Cn | Copernicium | Коперниций |
| 113 | Nh | Nihonium | Нихоний |
| 114 | Fl | Flerovium | Флеровий |
| 115 | Mc | Moscovium | Московий |
| 116 | Lv | Livermorium | Ливерморий |
| 117 | Ts | Tennessine | Теннесин |
| 118 | Og | Oganesson | Оганессон |
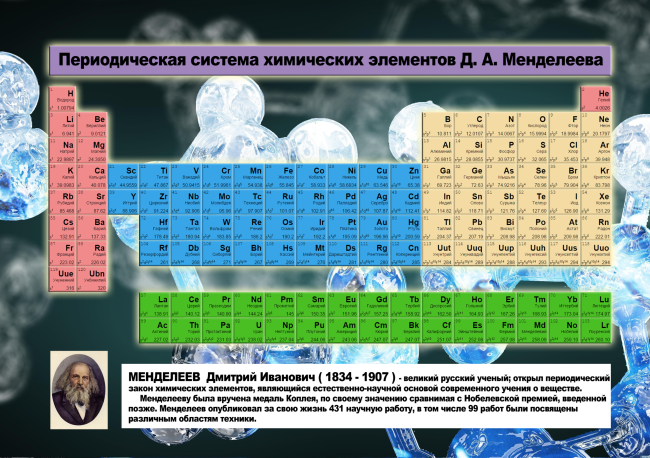
Таблица Менделеева в хорошем качестве
Предлагаем вам скачать несколько вариантов таблицы Менделеева в хорошем качестве, которые можно распечатать на принтере большого формата, как в черно-белом так и в цветном вариантах.
- Таблица Менделеева в хорошем качестве цветная
- Таблица Менделеева для печати черно-белая
Таблицы для ЕГЭ по химии
- 31.10.2020
Приводим таблицы, которые можно использовать на ЕГЭ по химии, эти таблицы можно использовать на ЕГЭ в любом году, входит в пакет разрешённых документов, т.е. то, чем можно пользоваться на ЕГЭ по химии.
Из года в год эти таблицы не меняются. В 2023 году поменялась только таблица растворимости — информацию обновили. Используйте ссылки ниже.
В состав документа входят:
- Таблица растворимости солей
- Таблица Менделеева
Добавить комментарий
Комментарии без регистрации. Несодержательные сообщения удаляются.
ТАБЛИЦА МЕНДЕЛЕЕВА — периодическая система химических элементов
Таблица Менделеева (периодическая система химических элементов) — это такая таблица, в которой классифицируются химические элементы по различным свойствам в зависимости от заряда их атомного ядра. Таблица является графическим изображением периодического закона, который открыл Дмитрий Иванович Менделеев в 1869 году. Изначальный вариант этой таблицы 1869 — 1871 гг. и устанавливал зависимость свойств элементов от их атомной массы. На данный момент элементы сводятся в двумерную таблицу, в которой каждый столбец — это группа, определяющая основные физико-химические свойства, а строки — это периоды, схожие друг с другом. Наиболее распространены 2 формы таблицы: короткая и длинная.
ТАБЛИЦА МЕНДЕЛЕЕВА

Порядковый номер элемента — это число равное числу протонов в ядре атома и числу электронов, которые вращаются вокруг него.
Чтобы посмотреть все свойства конкретного химического элемента нужно перейти по ссылке нажав на символ элемента в таблице.
| П. |
Группы химических элементов |
|||||||||
|
VIII |
||||||||||
| 1 |
1,00794 Водород |
4,0026 Гелий |
||||||||
| 2 |
6,941 Литий |
9,0122 Берилий |
10,811 Бор |
12,01115 Углерод |
14,0067 Азот |
15,9994 Кислород |
18,9984 Фтор |
20,179 Неон |
||
| 3 |
22,9898 Натрий |
24,305 Магний |
26,9815 Алюминий |
28,086 Кремний |
30,9738 Фосфор |
32,064 Сера |
35,454 Хлор |
39,948 Аргон |
||
| 4 |
39,0983 Калий |
40,08 Кальций |
44,956 Скандий |
47,88 Титан |
50,942 Ванадий |
51,996 Хром |
54,938 Марганец |
55,847 Железо |
58,9332 Кобальт |
58,69 Никель |
|
63,546 Медь |
65,39 Цинк |
69,72 Галлий |
72,61 Германий |
74,9216 Мышьяк |
78,96 Селен |
79,904 Бром |
83,80 Криптон |
|||
| 5 |
85,47 Рубидий |
87,62 Стронций |
88,906 Иттрий |
91,224 Цирконий |
92,906 Ниобий |
95,94 Молибден |
98,906 Технеций |
101,07 Рутений |
102,905 Родий |
106,42 Палладий |
|
107,868 Серебро |
112,41 Кадмий |
114,82 Индий |
118,71 Олово |
121,75 Сурьма |
127,60 Теллур |
126,9045 Йод |
131,30 Ксенон |
|||
| 6 |
132,905 Цезий |
137,327 Барий |
138,91 Лантан |
178,49 Гафний |
180,948 Тантал |
183,85 Вольфрам |
186,207 Рений |
190,2 Осмий |
192,22 Иридий |
195,09 Платина |
|
196,967 Золото |
200,59 Ртуть |
204,383 Таллий |
207,19 Свинец |
208,98 Висмут |
[209] Полоний |
[210] Астат |
[222] Радон |
|||
| 7 |
[223] Франций |
226,025 Радий |
[227] Актиний |
[261] Резерфордий |
[262] Дубний |
[263] Сиборгий |
[264] Борий |
[265] Хассий |
[266] Мейтнерий |
[281] Дармштадтий |
|
[281] Рентгений |
[285] Коперниций |
[284] Нихоний |
[289] Флеровий |
[288] Московий |
[293] Ливерморий |
[294] Теннесин |
[294] Оганесон |
|||
| 8 |
[316] Унуненний |
[320] Унбинилий |
||||||||
|
Высшие оксиды |
||||||||||
|
R2O |
RO |
R2O3 |
RO2 |
R2O5 |
RO3 |
R2O7 |
RO4 |
|||
|
Летучие водородные соединения |
||||||||||
|
RH4 |
RH3 |
H2R |
RH |
|
* ЛАНТАНОИДЫ |
|||||||||
|
114,16 Церий |
140,907 Празеодим |
144,24 Неодим |
[145] Прометий |
150,36 Самарий |
151,96 Европий |
157,25 Гадолиний |
158,924 Тербий |
162,5 Диспрозий |
164,93 Гольмий |
|
167,26 Эрбий |
168,94 Тулий |
173,04 Иттербий |
174,97 Лютеций |
||||||
|
** АКТИНОИДЫ |
|||||||||
|
232,038 Торий |
231,04 Протактиний |
238,03 Уран |
237,05 Нептуний |
[244] Плутоний |
[243] Америций |
[247] Кюрий |
[247] Берклий |
[251] Калифорний |
[254] Эйнштейний |
|
[257] Фермий |
[258] Менделевий |
[259] Нобелий |
260 Лоуренсий |
||||||
|
*** СУПЕРАКТИНОИДЫ |
|||||||||
|
320 Унбиуний |
* Унбибий |
* Унбитрий |
332 Унбиквадий |
* Унбипентий |
* Унбигексий |
||||
|
s – элементы |
p – элементы |
d – элементы |
f – элементы |
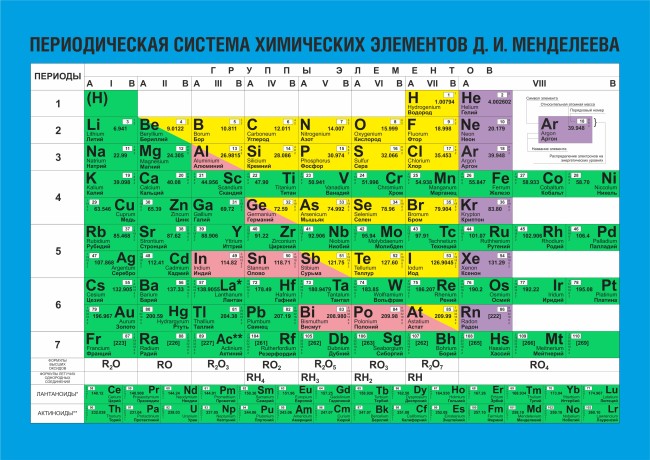
Периодическая система химических элементов Д.И. Менделеева
Расшифровка периодической системы химических элементов Д.И. Менделеева:
Периоды – горизонтальные строки химических элементов.
Группы – вертикальные столбцы химических элементов.
Подгруппы – А — главные (s- и р-элементы) и В — побочные (d- и f-элементы).
Номер периода – номер внешнего энергетического уровня в электронной формуле атома элемента.
Номер группы (для большинства элементов) – общее число валентных электронов (электронов внешнего энергетического уровня, а также предпоследнего d-подуровня, если он застроен не полностью).
Число элементов в периоде – максимальная емкость соответствующего энергетического уровня:
|
1 период |
2 элемента (1s2) |
5 период |
18 элементов (5s24d105p6) |
|
2 период |
8 элементов (2s22p6) |
6 период |
32 элемента (6s24f145d106p6) |
|
3 период |
8 элементов (3s23p6) |
7 период |
32 элемента (6s24f145d106p6) |
|
4 период |
18 элементов (4s23d104p6) |
8 период |
не завершен |
Построение периодов – в начале: два s-элемента, в конце: шесть р- элементов. В четвертом и пятом периодах между ними помещается по десять d-элементов, а в шестом и седьмом к ним добавляются четырнадцать f-элементов (формы электронных орбиталей).
В периоде – свойства химических элементов различаются между собой, т.к. электронные конфигурации валентных электронов их атомов различны.
В подгруппе – свойства элементов сходны между собой, т.к. электронные конфигурации валентных электронов их атомов сходны.
Причина периодичности свойств химических элементов заключается в периодической повторяемости сходных электронных конфигураций внешних энергетических уровней.
Формы электронных орбиталей (электронные семейства)
Классификация химических элементов по электронным конфигурациям их атомов (электронные орбитали)
|
Название семейства |
Тип конфигурации |
Застраиваемые подуровни |
|
s — элементы |
ns1–2 |
внешний (n) s-подуровень |
|
p -элементы |
ns2 np1–6 |
внешний (n) р-подуровень |
|
d — элементы |
(n-1)d1–10 ns1–2 |
предвнешний (n–1 ) d-подуровень |
|
f — элементы |
(n-2)f1–14 (n-1)d1–10 ns1–2 |
третий снаружи (n–2) f-подуровень |
Графическое изображение орбиталей
Свойства элементов таблицы Менделеева
Металлы – элементы главных подгрупп с числом валентных электронов от 1 до 3 (подгруппы IA, IIA, IIIА, кроме элемента бора), а также германий, олово, свинец, сурьма, висмут и полоний.
Неметаллы – бор и элементы главных подгрупп с числом валентных электронов от 4 до 7 (подгруппы IVA, VA, VIA, VIIA) кроме германия, олова, свинца, сурьмы, висмута и полония.
Переходные элементы – элементы побочных подгрупп (IB-VIIB); в виде простых веществ ведут себя как металлы.
Благородные газы – элементы подгруппы VIIIA, полностью застроенные энергетические подуровни s2p6, для гелия s2.
Галогены – элементы подгруппы VII(a) таблицы Менделеева, реагируют со всеми простыми веществами, кроме некот. неметаллов, являются энергичными окислителями, к ним относят F, Cl, Br, I, At, Ts.
Лантанойды – 15 элементов III группы 6-го периода, металлы с атомными номерами 57–71. Все они имеют стабильные изотопы, кроме прометия.
Актинойды – 15 радиоактивных элементов III группы 7-го периода с атомными номерами 89–103.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
— металлические свойства усиливаются и неметаллические свойства ослабевают;
— атомный радиус увеличивается;
— возрастает сила образованных элементом оснований и бескислородных кислот;
— уменьшается электроотрицательность.
В периодах с увеличением порядкового номера элемента прослеживается следующая закономерность:
— увеличивается электроотрицательность;
— металлические свойства ослабевают, неметаллические усиливаются;
— уменьшается атомный радиус.
Все элементы таблицы Менделеева, исключая гелий, неон и аргон, образуют кислородные соединения, которые изображены общими формулами под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где R — обозначает элемент группы.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения: RH4, RH3, RH2, RH. Соединения RH4 имеют нейтральный характер; RH3 – слабоосновной; RH2 – слабокислый; RH – сильнокислый характер.
История открытия периодического закона Менделеевым Д.И.
Самый важный вклад в систематизацию химических элементов внёс русский выдающийся химик Дмитрий Иванович Менделеев, автор труда «Основы химии», который в марте 1869 года представил Русскому химическому обществу (РХО) периодический закон химических элементов, изложенный в нескольких основных положениях.
В 1871 году Менделеев в итоговой статье «Периодическая законность химических элементов» дал формулировку Периодического закона: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел стоят в периодической зависимости от атомного веса». Тогда же Менделеев придал своей периодической таблице классический вид (короткая таблица, смотрите ниже).
В современном изложении периодический закон химических элементов звучит так: «Свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).»
Периодическая таблица элементов Менделеева длинная форма
Длинная форма таблицы Менделеева (или длиннопериодная форма) состоит из 18 групп с лева на право от щелочных металов до благородных газов. считается официальной версией с 1989 года.
Таблица Менделеева для печати в хорошем качестве скачать
Вы можете скачать таблицу Менделеева на выбор короткую или длинную форму в цветном и черно-белом цвете, для этого откройте по ссылке ниже изображение и сохраните его себе на компьютер.
1) Таблица Менделеева для печати в хорошем качестве цветная (короткая форма)
2) Таблица Менделеева для печати в хорошем качестве черно-белая (короткая форма)
3) Таблица Менделеева для печати в хорошем качестве цветная (длинная форма)
4) Таблица Менделеева для печати в хорошем качестве черно-белая (длинная форма)
____________
Источник информации:
1. Большой химический справочник / А.И.Волков, — М.: 2005.
2. Большая энциклопедия химических элементов. Периодическая таблица Менделеева / И.А.Леенсон. — Москва : 2014.
3. По материалам сайта ru.wikipedia.org
Мы нарисовали много разных вариантов
Выбери тот, который тебе по душе
-
полная таблица
Скачать
-
без лантаноидов и актиноидов
скачать
-
длинная, для крутых
скачать
-
нуарная
скачать
-
нуарная без лантаноидов и актиноидов
скачать
-
ну и официальная ФИПИшная
скачать
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности