Таблицы на ЕГЭ и ОГЭ по химии
На сдаче ЕГЭ и ОГЭ по химии можно использовать три таблицы:
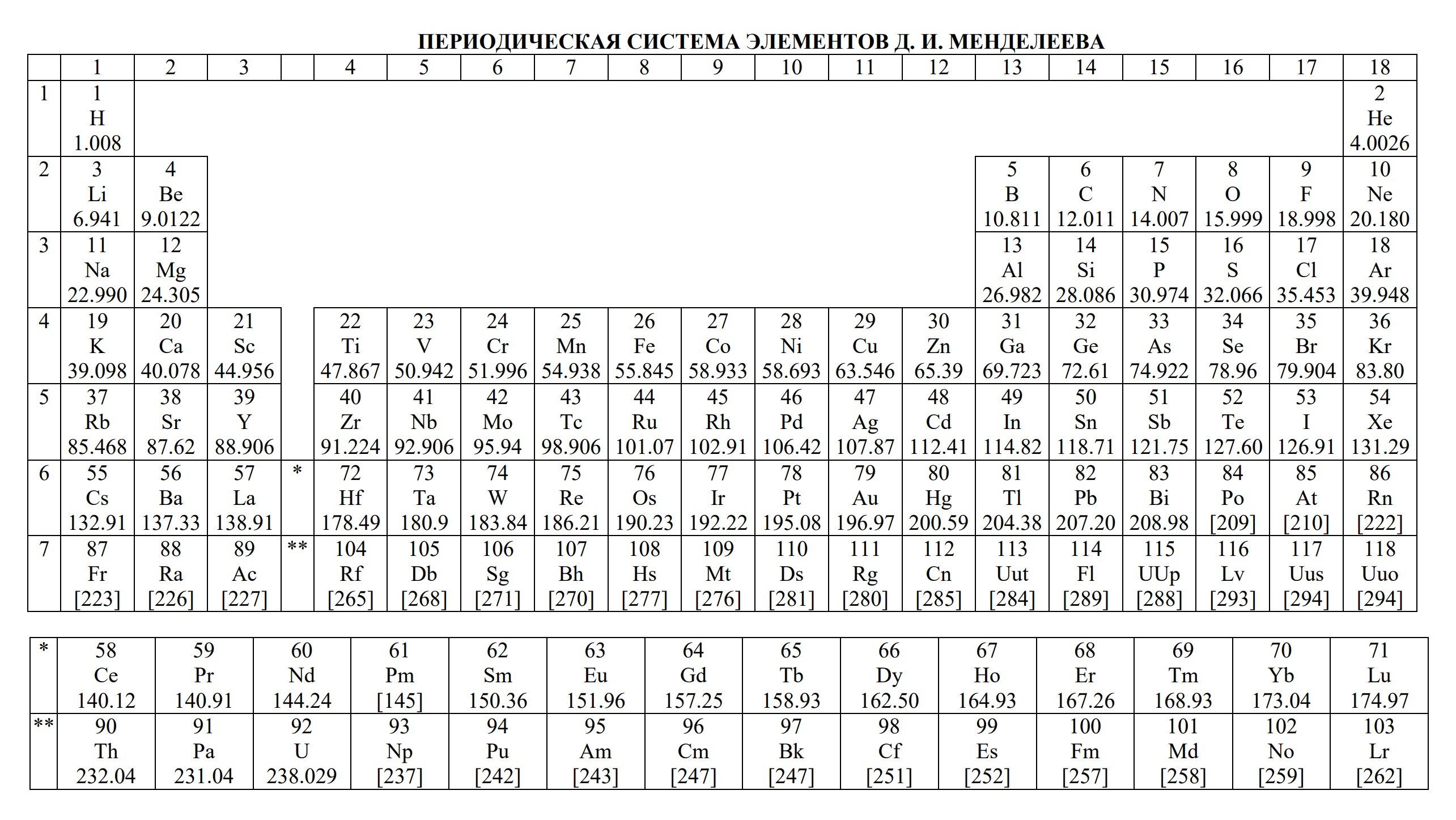
- периодическая система химических элементов Д.И. Менделеева
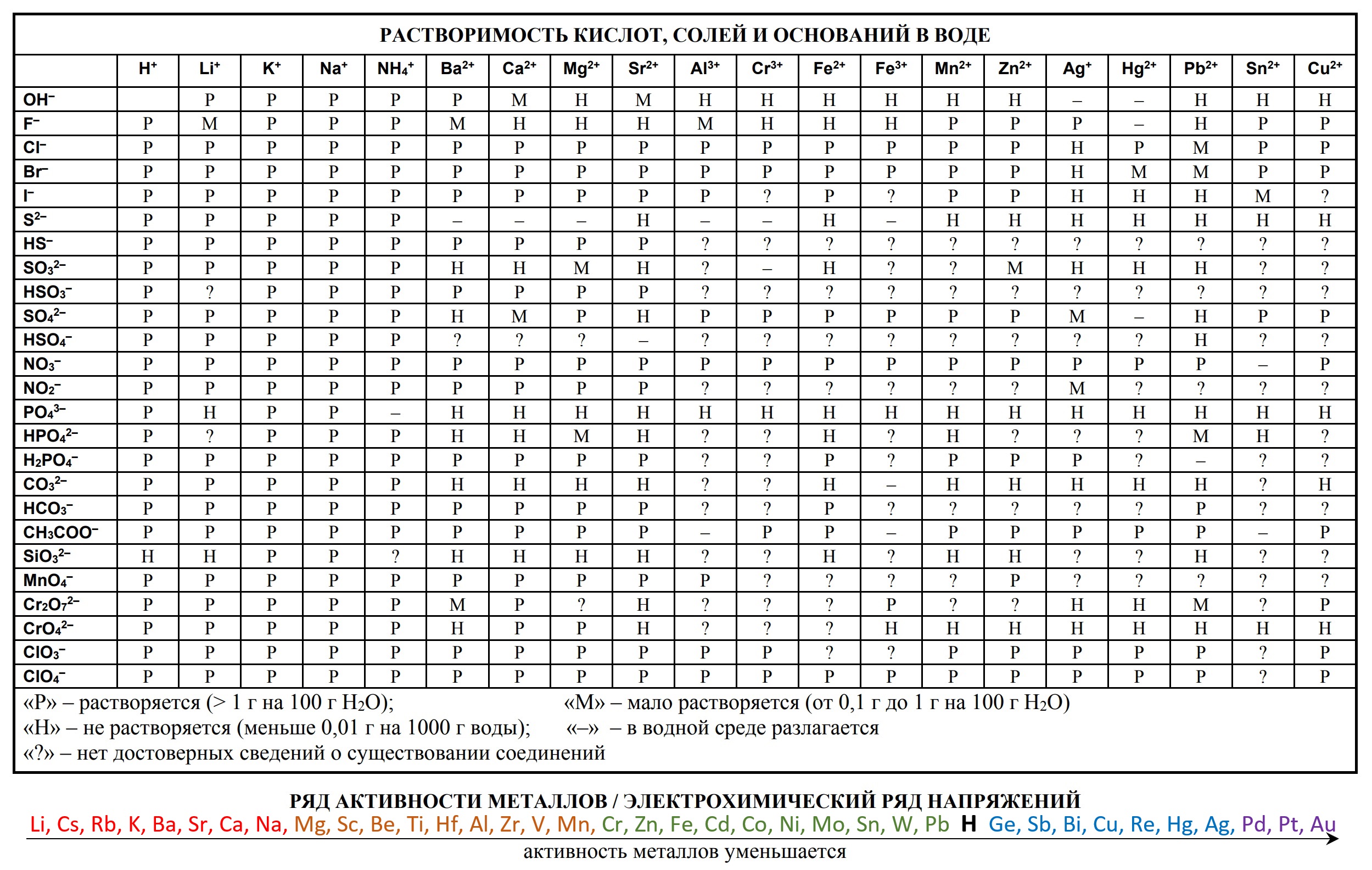
- таблица растворимости
- ряд активности металлов.
Они содержат в себе 80% информации, необходимой для решения большинства заданий.
Однако таблицы на форзацах разных учебников, продаваемые в книжных магазинах, располагающиеся на просторах интернета отличаются не только оформлением, но и содержанием. Что бы они оказались надёжно шпаргалкой, а не приятной неожиданностью, лучше с самого начала начинать работать с тем форматом, который официально разрешен на ЕГЭ твоего года.
Скачать эти таблицы можно ниже. А как сделать эти безликие таблицы наиболее информационными для тебя я расскажу на уроке.
- Таблица Д.И. Менделеева для ОГЭ и ЕГЭ
- Таблица растворимости и ряд активности для ОГЭ и ЕГЭ
- Таблица растворимости с расширенным рядом активности
- Таблица Д.И. Менделеева длиннопериодная для олимпиады
Таблицы ЕГЭ по химии
Ниже приведены таблицы, идентичные используемым на ЕГЭ по химии: «Периодическая система химических элементов Д.И.Менделеева»
«Растворимость солей, кислот и оснований в воде» и «Электрохимический ряд напряжений металлов»:
Тест для подготовки к ЕГЭ по химии «Периодическая система химических элементов Д.И. Менделеева»
При выборе может быть несколько правильных ответов.
1. Электронную конфигурацию инертного газа имеет атом:
1).Fe
3+
2). C l
—
3). Cu
2+
4). Fe
2+
2. Верны ли следующие суждения:
А. Барий более активный металл, чем стронций.
Б. Основной характер оксидов в ряду BaO — CaO — MgO
ослабевает.
1). Верно только А 2). Верно только Б 3). Верны оба 4). Оба
неверны.
3. Четыре электрона находятся на внешнем электронном слое
атомов каждого из химических элементов в ряду
1).C , Si, Sn 2).O, C l , I 3). N, C, S 4). Mg
4. В ряду химических элементов В—С—N
1) увеличивается заряд ядер атомов
2) возрастают кислотные свойства образуемых гидроксидов
3) увеличивается число электронных уровней
4) уменьшается электроотрицательность
5) возрастает атомный радиус
5. Химический элемент, в атомах которого распределение
электронов по слоям: 2, 8, 6, образует высший оксид
1) SeO
3
2) SO
3
3) N
2
O
3
4) P
2
O
3
6. В главных подгруппах Периодической системы с
увеличением заряда атомов химических элементов
1) усиливаются металлические свойства
2) уменьшаются металлические свойства
3) изменяется валентность в водородных соединениях
4) остается постоянной высшая валентность
7. В ряду элементов N—- P——As
1) уменьшается электроотрицательность
2) увеличивается сила образуемых кислородсодержащих кислот
3) уменьшаются основные свойства соединений Н
3
Э
4) уменьшается радиус атомов
5) увеличивается значение высшей степени окисления
8. Химическому элементу 3—го периода 5А – группы
соответствует схема распределения электронов по слоям:
1) 2,8,5 2) 2,8,3 3) 2,5 4) 2,3
9. Порядковый номер элемента в Периодической системе
соответствует
1) числу электронов в атоме
2) значению высшей валентности элемента по кислороду
3) числу электронов, недостающих до завершения внешнего
электронного слоя
4) числу электронных слоев в атоме
10. Атому аргона в основном состоянии соответствует
электронная конфигурация частицы : 1) Са
0
2) К
+
3) Cl
+
4) Zn
2+
11. Верны ли следующие суждения о свойствах кислорода и
серы?
А. Максимальная валентность этих элементов в соединениях равна
номеру группы
Б. При взаимодействии с водородом кислород и сера проявляют
окислительные свойства.
1). Верно только А 2) верно только Б 3) верны оба 4) оба неверны
12. Элемент, электронная конфигурация атома которого
1S
2
2S
2
2P
6
3S
2
3P
4
, образует водородное соединение
1) СН
4
2) SiH
4
3) H
2
O 4) H
2
S
13. В каком ряду химические элементы расположены в порядке
уменьшения их атомного радиуса?
1) С —В – Ве 2) Р — S—Cl 3) Si — Al — Mg 4) F — O – N
14.Оксиды состава ЭО и Э
2
О
3
образует каждый из двух элементов:
1) азот и железо 2) сера и селен 3) углерод и кремний 4) медь и
хром
15. Среди перечисленных элементов наиболее
электроотрицательным является 1) азот 2) кислород 3) хлор 4)
фтор
16. Номер периода в Периодической системе равен числу
1) электронов в атоме 2) электронов во внешнем уровне 3)
недостающих электронов до завершения электронного уровня 4)
заполняемых электронных слоев в атоме
17. Степень окисления +3 в соединениях могут проявлять
неметаллы
1) фосфор и хлор 2) углерод и кислород 3) азот и фтор 4) кремний
и селен
Для выполнения заданий(18-23) используйте следующий ряд
элементов
1) Na 2) K 3) Si 4) Mg 5) C
18. Определите, атомы каких элементов имеют на внешнем уровне
четыре электрона.
19. Из указанных элементов выберите три, которые в
Периодической системе стоят в одном периоде.
Расположите элементы в порядке возрастания их металлических
свойств.
20. Из числа данных элементов выберите два, которые проявляют
низшую степень окисления -4
Запишите номера выбранных элементов
21. Найдите неметаллы, запишите их в порядке возрастания
неметаллических свойств.
22. Выберите элементы, которые могут образовывать основные
оксиды.
23. Выберите элементы, которые имеют валентную конфигурацию:
nS
2
nP
2
Ответы:1-2, 2-3,3-1, 4-1, 5-12, 6- 14, 7-123, 8-1, 9-1,10-2, 11-2, 12-4,
13-2, 14-1, 15- 4. 16-4, 17- 1, 18- 35, 19-341, 20-35 , 21- 35, 22 -124 ,
23—35.
Уважаемый посетитель!
Если у вас есть вопрос, предложение или жалоба, пожалуйста, заполните короткую форму и изложите суть обращения в текстовом поле ниже. Мы обязательно с ним ознакомимся и в 30-дневный срок ответим на указанный вами адрес электронной почты
Статус Абитуриент Студент Родитель Соискатель Сотрудник Другое
Филиал Абакан Актобе Алагир Алматы Алушта Анапа Ангарск Архангельск Армавир Асбест Астана Астрахань Атырау Баку Балхаш Барановичи Барнаул Белая Калитва Белгород Бельцы Берлин Бишкек Благовещенск Бобров Бобруйск Борисов Боровичи Бронницы Брянск Бузулук Чехов Челябинск Череповец Черкесск Дамаск Дербент Димитровград Дмитров Долгопрудный Домодедово Дубай Дубна Душанбе Екатеринбург Электросталь Елец Элиста Ереван Евпатория Гана Гомель Гродно Грозный Хабаровск Ханты-Мансийск Хива Худжанд Иркутск Истра Иваново Ижевск Калининград Карабулак Караганда Каракол Кашира Казань Кемерово Киев Кинешма Киров Кизляр Королев Кострома Красноармейск Краснодар Красногорск Красноярск Краснознаменск Курган Курск Кызыл Липецк Лобня Магадан Махачкала Майкоп Минеральные Воды Минск Могилев Москва Моздок Мозырь Мурманск Набережные Челны Нальчик Наро-Фоминск Нижневартовск Нижний Новгород Нижний Тагил Ногинск Норильск Новокузнецк Новосибирск Новоуральск Ноябрьск Обнинск Одинцово Омск Орехово-Зуево Орел Оренбург Ош Озёры Павлодар Пенза Пермь Петропавловск Подольск Полоцк Псков Пушкино Пятигорск Радужный Ростов-на-Дону Рязань Рыбинск Ржев Сальск Самара Самарканд Санкт-Петербург Саратов Сергиев Посад Серпухов Севастополь Северодвинск Щербинка Шымкент Слоним Смоленск Солигорск Солнечногорск Ставрополь Сургут Светлогорск Сыктывкар Сызрань Тамбов Ташкент Тбилиси Терек Тихорецк Тобольск Тольятти Томск Троицк Тула Тверь Тюмень Уфа Ухта Улан-Удэ Ульяновск Ургенч Усть-Каменогорск Вёшенская Видное Владимир Владивосток Волгодонск Волгоград Волжск Воркута Воронеж Якутск Ярославль Юдино Жлобин Жуковский Златоуст Зубова Поляна Звенигород
Тип обращения Вопрос Предложение Благодарность Жалоба
Тема обращения Поступление Трудоустройство Обучение Оплата Кадровый резерв Внеучебная деятельность Работа автоматических сервисов университета Другое
* Все поля обязательны для заполнения
Я даю согласие на обработку персональных данных, согласен на получение информационных рассылок от Университета «Синергия» и соглашаюсь c политикой конфиденциальности