АЛКИНЫ —углеводороды, содержащие в молекуле одну ТРОЙНУЮ связь.
Общая формула алкинов: CnH2n-2
Тройная связь является комбинацией из одной σ- и двух π-связей, образуемых двумя sp-гибридизованными атомами углерода. σ-Cвязи, образуемые sp-гибридными орбиталями углерода, располагаются на одной прямой (под углом 1800 друг к другу).
Поэтому молекула ацетилена имеет линейное строение:
Номенклатура алкинов.
Первый член гомологического ряда – этин имеет историческое название:
НС≡СН ацетилен.
По систематической номенклатуре названия ацетиленовых углеводородов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ин:
H-C≡C-H — этИН СН3-С≡С-Н – пропИН и т.д.
Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь (т.е. она может быть не самой длинной).
Виды изомерии алкинов.
1.Изомерия положения тройной связи (начиная с С4Н6):
HC≡C-CH2-CH3 H3C-C≡C-CH3
бутин-1 бутин-2
2.Изомерия углеродного скелета (начиная с С5Н8):
НС≡С-СН2-СН2-СН3 НС≡С-СН-СН3
∣
СН3
3.Межклассовая изомерия с алкадиенами ( начиная с С3Н4) и циклоалкенами (начиная с С4Н6):
HC≡C-CH2-CH3 СН2=СН-СН=СН2 СН=СН
бутин-1 бутадиен ∣ ∣ циклобутен
СН2-СН2
ПОЛУЧЕНИЕ АЛКИНОВ.
|
1.Пиролиз метана: |
2СН4 —(1500ºС)🡪 C2H2 + 3H2 Реакцию проводят электродуговым способом, пропуская метан между электродами с временем контакта 0,1-0,01 секунды. Столь малое время нагревания обусловлено тем, что ацетилен при такой температуре может разлагаться на углерод и водород. |
|
2.Гидролиз карбида кальция: |
СаО + С -(t)🡪 СаС2 + СО СаС2 + Н2О 🡪 Са(ОН)2 + С2Н2 Карбид кальция образуется при нагревании оксида кальция СаО (жженой извести) и кокса до 2500ºС. При дальнейшем гидролизе выделяется ацетилен. |
|
3. Дегидрогалогенирование дигалогеналканов спиртовым раствором щелочи (щелочь и спирт берутся в избытке). |
R-CH2-CBr2-R + 2KOH —(спирт)🡪 R-C≡C-R + 2H2O + 2 KBr R-CHBr-CHBr-R + 2KOH —(спирт)🡪 R-C≡C-R + 2H2O + 2 KBr |
|
4. Удлинение цепи (алкилирование ацетиленидов) при действии на ацетилениды алкилгалогенидами. |
R-C≡CNa + Br-R’ 🡪 R-C≡C-R’ + NaBr |
СВОЙСТВА АЛКИНОВ
Особенности алкинов:
- π-Электроны более короткой тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью (подвижностью).
- Поэтому реакции ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ к алкинам протекают медленнее, чем к алкенам.
- Алкины с концевой тройной связью (алкины-1) проявляют КИСЛОТНЫЕ СВОЙСТВА и способны, вступая в реакции с активными металлами, образовывать соли.
1. Реакции присоединения.
А. Гидрирование:
В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается вторая π-связь):
При использовании менее активного катализатора [Pd/CaCO3/Pb(CH3COO)2] гидрирование останавливается на стадии образования алкенов.
Б. Галогенирование:
Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для алкенов (первая π-связь разрывается труднее, чем вторая):
Алкины обесцвечивают бромную воду (качественная реакция).
В. Гидрогалогенирование.
Присоединение галогеноводородов также идет по электрофильному механизму. Продукты присоединения к несимметричным алкинам определяются правилом Марковникова:
Г. Гидратация (реакция Кучерова):
Присоединение воды в присутствии катализатора соли ртути (II) идет через образование неустойчивого енола, который изомеризуется в альдегид или кетон.
Если гидратации подвергается АЦЕТИЛЕН, то образуется уксусный альдегид.
Из всех остальных алкинов при гидратации образуются кетоны (так как присоединение протекает по правилу Марковникова).
2. Димеризация и тримеризация алкинов.
1) Димеризация под действием водно-аммиачного раствора CuCl:
2) Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского):
3. Кислотные свойства алкинов с концевой тройной связью.
Образование солей: концевые атомы водорода у ацетилена и алкинов-1 могут замещаться атомами металла. При этом образуются соли – ацетилениды:
СН3-С≡С-Н + NaNH2 🡪 СН3-С≡С-Na + NH3
амид натрия ацетиленид натрия
При взаимодействии ацетилена (или R–C≡C–H) с аммиачными растворами оксида серебра или хлорида меди (I) выпадают осадки нерастворимых ацетиленидов:
HC≡CH + 2[Cu(NH3)2]OH 🡪 CuC≡CCu + 4NH3 + 2H2O
Образование серовато-белого осадка ацетиленида серебра (или красно-коричневого — ацетиленида меди) служит качественной реакцией на концевую тройную связь.
AgC≡CAg + Н2О – реакция не идет
AgC≡CAg + 2НСl 🡪 НC≡CН + 2АgCl
- Окисление алкинов:
Алкины обесцвечивают раствор KMnO4, что используется для их качественного определения.
1) Ацетилен окисляется раствором перманганата калия до соли щавелевой кислоты – оксалата калия (в нейтральной среде) или до щавелевой кислоты (кислая среда):
3НС≡СН + 8KMnO4 + 4H2O 🡪 3НООС-СООН + 8MnO2↓+ 8KOH
щавелевая кислота
3НС≡СН + 8KMnO4 🡪 2K2C2O4 + 8MnO2 ↓+ 2KOH + 2H2O
оксалат калия
2) Алкины окисляются перманганатом калия с расщеплением тройной связи и образованием карбоновых кислот:
5С2Н2 + 8KMnO4 + 12Н2SО4 🡪 5НООС-СООН + 8MnSO4 + 4K2SO4 + 12H2O
5R-C≡СН + 8KMnO4 + 12Н2SО4 🡪 5R-СООН + 5CO2 + 8MnSO4 + 4K2SO4 + 12H2O
5R-C≡С-R1 + 6KMnO4 + 9Н2SО4 🡪 5R-СООН + 5R1-COOH +6MnSO4 +3K2SO4 + 4H2O
14605. Из предложенного перечня выберите два вещества, взаимодействует с ацетиленом.
1. сульфат меди(II)2. азот3. вода4. гидроксид натрия (р-р)5. кислород

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 14605.
14603. Из предложенного перечня выберите два реактива, с каждым из которых при обычных условиях реагирует как ацетилен, так и этилен.
1. аммиачный раствор Ag2O2. оксид углерода(IV)3. оксид натрия4. водород5. хлорная вода

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 14603.
14591. Из предложенного перечня выберите два вещества, которые обесцвечивают бромную воду.
1. этин2. хлорэтан3. пропан4. пропен5. гексан

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 14591.
14584. Из предложенного перечня выберите две пары веществ, каждое из которых реагирует с раствором перманганата калия.
1. бутин-1 и бутин-22. 2-метилпентан и 2-метилгексан3. циклогексан и гексан4. этилен и бутан5. дивинил и пентен-1

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 14584.
14582. Из предложенного перечня выберите два вещества, которые вступают в реакцию гидратации.
1. циклобутан2. ацетилен3. 1,2-диметилбензол4. циклогексен5. толуол

P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 14582.
Для вас приятно генерировать тесты, создавайте их почаще
Всего: 140 1–20 | 21–40 | 41–60 | 61–80 | 81–100 | 101–120 …
Добавить в вариант
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) уксусная кислота и этанол
Б) бутин-1 и бутин-2
В) метан и пропилен
Г) этилен и ацетилен
РЕАКТИВ
1)
2) лакмус
3) фенолфталеин
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: ЕГЭ по химии 2021. Досрочная волна. Вариант 1
Задания Д18 № 651
Ацетилен будет реагировать с каждым из веществ, указанных в ряду:
1)
2)
3)
4)
5)
6)
Жидкое органическое вещество не смешивается с водой, но обесцвечивает бромную воду и раствор перманганата калия. Формула вещества
1) С5Н12
2) С6Н5СН=СН2
3) С6Н6
4) С2Н5ОН
Какое из указанных веществ при взаимодействии с водой в присутствии солей ртути образует альдегид?
1) бутин-2
2) этин
3) бутин-1
4) пропин
Источник: ЕГЭ по химии 10.06.2013. Основная волна. Урал. Вариант 2
В схеме превращений
веществом Х является
1)
2)
3)
4)
Источник: Демонстрационная версия ЕГЭ—2014 по химии
Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ВЕЩЕСТВА
А) пропанон и пропанол-2
Б) анилин и триэтиламин
В) пентин-2 и этилацетат
Г) бензол и гексен-2
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Демонстрационная версия ЕГЭ—2014 по химии
Для этина характерна(-о)
1) реакция этерификации
2) наличие двойной связи в молекуле
3) реакция изомеризации
4) взаимодействие с
5) реакция гидрирования
6) реакция тримеризации
Источник: ЕГЭ по химии 24.04.2014. Досрочная волна. Вариант 2
Некоторый углеводород содержит 12,19% водорода по массе. Молекула этого углеводорода содержит один четвертичный атом углерода. Установлено, что этот углеводород может взаимодействовать с аммиачным раствором оксида серебра с образованием бурого осадка. На основании этих данных:
1) установите простейшую формулу углеводорода,
2) составьте его структурную формулу,
3) приведите уравнение реакции его взаимодействия с аммиачным раствором оксида серебра.
Источник: Типовые тестовые задания по химии, под редакцией Ю. Н. Медведева. 2015 г.
Бутанон образуется при взаимодействии воды с
1) бутаном
2) бутеном-1
3) бутином-2
4) бутанолом-2
Установите соответствие между реагирующими веществами и углеродосодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберитесоответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) пропанол-1 и оксид меди (II)
Б) пропанол-2 и оксид меди (II)
В) пропанол-2 и муравьиная кислота
Г) пропин и вода
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) пропаналь
2) ацетон
3) пропен
4) изопропанол
5) пропилацетат
6) изопропилформиат
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: Типовые тестовые задания по химии под редакцией Ю. Н. Медведева. 2016 г.
Установите соответствие между парами веществ и реагентом, с помощью которых их можно различить: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГЕНТ
1)
2)
3) фенолфталеин
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Установите соответствие между реагирующими веществами и продуктом, который преимущественно образуется в реакции между ними: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Установите соответствие между формулой углеводорода и формулой органического продукта, который преимущественно образуется при взаимодействии углеводорода с водой (в присутствии необходимого катализатора): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
ФОРМУЛА ПРОДУКТА ВЗАИМОДЕЙСТВИЯ С ВОДОЙ
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Установите соответствие между названием углеводорода и формулой органического продукта его взаимодействия с подкисленным раствором перманганата калия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
УГЛЕВОДОРОД
А) пропин
Б) толуол
В) бутен-1
Г) этилбензол
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам.
Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЕДИНЕНИЯ
А) бутин
Б) циклогексен
В) бутадиен-1,2
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Установите соответствие между названием соединения и общей формулой гомологического ряда, к которому оно принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ СОЕДИНЕНИЯ
А) бутан
Б) бутин-1
В) циклогексан
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
Источник: РЕШУ ЕГЭ
Из предложенного перечня выберите два утверждения, которые характерны для этина.
1) линейное строение молекулы
2) sp2-гибридизация орбиталей атомов углерода
3) двойная связь между атомами углерода
4) неполярная связь между атомом углерода и атомом водорода
5) наличие двух -связей между атомами углерода
Запишите в поле ответа номера выбранных утверждений.
Источник: РЕШУ ЕГЭ
Изомерами пентина-1 являются
1) пентен-1
2) циклопентан
3) пентадиен-1,3
4) изопрен
5) дивинил
Запишите номера выбранных ответов.
В качестве мономеров для синтеза высокомолекулярных соединений используют:
1) пропен
2) бутин-1
3) толуол
4) бутадиен-1,3
5) пентадиен-1,4
Запишите номера выбранных ответов.
Перманганат калия в кислой среде реагирует с каждым из двух углеводородов:
1) гексаном и гексеном-1
2) пропином и толуолом
3) этилбензолом и бутеном-2
4) бензолом и этиленом
5) бензолом и бутином-2
Запишите номера выбранных соединений.
Всего: 140 1–20 | 21–40 | 41–60 | 61–80 | 81–100 | 101–120 …
АЛКИНЫ —углеводороды, содержащие в молекуле
одну ТРОЙНУЮ связь.
Общая формула алкинов: CnH2n-2
Тройная связь является комбинацией из одной σ-
и двух π-связей,
образуемых двумя sp-гибридизованными атомами углерода. σ-Cвязи,
образуемые sp-гибридными орбиталями углерода, располагаются на одной
прямой (под углом 1800 друг к другу).
Поэтому молекула ацетилена имеет линейное строение:
Номенклатура алкинов.
Первый член гомологического ряда – этин имеет историческое название:
НС≡СН ацетилен.
По систематической номенклатуре названия ацетиленовых углеводородов производят
от названий соответствующих алканов (с тем же числом атомов углерода) путем
замены суффикса –ан на –ин:
H—C≡C—H — этИН
СН3-С≡С-Н – пропИН и т.д.
Главная цепь выбирается таким образом, чтобы она обязательно включала в себя
тройную связь (т.е. она может быть не самой длинной).
Виды изомерии алкинов.
1.Изомерия
положения тройной связи (начиная с С4Н6):
HC≡C-CH2-CH3
H3C-C≡C-CH3
бутин-1
бутин-2
2.Изомерия
углеродного скелета (начиная с С5Н8):
НС≡С-СН2-СН2-СН3
НС≡С-СН-СН3
∣
СН3
3.Межклассовая
изомерия с алкадиенами ( начиная с С3Н4) и
циклоалкенами (начиная с С4Н6):
HC≡C—CH2—CH3 СН2=СН-СН=СН2
СН=СН
бутин-1 бутадиен ∣ ∣ циклобутен
СН2-СН2
ПОЛУЧЕНИЕ АЛКИНОВ.
|
1.Пиролиз |
Реакцию |
|
2.Гидролиз |
СаО СаС2 Карбид |
|
3. Дегидрогалогенирование |
R—CH2—CBr2—R + 2KOH —(спирт)à R—C≡C—R + R—CHBr—CHBr—R + 2KOH —(спирт)à R—C≡C—R + |
|
4. |
R-C≡CNa + Br-R’ |
СВОЙСТВА АЛКИНОВ
Особенности алкинов:
1. π-Электроны
более короткой тройной связи прочнее удерживаются ядрами атомов углерода и обладают
меньшей поляризуемостью (подвижностью).
2. Поэтому
реакции ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ к алкинам протекают медленнее,
чем к алкенам.
3. Алкины с
концевой тройной связью (алкины-1) проявляют КИСЛОТНЫЕ СВОЙСТВА
и способны, вступая в реакции с активными металлами, образовывать соли.
1. Реакции присоединения.
А. Гидрирование:
В
присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с
образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается
вторая π-связь):
При
использовании менее активного катализатора [Pd/CaCO3/Pb(CH3COO)2]
гидрирование останавливается на стадии образования алкенов.
Б. Галогенирование:
Электрофильное
присоединение галогенов к алкинам протекает медленнее, чем для алкенов (первая
π-связь разрывается труднее, чем вторая):
Алкины обесцвечивают бромную воду (качественная реакция).
В. Гидрогалогенирование.
Присоединение
галогеноводородов также идет по электрофильному механизму. Продукты присоединения к несимметричным алкинам
определяются правилом Марковникова:
Г. Гидратация (реакция Кучерова):
Присоединение воды в присутствии катализатора
соли ртути (II) идет через образование неустойчивого
енола, который изомеризуется в альдегид или кетон.
Если
гидратации подвергается АЦЕТИЛЕН, то образуется уксусный альдегид.
Из
всех остальных алкинов при гидратации образуются кетоны (так как присоединение
протекает по правилу Марковникова).
2. Димеризация и тримеризация алкинов.
1)
Димеризация
под действием водно-аммиачного раствора CuCl:
2) Тримеризация ацетилена над активированным
углем приводит к образованию бензола (реакция Зелинского):
3. Кислотные свойства алкинов с концевой
тройной связью.
Образование солей: концевые атомы
водорода у ацетилена и алкинов-1 могут замещаться атомами металла. При этом
образуются соли – ацетилениды:
СН3-С≡С-Н + NaNH2 à СН3-С≡С-Na + NH3
амид натрия ацетиленид натрия
При взаимодействии ацетилена (или R–C≡C–H) с аммиачными растворами оксида
серебра или хлорида меди (I) выпадают осадки нерастворимых ацетиленидов:
HC≡CH + 2[Cu(NH3)2]OH à CuC≡CCu + 4NH3 + 2H2O
Образование серовато-белого
осадка ацетиленида серебра (или красно-коричневого — ацетиленида меди) служит качественной
реакцией на концевую тройную связь.
AgC≡CAg + Н2О
– реакция не идет
AgC≡CAg + 2НСl à НC≡CН + 2АgCl
4. Окисление
алкинов:
Алкины обесцвечивают
раствор KMnO4, что используется для их качественного определения.
1)
Ацетилен окисляется раствором перманганата калия до соли щавелевой кислоты –
оксалата калия (в нейтральной среде) или до щавелевой кислоты (кислая среда):
3НС≡СН
+ 8KMnO4 + 4H2O à 3НООС-СООН + 8MnO2↓+ 8KOH
щавелевая кислота
3НС≡СН
+ 8KMnO4 à 2K2C2O4 + 8MnO2 ↓+ 2KOH + 2H2O
оксалат калия
2)
Алкины окисляются перманганатом калия с расщеплением тройной связи и образованием
карбоновых кислот:
5С2Н2 + 8KMnO4 + 12Н2SО4 à 5НООС-СООН + 8MnSO4 + 4K2SO4 + 12H2O
5R—C≡СН + 8KMnO4 + 12Н2SО4 à 5R-СООН + 5CO2 + 8MnSO4 + 4K2SO4 + 12H2O
5R—C≡С-R1 + 6KMnO4 + 9Н2SО4 à 5R-СООН + 5R1—COOH +6MnSO4 +3K2SO4 + 4H2O
АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ.
Это
циклические углеводороды с тремя двойными сопряженными связями в цикле.

– родоначальник ароматических углеводородов. Впервые выделен Фарадеем в 1825г
из светильного газа.
Каждый из шести атомов углерода в его молекуле находится в состоянии sp2-гибридизации
и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. Валентные
углы между каждой парой π-связей равны 1200.
Таким образом, скелет σ-связей представляет собой правильный шестиугольник, в
котором все атомы углерода и все σ-связи С–С и С–Н лежат в одной плоскости.
р-Электроны всех атомов углерода образуют единое циклическое π-электронное
облако, сосредоточенное над и под плоскостью кольца.
Все связи С–С в бензоле равноценны, их длина равна 0,140 нм, что соответствует
промежуточному значению между одинарной и двойной.
Это означает, что в молекуле бензола между углеродными атомами нет чисто
простых и двойных связей (как в формуле, предложенной в 1865
г. немецким химиком Ф.Кекуле), а все они выровнены (делокализованы).
Общая формула гомологического ряда бензола CnH2n-6
(n ≥ 6).
|
Вещество |
Название |
Историческое |
|
С6Н5-СН3 |
метилбензол |
Толуол |
|
С6Н5-СН2-СН3 |
этилбензол |
— |
|
СН3-С6Н4-СН3 |
диметилбензол |
ксилол |
|
С6Н5-СН(СН3)2 |
изопропилбензол |
кумол |

Если радикалов два или более, их положение указывается номерами атомов углерода
в кольце, с которыми они связаны. Кольцо нумерют так, чтобы номера радикалов
были наименьшими.
Для дизамещенных бензолов
R-C6H4-R‘
используется также другой способ построения названий:
орто— (о-) заместители у соседних атомов углерода
кольца, 1,2-;
мета— (м-) заместители через один атом углерода
(1,3-);
пара-(п-) заместители на противоположных сторонах
кольца(1,4-).
Изомерия у аренов.
Определяется числом заместителей, их расположением в бензольном кольце и возможностью
изомерии углеродного скелета в заместителях, содержащих более трёх атомов углерода.

существуют 4 изомера: орто-, мета- и пара-ксилолы и этилбензол.
ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
1. Дегидрирование циклоалканов
2. Дегидроциклизация (дегидрирование и циклизация) алканов в присутствии
катализатора

3.Тримеризация ацетилена над активированным
углем (реакция Зелинского):

4.Алкилирование бензола галогеналканами в присутствии
безводного хлорида алюминия или алкенами:
ФИЗИЧЕСКИЕ СВОЙСТВА.
Бензол
и его ближайшие гомологи – бесцветные жидкости с характерным запахом, с
плотностью менее 1 г/мл. Огнеопасны. Нерастворимы в воде, но хорошо растворимы
в неполярных растворителях. Бензол и толуол ядовиты (поражают почки, печень, костный
мозг, кровь).
Высшие арены – твердые вещества.
ХИМИЧЕСКИЕ СВОЙСТВА.
Из-за наличия делокализованой -системы арены мало характерны
реакции присоединения или окисления, которые ведут к нарушению ароматичности.
Для них наиболее характерны реакции электрофильного замещения атомов
водорода, связанных с циклом — SЕ.
1. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
В
реакции присоединения, приводящие к разрушению ароматической структуры бензольного
кольца, арены могут вступать с большим трудом.
а. Гидрирование. Присоединение водорода к
бензолу и его гомологам происходит при повышенной температуре и давлении в
присутствии металлических катализаторов.
б. Радикальное хлорирование. При радикальном
хлорировании бензола получается гексахлорциклогексан — «гексахлоран»
(средство борьбы с вредными насекомыми).
2. РЕАКЦИИ РАДИКАЛЬНОГО ЗАМЕЩЕНИЯ АТОМОВ ВОДОРОДА В БОКОВОЙ
ЦЕПИ:
В
случае гомологов бензола при действии хлора на свету или при нагревании
происходит реакция радикального замещения в боковой цепи:
3. Реакции
окисления аренов
Бензол
не окисляется даже под действием сильных окислителей (KMnO4, K2Cr2O7
и т.п.). Поэтому он часто используется как инертный растворитель при проведении
реакций окисления других органических соединений.
В отличие от бензола его гомологи окисляются довольно легко. При действии
раствора KMnO4 в кислой среде и нагревании в гомологах бензола
окислению подвергаются только боковые цепи, при этом от боковой цепи остаётся
карбоксильная группа, а остальное – переходит в углекислый газ:
5С6Н5—СН3 +6КМnO4+9H2SO4
à5C6H5—COOH +6MnSO4+3K2SO4+14H2O
5С6Н5—CH2—CH3
+12КМnO4+18H2SO4à5C6H5—COOH +5СО2+12MnSO4+
+6K2SO4+28H2O
Если
окисление идёт в нейтральном растворе при нагревании, то образуется соль
бензойной кислоты и карбонат калия:
С6Н5—СН2—СН3+4KMnO4àC6H5 – COOK+K2CO3+4MnO2+KOH+2H2O
4.РЕАКЦИИ ЗАМЕЩЕНИЯ В БЕНЗОЛЬНОМ КОЛЬЦЕ
1. Галогенирование
Замещение
атома водорода в бензольном кольце на галоген происходит в присутствии
катализаторов AlCl3, AlBr3, FeCl3 и т.п.:
2. Нитрование
Бензол
реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот):
3.
Алкилирование
Замещение
атома водорода в бензольном кольце на алкильную группу(алкилирование)
происходит под действием алкилгалогенидов в присутствии катализаторов
AlCl3, FeBr3или алкенов в присутствии фосфорной кислоты:
ЗАМЕЩЕНИЕ В
АЛКИЛБЕНЗОЛАХ
Гомологи бензола (алкилбензолы) более активно вступают в реакции замещения по
сравнению с бензолом. Например, при нитровании толуола С6Н5-CH3
может происходить замещение не одного, а трех атомов водорода с образованием
2,4,6-тринитротолуола, причём в орто- и пара- положениях:
ОРИЕНТИРУЮЩЕЕ ДЕЙСТВИЕ ЗАМЕСТИТЕЛЕЙ
В БЕНЗОЛЬНОМ КОЛЬЦЕ.
Если в
бензольном кольце имеются заместители, не только алкильные, но и
содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции
замещения атомов водорода в ароматической системе протекают строго определенным
образом, в соответствии с характером влияния заместителя на ароматическую
π-систему.
Заместители подразделяют на две группы в зависимости от проявляемого ими
эффекта (мезомерного или индуктивного): электронодонорные (первого рода) и
электроноакцепторные (второго рода).
ЭЛЕКТРОНОДОНОРНЫЕ ЗАМЕСТИТЕЛИ проявляют
повышают электронную плотность в сопряженной системе.
К ним относятся гидроксильная группа —ОН и аминогруппа —NН2. Неподеленная
пара электронов в этих группах вступает в общее сопряжение с p -электронной
системой бензольного кольца и увеличивает длину сопряженной системы. В результате
электронная плотность сосредоточивается в орто-
и пара-положениях:
Алкильные группы не могут участвовать в сопряжении, но они проявляют +I-эффект,
под действием которого происходит аналогичное перераспределение p -электронной
плотности.
Заместители, обладающие +I-эффектом
или +М-эффектом, способствуют электрофильному замещению в орто- и
пара— положениях бензольного кольца и называются заместителями
(ориентантами) первого рода:
Так,
толуол, содержащий заместитель первого рода, нитруется и бромируется в пара- и
орто-положения:
ЭЛЕКТРОНОАКЦЕПТОРНЫЕ ЗАМЕСТИТЕЛИ снижают
электронную плотность в сопряженной системе.
К ним относятся нитрогрупла —NO2, сульфогруппа —SO3Н,
альдегидная —СНО и карбоксильная —СООН группы. Эти заместители образуют с
бензольным кольцом общую сопряженную систему, но общее электронное облако
смещается в сторону этих групп. Таким образом, общая электронная плотность в
кольце уменьшается, но меньше всего она уменьшается в
мета-положениях:
Полностью галогенизированные алкильные радикалы (например, —ССl3)
проявляют -I-эффект и также способствуют понижению электронной плотности кольца.
Заместители, обладающие -I-эффектом или
-М-эффектом, направляют электрофильное замещение в мета-положения
бензольного кольца и называются заместителями (ориентантами) второго
рода:
Нитробензол, содержащий заместитель второго рода, нитруется и бромируется в мета-положение:

СТИРОЛ (винилбензол) С8Н8
–
производное бензола, которое имеет в своём составе двойную связь в боковом заместителе, поэтому он НЕ
относится к гомологическому ряду аренов.
Получение стирола:
1. Дегидрирование
этилбензола: С6Н5-СН2-СН3 -(t,кат)à C6H5—CH=CH2 + H2
2. Дегидрогалогенирование
фенилбромэтана:
C6H5-CH-CH3
+KOH –(спирт) à C6H5-CH=CH2
+KBr +H2O
│
Br
Свойства стирола:
Стирол проявляет свойства, характерные для алкенов – реакции
присоединения, окисления, полимеризации.
Реакции
присоединения к стиролу: протекают в соответствии с правилом
Марковникова.
С6Н5-СН=СН2
+Н2О à С6Н5-СН-СН3
│
ОН
Мягкое
окисление стирола:
3С6Н5-СН=СН2
+2 KMnO4 + 4Н2О
à3 С6Н5-СН-СН2
+ 2MnO2 + 2KOH
│ │
OH OH фенилэтиленгликоль
Жесткое
окисление стирола:
С6Н5-СН=СН2
+ 2KMnO4 + 3Н2SO4 à С6Н5-СOOН + CO2 + 2MnSO4 + K2SO4 + 4H2O
бензойная кислота
3С6Н5-СН=СН2
+ 10KMnO4 —toà 3С6Н5-СOOК + 3К2CO3 + 10MnO2 + KOH+ 4Н2О
бензоат калия
Полимеризация
стирола:
в результате получают полистирол.
…
В настоящем разделе представлены задачи по теме Алкины с готовыми решениями: изомерия, номенклатура, способы получения и свойства.
1)Напишите структурные формулы следующих алкинов: а) 4-этил-2-гексин; б) 4-метил-4-изобутил-1-децин; в) 5,10-диметил-5-изобутил-2-додецин; г) 3,7-диметил-6-изопропил-4-децин; д) 1,5-гексадиин; е) 2-метил-винилацетилен;
Показать решение »
2)Назовите по систематической номенклатуре ИЮПАК соединение:
Показать решение »
Нумеруем самую длинную углерод-углеродную цепь, начиная с того конца, к которому ближе расположена тройная связь:
Данное соединение относится к классу алкинов, поэтому корень соединения —ундец, суффикс – ин. Тройная связь расположена во втором положении, поэтому – 2-ундецин
Теперь рассмотрим, какие заместители присутствуют в этом соединении:
- При четвертом атоме углерода расположена изопропильная группа, следовательно, прибавляем 4-изопропил;
- При шестом атоме углерода расположена более сложная группа, не имеющая тривиального названия, поэтому назовем ее отдельно:
Самая длинная цепь состоит из трех атомов углерода, все связи насыщенные. В первом и втором положении находятся две метильные группы (при их нумерации используем обозначения, отличающиеся от обозначения главной цепи, например, 1`, 2`). Таким образом, данная группа называется — 1`, 2`- диметилпропил.
Теперь дадим полное название соединению по систематической номенклатуре ИЮПАК:
4-изопропил-6-(1`, 2`- диметилпропил)-2-ундецин
3)Волокно виньон используют для изготовления рыболовных сетей, электроизоляции и др. Его получают сополимеризацией хлористого винила с винилацетатом. Напишите уравнения реакций получения винилхлорида и винилацетата, исходя из ацетилена, уксусной кислоты и хлороводорода, а также схему реакции сополимеризации хлорвинила с винилацетатом.
Показать решение »
4)Образец индивидуального газообразного вещества может быть этаном, этиленом, ацетиленом. Каким образом качественно можно установить природу этого газа? Охарактеризуйте углерод-углеродные связи в этом ряду соединений.
Показать решение »
Для того, чтобы доказать присутствие этилена можно воспользоваться реакцией его взаимодействия с бромной водой. При этом происходит обесцвечивание раствора брома (в этом случае выделение бромоводорода не должно наблюдаться):
Часто применяется качественная реакция окисления алкенов нейтральным раствором перманганата калия до гликолей; при этом малиновый цвет перманганата меняется на бурый цвет МnO2:
Реакция с солями меди (I) очень чувствительна на присутствие ацетилена в газовой фазе. При пропускании ацетилена в бесцветный аммиачный раствор ацетата меди (I) образуется красновато-коричневый или фиолетовый аморфный осадок карбида меди (Cu2C2).
Этан химически инертен. Его можно определить по отсутствию реакций с перманганатом калия и солями меди (I). Этан с этими веществами не реагирует.
Углерод-углеродные связи алканов представлены в разделе Строение и физические свойства алканов; связи алкенов – в разделе Строение, изомерия и номенклатура алкенов; связи алкинов – в разделе Строение алкинов, а также в задаче 5 данного раздела.
5)Нарисуйте схемы образования σ- и π-связей для соединений: а) метилацетилена; б) винилацетилена; в) диметилацетилена. Обозначьте валентные состояния атомов углерода, виды σ — и π -связей и углы между направлениями σ-связей. Какие эффекты взаимного влияния атомов возникают в молекулах этих веществ?
Показать решение »
σ-Связь – это ковалентная связь, возникшая при перекрывании s-, p- и гибридных атомных орбиталей вдоль оси, проходящей через центры ядер связываемых атомов (осевое перекрывание).
π-Связь – это ковалентная связь, образованная боковым перекрытием негибридных р-орбиталей. Такое перекрывание происходит вне оси, соединяющей ядра атомов.
Рассмотрим виды гибридизаций, характерных для атома углерода органических соединений.
sp-Гибридизация
Тройная связь включает одну σ- и две π-связи, образуемые двумя sp-гибридизованными атомами углерода.
σ-Связь возникает при осевом перекрывании sp-гибридизованных орбиталей двух расположенных рядом атомов углерода;
одна из π-связей образуется при боковом перекрывании рy-орбиталей, другая – при боковом перекрывании рz-орбиталей. π-Cвязи находятся во взаимно перпендикулярных плоскостях.
Образование связей на примере молекулы ацетилена H–C≡C–H можно изобразить в виде схемы:
C≡C σ-связь (перекрывание 2sp-2sp);
π-связь (2рy-2рy);
π-связь (2рz-2рz);
С–Н σ-связь (перекрывание 2sp-орбиталей углерода и 1s-орбитали водорода).
sp2-Гибридизация
Двойная связь включает одну σ- и одну π-связи.
σ-Связь возникает при осевом перекрывании sp2-гибридизованных орбиталей, а π-связь – при боковом перекрывании р-орбиталей двух соседних гибридных атомов углерода. σ-Связи, образованные sp2-гибридными атомными орбиталями, лежат в одной плоскости под углом 120°. По своей природе π-связь резко отличается от σ-связи: π-связь менее прочная из-за меньшей эффективности перекрывания р-орбиталей.
Образование связей в молекуле этилена можно изобразить следующей схемой:
С=С σ-связь (перекрывание 2sp2-2sp2) и π-связь (2рz-2рz)
С–Н σ-связь (перекрывание 2sp2— орбиталей углерода и 1s-орбитали водорода).
sp3-Гибридизация (тетраэдрическая)
При гибридизации одной s- и три р-орбиталей образуются четыре равноценных по форме и энергии sp3-гибридные орбитали. Оси sp3-гибридизованных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28′, что соответствует наименьшей энергии отталкивания электронов.
Для атома углерода и других элементов 2-го периода этот процесс может быть представлен в виде следующей схемы:
2s + 2px + 2py + 2pz = 4 (2sp3)
Теперь рассмотрим конкретные соединения из задачи.
а) Метилацетилен
В молекуле метилацетилена проявляются положительные индуктивный и мезомерный эффекты.
б) Винилацетилен
В молекуле винилацетилена проявляются положительные индуктивный и мезомерный эффекты.
в)Диметилацетилен
В молекуле диметилацетилена проявляются положительные индуктивный и мезомерный эффекты.
6)Волокно нитрон ближе всех других синтетических волокон приближается по свойствам к натуральной шерсти. Материал для него получают полимеризацией акрилонитрила, который синтезируют из ацетилена и синильной кислоты. Охарактеризуйте виды связей в молекуле этого соединения. Напишите уравнение реакции получения акрилонитрила и схему его полимеризации.
Показать решение »
В акрилонитриле присутствует два вида связей: ковалентная полярная (С – N, C – H) и ковалентная неполярная (C – C). Шесть σ-связей и три π-связи.
7)Получите 3-метилпептин-1 двумя способами и составьте для него уравнения реакций: а) с водой в присутствии катализатора (реакция Кучерова); б) с аммиачным раствором оксида серебра; в) с бутанолом-2; г) с уксусной кислотой. Все вещества назовите.
Показать решение »
Получить алкины можно, например, путем дегалогенирования дигалогенпроизводных (1) или алкилирования солей ацетиленовых углеводородов (2):
Составим схемы уравнений реакций полученного 3-метилпентина-1 с H2O (Hg2+) – реакция Кучерова, с аммиачным раствором Ag2O, с C4H9OH, c CH3COOH:
8)Напишите уравнения реакций, с помощью которых можно осуществлять следующие превращения: а) бутина-1 в изопропилэтилацетилен; б) 3,3-диметилбутена-1 в 3,3-диметилбутин-1; в) пентина-1 в пентин-2.
Показать решение »
В реакции а) Изопропилэтилацетилен можно получить из бутина-1 с помощью реакций замещения водородного атома при тройной связи на металлический натрий (в жидком аммиаке). Далее, при прибавлении 2-хлорпропана получается изопропилэтилацетилен.
В реакциях б) и в) нужные продукты реакции можно получить путем присоединения молекулы галогена (б) или галогенводорода (в) и последующем отщеплением HCl от полученного галогенпроизводного:
Подробнее о способах получения алкинов и способах их получения смотрите в разделах Получение алкинов и Свойства алкинов
Алкины.
1.
Из
предложенного перечня выберите два вещества, которые являются структурными
изомерами бутена-1.
1) бутан
2) циклобутан
3) бутин-2
4) бутадиен-1,3
5) метилпропен
2.
Из
предложенного перечня выберите два вещества, которые являются структурными
изомерами гексена-2.
1) циклогексан
2) циклобутан
3) гексан
4) гексен-1
5) 2,3-диметилпентен-2
3.
Из
предложенного перечня выберите два вещества, которые являются изомерами гексина-2.
1) гексадиен-2,4
2) 2-метилбутен-2
3) 3-метилбутин-1
4) циклогексен
5) гексен-2
4. Из предложенного перечня выберите два утверждения, которые
характерны для этина.
1) линейное строение молекулы
2) sp2-гибридизация орбиталей атомов
углерода
3) двойная связь между атомами углерода
4) неполярная связь между атомом углерода и атомом водорода
5) наличие двух -связей
между атомами углерода
5.
Из
предложенного перечня выберите два вещества, для которых алкины
являются структурными изомерами.
1) алкадиен
2) алкан
3) циклоалкан
4) циклоалкен
5) алкен
6.
Из
предложенного перечня выберите два вещества, которые являются
изомерами бутина-1.
1) бутен-1
2) бутан
3) циклобутан
4) бутин-2
5) бутадиен-1,3
7.
Из
предложенного перечня выберите два вещества, у которых есть атомы углерода
в состоянии sp2-гибридизации.
1) ацетон
2) пропанол
3) пропин
4) бутан
5) этилен
8.
Из
предложенного перечня выберите два вещества, которые являются
изомерами циклогексана.
1) 2-метилпентен-2
2) бензол
3) гексен-1
4) циклопентан
5) гексан
9.
Из
предложенного перечня выберите два вещества, которые являются
изомерами гексина-2.
1) гексадиен-2,4
2) 2-метилбутен-2
3) 3-метилбутин-1
4) 3-метилпентин-1
5) гексен-2
10. Из предложенного перечня
выберите два вещества, которые являются изомерами 4,4-диметилпентина-1.
1) 2,3-диметилпентан
2) 3 -этилпентадиен-1,3
3) 2,3-диметилбутан
4) гептадиен-1,3
5) 2,3,3-триметилбутен-1
11. Из предложенного
перечня выберите два ряда веществ, с каждым из которых может реагировать
бутен-1.
1) H2,
Cl2, HCl
2) H2,
N2, Br2
3) Na, NaOH, HCl
4) H2O,
HBr, KMnO4
5) Cl2, CO2, H2SO4
12. Из предложенного
перечня выберите два вещества, в молекулах которых присутствуют две -связи.
1) пропин
2) бутен-1
3) циклобутан
4) пропан
5) ацетилен
13. Из предложенного
перечня выберите два вещества, которые могут реагировать с каждым из веществ:
водой, бромоводородом, водородом.
1) пропан
2) этилен
3) бутен-1
4) этан
5) хлорметан
14. Из предложенного
перечня выберите два вещества, которые склонны вступать в реакцию
присоединения.
1) пропан
2) циклопропан
3) пентан
4) циклогексан
5) этилен
15. Из предложенного
перечня выберите две пары углеводородов, с которыми реагирует хлороводород.
1) пропен и циклопропан
2) бензол и толуол
3) метан и этан
4) этилен и ацетилен
5) бутадиен и бутан
16. Из предложенного
перечня выберите два вещества, с которыми реагируют и пропен, и пропин.
1) KMnO4 (раствор)
2) аммиачный раствор Ag2O
3) Cu(OH)2
4) CuO
5) HCl
17. Из предложенного
перечня выберите два вещества, с которыми реагирует и гексан, и гексен-2.
1) вода
2) кислород
3) водород
4) бромоводород
5) хлор
18. Из предложенного
перечня выберите два вещества, с которыми реагирует бутин-1, в отличие от
бутена-1.
1) калий
2) водород
3) бром
4) аммиачный раствор оксида меди (I)
5) кислород
19. Из предложенного
перечня выберите два вещества, которые реагируют с аммиачным раствором оксида
серебра.
1) пентин-1
2) бутин-2
3) пропен
4) бутин-1
5) циклопропан
20. Из предложенного перечня
выберите два вещества, с которыми реагируют и ацетилен, и этилен при обычных
условиях.
1) оксид натрия
2) хлорная вода
3) аммиачный раствор Ag2O
4) бром
5) калий
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций используйте структурные формулы органических веществ.
6
Решение
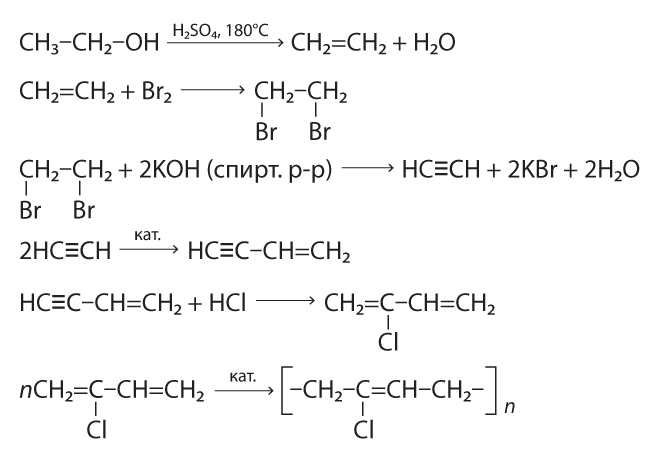
Авторизуйтесь на сайте, чтобы пройти тест.
Следующий вопрос →
Объяснение понятно.
изменить
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
Видео с разбором теста
Обсуждение вопросов по теме теста
Версия для печати
Решаемость этого задания 86%



























