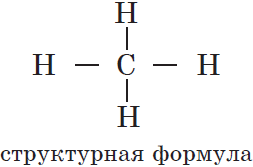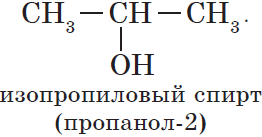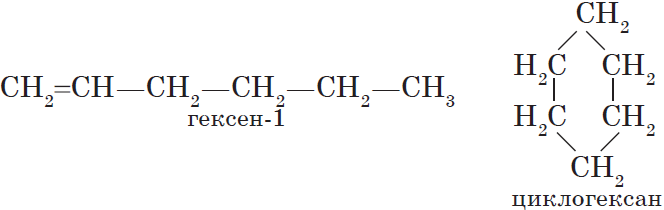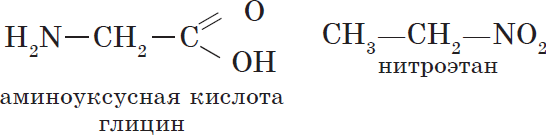Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
Теория химического строения органических соединений А. М. Бутлерова
Подобно тому, как для неорганической химии основой развития являются Периодический закон и Периодическая система химических элементов Д. И. Менделеева, для органической химии основополагающей стала теория строения органических соединений А. М. Бутлерова.
Основным постулатом теории Бутлерова является положение о химическом строении вещества, под которым понимается порядок, последовательность взаимного соединения атомов в молекулы, т.е. химическая связь.
Под химическим строением понимают порядок соединения атомов химических элементов в молекуле согласно их валентности.
Этот порядок может быть отображен при помощи структурных формул, в которых валентности атомов обозначаются черточками: одна черточка соответствует единице валентности атома химического элемента. Например, для органического вещества метана, имеющего молекулярную формулу $СН_4$, структурная формула выглядит так:
Основные положения теории А. М. Бутлерова
- Атомы в молекулах органических веществ связаны друг с другом согласно их валентности. Углерод в органических соединениях всегда четырехвалентен, а его атомы способны соединяться друг с другом, образуя различные цепи.
- Свойства веществ определяются не только их качественным и количественным составом, но и порядком соединения атомов в молекуле, т. е. химическим строением вещества.
- Свойства органических соединений зависят не только от состава вещества и порядка соединения атомов в его молекуле, но и от взаимного влияния атомов и групп атомов друг на друга.
Теория строения органических соединений является динамичным и развивающимся учением. По мере развития знаний о природе химической связи, о влиянии электронного строения молекул органических веществ стали пользоваться, кроме эмпирических и структурных, электронными формулами. В таких формулах указывают направление смещения электронных пар в молекуле.
Квантовая химия и химия строения органических соединений подтвердили учение о пространственном направлении химических связей (цис- и трансизомерия), изучили энергетические характеристики взаимных переходов у изомеров, позволили судить о взаимном влиянии атомов в молекулах различных веществ, создали предпосылки для прогнозирования видов изомерии и направления и механизма протекания химических реакций.
Органические вещества имеют ряд особенностей:
- В состав всех органических веществ входят углерод и водород, поэтому при горении они образуют углекислый газ и воду.
- Органические вещества построены сложно и могут иметь огромную молекулярную массу (белки, жиры, углеводы).
- Органические вещества можно расположить в ряды сходных по составу, строению и свойствам гомологов.
- Для органических веществ характерной является изомерия.
Изомерия и гомология органических веществ
Свойства органических веществ зависят не только от их состава, но и от порядка соединения атомов в молекуле.
Изомерия — это явление существования разных веществ — изомеров с одинаковым качественным и количественным составом, т.е. с одинаковой молекулярной формулой.
Различают два вида изомерии: структурную и пространственную (стереоизомерию). Структурные изомеры отличаются друг от друга порядком связи атомов в молекуле; стереоизомеры — расположением атомов в пространстве при одинаковом порядке связей между ними.
Выделяют следующие разновидности структурной изомерии: изомерию углеродного скелета, изомерию положения, изомерию различных классов органических соединений (межклассовую изомерию).
Структурная изомерия
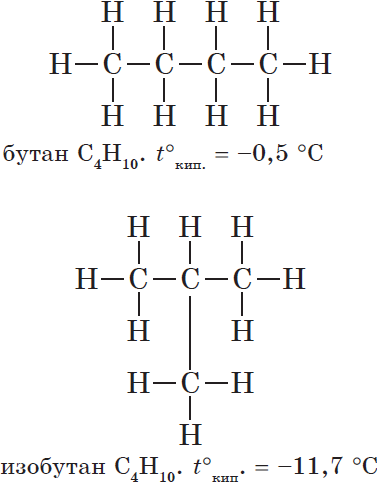
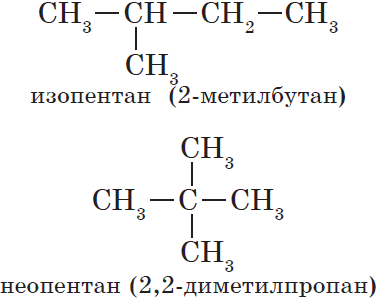
Изомерия углеродного скелета обусловлена различным порядком связи между атомами углерода, образующими скелет молекулы. Как уже было показано, молекулярной формуле $С_4Н_{10}$ соответствуют два углеводорода: н-бутан и изобутан. Для углеводорода $С_5Н_{12}$ возможны три изомера: пентан, изопентан и неопентан:
$СН_3—СН_2—{СН_2}↙{пентан}—СН_2—СН_3$
С увеличением числа атомов углерода в молекуле число изомеров быстро растет. Для углеводорода $С_{10}Н_{22}$ их уже $75$, а для углеводорода $С_{20}Н_{44}$ — $366 319$.
Изомерия положения обусловлена различным положением кратной связи, заместителя, функциональной группы при одинаковом углеродном скелете молекулы:
$CH_2={CH-CH_2}↙{бутен-1}-CH_3$ $CH_3-{CH=CH}↙{бутен-2}-CH_3$
${CH_3-CH_2-CH_2-OH}↙{н-пропиловый спирт(пропанол-1)}$
Изомерия различных классов органических соединений (межклассовая изомерия) обусловлена различным положением и сочетанием атомов в молекулах веществ, имеющих одинаковую молекулярную формулу, но принадлежащих к разным классам. Так, молекулярной формуле $С_6Н_{12}$ соответствует ненасыщенный углеводород гексен-1 и циклический углеводород циклогексан:
Изомерами являются углеводород, относящийся к алкинам, — бутин-1 и углеводород с двумя двойными связями в цепи бутадиен-1,3:
$CH≡C-{CH_2}↙{бутин-1}-CH_2$ $CH_2={CH-CH}↙{бутадиен-1,3}=CH_2$
Диэтиловый эфир и бутиловый спирт имеют одинаковую молекулярную формулу $С_4Н_{10}О$:
${CH_3CH_2OCH_2CH_3}↙{text»диэтиловый эфир»}$ ${CH_3CH_2CH_2CH_2OH}↙{text»н-бутиловый спирт (бутанол-1)»}$
Структурными изомерами являются аминоуксусная кислота и нитроэтан, отвечающие молекулярной формуле $С_2Н_5NO_2$:
Изомеры этого типа содержат различные функциональные группы и относятся к разным классам веществ. Поэтому они отличаются по физическим и химическим свойствам значительно больше, чем изомеры углеродного скелета или изомеры положения.
Пространственная изомерия
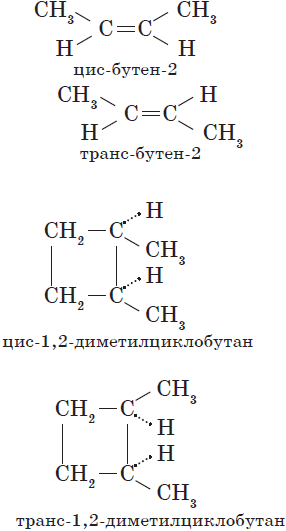
Пространственная изомерия подразделяется на два вида: геометрическую и оптическую. Геометрическая изомерия характерна для соединений, содержащих двойные связи, и циклических соединений. Так как свободное вращение атомов вокруг двойной связи или в цикле невозможно, заместители могут располагаться либо по одну сторону плоскости двойной связи или цикла (цис-положение), либо по разные стороны (транс-положение). Обозначения цис- и транс- обычно относят к паре одинаковых заместителей:
Геометрические изомеры различаются по физическим и химическим свойствам.
Оптическая изомерия возникает, если молекула несовместима со своим изображением в зеркале. Это возможно, когда у атома углерода в молекуле четыре различных заместителя. Этот атом называют асимметрическим. Примером такой молекулы является молекула $α$-аминопропионовой кислоты ($α$-аланина) $СН_3СН(NH_2)COOH$.
Молекула $α$-аланина ни при каком перемещении не может совпасть со своим зеркальным отражением. Такие пространственные изомеры называются зеркальными, оптическими антиподами, или энантиомерами. Все физические и практически все химические свойства таких изомеров идентичны.
Изучение оптической изомерии необходимо при рассмотрении многих реакций, протекающих в организме. Большинство этих реакций идет под действием ферментов — биологических катализаторов. Молекулы этих веществ должны подходить к молекулам соединений, на которые они действуют, как ключ к замку, следовательно, пространственное строение, взаимное расположение участков молекул и другие пространственные факторы имеют для течения этих реакций большое значение. Такие реакции называются стереоселективными.
Большинство природных соединений являются индивидуальными энантиомерами, и их биологическое действие резко отличается от свойств их оптических антиподов, полученных в лаборатории. Подобное различие в биологической активности имеет огромное значение, так как лежит в основе важнейшего свойства всех живых организмов — обмена веществ.
Гомологическим рядом называется ряд веществ, расположенных в порядке возрастания их относительных молекулярных масс, сходных по строению и химическим свойствам, где каждый член отличается от предыдущего на гомологическую разность $CH_2$. Например: $CH_4$ — метан, $C_2H_6$ — этан, $C_3H_8$ — пропан, $C_4H_{10}$ — бутан и т. д.
Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Типы связей в молекулах органических веществ.
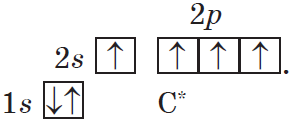
В органических соединениях углерод всегда четырехвалентен. В возбужденном состоянии в его атоме происходит разрыв пары $2s^3$-электронов и переход одного из них на р-орбиталь:
Такой атом имеет четыре неспаренных электрона и может принимать участие в образовании четырех ковалентных связей.
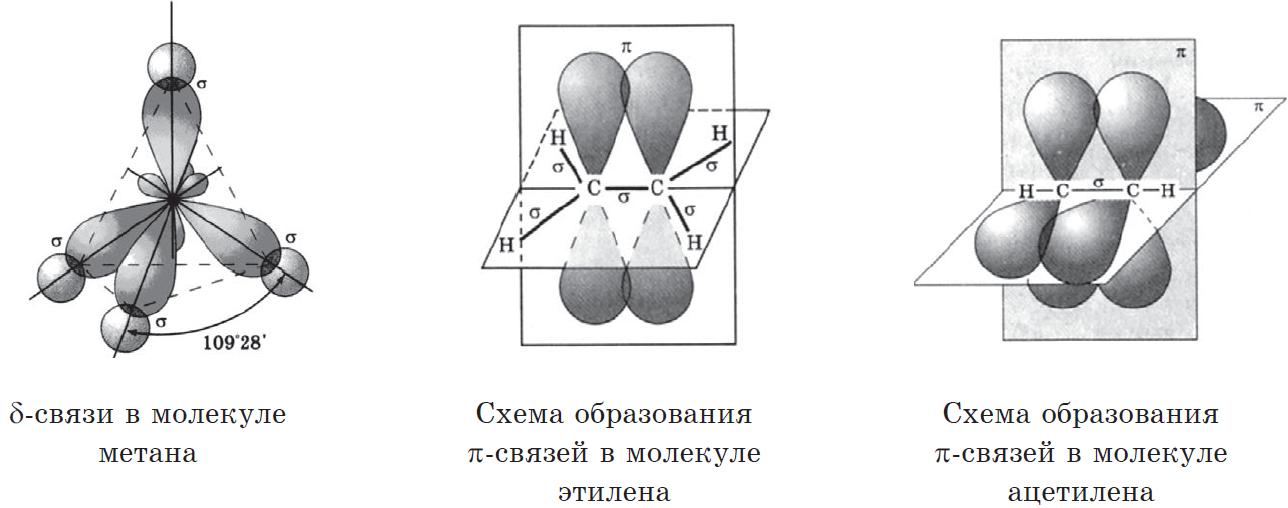
На основании приведенной электронной формулы валентного уровня атома углерода можно было бы ожидать, что на нем находится один $s$-электрон (сферическая симметричная орбиталь) и три $р$-электрона, имеющих взаимно перпендикулярные орбитали ($2р_х, 2р_у, 2p_z$-орбиталь). В действительности же все четыре валентных электрона атома углерода полностью эквивалентны и углы между их орбиталями равны $109°28’$. Кроме того, расчеты показывают, что каждая из четырех химических связей углерода в молекуле метана ($СН_4$) на $25%$ является $s-$ и на $75%$ — $p$-связью, т.е. происходит смешивание $s-$ и $р-$состояний электронов. Это явление называют гибридизацией, а смешанные орбитали — гибридными.
Атом углерода в $sp^3$-валентном состоянии имеет четыре орбитали, на каждой из которых находится по одному электрону. В соответствии с теорией ковалентной связи он имеет возможность образовывать четыре ковалентные связи с атомами любых одновалентных элементов ($СН_4, CHCl_3, CCl_4$) или с другими атомами углерода. Такие связи называются $σ$-связями. Если атом углерода имеет одну $С—С$ связь, то он называется первичным ($Н_3С—СН_3$), если две — вторичным ($Н_3С—СН_2—СН_3$), если три — третичным (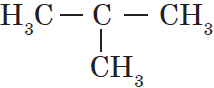
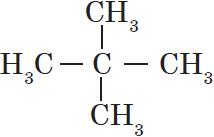
Одной из характерных особенностей атомов углерода является их способность образовывать химические связи за счет обобщения только $р$-электронов. Такие связи называются $π$-связями. $π$-связи в молекулах органических соединений образуются только в присутствии $σ$-связей между атомами. Так, в молекуле этилена $Н_2С=СН_2$ атомы углерода связаны $σ-$ и одной $π$-связью, в молекуле ацетилена $НС=СН$ — одной $σ-$ и двумя $π$-связями. Химические связи, образовавшиеся с участием $π$-связей, называются кратными (в молекуле этилена — двойная, в молекуле ацетилена — тройная), а соединения с кратными связями — ненасыщенными.
Явление $sp^3$-, $sp^2$- и $sp$ — гибридизации атома углерода.
При образовании $π$-связей изменяется гибридное состояние атомных орбиталей атома углерода. Так как образование $π$-связей происходит за счет р-электронов, то в молекулах с двойной связью электроны будут иметь $sp^2$-гибридизацию (была $sp^3$, но один р-электрон отходит на $π$-орбиталь), а с тройной — $sp$-гибридизацию (два р-электрона отошли на $π$-орбиталь). Характер гибридизации изменяет направленность $σ$-связей. Если при $sp^3$-гибридизации они образовывают пространственно разветвленные структуры ($а$), то при $sp^2$-гибридизации все атомы лежат в одной плоскости и углы между $σ$-связями равны $120°$(б), а при $sp$-гибридизации молекула линейна (в):
При этом оси $π$-орбиталей перпендикулярны оси $σ$-связи.
Как $σ$-, так и $π$-связи являются ковалентными, значит, должны характеризоваться длиной, энергией, пространственной направленностью и полярностью.
Характеристики одинарных и кратных связей между атомами С.
| Молекула | Тип гибридизации | Валентный угол | Длина связи, нм | Энергия связи, кДж/моль |
| $CH_3-CH_3$ | $sp^3$ | $109°5’$ | $0.154$ | $369$ |
| $CH_2=CH_2$ | $sp^2$ | $120°$ | $0.134$ | $712$ |
| $CH≡CH$ | $sp^3$ | $180°$ | $0.120$ | $962$ |
Радикал. Функциональная группа.
Одной из особенностей органических соединений является то, что в химических реакциях их молекулы обмениваются не отдельными атомами, а группами атомов. Если эта группа атомов состоит только из атомов углерода и водорода, то она называется углеводородным радикалом, если же она имеет атомы других элементов, то она называется функциональной группой. Так, например, метил ($СН_3$—) и этил ($С_2Н_5$—) являются углеводородными радикалами, а оксигруппа (—$ОН$), альдегидная группа (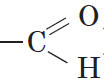
Как правило, функциональная группа определяет химические свойства органического соединения и поэтому является основой их классификации.
| 1 | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ | |
| 1.1 | Современные представления о строении атома | |
| 1.1.1 | Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов. | |
| 1.2 | Периодический закон и периодическая система химических элементов Д.И. Менделеева | |
| 1.2.1 | Закономерности изменения химических свойств элементов и их соединений по периодам и группам периодической таблицы химических элементов. | |
| 1.2.2 | Общая характеристика металлов IА–IIIА групп в связи с их положением в периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | |
| 1.2.3 | Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в периодической системе химических элементов Д.И.Менделеева и особенностям строения их атомов. | |
| 1.3 | Химическая связь и строение вещества | |
| 1.3.1 | Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь. | |
| 1.3.2 | Электроотрицательность. Степень окисления и валентность химических элементов. | |
| 1.3.3 | Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения. | |
| 1.4 | Химическая реакция | |
| 1.4.1 | Классификация химических реакций в неорганической и органической химии. | |
| 1.4.2 | Тепловой эффект химической реакции. Термохимические уравнения. | |
| 1.4.3 | Скорость реакции, ее зависимость от различных факторов. | |
| 1.4.4 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов. | |
| 1.4.5 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. | |
| 1.4.6 | Реакции ионного обмена. | |
| Особенности взаимодействия кислых солей со щелочами. | ||
| 1.4.7 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная. | |
| Необратимый гидролиз бинарных соединений. | ||
| 1.4.8 | Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее. | |
| 1.4.9 | Электролиз расплавов и растворов (солей, щелочей,кислот). | |
| 2 | НЕОРГАНИЧЕСКАЯ ХИМИЯ | |
| 2.1 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная). | |
| 2.2 | Химические свойства простых веществ — металлов | |
| 2.2.1 | Характерные химические свойства щелочных металлов. | |
| 2.2.2 | Характерные химические свойства бериллия, магния и щелочноземельных металлов. | |
| 2.2.3 | Характерные химические свойства алюминия. | |
| 2.2.4 | Химические свойства переходных металлов (меди, цинка, хрома, железа). | |
| 2.3 | Химические свойства простых веществ — неметаллов | |
| 2.3.1 | Химические свойства водорода и галогенов. | |
| 2.3.2 | Химические свойства кислорода и серы. | |
| 2.3.3 | Химические свойства азота и фосфора. | |
| 2.3.4 | Химические свойства углерода и кремния. | |
| 2.4 | Характерные химические свойства оксидов: основных, амфотерных, кислотных. | |
| 2.5 | Характерные химические свойства оснований и амфотерных гидроксидов. | |
| 2.6 | Характерные химические свойства кислот. | |
| 2.7 | Характерные химические свойства солей: средних, кислых, основных, комплексных (на примере соединений алюминия и цинка). | |
| 3 | ОРГАНИЧЕСКАЯ ХИМИЯ | |
| 3.1 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. | |
| 3.2 | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа. | |
| 3.3 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная). | |
| 3.4 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). | |
| 3.5 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола. | |
| 3.6 | Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. | |
| 3.7 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. | |
| 3.8 | Биологически важные вещества: жиры, белки, углеводы (моносахарады, дисахариды, полисахариды) | |
| 3.8.1 | Жиры. | |
| 3.8.2 | Белки. | |
| 3.8.3 | Углеводы (моносахариды, дисахариды, полисахариды). | |
| 3.9 | Взаимосвязь органических соединений. | |
| 4 | МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ | |
| 4.1 | Экспериментальные основы химии | |
| 4.1.1 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. | |
| 4.1.2 | Методы разделения смесей и очистки веществ. | |
| 4.1.3 | Определение характера среды водных растворов веществ. Индикаторы. | |
| 4.1.4 | Качественные реакции на неорганические вещества и ионы. | |
| 4.1.5 | Качественные реакции органических соединений. | |
| 4.1.7 | Основные способы получения углеводородов. | |
| 4.1.8 | Основные способы получения кислородсодержащих соединений. | |
| 4.2 | Общие представления о промышленных способах получения важнейших веществ | |
| 4.2.1 | Понятие о металлургии: общие способы получения металлов. | |
| 4.2.2.1 | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). | |
| 4.2.3 | Природные источники углеводородов, их переработка. | |
| 4.2.4 | Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки. | |
| 4.3 | Рачеты по химическим формулам и уравнениям реакций | |
| 4.3.1 | Расчеты с использованием понятия «массовая доля вещества в растворе». | |
| 4.3.2 | Расчеты объемных отношений газов при химических реакциях. | |
| 4.3.3 | Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ. | |
| 4.3.4 | Расчеты теплового эффекта реакции. | |
| 4.3.5 | Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси). | |
| 4.3.6 | Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества. |
Тема 2. СТРОЕНИЕ АТОМА.
Атом – мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Электронная оболочка – совокупность движущихся вокруг ядра электронов.
Атомное ядро – центральная, положительно заряженная, часть атома, состоящая из протонов и нейтронов, связанных между собой ядерными силами.
|
Протон р+ |
Нейтрон n0 |
Электрон е |
|
|
Заряд частицы |
+1 |
0 |
-1 |
|
Масса частицы |
1,00728 а.е.м. |
1,00866 а.е.м. |
1/1840 от массы протона |
Заряд ядра атома Z равен порядковому номеру элемента в периодической системе.
Химический элемент – вид атомов, с определённым зарядом ядра.
Так как атом – электронейтрален (не заряжен), то число протонов в атоме равно числу электронов (число + = числу — ): N(e—) = N(p) = Z
Массовое число атома А складывается из числа протонов и нейтронов в ядре данного изотопа. Число нейтронов можно найти, вычитая заряд ядра атома из массового числа. А = N(p) + N(n) N(n) = A – Z
Oдин и тот же химический элемент может существовать в виде двух или нескольких изотопов.
Изотопы – атомы с одинаковым зарядом ядра, но разным массовым числом, т.е разным числом нейтронов в ядре.
Нейтроны практически не влияют на химические свойства элементов, все изотопы одного и того же элемента химически неотличимы.
Пример 1: Определить число нейтронов у изотопов углерода: 12С и 14С.
Решение: у 12С – 6 нейтронов (12-6=6), у 14С – 8 нейтронов (14-6=8).
Пример 2: определить число протонов и нейтронов в ядре изотопа мышьяка с массовым числом 75.
Решение: порядковый номер у As – 33. Следовательно, заряд ядра Z= +33, число протонов – 33. Число нейтронов: A – Z = 75 – 33 = 42.
ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА.
В 1913 г датский физик Н. Бор предложил модель атома, в которой электроны вращаются вокруг ядра атома, как планеты обращаются вокруг Солнца.
|
|
Бор предположил, что электроны в атоме могут устойчиво существовать только на орбитах, удаленных от ядра на строго определенные расстояния. Эти орбиты он назвал стационарными. Электронные орбиты в модели Бора обозначаются целыми числами: 1, 2, …, n, начиная от ближайшей к ядру. |
Такие орбиты называют электронными уровнями (слоями).
Уровни состоят из близких по энергии подуровней (электронных оболочек).
Их обозначают s, p, d, f.
Подуровни состоят из одинаковых по энергии орбиталей.
На каждой орбитали может быть не больше двух электронов.
Они отличаются так называемым СПИНОМ, упрощенно – направлением вращения.
Принцип Паули (запрет Паули) ограничивает число электронов, которые могут находиться на одной орбитали.
Согласно принципу Паули, на любой орбитали может находиться не более двух электронов и лишь если они имеют противоположные спины.
Правило Хунда определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию. Оно было выведено немецким физиком-теоретиком Ф. Хундом в 1927 г. на основе анализа атомных спектров.
Согласно правилу Хунда, заполнение орбиталей одного и того же подуровня происходит таким образом: сначала каждую орбиталь занимают по одному электрону, а затем уже по второму, с противоположным спином.
Пример: атом азота имеет три электрона, находящиеся на 2р-подуровне. Согласно правилу Хунда, они должны располагаться поодиночке на каждой из трех 2р-орбиталей. При этом все три электрона должны иметь параллельные спины:
Связь между уровнем и подуровнями.
|
Номер электронного слоя (уровня) |
Электронные подуровни |
Максимальное число электронов |
|
n = 1 |
1s ◻ |
2e |
|
n = 2 |
2s ◻ 2p ◻◻◻ |
2e 6e |
|
n = 3 |
3s ◻ 3p ◻◻◻ 3d ◻◻◻◻◻ |
2e 6e 10e |
|
n = 4 |
4s ◻ 4p ◻◻◻ 4d ◻◻◻◻◻ 4f ◻◻◻◻◻◻◻ |
2e 6e 10e 14e |
ЭЛЕКТРОННЫЕ КОНФИГУРАЦИИ АТОМОВ
Изображение орбиталей с учетом их энергии называется энергетической диаграммой атома.
На каждом s-подуровне (одна орбиталь) могут находиться два электрона, на каждом p-подуровне (три орбитали) — шесть электронов, на каждом d-подуровне (пять орбиталей) — десять электронов.
Принцип минимума энергии определяет порядок заселения атомных орбиталей, имеющих различные энергии. Согласно принципу минимума энергии, электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.
Энергия подуровней растет в ряду:
1s < 2s < 2 p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f∼5d < 6p < 7s <5f∼6d…
Оказалось, что у одних элементов более низкую энергию имеет 4f-подуровень, а у других — 5d-подуровень.
То же самое наблюдается для 5f- и 6d-подуровней.
ПОСЛЕДОВАТЕЛЬНОСТЬ ЗАПОЛНЕНИЯ ОРБИТАЛЕЙ У ПЕРВЫХ 36 АТОМОВ.
Электронная формула атома – запись распределения электронов по орбиталям в основном (невозбужденном) состоянии атома или его ионов: 1s22s22p63s23p6… и т.д.
Заполнение электронных оболочек атомов первых 4-х периодов.
Водород (1е): Н 1s1 – заполняется первый уровень.
Гелий (2е) Не 1s2
ПЕРВЫЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ ЗАПОЛНЕН.
Литий (3е) — начинает заполняться второй уровень: Li 1s22s1
Бериллий на 2s-подуровень приходит второй электрон.
Затем у бора начинается заполнение 2p-подуровня:
В 1s22s22p1
У следующих за бором пяти атомов продолжается заполнение 2р-подуровня, вплоть до неона: Ne 1s22s22p6
ВТОРОЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ ПОЛНОСТЬЮ ЗАВЕРШЕН.
Начинается третий период – сначала происходит заполнение 3s-подуровня у натрия и магния (это s-элементы), а потом заполняется 3р-подуровень у шести р-элементов: от алюминия до аргона.
Na 1s22s22р63s1 Mg 1s22s22р63s2
Al 1s22s22р63s23p1 ….. Ar 1s22s22р63s23p6
У аргона — инертного газа на внешнем слое 8 электронов.
Распределение электронов по электронным уровням у атома № 18 — аргона выглядит так: 2,8,8.
При этом третий электронный уровень ещё не заполнен: в нём есть 3d-подуровень.
Однако атом № 19 – калий является первым элементом 4 периода, у него идёт заполнение 4s-подуровня.
Калий — это s-элемент.
K 1s22s22p63s23p64s1
3d-подуровень пока остаётся незаполненным.
4s-подуровень заполняется и у кальция: Са 1s22s22p63s23p64s2
И вот ТОЛЬКО у следующих 10 элементов (от скандия до цинка) происходит заполнение 3d-подуровня. Это d-элементы.
Sc 1s22s22p63s23p63d14s2
Ti 1s22s22p63s23p63d24s2
V 1s22s22p63s23p63d34s2
У ванадия на d-подуровне 3 электрона, на 4s — 2 электрона.
Казалось бы, у хрома должно получиться: Сr …3d44s2
Однако у хрома происходит переход одного электрона с s-подуровня на d-подуровень: Сr…3d54s1
Это явление называется ПРОВАЛ ЭЛЕКТРОНА, причина такого явления — более выгодная по энергии полузаполненная d-оболочка.
Дальше у марганца снова происходит «возвращение» электрона на 4s-подуровень: Mn…3d54s2
У атомов с №26 (железо) до № 28 (никель) происходит дальнейшее заполнение 3d-подуровня.
У никеля на d-подуровне 8 электронов, на 4s — 2 электрона. У меди вновь происходит переход одного электрона с s на d-подуровень: Сu …3d104s1
Это снова ПРОВАЛ ЭЛЕКТРОНА, причина которого — более выгодная по энергии полностью заполненная d-оболочка.
И наконец, цинк завершает ряд из 10 d-элементов 4 периода:
Zn 1s22s22p63s23p63d104s2
ТРЕТИЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ только теперь ЗАВЕРШЕН – на нем 18 электронов.
Со следующего элемента 4 периода — галлия вновь начинается заполнение внешнего электронного уровня (№4), теперь уже 4p-подуровня – от галлия до криптона.
Ga 1s22s22p63s23p63d104s24p1 ……… Kr 1s22s22p63s23p63d104s24p6
Для краткости записи электронной конфигурации атома вместо орбиталей, полностью заселенных электронами, иногда записывают символ благородного газа, имеющего соответствующую электронную формулу: 1s2 = [He] 1s22s22p6 = [Ne]
Пример: электронная формула атома хлора 1s22s22p63s23p5, или [Ne]3s23p5.
ЭЛЕКТРОННЫЕ ФОРМУЛЫ ИОНОВ.
Ионы – заряженные частицы; катионы – положительно заряженные ионы, анионы – отрицательно заряженные ионы.
Ионы получаются из атомов путем отдачи электронов (тогда образуются катионы) или принятия электронов (образуются анионы).
S0 (атом серы)+ 2e → S2−(сульфид-анион)
Cu0(атом меди) -2е →Cu2+ (катион меди)
Электронная формула иона получается путём добавления или отнятия электронов в электронной формуле атома.
Электроны сначала уходят с внешнего электронного уровня!
Пример: составить электронные формулы ионов: As3- ; Cu2+.
1) As0 1s22s22p63s23p63d104s24p3 → As3- 1s22s22p63s23p63d104s24p6 (добавились ещё 3 электрона на внешний уровень – их стало 8, а всего – 36е: оболочка инертного газа криптона)
2) Cu01s22s22p63s23p63d104s1 → Cu2+1s22s22p63s23p6 3d9 (уходят 2 электрона, сначала ВНЕШНИЙ 4s-электрон, а потом – 3d-электроны! )
Изоэлектронные частицы – это атомы и ионы, имеющие одинаковое строение электронной оболочки. Например, ион Са2+ и атом аргона – имеют одинаковую 18- электронную оболочку.
Пример: какие из этих солей образованы изоэлектронными ионами: хлорид натрия, фторид бария, бромид магния, сульфид кальция.
NaCl Na+(10e), Cl —(18e), BaF2 Ba2+(54 e), F — (10e);
MgBr2 Mg2+(10e),Br — (36e) CaS Ca2+(18e),S2-(18e)–ионы изоэлектронны. Ответ: CaS
ОСНОВНОЕ И ВОЗБУЖДЕННОЕ СОСТОЯНИЕ АТОМА.
Основное состояние атома — это наиболее выгодное по энергии состояние, которое получается в результате последовательного заполнения оболочек электронами согласно правилу Хунда и принципу минимума энергии.
Поэтому ПРИ НАЛИЧИИ СВОБОДНЫХ ОРБИТАЛЕЙ и при наличии некоторой ЭНЕРГИИ (энергия возбуждения) электроны атома могут РАСПАРИВАТЬСЯ и атом переходит в возбужденное состояние. При этом число неспаренных электронов, а, следовательно, ЧИСЛО СВЯЗЕЙ, образуемых атомом, УВЕЛИЧИВАЕТСЯ.
Пример: у атома углерода на внешнем валентном слое есть 4 электрона. В невозбуждённом (основном) состоянии число неспаренных электронов равно ДВУМ: С … 2s2 2p2
|
↑↓ |
↑ |
↑ |
При переходе одного электрона с s-оболочки на р – оболочку число неспаренных электронов становится равным ЧЕТЫРЁМ: С* …2s12p3
|
↑ |
↑ |
↑ |
↑ |
Это возбужденное состояние углерода.
Тема 3. ПЕРИОДИЧЕСКИЙ ЗАКОН
Д.И. Менделеев в 1869 году так сформулировал Периодический закон: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел находятся в периодической зависимости от их атомного веса«.
Менделеев учитывал, что для некоторых элементов атомные массы могли быть определены недостаточно точно. После того, как было доказано ядерное строение атома и равенство порядкового номера элемента заряду ядра его атома, Периодический закон получил новую формулировку:
«Свойства элементов, а также образуемых ими веществ находятся в периодической зависимости от заряда их атомных ядер».
Современная Периодическая система состоит из 7 периодов (седьмой период заканчивается 118-м элементом).
Короткопериодный вариант Периодической системы содержит 8 групп элементов, каждая из которых условно подразделяется на группу А (главную) и группу Б (побочную). В длиннопериодном варианте Периодической системы — 18 групп, имеющих те же обозначения, что и в короткопериодном.
В группах, обозначенных буквой А (главных подгруппах), содержатся элементы, в которых идет заселение s- и р-оболочек: s-элементы (IA- и IIA-группы) и р-элементы (IIIA-VIIIA-группы). В группах, обозначенной буквой Б (побочных подгруппах), находятся элементы, в которых заселяются d-подуровни — d-элементы.
Номер периода в Периодической системе соответствует числу энергетических уровней атома данного элемента, заполненных электронами.
Номер периода = Число энергетических уровней, заполненных электронами = номер последнего энергетического уровня
Номер группы в Периодической системе определяет число валентных электронов в атомах s- и p-элементов.
ЗАКОНОМЕРНОСТИ ИЗМЕНЕНИЯ СВОЙСТВ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ.
1) Атомные и ионные радиусы.
Радиус атома – это расстояние от центра ядра до внешнего уровня (области максимальной электронной плотности внешнего уровня).
В периодах орбитальные атомные радиусы по мере увеличения заряда ядра уменьшаются, т.к. растет заряд ядра и => притяжение внешнего электронного уровня к ядру.
В подгруппах радиусы в основном увеличиваются из-за возрастания числа электронных слоёв.
У s- и p-элементов изменение радиусов как в периодах, так и в подгруппах более заметно, чем у d- и f-элементов, поскольку d- и f-электроны находятся на внутренних, а не внешних уровнях.
Уменьшение радиусов у d- и f-элементов в периодах называется d- и f-сжатием.
Образование ионов приводит к изменению ионных радиусов по сравнению с атомными.
Радиусы катионов всегда меньше, а радиусы анионов всегда больше соответствующих атомных радиусов.
Изоэлектронные ионы – это ионы, имеющие одинаковое электронное строение.
Радиус изоэлектронных ионов уменьшается слева направо по периоду, т.к. заряд ядра увеличивается и растёт притяжение внешнего электронного уровня к ядру.
Пример: изоэлектронные ионы с электронной оболочкой, соответствующей аргону – (18 е): S2-, Cl—, K+, Ca2+ и т.п. В этом ряду радиус уменьшается, т.к. растёт заряд ядра.
2) Электроотрицательность— это способность атома элемента к притягивать к себе электроны в химической связи.
Электроны в общей электронной паре смещены к атому того элемента, который имеет большую электроотрицательность.
Слева направо по периоду происходит увеличение электроотрицательности, т.к. растёт заряд ядра и внешний уровень притягивается к ядру сильнее.
Сверху вниз по подгруппе электроотрицательность уменьшается, т.к. увеличивается число электронных уровней и увеличение радиуса. Внешние электроны слабее притягиваются к ядру.
На рис. приведены значения электроотрицательности различных элементов по Полингу.
Металлами являются:
-все элементы побочных подгрупп (d-элементы);
— лантаноиды, актиноиды;
-все s- элементы, кроме водорода и гелия.
р-элементы делятся диагональю на металлы и неметаллы:
|
Ве |
В |
||||
|
Al |
Si |
||||
|
Ge |
As |
неметаллы |
|||
|
металлы |
Sb |
Te |
22 штуки |
||
|
Po |
At |
Каждый период начинается щелочным металлом (или водородом), а заканчивается инертным газом.
3) Валентность – число связей, которые образует атом в молекуле.
Высшая валентность как правило равна номеру группы (исключения – элементы второй половины второго периода – азот, кислород, фтор, инертные газы – гелий, неон, аргон, а также металлы побочных подгрупп первой и VIIIB группы (второй и третий элемент «триады»)).
4) Степень окисления – условный заряд у атома в молекуле, рассчитанный, исходя из предположения, что все связи в молекуле – ионные (т.е. электроны полностью смещены от менее электроотрицательного атома к более электроотрицательному.
Высшая положительная степень окисления определяется числом валентных электронов и равна номеру группы. У s- и р-элементов она равна числу внешних электронов. У d-элементов (кроме групп IB,IIB и VIIIB) — она равна числу d+s электронов.
Исключения: 1) фтор, кислород
2) инертные газы – гелий, неон, аргон.
3) медь, серебро, золото
4) кобальт, никель, родий, палладий, иридий, платина.
Для неметаллов также характерна низшая (отрицательная) степень окисления:
Отрицательная степень окисления неметалла = 8 – номер группы.
5) Высшие оксиды и гидроксиды.
1) Степень окисления элемента в высшем оксиде и гидроксиде равна номеру группы:
SeO3 – высший оксид селена.
2) Чем активнее металл, тем более выражены основные свойства высшего оксида и гидроксида.
3) Чем активнее неметалл и чем больше высшая степень окисления – тем сильнее выражены кислотные свойства.
6) ВОДОРОДНЫЕ СОЕДИНЕНИЯ.
Существует два типа водородных соединений:
- Ионные солеобразные гидриды
Это соединения активных металлов с водородом, в которых водород имеет отрицательную степень окисления: СаН2 – гидрид кальция. Это кристаллические вещества, похожие по виду на соли, поэтому их называют СОЛЕОБРАЗНЫМИ.
- ЛЕТУЧИЕ водородные соединения – их образуют только НЕМЕТАЛЛЫ.
В них отрицательную степень окисления имеет неметалл, а водород имеет степень окисления +1. Все газы, кроме воды.
Особенности свойств летучих водородных соединений.
Химия Кодификатор ЕГЭ
Государственная итоговая аттестация в форме единого государственного экзамена (ЕГЭ)
Химия Кодификатор ЕГЭ элементов содержания и требований к уровню подготовки обучающихся
для проведения ГИА по ХИМИИ. Ссылки на конспекты
Элементы содержания, проверяемые заданиями экзаменационной работы,
ссылки на конспекты уроков.
| Код элемента | Элементы содержания, проверяемые заданиями КИМ | Ссылки на конспекты |
| 1. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ | ||
| 1.1. Современные представления о строении атома | ||
| 1.1.1 | Строение электронных оболочек атомов элементов первых четырёх периодов: s–, р– и d–элементы. Электронная конфигурация атомов и ионов. Основное и возбуждённое состояния атомов | КОНСПЕКТ |
| 1.2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева | ||
| 1.2.1 | Закономерности изменения свойств элементов и их соединений по периодам и группам | КОНСПЕКТ |
| 1.2.2 | Общая характеристика металлов IA-IIIA групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | КОНСПЕКТ |
| 1.2.3 | Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов | КОНСПЕКТ |
| 1.2.4 | Общая характеристика неметаллов IVA-VIIA групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | КОНСПЕКТ |
| 1.3. Химическая связь и строение вещества | ||
| 1.3.1 | Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь | Ионная связь, Ковалентная, Металлическая, Водородная |
| 1.3.2 | Электроотрицательность. Степень окисления и валентность химических элементов | |
| 1.3.3 | Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения | |
| 1.4. Химическая реакция | Справочник ОГЭ | |
| 1.4.1 | Классификация химических реакций в неорганической и органической химии | КОНСПЕКТ |
| 1.4.2 | Тепловой эффект химической реакции. Термохимические уравнения | |
| 1.4.3 | Скорость реакции, её зависимость от различных факторов | КОНСПЕКТ |
| 1.4.4 | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов | КОНСПЕКТ |
| 1.4.5 | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты | КОНСПЕКТ |
| 1.4.6 | Реакции ионного обмена | КОНСПЕКТ |
| 1.4.7 | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная | КОНСПЕКТ |
| 1.4.8 | Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от неё | КОНСПЕКТ |
| 1.4.9 | Электролиз расплавов и растворов (солей, щелочей, кислот) | КОНСПЕКТ |
| 1.4.10 | Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии | |
| 2. НЕОРГАНИЧЕСКАЯ ХИМИЯ | ||
| 2.1 | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная) | |
| 2.2 | Характерные химические свойства простых веществ -металлов: щелочных, щёлочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа) | Щелочные, Щёлочноземельные, Магний, Алюминий; Медь, Цинк, Хром, Железо |
| 2.3 | Характерные химические свойства простых веществ -неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния | Водород, Свойства водорода, Галогены, Кислород, Сера, Азот, Фосфор, Углерод, Кремний |
| 2.4 | Характерные химические свойства оксидов: основных, амфотерных, кислотных | Оксиды, Свойства оксидов, Амфотерные оксиды |
| 2.5 | Характерные химические свойства оснований и амфотерных гидроксидов | Основания, Амфотерные гидрооксиды |
| 2.6 | Характерные химические свойства кислот | Кислоты |
| 2.7 | Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка) | Соли |
| 2.8 | Взаимосвязь различных классов неорганических веществ | |
| 3. ОРГАНИЧЕСКАЯ ХИМИЯ | ||
| 3.1 | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах | |
| 3.2 | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа | |
| 3.3 | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) | |
| 3.4 | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола) | Алканы, Циклоалканы, Алкены, Диены, Алкины, Ароматические углеводороды |
| 3.5 | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола | Одноатомные спирты, Многоатомные спирты, Фенол |
| 3.6 | Характерные химические свойства альдегидов, карбоновых кислот, сложных эфиров | Альдегиды, Карбоновые кислоты, Сложные эфиры |
| 3.7 | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот | Амины, Аминокислоты |
| 3.8 | Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды) | Жиры, Белки, Углеводы |
| 3.9 | Взаимосвязь органических соединений | |
| 4. МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ и ЖИЗНЬ | ||
| 4.1. Экспериментальные основы химии | ||
| 4.1.1 | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии | КОНСПЕКТ |
| 4.1.2 | Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ | КОНСПЕКТ |
| 4.1.3 | Определение характера среды водных растворов веществ. Индикаторы | КОНСПЕКТ |
| 4.1.4 | Качественные реакции на неорганические вещества и ионы | КОНСПЕКТ |
| 4.1.5 | Качественные реакции органических соединений | КОНСПЕКТ |
| 4.1.6 | Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений | КОНСПЕКТ |
| 4.1.7 | Основные способы получения углеводородов (в лаборатории) | КОНСПЕКТ |
| 4.1.8 | Основные способы получения органических кислородсодержащих соединений (в лаборатории) | КОНСПЕКТ |
| 4.2. Общие представления о промышленных способах получения важнейших веществ. Применение веществ | ||
| 4.2.1 | Понятие о металлургии: общие способы получения металлов | КОНСПЕКТ |
| 4.2.2 | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия | КОНСПЕКТ |
| 4.2.3 | Природные источники углеводородов, их переработка | КОНСПЕКТ |
| 4.2.4 | Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки | КОНСПЕКТ |
| 4.2.5 | Применение изученных неорганических и органических веществ | КОНСПЕКТ |
| 4.3. Расчёты по химическим формулам и уравнениям реакций | ||
| 4.3.1 | Расчёты с использованием понятий «растворимость», «массовая доля вещества в растворе» | Задачи с решениями |
| 4.3.2 | Расчёты объёмных отношений газов при химических реакциях | Задачи с решениями |
| 4.3.3 | Расчёты массы вещества или объёма газов по известному количеству вещества, массе или объёму одного из участвующих в реакции веществ | |
| 4.3.4 | Расчёты теплового эффекта реакции | |
| 4.3.5 | Расчёты массы (объёма, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси) | Задачи с ответами |
| 4.3.6 | Расчёты массы (объёма, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определённой массовой долей растворённого вещества | |
| 4.3.7 | Установление молекулярной и структурной формул вещества | |
| 4.3.8 | Расчёты массовой или объёмной доли выхода продукта реакции от теоретически возможного | |
| 4.3.9 | Расчёты массовой доли (массы) химического соединения в смеси |
Список конспектов по химии
Проверить знания (онлайн-тесты)
Вы смотрели: Химия Кодификатор ЕГЭ элементов содержания, проверяемых заданиями экзаменационной работы,
ссылки на конспекты, размещенные на сайте Учитель PRO.